Пересадка костного мозга : показания и противопоказания к проведению
Как делают пересадку костного мозга?
Для начала, после того, как больному было проведено лечение при помощи химиотерапии или же радикального облучения, пациенту вводят внутривенно при помощи катетера плюрипотентные СК. Зачастую это безболезненно и длиться примерно около часа. После этого наступает процесс приживления донорских или своих клеток, для того, чтобы ускорить процесс приживления иногда используют препараты стимулирующие работу органа кроветворения.
Если вы хотите знать, как делают пересадку костного мозга, вам будет необходимо понимать какие процессы, происходят в организме после его трансплантации, а также следует разобраться в механизмах воздействия пересаженных клеток. В процессе приживления, каждый день забирается кровь пациента на анализ. В качестве показателя используются нейтрофилы. Необходим определенный уровень их количества в крови, если их показатель в крови достигает количества 500 в течении трех дней, то это является положительным результатом и свидетельствует о том, что замененные плюрипотентные СК прижились.
Операция по пересадке костного мозга
Операция по пересадке костного мозга предваряется мощной радиотерапией или интенсивной химиотерапией пациента, иногда оба этих элемента лечения практикуются вместе. Эти процедуры применяют для уничтожения раковых клеток, но в процессе также убивают и здоровые плюрипотентные СК пациента. Вышеперечисленные процедуры при замене стволовых клеток называются – подготовительным режимом. Длится этот режим столько, сколько требует конкретное заболевание пациента и рекомендации его лечащего врача.
Далее в вену (на шее) пациенту устанавливают катетер, при помощи которого будут вводиться лекарства, клеточные элементы крови и забираться кровь на анализ. Спустя два дня после радиотерапии или химиотерапии проводится хирургическое вмешательство, во время которой стволовые клетки вводятся внутривенно.
После замены стволовых клеток, на протяжении от 2 до 4 недель следует ожидать приживление клеток органа кроветворения.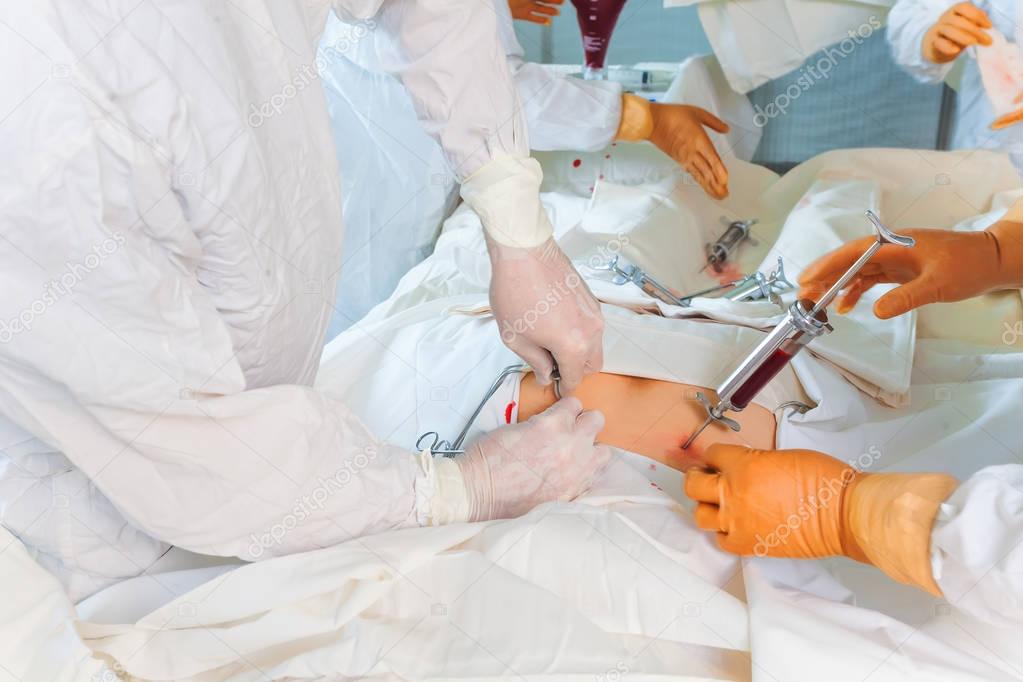 В этот период больному вводят антибиотики, которые помогут справиться с инфекцией и делают переливание тромбоцитов для того что бы избежать кровотечений. Пациентам, подвергшимся трансплантации от неродственного или родственного, но несовместимого донора требуются препараты, которые помогут минимизировать отторжение пересаженных стволовых клеток организмом.
В этот период больному вводят антибиотики, которые помогут справиться с инфекцией и делают переливание тромбоцитов для того что бы избежать кровотечений. Пациентам, подвергшимся трансплантации от неродственного или родственного, но несовместимого донора требуются препараты, которые помогут минимизировать отторжение пересаженных стволовых клеток организмом.
После пересадки СК пациенты могут испытывать ощущение слабости, в ряде случаем могут открыться кровотечения, нарушение работы печени, тошнота, во рту возможно появление небольших язв, в редких случаях есть вероятность развития небольших психических отклонений. Как правило, персонал больницы достаточно компетентен и способен создать максимально комфортные условия для преодоления такого рода трудностей. И естественно одним из важных аспектов, которые приведут пациента к скорому выздоровлению, является внимание и участие родных и близких пациента.
Пересадка костного мозга при ВИЧ
Пересадка костного мозга при ВИЧ от здорового донора, позволит вылечить реципиента от этого заболевании.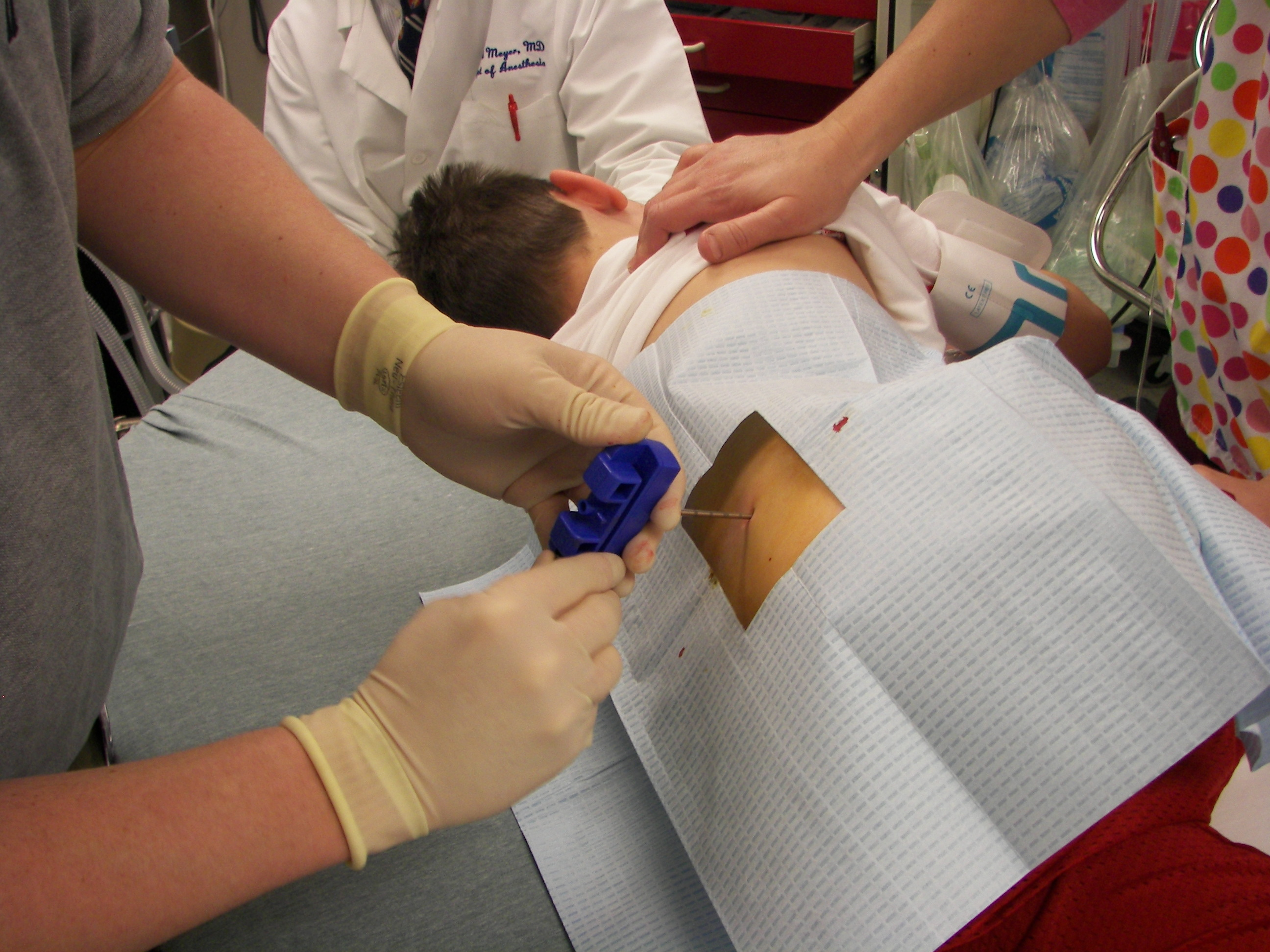 Для того чтобы осуществить эту процедуру, необходимо выбрать донора с особой генетической мутацией. Встречается она только лишь у 3% европейцев. Это делает такого человека восприимчивым ко всем известным штаммам ВИЧ. Данная мутация затрагивает структуру рецептора CCR5, таким образом, не позволяя «вирусу» связаться с клеточными элементами человеческого мозга.
Для того чтобы осуществить эту процедуру, необходимо выбрать донора с особой генетической мутацией. Встречается она только лишь у 3% европейцев. Это делает такого человека восприимчивым ко всем известным штаммам ВИЧ. Данная мутация затрагивает структуру рецептора CCR5, таким образом, не позволяя «вирусу» связаться с клеточными элементами человеческого мозга.
Перед самой процедурой реципиенту необходимо пройти курс лучевой и лекарственной терапии. Это позволит уничтожить собственные плюрипотентные СК. Лекарства против самой ВИЧ-инфекции не принимаются. Спустя 20 месяцев со дня операции проводится исследование. Как правило, реципиент является полностью здоровым. Более того, он не носит вирус ВИЧ в крови, органе кроветворения и других органах и тканях. Проще говоря, во всех резервуарах, где он может быть.
Данное хирургическое вмешательство связано с высоким риском инфекционных осложнений. Вполне вероятно, что достигнутый результат может поспособствовать развитию нового направления в области генной терапии ВИЧ-инфекции.
[8], [9], [10], [11], [12]
Пересадка костного мозга при лейкозе
Зачастую она применяется в случае острых миелобластных лейкозах и при рецидивах острых лейкозов. Чтобы провести операцию, необходима полная клинико-гематологическая ремиссия. Перед самой процедурой проводится курс химиотерапии, зачастую в сочетании с лучевой терапией. Это позволит полностью уничтожить лейкозные клетки в организме.
Чувствительность лифом к химиотерапии напрямую зависит от дозы, даже во время рецидивов. Шанс на достижение ремиссии в основном дает выскокодозная химиотерапия, а также она, но в сочетании с облучением всего тела. Правда, в этом случае такой подход чреват глубоким и продолжительным угнетением кроветворения.
Метод подразумевает проведение трансплантации стволовых клеток, источником которых может быть как орган кроветворения так и кровь больного или же донора. Если речь идет о изотрансплантации, то донором может выступить однояйцовый близнец. При аллотрансплантации даже родственник. При аутотрансплантации сам больной.
При аутотрансплантации сам больной.
Если речь идет о лимфопролиферативных заболеваниях, то зачастую применяются именно аутотрансплантация СК крови. Такой метод получил всеобщее признание в лечении резистентных лимфом и рецидивов.
[13], [14], [15], [16], [17]
Пересадка костного мозга у детей
Пересадка костного мозга у детей используется в тех случаях, когда пациент страдает лейкозом. Более того, этот метод применяется и при апластической анемии, множественной миеломе и при нарушениях иммунной системы.
Когда плюрипотентные СК начинают несколько неправильно функционировать, тем самым провоцирую избыточное количество дефектных или незрелых клеток, развивается лейкоз. Если же наоборот, мозг резко уменьшает их выработку, то это приводит к развитию апластической анемии.
Незрелые клетки крови полностью заполняют орган кроветворения и сосуды. Тем самым они вытесняют нормальные клеточные элементы и распространяются в другие ткани и органы. Чтобы исправить положение дел и уничтожить лишние клетки, прибегают к использованию химиотерапии или радиотерапии.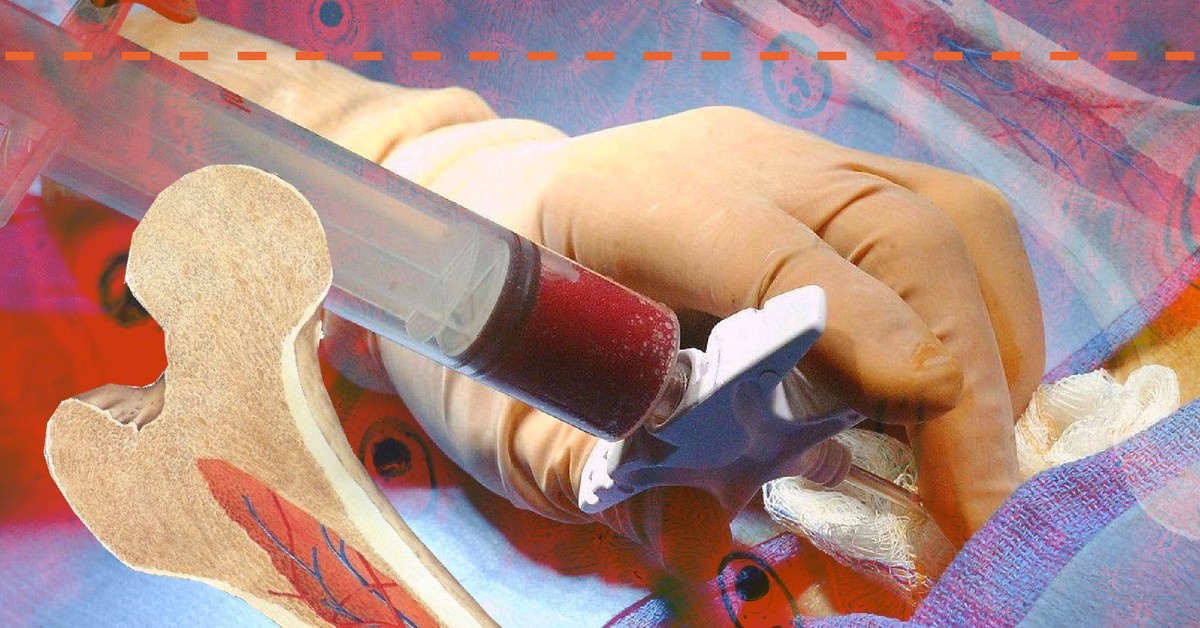 Такое лечение способно повредить не только дефектные, но и здоровые клеточные элементы мозга. Если трансплантация пройдет успешно, то пересаженный орган начнет вырабатывать нормальные клетки крови.
Такое лечение способно повредить не только дефектные, но и здоровые клеточные элементы мозга. Если трансплантация пройдет успешно, то пересаженный орган начнет вырабатывать нормальные клетки крови.
Если донорский орган кроветворения был получен от идентичного близнеца, то трансплантация в этом случае называется аллогенной. В этом случае, мозг должен генетически соответствовать собственному мозгу пациента. Чтобы выявить совместимость, проводятся специальные анализы крови.
[18], [19], [20], [21]
Повторная пересадка костного мозга
Порой одной операции становится не достаточно. Так, орган кроветворения может не прижиться на новом месте. В этом случае проводится повторная операция.
Она ничем не отличается от обыкновенной трансплантации, только вот называют ее уже ретрансплантация. Перед тем как выполнить эту процедуру проводится диагностирование. Ведь необходимо определить, почему в первый раз орган кроветворения не смог прижиться.
После того как все процедуры будут выполнены, можно приступать к повторной операции.
Сама по себе операция является сложной. Но многое в этом случае зависит и от стараний пациента. Если он тщательно соблюдает все рекомендации врача, то рецидива можно избежать.
[22], [23], [24], [25], [26]
Лечение пересадки костного мозга в Израиле
Содержание статьи:
1. Как происходит пересадка костного мозга
2. Донор для пересадки костного мозга
3. Что происходит после пересадки костного мозга
4. Пересадка костного мозга в Израиле
Первая успешная операция по пересадке костного мозга, необходимая для терапии многих ранее считавшихся неизлечимыми заболеваний, была проведена сравнительно недавно, в 1968 году.
– Серьёзные нарушения иммунитета;
– Множественные миеломы;
– Лимфомы Ходжкина и лимфогранулематоз;
– Апластическая анемия;
– Лейкоз или рак крови и некоторые другие видов злокачественных опухолей.
Эта тяжёлая операция считается методом последнего шанса и проводится только в самых крайних случаях. Специалисты прибегают к трансплантации тогда, когда все другие способы лечения серьёзных заболеваний были испробованы неоднократно и не дали каких-либо результатов. Связано это с тем, что данная дорогостоящая процедура несёт для организма пациента большие риски.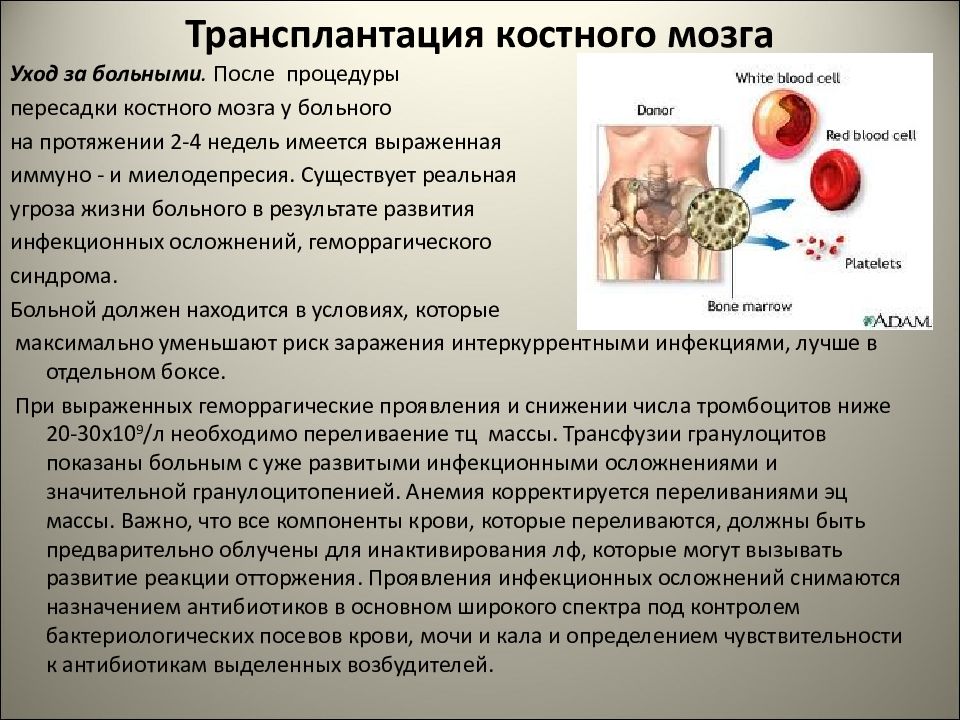
КАК ПРОИСХОДИТ ПЕРЕСАДКА КОСТНОГО МОЗГА
В случае потери костным мозгом способности к произведению новых кровяных клеток, необходимых для борьбы с тяжёлыми заболеваниями, требуется их замена на здоровые. Она проводится одним из трёх способов:
- Аллогенный, при котором донором выступает посторонний человек, подходящий больному по ряду признаков;
- Аутологичный. Для пересадки используются собственные здоровые клетки костного мозга пациента, взятые до химиотерапии;
- Сингенный, наиболее редкий метод. При нём материал для трансплантации берётся от однояйцевого близнеца пациента.
Способ пересадки выбирается врачом-трансплантологом с учётом различных факторов. Во внимание должны приниматься наличие подходящего донора, общее состояние и возраст пациента, а также вид поразившего его рака. Меньшее количество побочных эффектов вызывает аутологичная трансплантация, однако она при некоторых онкологических заболеваниях бывает недостаточно эффективной. Оперативное вмешательство такого типа состоит из нескольких этапов:
Меньшее количество побочных эффектов вызывает аутологичная трансплантация, однако она при некоторых онкологических заболеваниях бывает недостаточно эффективной. Оперативное вмешательство такого типа состоит из нескольких этапов:
· Подготовка пациента, заключающаяся в проведении интенсивных курсов химиотерапии, разрушающих все клетки костного мозга. Этот этап считается при данной процедуре одним из самых длительных и сложных. Он продолжается приблизительно неделю. Во время его проведения происходит подготовка костных тканей к заселению здоровыми клетками;
· Обработка полученного биологического материала и собственно его пересадка. Процедура, сходная по методу проведения с переливанием крови, длится не более часа. Для снижения рисков возникновения таких побочных эффектов, как анафилактический шок или аллергия, пациенту перед ней вводят большое количество противовоспалительных и антигистаминных препаратов;
Нейтропения (снижение иммунитета). Продолжительность его составляет около месяца. Он считается самым опасным для пациента. Иммунная система человека в это время практически перестаёт работать, так как пересаженные стволовые клетки не могут прижиться сразу. На данном этапе требуется полная изоляция больного от любых инфекций. Это снижает риск возникновения возможных осложнений;
Продолжительность его составляет около месяца. Он считается самым опасным для пациента. Иммунная система человека в это время практически перестаёт работать, так как пересаженные стволовые клетки не могут прижиться сразу. На данном этапе требуется полная изоляция больного от любых инфекций. Это снижает риск возникновения возможных осложнений;
Приживление костного мозга. Во время его общее состояние пациента постепенно улучшается. У него перестают проявляться признаки инфекционных заболеваний, нормализуется температура;
Этап после приживления может длиться от пары месяцев до нескольких лет. В этот период восстанавливающаяся иммунная система может не справиться с возникшим инфицированием, поэтому пациенту необходимо находиться под амбулаторным наблюдением докторов.
Для того, чтобы данная операция прошла с наибольшим успехом, требуется высококвалифицированная медицинская команда, специалисты из которой смогут правильно и быстро отреагировать на любые отклонения в ходе лечения. Врачей и медсестёр, выполняющих процедуру трансплантации, учат немедленному определению возникающих в ходе её побочных эффектов и всем возможным способам правильного их решения. Именно поэтому правильный выбор медицинского центра, где делают эту операцию, очень важен.
Врачей и медсестёр, выполняющих процедуру трансплантации, учат немедленному определению возникающих в ходе её побочных эффектов и всем возможным способам правильного их решения. Именно поэтому правильный выбор медицинского центра, где делают эту операцию, очень важен.
ДОНОР ДЛЯ ПЕРЕСАДКИ КОСТНОГО МОЗГА
Подбор подходящего для трансплантации донора это длительный, вызывающий множество сложностей процесс, являющийся во время проведения данной процедуры самым значительным ограничением. Для него используется один из трёх вариантов:
1. Аутотрансплантация, при которой необходимый для операции биоматериал получают непосредственно от пациента;
2. Сингенная трансплантация, когда донором становится его однояйцевый близнец;
3. Аллотрансплантация при которой клетки костного мозга берутся от сходного по всем генетическим параметрам постороннего человека или кровного родственника.
Перед проведением такого оперативного вмешательства в Израиле в обязательном порядке выполняются иммунногистохимические исследования, дающие возможность определить, какой из доноров лучше всего подойдёт для этой процедуры. В случае невозможности использования мозга самого пациента (при лейкозах) поиск донора осуществляется через банк хранения органов этой страны или западноевропейских государств и США.
Когда подходящий генетически материал найден и доставлен пациенту, начинается процедура пересадки. Опасность использования донорских клеток, взятых от постороннего человека, в том, что велика возможность их отторжения.
ЧТО ПРОИСХОДИТ ПОСЛЕ ПЕРЕСАДКИ КОСТНОГО МОЗГА
После проведённой процедуры трансплантации жизнь пациента значительно меняется. В период между вливанием стволовых клеток и их приживлением у больного наблюдается сильная панцитопения. Это резкое снижение количества всех кровяных телец. Для восполнения их дефицита требуется заместительная терапия, заключающаяся в постоянных переливаниях крови.
Для восполнения их дефицита требуется заместительная терапия, заключающаяся в постоянных переливаниях крови.
Кроме этого, из-за уменьшения уровня лейкоцитов падает сопротивляемость организма человека инфекциям. Из-за этого пациент должен находиться в такой палате, где соблюдается режим полной стерильности. Медперсонал и посещающие его родственники заходят в неё в специальных костюмах, масках и медицинских перчатках, предотвращающих возможность инфицирования.
Даже после того, как донорские стволовые клетки примут на себя кроветворную функцию, у человека из-за перенесённой химиотерапии сохраняется ощущение сильной усталости и слабости. Может возникнуть отторжение чужого костного мозга. Чтобы избежать этого, пациенту необходим приём иммунодепрессантов, блокирующих выработку пересаженными здоровыми клетками антител.
После того, как больной возвратится к обычному образу жизни, ему также необходимо уделять повышенное внимание защите от различных инфекций.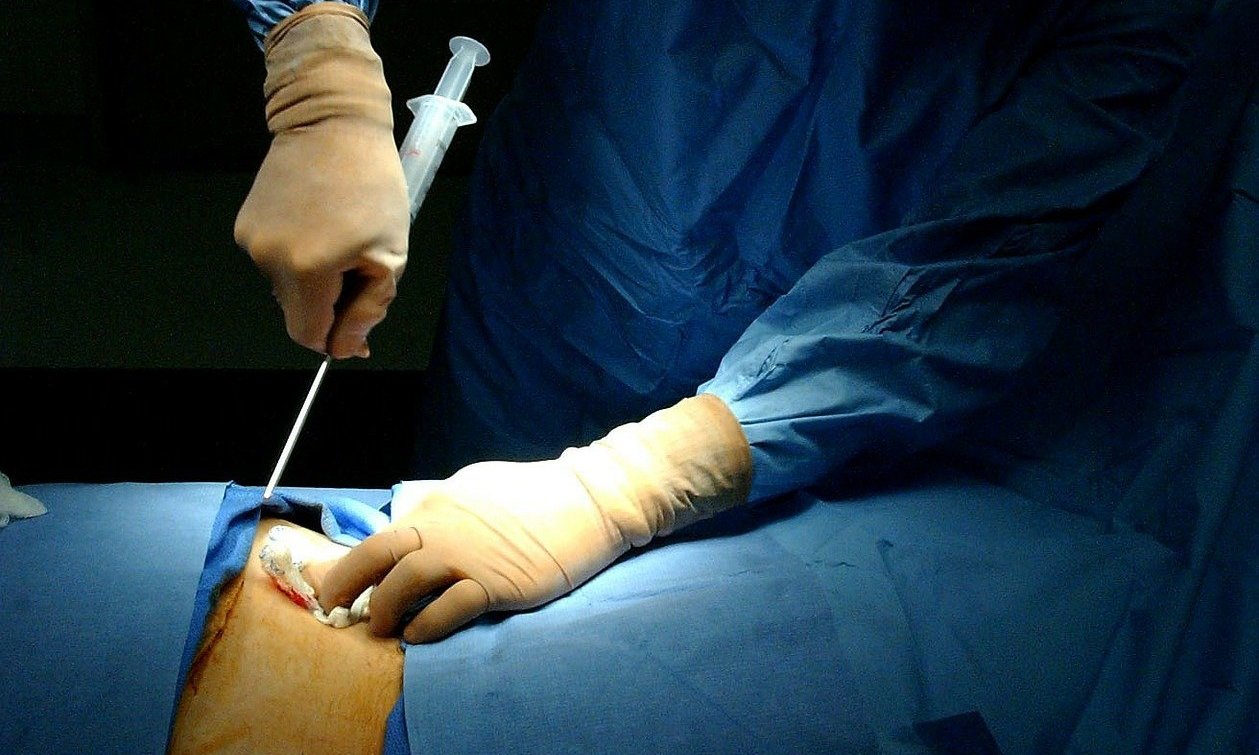
РЕАБИЛИТАЦИЯ ПОСЛЕ ПЕРЕСАДКИ КОСТНОГО МОЗГА
Реабилитационный период, продолжающийся от 1 до 1,5 месяцев, начинается сразу после проведения процедуры трансплантации. Всё это время пациент находится в специальной антибактериальной камере под пристальным наблюдением врачей-гомеологов. В это время человеку необходим приём большого количества антибиотиков и противовирусных препаратов, снижающих риск возникновения инфицирования организма. Выписывается пациент только в том случае, если в течение определённого периода времени не наступило отторжение донорского материала.
Также при реабилитации необходимо симптоматическое лечение, снижающее проявление побочных эффектов химиотерапии, таких как склонность к внутренним и наружным кровотечениям, быстрая утомляемость, тошнота и рвота. Квалифицированный персонал клиник следит за общим состоянием пациента и проводит мониторинг работоспособности всех жизненно важных органов. После выписки из стационара восстановительный период продолжается ещё приблизительно полгода.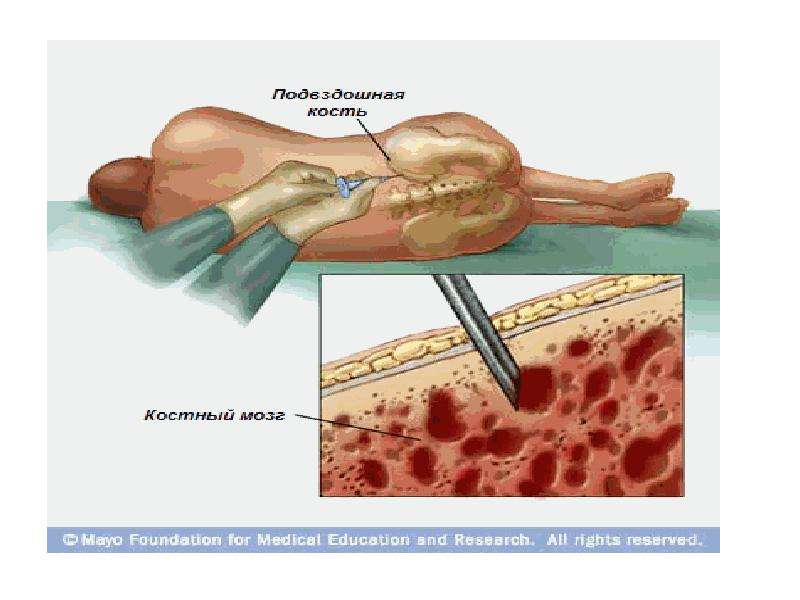 Всё это время человек должен находиться неподалёку от клиники и проходить плановые медицинские осмотры.
Всё это время человек должен находиться неподалёку от клиники и проходить плановые медицинские осмотры.
ОСЛОЖНЕНИЯ ПОСЛЕ ПЕРЕСАДКИ КОСТНОГО МОЗГА
На пути выздоровления стоят две угрозы. Первая заключается в том, что в течение 2-3 постоперационных месяцев организм человека практически полностью лишён иммунной системы, а вторая угроза – это возможное отторжение трансплантата. В это время малейшее инфицирование приводит к летальному исходу. Для полного восстановления иммунитета требуется около года. В том случае, когда пациент начинает чувствовать ухудшение самочувствия, его госпитализируют повторно. Для того, чтобы процесс реабилитации прошёл успешно, специалисты советуют применять следующие терапевтические методы:
· После трансплантации костного мозга при лейкемии у человека длительное время сохраняются такие негативные признаки, как кровоточивость дёсен, частые и длительные простудные заболевания, а также необоснованное появление синяков в любой части тела. Могут возникать и внутренние кровотечения. Это вызывается тем, что в его крови сохраняется большое количество бластов – незрелых белых клеток. Чтобы снизить риск развития этих побочных эффектов, человеку рекомендуется совмещать полноценный отдых с занятиями посильными видами спорта. Также специалисты рекомендуют соблюдение соответствующей диеты и ограничение пребывания на открытом солнце;
Могут возникать и внутренние кровотечения. Это вызывается тем, что в его крови сохраняется большое количество бластов – незрелых белых клеток. Чтобы снизить риск развития этих побочных эффектов, человеку рекомендуется совмещать полноценный отдых с занятиями посильными видами спорта. Также специалисты рекомендуют соблюдение соответствующей диеты и ограничение пребывания на открытом солнце;
· У больных апластической анемией после проведения пересадки костного мозга сохраняется сильная одышка и быстрая утомляемость, вызываемые даже незначительными нагрузками. Также высок риск возникновения как внутренних, так и наружных кровотечений, остановить которые очень трудно. Пациентам с выполненной трансплантацией при этом заболевании рекомендованы занятия неконтактными видами спорта. Также специалисты советуют им обращать усиленное внимание на соблюдение правил личной гигиены и избегание любых контактов с больными людьми. При самых незначительных признаках инфицирования следует обращаться к врачу;
· Больным с лимфомами после проведённой трансплантации грозит дальнейшее продолжение увеличения лимфоузлов на протяжении длительного времени. Им тоже рекомендуются занятия посильными видами спорта и соблюдение соответствующей диеты, подобранной специалистом.
Им тоже рекомендуются занятия посильными видами спорта и соблюдение соответствующей диеты, подобранной специалистом.
ПЕРЕСАДКА КОСТНОГО МОЗГА В ИЗРАИЛЕ
В стране имеется ряд крупных медицинских центров, в которых выполняется процедура трансплантации. У персонала огромный опыт проведения данной операции при самых разных заболеваниях. В израильских клиниках пересадка выполняется в следующих онкоцентрах:
- Государственная больница имени Хаима Шиба. В ней специалистами разрабатываются наиболее грамотные диагностические программы;
- Клиника Ихилов, врачи которой добились минимального травмирования здоровых тканей. Это является очень важным для процесса дальнейшего выздоровления;
- В онкоцентре сети клиник Ассута при госпитализации больному предоставляются расширенные первичные консультации.
Каждый год в Израиле проводятся и экспериментальные оперативные вмешательства такого типа. Они позволяют увеличивать срок жизни пациента при считавшихся ранее неизлечимыми заболеваниях. Перед трансплантацией во всех выполняющих её онкоцентрах этой страны для каждого больного проводится обязательное подготовительное лечение. Оно состоит из курсов радио- и химиотерапии, с помощью которых уничтожаются мутировавшие клетки крови, а также детоксикации, направленной на полное очищение организма.
Они позволяют увеличивать срок жизни пациента при считавшихся ранее неизлечимыми заболеваниях. Перед трансплантацией во всех выполняющих её онкоцентрах этой страны для каждого больного проводится обязательное подготовительное лечение. Оно состоит из курсов радио- и химиотерапии, с помощью которых уничтожаются мутировавшие клетки крови, а также детоксикации, направленной на полное очищение организма.
Операция по пересадке костного мозга в Израиле осуществляется прошедшими специальную подготовку специалистами. Для врачей-онкологов, выполняющих процедуру трансплантации, широко распространена практика стажировки, проводимой в ведущих медицинских центрах США, занимающихся данной проблемой. Это даёт израильским специалистам возможность овладеть всеми возможными методами выполнения операции.
Также гематологи этой страны являются первыми, кто начал применять при аллогенной трансплантации пересадку стволовых клеток. При проведении процедуры таким методом донором может быть любой человек.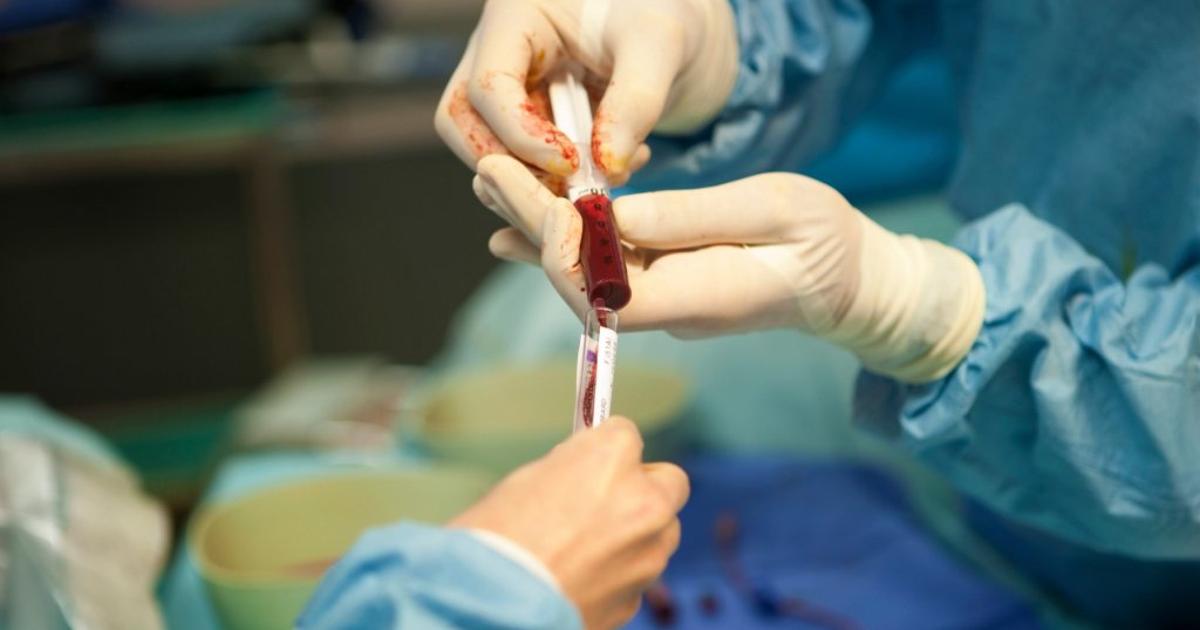 Кровное родство здесь не играет никакой роли.
Кровное родство здесь не играет никакой роли.
Особенности и преимущества замены костного мозга в Израиле заключаются в следующем:
· Огромный опыт врачей гематоонкологов из крупных клиник, в которых ежегодно проводится до 200 операций по пересадке костного мозга при разных заболеваниях. Процент успешных трансплантаций в израильских медицинских центрах заслуженно считается одним из самых высоких в мире;
· Возможность быстрого поиска донора для аллогенной трансплантации в связи с тем, что во всех клиниках имеются собственные банки органов. Помимо этого хорошо развито сотрудничество с Международным банком, содержащим сведения о людях, готовых сдать для спасения человека костный мозг;
· В палатах пациентов, перенёсших эту тяжёлую процедуру, имеется новейшее оборудование. Люди после операции уязвимы для всевозможных инфекций, так как их иммунная система функционирует недостаточно эффективно.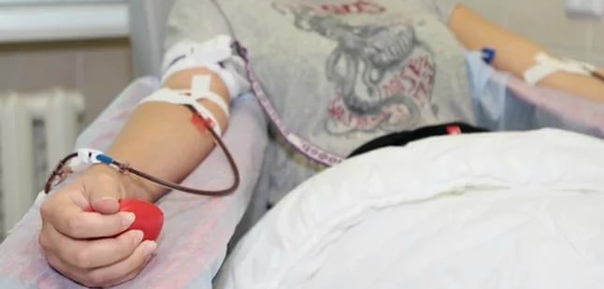 Для них предусмотрены отдельные стерильные камеры, имеющие особые системы фильтрации и вентиляции воздуха от микробов.
Для них предусмотрены отдельные стерильные камеры, имеющие особые системы фильтрации и вентиляции воздуха от микробов.
———————————————————————————————————————————————–
По вопросам проведения пересадки костного мозга или лечения в Израиле звоните нам по тел. +7-495-150-9020 (Россия) или оставьте заявку на бесплатную консультацию или же напишите нам на электронную почту [email protected]
Мы свяжемся с вами в самое ближайшее время!
——————————————————————————————————————————————–
Цены на пересадку костного мозга в Израиле
——————————————————————————————————————————————–
Отзывы о пересадке костного мозга
——————————————————————————————————————————————-
Пересадка костного мозга!
1. Что такое пересадка костного мозга?
Что такое пересадка костного мозга?
Пересадка костного мозга – это новейшая методика лечения. Применяется она для лечения болезней, ранее считавшихся неизлечимыми: лимфома, лейкоз, апластическая анемия, множественная миелома, рак груди или яичников и ряда других онкологических заболеваний. К сожалению, лишь 30% нуждающихся в пересадке костного мозга удаётся найти совместимого донора. Тем не менее, каждый год тысячи больных получают это спасительное лечение.
Основная функция костного мозга – кроветворение. Лейкоциты, тромбоциты и эритроциты вырабатываются из стволовых клеток костного мозга; кроме того, стволовые клетки обладают уникальной способностью превращаться в клетки любой ткани или органа. Наибольшее содержание этих ценных клеток — в костном мозгу крупных костей таза, грудины, а также в рёбрах и позвоночнике.
При ряде тяжелых заболеваний функция стволовых клеток искажается, в результате чего нарушается процесс кроветворения. Кровяных телец определённых групп становится слишком мало, или воспроизводятся они незрелыми, слишком большими, неспособными адекватно выполнять свои «задачи».
Кровяных телец определённых групп становится слишком мало, или воспроизводятся они незрелыми, слишком большими, неспособными адекватно выполнять свои «задачи».
Долгое время единственным способом лечения онкологических заболеваний была химиотерапия. Надо признать, что это вынужденное, но очень тяжёлое лечение с применением высокотоксичных веществ. Механизм действия химиотерапии таков, что вместе с больными клетками происходит массовая гибель и здоровых клеток, которых иногда и без того уже организм вырабатывает недостаточно. Но даже с таким отчаянным и очень мощным лечением многие больные были обречены, а некоторые из-за общего истощения с трудом переносили саму терапию.
Пересадка костного мозга, применяемая совместно с традиционным лечением, восполняет стволовые клетки, разрушаемые болезнью и дополнительно страдающие от лекарств. Для многих пациентов это единственный шанс продлить жизнь или полностью выздороветь.
Обязательно для ознакомления!
Помощь в лечении и госпитализации!
2. Совместимость костного мозга, получение костного мозга от донора
Совместимость костного мозга, получение костного мозга от донора
Совместимость костного мозга
Схема лечения с использованием донорского костного мозга включает два этапа:
- разрушение больных клеток собственного костного мозга;
- трансплантация здоровых стволовых клеток от донора.
Основная проблема для каждого кандидата на трансплантацию костного мозга – это поиск донора. Наиболее благоприятным прогноз является в том случае, если стволовые клетки получены от ближайшего родственника (в идеале – близнеца). Если среди родных нет подходящего для донорства человека, приходится искать в международном реестре доноров костного мозга. Чем генетически ближе клетки донора клеткам реципиента, тем меньше вероятность, что организм воспримет его как чужеродный и начнёт отторгать. Ещё опаснее, если в самом пересаженном материале включится иммунная защита и начнёт атаковать своего нового хозяина.
Иногда материалом для пересадки может стать собственный костный мозг больного.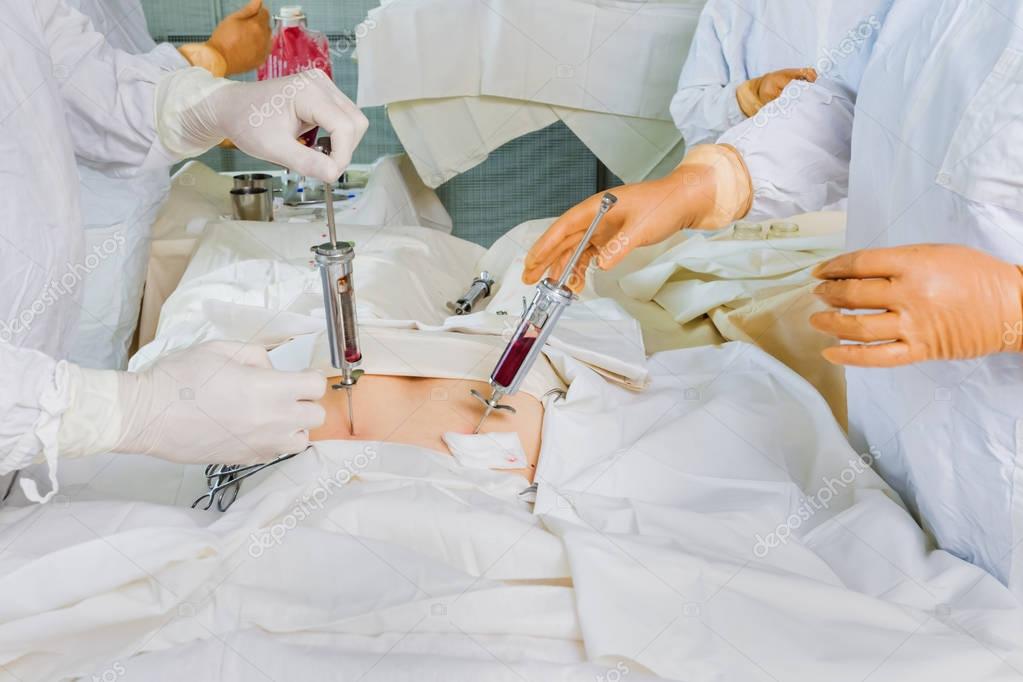 Такая операция, называемая «аутотрансплантация» , возможна при ряде злокачественных образований, локализованных в больных органах, но ещё не затронувших костный мозг. Иногда прибегают к фильтрации собственных стволовых клеток от затронутых болезнью, чтобы получить материал, пригодный для аутоиммунной пересадки.
Такая операция, называемая «аутотрансплантация» , возможна при ряде злокачественных образований, локализованных в больных органах, но ещё не затронувших костный мозг. Иногда прибегают к фильтрации собственных стволовых клеток от затронутых болезнью, чтобы получить материал, пригодный для аутоиммунной пересадки.
Получение костного мозга от донора
В зависимости от роста и массы реципиента, ожидающего пересадки, необходимое количество донорского материала может составлять от 950 до 2000 мл. Забор костного мозга происходит под общим наркозом, хотя не требует никаких разрезов кожи или тканей. Через проколы в тазовых и бедренных костях у донора в несколько приёмов шприцем изымается костный мозг, перемешанный с кровью. После процедуры забора костного мозга возможна болезненность в местах проколов, как после удара по кости, но обычно по выходу из состояния наркоза никаких неприятных ощущений не остается, и за несколько недель объём костного мозга у донора полностью восстанавливается.
Собранный материал при необходимости исследуется, очищается и замораживается.
Посетите нашу страницу
Онкология
3.Подготовка больного к пересадке костного мозга
Сама по себе процедура внедрения в организм донорского костного мозга достаточно проста. Стволовые клетки вводятся внутривенно и по кровеносной системе транспортируются в кости, где они должны прижиться. Проблема в другом: процесс присвоения донорского материала достаточно длителен и протекать он может тяжело. Для оценки целесообразности такой операции потенциального реципиента тщательно обследуют, чтобы взвесить показания и степень риска: достаточно ли в организме сил, чтобы пережить этот сложный период.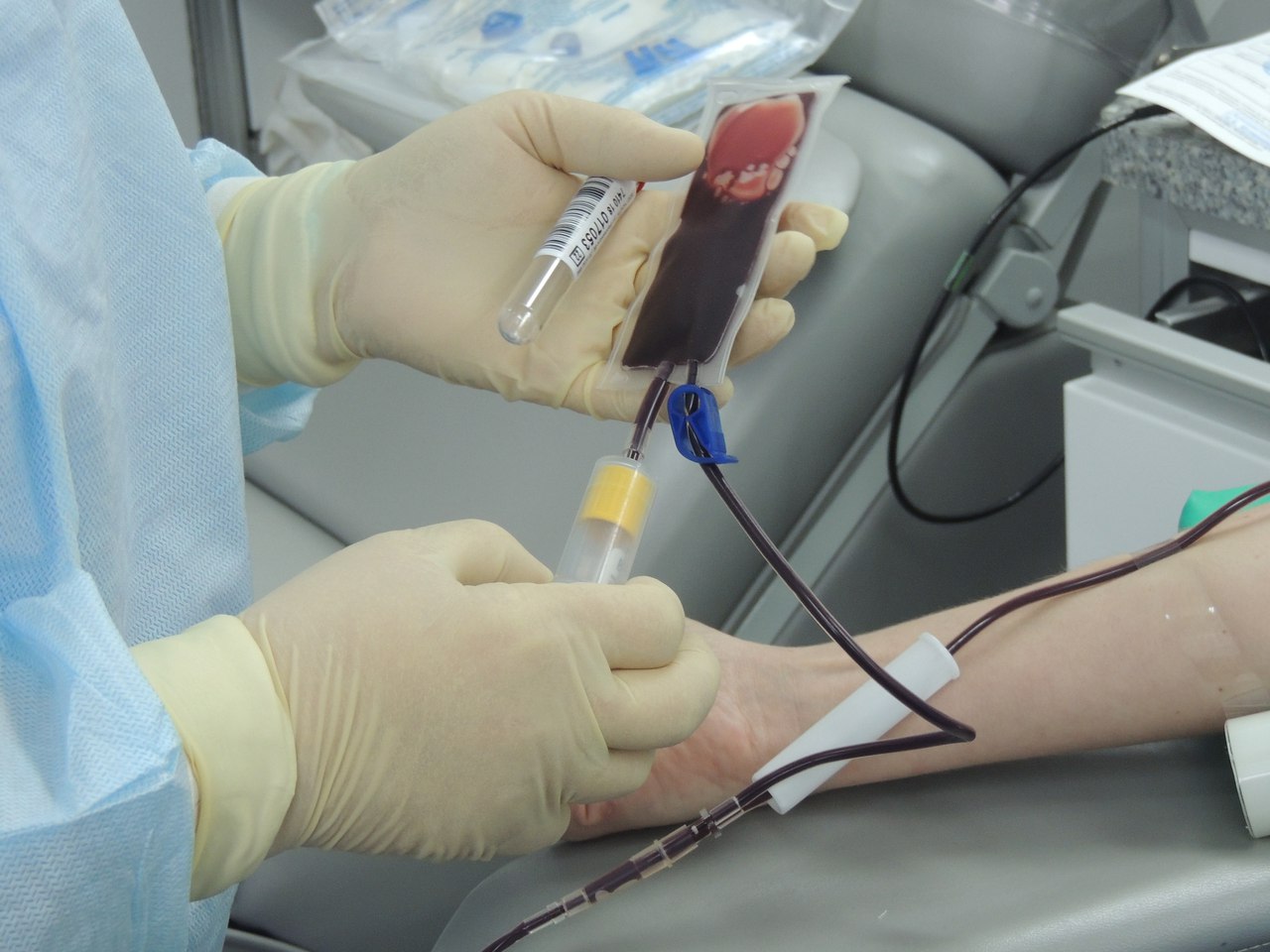 Все тяжёлые заболевания, требующие пересадки костного мозга, стремительно истощают организм, поэтому ресурсов на восстановление может просто не хватить, – несмотря на обязательную поддерживающую терапию, в том числе и гормональную.
Все тяжёлые заболевания, требующие пересадки костного мозга, стремительно истощают организм, поэтому ресурсов на восстановление может просто не хватить, – несмотря на обязательную поддерживающую терапию, в том числе и гормональную.
Важный подготовительный этап перед введением в организм здоровых клеток – это интенсивный курс химиотерапии и облучения, разрушающий собственные больные клетки. На этой стадии происходит подготовка костных тканей для заселения здоровыми клетками. Дозы воздействия перед трансплантацией костного мозга всегда выше тех доз, которые назначаются при стандартном лечении с использованием химио- и лучевой терапии.
Затем больному в крупную вену шеи устанавливается катетер, через который будет вводиться в организм донорский материал, а также все необходимые для восстановления лекарства.
Процедура пересадки, по сути, мало чем отличается от переливания крови. Производится она через один-два дня после химического и радиационного уничтожения собственного костного мозга, а затем наступает самый трудный для пациента период – адаптации и ожидания.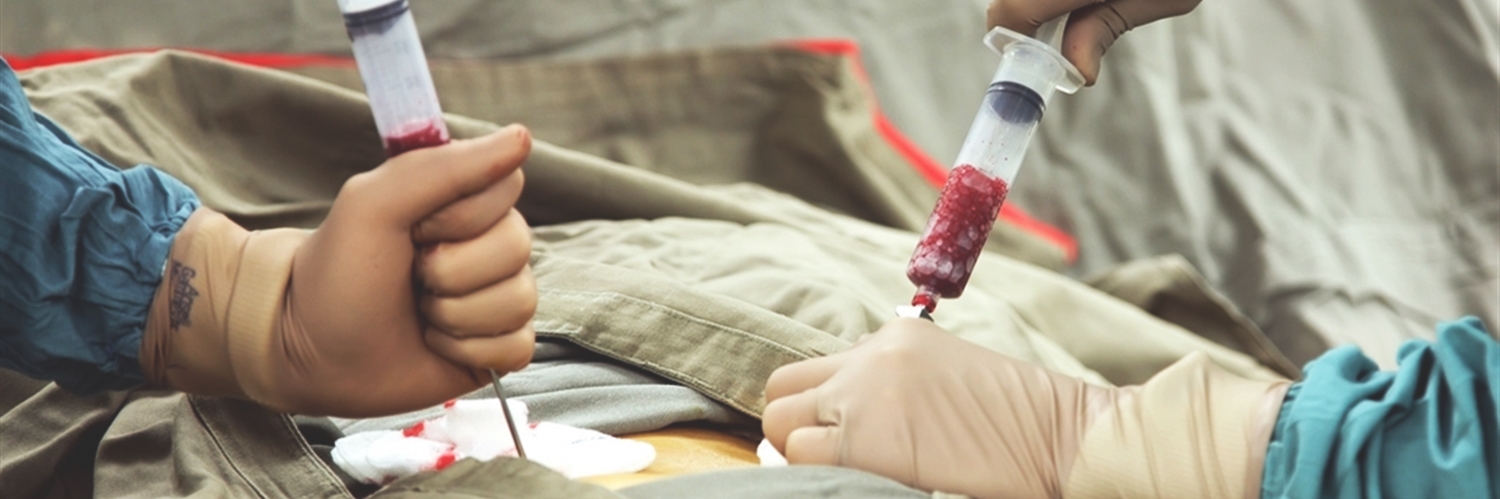
О нашей клинике
м. Чистые пруды
Страница Мединтерком!
4.Приживление костного мозга
До того момента, когда пересаженные стволовые клетки приживутся в новом для них организме и начнут работать, производя кровь и возвращая утраченный иммунитет, проходит 2-4 недели. В течение всего этого периода главной задачей является, в буквальном смысле слова, сохранение жизни больному. Высокие дозы химиотерапии перед трансплантацией полностью уничтожают иммунитет, состав крови почти не позволяет организму самостоятельно бороться с инфекциями и предотвращать кровотечения. На поддержание жизнедеятельности направлен ряд регулярных процедур: переливания крови, профилактический приём антибиотиков, постоянный ввод препаратов, снижающие риск отторжения нового костного мозга.
Принимаются также чрезвычайные асептические меры, по возможности исключающие занесение в палату вирусов и бактерий. Строго ограничиваются посещения, предметы и еда, которые передаются больному. Сам больной при необходимости выйти из палаты надевает перчатки, халат и маску, чтобы уменьшить риск инфицирования в нестерильной среде. Воздух в палате подвергается постоянной фильтрации и очистке.
Ежедневно у больного проводится забор анализов крови, позволяющий контролировать процессы приживления костного мозга и динамику выработки кровяных телец. По мере того, как новые стволовые клетки начинают выполнять свои функции, постепенно отменяются реабилитационные процедуры и снижается уровень изоляции от окружающей среды.
Весь период реабилитации длится от 4 до 8 недель. Большую часть времени состояние пациента остаётся достаточно тяжёлым: тошнота, выраженная слабость, поносы, лихорадка, изъязвление слизистых, кровотечения. Самочувствие схоже с симптоматикой гриппа, только очень затяжного, что само по себе истощает и без того ослабленный организм. Состояние изо дня в день может колебаться от удовлетворительного до очень тяжёлого. При всех болезненных и опасных проявлениях оказывается срочная симптоматическая медицинская помощь.
Состояние изо дня в день может колебаться от удовлетворительного до очень тяжёлого. При всех болезненных и опасных проявлениях оказывается срочная симптоматическая медицинская помощь.
Когда анализы показывают, что приживление костного мозга прошло успешно и больной больше не нуждается в поддерживающих и реабилитационных процедурах, врач принимает решение о выписке пациента. Как правило, ещё в течение года с этого момента человек не может вернуться в состояние полной работоспособности. Он очень слаб и должен регулярно посещать больницу для контроля состава крови, получения некоторых препаратов и даже переливаний крови, поскольку в этот период уровень необходимых кровяных телец может сильно снижаться. Не рекомендуется посещение мест большого скопления людей, полноценная активная жизнь и привычная деятельность не представляются возможными до тех пор, пока не произойдёт полное восстановление сил и не будет достигнута стабильность в работе нового костного мозга.
Необходимо отметить, что, несмотря на тяжесть процедуры и все опасности восстановительного периода, удачная пересадка костного мозга спасает жизнь и в значительной степени восстанавливает качество жизни. Оказавшись на грани неизбежной, казалось бы, смерти и «чудом» избежав ее, многие выздоравливающие переоценивают своё отношение к миру, заново открывая для себя то, что действительно важно.
Как происходит трансплантация костного мозга
При тщательном изучении прослеживается, что пересадка костного мозга – это процесс, имеющий технические сложности. Если человек желает быть донором, необязательно, что он им будет. Из-за реакций иммунной несовместимости сложно подобрать оптимальный материал для пересадки пациенту с лейкозом, лимфомой.
При планировании трансплантации костномозговой ткани требуется не только подобрать орган по системе HLA, но и изучить антигены других вариантов гистосовместимости. Нельзя выбрать идеальную ткань, так как всегда найдутся чужеродные химические вещества, которые будут отторгаться организмом реципиента. Задача при трансплантации костного мозга – подобрать материал с минимальным количеством несовместимых антигенов, что позволит контролировать реакции отторжения. Даже аутотрансплантация (пересадка собственных тканей) не является оптимальным вариантом при лимфомах и лейкозах, так как стволовые клетки не очищены от раковых структур. Повторное внедрение онкогенов способно спровоцировать обострение или облегчения клинических симптомов. Решение – на выбор врача при отсутствии альтернативных вариантов.
Как происходит пересадка
Перед трансплантацией реципиенту проводится «мощное» химиотерапевтическое воздействие, лучевое облучение. Задача процедуры – это уничтожение пораженных форменных элементов, находящихся внутри костномозгового канала. После полной нейтрализации зараженных клеток требуется пересадка здоровых стволовых клеток. После приживления донорских тканей можно рассчитывать на оптимальное кроветворение, но нужно контролировать реакции отторжения. Независимо от качества проводимой операции по пересадке костного мозга, нарушает приживление иммунное отторжение чужеродных тканей.
Существует 3 варианта взятия стволовых клеток у донора:
- Биопсия пунктата мозга путем хирургического вмешательства с обезболиванием. Самое распространенное место – плоские кости таза;
- Гемопоэтические стволовые клетки получаются после введения лекарственных препаратов, направленных на усиление выделения зачатков форменных элементов крови из внутрикостной полости. Забор осуществляется из вены путем пропускания крови через фильтры-сепараторы;
- При рождении ребенка трансплантат можно получить из пуповинной крови.
Последний вариант редко используется из-за невозможности точного определения фенотипа крови плода заранее. Только при необходимости внедрения большого количества стволовых клеток вариант с кровью из пуповины является идеальным.
Отдельный вариант – аутологичная трансплантация. Методика предполагает внедрение здоровых стволов клеток больного человека. Для выполнения манипуляции требуется заранее подготовить материал до возникновения болезни.
Некоторые онкологи используют технологии очистки крови больного, предполагающие до проведения химиотерапии взятие забора поврежденных клеток пациента. После уничтожения внутрикостного состава проводится подсадка собранного материала. Способ редко дает положительные результаты, но позволяет продлить жизнь при лейкозе, лимфомах (Ходжкина, неходжкинских).
Европейские ученые проводят исследования на предмет разработки уничтожения раковых клеток, взятых из костного мозга больного. Теоретически, после очистки крови от лейкозных зачатков, можно провести химиотерапию и внедрить излеченные стволовые клетки. Для этих целей проводится обработка специальными веществами, замораживание. Результаты экспериментов показывают высокую вероятность рецидивов после использования аутогенных тканей.
Какая пересадка лучше
Идеально проходит трансплантация материала с максимальной генетической схожестью. Такой костный мозг получается от сестры или брата с идентичной генной структурой. Сибсы обладают одинаковым генетическим кодом, аллогенная пересадка – это лучший вариант.
Еще одним достоинством способа является уменьшение дозы химиотерапии, так как аллогенные стволовые клетки не отторгаются.
Несмотря на полное отсутствие собственных тканей аутологичная трансплантация не обладает массой побочных эффектов. Внедрение собственных клеток, пораженных раком, при определенных болезнях не способствует избавлению от патологии.
При аллогенной трансплантации донорский иммунитет передается вместе со стволовыми клетками. Она находит раковые клетки и активно их уничтожает. Состояние в медицине определяется, как «реакция трансплантат против опухоли». При внедрении зачаточных клеток она имеет положительное значение, так как позволяет выработать защиту против лимфомы, лейкозов.
При пересадке органа с наличием чужеродных антигенов возникает второй вид реакции – «трансплантат против хозяина» (РТПХ). Состояние является неблагоприятным, так как организм уничтожает внедренные клетки, что приводит к отторжению нового костного мозга. Для исключения несовместимости гематологи перед пересадкой тщательно проверяют фенотипы реципиента и донора.
РТПХ после костномозговой пересадки исключается правильным подбором донора. По совместимости выделяют 3 варианта:
- С аналогичным генетическим кодом (совместимый). Иммунитет реципиента не отторгает ткани с аналогичным кодом, что обеспечивает максимальную эффективность. Лучшим кандидатом для подобной трансплантации являются родные сестра и братья. Гены родителей или детей не подходят, так как не обладают сходной информацией;
- Неродственное донорство предполагает трансплантацию от чужого человека с максимально подобными генами. Поиск осуществляется по отечественным и зарубежным регистрам;
- Несовместимое донорство. Внедрение элементов с несовместимым кодом также возможно, но только после специальной обработки, направленной на подавление реакций отторжения. Кровь пуповины ребенка богата стволовыми клетками, поэтому идеально приживается, но для исключения РТПХ требуется обработка.
Что нужно сделать перед пересадкой костного мозга
Перед процедурой необходимо полноценное обследование донора. За время от регистрации в регистре до выполнения трансплантации может пройти много лет и возникнут противопоказания к донорству.
После получения разрешения к сдаче костного мозга по медицинским показаниям проводится объяснение человеку сути последующих процедур, последствий для здоровья.
В больнице нужно будет провести несколько недель, поэтому потребуется решение бытовых вопросов с близкими родственниками, друзьями. Некоторые доноры составляют завещание в целях защиты от возможного отказа от дееспособности. Конечно, редко реакция на наркоз приводит к гибели человека. Риски минимизированы, но полностью не устранены.
Из-за особенностей здоровья может потребоваться введение определенных лекарственных препаратов. Избежать вторичных вливаний внутривенно помогает установка центрального катетера. Устройство используется на случай необходимости проведения экстренных медицинских процедур. Медицинский персонал ознакомлен с особенностями манипуляции, поэтому готов всегда оперативно оказать необходимую помощь.
Основные источники для забора материала – кровь или кость. Извлечение стволовых клеток из плоских костей таза осуществляется под эпидуральным обезболиванием. При процедуре пункция костномозгового субстрата проводится иглой. Точечная «откачка» осуществляется из некоторых участков тазовых костей и бедра. Другие источники среди специалистов менее популярны из-за сложности с доступом.
Для отбора гемопоэтических стволовых клеток проводится аферез. Суть манипуляции – подключение катетера на одну руку. Фильтрация аппаратом афереза и повторное возвращение крови донору через вену другой руки. Манипуляция осуществляется без обезболивания. Для увеличения количества стволовых клеток нужно будет выпить лекарственный препарат.
Последующее лечение донора проводится гранулоцитарным фактором роста.
Забор костного мозга происходит за день до планируемой трансплантации. С пересадкой медлить нельзя, так как иммунная система реципиента практически уничтожена химиотерапией, поэтому сильно подвержена инфицированию.
Как пересаживают костный мозг в Беларуси и Израиле
Популярность такой страны, как Беларусь для пересадки объясняется низкими ценами и высококвалифицированными трансплантолагами, которые поддерживаются на государственном уровне.
Белорусские врачи освоили изотрансплантологию, аллотрансплантацию, проводят операции при лимфоме, лейкозе, других гемобластозах.
Аутотрансплантация при лимфоме обеспечивает резистентность организма к новым тканям, но возникают недостатки, описанные выше.
Некоторое время стандартом лечения лимфопролиферативных лейкозов считалась аутотрансплантация, так как собственные стволовые клетки не должны были отторгаться. Белорусские врачи стали применять аллотрансплантацию при лимфомах с целью формирования реакции трансплантат против опухоли. При этом удалось снизить дозу химиотерапии.
При повторном появлении В-крупноклеточной лимфомы при аутотрансплантации костного мозга требовалась высокодозная химиотерапия для формирования стойкого безрецидивного периода. При этом большая часть умирала не от рака крови, а из-за последствий химиотерапевтического воздействия.
Белорусские онкогематологи добились смертности от химиотерапевтического воздействия при лейкозе не выше 5%.
Израильские ученые добились успехов при аллогенной трансплантации. Цены на медицинские услуги в этой стране не дешевы, но оправдываются непревзойденным качеством операции.
Аутологическая трансплантация не является хорошим вариантом при лимфомах и лейкозах. Больные стволовые ростки после повторного внедрения способны спровоцировать повторное возникновение гемобластоза. Пораженные лимфоциты не борются с онкологией, что не позволяет сформировать стойкую ремиссию.
Аллогенная пересадка костного мозга в Израиле также имеет риски. Положительным моментом является информационный обмен между схожими иммунными комплексами обоих участников процесса, но негативный момент – реакция трансплантат против хозяина (РТПХ). Ее подавление достигается использованием лекарственных препаратов, но дополнительные медикаменты формируют побочное действие.
Диета
При трансплантации состояние здоровье реципиента далеко от идеального, поэтому назначается диета. Основные принципы питания после костномозговой трансплантации:
- Употреблять только свежие блюда;
- Нельзя кушать пастеризованные продукты, свежее молоко, еду с длительными сроками хранения;
- Для предотвращения инфицирования ослабленного организма нельзя употреблять хлеб с плесенью, сыры;
- Разрешена свежая птица, рыба;
- Овощи разрешаются только в вареном виде;
- Минеральную воду, соки, напитки нужно пить сразу после открытия бутылки, иначе повышается вероятность инфицирования;
- Травы подаются на стол только варенными.
После костномозговой пересадки существенно уменьшается число белых кровяных клеток крови, что не позволяет организму справиться с инфекциями, поэтому после манипуляции проводится миелоаблативная терапия, направленная на повышение стимуляции выработки лейкоцитов.
После лечения осуществляется профилактика. Нельзя кушать грязными руками. Овощи и фрукты обязательно мыть. Для питья используется только стерилизованная вода. Душевые процедуры разрешены, но следует их проводить в чистом помещении после антисептической обработки.
Индивидуальная диета при трансплантации костного мозга назначается врачом, так как каждый случай лейкоза уникален.
В финальной части статьи опишем последствия костномозговой трансплантации.
У большинства больных после пересадки снижена иммунная защита организма, высока вероятность кровотечения по причине минимального числа тромбоцитарных факторов. Для предотвращения осложнений врачи назначают антибиотики, миелоаблативное лечение.
Динамический контроль состояния крови пациента проводится для определения необходимости вливания тромбоцитарной массы при угрозе кровотечения.
Краткосрочные последствия трансплантации – избыточная утомляемость, кожная реактивность, рвотный рефлекс, нарушение аппетита.
Другие осложнения появляются из-за лучевой и химиотерапевтической активности – помутнение хрусталика, катаракта, поражение сердца и почек, вторичные онкологические болезни. При выборе тактики ведения пациента с лейкозом врачи ориентируются на вред и пользу каждого способа терапии в индивидуальном случае. Если побочный эффект препаратов меньше, чем вред от раковой опухоли, требуется медикаментозная коррекция состояния. Трансплантологам сложно обойтись без лекарств, подавляющих реакции несовместимости чужеродных тканей.
Пересадка костного мозга при заболеваниях крови. Медкор
Пересадка костного мозга является либо завершающим этапом лечения, когда предыдущие методы не дали 100% положительного результата, либо основным при рецидиве рака крови.
В случае аллогенной трансплантации забор клеток костного мозга производится у донора. Напомним, что 9 пациентам из 10 необходимо ожидать в очереди на получение донора из общей базы при совпадении антител HLA.
Если планируется пересадка собственных стволовых клеток костного мозга, то забор этих клеток делают заранее. Если от донора, то незадолго до процедуры. Особая подготовка не требуется, только обследование.
Стволовые клетки для пересадки берут из тазовой кости пункцией, однако, наиболее современный и щадящий способ – это фильтрование стволовых клеток из периферийной крови после лекарственной стимуляции выброса нужных клеток в кровь (недельный прием препарата). Болезненные последствия для донора или самого пациента отсутствуют. Не больно.
Перед процедурой необходимо буквально «убить» собственный костный мозг, который производит мутированные кровяные клетки. Для этого проводится интенсивная высокодозная химиотерапия или высокоточная лучевая терапия. Если вариант ТКМ с донором, то дополнительно применяют большие дозы иммуносупрессоров, чтобы организм сразу не отверг чужой костный мозг.
Операция по пересадке костного мозга не что иное, как переливание, ведь костный мозг выглядит просто как пакет крови для переливания.
На 2-4 недели после пересадки пациента помещают в стерильную палату клиники, так как он находится в состоянии цитопении: старый костный мозг убит и не работает, новый костный мозг еще не прижился. В этот период для пациента опасны любые возможные инфекции, даже самые незначительные.
Еще в течение 2 месяцев после выписки из стерильной палаты пациента наблюдают или стационарно или амбулаторно. Каждую неделю он сдает анализы крови, мочи, находится под контролем своего онколога.
По окончании всего этапа лечения, пациент проходит обследование каждые 3 месяца в течение 1 года. Далее еще 4 года – каждые 6 месяцев. Перешагнув 5-летний рубеж выживаемости, пациент вступает в период длительной ремиссии, что в 80% случаях означает полное излечение. Обследование раз в год!
Итак, вся процедура трансплантации костного мозга при лейкозе крови, лейкемии, при множественной миеломе (миеломной болезни), лимфоме Ходжкина и неходжкинской лимфоме занимает 3-4 месяца.
Трансплантация костного мозга: виды, процедура и стоимость
6. Основные сведения о процедуре пересадки костного мозга
Перед трансплантацией
Перед началом трансплантации костного мозга необходимо провести обследование костного мозга. Тест костного мозга используется для определения необходимых вам типов клеток костного мозга. Ваш врач костного мозга определит, на какую процедуру анализа костного мозга пойти.
Если вы лечитесь от рака, вам могут сделать аспирацию костного мозга и биопсию костного мозга. Обычно он спрашивает у вас историю болезни и проводит медицинский осмотр. Это важный шаг, потому что врач должен быть уверен, что вы подходите для процедуры трансплантации. Эта фаза тестирования может занять несколько дней.
Процесс кондиционирования
Специалист по костному мозгу может назначить вам лучевую или химиотерапию, либо и то, и другое.Это делается перед процедурой пересадки костного мозга. Это можно сделать двумя способами.
- Мини-трансплантация или лечение пониженной интенсивности – это процесс, при котором лучевая и химиотерапия проводится в меньших дозах. Это в основном для пожилых людей и тех людей, которые уже страдают от проблем со здоровьем.
- Миелоаблативное или абляционное лечение – это процесс, при котором вам назначают лучевую терапию, химиотерапию или комбинацию обоих видов лечения в высоких дозах.Это используется для уничтожения раковых клеток, находящихся в организме. Обратите внимание, что в этом процессе погибают даже здоровые клетки костного мозга.
Причина, по которой процесс кондиционирования выполняется, состоит в том, чтобы подавить вашу иммунную систему, уничтожить раковые клетки (если вы страдаете от какого-либо типа рака) и позволить вашему костному мозгу быть готовым к новым здоровым стволовым клеткам, которые будут трансплантированы. Процесс кондиционирования может иметь один или несколько побочных эффектов, таких как осложнения со стороны органов, усталость, выпадение волос, рвота, катаракта, бесплодие, язвы во рту и диарея.
Центр трансплантации костного мозга | Больница Эмси
Что такое трансплантация костного мозга?
Трансплантация костного мозга – это метод лечения, который практикуется, когда дисфункция костного мозга развивается у пациентов с тяжелым заболеванием крови, некоторыми видами рака и заболеваниями иммунной системы или генетическими нарушениями.
Почему важна трансплантация костного мозга?
Костный мозг можно рассматривать как фабрику, где из стволовых клеток производятся эритроциты, лейкоциты и тромбоциты.Поскольку любое повреждение этого фактора может напрямую повредить стволовые клетки, это также влияет на производство клеток крови. Следовательно, при лечении некоторых заболеваний стволовые клетки следует заменять. Процедура в просторечии называется переносом костного мозга, но на самом деле это трансплантация стволовых клеток, собранных из определенных источников, таких как костный мозг, периферическая кровь и пуповинная кровь. Клетки крови – это красные кровяные тельца, белые кровяные тельца и тромбоциты. Красные кровяные тельца переносят кислород, который имеет жизненно важное значение для организма, в то время как белые кровяные тельца помогают бороться с инфекциями, а тромбоциты контролируют кровотечение.Эти три серии должны нормально функционировать, чтобы быть здоровым человеком. Когда болезнь поражает костный мозг и вызывает дисфункцию, трансплантация стволовых клеток, полученных из костного мозга, периферической крови и пуповинной крови, может быть лучшим вариантом лечения.
Какие заболевания требуют трансплантации костного мозга? Лейкемия и лимфомы, множественная миелома и некоторые другие заболевания плазматических клеток. Миелодиспластические синдромы и миелопролиферативные заболевания. Тяжелая апластическая анемия и другие нарушения работы костного мозга: тяжелый комбинированный иммунодефицит и другие генетические нарушения иммунной системы.Гемоглобинопатии. Некоторые генетические нарушения обмена веществ. Другие случаи рака для назначения высоких доз лекарств / лучевой терапии.
Кто являются донорами костного мозга (стволовых клеток) и как хранятся стволовые клетки?
Донор – это человек, который жертвует стволовые клетки. Донор требует, чтобы тканевые антигены (HLA) были совместимы с пациентом. Совместимость тканевых антигенов является обычным явлением у братьев и сестер, поэтому в первую очередь анализируются братья и сестры. Если братьев и сестер нет, проверяются мать, отец и другие члены семьи.Если среди родственников не удается найти подходящего донора, проводится проверка банков костного мозга. Во-первых, проверяются местные банки, и, если соответствующий донор не найден, проверка продолжается в международных банках.
Оказывается ли отрицательное влияние на здоровье донора костного мозга (стволовых клеток)?
Нет, донорство стволовых клеток не вредит здоровью донора. Если человек будет донором стволовых клеток для родственника, возрастные ограничения не учитываются. Однако людям, которые хотят пожертвовать стволовые клетки из банка тканей, должно быть от 18 до 55 лет.Донору вводят определенный препарат на 5 дней, чтобы мобилизовать стволовые клетки в кровоток. Когда количество стволовых клеток в крови достигает определенного уровня, они берутся из вены на руке, например, при заборе крови.
Какие бывают виды трансплантации костного мозга?
Из собственного тела пациента (аутологичный)
От кого-то другому пациенту (аллогенный)
Аллогенная трансплантация костного мозга требует родственного или неродственного донора.
Как проводится трансплантация?
Трансплантация аутологичных стволовых клеток – не вариант лечения всех заболеваний. Однако химиотерапия в высоких дозах и / или лучевая терапия необходимы в зависимости от заболевания. Высокие дозы химиотерапии вызывают гибель здоровых стволовых клеток. Таким образом, стволовые клетки пациента собираются, замораживаются и хранятся до того, как они будут повреждены. Замороженные стволовые клетки размораживают до температуры тела и вводят пациенту после завершения лечения высокими дозами лекарств и / или лучевой терапии.При аллогенной трансплантации стволовые клетки берут не из собственного тела пациента, а от здорового донора. Клетки, собранные у донора, пересаживают снова после того, как пациент получит лечение высокими дозами лекарств и / или лучевую терапию.
Чего следует ожидать пациентам в посттрансплантационный период?
Для всех трансплантатов наиболее острой проблемой является рецидив заболевания. В противном случае пациенты не испытывают особых проблем после аутотрансплантации.Основная проблема может развиться после аллогенной трансплантации. Хотя стволовые клетки пересаживаются от совпадающего донора или даже от брата или сестры, донор и пациент чужды друг для друга. Сильные клетки донора реагируют на клетки реципиента и повреждают их; таким образом, может развиться клиническая картина заболевания, называемого РТПХ (болезнь трансплантат против хозяина). Эта картина сопровождается кожной сыпью, болью во рту, сухостью глаз, диареей и желтухой. Пациенту будут назначены различные лекарства, чтобы предотвратить эти побочные эффекты во время трансплантации, но они могут наблюдаться, несмотря на все эти усилия.Наша цель – подавить РТПХ до легкой клинической картины. Здоровые клетки донора также повреждают больные клетки, и это ожидаемый эффект от лечения.
Новый метод трансплантации костного мозга без химиотерапии – ScienceDaily
Трансплантация стволовых клеток крови, широко известная как трансплантация костного мозга, является мощным методом, который потенциально может обеспечить пожизненное излечение от множества заболеваний.Но процедура настолько токсична, что в настоящее время применяется для лечения только самых критических случаев.
Теперь исследователи из Медицинской школы Стэнфордского университета придумали способ проведения терапии, которая на мышах значительно снижает ее токсичность. Если метод в конечном итоге окажется безопасным и эффективным для людей, он потенциально может быть использован для лечения аутоиммунных заболеваний, таких как волчанка, ювенильный диабет и рассеянный склероз; исправить врожденные нарушения обмена веществ, такие как болезнь пузыря; и лечить многие другие виды рака, а также делать трансплантацию органов более безопасной и успешной.
«Практически нет категории заболеваний или трансплантатов органов, на которые не повлияло бы это исследование», – сказал Ирвинг Вайсман, доктор медицины, соавтор исследования и профессор патологии и биологии развития в Стэнфорде. Документ с описанием этой техники будет опубликован 10 августа в журнале « Science Translational Medicine ».
Старший автор статьи – Джудит Шизуру, доктор медицинских наук, профессор медицины. Ведущими авторами являются научный сотрудник Аканкша Чхабра, доктор философии, и бывшие аспиранты Аарон Ринг, доктор медицинских наук, и Кипп Вейскопф, доктор медицины, доктор философии.
Токсичное лечение
Для успешной трансплантации стволовых клеток крови необходимо убить собственную популяцию стволовых клеток крови пациента. В настоящее время это делается с помощью химиотерапии или лучевой терапии, методов лечения, которые достаточно токсичны, чтобы повредить различные органы и даже привести к смерти. «Химиотерапия и облучение, используемые для трансплантации, повреждают ДНК и могут вызвать как немедленные проблемы, так и долгосрочное повреждение многих тканей тела», – сказал Шизуру. “Среди многих известных токсических побочных эффектов эти методы лечения могут вызвать повреждение печени, репродуктивных органов и мозга, потенциально вызывая судороги и нарушая неврологическое развитие и рост у детей.”По этим причинам трансплантация стволовых клеток крови используется только тогда, когда риски серьезного заболевания перевешивают осложнения после трансплантации.
Чтобы избежать этих ужасных побочных эффектов, исследователи из Стэнфорда составили симфонию биологических инструментов, которые открывают путь для трансплантации стволовых клеток крови без использования химиотерапии или лучевой терапии.
С использованием антител
Ученые начали с антитела против белка клеточной поверхности под названием c-kit, который является основным маркером стволовых клеток крови.Присоединение антитела к c-kit привело к истощению стволовых клеток крови у мышей с иммунодефицитом. «Однако само по себе это антитело не будет эффективным для иммунокомпетентных реципиентов, которые представляют большинство потенциальных реципиентов трансплантата костного мозга», – сказал Чабра. Исследователи стремились повысить эффективность, объединив его с антителами или с биологическими агентами, которые блокируют другой белок клеточной поверхности, называемый CD47. Блокирование CD47 высвобождает макрофаги, чтобы «съесть» клетки-мишени, покрытые антителом c-kit, сказал Чабра.
С заблокированным маркером CD47 и антителом, присоединенным к белкам c-kit, иммунная система эффективно истощила кроветворные стволовые клетки животных, расчищая путь для трансплантированных стволовых клеток крови от донора, чтобы они поселились в костном мозге и генерировать новую кровь и иммунную систему.
Сравнивая трансплантацию стволовых клеток крови с посадкой нового поля сельскохозяйственных культур, Шизуру отметил, что исследователи не только нашли более безопасный способ расчистить поле для посадки, но «мы также использовали более безопасные методы для засева новых кроветворных клеток.«В настоящее время трансплантаты костного мозга включают смесь клеток, которая включает в себя стволовые клетки крови, а также различные иммунные клетки от донора, которые могут атаковать ткань реципиента трансплантата. Эта иммунная атака приводит к так называемой болезни” трансплантат против хозяина “. , которые могут повредить ткани и даже убить пациентов.
Опираясь на знания, полученные в ходе предыдущих исследований, команда очистила донорскую ткань так, чтобы она содержала только стволовые клетки крови, а не другие иммунные клетки, вызывающие реакцию «трансплантат против хозяина».
Успех этих методов на мышах вселяет надежду на то, что аналогичные методы будут успешными и у людей. «Если это сработает на людях, как на мышах, можно ожидать, что риск смерти от трансплантации стволовых клеток крови упадет с 20 процентов до практически нуля», – говорит Шизуру.
«Новая эра в лечении болезней»
«Если и когда это будет достигнуто, наступит совершенно новая эра в лечении заболеваний и регенеративной медицине», – сказал Вайсман, директор Стэнфордского института биологии стволовых клеток и регенеративной медицины, а также директор Ludwig Центр исследования стволовых клеток рака и медицины.
Как только кровь и иммунная система пациента могут быть безопасно заменены, любое заболевание, вызванное собственной кровью и иммунными клетками пациента, потенциально может быть излечено с помощью одноразовой трансплантации стволовых клеток крови, сказали они. Безопасная замена крови пациента и иммунных клеток позволит избавиться от клеток, которые атакуют их собственные ткани и вызывают такие заболевания, как ревматоидный артрит и диабет 1 типа.
Метод безопасной трансплантации стволовых клеток крови также потенциально может сделать трансплантацию органов более безопасной и простой, говорят исследователи.В настоящее время люди, которым делают трансплантацию органа, должны всю оставшуюся жизнь оставаться на лекарствах, которые не дают их иммунной системе атаковать пересаженный орган. «Даже если вы принимаете иммунодепрессанты, функции большинства трансплантатов органов со временем ухудшаются или перестают работать, а сами иммунодепрессанты делают пациента более восприимчивым к опасным для жизни инфекциям или вновь формирующимся ракам», – сказал Вайсман.
Но если кровь и иммунные стволовые клетки от донора органа могут быть трансплантированы одновременно с органом, новая иммунная система распознает донорский орган, а не атакует его, говорят исследователи.«Пересаженные клетки, донорский орган и собственные ткани пациента учатся сосуществовать», – сказал Шизуру. «Стволовые клетки донорской крови перевоспитывают иммунную систему пациента, и трансплантированный орган не выбрасывается».
Трансплантация крови и иммунных стволовых клеток также может иметь решающее значение для успеха новой эры регенеративной медицины. Если стволовые клетки для органов или тканей, таких как сердце или печень, выращиваются для общей трансплантации, то есть не предназначены специально для одного пациента, пациенту потребуется иммунное кондиционирование посредством трансплантации стволовых клеток крови, чтобы стволовые клетки не отвергались как чужеродные. тела, сказали исследователи.
Thalassemia.com: Трансплантация костного мозга
ТРАНСПЛАНТАЦИЯ ГЕМАТОПЕЙСКИХ КЛЕТОК
Трансплантация гемопоэтических клеток (HCT) – единственное лечение, которое предлагает потенциальное излечение от талассемии в настоящее время. HCT полагается на химиотерапию с высокими дозами для устранения клеток, продуцирующих талассемию, в костном мозге и замены их здоровыми донорскими клетками из костного мозга или пуповинной крови, обычно взятых из совпадения человеческого лейкоцитарного антигена (HLA): идентичного брата или сестры.Эту терапию следует рассматривать для всех пациентов, у которых есть подходящий донор. Рекомендуется раннее направление в центр трансплантологии, так как HCT дает лучший результат у более молодых пациентов.
Пациенты до HCT классифицируются как пациенты 1, 2 или 3 класса на основании факторов риска, которые влияют на исход после HCT. Эти факторы риска включают:
- возраст пациента
- адекватность хелатирования
- Наличие или отсутствие фиброза печени
- Наличие или отсутствие гепатомегалии
Общая выживаемость без талассемии у пациентов с трансплантацией стволовых клеток братьев и сестер с низким риском и HLA-сопоставлением составляет от 85 до 90 процентов, с общей выживаемостью 95 процентов.Хотя новые подходы к пациентам 2 и 3 классов не столь эффективны, они значительно улучшили их общую выживаемость. Проблемы отторжения и приживления трансплантата у этих пациентов улучшаются с использованием более интенсивной иммуносупрессивной терапии.
Если рассматривается возможность HCT, пациентов следует направлять в ближайший центр трансплантологии, имеющий опыт проведения HCT при генетических заболеваниях. Печень, легкие, сердце и скелет являются конкретными мишенями для осложнений талассемии и хронического переливания крови.Перед HCT необходимо провести следующие исследования.
- Определение стадии фиброза печени и воспалительных поражений с помощью биопсии печени в соответствии с числовой балльной системой Knodell (Knodell, R.G., et al. Hepatology 1 [1981]: 431.) с измерением LIC
- Измерение функции печени, сердца, эндокринной системы, почек и легких
- Стоматологическая экспертиза и реставрация
Перегрузка железом после HCT
После успешного HCT показано непрерывное лечение уже существовавшей перегрузки железом.
После HCT следует проводить флеботомию 5 см3 / кг в месяц до тех пор, пока содержание железа в печени не станет менее 7,5 мг / г сухого веса. Для пациентов, которым невозможно провести флеботомию, также эффективна хелатирующая терапия с использованием дефероксамина, но она более трудоемка и дорогостоящая, чем флеботомия.
Если предтрансплантационная биопсия печени была выполнена более чем за два года до начала флеботомии, рассмотрите возможность повторного измерения LIC неинвазивными методами или биопсией печени, чтобы подтвердить исходный уровень железа в печени.Измерение LIC неинвазивными методами или биопсией печени следует продолжать каждые 12–24 месяца, чтобы контролировать реакцию на флеботомию. Флеботомия после HCT должна выполняться, если содержание железа в печени до HCT превышает 7 мг / г сухого веса, или если уровень ферритина превышает 2000 нг / мл.
Экспериментальный HCT
Поскольку трансплантация HLA-совместимого брата у здоровых пациентов с талассемией обеспечивает очень высокий уровень излечения, изучаются варианты стволовых клеток для семей, не имеющих одинаковых братьев и сестер.У большинства пациентов нет HLA-подходящего брата или сестры. Проводятся экспериментальные испытания с неродственной, подобранной трансплантацией пуповинной крови или стволовых клеток. Альтернативные иммуносупрессивные препараты и терапия изучаются для уменьшения реакции «трансплантат против хозяина» и повышения выживаемости трансплантата. Беременные матери больных детей чаще проходят пренатальную диагностику талассемии и определяют HLA-типирование плода на пренатальном образце. Если есть совпадение с братом или сестрой, клетки пуповинной крови можно сохранить для трансплантации.Экспериментальная процедура, называемая предимплантационной генетической диагностикой, является опцией, доступной для предварительно выбранных HLA-совместимых доноров пораженных братьев и сестер.
Загрузите информационный бюллетень BMT (PDF) для пациентов.
747 52nd Street, Окленд, Калифорния 94609 •
Телефон: (510) 428-3347 • Факс: (510) 450-5647
© 2003-2012 Детская больница и исследовательский центр Окленда
Центр трансплантации костного мозга Memorial
О отделе
Группа здравоохранения Memorial, имеющая международную репутацию в области трансплантации органов, предлагает услуги через Центр трансплантации костного мозга Memorial в соответствии со своим видением быть справочным центром во многих филиалах в Турции.Отделение, которое нацелено на удовлетворение потребностей в трансплантации костного мозга пациентам, приехавшим из многих других стран, включая Стамбул и Турцию, имеет все возможности, полученные с помощью современных технологий.
Наличие 3 разных центров трансплантации костного мозга в 3 разных городах Турции дает пациентам преимущество в выборе и гибкости сроков.
Помимо соблюдения международных стандартов трансплантации костного мозга, центр предлагает все услуги, необходимые пациентам.Тем, у кого есть заболевания крови, такие как множественная миелома (злокачественное заболевание костного мозга, вызванное плазматическими клетками), лимфома (гематологический рак лимфатических узлов), острый лейкоз (рак крови) и хронический лейкоз, апластическая анемия, могут пройти трансплантацию костного мозга в центре где процессы лечения проводятся в рамках междисциплинарной структуры.
Пересадка костного мозга / трансплантация стволовых клеток
Стволовые клетки – это клетки, которые отвечают за производство крови в организме человека.Трансплантат этих клеток, которые выполняют совершенно особые функции, обычно называют «трансплантацией костного мозга» или «трансплантатом стволовых клеток». Трансплантация костного мозга называется «аутологичной трансплантацией», когда она выполняется пациенту с использованием его собственных стволовых клеток, и называется «аллогенной трансплантацией», когда она выполняется клетками, взятыми у родственников или от неродственных доноров, совместимых с тканями. Стволовые клетки крови пересаживаются в трансплантат костного мозга.
Раньше стволовые клетки собирали непосредственно из костного мозга с помощью специальных игл в условиях операционной.Однако сегодня этот метод применяется редко. В последние годы стволовые клетки переносятся из костного мозга в кровь с помощью специального лекарства, а клетки собираются методом, называемым «аферез». Этот метод не требует хирургического вмешательства. Трансплантация костного мозга также не требует хирургического вмешательства. Костный мозг пересаживается пациенту через сосудистый доступ, клетки костного мозга сами находят костный мозг по своим биологическим свойствам и начинают производство крови.

 Что такое пересадка костного мозга?
Что такое пересадка костного мозга? Совместимость костного мозга, получение костного мозга от донора
Совместимость костного мозга, получение костного мозга от донора