симптомы и лечение у взрослых
Риносинусит хронический – это хроническое воспаление слизистой оболочки полости носа с распространением на околоносовые пазухи. Воспаление в околоносовой пазухе приводит к отеку слизистой оболочки, в том числе в области соустья (отверстия, соединяющего полость пазухи с полостью носа), просвет соустья сужается, что приводит к уменьшению поступления в пазуху кислорода с вдыхаемым воздухом. Недостаток кислорода способствует дальнейшему воспалению и отеку слизистой оболочки. Далее рассмотрим, что это такое, какие симптомы и признаки у взрослых, а также какое лечение применяют.
О хроническом риносинусите
Хронический риносинусит – это воспалительный недуг хронического характера, поражающий слизистые оболочки носа и постепенно распространяющийся на околоносовые пазухи. Чаще патология поражает людей из возрастной категории 45–70 лет. Представительницы прекрасного пола болеют чаще, чем мужчины.
Хронический риносинусит может поражать гайморову, фронтальную, сфеноидальную и решетчатую околоносовые пазухи.
По мере прогрессирования недуга слизистая пазух и носа из-за воспаления становится толще, и отекает. При этом соустья блокируются – формируется специфическая камера, в которой постепенно скапливается экссудат слизистого или гнойного характера. Длительность хронического риносинусита – около 12 недель. Код по МКБ-10 – J32.
Причины
Основные причины:
- Нелеченный или недолеченный острый риносинусит (воспаление околоносовых пазух).
- Анатомические особенности носовой полости, препятствующие нормальной вентиляции околоносовых пазух (например, искривления перегородки носа). Могут быть врожденными и приобретенными (в результате травмы носа, лица).
- Причиной хронического верхнечелюстного синусита (гайморита) могут быть заболевания зубов верхней челюсти или стоматологические вмешательства на них.
- Аллергия.
- Неблагоприятные факторы внешней среды (вдыхание запыленного, загазованного воздуха, токсических веществ).
- Курение, злоупотребление алкоголем.

Виды
Название «риносинусит» редко используется лор-врачами старой, постсоветской школы. В отечественной оториноларингологии принято разделять воспалительный процесс по его локализации:
- Полость носа – ринит;
- Верхнечелюстная пазуха – гайморит;
- Лобная пазуха – фронтит;
- Клиновидная – сфеноидит;
- Решетчатая пазуха – этмоидит.
Такое разделение облегчает классификацию заболевания по МКБ-10, структурирует лечение, но не учитывает того факта, что при воспалении в одной пазухе, так или иначе в инфекционный процесс вовлекаются все придаточные пазухи и полость носа. Симптомы и лечение хронического риносинусита у взрослых зависят преимущественно от типа заболевания.
Можно выделить следующие разновидности патологии:
- Гнойный;
- Гиперпластический: кистозный, полипозный, кистозно-полипозный;
- Гнойно-гиперпластический;
- Отечный (при хроническом или вазомоторном рините).
По МКБ-10 нет единого кода для хронического риносинусита. Номенклатура зависит от вида процесса.
Номенклатура зависит от вида процесса.
Симптомы у взрослых
Симптомы патологии проявляются у пациента постепенно. Иногда они могут быть выражены не ярко, и сам больной не обращает на них внимания. Но по мере прогрессирования недуга проявляются такие признаки:
- снижение обоняния;
- заложенность носа. Данный симптом доставляет пациенту много неудобств, так как он не может полноценно дышать;
- голос становится гнусавым;
- из носа может периодически выделяться гнойный экссудат;
- слизь из носа стекает по задней стенке глотки;
- слезотечение;
- тяжесть в различных участках лица. Данный симптом обусловлен скоплением экссудата в пазухах;
- головная боль. Приём обезболивающих препаратов даёт только временное облегчение, после чего этот симптом снова возвращается.
В период обострения наблюдаются такие симптомы:
- усиление заложенности носа;
- гипертермия, но не выше 37,5–38 градусов;
- из носовой полости выделяется вязкая слизь коричневого, зелёного или белого цвета;
- боль в лицевой области;
- выраженная головная боль.
 Данный симптом проявляет себя наиболее интенсивно в случае прогрессирования гнойного процесса.
Данный симптом проявляет себя наиболее интенсивно в случае прогрессирования гнойного процесса.
Осложнения
Вирусный синусит, как правило, не представляет опасности, а вот бактериальная инфекция может иметь тяжелые последствия, особенно, если ее не пролечить правильным образом. Осложнения риносинусита возникают, как прямая эрозия тонких стенок пазух, прилегающих к орбите и черепу, или через гематогенное распространение.
Среди возможных осложнений может быть:
- орбитальный целлюлит;
- орбитальный абсцесс;
- остеомиелит;
- субдуральная или эпидуральная эмпиема;
- менингит;
- энцефалит мозга;
- корковый тромбофлебит;
- кавернозный синусовый тромбоз.
Раннее обнаружение этих осложнений жизненно важно.
Признаки тяжелого течения болезни включают:
- лихорадку;
- отек вокруг глаз;
- красную и воспаленную кожу;
- сильную лицевую боль;
- чувствительность к свету;
- диплопию и уменьшение остроты зрения.

Если вы замечаете подобные симптомы – срочно обратитесь к врачу!
Методы диагностики
Диагностировать хронический риносинусит может только доктор после осмотра пациента. Используются:
- Риноскопия;
- Отоскопия;
- Фарингоскопия.
Также важно, какие симптомы опишет пациент. Впоследствии будут назначены лабораторные исследования, которые смогут подтвердить или опровергнуть предварительный диагноз. Например, микробиологическое исследование содержимого носоглотки и пазух позволяет понять, что является возбудителем заболевания: бактерии, аллергия, инфекции и т.д.
Также может быть назначена компьютерная томография или рентгенография для выявления жидкости в пазухах.
Лечение хронического риносинусита у взрослых
Лечение хронического риносинусита у взрослых и детей направлено на:
- снижение отека синусовых тканей;
- облегчение дренирования слизи;
- устранение сопутствующих инфекций.

Кроме того, чтобы вылечить риносинусит, нужно ликвидировать такие предрасполагающие факторы, как аллергия, искривление перегородки носа, полипы и т.д. Пациентам с иммунодефицитом следует вводить внутривенную иммуноглобулиновую терапию.
Четкий принцип лечения хронического риносинусита до конца не установлен, по большей части из-за того, что врачи не могут определить точные причины его происхождения.
Препараты и операция
В разных случаях применяют такие методы:
- Кортикостероиды. Они снимают симптомы болезни, но неясно, связано ли это с уменьшением заложенности носа или уменьшением воспаления в самих пазухах. Имеются данные о том, что кортикостероиды эффективны при полипозном хроническом риносинусите. Предпочтительно использовать назальные средства, то есть капли и спреи: «Назонекс», «Беконазе», «Ризонел», «Назофан». Они подходят для лечения хронического риносинусита у детей и взрослых. Курс лечения длится 1-3 месяца или больше.
 В тяжелых случаях или перед проведением операции могут порекомендовать пройти 3-5-дневный курс оральных кортикостероидов.
В тяжелых случаях или перед проведением операции могут порекомендовать пройти 3-5-дневный курс оральных кортикостероидов. - Противоотечные средства. Для устранения заложенности носа и насморка можно периодически использовать сосудосуживающие средства («Нафтизин», «Назолонг», «Ксинос», «Риноксил», «Назол» или др.), которые устраняют отек. Беременным их можно применять только с разрешения врача!
- Орошение гипертоническим солевым раствором. Этот способ помогает очистить носовые ходы и облегчить симптомы болезни, но не лечит ее. В аптеке можно приобрести готовый солевой раствор для промывания носа в удобном флаконе, например, «Но-Соль», «Физиодоза», «Носален», «Физиомер», «Аква Марис». Делать промывания носа полезно при любом виде хронического риносинусита, причем такие процедуры можно совмещать с любыми другими лекарственными средствами. Солевой раствор безопасен даже для самых маленьких детей и беременных женщин.
- Антигистамины. Аллергический хронический риносинусит нужно дополнительно лечить противоаллергическими препаратами.

- Антибиотики. Они показаны при гнойном риносинусите, но их не следует вводить, если нет подозрений на острую бактериальную инфекцию. Беременным антибиотики прописывают в крайних случаях. Препаратом первой линии обычно является «Амоксициллин» или «Амоксиклав». Если они не дают результата, то назначают другой антибиотик, с более широким спектром действия. Длительность курса при хронической форме составляет 2-3 недели, но при необходимости его продлевают.
- Противогрибковые препараты. Они необходимы, если болезнь вызвана грибками. Местные противогрибковые средства (например, Амфотерицин В) подавляют рост грибков и уменьшают воспаление.
- Хирургия. Уже давно является методом выбора для запущенных случаев хронического риносинусита, который не поддается медикаментозному лечению.
 С появлением эндоскопии большинство операций теперь минимально инвазивны. Целью хирургического лечения является восстановление вентиляции синусов, коррекция и восстановление функциональности слизистой оболочки. Функциональная эндоскопическая операция при хроническом риносинусите помогает добиться позитивных результатов с полным или умеренным облегчением симптомов у 80-90% пациентов. Конечно же, операцию необходимо дополнять медикаментозной терапией.
С появлением эндоскопии большинство операций теперь минимально инвазивны. Целью хирургического лечения является восстановление вентиляции синусов, коррекция и восстановление функциональности слизистой оболочки. Функциональная эндоскопическая операция при хроническом риносинусите помогает добиться позитивных результатов с полным или умеренным облегчением симптомов у 80-90% пациентов. Конечно же, операцию необходимо дополнять медикаментозной терапией.
👩🏻⚕️ Терапию продолжают до тех пор, пока не наступит ремиссия, но через какое-то время может случиться обострение. Обострение риносинусита хронической формы снова подвергают лечению по той же схеме или при необходимости рассматривают другие варианты.
Народные средства
Как лечить хронический риносуинусит при помощи народной медицины? Эффективными выступают следующие народные средства:
- Отвар коры дуба. 5-10 грамм высушенной коры залить крутым кипятком. Оставить настаиваться, после чего процедить и можно приступать к промыванию полостей носа.
 Благодаря этому нормализуется состояние слизистой носа. Значительно ускоряется процесс восстановления. Такой отвар обладает антифлогистическим эффектом.
Благодаря этому нормализуется состояние слизистой носа. Значительно ускоряется процесс восстановления. Такой отвар обладает антифлогистическим эффектом. - Отвар календулы и ромашки. Календула оказывает благоприятное воздействие на весь организм. Ромашка выступает сильным антисептиком. Календулу возможно заменить на зверобой либо тысячелистник.
- Применение эфирных олиф. С их помощью делаются ингаляции либо просто наносить на пазухи носа. В этом случае облегчается дыхание больного.
- Состав из соли и соды. Характеризуется противобактериальным и антисептическим эффектом. Состав готовят 1:1 и разбавляют 0,25 литрами жидкости. Она должна быть горячей.
- Справиться с недугом также помогают мед и алоэ. Сладкий нектар разводится теплой водой и закапывается в нос. Сок алоэ устраняет заложенность носа.
Хронический риносинусит – это недуг, требующий пристального внимания и грамотного излечения. В противном случае возникают тяжелые обострения и осложнения. Больной может страдать от симптомов недуга на протяжении нескольких лет.
Больной может страдать от симптомов недуга на протяжении нескольких лет.
Риносинусит операция – полипозный, хронический
В особо тяжелых случаях единственной эффективной помощью при воспалении слизистых оболочек носа и придаточных пазух, что диагностируется как риносинусит, является операция.
Обусловлено это тем, что очаги воспаления и отмершие ткани не всегда удается устранить при помощи фармакологических препаратов, а это увеличивает вероятность рецидивов.
Также существует риск распространения инфекции на ткани глаз или в кору головного мозга, что нередко приводит к летальному исходу.
Нос человека – уникальный орган, имеющий особую транспортную систему. Его внутренняя оболочка покрыта эпителием с ресничками, которые обеспечивают движение выделяемой слизи.
В процессе дыхания в нос попадает множество частичек пыли, грязи, вредоносные микроорганизмы.
Подталкиваемая расположенными по направлению внутрь ресничками, слизь омывает все полости органа, включая пазухи, после чего другие реснички выталкивают ее к выходу.
Острые или хронические воспалительные процессы провоцируют отек слизистой оболочки, что приводит к нарушению воздушной вентиляции, дренажной функции пазух, к накапливанию в них секрета.
Несмотря на развитие современной медицины, воспаление оболочки носа и околоносовых пазух — наиболее распространенная патология из всех существующих заболеваний верхних дыхательных путей.
Определение
Риносинусит чаще бывает вызван вирусными инфекциями, реже — сезонной или круглогодичной аллергией, при этом нередко наблюдается развитие осложнения в виде бактериальных воспалений.
В отоларингологической практике первичным считается острым, симптомы которого после адекватного лечения полностью исчезают. Повторные вспышки заболевания называются рецидивирующим.
Повторяющиеся 3–4 раза на протяжении года признаки инфекции или не исчезающие более 12 недель уже определяются как хронический процесс.
Воспаление может быть локализовано в одной из пазух:
- верхнечелюстной;
- клиновидной;
- лобной.

Нередки случая, когда воспаляются сразу несколько пазух и ячейки решетчатой кости.
Опасной разновидностью является полипозный риносинусит, для которого характерен хронический отек тканей, что ведет к патологическому разрастанию слизистой оболочки и образованию полипов, перекрывающих носовые ходы.
Показания
Показаниями к проведению хирургического лечения являются:
- воспалительные гнойные процессы полости носа и пазух;
- грубое затруднение дыхания через нос;
- наличие локальных или массивных полипозных образований;
- аномалии в строении эндоназальных структур;
- слизистые кисты;
- распространение инфекции;
- грибковые поражения пазух.
Противопоказания
Операция противопоказана у пациентов:
- во время обострения бронхиальной астмы или хронического обструктивного бронхита;
- при наличии сезонной аллергии в период цветения растений.

Всегда ли нужно делать операцию при риносинусите
Операция при риносинусите проводится не во всех случаях.
В первую очередь отдается предпочтение медикаментозному лечению, которое включает:
- антибактериальную терапию;
- сосудосуживающие и противоотечные препараты;
- противовоспалительные и муколитические средства;
- иммуномодулирующие;
- антигистаминные, глюкокортикостероидные препараты.
При отсутствии полипов эффективно промывание пораженных пазух раствором антисептика. Иногда целесообразно введение катетера, через который происходит отток жидкости.
Назначаются:
- теплые носовые души изотоническим раствором;
- физиотерапия.
Хирургическое лечение проводится только в крайних случаях:
- если медикаментозная терапия оказалась неэффективной;
- существует угроза развития орбитальных или мозговых осложнений.
Видео: Как удаляют полипы
youtube.com/embed/7TNhI_K0VVE” frameborder=”0″ allowfullscreen=””/>
Нужно ли хирургическое вмешательство при полипозной форме
Операция при полипозном риносинусите также необходима не всегда, а только в случаях неэффективности медикаментозной терапии.
Но на практике хирургическое вмешательство проводится чаще, что обусловлено несвоевременным обращением пациентов к врачу.
При стойкой обструкции и при наличии обтурирующих полипов показан комплексный подход.
Операция проводится в обязательном порядке и позволяет устранить внутрисинусовые аномалии, а также значительно снизить вероятность рецидивов, если:
- поллипозный процесс локальный и односторонний;
- имеются перекрывающие просветы (обтутирующие) полипы;
- деформирована перегородка;
- нарушена структура средних носовых раковин;
- присутствуют аномалии в строении остиомеатального комплекса.
Эндоскопическая внутрисинусовая хирургия (с использованием шейвера, микродебридера) показана при локальных формах полипозного риносинусита и не требует приема медикаментов.
Вместе с полипами удаляется и измененная слизистая оболочка, чтобы не спровоцировать повторный рост образований.
Также при необходимости корректируется носовая перегородка, расширяются естественные соустья пазух, устраняются добавочные отверстия и др.
Хирургическое лечение совмещается с приемом глюкокортикостероидов в случаях:
- индивидуальной непереносимости нестероидных противовоспалительных препаратов;
- наличия аллергии;
- сочетания риносинусита с бронхиальной астмой;
- гиперактивности бронхов.
Прием глюкокортикостероидов перед операцией:
- влияет на уменьшение отечности и размеров полипов;
- предупреждает обструкцию бронхов;
- а также снижает приток крови к тканям, что позволяет провести вмешательство с минимальными травмами слизистой оболочки.
Стоить отметить, что вмешательство имеет максимально щадящую форму и инвазивность.
Оно проводится под контролем оптических приборов (эндоскоп или операционный микроскоп).
Это позволяет не нарушить внутреннюю анатомическую структуру, что является важным моментом для сохранения всех физиологических функций органа.
Что делать при хронической форме
Хроническая форма заболевания полностью не излечима, требует комплексного подхода, целью которого является достижение стойкой ремиссии и длительного отсутствия симптомов.
Помимо эндоскопического мини-инвазивного удаления полипов необходимо системное и профилактическое применение местных топических глюкокортикостероидов.
Приоритетным считается консервативное лечение. Но лекарства не могут убрать все полипы из пазух, а только приостанавливают их рост или несколько уменьшают размеры.
Эндоскопическая операция же позволяет полностью удалить полипозные образования, благодаря хорошему обзору пазух.
Однако по многочисленным исследованиям зарубежных ученых можно сделать вывод, что удаление всех полипозных структур не влияет на длительность бессимптомного периода.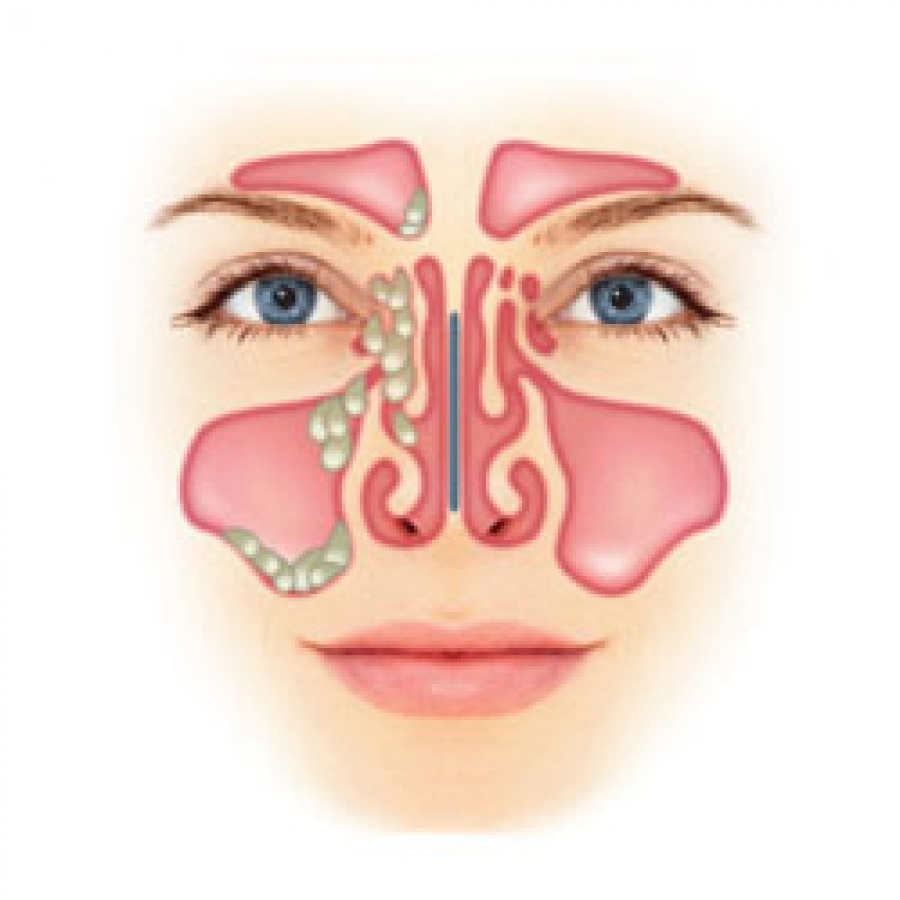
Какие осложнения аллергического риносинусита? Ответ тут.
Более того, хирургическое лечение не только не снижает интенсивность роста полипозной ткани, а, наоборот, повышает, поэтому нередко удалять образования приходится несколько раз в год.
Любое оперативное вмешательство у пациентов с бронхиальной астмой может спровоцировать астматический приступ.
Но полипы, в свою очередь, затрудняют дыхание через нос и могут воздействовать на астмогенные зоны, расположенные в носовой полости, что также приводит к увеличению частоты приступов.
Операция при хроническом риносинусите проводится в случае, когда медикаментозная терапия не приносит существенного облегчения и длительного устранения симптомов.
Вмешательство чаще показано с целью очистить носовые ходы для доступа интерназальных средств, которые используются в качестве поддерживающей терапии.
Рекомендации пациентам после хирургического вмешательства
Чтобы не допустить развития данной патологии и полипозного процесса вновь, после хирургического лечения следует придерживаться некоторых рекомендаций:
- Необходима тампонада носа для остановки кровотечения сразу после операции на срок до 1 дня.

- В течение последующих трех дней системная кортикостероидная терапия должная быть продолжена. Дозировку препаратов снижают постепенно до полного прекращения. Хирургическое вмешательство позволяет использовать в дальнейшем средства для местного интраназального применения в виде спрея, что значительно повышает их эффективность и считается предпочтительнее.
- Показано промывание пазух носа физиологическим раствором 3–4 недели, чтобы удалить сгустки крови и слизи из прооперированных участков. Это необходимо для предотвращения послеоперационного воспалительного процесса.
- На протяжении двух недель пациенту нужно раз в 4–5 дней посещать ЛОР-кабинет для осмотра, осуществления туалета полости носа и удаления корок.
- Пациенту следует проходить профилактические консультации врача в течение года после хирургического лечения не реже одного раза в 3–4 месяца.
- Любые острые заболевания или обострения хронических инфекций, характеризующиеся обструкцией верхних дыхательных путей, могу привести к рецидиву, поэтому требуют незамедлительного лечения под наблюдением врача.

Осложнения
Эндоскопический метод позволяет избавиться от полипов легко и безболезненно и практически не вызывает осложнений, так как проводится под точным наблюдением за всеми движениями хирурга на мониторе.
Редко могут появляться:
- аллергическая реакция на анестезию или препараты, используемые во время операции;
- инфицирование затронутых тканей;
- кровотечения.
К сожалению, отечественная медицина не настолько развитая, чтобы широко использовать щадящий способ удаления полипов.
Чаще они срезаются полипными петлями «вслепую», что не позволяет полностью удалить все образования из труднодоступных мест, а также чревато серьезными осложнениями:
- иссечением вместе с полипами значительных участков слизистой оболочки;
- сильным послеоперационным кровотечением;
- негативным влиянием на состояние всей легочной и бронхиальной системы;
- сепсисом;
- потерей зрения.
Почему появляется риносинусит у детей? Читать далее.
Что такое себорейная экзема на лице? Подробности здесь.
Прогноз
Прогноз благоприятен в случае локального полипозного риносинусита и практически исключает рецидивы.
Длительной ремиссии можно добиться путем правильно подобранной базисной лекарственной терапии при условии своевременного начала лечения.
Профилактический прием глюкокортикостероидов снижает вероятность возникновения воспаления вновь.
Прогноз напрямую зависит от количества и качества хирургических вмешательств.
И чем их больше, тем более возрастает риск повторного образования полипов на фоне инфекции. Рецидивы обычно наблюдаются в течение 3–5 лет после операции, а у людей моложе 30 лет намного раньше.
Важно понимать, что каждая последующая операция даже с минимальной инвазией нарушает естественные метаболические процессы в полости носа, что влияет на увеличение количества эозинофилов и появления полипов вновь.
Поэтому о целесообразности каждого повторного хирургического вмешательства решает лечащий врач, исходя из строго индивидуальных симптомов и течения заболевания.
Полипозный риносинусит – хронический, лечение, народными средствами, симптомы
Полипозный риносинусит – заболевание, при котором затруднено носовое дыхание и выход жидкости из пазух из-за образовавшихся в них полипов.
В случае когда полипы полностью заполняют носовые ходы, больной может дышать только через рот. Данное заболевание диагностируют у 1- 4% населения, причем встречается оно у мужчин в 4 раза чаще, чем у женщин.
Что такое полипы
Полипы – это доброкачественные новообразования. Могут иметь округлую, каплеобразную или неправильную форму, располагаются на стенках полых органов, имеющих слизистую оболочку, и выступают в их просвет.
С какого возраста появляются
Заболевание редко можно встретить среди детей и подростков.
Развитие болезни в основном приходится на возраст заболевших от 30 лет и старше, среди которых основная часть — в возрасте 50-60 лет.
Причины появления
Причины появления полипов в носовой полости до конца не установлены.
Однако, известны некоторые факторы, которые приводят к возникновению полипозного риносинусита.
Среди них:
- аллергические реакции в организме;
- наличие грибковых инфекций;
- нарушенный обмен арахидоновой кислоты;
- хронические воспаления, сопровождаемые гнойными выделениями из носа;
- непереносимость салициловой кислоты;
- муковисцидоз;
- наследственная предрасположенность.
Полипозный риносинусит редко становится следствием, какого-либо одного из этих факторов.
Зачастую он развивается в сочетании нескольких из них.
Особенности проявления симптомов
Образование полипов не происходит за один день.
Заболевание развивается постепенно и сопровождается:
- ноющими головными болями;
- чувством тяжести под глазами;
- дискомфортом в области переносицы.
Ему присущи регулярные слизистые и гнойные выделения из носа.
Когда полипы разрастаются и выходят в пазухи, возникает ощущение инородного тела внутри, наступает полная заложенность носа, от которой не избавляет ни один препарат.
Случается также резкое ослабевание обоняния, иногда оно исчезает вовсе. Наблюдается существенное ухудшение общего состояния здоровья.
Как можно заподозрить полипозный риносинусит
Для данного заболевания характерны следующие проявления:
- затрудненное носовое дыхание и заложенность носа;
- ослабление либо полное отсутствие обоняния;
- ощущение инородного тела внутри носа;
- в запущенных случаях становится тяжело глотать пищу;
- боль в голове и в области околоносовых пазух;
- слизистые или гнойные выделения из носа.
Затягивать с обращением к специалистам ни в коем случае нельзя, болезнь может стремительно прогрессировать, и один из носовых ходов может полностью закрыться.
Опасности хронической формы
Хронический полипозный риносинисит часто является следствием отсутствия своевременного лечения.
Для этой формы течения болезни характерны полное отсутствие носового дыхания и обоняния.
Такое состояние также зачастую сопровождается застоем в пазухах большого количества гнойных масс, активизирующих воспалительные процессы в организме и могут послужить платформой для развития сопутствующих осложнений, таких как поражения тканей глазных яблок и даже менингита.
Способы диагностики
Для постановки диагноза используются следующие основные методы диагностики:
- рентгенография;
- компьютерная томография;
- эндоскопическое исследование.
Наилучшим образом зарекомендовала себя именно эндоскопическая диагностика. Она является наименее инвазивной медицинской процедурой и используется для исследования внутренней поверхности органа или ткани.
Проводится данная процедура с помощью специального прибора – назального эндоскопа.
Устройство состоит из тонкой, жесткой трубки с волоконно-оптическим кабелем и позволяет проводить осмотр полости носа под разными углами.
Таким образом устанавливается наличие мельчайших новообразований и разрастаний слизистой.
В результате исследования максимально точно удается определить форму, размер и место расположения новообразований, а также степень их распространения.
Полученная информация выводится на монитор, делается снимок для отслеживания динамики лечения.
Видео: Удаление полипов
Методы лечения
На сегодняшний день существует множество способов лечения полипов в носу, однако ни один из них не приводит к полному выздоровлению. При любом способе лечения никто не даст гарантии, что полипы не появятся снова.
Многие годы медики проводили апробацию различных методик медикаментозного нехирургического лечения, но чаще всего удавалось добиться лишь приостановления роста полипов или увеличения промежутка между рецидивами.
Один из вариантов медикаментозной полипотомии заключается в том, что лекарственный препарат вводят непосредственно в полип.
Лекарства подбираются индивидуально для каждого пациента, обычно это гормональные препараты на основе кортикостероидов.
Полип отмирает и удаляется во время высмаркивания. Достаточно 1-2 инъекций с интервалом в 1-2 недели.
Преимущество такого метода лечения заключается в том, что лекарственный препарат не всасывается в кровь, что, в свою очередь, позволяет избежать побочных действий гормональной терапии.
Кроме того, если препарат подобран правильно можно добиться полного исчезновения полипов и значительно отсрочить наступление рецидива.
Местное лечение полипозного риносинусита заключается в промывании носовой полости солевыми растворами, которые можно приобрести в аптеке (физиологический раствор, аква-марис, квикс и др.) либо приготовить дома.
Для приготовления солевого раствора дома необходимо 1 столовую ложку морской соли растворить в 1 л кипяченой воды.
Полученную жидкость следует пропустить через несколько слоев марли, чтобы избавиться от осадка.
Ополаскивание полости носа удобно проводить с помощью пульверизатора:
- Процедуру необходимо повторять 2-3 раза в день по 3-4 впрыскивания в каждую ноздрю.
- Спустя пару минут после ополаскивания необходимо тщательно высморкаться и впрыснуть в носовые ходы спрей тафен назаль (по 2 впрыскивания 1 раз в день).
- Длительность такого лечения составляет 10 суток. Курс рекомендуют повторять через каждые полгода.
Бывают ситуации, когда консервативное лечение не приносит результата и тогда назначается проведение операции по удалению полипов.
Показаниями к операции являются:
- сильное нарушение носового дыхания, а в крайне запущенных случаях, его полное отсутствие;
- гнойные воспаления в носовой полости.
Существуют различные способы удаления полипов в носу.
Самым современным, щадящим и эффективным способом удаления полипов признан метод функциональной эндоскопической эндоназальной хирургии полости носа и придаточных пазух.
Операция проводится через носовую полость (эндоназально), что позволяет избежать разрезов.
Хирург работает специальным инструментом, который предельно точно помогает отделить полип, сведя травмирование слизистой к минимуму.
Благодаря малой травматичности и бескровности операции, пациенты практически сразу возвращаются к обычной жизни.
Этот метод также позволяет полностью удалить полипы и создает наиболее благоприятные условия для лечения специальными ингаляторами для предотвращения повторного роста полипов.
Значительную роль играет послеоперационное лечение и уход за полостью носа. Проведение актуальной медикаментозной терапии заключается в ежедневных полосканиях или применении носовых стероидных спреев.
Затем проводится долгосрочная поддерживающая терапия, которая включает в себя лекарственные орошения носовой полости, использование назальных капель.
По прошествии некоторого времени после операции врач назначает проведение эндоскопического обследования, в ходе которого тщательно изучается поверхность слизистой оболочки пазух носа.
Такое обследование необходимо, так как у большой части пациентов симптомы наличия полипов в носу могут не проявляться в течении нескольких месяцев и даже лет.
Народные рецепты в помощь
Для лечения полипозного риносинусита народными средствами чаще всего используют травы.
Эффективными являются следующие лекарственные растворы:
- капли на основе чистотела. Для приготовления лекарства столовую ложку травы необходимо растворить в 300 мл кипятка и оставляют настояться в течение часа. Затем настой процеживают, пропуская через марлю, сложенную в несколько слоев. Закапывать нужно по 2-3 капли 3 раза в день.
- капли на основе мумиё. Для приготовления этого лекарства 2 г предварительно измельченного мумиё растворяют в 20 г кипяченой воды, в которую добавлены 5 г глицерина. Закапывать 3 раза в день по 2 капли. Продолжительность курса — 3 недели. Повторять курс можно до полного излечения, делая перерывы продолжительностью 4 дня.
- капли на основе соков облепихи и зверобоя. Чтобы получить сок из зверобоя свежее растение необходимо измельчить, хорошенько растолочь его и добавить немного воды. Получившуюся массу процедить с помощью марлевого мешочка. Затем смешать с предварительно отжатым соком облепихи в соотношении 1:1.
Лучше всего для хранения состава подойдет холодильник.
Закапывания необходимо производить 2 раза в день по 4-5 капель в каждую ноздрю. Курс лечения продолжается один год.
О возможности, целесообразности и необходимости применения народных методов лечения необходимо проконсультироваться с врачом, чтобы оценить степень заболевания и подобрать оптимальный вариант подобной терапии.
Профилактика
При выделениях из носа не стоит злоупотреблять сосудосуживающими препаратами (Нафтизин, Назол и т.п.) и использовать их более 5 дней. Эффективны в борьбе с насморком горячие ванночки для ног и точечный массаж.
Необходимо отказаться от алкоголя и курения, которые пагубно сказываются на дыхательной и сердечно-сосудистой системах.
Эти вредные привычки, ко всему прочему, способствуют снижению защитных функций и тонуса сосудистой стенки носовой полости.
При наличии аллергии не стоит просто пытаться избежать аллергена. Необходимо обратиться к врачу аллергологу, который после проведения внутрикожной пробы точно определит тип аллергена.
В противном случае постоянная аллергическая реакция, протекающая в организме длительное время, может стать причиной образования полипов.
Прогноз
При проведении адекватной терапии, назначенной на ранней стадии, можно достигнуть длительной ремиссии.
Однако часты случаи, когда после отмены интраназальных глюкокортикостероидов случаются рецидивы в короткие сроки.
Благоприятность прогноза зависит также и от формы полипозного риносинусита.
При диффузном полипозе рецидивы наблюдаются через 3-5 лет после операции, а для пациентов в возрасте до 30 лет эти сроки еще короче.
При локальной форме заболевания прогноз более благоприятный.
Часто задаваемые вопросы
Какие существуют методы удаления полипов в носовой полости?
Медицина предлагает несколько вариантов. Основные из них:
- полипотомия. Удаление полипов осуществляется с помощью петли. Проводится под местным обезболиванием. Петля вводится через ноздрю и производится захват полипа. Постепенно петлю сжимают вокруг ножки полипа, после чего производят его отсечение. Продолжительность такой процедуры в среднем составляет 45 минут.
Главным недостатком этого способа является высокий процент повторного образования полипов (до 70% случаев). Таким образом, проведение операции снова может понадобиться уже через полгода или год.
- эндоскопическая операция. Осуществляется с помощью эндоскопа, который помещают в носовую полость. Изображение выводится на монитор, что позволяет с максимальной точностью определить размер и место расположения полипов. Этот способ позволяет удалить полипы, практически не травмируя слизистую оболочку, и является одним из самых современных и высокоэффективных.
- удаление полипов с помощью лазера. Этот тип операции проводится в амбулаторных условиях. Анестезия вводится непосредственно в область полипа. Эндоскоп с камерой вместе с лазерным оборудованием вводят через носовую полость. Лазерный луч нагревает клетки, составляющие полип, в следствие чего он испаряется. В процессе происходит запаивание сосудов, предотвращая возникновение кровотечения. Кроме того, при такой операции полностью исключена вероятность занесения инфекции.
Выбор того или иного способа операции производится врачом после проведения необходимых исследований.
Какова эффективность применения народной медицины в лечении данной болезни?
Официальная медицина не признает народные способы лечения данной патологии, не считает их эффективными.
Основные опасения врачей заключаются в том, что многие средства, применяемые при лечении этого заболевания (такие как мед, прополис, различные эфирные масла), являются сильными аллергенами, способными ухудшить ситуацию.
Лечение полипов с помощью народных средств направлено на устранение причины заболевания.
Природные компоненты, содержащиеся в травах, помогают наладить работу слизистой и способны уменьшить полипы в размерах.
Такая терапия уместна как поддерживающая и пригодна также для применения в послеоперационном периоде.
Подведя итог, отметим, что полипозный риносинусит – заболевание, нелегко поддающееся лечению.
Поэтому крайне важно соблюдать все меры профилактики, а также, в случае появления симптомов заболевания, своевременно начинать лечение, т.к. от этого напрямую зависит его эффективность.
Полипозный риносинусит. Современные подходы к изучению патогенеза, диагностике и лечению – Вестник оториноларингологии – 2015-04
Полипозный риносинусит (ПРС) — хроническое заболевание слизистой оболочки носа и околоносовых пазух (ОНП), в основе патогенеза которого лежит воспалительная реакция, характеризующееся образованием и рецидивирующим ростом полипов с доминированием эозинофилов или нейтрофилов [1].
Хронический риносинусит (ХРС) подразделяется на две подгруппы в зависимости от наличия или отсутствия полипов в среднем носовом ходе [2]. Для патогенетических механизмов этих фенотипов характерны Тh2-тип иммунного реагирования при ХРС без полипов и Тh3-направленным иммунным воспалением при полипозном процессе. В свою очередь ПРС подразделяется на европейский тип, где полипозная ткань на 77—85% представлена эозинофилами, и на азиатский тип с преобладанием нейтрофилов. По гистологическому строению встречаются полипы 4 типов: 1) отечные эозинофильные полипы, 2) воспалительные фиброзные полипы, 3) полипы с гиперплазией серозно-слизистых желез, 4) полипы с атипией стромальной ткани [1].
В среднем по России показатель обращаемости больных ПРС составляет 4,9 на 10 000 населения, при этом отмечается около 70000 новых случаев ПРС в год [1]. Исходя из этих статистических данных, в России ПРС может встречаться примерно у 1 млн 400 тыс. человек. По данным шведских исследователей, ПРС страдает 2,7%, в Южной Корее — 0,5%, в Финляндии 4,3%, во Франции — 2,1% от общей численности населения [2]. Интересные данные были опубликованы коллегами из Дании. При аутопсии после удаления целых назо-решетчатых блоков полипы были обнаружены в 5 из 19 образцов [3]. При выполнении эндоскопической диссекции на кадаверах полипы находили в 42% случаев [4], при этом при проведении только передней риноскопии на трупном материале полипы полости носа определялись лишь в 2% наблюдений [5]. Возраст кадаверов с выявленным полипозным процессом в этих аутопсических исследованиях колебался от 70 до 79 лет, на основании этого был сделан вывод, что ряд пациентов с ПРС либо за медицинской помощью не обращались, либо у них вместо ПРС диагностировали другой патологический процесс. Соответственно уровень заболеваемости ПРС значительно выше, чем в приведенных официальных источниках. Средний возраст пациентов для дебюта ПРС составляет 42 года [6], мужчины подвержены этому заболеванию чаще женщин в соотношении 2—3:1 [7].
Иммунопатогенез ПРС в настоящее время остается неизвестным, поэтому данное заболевание считается мультифакторным. Современные исследования фокусируются на изучении отдельных патогенов, молекул или клеток в патогенезе заболевания, а также на возможностях его успешного лечения при воздействии на определенные механизмы. Пусковым моментом может быть воздействие определенных триггерных факторов на мерцательный эпителий. Неоднократно отмечалось выраженное угнетение транспортной функции респираторного эпителия слизистой носа и ОНП [8]. При этом вторичная мерцательная дискинезия у пациентов с ПРС, как правило, обратима. Наследственная патология с врожденным дефектом ультраструктуры ресничек, встречающаяся при синдроме Картагенера, кистозном фиброзе легких приводит к особому механизму полипообразования [9]. Распространенность ПРС у этих пациентов составляет более 40%, заболевание протекает с частыми рецидивами и требует мультидисциплинарного подхода при определении тактики лечения.
Роль IgE–зависимой аллергической реакции в патогенезе ПРС достоверно не доказана, несмотря на то, что этой теме посвящено значительное количество работ. Однако критический анализ исследований, связывающих атопию как фактор риска ПРС, показывает, что имели место повышенное ожидание и заинтересованность докторов в желаемых результатах. Ряд авторов отмечают, что у 24% пациентов с ХПР, перенесших эндоскопические операции на околоносовых пазухах, ранее был поставлен диагноз аллергического ринита. Позитивные кожные тесты отмечались у данных больных в 50—84%, при этом в 60% они имели поливалентный характер [10]. Другие исследователи приводят данные о том, что у 0,5—4,5% пациентов с аллергическим ринитом при осмотре визуализировались полипы полости носа [11]. При этом в период цветения у этих больных не наблюдалось достоверно значимого повышения частоты рецидивов хронического синусита [12], что ставит под сомнение причинно-следственную связь аллергии и ПРС. Прямая корреляционная связь, обнаруженная C. Bachert и соавт. между уровнем общего IgE сыворотки и эозинофильной инфильтрацией полипозной ткани, не имела никакого отношения к результатам кожных тестов [13]. Интересным является факт регистрации положительных кожных тестов с пищевыми аллергенами у 81% пациентов с ПРС по сравнению с контрольной группой (11%), что требует дальнейшего изучения [14].
Другие корреляции наблюдаются при изучении взаимосвязи бронхиальной астмы (БА) и полипозного риносинусита. У больных БА частота ПРС значительно выше, чем в популяции, составляя 7—15% и, наоборот, среди пациентов с ПРС астма диагностируется в 29—70% случаев [15]. Компьютерная томография позволила установить у 100% пациентов стероидзависимой БА изменения в околоносовых пазухах [16]. При сочетании ПРС и БА отмечается взаимное утяжеление этих заболеваний, увеличение выраженности симптомов как со стороны верхних, так и нижних дыхательных путей, что в совокупности демонстрирует низкое качество жизни и сложность проведения лечебных мероприятий.
Нарушение метаболизма арахидоновой кислоты с вытекающей из этого непереносимостью нестероидных противовоспалительных средств (НПВС), особенно аспирина, в 36—96% сочетается с ПРС [17]. Ингибирование фермента циклооксигеназы ведет к активизации альтернативного пути метаболизма арахидоновой кислоты, катализируемого 5-липоксигеназой. Образующиеся при этом лейкотриены LTC-4, LTD-4, LTE-4 являются мощными медиаторами воспаления и прямыми хемоаттрактантами для привлечения эозинофилов и нейтрофилов в слизистую оболочку дыхательных путей. Хотя детальный анализ не выявил разницы в гистологической картине носовых полипов за исключением CD3+Т-лимфоцитов, концентрации альбумина, секреторных белков (лактоферрин, лизоцим) и медиаторов воспаления (гистамин, PGD2, LTC4/LTD4) в назальной жидкости пациентов с непереносимостью НПВС и аспирин-толерантных больных, обе группы имели различные профили цитокинов [18]. У пациентов с непереносимостью НПВС в ткани полипов преобладали провоспалительные цитокины, в том числе γ-интерферон, в отличие от других пациентов, у которых доминировали ИЛ-4, ИЛ-13. Все исследователи отмечают выраженный агрессивный характер эозинофильного воспаления, снижение апоптоза эозинофилов, увеличение количества эозинофильного катионного протеина в группе ПРС с нарушением метаболизма арахидоновой кислоты, что свидетельствует о принципиально разных механизмах патогенеза полипозного процесса [19].
При упорном рецидивирующем течении ПРС всегда выявляется иммунная дисфункция. Нарушение фагоцитирующей способности макрофагов, низкий уровень sIgA, снижение экспрессиии рецепторов к IgA на клетках назального эпителия приводят к дефекту иммунной защиты слизистой оболочки и имеют прямую связь с развитием Th3-зависимого эозинофильного воспаления дыхательных путей [20]. У ВИЧ-инфицированных пациентов полипозный риносинусит присутствовал в 34% случаев, выраженность назальных симптомов при этом коррелировала с уровнем снижения CD4±лимфоцитов [21].
Интересная статистика приведена по поводу влияния анатомических вариаций внутриносовых структур на развитие ХПР. Несмотря на то, что анатомические аномалии строения (искривление перегородки носа, аномалии средней носовой раковины, крючковидного отростка), приводящие к нарушениям аэродинамики полости носа, были предложены в качестве потенциальных факторов риска для развития ХПР, W. Bolger и соавт. [22] и S. Nouraei и соавт. [23] не нашли никакой корреляции между ХПР и этими анатомическими структурами. Некоторые авторы говорят об отсутствии разницы в распространенности этих анатомических вариаций среди здоровых людей и у пациентов с ХРС с полипами и без полипов [24]. Разнятся мнения об участии искривления перегородки носа в патогенезе риносинусита. Ряд авторов утверждают, что значимым для ХРС является отклонение носовой перегородки от средней линии более 3 мм [25], другие полностью отрицают связь между этими процессами [26]. Таким образом, единое доказательное решение о наличии причинно-следственной связи между анатомическими изменениями полости носа и развитием ХРС в настоящий момент отсутствует.
Многие патогенные бактерии, образующие биопленки на слизистой оболочке носа и околоносовых пазух, не являясь при этом основным этиологическим агентом ПРС, усугубляют течение воспалительного процесса в послеоперационном периоде [27]. Staph. aureus является наиболее распространенным микроорганизмом в составе биопленок пациентов с ХРС. Cуперантиген Staph. aureus вызывает поликлональную активацию и антигенспецифическую пролиферацию лимфоцитов с гиперпродукцией цитокинов и активацией других иммунокомпетентных клеток [28].
Таким образом, можно констатировать, что патогенез полипозного риносинусита в настоящий момент остается неясным. Альтернативная «грибковая» гипотеза гиперинтенсивного иммунного ответа на грибы рода Alternaria [29] не находит подтверждения, хотя грибы могут играть роль триггеров или модификаторов в течении ПРС, в частности снижать плотность эпителиального барьера, уменьшая экспрессию TJ-белков [1]. Гипотеза развития полипов при дефекте биосинтеза эйкозаноидов с увеличением синтеза провоспалительных лейкотриенов и снижением синтеза противовоспалительных простагландинов (PGE2) поддерживалась многими исследователями, которые объясняли развитие ПРС как у пациентов с непереносимостью аспирина, так и у аспирин-толерантных больных. К сожалению, эта теория не подтвердилась в связи с ограниченной клинической эффективностью ингибиторов синтеза лейкотриенов. Роль суперантигена Staph. aureus в сдвиге иммунного ответа в сторону Th3-типа, торможении Treg-клеток, последующей активацией эозинофилов, тучных клеток и ремоделированием слизистой прослеживается только у половины пациентов с ПРС; следовательно, стафилококковые суперантигены могут рассматриваться в качестве модификаторов болезни, а не как дискретные этиологические факторы.
Можно констатировать, что в настоящее время главенствующей считается иммунологическая гипотеза. Основой патологического процесса, ведущего к образованию полипов, является аномальный иммунный ответ вследствие воздействия на респираторную слизистую оболочку триггерных агентов, включая респираторные вирусы, биопленки, состоящие из кокковой флоры и включений грибов [2]. Комбинированный иммунный дефицит, взаимодействие медиаторов и цитокинов, продуцируемых активированными иммунокомпетентными клетками и клетками микроокружения, вызывают развитие персистирующего эозинофильного воспаления, приводящего к ремоделированию слизистой оболочки и формированию продуктивного процесса в виде ХПР.
Клиническая диагностика ХПР базируется на жалобах пациента, данных эндоскопического осмотра и компьютерной томографии (КТ). Основные жалобы — нарушение носового дыхания, заложенность носа, выделения из носа или стекающие по задней стенке глотки, чувство давления или боль в лицевой области (20%) и снижение обоняния [2]. Дополнительно пациентов может беспокоить головокружение, боль или давление в ушах, неприятный запах изо рта, зубная боль, кашель, дисфония, слабость, нарушение сна. При эндоскопическом осмотре патогномоничным признаком ПРС являются полипы, которые могут ограничиваться средним носовым ходом или выходить за его пределы, в том числе тотально или субтотально занимать полость носа и носоглотку. При этом эндоскопические находки могут не коррелировать с выраженностью жалоб пациента. Для оценки выраженности патологического процесса в ОНП при КТ используют шкалу Lund-Mackay, которая была утверждена в нескольких клинических испытаниях: 0 баллов — нет патологических изменений; 1 балл — частичное затемнение; 2 балла — тотальное затемнение. Оценивают по отдельности состояние верхнечелюстной, лобной, клиновидной, решетчатой пазух и остиомеатального комплекса с каждой стороны. Сумма баллов может варьировать от 0 до 24 [30].
При проведении научных исследований дополнительно проводится изучение состояния мукоцилиарного клиренса, функции носового дыхания (риноманометрия, акустическая ринометрия, ринорезистометрия), оценка обонятельного анализатора [2]. При диагностике нельзя упускать онкологическую настороженность. Наличие полипозной ткани только в одной половине носа должно быть поводом для тщательного обследования больного. Односторонний полипозный процесс может быть как банальным антро-хоанальным полипом, так и инвертированной папилломой. Не редки случаи, когда полип маскирует ангиофиброму либо рак.
С позиций международных согласительных документов и клинических рекомендаций к лечению ПРС следует изначально подходить с терапевтических позиций. Учитывая, что развитие носовых полипов может иметь различный генез, лечение ПРС может быть только консервативным или комбинированным (хирургическое лечение + консервативная терапия), при некоторых формах — только хирургическим [1].
Глюкокортикостероидная (ГКС) терапия имеет патогенетический характер и направлена на блокирование эффектов биологически активных веществ практически всех клеток — участников патологического процесса, способствует уменьшению ремоделирования как за счет непосредственного противовоспалительного действия, так и за счет уменьшения отложения коллагена. Топическая кортикостероидная терапия имеет высший уровень доказательности и клинических рекомендаций, так же как и системная кортикостероидная терапия. В силу высокой (100%) биодоступности системных глюкокортикостероидов и, следовательно, риска развития побочных явлений, при ПРС следует проводить короткие курсы лечения системными препаратами с последующим долгосрочным лечением местными ГКС [31].
Согласно статье 43 РФ «Основы законодательства РФ об охране здоровья граждан» в клинической практике могут использоваться только лекарственные средства, разрешенные к применению в установленном законом порядке после государственной регистрации и по зарегистрированным показаниям. Отсутствие в инструкции указаний на возможность приема препарата при конкретной нозологии свидетельствует о том, что не были проведены клинические испытания или анализ эффективности применения лекарства при этом заболевании, или полученные данные не были одобрены фармакологическим комитетом.
При ХПР показания к применению указаны в инструкциях только у 3 топических кортикостероидов — мометазона фуроата (назонекс), беклометазона (альдецин) и будесонида (тафен назаль). Назначение интраназальных глюкокортикостероидов (ИнГКС) позволяет уменьшить клиническую симптоматику, включая ощущение заложенности носа и нарушение обоняния, сократить размеры полипов, улучшить исходы операции и вероятность рецидива после оперативного лечения. Профиль безопасности ИнГКС определяется его биодоступностью, которая зависит от попадания вещества в системный кровоток с поверхности слизистой оболочки носа, объема абсорбции препарата в желудочно-кишечном тракте и выраженности эффекта «первого прохождения» через печень, благодаря чему в системный кровоток поступают уже неактивные метаболиты. Выбор ИнГКС с низкой биодоступностью позволяет свести к минимуму общее системное воздействие. Мометазона фуроат имеет доказанную минимальную биодоступность — менее 1% по сравнению с будесонидом — 31% и беклометазоном — 44% [32]. Очевидным преимуществом мометазона фуроата также является отсутствие угнетения гипоталамо-гипофизарно-надпочечниковой системы, что подтверждается отсутствием снижения уровня свободного кортизола (при суточном мониторинге кортизола или определении его уровня в утренние часы в крови/моче) при интраназальном применении [33]. У препарата выявлена максимально высокая авидность (степень прочности связывания) к глюкокортикоидным рецепторам [34], высокий терапевтический индекс (соотношение местной противовоспалительной активности и системного действия) по сравнению с будесонидом [35]. Все это объясняет подтвержденный клинический эффект мометозона фуроата при ПРС в сочетании с высоким профилем безопасности на местном и системном уровнях, что позволяет проводить длительные курсы терапии. Согласно клиническим рекомендациям мометозона фуроат назначают в виде интраназального аэрозоля длительными курсами от 3 до 6 мес и более в дозе не менее 400 мкг в сутки [1, 36].
В качестве многообещающего лекарственного средства в течение последних 20 лет рассматривались макролиды. Однако лечение макролидами коротким курсом, равным 3 нед, показало как положительный, так и отрицательный эффект, поэтому однозначных рекомендаций нет. Длительный курс лечения кларитромицином по 400 мг в сутки более 3 мес показал хороший клинический эффект, но в связи с отсутствием ряда данных для оценки этого метода необходимы дальнейшие исследования [37, 38].
Были попытки лечения ПРС анти-IgE-препаратами, в частности омализумабом. К сожалению, он не показал клинической эффективности, так же как антигистаминный препарат цитиризин. Применение фуросемида в виде назального спрея также не дало значимых результатов. Перспективными могут быть рекомбинантные антагонисты ИЛ-5 (Reslizulab, Mepolizulab), при их использовании отмечалось значительное уменьшение размера полипов в 50—60% [39]. Ведутся клинические испытания. Также проходят испытания по применению гепарина и активированного протеина С при ПРС. Получен хороший эффект за счет противовоспалительного действия, ингибирования гиперсекреции слизи этими препаратами [40].
В современных клинических рекомендациях категорически не рекомендуется местное использование амфотерицина В, системное применение противогрибковых препаратов и антагонистов лейкотриеновых рецепторов.
Хирургическое лечение при ПРС во многом зависит от оснащения клиники и опыта врачей. Основным методом лечения являются эндоскопические и микроскопические внутриносовые вмешательства. При этом рутинным становится применение навигационных систем. Однако однозначного мнения об объеме операции также нет. Рекомендации начинаются от простой полипотомии носа до так называемой назализации, т. е. удаления не только видимых полипов из полости носа и ОНП, но и тотальном удалении клеток решетчатого лабиринта, носовых раковин, создания больших соустий между полостью носа и ОНП. Таким образом, необходимо отметить, что оптимальной методики хирургического лечения ПРС в настоящее время не найдено. Основной проблемой является рецидив полипозного процесса. Частота рецидивов вне зависимости от методики хирургического вмешательства достигает 60% в среднем через 2 года после операции. Именно поэтому для успешного исхода необходимо правильно разработать тактику — объем оперативного лечения, медикаментозное лечение в пред- и пост-операционном периоде и длительность ее проведения. Следует признать, что, несмотря на использование даже самых последних достижений ринохирургии, она позволяет воздействовать лишь на исход патологического процесса, не влияя на звенья патогенеза ПРС [41].
Полипозный риносинусит остается распространенным заболеванием, существенно влияющим на здоровье человека. Исследования, проводимые для изучения патогенеза данного заболевания, позволяют лишь констатировать, что оно является мультифакторным и, следовательно, не до конца понятным. Рассматривая данную проблему, мы сознательно привели преимущественно результаты анализа зарубежной литературы, отраженной в EPOS 2012. В современных условиях отечественные ЛОР-врачи все чаще следуют общемировым тенденциям развития оториноларингологии. Во многих клиниках широко внедрены эндоскопические технологии. Диагностика базируется на данных эндоскопии и компьютерной томографии. Учитывая территориальные и национальные особенности Российской Федерации, где есть европейская и азиатская части, весьма перспективным будет детальное изучение особенностей течения полипозного риносинусита у жителей нашей страны.
хронический полипозный риносинусит » Медвестник
По некоторым данным, клинические проявления полипозного риносинусита встречаются у 3-5% населения. В России около 1,5 млн человек страдают полипозным риносинуситом.3,4
На данный момент отсутствует четкое понимание причин появления полипов. Среди возможных причин, способствующих развитию и рецидивированию полипозного процесса, обсуждается участие аллергии, бронхиальной астмы, хронических воспалительных процессов в околоносовых пазухах, вызванных бактериальной флорой, вирусными агентами, рассматривается влияние различных анатомических аномалий, способствующих нарушению аэрации и поддержанию воспалительного процесса, и наличие генетической предрасположенности.5 Около 50% пациентов с ХПРС страдают от астмы6,7, 50-80% пациентов также имеют аллергический ринит7,8, и около 15% имеют НПВП-ИРЗ7,9 – респираторное заболевание, вызванное применением нестероидных противовоспалительных препаратов (НПВП).
Небольшие по размеру и количеству полипы, как правило, не доставляют дискомфорта и существуют бессимптомно, однако большие и многочисленные образования могут перекрывать носовые ходы и тем самым приводить к проблемам с носовым дыханием.
Основные симптомы хронического синусита мало отличаются от симптомов обычной простуды: постоянная заложенность носа и насморк, ощущение отека и давления в области лица, снижение обоняния и потеря вкуса. Несмотря на это, от обычной простуды хронический синусит отличается продолжительностью состояния.1
Полипозный риносинусит оказывает отрицательное влияние на повседневную жизнь. Одна из проблем – нарушение сна из-за затрудненного дыхания, и как следствие, – общее снижение настроения и быстрая утомляемость10,11. Симптомы ХПРС оказывают влияние на продуктивность, возможность получать удовольствие от еды, напитков и запахов12. Из-за снижения обоняния и потери вкуса человек не всегда сразу может распознать потенциальную опасность – запах дыма, огня или испорченной еды11. У пациентов с ХПРС чаще встречается бронхиальная астма, трудно поддающаяся лечению7.
Диагностикой заболевания занимается врач-оториноларинголог. Он устанавливает диагноз на основе симптомов и осмотра носовых ходов с помощью специальных инструментов. При диагностических сложностях врач может применить дополнительные методы исследования, например, компьютерную томографию, или привлечь других специалистов для уточнения диагноза. Обычно требуется дополнительная помощь аллерголога и пульмонолога, чтобы подтвердить или исключить сопутствующие заболевания и уточнить спектр аллергенов, к которым имеется повышенная чувствительность.
Существующие методы лечения не всегда позволяют полностью избавиться от полипов, однако возможно снизить проявление симптомов5. Терапия ХПРС может состоять из нескольких этапов. Для начала врач может назначить интраназальные кортикостероиды, однако они иногда не способны облегчить симптомы при тяжелых формах заболевания. Если интраназальные кортикостероиды оказались неэффективными, врач может назначить системные кортикостероиды короткими курсами. Лечение системными кортикостероидами может увеличивать риск проявления нежелательных побочных эффектов, именно поэтому их назначают короткими курсами12,13. Если назначенная врачом терапия не приводит к необходимому результату и не позволяет контролировать заболевание, врач совместно с пациентом могут принять решение о хирургическом лечении. По статистике, половине пациентов с ХПРС требуется хирургическое вмешательство из-за блокады носовых ходов полипозными разрастаниями и невозможности облегчения симптомов.14
В настоящее время продолжается ряд исследований инновационных лекарственных препаратов, которые могут прицельно воздействовать на воспаление, лежащее в основе заболевания, и дать пациентам надежду на новую жизнь без симптомов и повторных хирургических вмешательств.
Литература
- Fokkens WJ, Lund VJ, Hopkins C, et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2020. Rhinology. 2020 Feb 20; 58(Suppl S29):1-464. [Неофициальный перевод: Фоккенс В.ДЖ., Лунд В.ДЖ, Хопкинс С и др. Европейская позиция по ХПРС 2020. Ринология. 2020]P. Gevaert, L. Calus, and N. van Bruaene, «Allergic Sensitization, High Local IL-5 and IgE Predict Surgical Outcome 12 Years after Endoscopic Sinus Surgery for Chronic Rhinosinusitis with Nasal Polyposis,» J Allergy Clin Immunol, vol. 135, no. 2, p. AB238, 2015. [Неофициальный перевод: П.Геяерт, Л.Калус и Н.ван Брюне «Сенсибилизация к аллергенам, высокий уровень IL-5 и IgE в слизистой оболочке носа предсказывают хирургический исход через 12 лет после эндоскопической синоназальной хирургии при хроническом полипозном риносинусите. Журнал аллергии и клинической иммунологии, выпуск 135, номер 2, стр. AB238, 2015]
- Арефьева Н.А., Вишняков В.В., Вахрушев С.Г. Полипозный риносинусит: Клинические рекомендации. М.; 2010.
- Рязанцев С.В., Артюшкина В.К., Начаров П.В., Лаптиева М.А. Современные аспекты системной кортикостероидной терапии у больных хроническим полипозным риносинуситом. Российская оториноларингология. 2013;(2):114-121.
- С.В. Рязанцев, М.А. Будковая. Современный взгляд на лечение хронического полипозного риносинусита. Российская ринология, 1, 2017
- Cahill, K.N., et al. Automated identification of an aspirin-exacerbated respiratory disease cohort. J Allergy Clin Immunol. 2017; 139(3): 819-825. [Неофициальный перевод: Кахилл К.Н. и др. Автоматическая идентификация когорт аспириновой бронхиальной астмы. Журнал аллергии и клинической иммунологии, 2017; 139(3): 819-825.]
- Khan A, et al. The Global Allergy and Asthma European Network (GALEN) Rhinosinusitis Cohort: A Large European Cross-Sectional Study of Chronic Rhinosinusitis Patients with and Without Nasal Polyps. Rhinology. 2018 Jun 17. [Неофициальный перевод: Хан А. и др, Глобальная европейская сеть аллергии и астмы (GALEN), когорта риносунусита: Крупное европейское перекрестное исследование пациентов с хроническим риносинуситом с назальными полипами и без них. Ринология, 17 июня 2017]
- Bachert, C., et al. Atopic Comorbidities and Biomarkers of Type 2 Inflammation in Patients with Chronic Rhinosinusitis With Nasal Polyposis (CRSwNP) Who Failed Intranasal Corticosteroids. J Allergy Clin Immunol. 2018; 141(2): AB90. [Неофициальный перевод: Бачерт С. И др. Атопические сопутствующие заболевания и биомаркеры воспаления 2 типа у пациентов с хроническим полипозным риносинуситом (ХПРС), которые не ответили на терапию интраназальными кортикостероидами. Журнал аллергии и клинической иммунологии. 2018; 141(2): AB90.]
- Stevens, W.W., et al. Clinical Characteristics of Patients with Chronic Rhinosinusitis with Nasal Polyps, Asthma, and Aspirin-Exacerbated Respiratory Disease. J Allergy Clin Immunol Pract. 2017. 5(4): 1061-1070. [Неофициальный перевод: Стивенс В.В. и др. Клинические характеристики пациентов с хроническим полипозным риносинуситом, астмой и аспириновой бронхиальной астмой. Журнал аллергии и клинической иммунологии: В практике. 2017. 5(4): 1061-1070.]
- Stull DE, Roberts L, Frank L, Heithoff K. Relationship of nasal congestion with sleep, mood, and productivity. Curr Med Res Opin. 2007 Apr; 23(4):811-9. [Неофициальный перевод: Шталл Д.Е. Робертс Л, Франк Л, Хейсофф К. Связь заложенности носа со сном, настроением и продуктивностью. Журнал Текущие медицинские исследования и мнения. 2007 Апрель; 23(4):811-9.]
- Stewart, M., Ferguson, B., Fromer, L. Epidemiology and burden of nasal congestion. Int J Gen Med. 2010; 3: 37-45. [Неофициальный перевод: Стюард М, Фнергюсон Б., Фромер Л, Эпидемиология и бремя заложенности носа. Международный журнал общей медицины. 2010; 3: 37-45.]
- Полипозные риносинуситы: Этиология, патогенез, клиника и современные методы лечения. Методические рекомендации. Подготовлены заместителем директора Санкт-Петербургского НИИ уха, горла, носа и речи профессором С.В. Рязанцевым. ФГУ «Санкт-Петербургский научно-исследовательский институт уха, горла, носа и речи. 2014 г. 28 с.
- Егоров В.И., Лопатин А.С., Пискунов Г.З., Рязанцев С.В. Полипозный риносинусит. Клинические рекомендации. Национальная ассоциация оториноларингологов. 2016 г.
- Philpott, C., et al. The burden of revision sinonasal surgery in the UK-data from the Chronic Rhinosinusitis Epidemiology Study (CRES): a cross-sectional study. BMJ Open. 2015; 5(4): e006680. [Филпотт С и др. Бремя ревизионной синоназальной хирургии в Великобритании — данные эпидемиологического исследования хронического риносинусита (CRES): перекрестное исследование. Журнал BMJ Open. 2015; 5(4): e006680.]
Полипоз носа: что это такое, лечение и препараты, образование ткани в носу
Данное заболевание гораздо более широко известно, как полипы в носу. Полипы представляют собой доброкачественные образования одиночного, чаще множественного характера. Образуются в результате разрастания слизистой оболочки. Сами по себе безболезненны, однако доставляют сильный дискомфорт и могут привести к возникновению осложнений.
- Консервативная терапия
- Хирургические методы
Механизм образования полипов
Для того, чтобы понять, по какой причине слизистая оболочка начинает разрастаться, надо знать принцип и цель ее функционирования.
Основная функция слизистой оболочки – защита той полости, поверхность которой она выстилает. В данном случае речь идет о носовой полости.
При появлении какой-либо угрозы, как то поражение микроорганизмами, воздействие некоторых химических элементов и др., слизистая оболочка начинает интенсивно работать. Ее верхний слой отслаивается, из носовых ходов отходит слизь, которую принято называть насморком.
Слизистая оболочка носа
По сути, отторжение слизи есть защитная функция оболочки в действии. Благодаря работе желез, их выделения способны до определенной степени справляться с угрозой, выводя ее наружу. Однако при сильном воспалении, инфекции, различных заболеваниях и прочих травмирующих факторах, слизистая не справляется с проблемой. Тогда организм реагирует вполне логичным образом – пытается увеличить площадь оболочки.
В этот момент соединительная ткань начинает расти. Процесс этот происходит в одной из околоносовых пазух (гайморовой, решетчатого лабиринта). Когда разрастание достигает определенной величины, оно через отверстие пазухи выступает в носовую полость. С этого момента образование диагностируется как назальный полип.
В зависимости от пазухи, в которой они образовались, полипы могут иметь некоторые особенности. Например, из гайморовой пазухи появляются преимущественно одиночные, односторонние разрастания, из решетчатого лабиринта – множественные, расположенные по обеим сторонам. Второе встречается много чаще.
С безоговорочной точностью установить полный перечень причин сложно. Существует ряд мнений об условиях и обстоятельствах, провоцирующих возникновение данных образований. Среди них можно выделить следующие возможные причины:
- хронические воспалительные процессы в околоносовых пазухах,
- аллергические реакции респираторной направленности (на пыль, пыльцу, шерсть и т.д.),
- неаллергическая астма,
- часто повторяющиеся респираторные заболевания (простуды, ОРВИ, ОРЗ и т.д.),
- назальный мастоцитоз,
- кистозный фиброз,
- врожденные или приобретенные деформации носовой перегородки.
Существуют и иные заболевания, в некоторых случаях приводящие к формированию подобных разрастаний, например синдром Янга. Также считается, что в данном случае определенное значение имеет наследственная предрасположенность к образованию полипов, а также дисфункция иммунной системы.
Симптомы полипоза носа
Вполне понятно, что при появлении полипов в носовых ходах человек испытывает дискомфорт. Новообразования мешают, создают эффект перманентного присутствия инородного тела в носу. Это обстоятельство, конечно, изнуряет и требует вмешательства. Помимо этого, наблюдаются следующие симптомы:
- постоянное отторжение слизи из носа, вызванное усилением работы слизистой оболочки,
- трудности при носовом дыхании, усиливающиеся по мере разрастания полипозных образований,
- утрата обоняния, вплоть до неспособности различать вкус употребляемой пищи,
- изменение голоса (гнусавость),
- приступы чихания из-за раздражения новообразованиями носовых ходов,
- болевые ощущения в области околоносовых пазух, общая головная боль.
Несмотря на кажущуюся незначительность описанных выше симптомов, человек, страдающий полипозным риносинуситом, в значительной степени утрачивает способность вести привычный активный образ жизни.
В первую очередь, следует отметить, что сосудосуживающие препараты, средства от насморка и даже обезболивающие не дают длительного устойчивого эффекта.
В результате человек постоянно чувствует болезненное состояние, вызывающее ослабление организма по вполне объективным причинам:
- из-за невозможности полноценно дышать, а также по причине головных болей нарушается сон, накапливается усталость, человек становится рассеянным, боль в голове усиливается,
- по причине утраты обоняния снижается аппетит, что в совокупности с усталостью приводит к общему упадку сил,
- непрекращающийся насморк и прочие симптомы снижают работоспособность, отвлекают человека, вынуждают концентрировать внимание на болезненном состоянии.
Без устранения причины данного состояния, т.е. полипов, изменить его не удастся. Симптоматическое воздействие бессмысленно, поскольку слизистая оболочка в условиях подобной деформации не сможет войти в нормальный режим функционирования. Следовательно, лечение полипоза носа – обязательный, неизбежный процесс.
Способы лечения
Прежде чем приступить к лечению полипов, необходимо установить природу патологического процесса. С этой целью в первую очередь производится обследование пациента врачом-аллергологом.
Если причиной возникновения новообразований послужила аллергическая реакция, то необходимо ее устранить. В противном случае удаление полипов не решит проблему, поскольку в скором времени они возникнут снова.
Если же аллергический фон отсутствует, то лечение заключается в удалении непосредственно самих разрастаний. В этом случае возможно два вида воздействия – консервативное лечение и хирургическое вмешательство. Если полипов немного и они небольшие, то можно обойтись без операции. Когда процесс уже слишком запущен, требуется операция. В данном случае она является малоинвазивной, приносит пациенту минимум неудобств.
Консервативная терапия
В подавляющем большинстве случаев пациенты хотят обойтись без операции. Такая возможность существует, когда болезнь находится в стадии развития, а полипы не образовали больших множественных разрастаний.
В любом случае, прежде чем определить способ лечения, врач назначает компьютерную томографию околоносовых пазух, а также видеоэндоскопию, с помощью которой исследуется полость носа и носоглотки.
Если результаты данных диагностических исследований позволяют назначить пациенту консервативное лечение, то врач в индивидуальном порядке подбирает необходимые лекарственные средства и определяет схему лечебного процесса. В этом случае непосредственно в полость полипа вводится лекарственное средство (Дипроспан). В результате новообразование уменьшается в размерах, а затем полностью исчезает.
Также применяются такие средства:
- сосудосуживающие (Назоферон, Отривин),
- антибиотики (Аугментин, Сумамед),
- местные противовоспалительные (Протаргол),
- растворы для промывания полости носа (Маример, Но-соль),
- иммуномодулирующие (ИРС-19),
- антигистаминные (Супрастин, Кларитин),
- гомеопатические (Синупрет).
Хирургические методы
Существует несколько способов хирургического вмешательства с целью устранения полипозных разрастаний. К ним относятся:
- лазерное удаление,
- операция с помощью эндоскопа,
- удаление шейвером (относится виду эндоскопических операций),
- удаление методом полипотомии (с помощью режущей петли).
Последний метод считается самым травматичным из перечисленных, но иногда применяется. Остальные способы удаления отличаются эффективностью, практически не оставляют следов. В этом отношении операция с помощью лазера является наиболее предпочтительной. После удаления полипов следует периодически проходить профилактический осмотр, поскольку повторное их возникновение отмечается довольно часто.
Загрузка…Функциональная эндоскопическая хирургия носовых пазух – Американский семейный врач
ROBERT SLACK, B.SC., FRCS, Royal United Hospital, Bath, England
GRANT BATES, B.SC., FRCS, Radcliffe Infirmary, Oxford, England
Am Фам Врач. 1 сентября 1998; 58 (3): 707-718.
Функциональная эндоскопическая хирургия носовых пазух – это малоинвазивная методика, используемая для восстановления вентиляции пазух и нормальной функции. Наиболее подходящие кандидаты для этой процедуры имеют рецидивирующий острый или хронический инфекционный синусит, и после процедуры можно ожидать улучшения симптомов до 90 процентов.Волоконно-оптические телескопы используются для диагностики и во время процедуры, а компьютерная томография используется для оценки анатомии и выявления пораженных участков. Функциональную эндоскопическую хирургию придаточных пазух носа следует использовать только у пациентов, у которых лечение оказалось неэффективным. Процедура может проводиться под общей или местной анестезией в амбулаторных условиях, и пациенты обычно испытывают минимальный дискомфорт. Частота осложнений при этой процедуре ниже, чем при обычной хирургии носовых пазух.
Функциональная эндоскопическая хирургия носовых пазух (FESS) – это малоинвазивная методика, при которой воздушные клетки пазухи и устья пазух открываются под прямой визуализацией.Целью этой процедуры является восстановление вентиляции и нормальной функции носовых пазух.1–4
Возможность лечения заболеваний околоносовых пазух произвела революцию благодаря волоконно-оптическим эндоскопам и компьютерной томографии (КТ). Волоконно-оптические эндоскопы позволили тщательно обследовать нос от передних ноздрей до постназального пространства. Эндоскопическая процедура требует местной анестезии и может выполняться в офисе (рисунки с 1 по 3). Специфические особенности, которые необходимо идентифицировать и оценивать во время обследования, – это средняя носовая раковина и средний проход (остеомеатальный комплекс), анатомическая непроходимость, слизистая оболочка и полипы носа (рисунки с 4 по 6).
РИСУНОК 1.
Пациент, перенесший назальную эндоскопию.
Просмотр / печать Рисунок
РИСУНОК 2.
Эндоскопический вид левой ноздри в нормальном носу. Слева видна перегородка, также видны нижняя и средняя носовые раковины.
РИСУНОК 2.
Эндоскопический вид левой ноздри нормального носа. Слева видна перегородка, также видны нижняя и средняя носовые раковины.
Просмотр / печать Рисунок
РИСУНОК 3.
Эндоскопический вид нормального постназального пространства. Слева видно правое отверстие евстахиевой трубы.
РИСУНОК 3.
Эндоскопический вид нормального постназального пространства. Слева видно правое отверстие евстахиевой трубы.
Просмотр / печать Рисунок
РИСУНОК 4.
Эндоскопический вид нормальной средней носовой раковины, глядя в правую ноздрю.Перегородка справа, боковая стенка носа слева.
РИСУНОК 4.
Эндоскопический вид нормальной средней носовой раковины при взгляде в правую ноздрю. Перегородка справа, боковая стенка носа слева.
Просмотр / печать Рисунок
РИСУНОК 5.
Эндоскопическая картина острого инфекционного синусита с выделением гноя из-под правой носовой раковины вниз в средний проход.
РИСУНОК 5.
Эндоскопическая картина острого инфекционного синусита с выделением гноя из-под правой носовой раковины вниз в средний проход.
Просмотр / печать Рисунок
РИСУНОК 6.
Носовые полипы в левой ноздре, блокирующие остеомеатальный комплекс.
РИСУНОК 6.
Носовые полипы в левой ноздре, блокирующие остеомеатальный комплекс.
КТ-сканирование определяет анатомические взаимоотношения ключевых структур (орбитального содержимого, зрительного нерва и сонной артерии) с пораженными участками – процесс, который имеет жизненно важное значение для хирургического планирования.КТ также определяет степень заболевания в каждом отдельном синусе, а также любые лежащие в основе анатомические аномалии, которые могут предрасполагать пациента к синуситу (рисунки с 7 по 10).
Просмотр / печать Рисунок
РИСУНОК 7.
Коронарное компьютерное томографическое сканирование, показывающее нормальный остеомеатальный комплекс. Открытые устья видны с обеих сторон, пазухи хорошо вентилируются.
РИСУНОК 7.
Корональная компьютерная томография, показывающая нормальный остеомеатальный комплекс.Открытые устья видны с обеих сторон, пазухи хорошо вентилируются.
Просмотр / печать Рисунок
РИСУНОК 8.
Коронарный компьютерный томографический снимок, показывающий решетчатые полипы. Помутнение решетчатой кости полное из-за полипов носа с вторичным уровнем жидкости в антральном отделе левой верхней челюсти.
РИСУНОК 8.
Корональная компьютерная томография, показывающая решетчатые полипы. Помутнение решетчатой кости полное из-за полипов носа с вторичным уровнем жидкости в антральном отделе левой верхней челюсти.
Просмотр / печать Рисунок
РИСУНОК 9.
Коронарная компьютерная томография, показывающая риносинусит с заблокированным остеомеатальным комплексом и вторичной инфекцией в верхнечелюстных пазухах.
РИСУНОК 9.
Корональная компьютерная томография, показывающая риносинусит с заблокированным остеомеатальным комплексом и вторичной инфекцией в верхнечелюстных пазухах.
Просмотр / печать Рисунок
РИСУНОК 10.
Коронарное компьютерное томографическое сканирование, показывающее развитую правую среднюю носовую раковину (буллезную раковину) и искривленную носовую перегородку.
РИСУНОК 10.
Корональная компьютерная томография, показывающая развитую правую среднюю носовую раковину (concha bullosa) и искривленную носовую перегородку.
Доводы и концепции, поддерживающие использование FESS, в последнее время получили широкое признание. (Термин «функциональный» был введен, чтобы отличить этот тип эндоскопической хирургии от неэндоскопических, «традиционных» процедур.3,4) Цель FESS – вернуть мукоцилиарный дренаж носовых пазух к нормальному функционированию. Состояние придаточных пазух носа поддерживается в здоровом состоянии за счет вентиляции через отдельные устья и с помощью механизма мукоцилиарного транспорта, который поддерживает непрерывный защитный слой слизи, вытекающей из носовых пазух.
Патофизиология синусита
Все носовые пазухи нуждаются в вентиляции для предотвращения инфекции. В нормальном состоянии эта вентиляция осуществляется через отверстия (устья) в нос (рисунки 11 и 12).Естественные устья открываются в средний проход под средней носовой раковиной, за исключением задних решетчатых воздушных ячеек и клиновидной пазухи, у которых устья расположены ближе кзади. Ресничная активность в пазухах направляет поток слизи к этим устьям. Средняя носовая раковина и средний носовой ход вместе представляют ключевую область носа, известную как остеомеатальный комплекс.
Просмотр / печать Рисунок
РИСУНОК 11.
(вверху) Боковая стенка носа (правая сторона) с носовыми раковинами и передними клиновидными пазухами.(Внизу) Боковая стенка носа (правая сторона), носовые раковины разрезаны.
РИСУНОК 11.
(вверху) Боковая стенка носа (правая сторона) с носовыми раковинами и передними клиновидными пазухами. (Внизу) Боковая стенка носа (правая сторона), носовые раковины разрезаны.
Просмотр / печать Рисунок
РИСУНОК 12.
Анатомия носовых пазух. (Слева) Сужение обведенной области (средний носовой ход, средняя носовая раковина, крючковидный отросток) может спровоцировать синусит.(Справа) После функциональной эндоскопической хирургии носовых пазух остеомеатальная область открыта.
РИСУНОК 12.
Анатомия носовых пазух. (Слева) Сужение обведенной области (средний носовой ход, средняя носовая раковина, крючковидный отросток) может спровоцировать синусит. (Справа) После функциональной эндоскопической хирургии носовых пазух остеомеатальная область открыта.
Большинство случаев синусита вызвано проблемами в носу (риногенными). Иногда к синуситу приводит другая проблема, например, первичная зубная инфекция.Во время любого эпизода риносинусита реснички функционируют менее эффективно, что приводит к застою слизи. Слизистая пазухи носа набухает, часто закрывая устье. Результатом является плохо вентилируемый синус, а гипоксия и застой слизи создают идеальные условия для бактериальной инфекции.
Первоначальная оценка и лечение
Как и во многих случаях заболевания, анамнез пациента с синуситом, вероятно, является наиболее важной частью предоперационной оценки (Таблица 1). Все пациенты с тяжелыми или стойкими симптомами должны быть обследованы, и многим можно помочь советом и лечением.
Посмотреть / распечатать таблицу
ТАБЛИЦА 1Симптомы риносинусита
Обструкция носа |
Синофациальная боль или головная боль |
Снижение обоняния и вкуса |
Симптомы риносинусита
Обструкция носа и обструкция носа | |
53 | |
53 | Болезнь носа или рикофалита |
Чихание | |
Снижение обоняния и вкуса |
Волоконно-оптический эндоскоп позволяет хирургу детально исследовать нос и является важным инструментом для диагностики.Пациентам с сезонным или круглогодичным ринитом следует посоветовать избегать аллергенов и лечить местными назальными стероидными спреями и антигистаминными препаратами. Острый инфекционный синусит лечится с помощью антибиотиков и сосудосуживающих назальных спреев. Если лечение не помогло, пациент может быть подходящим кандидатом на эндоскопическую процедуру.
Кандидаты на операцию на носовых пазухах
FESS (как и любая операция на носовых пазухах) наиболее эффективен у пациентов с рецидивирующим острым или хроническим инфекционным синуситом.Пациенты, у которых преобладающими симптомами являются боль в лице и заложенность носа, обычно хорошо реагируют. Обоняние часто улучшается после такого типа операции.
КТ перед FESS является обязательной для определения анатомии решетчатой кости пациента и ее соотношения с основанием и орбитой черепа. КТ-сканирование также позволяет определить степень заболевания, а также любые анатомические аномалии, которые могут предрасполагать пациента к синуситу.
Таким образом, отбор пациентов включает в себя тщательный сбор анамнеза и физикальное обследование, пробное лечение и, наконец, компьютерную томографию.В результате получилась тщательно отобранная группа пациентов, которые могут ожидать улучшения своих симптомов до 90 процентов.
У пациентов с назальным полипозом, который не контролируется местными кортикостероидами, FESS позволяет точно удалить полипы с помощью отсасывающих ножей.5 Неизвестно, продлен ли интервал без заболевания для пациентов, перенесших эндоскопическую этмоидэктомию по поводу полипоза, по сравнению с обычным полипом. операция, но послеоперационный дискомфорт минимален.
Нендоскопическая «традиционная» хирургия носовых пазух vs.FESS
Ранее считалось, что после хронического воспаления слизистая оболочка необратимо повреждается и ее необходимо удалить. Это было обоснованием хирургической техники Колдуэлла-Люка, которая включает удаление пораженной слизистой оболочки антрального отдела верхней челюсти (рис. 13). Точно так же внешние хирургические доступы к решетчатой и лобной пазухам были разработаны как «радикальные операции», в ходе которых болезнь полностью исчезла. Эти процедуры оставили шрамы и вызвали значительные синяки и дискомфорт.Процедура Колдуэлла-Люка также вызвала онемение зубов. Эти «обычные процедуры», а также промывание носовых пазух концентрируются на вторично инфицированных носовых пазухах, игнорируя при этом важную патологию носа.
Просмотр / печать Рисунок
РИСУНОК 13.
Пациент, перенесший операцию по Колдуэллу-Люку, включающую удаление пораженной слизистой оболочки антрального отдела верхней челюсти.
РИСУНОК 13.
Пациент, перенесший операцию Caldwell-Luc, включающую удаление пораженной слизистой оболочки антрального отдела верхней челюсти.
Обоснование FESS состоит в том, что локализованная патология в остеомеатальном комплексе блокирует устье и приводит к воспалению в зависимых пазухах (рис. 12). Хирургические вмешательства процедуры предназначены для устранения остеомеатальной закупорки и восстановления нормальной вентиляции пазух и мукоцилиарной функции (рис. 12).
FESS, как и любая малоинвазивная хирургия, разработана таким образом, чтобы сочетать отличный результат с минимальным дискомфортом для пациента. Как уже упоминалось, главное преимущество FESS по сравнению с традиционными методами заключается в том, что он менее инвазивен, что приводит к минимальному послеоперационному дискомфорту.Также исключаются шрамы и повреждение нервной системы зубов. Использование эндоскопа позволяет лучше видеть операционное поле, и это, вероятно, является причиной меньшего количества осложнений.
Центром хирургии является остеомеатальный комплекс. Процедура может проводиться под местной анестезией, с седацией или без нее. FESS подходит для амбулаторной хирургии.
Хирургическая техника
После подходящей вазоконстрикции с помощью кокаина или эфедрина определяется средняя носовая раковина.Это самый важный ориентир для процедуры. На боковой стенке носа на уровне переднего конца средней носовой раковины лежит крючковидный отросток. Его удаляют (рис. 14), обнажая решетчатую буллу и отверстие, называемое полулунным перерывом, в которое впадают лобная и верхнечелюстная пазухи.
РИСУНОК 14.
Хирургическое удаление крючковидного отростка.
Затем открываются передние решетчатые воздушные ячейки, обеспечивая лучшую вентиляцию, но оставляя кость покрытой слизистой оболочкой.После этого осматривается устье верхней челюсти и, в случае его закупорки, открывается с помощью антростомы среднего носового отверстия (рис. 15). Этой минимальной операции часто бывает достаточно, чтобы значительно улучшить функцию остеомеатального комплекса и, следовательно, обеспечить лучшую вентиляцию верхнечелюстных, решетчатых и лобных пазух.
РИСУНОК 15.
Антростома среднего носа в правой ноздре.
Иногда компьютерная томография выявляет поражение задних решетчатых костей и клиновидной пазухи.Затем необходимо продвинуться дальше в эти пазухи. Однако в большинстве случаев синусита воспаление ограничивается остеомеатальным комплексом и передними решетчатыми костями.
Послеоперационный уход
В послеоперационном периоде важно, чтобы на носу не образовывались корки. Методы, используемые для этого, варьируются от трудоемкого носового туалета, выполняемого хирургом два-три раза в неделю, до простого спринцевания, выполняемого пациентом несколько раз в день.Нормальное функционирование обычно возвращается в течение одного-двух месяцев. У пациентов с выраженным воспалением или полипами короткий курс системных стероидов в сочетании с антибиотиками может ускорить послеоперационное выздоровление. Актуальные стероиды используются в послеоперационном периоде у пациентов, у которых были удалены полипы.
Результат
Результаты после FESS являются хорошими, при этом большинство исследований сообщают об успешности от 80 до 90 процентов.6–9 Хорошие результаты были также получены у пациентов, которые ранее перенесли операцию на носовых пазухах.
Процедура считается успешной, если исчезло большинство симптомов пациента. Скорее всего, удастся облегчить заложенность носа и лицевую боль, хотя постназальное выделение жидкости часто остается проблемой. Техника сравнивалась с процедурой Колдуэлла-Люка, и, хотя оба метода были признаны эффективными, пациенты сильно предпочли FESS.10 Степень заболевания влияет на результат, причем наилучшие результаты были получены у пациентов с ограниченным носовым ходом. патология, вызывающая вторичный синусит.11
Осложнения
Самым катастрофическим осложнением FESS является слепота в результате повреждения зрительного нерва. Однако имеющиеся данные показывают, что частота этого осложнения чрезвычайно мала.12,13
Утечка спинномозговой жидкости – единственное наиболее частое серьезное осложнение FESS, возникающее примерно в 0,2% случаев.13 Утечка обычно распознается в то время. хирургического вмешательства и легко поддаются ремонту; это следует подозревать, если в послеоперационном периоде наблюдаются четкие выделения из носа.Если выделения не загрязнены кровью, наличие глюкозы означает, что это, скорее всего, спинномозговая жидкость. Абсолютное подтверждение может быть получено при тестировании образца на наличие бета 2 трансферрина.
Другие, менее серьезные, но все же редкие осложнения включают гематому орбиты и стеноз носослезного протока. Следует подчеркнуть, что все эти осложнения также могут возникать при «традиционной» хирургии носовых пазух и, следовательно, пациенты не проходят новый курс лечения с более серьезными или более частыми осложнениями, чем при других операциях.В Соединенном Королевстве общая частота серьезных осложнений FESS составила 0,44 процента по сравнению с 1,4 процента у пациентов, перенесших аналогичные неэндоскопические процедуры.13
Расширенное использование FESS
Эндоскопическая дакриоциториностомия
Эту процедуру обычно выполняет отоларинголог и офтальмохирург, работающий вместе. Это может быть выполнено под местной анестезией во время визита в офис. Закупорка слезного протока подтверждается контрастной дакриоцистограммой.Хирург-офтальмолог расширяет проток и пропускает тонкий гибкий волоконно-оптический световод вниз по протоку, так что хирург-эндоскопист может идентифицировать свет в боковой стенке носа, обычно прямо перед средней носовой раковиной. Эндоскопист использует микродрель или лазер для удаления кости, лежащей над протоком. Стенты вставляются и остаются на месте на шесть недель. Показатель успешности такой же, как при наружной дакриориностомии (от 80 до 90 процентов), при этом избегают внешнего разреза.14
Эндоскопическая орбитальная декомпрессия
Показания к эндоскопической орбитальной декомпрессии включают оптическую нейропатию и проблемы, связанные с экзофтальмом щитовидной железы глаза. болезнь (рисунок 16).Эндоскопическая декомпрессия орбиты достигается сначала полным удалением ячеек решетчатой кости, а затем удалением тонкой кости (lamina papyracea), которая формирует медиальную стенку орбиты. Также может быть удалена медиальная часть орбитального дна. При необходимости толстую кость, которая непосредственно покрывает зрительный нерв на вершине глазницы, можно удалить с помощью микродрели. После полного раскрытия надкостницу глазницы продольно надрезают, позволяя орбитальному жиру выпадать в решетчатые полости.Обычно достигается уменьшение проптоза на 4-5 мм, и этот показатель выгодно отличается от методов декомпрессии, основанных на внешних разрезах.15
Просмотр / печать Рисунок
РИСУНОК 16.
Пациент при экзофтальме щитовидной железы до (вверху) и после (внизу) операции по уменьшению проптоза и воспаления.
РИСУНОК 16.
Пациент с экзофтальмом при заболевании щитовидной железы до (вверху) и после (внизу) операции по уменьшению проптоза и воспаления.
Доступ к областям, которые иначе трудно достичь
Эндоскоп обеспечивает доступ к областям, которые трудно увидеть с помощью обычных методов, например, к клиновидной пазухе. Возможно дренирование большинства лобных, решетчатых или клиновидных мукоцеле. Небольшие опухоли гипофиза также можно удалить эндоскопически.
Ограничения FESS
Острый тяжелый решетчатый и лобный синусит
Гной в результате острого решетчатого синусита (рис. 17) может прорваться через пластинку папируса и вызвать болезненные ощущения в глазу с риском потери зрения.Если ответ на внутривенные антибиотики не очень быстрый, требуется срочная декомпрессия орбиты. Кровотечение может возникать из-за острого воспаления, что чрезвычайно затрудняет эндоскопическую операцию. Этмоидэктомия через внешний разрез может быть предпочтительным вариантом.
РИСУНОК 17.
Пациент с острым этмоидитом, угрожающим зрению.
Тяжелый лобный синусит может быть связан с внутричерепным сепсисом, и в этих условиях прямой трепан во фронтальную пазуху вместе с соответствующим нейрохирургическим вмешательством является лучшим вариантом.
Злокачественные новообразования носа и пазух
Злокачественные новообразования носа и носовых пазух встречаются редко и часто проявляются поздно. Если показана радикальная операция, ее лучше всего проводить наружным доступом, например, отслаиванием средней зоны лица, боковой ринотомией и различными черепно-лицевыми процедурами. Однако эндоскоп полезен для диагностики и биопсии опухолей, а также для наблюдения за пациентами, перенесшими радикальную операцию по поводу рака.
Хронический риносинусит с полипозом носа: шаг вперед к биологической терапии
В центре внимания хронический риносинусит с полипозом носа: оставив в стороне эндоскопическую хирургию, шаг к биологической терапии.Это название исследования, опубликованного в Journal of Otolaryngology, в котором приняли участие несколько специалистов Humanitas, такие как доктор Лука Мальвецци, доктор Маттео Феррандо, доктор Франческа Пуджони, профессор Энрико Хеффлер и профессор Джорджио Вальтер Каноника.
Как объясняет д-р Лука Мальвецци, специалист в области оториноларингологии и лицевой хирургии шейки матки Humanitas: «Хронический риносинусит с полипозом носа и без него – сложное заболевание. В 2017 году нельзя больше допускать ошибку, заключающуюся в недооценке рецидивирующего или хронического воспаления дыхательных путей, называя его простой простудой или сезонным заболеванием, когда поражены верхние дыхательные пути, трахеитом или бронхитом, когда поражены нижние дыхательные пути.
В частности, хронический риносинусит с назальным полипозом или без него, а также с высокой частотой встречаемости часто связан с астмой и аллергическим ринитом. Ввиду такой тесной корреляции между верхними и нижними дыхательными путями пациенты с этими заболеваниями страдают нарушениями сна, глазными симптомами и колеблющимися нарушениями восприятия звука, относящимися к классическим ушным вкладышам, с немалой скоростью. Таким образом, эти пациенты имеют сложную клиническую и симптоматологическую картину со значительным негативным влиянием на качество жизни в виде отсутствия на работе, снижения успеваемости в школе, снижения внимания и концентрации (в том числе вождения собственного транспорта), снижения социальной активности, включая сексуальную активность.Короче говоря, болезнь, влияющая на качество жизни и социальные аспекты, не имеет значения также с точки зрения государственных расходов ».
Важность мультидисциплинарного лечения
«Риносинит все еще недооценивается даже в специализированной сфере, и его возможности для мультидисциплинарного лечения недостаточны. Фактически, если диагностировать риносинусит относительно просто, часто достаточно собрать подробный анамнез и эндоскопическое клиническое обследование верхних проводящих путей, роль специалиста сегодня должна заключаться в фенотипировании заболевания.Специалист должен инициировать междисциплинарное исследование и процесс управления с участием аллерголога и пульмонолога для выяснения наличия сопутствующих заболеваний, таких как аллергия и астма, должен исследовать эпителий дыхательных путей на предмет респираторных, биологических и иммунологических характеристик заболевания, чтобы предложить пациенту наиболее подходящее лечение по отношению к характеристикам того же самого. Мы должны все больше персонализировать лечение, применяя так называемую точную медицину », – сказал д-р.Мальвецци подчеркивает.
Роль хирургии
«Сегодня золотым стандартом хирургического лечения хронического риносинита с носовыми полипами и без носовых полипов является эндоскопическая хирургия риносинуса, которая развивается технологически и становится все более и более распространенной во всем мире. Мы можем предложить пациентам хирургическое лечение с использованием исключительно передовых технологических инструментов, но в отношении риносинусита с полипозом носа мы еще не можем гарантировать полное выздоровление.Это легко понять по количеству посещений по поводу полипоза носа и по частому плохому контролю симптомов.
Однако мы не должны попадаться в ловушку лечения такого заболевания, как полипоз носа, без ухода за пациентом. Понятно, что хирургия риносинусита все еще будет иметь важное место в будущем, поскольку эти заболевания являются показанием для хирургического лечения. Однако сейчас мы должны стремиться к тому, чтобы определить, почему, когда и как проводить лечение, лечение, которому должно предшествовать клиническое исследование, определяющее выбор лечения.Выявление иммунологических характеристик риносинусита с носовыми полипами или без них означает наличие четкой картины естественной эволюционной истории болезни, даже в условиях термиков, которые имеют тенденцию к рецидиву. Это также означает, что хирургическая процедура может быть изменена с учетом биологических характеристик человека, а не только патологии, которую мы будем лечить », – поясняет специалист.
Биологические препараты
«Важно иметь возможность предложить пациенту терапевтическую альтернативу хирургическому вмешательству.Это означает предложение лекарственного лечения, отличного от обычного, и часто повторяющегося лечения кортизоном, которое должно играть все более ограниченную роль, особенно для определенных возрастных групп и пациентов из группы риска.
В современную эпоху биологические лекарства – это новый терапевтический рубеж. Так что сегодня благодаря растущему интересу к иммунологическим основам, характеризующим ремоделирование слизистой оболочки носовых ям, придаточных пазух носа и нижних дыхательных путей, а также благодаря некоторым дополнительным знаниям о патофизиологических механизмах, регулирующих воспаление, и нововведениям в В области фармакологии у нас есть другой терапевтический выбор, ориентированный на биологические методы лечения (как в случае с моноклональными антителами), чтобы доминировать, например, при формах хронического риносинита с более тяжелыми носовыми полипами, характеризующимися ассоциацией с астмой, гиперэозинофилией и непереносимостью ацетилсалициловой кислоты. кислота.Этот новый терапевтический выбор заставил нас задуматься о роли эндоскопической хирургии риносинуса, которую сегодня необходимо полностью переосмыслить.
Моноклональные антитела – это препараты, которые модулируют воспаление и, в частности, репликацию и пролиферацию тех клеток, которые доминируют в воспалении, усиливая и воспроизводя его, например, эозинофилов », – отмечает специалист.
Роль точной медицины
«Прецизионная медицина должна быть единственным лекарством, рекомендуемым лекарством, которое будет предложено в 2017 году и в будущем каждому пациенту, потому что результаты показывают, что это решающий путь для пациентов, которые представляют повторное появление болезни после лечения или перед операцией », – заключает д-р.Мальвецци.
Хронический синусит и полипоз носа
ХРОНИЧЕСКИЙ СИНУСИТ И НАЗАЛЬНЫЙ ПОЛИПОЗ
ЭНТОНИ А. МАНКУЗО, УИЛЬЯМ О. КОЛЛИНС И КЭРОЛ Дж. ЛАНГДОК
КЛЮЧЕВЫЕ ТОЧКИ упорядоченная группа пациентов с клиническим диагнозом хронического риносинусита.
Этиология
Риносинусит
Синусит – воспаление слизистой оболочки придаточных пазух носа. Риносинусит в настоящее время является предпочтительным термином для этого состояния, потому что слизистая оболочка носа почти всегда одновременно поражается при возникновении синусита. 1–4 Отоларингология Рабочая группа по риносинуситу определила острый синусит как продолжающийся до 4 недель, подострый синусит продолжительностью более 4 недель, но более 12 недель и хронический синусит, когда симптомы длятся менее 12 недель. Рецидивирующий острый синусит определяется как более четырех эпизодов в год с полным исчезновением инфекций. Острый и подострый инфекционный риносинусит обсуждается в главе 84. Хронический риносинусит (ХРС) и часто связанный с ним полипоз придаточных пазух носа – темы этой главы.Другие соображения в этой главе включают частую связь этого заболевания с образованием мукоцеле и грибковой колонизацией.
Патофизиология СВК определена плохо, но многие медиаторы воспалительного заболевания были идентифицированы как часть процесса заболевания, в результате чего СВК является преимущественно воспалительным заболеванием. Способствующие факторы описаны в следующем разделе патофизиологии.
Хронический синусит, который когда-то считался заразным, теперь считается реже вызванным инфекционной этиологией, хотя пациенты могли заболеть инфекцией или заразиться в результате хронической обструкции придаточных пазух носа.Пациенты с аллергией, профессиональным или вазомоторным ринитом, полипами в носу или анатомической обструкцией, такой как отклонение перегородки и буллезная раковина, в анамнезе предрасположены к хроническим инфекциям. Риносинусит чаще встречается у пациентов с иммунодефицитом; у людей с проблемами перистальтики ресничек, такими как синдром Картагенера; и у пациентов с проблемами слизистого покрова, таких как пациенты с кистозным фиброзом (CF).
Термин хронический риносинусит теперь используется для описания этого состояния.Наличие СВК требует наличия двух или более из следующих симптомов: слизисто-гнойный дренаж, заложенность носа или некоторая комбинация лицевой боли, давления и / или полноты; гипосомия; высокая температура; кашель; зубная боль; и усталость. Также должно быть эндоскопическое присутствие воспаления и признаки риносинусита на изображениях.
Распространенными осложнениями хронического синусита являются наложение острого синусита, а у детей – аденоидита с вторичным серозным или гнойным средним отитом. Дакриоцистит и ларингит также могут возникать как осложнения хронического синусита у детей.Другие осложнения включают остеомиелит и образование мукоцеле.
Осложнения орбиты (группа 84) включают пресептальный и постсептальный целлюлит, поднадкостничный абсцесс, орбитальный целлюлит, орбитальный абсцесс и тромбоз кавернозного синуса. Внутричерепные осложнения (Глава 84) включают менингит, эпидуральный абсцесс, субдуральный абсцесс и абсцесс мозга.
Полипоз носа
Полипы носа возникают из любой части слизистой оболочки носа или придаточных пазух носа в результате различных заболеваний придаточных пазух носа.Наиболее распространенные полипы слизистой оболочки – это доброкачественные воспалительные поражения полости носа, которые возникают на слизистой оболочке носовой полости или придаточных пазух носа, часто в выходном тракте пазух. Они имеют воспалительную этиологию, но точные механизмы не определены, как обсуждается в следующем разделе патофизиологии.
Множественные полипы часто возникают у пациентов с хроническим синуситом, аллергическим ринитом, возможно связанным с аллергическим грибковым синуситом (AFS), и CF. Полипы связаны как с неаллергическими, так и с аллергическими заболеваниями.Термин «полип» может использоваться для описания любого из ряда доброкачественных или злокачественных опухолей или врожденных поражений, но это не значение термина в этой главе, хотя эти состояния могут быть включены в дифференциальный диагноз.
Распространенность и эпидемиология
СВК поражает от 10% до 15% населения США, что делает его более распространенным, чем любое другое хроническое заболевание. Заболеваемость увеличивается по неизвестным причинам.
Риносинусит чаще встречается у детей, вероятно, вторичный по отношению к учащению инфекций верхних дыхательных путей и астмы в педиатрической популяции.
Множественные воспалительные полипы носа обычно возникают у пациентов старше 20 лет и чаще встречаются у пациентов старше 40 лет. Носовые полипы редко встречаются у детей младше 10 лет, за исключением детей с МВ.
Заболеваемость во всем мире такая же, как в США. Вероятность возникновения воспалительных полипов у мужчин как минимум в два раза выше, чем у женщин.
Клиническая презентация
Симптомы СВК пересекаются с другими процессами заболевания, и может быть плохая корреляция между симптомами и результатами эндоскопии и визуализации.Пациенты с неосложненным риносинуситом могут иметь ринорею, заложенность носа, лицевое давление и боль, снижение обоняния и, возможно, лихорадку. Менее коррелирующие симптомы включают головную боль, боль в ушах или чувство полноты, неприятный запах изо рта, зубную боль, кашель, жар и усталость.
Маленькие полипы могут не вызывать симптомов, их можно увидеть только во время передней риноскопии. Небольшие полипы могут также блокировать отток носовых пазух, вызывая хронические или повторяющиеся симптомы острого синусита.
Более крупные и / или более обширные полипы могут вызывать обструкцию носовых дыхательных путей, постназальный дренаж, головные боли, храп и ринорею.Нарушения обоняния свидетельствуют о наличии полипов, препятствующих потоку воздуха в обонятельную щель, а не только о хроническом синусите. Может возникнуть носовое кровотечение, которое всегда вызывает опасения по поводу более серьезных поражений носовой полости.
Обширный полипоз или единственный большой полип, закупоривающий носовые полости и / или носоглотку, могут вызывать симптомы обструктивного сна и хроническое дыхание через рот. Мукоцеле как осложнение может изменить черепно-лицевую структуру, особенно у детей. Жалобы могут быть вызваны проптозом, гипертелоризмом и диплопией.Компрессия зрительного нерва возникает редко, а неврологические симптомы – крайне редко при отсутствии осложняющей внутричерепной инфекции.
Анатомия
Пазухи делятся на переднюю и заднюю группы, которые впадают в средний проход спереди и в клиновидно-этмоидальную выемку и верхний проход сзади. Анатомия подробно обсуждается в главе 78, а физиология выведения слизи из придаточных пазух носа, связанная с этой анатомией, рассматривается в следующем материале, а также в главе 83, посвященной эндоскопической хирургии носовых пазух (ESS).
Придаточные пазухи носа выстланы псевдостратифицированным столбчатым (респираторным) эпителием, который непрерывен со слизистой оболочкой носа. Слизисто-надкостничный синус и слизистая оболочка носа производят слизистые выделения, которые задерживают бактерии, и как слизь, так и бактерии транспортируются по слизистому покрову через устье синуса, чтобы проглотить или отхаркивать. Это нормальный процесс в пазухах, наполненных воздухом и сообщающихся с носовыми ходами через открытые устья.
Патология и характер заболевания
Патофизиология СВК плохо определена, но многие медиаторы воспалительного заболевания были идентифицированы как часть процесса заболевания, что делает СВК преимущественно воспалительным заболеванием.Факторы, способствующие развитию у некоторых пациентов, включают аллергию; иммунодефицит; аутоиммунное заболевание; колонизирующие грибы, вызывающие продолжающееся эозинофильное воспаление; хроническая инфекция, включая биопленки, остит и бактериальные супертоксины; внутренние факторы верхних дыхательных путей; химическое раздражение; и метаболические нарушения, такие как чувствительность к аспирину.
Все эти факторы могут нарушить мукоцилиарную транспортную систему, как описано в главах 83 и 84, и стимулировать рост бактерий, способствующих усилению воспаления слизистой оболочки.
Патогенез полипоза носа неизвестен. Развитие полипа в основном связано с хроническим воспалением; таким образом, состояния, приводящие к хроническому воспалению в полости носа, могут привести к носовым полипам. К таким процессам относятся бронхиальная астма, CF, аллергический ринит, AFS, CRS, первичная цилиарная дискинезия, непереносимость аспирина, непереносимость алкоголя, синдром Черга-Стросса и синдром Юнга и неаллергический ринит с синдромом эозинофилии (NARES), дисфункция вегетативной нервной системы и генетическая предрасположенность. условия могут быть способствующими факторами.
Полипы представляют собой дольчатые, выпуклые или выступающие области слизистой оболочки носа или носовых пазух, которые смещены лежащей под ним отечной стромой, часто в сочетании с некоторой степенью воспаления слизистой оболочки (рис. 85.1 и 85.2). Воспалительные изменения, вероятно, сначала возникают в боковой стенке носа или слизистой оболочке носовых пазух в результате действия вирусного бактериального или бактериального «триггера», который запускает воспалительную реакцию, причем этот процесс, возможно, усиливается турбулентным потоком воздуха. Исходный инцидент не может быть установлен.
Полипы чаще всего возникают в областях контакта в среднем проходе, которые создают турбулентный поток воздуха, сужение и связанное с ним завихрение, которое затем усугубляется воспалением слизистой оболочки (рис. 85.1). Считается, что анатомические аномалии, которые приводят к сужению среднего прохода, могут увеличить риск образования полипа. Изъязвление или выпадение подслизистой оболочки происходит вместе с восстановлением эпителия и образованием новых желез. Затем на слизистой оболочке может образоваться полип из-за усиленного продолжающегося воспалительного процесса эпителиальных клеток, эндотелиальных клеток сосудов и фибробластов.Этот цикл высвобождает медиаторы, которые создают условия, благоприятные для удержания воды, что увеличивает объем полипов (рис. 85.2). Вазомоторный дисбаланс может способствовать увеличению проницаемости сосудов и нарушению регуляции сосудов в строме полипа, что приводит к более выраженному отеку. Этот фактор отражается в бедной клетками строме полипов, которая также плохо васкуляризована и не контролирует вазомоторный контроль. Пациенты с МВ имеют клеточный дефект, что подтверждает теорию задержки воды как фактора, способствующего образованию полипов (рис.85,2).
РИСУНОК 85.1. A, B: Коронарные и сагиттальные переформатированные изображения, показывающие сложное развитие воздушных ячеек во фронтальной нише и в области воронки ( стрелки, ), которые могут способствовать изменению схемы воздушного потока и помогают создать обстоятельства, приводящие к хроническим заболеваниям. заболевание слизистой оболочки. Справа видна больная буллезная раковина ( наконечник стрелки ), которая может еще больше усугубить ситуацию и может объяснить, почему изменения справа сильнее, чем слева. C: Реформация коронарной компьютерной томографии (КТ), показывающая, что дренаж из воронки верхнечелюстной пазухи ( стрелок ) направляется в передние воздушные ячейки решетчатой кости ( стрелки ), а не непосредственно в средний проход. Такой вариант дренажных путей может быть фактором, способствующим хронической болезни носовых пазух. Это также можно рассматривать как нормальный вариант при отсутствии такого заболевания. D: На правой стороне этого коронарного КТ-разреза имеется нормальное устье верхнечелюстной пазухи ( наконечник стрелки ) и конфигурация пазухи по сравнению с гипоплазированной пазухой на левой стороне с ненормальным расположением медиальной стенки пазухи. это, вероятно, связано с нарушением движения ресничек, что приводит к хроническому утолщению слизистой оболочки ( стрелка ). E: Пациент с болью в лобной области. Эта простая пленка показывает нормально аэрируемую лобную пазуху с правой стороны ( белая стрелка ) и его нормальный несколько волнистый край ( белая стрелка ). Левая часть лобной пазухи, очевидно, хуже аэрируется ( стрелка ) и потеряла волнообразный край, что указывает на регрессивное ремоделирование из-за мукоцеле ( стрелок ). Хотя это показывает, что простые пленки могут успешно обнаруживать относительно запущенное заболевание носовых пазух, они не так надежны, как КТ, для исключения болезни и, конечно, не для исключения эрозивных костных изменений.
РИСУНОК 85.2. Компьютерная томография (КТ) и изображения магнитного резонанса (МРТ) у трех пациентов, предназначенные для иллюстрации патофизиологии хронического риносинусита (ХРС). A: КТ с аксиальным контрастированием показывает утолщение слизистой оболочки ( стрелка ). Имеется подслизистый отек ( наконечников стрелок ), который способствует формированию полиповидного хронического заболевания слизистой оболочки, которое выступает через медиальную стенку пазухи в полость носа. B: Сагиттальная реформация пазухи, видимая на ( B ), указывает на первичное воспаление слизистой ( белая стрелка ), вторичное изменение физиологии подслизистой оболочки и накопление жидкости в этом слое ( белые стрелки ). ) способствующие образованию полипа. На этом этапе развития заболевания в просвете пазухи еще остается значительное количество секрета ( черная стрелка ). C, D: МРТ-изображения 18-летнего мужчины с CRS, первоначально считавшимся ювенильной ангиофибромой, до тех пор, пока визуализация не показала полипы CRS-типа.В ( C ) Т1-взвешенное изображение с контрастным усилением демонстрирует утолщение слизистой оболочки правой верхнечелюстной пазухи ( белая стрелка ) и подслизистый отек ( белая стрелка ). Эти изменения становятся субстратом для возможного образования полипа, как показано в ( A ) и ( B ). Агрегатное полиповидное утолщение слизистой оболочки выпирало из костной части пазухи в полость носа ( черных наконечников стрелок ). Избыточная воспаленная слизистая оболочка ( черная стрелка ) присутствует в решетчатых костях и способствует генерализованному утолщению правой полиповидной слизистой оболочки.В какой-то момент патогенеза это полиповидное утолщение слизистой оболочки создает обструкцию выходного отверстия пазухи, как это наблюдается у этого пациента, и в конечном итоге может вызвать образование вторичного мукоцеле. В ( D ) Т2-взвешенное корональное изображение иллюстрирует вклад водянистых подслизистых изменений в эту патофизиологию. Подслизистый отек в пазухе ( белая стрелка ) на самом деле состоит из большего количества свободной воды, чем слизистые выделения просвета ( белая стрелка ). Отечная строма подслизистого компонента полипа создает большую часть полипа, как видно, выступающей в носовую полость ( черных наконечников стрелок ).Сочетание отека подслизистой оболочки и промежуточных выделений или утолщения слизистой оболочки проиллюстрировано в пазухах решетчатой кости ( черная стрелка ). E, F: Другой пациент демонстрирует, как дистрофические изменения могут влиять на слизистую оболочку при хроническом заболевании. В ( E ) плотности, выстилающие поверхность слизистой оболочки и, возможно, внутри просвета секрета, могут представлять собой сгущенные выделения, области грибковой колонизации и / или дистрофическую кальцификацию слизистой оболочки. Дистрофический кальциноз чаще бывает периферическим ( белая стрелка ).Грибковые изменения и изменения, вызванные сгущенными выделениями ( белых стрелок ), более вероятно, будут центральными. В ( F ) на аксиальном изображении показаны выделения, которые преимущественно выстилают поверхность слизистой оболочки ( стрелки, ) – результаты более соответствуют дистрофическим изменениям внутри слизистой оболочки, чем колонизации грибков.
Осложнения
Мукоцеле
Формирование мукоцеле требует обструкции дренирующего устья, полного помутнения пазухи или отдельной воздушной ячейки в комплексе пазух (рис.85,3–85,10). Эти состояния чаще всего встречаются у пациентов с СВК и особенно у пациентов с полипозом носа. Часто встречается предшествующий анамнез либо травмы, либо предыдущая операция на носовых пазухах или лице. Фактически, пациенты с СВК и полипозом носа могут иметь очень обширные мукоцеле, вовлекающие одну или несколько пазух с одной или обеих сторон. Мукоцеле может быть источником очень серьезных последствий, включая нарушения моторики глаз, проптоз, гипертелоризм, компрессионную оптическую невропатию и деформацию лица.Они также могут остро инфицироваться, образуя мукопиоцеле, что может привести к острым орбитальным и внутричерепным осложнениям, как описано в главе 84.
РИСУНОК 85.3. Изображения двух пациентов с мукоцеле клиновидной пазухи. A – C: Пациент 1. В ( A ) коронковая реформация показывает хронические полипы, сформированные внутри клиновидной пазухи ( стрелка ), выступающие через костную часть синуса и в носовую полость ( наконечников стрелок ) в виде сфенохоанальной полости. полип.В ( B ) та же полиповидная масса вызвала регрессивное ремоделирование на краях клиновидной пазухи с центральным основанием черепа и вторичным мукоцеле, состоящим из сильно уплотненного секрета, распространяющегося в пространство жевательного аппарата и основание крыловидных пластин ( стрелки ). (продолжение) В ( C ) продолжающееся расширение мукоцеле клиновидной пазухи с поврежденными выделениями включает широкую зону расхождения с дном средней черепной ямки ( наконечник стрелки ), и продолжающееся расширение в подвисочную ямку является признаком того, что насколько сложным может стать развитие мукоцеле.Плотность содержимого просвета пазухи может быть обусловлена просто высыханием секрета, но связь с грибковой колонизацией и такой высыханием относительно высока. D – F: Пациент 2 с мукоцеле клиновидной пазухи. В ( D ) мукоцеле выпирает через костную часть пазухи, вызывая очевидное регрессивное ремоделирование стенок пазух ( наконечников стрелок ). Содержимое кажется плотным и, вероятно, высохшим и, возможно, колонизированным грибами, на что указывает центральная область с более высокой плотностью ( стрелка ).В ( E ) Т1-взвешенный (T1W) магнитный резонанс (MR) с контрастным усилением показывает, что мукоцеле состоит из относительно тонкой увеличивающейся слизистой оболочки ( белые стрелки, ) с несколько более толстой усиливающейся слизистой, блокирующей устье ( черная стрелка). ). Выделения просвета имеют несколько большую интенсивность сигнала, чем жидкость ( белая стрелка ). В ( F ) Т2-взвешенная (T2W) МРТ демонстрирует патофизиологию, возможно, более наглядно. Отечная слизистая оболочка пазухи снова остается относительно тонкой ( стрелки, ) с несколько более толстым ( черная стрелка ) полиповидным утолщением слизистой оболочки в клиновидной выемке и вокруг устья клиновидной кости, вызывая первичную обструкцию.Изображение T2W дает лучшее представление об обезвоженной природе просвета секрета ( белая стрелка ), чем изображение T1W.
Только золотые участники могут продолжить чтение. Войдите или зарегистрируйтесь, чтобы продолжитьСвязанные
Frontiers | Золотистый стафилококк на культуре носовых пазух ассоциируется с рецидивом хронического риносинусита после эндоскопической хирургии носовых пазух
Введение
Хронический риносинусит (ХРС) характеризуется как хроническое воспаление придаточных пазух носа и считается одним из наиболее частых хронических воспалительных заболеваний, которым в настоящее время подвержено около 10% населения (Chen et al., 2003; Hastan et al., 2011). Хирургическое лечение является обычным явлением: только в Соединенных Штатах ежегодно выполняется более 400 000 операций на носовых пазухах (Anand, 2004). К сожалению, до одного из трех (DeConde and Soler, 2016) пациентов с CRS не справятся с эндоскопической хирургией носовых пазух (ESS) и послеоперационной медикаментозной терапией, что делает их невосприимчивыми к максимальному медико-хирургическому лечению. У пациентов с рефрактерным заболеванием наблюдается снижение качества жизни, плохой сон, утомляемость и обострение СВК, что приводит к значительному увеличению экономического бремени болезни (Rudmik et al., 2014), который в настоящее время оценивается в 10 000 долларов в год на одного рефрактерного пациента, или 12,8 млрд долларов в целом только в Соединенных Штатах.
К сожалению, несмотря на высокую стоимость СВК, его патогенез остается неясным, что тормозит разработку новых терапевтических стратегий. Авторы сообщили о различных факторах, связанных с отказом ESS, будь то анатомические аномалии или сопутствующие медицинские сопутствующие заболевания, среди нескольких других сообщенных этиологий (Mendelsohn et al., 2011). Кроме того, наша группа и другие описали параметры заболевания, которые могут сделать пациента более подверженным риску пересмотра ESS с максимальной неэффективностью медикаментозной терапии, например, предыдущее ESS для CRS, повышенный уровень сывороточного IgE (≥150 kIU / L) и / или уровни эозинофилов (≥500 клеток / мм), молодой возраст (≤38) (Nader et al., 2010).
Одна из основных проблем заключается в том, что мало что известно о первых событиях, приведших к разработке CRS. Наблюдение за пациентами после ESS может стать средством улучшения нашего понимания. В то время как при других респираторных заболеваниях, таких как астма и аллергические расстройства, когорты рождения, отслеживающие популяцию с раннего возраста, помогли выявить факторы, влияющие на развитие болезни (Jackson et al., 2017), у нас, к сожалению, еще нет «когорт рождения» для CRS. .Тем не менее, наблюдение за полостью пазух после ESS может предоставить возможность. CRS отличается от астмы и других атопических расстройств тем, что доступно хирургическое лечение, которое может вылечить болезнь. Несмотря на то, что этот контроль после ESS может быть только временным, наблюдение за пациентами после ESS можно рассматривать почти как когорту рождения, поскольку после операции мы можем профилировать изменения в молекулярных механизмах и микробиоме, поскольку полость заживления восстанавливает эпителий и повторно заселяет его микробиом. Эти ранние изменения после ESS кажутся важными для рецидива заболевания, поскольку результат кажется относительно стабильным по истечении 6 месяцев после временной точки ESS (Rudmik et al., 2014). Таким образом, этот параметр может предложить привилегированную среду для выявления факторов, связанных с ремиссией или рецидивом заболевания.
Мы предположили, что пациенты с предшествующими вмешательствами на носовых пазухах и с очень вирулентными патогенами, такими как грамотрицательные бактерии и Staphylococcus aureus , будут связаны с более плохим исходом после ESS. Чтобы проспективно оценить эту гипотезу и в дальнейшем определить факторы, влияющие на развитие заболевания, мы провели клиническое испытание, в котором оценивали развитие заболевания после ESS у группы пациентов с высоким риском рецидива после ESS, оценивая эпидемиологические, клинические, биохимические и микробные исходы. после ESS для CRS.
Материалы и методы
Дизайн исследования и группа пациентов
Проспективное исследование было проведено в период с ноября 2014 г. по декабрь 2016 г. в нашем медицинском центре третичного уровня для мониторинга развития пост-ESS в когорте пациентов с СВК (с назальным полипозом или без него) старше 18 лет с высоким риском рецидива заболевания. . Все операции были выполнены старшим автором (MD), который выполнил все послеоперационное ведение и оценку. Это исследование было одобрено Наблюдательным советом по этике Медицинского центра Монреальского университета (Center Hospitalier de l’Université de Montréal) CHUM-14.140.
Все пациенты были набраны, и до операции было получено информированное письменное согласие. Набор проводился членом исследовательской группы, не участвовавшим в уходе за пациентом в день операции, на последовательных пациентах между датами исследования, которые соответствовали критериям включения. Пациенты включались в исследование, если у них был хотя бы один из критериев, используемых для квалификации пациента с «высоким риском» рецидива, перечисленных ранее. Критерии исключения включали пациентов, которые получали антибиотики местного или системного действия за 4 недели до хирургического вмешательства.Кроме того, из исследования были исключены пациенты с муковисцидозом, перевернутой папилломой, остеомой, кистозными образованиями, мукоцеле, поражениями основания черепа или любыми другими опухолями носовых пазух.
Всем пациентам проводилось лечение ESS с сохранением слизистой и средней носовых раковин, что требовалось для выздоровления, которое обычно включало полную сфеноэтмоидэктомию и фронтальную синусотомию. Септопластика выполнялась по мере необходимости, обычно с использованием целевой эндоскопической техники. Все пациенты получали антибиотики широкого спектра действия и постепенно снижали дозу преднизона в течение 14 дней после операции.Пациенты были осмотрены для очистки полости через 14 дней (± 3 дня), после чего было начато и продолжено послеоперационное орошение носа один раз в день ампулами будесонида (BUD) 1,0 мг (Pulmicort Respules, AstraZeneca, Mississauga, ON, Canada). на протяжении всего остального 4-месячного периода наблюдения.
Оценки были выполнены в день операции (визит 1) и повторены через 4 месяца после операции (визит 2).
Оценка пациента
Все пациенты прошли следующие лабораторные тесты при приеме на работу и через 4 месяца наблюдения: общий IgE, высокоспецифичный С-реактивный белок (hsCRP) и полный анализ крови (CBC).Сыворотка также извлекалась и сохранялась для будущих анализов при каждом посещении. Ориентированные на пациента исходы оценивались с помощью вопросников с использованием шкалы сино-назальных симптомов (SNSS), а также теста сино-назальных исходов (SNOT-22) (Piccirillo et al., 2002). Эндоскопическая оценка придаточных пазух носа проводилась во время визита 2 и оценивалась с использованием модифицированной системы оценки Лунда-Кеннеди (Psaltis et al., 2014).
Определение рецидива заболевания и ремиссии
Чтобы свести к минимуму вариабельность оценки из-за различного восприятия пациентом болезни, мы использовали строгое определение с использованием эндоскопической оценки заболевания слизистой оболочки.Мы основали эту концепцию на критериях, используемых для диагностики СВК, когда нельзя полагаться только на симптомы и должны присутствовать объективные доказательства болезни. Таким образом, мы определили «ремиссию заболевания» как отсутствие поражения слизистой оболочки при эндоскопии. Отсутствие заболевания определяли эндоскопически как отек ≤1 по модифицированной шкале оценки слизистой оболочки Лунда-Кеннеди. Любое доказательство рецидива полипоза считалось рецидивирующим заболеванием.
Бактериология
Взятие мазков культуры проводили в начале каждого ESS и во время визита 2 на уровне решетчатого пузыря с помощью тампона с тонкой алюминиевой проволокой и тампона с мини-наконечником (BBL Cultureswab PLUS — BD Diagnostics Inc., Франклин Лейкс, штат Нью-Джерси) при прямой жесткой эндоскопии. Были приняты меры, чтобы избежать загрязнения тампона, касаясь преддверия носа или стенки полости. Образцы обрабатывались в больничной лаборатории, где их помещали на чашки и наносили штрихами для выделения аэробных бактерий на агар с маннитоловой солью, шоколадный агар Haemophilus и агаре МакКонки (Oxoid Inc, Nepean, ON). Выделение анаэробных бактерий проводили на агаре Brucella с 5% овечьей крови и в анаэробном бульоне Schaedler (Oxoid Inc, Nepean, ON).
Статистический анализ
Все данные были сведены в таблицу с использованием Microsoft Excel, а все статистические анализы были выполнены с использованием STATA 13.1 (STATACorp LP, College Station, TX). Количественные переменные представлены для описания истории болезни и хирургического вмешательства пациента, а также сопутствующих патологий. Двусторонний критерий хи-квадрат Пирсона или точные тесты Фишера использовались для анализа распространенности и соотношения демографических переменных и конкретных бактериальных штаммов между пациентами. Показатели SNSS и SNOT-22, а также лабораторные показатели среди пациентов до и после ESS оценивались с использованием двухвыборочного теста Стьюдента T с неравными дисперсиями.Коэффициент корреляции Пирсона использовался для оценки любой клинически значимой корреляции между непрерывными переменными. Дифференциальная относительная численность любых видов бактерий между типами культур измерялась с использованием знакового рангового критерия Вилкоксона. Для всех статистических анализов статистически значимым считалось p <0,05.
Результаты
В период с ноября 2014 года по декабрь 2016 года в общей сложности 116 пациентов из группы высокого риска, соответствующих нашим критериям включения, заинтересованных в участии и доступных для последующего наблюдения, прошли ESS для CRSwNP или CRSsNP.Демографические данные представлены в таблице 1. В целом пациенты хорошо ответили на ESS с клинически и статистически значимым средним снижением 12-балльной шкалы SNSS и SNOT-22 на 3,4 и 21,3, соответственно. Анкеты SNSS и SNOT-22 продемонстрировали сильную корреляцию между собой как на визите 1 ( r = 0,762; p <0,001), так и на визите 2 ( r = 0,761; p <0,001). Использование минимальной клинически важной разницы (MCID) для SNOT-22 из 9.5 (Browne et al., 2007) 75 пациентов (69,4%) достигли MCID SNOT-22 или выше через 4 месяца (среднее значение = 33,4, диапазон 9–75). Показатели SNSS и SNOT-22 до операции продемонстрировали умеренную корреляцию с оценками SNSS и SNOT-22 послеоперационного визита 2 ( r = 0,385; p <0,001 и r = 0,395; p <0,001, соответственно). SNOT-22 визита 2 имел небольшую корреляцию с общими баллами Лунда-Кеннеди ( r = 0,236; p = 0,014), в то время как оценки SNSS посещения 1 и SNOT-22 и посещения 2 не коррелировали с оценками Лунда-Кеннеди. Посетите 2 балла.
Таблица 1 . Демографические данные пациента.
Болезнь Ремиссия против рецидива
Согласно нашим строгим критериям заболевания, рецидив после ESS + BUD был значимо связан с пациентами, подвергавшимися повторной ESS ( p = 0,001), или с аллергией / непереносимостью нестероидных противовоспалительных препаратов (NSAID) ( p ). = 0,036) (таблица 2). В то время как наблюдалась тенденция к более высокому уровню неудач у пациентов с астмой ( p = 0.080) или CRS без полипоза ( p = 0,061), это не достигло значимости. Никакие лабораторные показатели достоверно не различались между пациентами с ремиссией или рецидивом заболевания после ESS. Кроме того, не было статистически значимой разницы между группами «ремиссии» и «рецидива» в отношении оценок SNSS и SNOT-22 на визите 2 ( p = 0,306 и p = 0,098, соответственно).
Таблица 2 . Ремиссия болезни vs.рецидив у всех пациентов.
Бактериальные мазки продемонстрировали статистически значимую связь между присутствием S. aureus до операции и рецидивом заболевания после ESS + BUD через 4 месяца после операции. Присутствие S. aureus на визите 2 также значимо ассоциировалось с рецидивом заболевания. В группе с рецидивом заболевания у 14 пациентов до операции было S. aureus , из которых 3 (21%) имели микробных мазков S. aureus после операции, в то время как 9 (64%) не смогли очистите его и еще 15 новых колонизаций.
Ревизия ESS Пациенты: ремиссия болезни против рецидива
Анализ подгрупп проводился только для пациентов, подвергшихся ревизии ESS по поводу CRS ( n = 80) (Таблица 3). Из них 35 (43,8%) имели более одного ESS для CRS до их включения в это исследование (диапазон 2–5). Шестьдесят процентов ( n = 48) продемонстрировали эндоскопические признаки рецидива заболевания во время визита 2. И снова, присутствие S. aureus в послеоперационном периоде было значимо связано с неудачей.Наличие сезонной аллергии было незначительным статистически значимым защитным фактором в этой подгруппе пациентов. Не было значительных различий в различных оцененных лабораторных значениях.
Таблица 3 . Ремиссия заболевания против рецидива у ревизионных пациентов ESS.
Обсуждение
Рефрактерный ХРС, не отвечающий на максимальную медикаментозную и хирургическую терапию, остается важным и растущим бременем, и в некоторых подгруппах его можно даже недооценивать.В этом исследовании мы оценили результаты первичного или повторного ESS с последующими 4 месяцами орошения носа будесонидом (BUD) в подгруппе пациентов с высоким риском рецидива заболевания после ESS. В предыдущих ретроспективных отчетах нашей группы мы сообщали о частоте рецидивов чуть более 30% (Maniakas and Desrosiers, 2014). В этом проспективном исследовании с использованием хорошо задокументированной строгой эндоскопической оценки заболевания слизистых оболочек частота неудач оказалась выше, достигая 50% в этой популяции пациентов с высоким риском.
Пациенты с предыдущим ESS подвергались наибольшему риску неудачи лечения. Это представляет особый интерес, так как более 80% пациентов, не прошедших ESS + BUD, имели хотя бы один ESS до включения в исследование. Это согласуется с современной литературой, согласно которой пересмотр ESS является плохим прогностическим фактором (Lee et al., 2008; Philpott et al., 2015). Бремя пересмотра ESS также отражается в частоте процедур, которым может подвергнуться один пациент в попытке контролировать болезнь. В этом исследовании из 80 пациентов, ранее имевших ESS, около 45% перенесли от 1 до 5 процедур.Этот показатель сопоставим с некоторыми недавними исследованиями, которые демонстрируют аналогичную проблему (Philpott et al., 2015). Таким образом, пациенты подвергаются риску различных интра- и послеоперационных осложнений, связанных с ESS, которые далеко не незначительны и, как известно, значительно чаще встречаются в ранее прооперированных носовых полостях. Что остается определенным, так это необходимость в дополнительных клинически значимых терапевтических вариантах, которые могут предложить долгосрочное альтернативное решение пересмотра ESS.
Самым интересным открытием нашего проспективного исследования было участие микробов в раннем рецидиве заболевания.Колонизация S. aureus присутствовала почти у половины всех пациентов, потерпевших неудачу ESS + BUD через 4 месяца, по сравнению только с 13% пациентов с ремиссией заболевания. Этот результат согласуется с современной литературой, в которой положительный посев на S. aureus описывается как плохой прогностический фактор после ESS (Jervis-Bardy et al., 2011). Интересно, что при наличии до операции S. aureus исчезло у 75% пациентов с ремиссией заболевания, но только 21% исчезло в группе с рецидивом заболевания.
Роль S. aureus в развитии или сохранении болезни давно подозревалась. В более ранней публикации мы показали, что восстановление S aureus выше в пораженных полостях после ESS, чем в здоровых (Al-Shemari et al., 2007). Это может отражать специфическое для изолята поведение в S. aureus . Наша группа ранее продемонстрировала, что способность S. aureus формировать биопленку была связана с худшим исходом (Bendouah et al., 2006), а Tan et al.продемонстрировали, что наличие интраэпителиальных форм варианта S. aureus с малыми колониями было связано с отрицательным исходом (Tan et al., 2014), возможно, через снижение иммунитета (Ou et al., 2016).
Хотя механизмы этого постулируются как включающие (i) модуляцию иммунной системы через энтеротоксин-опосредованную активацию иммунной системы суперантигеном и (ii) образование бактериальной биопленки S. .aureus может также использовать другие стратегии, что делает его реалистичным маркером развития болезни и мишенью для терапии. В дополнение к уже описанным стратегиям вирулентности для S. aureus наша группа недавно предложила две новые: (i) иммуномодулирующий эффект, модулируемый за счет индукции чрезмерно высоких уровней IL-10, противовоспалительного цитокина (Chau et al. al., 2009; Schwartz et al., 2017), и (ii) вредное воздействие на in vitro моделей эпителиальной регенерации и заживления ран, особенно в культурах клеток, выращенных у пациентов с СВК (Valera et al., под давлением).
Что еще предстоит определить, и на чем исследовательские группы сосредоточивают значительное время, так это на происхождении внешнего вида этого патогена на слизистой оболочке, либо в результате неоколонизации из внешней среды, либо из-за преддверия носа, введенного в решетчатые полости во время операции. или посредством планктонного распространения после хирургического разрушения существующей биопленки S. aureus (Jervis-Bardy et al., 2011). По всей видимости, на это не влияет использование послеоперационных антибиотиков: в проспективном исследовании, сравнивающем послеоперационное использование китайских трав, амоксициллина и плацебо после ESS, колонизация с S.aureus присутствовал на одинаковом уровне во всех трех группах, при этом примерно половина всех пациентов после ESS демонстрировала признаки неоколонизации S. aureus (Liang et al., 2011). Кроме того, возникает вопрос о том, являются ли некоторые люди генетически предрасположенными к колонизации S. aureus . Предыдущее сканирование геномных ассоциаций на основе пулов (pGWAS) (Cormier et al., 2014) показало, что вариации генов-кандидатов, участвующих в поглощении и разрушении бактерий, а также влияющих на функцию эпителиального барьера, связаны с S.aureus у пациентов с СВК, что предполагает потенциальную генетически обусловленную основу для восприимчивости.
Астма с полипозом носа и непереносимостью нестероидных противовоспалительных средств, также известная как аспириновое обострение респираторного заболевания (AERD), также была значительной связью с неэффективностью ESS + BUD. Из 17 пациентов с этим диагнозом у 13 (76,5%) был рецидив заболевания. Эти данные согласуются с современной литературой по этому заболеванию и дополняют выводы Mendelsohn et al.(Nader et al., 2010), которые продемонстрировали повышенную частоту рецидивов заболевания и пересмотр ESS.
Интересно, что хотя показатели SNSS и SNOT-22 были выше в группе с рецидивом заболевания, они не различались статистически значимо между двумя группами в любой момент времени. Наши результаты продемонстрировали сильную корреляцию между двумя показателями и еще больше усилили сопоставимость SNSS с оценкой SNOT-22 при оценке активного заболевания. Однако оценки SNOT-22 показали лишь небольшую, хотя и значительную корреляцию с плохой оценкой Лунда-Кеннеди.Это несоответствие, возможно, связано с предвзятостью самооценки субъективных оценок. Значительно более высокие баллы Лунда-Кеннеди наблюдались в группах рецидивов заболевания, несмотря на аналогичную интенсивность симптомов, что подчеркивает важность рассмотрения объективных результатов в дополнение к результатам, сообщаемым пациентами.
Потенциальным ограничением нашего исследования можно утверждать, что 4 месяца можно рассматривать как короткий период наблюдения после ESS. Однако несколько авторов ранее показали, что эндоскопические признаки рецидива появляются уже через 4 месяца (Stjärne et al., 2009; Amali et al., 2015) и что они кажутся стабильными в течение дополнительного 12-месячного периода наблюдения (DeConde and Soler, 2016). Кроме того, данные о SNSS и SNOT-22 являются самооценками, и пациенты могут либо неточно вспоминать тяжесть или распространенность своих симптомов, что приводит к смещению воспоминаний, это также может привести к смещению ответа из-за личного перцептивного влияния на симптоматологию. Именно по этим причинам исследования с использованием субъективных вопросников требуют объективных измеримых значений, таких как эндоскопическая шкала Лунда-Кеннеди.
Заключение
Пациенты, которым проводится ревизия ESS, подвергаются высокому риску рецидива заболевания, даже если ирригация будесонидом используется в послеоперационном периоде. Наличие S. aureus в культуре до операции или через 4 месяца после ESS связано с отрицательным результатом. Это предполагает, что S. aureus отрицательно влияет на исход, возможно, через ряд потенциальных взаимодействий с (i) иммунной системой, (ii) регенерацией и восстановлением эпителия носовых пазух или (iii) вмешательством в микробиом носовых пазух.Это говорит о том, что S. aureus может быть простым и недорогим биомаркером тяжести заболевания, и указывает на явную необходимость лучше оценить механистический вклад S. aureus в развитие и стойкость заболевания, чтобы разработать целевые терапевтические стратегии. Дополнительные исследования микробиома и экспрессии генов слизистой оболочки носовых пазух помогут понять некоторые сохраняющиеся патофизиологические вопросы.
Взносы авторов
AM: дизайн исследования; сбор и анализ данных; Составление рукописей, рецензирование, окончательное утверждение, ответственность по всем аспектам работы; M-HA: сбор и анализ данных; Рецензирование рукописей, окончательное согласование, ответственность по всем аспектам работы; AR и SA: сбор данных; Рецензирование рукописей, окончательное согласование, ответственность по всем аспектам работы; SN: сбор данных; рецензирование рукописей; окончательное согласование, ответственность по всем аспектам работы; LM: сбор и анализ данных; составление рукописей; окончательное согласование, ответственность по всем аспектам работы; MD: дизайн исследования; анализ данных; Написание рукописей, рецензирование, окончательное утверждение, ответственность по всем аспектам работы.
Финансирование
Эта работа была поддержана Канадским институтом исследований в области здравоохранения (CIHR) (AM), грантом Fonds de Recherche du Québec-Santé (FRQS) (AM) и неограниченным образовательным грантом от Pfizer Canada (AM).
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
Аль-Шемари, Х., Абу-Хамад, В., Либман, М., и Дерозье, М. (2007). Бактериология полостей пазух бессимптомных лиц после эндоскопических операций на пазухах. J. Отоларингол. 36, 43–48. DOI: 10.2310 / 7070.2006.0019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Амали, А., Саеди, Б., Рахави-Эзабади, С., Газави, Х., и Хассанпур, Н. (2015). Долгосрочный послеоперационный азитромицин у пациентов с хроническим риносинуситом: рандомизированное клиническое исследование. Am.J. Rhinol. Аллергия 29, 421–424. DOI: 10.2500 / ajra.2015.29.4244
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бендуа, З., Барбо, Дж., Хамад, В., и Дерозье, М. (2006). Формирование биопленки Staphylococcus aureus и Pseudomonas aeruginosa связано с неблагоприятным развитием после операции по поводу хронического синусита и полипоза носа. Отоларингол. Head Neck Surg. 134, 991–996. DOI: 10.1016 / j.otohns.2006.03.001
CrossRef Полный текст | Google Scholar
Браун, Дж. П., Хопкинс, К., Слэк, Р., и Кано, С. Дж. (2007). Тест сино-назального исхода (SNOT): можем ли мы сделать его более значимым с клинической точки зрения? Отоларингол. Head Neck Surg. 136, 736–741. DOI: 10.1016 / j.otohns.2007.01.024
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чау Т.А., Маккалли М.Л., Бринтнелл В. и др. (2009). Лиганды Toll-подобного рецептора 2 на стенке стафилококковых клеток подавляют активацию Т-клеток, индуцированную суперантигеном, и предотвращают синдром токсического шока. Нац. Med. 15, 641–648. DOI: 10,1038 / нм.1965
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Cormier, C., Mfuna Endam, L., Filali-Mouhim, A., Boisvert, P., Boulet, L.P., Boulay, M.E., et al. (2014). Основанное на объединении геномное исследование ассоциации выявляет генетические варианты, связанные с колонизацией Staphylococcus aureus у пациентов с хроническим риносинуситом. Внутр. Форум Allergy Rhinol. 4, 207–215. DOI: 10.1002 / alr.21276
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хастан, Д., Fokkens, W.J., Bachert, C., Newson, R.B., Bislimovska, J., Bockelbrink, A., et al. (2011). Хронический риносинусит в Европе – недооцененное заболевание. Исследование GA (2) LEN. Аллергия 66, 1216–1223. DOI: 10.1111 / j.1398-9995.2011.02646.x
CrossRef Полный текст | Google Scholar
Джексон Д. Дж., Герн Дж. Э. и Леманске Р. Ф. младший (2017). Уроки, извлеченные из когортных исследований новорожденных, проведенных в различных условиях. J. Allergy Clin. Иммунол. 139, 379–386.DOI: 10.1016 / j.jaci.2016.12.941
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джервис-Барди, Дж., Форман, А., Боуз, С., Валентайн, Р., и Вормальд, П.-Дж. (2011). Каково происхождение золотистого стафилококка в ранней послеоперационной полости носовых пазух? Внутр. Форум Allergy Rhinol. 1, 308–312. DOI: 10.1002 / alr.20050
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, Дж. Й., Ли, С. У., и Ли, Дж. Д.(2008). Сравнение результатов хирургического вмешательства при первичной и ревизионной эндоскопической хирургии носовых пазух при хроническом риносинусите с полипозом носа. Am. J. Otolaryngol. 29, 379–384. DOI: 10.1016 / j.amjoto.2007.11.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Псалтис, А. Дж., Ли, Г., Везеафшар, Р., Чо, К. С., и Хванг, П. Х. (2014). Модификация эндоскопической балльной системы Лунда-Кеннеди улучшает ее надежность и корреляцию с показателями результатов, сообщаемыми пациентами. Ларингоскоп 124, 2216–2223. DOI: 10.1002 / lary.24654
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лян, К. Л., Су, Ю. К., Цай, К. К., Лин, Дж. С., Цзян, Р. С., и Су, М. С. (2011). Послеоперационный уход с применением китайских трав или амоксициллина после функциональной эндоскопической хирургии носовых пазух: рандомизированное, двойное слепое, плацебо-контролируемое исследование. Am. J. Rhinol. Аллергия 25, 170–175. DOI: 10.2500 / ajra.2011.25.3610
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Маньякас, А., и Десрозье, М. (2014). Дополнительная терапия азитромицином у пациентов с постендоскопическим хирургическим вмешательством носовых пазух с высоким риском и неэффективностью ирригации кортикостероидами: аудит клинической практики. Am. J. Rhinol. Аллергия 28, 151–155. DOI: 10.2500 / ajra.2013.27.4017
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мендельсон Д., Еремич Г., Райт Э. Д. и Ротенберг Б. В. (2011). Частота ревизий после эндоскопической хирургии носовых пазух: анализ рецидивов. Ann. Отол. Ринол.Ларингол. 120, 162–166. DOI: 10.1177 / 000348941112000304
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Надер, М.-Е., Абу-Жауд, П., Кабалуна, М., и Дерозье, М. (2010). Использование ответа на стандартизированное лечение для выявления фенотипов для генетических исследований хронического риносинусита. J. Отоларингол. Head Neck Surg. 39, 69–75.
PubMed Аннотация | Google Scholar
Ou, J.J., Drilling, A.J., Cooksley, C., et al.(2016). Снижение врожденного иммунного ответа на вариант небольшой колонии Staphylococcus aureus по сравнению с его родительским штаммом дикого типа. Фронт. Cell. Заразить. Microbiol. 6: 187. DOI: 10.3389 / fcimb.2016.00187
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Филпотт, К., Хопкинс, К., Эрскин, С., Кумар, Н., Робертсон, А., Фарбауд, А., и др. (2015). Бремя повторной хирургии носовых пазух в Великобритании – данные Эпидемиологического исследования хронического риносинусита (CRES): кросс-секционное исследование. BMJ Open 5: e006680. DOI: 10.1136 / bmjopen-2014-006680
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пиччирилло, Дж. Ф., Мерритт, М. Дж. Мл., И Ричардс, М. Л. (2002). Психометрическая и клиническая валидность теста сино-назального исхода из 20 пунктов (SNOT-20). Отоларингол. Head Neck Surg. 126, 41–47. DOI: 10.1067 / mhn.2002.121022
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рудмик, Л., Смит, Т. Л., Шлоссер, Р.Дж., Хванг, П. Х., Мейс, Дж. К., и Солер, З. М. (2014). Затраты на продуктивность у пациентов с рефрактерным хроническим риносинуситом. Ларингоскоп 124, 2007–2012. DOI: 10.1002 / lary.24630
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шварц, Дж. С., Аль-Мот, С., Эндэм, М. Ф., Алромай, С., Мадренас, Дж., И Десрозье, М. (2017). Бактериальное уклонение от иммунитета через ответ хозяина, опосредованный IL-10, новый патофизиологический механизм хронического риносинусита. Ринология 155, 227–233. DOI: 10.4193 / Rhin16.199
CrossRef Полный текст | Google Scholar
Stjärne, P., Olsson, P., and Alenius, M. (2009). Использование мометазона фуроата для предотвращения рецидива полипа после эндоскопической хирургии носовых пазух. Arch. Отоларингол. Head Neck Surg. 135, 296–302. DOI: 10.1001 / archoto.2009.2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тан, Н. К., Куксли, К. М., Роскиоли, Э., Дриллинг, А. Дж., Дуглас, Р., Wormald, P.J., et al. (2014). Варианты малых колоний и переключение фенотипа внутриклеточного Staphylococcus aureus при хроническом риносинусите. Аллергия 69, 1364–1371. DOI: 10.1111 / all.12457
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Валера, Ф., Раффин, М., Адам, Д., Мэйл, Э., Ибрагим, Б., Беруб, Э, Дж., И др. (под давлением). Staphylococcus aureus нарушает восстановление эпителия придаточных пазух носа: эффекты у контрольных субъектов CRSwNP. J. Allergy Clinical Immunol. .
Лекарство, эффективное при лечении полипов носа у пациентов с хроническим синуситом – ScienceDaily
Использование препарата дупилумаб привело к улучшению назальных полипов у пациентов с хроническим синуситом и полипозом носа, не поддающимся лечению только интраназальными кортикостероидами, согласно исследованию, проведенному в феврале. 2 выпуск JAMA .
Хронический синусит, воспалительное состояние носовых пазух, является обычным явлением, распространенность которого в западных странах достигает 12 процентов.На основании результатов эндоскопии заболевание можно разделить на хронический синусит с полипозом носа или без него. Носовые полипы возникают в пазухах и закупоривают пазухи и носовые ходы. Дупилумаб продемонстрировал клиническую эффективность при астме и атопическом дерматите, а также улучшил сино-назальные симптомы у пациентов с астмой.
Клаус Бахерт, доктор медицинских наук, Университетская больница Гента, Гент, Бельгия, и его коллеги случайным образом отобрали 60 взрослых с хроническим синуситом и полипозом носа, не реагирующих на интраназальные кортикостероиды, на дупилумаб (путем инъекции; n = 30) или плацебо ( n = 30) плюс назальный спрей мометазона фуроат в течение 16 недель.Исследование проводилось в 13 центрах США и Европы. Первичным измеренным результатом было изменение эндоскопической оценки полипа носа (на основе размера полипа).
Среди 60 рандомизированных пациентов 51 завершил исследование. Исследователи обнаружили, что лечение дупилумабом было связано со значительным улучшением эндоскопических, клинических, рентгенографических и фармакодинамических конечных точек через 16 недель. Сообщалось о значительном улучшении качества жизни и основных симптомов, таких как субъективное обоняние, заложенность или заложенность носа и ночные пробуждения.
Дупилумаб в целом хорошо переносился, и серьезных побочных эффектов, связанных с приемом дупилумаба, не считалось.



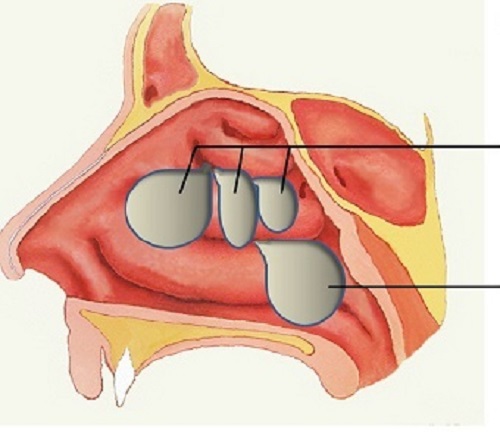 Данный симптом проявляет себя наиболее интенсивно в случае прогрессирования гнойного процесса.
Данный симптом проявляет себя наиболее интенсивно в случае прогрессирования гнойного процесса.

 В тяжелых случаях или перед проведением операции могут порекомендовать пройти 3-5-дневный курс оральных кортикостероидов.
В тяжелых случаях или перед проведением операции могут порекомендовать пройти 3-5-дневный курс оральных кортикостероидов.
 С появлением эндоскопии большинство операций теперь минимально инвазивны. Целью хирургического лечения является восстановление вентиляции синусов, коррекция и восстановление функциональности слизистой оболочки. Функциональная эндоскопическая операция при хроническом риносинусите помогает добиться позитивных результатов с полным или умеренным облегчением симптомов у 80-90% пациентов. Конечно же, операцию необходимо дополнять медикаментозной терапией.
С появлением эндоскопии большинство операций теперь минимально инвазивны. Целью хирургического лечения является восстановление вентиляции синусов, коррекция и восстановление функциональности слизистой оболочки. Функциональная эндоскопическая операция при хроническом риносинусите помогает добиться позитивных результатов с полным или умеренным облегчением симптомов у 80-90% пациентов. Конечно же, операцию необходимо дополнять медикаментозной терапией. Благодаря этому нормализуется состояние слизистой носа. Значительно ускоряется процесс восстановления. Такой отвар обладает антифлогистическим эффектом.
Благодаря этому нормализуется состояние слизистой носа. Значительно ускоряется процесс восстановления. Такой отвар обладает антифлогистическим эффектом.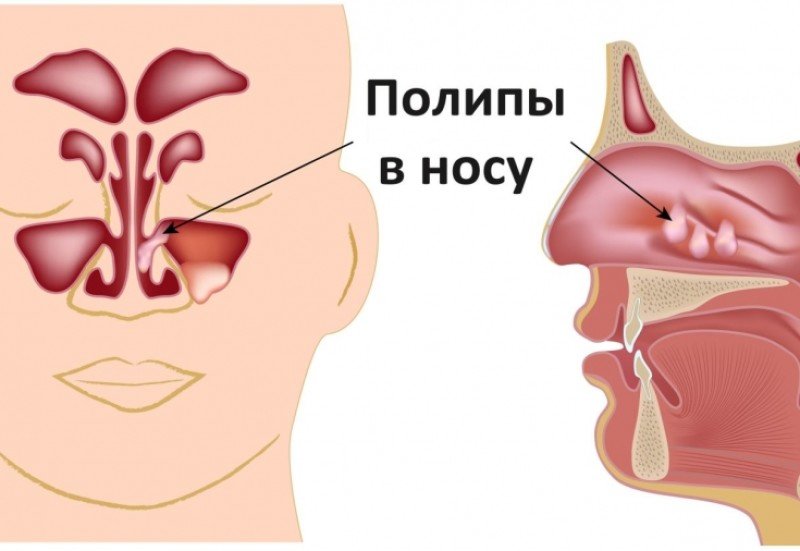

 Оно проводится под контролем оптических приборов (эндоскоп или операционный микроскоп).
Оно проводится под контролем оптических приборов (эндоскоп или операционный микроскоп).
