Микобактерии туберкулеза, определение ДНК (Mycobacterium tuberculosis, DNA) в сыворотке крови
Метод определения ПЦР с детекцией в режиме «реального времени».
Исследуемый материал Сыворотка крови
Доступен выезд на дом
Онлайн-регистрацияОпределение ДНК возбудителей туберкулеза, комплекса микобактерий: M. tuberculosis, M. bovis, M. bovis BCG, M. microti, M. africanum в сыворотке крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени».
Туберкулёз (от лат. tuberculum — бугорок) – распространённое, социально зависимое заболевание человека. Болеют им и животные. Возбудитель туберкулёза открыт Р. Кохом в 1882 г. Это кислотоустойчивые аэробные бактерии (74 вида) рода Мycobacterium, широко распространённые в почве, воде и у животных. У человека чаще всего возбудителем является Mycobacterium tuberculosis. Второй по частоте является Mycobacterium bovis. Оба вида очень устойчивы ко многим факторам внешней среды, а в организме очень долго остаются жизнеспособными и могут вызвать заболевание через многие годы после заражения. Очень важно, что микобактерии туберкулёза могут образовывать так называемые L-формы. Сохраняясь в организме, они создают противотуберкулёзный иммунитет.
Длительное время туберкулёз может протекать скрыто и обнаруживаться случайно, хотя нередко уже проявляются такие симптомы, как слабость, быстрая утомляемость, субфебрильная температура, ночная потливость, а в крови – анемия и лейкопения. В настоящее время, несмотря на все достижения антимикробной терапии, туберкулёз угрожает будущему нации.
Существует много методов лабораторной диагностики туберкулёза: микроскопия мазка (чаще всего для этого используют мокроту), классический культуральный метод, ИФА. Всем им присущи достоинства, но и определённые недостатки, в частности, обнаружение микобактерий только в случае их достаточного количества.
В последние годы для диагностики используют полимеразную цепную реакцию (ПЦР). Её высокая чувствительность позволяет обнаружить в исследуемом материале единичные клетки и даже их фрагменты ДНК. Метод исключает перекрёстные реакции и специфичность достигает 100%. ПЦР позволяет дифференцировать ограниченные и диссеминированные формы туберкулёза, особенно у детей даже при отрицательных результатах микробиологических исследований.
Аналитические показатели:
- определяемый фрагмент – специфичные участки ДНК микобактерий;
- чувствительность определения- 100 копий ДНК микобактерий в образце.
Литература
- Макаревич А.Э. Заболевания органов дыхания – М. Высшая школа, 2000. – 368 с.
- Jacobs D. et al. Laboratory test handbook/ Lexi-Comp./2002 – pр. 828 – 829.
Микобактерии туберкулеза, определение ДНК (Mycobacterium tuberculosis, DNA) в мокроте, смывах, лаважной жидкости
Метод определения ПЦР с детекцией в режиме «реального времени».
Исследуемый материал Мокрота, смывы, лаважная жидкость
Доступен выезд на дом
Определение ДНК возбудителей туберкулеза: комплекса микобактерий: M.
Туберкулёз (от лат. tuberculum — бугорок) – распространённое, социально зависимое заболевание человека. Болеют им и животные. Возбудитель туберкулёза открыт Р. Кохом в 1882 г. Это кислотоустойчивые аэробные бактерии (74 вида) рода mycobacterium, широко распространённые в почве, воде и у животных. У человека чаще всего возбудителем является Mycobacterium tuberculosis. Второй по частоте является Mycobacterium bovis. Оба вида очень очень устойчивы ко многим факторам внешней среды, а в организме очень долго остаются жизнеспособными и могут вызвать заболевание через многие годы после заражения. Очень важно, что микобактерии туберкулёза могут образовывать так называемые L-формы. Сохраняясь в организме, они создают противотуберкулёзный иммунитет. Длительное время туберкулёз может протекать скрыто и обнаруживаться случайно, хотя нередко уже проявляются такие симптомы, как слабость, быстрая утомляемость, субфебрильная температура, ночная потливость, а в крови – анемия и лейкопения.
В настоящее время, несмотря на все достижения антимикробной терапии, туберкулёз угрожает будущему нации. Поэтому все методы диагностики, особенно его латентных форм являются крайне важными.
Существует много методов лабораторной диагностики туберкулёза: микроскопия мазка (чаще всего для этого используют мокроту), классический культуральный метод, ИФА. Всем им присущи достоинства, но и определённые недостатки, в частности, обнаружение микобактерий только в случае их достаточного количества.
В последние годы для диагностики используют полимеразную цепную реакцию (ПЦР). Её высокая чувствительность позволяет обнаружить в исследуемом материале единичные клетки и даже их фрагменты ДНК. Метод исключает перекрёстные реакции и специфичность достигает 100%. ПЦР позволяет дифференцировать ограниченные и диссеминированные формы туберкулёза, особенно у детей даже при отрицательных результатах микробиологических исследований.
Аналитические показатели:
- определяемый фрагмент – специфические участки ДНК микобактерий;
- специфичность определения – 100%;
- чувствительность определения – 100 копий ДНК микобактерий в образце.
Литература
- Макаревич А.Э. Заболевания органов дыхания – М. Высшая школа, 2000. – 368 с.
- Jacobs D. et al. Laboratory test handbook/ Lexi-Comp./2002 – pр. 828 – 829.
T-SPOT.TB, сдать анализ на туберкулез
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Форма представления результата и интерпретация:
В ответе указывается количество спотов (специфически сенсибилизированных Т-лимфоцитов) после инкубации по антигенам А (ESAT-6) и B (CFP-10). Приводится общая оценка результата теста в качественной форме.
Интерпретация по количеству спотов:
- ≤ 4 – отрицательный;
- 5-7 – сомнительный;
- ≥ 8 – положительный.
Возможные формы заключения: «положительный», «отрицательный», «сомнительный».
«Положительный»: образец содержит эффекторные Т-клетки, реактивные (специфически сенсибилизированные) к M. tuberculosis.
«Отрицательный»: образец не содержит эффекторных Т-клеток, реактивных (специфически сенсибилизированных) к M. tuberculosis в значимой концентрации.
«Сомнительный»: Получен пограничный результат. Целесообразно провести повторное исследование через 1-2 месяца. При повторном получении пограничного результата для уточнения статуса пациента по ТВ инфекции следует использовать другие методы обследования и/или данные эпиданамнеза.
При повторном получении пограничного результата для уточнения статуса пациента по ТВ инфекции следует использовать другие методы обследования и/или данные эпиданамнеза.
Для использования в целях установления диагноза или исключения туберкулеза, а также для оценки вероятности наличия латентной туберкулезной инфекции, при интерпретации результатов T-SPOT.TB необходимо принимать во внимание весь комплекс эпидемиологических, анамнестических и клинических данных и результаты других проведенных диагностических исследований.
Примечание. Отрицательный результат не исключает возможности экспозиции к M. tuberculosis или текущей инфекции. При получении отрицательного результата T-SPOT.TB теста лицам, имевшим недавний контакт с инфицированными и отрицательный результат T-SPOT.TB теста, а также при наличии значимых клинических признаков возможной инфекции следует повторить тестирование через шесть недель. По оценкам, приведенным производителем, чувствительность метода при исследовании лиц с подтвержденным культуральным методом туберкулезом составила 95,6%.
Положительный результат не позволяет различить латентную инфекцию и активное заболевание. Для подтверждения активной формы туберкулеза следует применить другие тесты (ПЦР или культуральное исследование мокроты, рентгенографию грудной клетки). Хотя применяемые в данном тесте антигены отсутствуют в вакцине БЦЖ и у большинства других микобактерий, ложноположительный результат может отмечаться у лиц с инфекцией M. kansasii, M. szulgai, M. gordonae или M. marinum. При подозрении на такие инфекции могут потребоваться альтернативные тесты. Применение T-SPOT.TB теста не оценивали у лиц, получавших более одного месяца противотуберкулезную терапию. По оценкам, приведенным производителем, специфичность метода в группе лиц с низким риском туберкулеза составила 97,1%.
какие сдавать, методы диагностики, где можно сдать
Микроскопия мазка подразумевает поиск возбудителя туберкулеза в отделяемой при кашле жидкости — мокроте.

Подробнее…
Метод ИФА подходит в качестве уточняющего шага, а также для диагностики скрыто протекающего и внелегочного туберкулеза.
Узнать цены…
Метод ПЦР позволяет обнаружить туберкулез даже тогда, когда все другие методики показывают отрицательный результат.
ПЦР: что это такое?
Эксперты констатируют: туберкулез в России — больше, чем просто болезнь. Это — неприятное социальное клеймо, которое, помимо физических страданий, становится для заболевшего человека источником серьезного психологического дискомфорта, а иногда и вынуждает на долгие месяцы и годы отказаться от привычного образа жизни, карьеры и планов на будущее.
Лечение туберкулеза — процесс сложный и длительный, а успех во многом определяется тем, насколько своевременно было выявлено заболевание. С учетом того, что никто из нас не застрахован от заражения, крайне важно регулярно проходить профилактическое скрининговое обследование, а при малейших подозрениях на недуг — обращаться к уточняющим анализам. Лишь такое ответственное поведение убережет вас от беды.
Когда сдать анализы на туберкулез и почему не стоит с этим медлить
По мнению обывателей, туберкулезом страдают лишь неблагополучные люди, проживающие на грани нищеты, а также выходцы из мест лишения свободы. Однако такой взгляд, как отмечают врачи, не имеет ничего общего с реальностью. Пациентами фтизиатров нередко становятся и учителя, и бизнесмены, и чиновники, и даже сами доктора. Ведь ключевой фактор, приводящий к развитию заболевания, — это отнюдь не финансовое благополучие, а состояние иммунитета. Если по каким-то причинам (стресс, сопутствующее заболевание, беременность, перенесенная операция, погрешности в питании) организм ослаблен — туберкулезная палочка не упустит шанса для атаки.
Важно знать
По статистике в России ежегодно туберкулез выявляют более чем у 80-ти тысяч человек. Каждый третий заболевший погибает от этой болезни. При этом важно понимать, что 90% жителей уже инфицированы — то есть в их легких живет возбудитель заболевания. Но сильный иммунитет не дает болезни развиться, поэтому лишь 1% инфицированных столкнется с какими-либо симптомами туберкулеза.
При этом важно понимать, что 90% жителей уже инфицированы — то есть в их легких живет возбудитель заболевания. Но сильный иммунитет не дает болезни развиться, поэтому лишь 1% инфицированных столкнется с какими-либо симптомами туберкулеза.
Болезнь развивается постепенно, начинаясь в лимфатических узлах, а затем распространяясь по органам и тканям организма. Чаще туберкулез поражает легкие, однако в некоторых случаях, а также при отсутствии лечения бактерии размножаются в пищеварительном тракте, органах мочеполовой системы, костях, коже, оболочках головного и спинного мозга и даже в глазах.
Коварная особенность возбудителя заболевания — микобактерии туберкулеза — умение быстро приобретать устойчивость к антибактериальным препаратам, без которых невозможно успешное лечение. Ученые вынуждены разрабатывать все новые и новые лекарства, что в конечном итоге делает терапию дорогой, а также приводит к неизбежным побочным эффектам, таким как поражение печени. Поэтому важным этапом диагностики туберкулеза является определение чувствительности выявленного возбудителя к различным антибиотикам, это помогает врачам подобрать эффективное лечение.
В силу широкого распространения туберкулеза в нашей стране (70% от общего числа российских больных инфекционными и паразитарными заболеваниями умирают именно из-за такого диагноза) выявление зараженных микобактериями среди детей и взрослых организовано достаточно хорошо.
Так, детям и подросткам до 18-ти лет время от времени проводят туберкулиновые пробы, знакомые нам всем как реакция Манту. После достижения совершеннолетия основным методом диагностики становится флюорография, которую каждый гражданин РФ обязан проходить раз в два года, а определенные категории людей — каждый год. Без такого рентгеновского снимка вас, скорее всего, не допустят к работе: результаты флюорографии необходимо предъявлять при трудоустройстве, а в дальнейшем — повторять процедуру в ходе регулярных медосмотров. Таким образом медики стараются минимизировать количество больных туберкулезом, которые не получают лечение и заражают окружающих.
Помимо этих правил, провериться на туберкулез нужно в случаях, если у вас появились симптомы, указывающие на вероятность развития заболевания (слабость, ночное потоотделение, необъяснимая потеря веса, небольшое повышение температуры по вечерам, увеличение лимфоузлов, хронический кашель). Иногда догадка о возможной причине такого недомогания возникает у врача, но вы и сами можете пройти обследование и сдать анализы, чтобы исключить вероятность инфекции.
Какие анализы сдают на выявление микобактерии туберкулеза
Выявить туберкулез можно несколькими путями. Основной задачей диагностики в детском возрасте является определение самого факта инфицирования, ведь в этот период вероятность, что бактерия, попавшая в организм, сразу вызовет патологический процесс, значительно выше, чем у взрослых. По этой причине ведущей методикой первичного скрининга остается туберкулиновая проба.
Оценить признаки поражения легких — наиболее типичное клиническое свидетельство начала заболевания — позволяет флюорография. В случае сомнений для уточняющей диагностики врач назначит рентген — развернутую визуализацию легочной ткани.
Лабораторные анализы крови и мочи помогают «поймать» возбудителя туберкулеза или зафиксировать следы его присутствия в организме. Их назначают для окончательного установления диагноза, а также в целях уточнения степени тяжести заболевания и чувствительности микобактерии к антибиотикам.
Туберкулиновая проба-тест
Туберкулин — это смесь белков, выделенных из погибших возбудителей туберкулеза. Введение небольшого количества такого препарата под кожу вызывает реакцию иммунитета у всех людей, однако в зависимости от состояния их здоровья она проявится по-разному. Так, у пациентов, в организме которых отсутствует микобактерия туберкулеза, через двое суток после пробы останется лишь незначительный след от укола (или его не будет вовсе). Если же размер красной отметины в месте введения туберкулина больше сантиметра или в этой области на коже появился гнойник — высока вероятность, что человек заражен.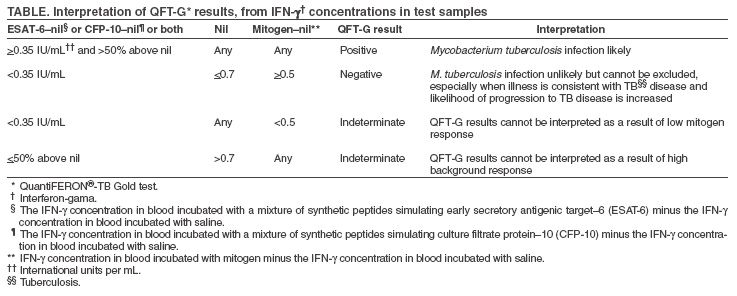
Напомним, реакция Манту — метод первичной диагностики, он не может со 100%-ной вероятностью ответить на вопрос, болен ли человек туберкулезом, но позволяет выделить группу риска, которой предстоит пройти дополнительные обследования.
Аппаратные методы диагностики
Поскольку степень инфицирования населения в России микобактериями туберкулеза очень высока, у лиц старше 18-ти лет врачи по умолчанию допускают контакт с инфекцией. Задачей становится поиск больных со скрыто протекающей инфекцией, которые не знают о своем состоянии.
- Флюорография
Оптимальным методом массовой диагностики в этом случае была и остается флюорография. Это — фотоснимок экрана рентгеновского аппарата, который можно получить очень быстро, не подвергая при этом человека значительной лучевой нагрузке. Поэтому кабинеты флюорографии есть практически во всех населенных пунктах нашей страны, а пройти процедуру можно за считанные минуты. - Рентген и КТ
В случае если человек не предъявляет никаких жалоб на самочувствие, а флюорография не выявила признаков изменения легочной ткани, врачи делают заключение, что туберкулеза у пациента нет. Но для более тщательной проверки легких может быть назначено развернутое рентгенографическое исследование (когда снимки делаются не только в прямой, но и в боковой проекции, а специалист лучевой диагностики тщательно изучает каждый сантиметр изображения), а также компьютерная томография (КТ), позволяющая с наибольшей степенью достоверности выявить визуальные признаки туберкулеза и оценить степень распространения патологического процесса.
Типы лабораторных анализов на туберкулез
Некоторые из лабораторных анализов, назначаемых при подозрении на туберкулез, являются специфическими — они проводятся только при этом заболевании. Другие же вы можете пройти в рамках общего медицинского осмотра: это ценный источник информации о вашем состоянии здоровья, который способен указать на наличие инфекционного процесса.
- Общий анализ крови/мочи является диагностическим стандартом при самых разных патологиях. В случае с туберкулезом исследование крови покажет повышение уровня лейкоцитов (сдвиг лейкоцитарной формулы влево) и ускоренную скорость оседания эритроцитов (СОЭ). Изменения в анализе мочи будут наблюдаться при поражении микобактериями почек и мочевыводящих путей — в этом случае в образце обнаружатся признаки амилоидоза.
- Микроскопия мазка подразумевает поиск возбудителя туберкулеза в отделяемой при кашле жидкости — мокроте. Пациенты с подозрением на заболевание особым образом собирают мокроту в стерильную банку, после чего доставляют анализ в лабораторию. Там частицы мокроты переносят на предметное стекло и окрашивают методом по Цилю-Нильсену (при этом микобактерии туберкулеза приобретают хорошо различимый под микроскопом красный цвет, а большинство остальных микроорганизмов — синий).
- Классический культуральный метод. Если в ходе микроскопии лаборант выявил в мокроте микобактерии в достаточном количестве (более 5-ти в поле зрения), то следующим этапом лабораторной диагностики туберкулеза становится бактериологический посев образца в питательную среду. Будучи помещенными в оптимальные температурные условия, микроорганизмы быстро растут, что позволяет уточнить их вид и провести оценку чувствительности к различным типам антибиотиков.
- ИФА (метод иммуноферментного анализа) обнаруживает в крови у пациента антитела к туберкулезу, что указывает на инфицированность (но не обязательно на заболевание). Данный метод подходит в качестве уточняющего шага, а также для диагностики скрыто протекающего и внелегочного туберкулеза.
- ПЦР (метод полимеразной цепной реакции) выявляет ДНК микобактерий в различных средах — в сыворотке крови, моче, мокроте, спинномозговой жидкости и так далее. Это крайне точный метод, который с достоверностью в 100% может дать ответ на вопрос о том, присутствует ли возбудитель в конкретном органе человека.
 Чувствительность ПЦР так высока, что в некоторых случаях этот анализ позволяет обнаружить туберкулез даже тогда, когда все другие методики показывают отрицательный результат.
Чувствительность ПЦР так высока, что в некоторых случаях этот анализ позволяет обнаружить туберкулез даже тогда, когда все другие методики показывают отрицательный результат. - Гистологические анализы (биопсия) подразумевают изъятие маленького фрагмента ткани из тела пациента с целью его обстоятельного микроскопического изучения. Биопсия является важным методом диагностики, особенно в ситуациях, когда исследовать биологические жидкости при помощи других анализов не представляется возможным (например, в случае вялотекущего туберкулеза костей).
Диагностика туберкулеза — сложная и крайне ответственная задача, но благодаря развитию современных медицинских технологий получить точную информацию о состоянии здоровья и ответ на вопрос «болею ли я туберкулезом?» — стало доступно каждому. При наличии малейших подозрений на инфекцию — не откладывайте визит к врачу, ведь от вашей сознательности зависит не только прогноз заболевания — но и благополучие окружающих.
Посев мокроты и др. отделяемого нижних дыхательных путей на микрофлору и определение чувствительности к антибиотикам (с микроскопией мазка мокроты) (Lower Respiratory (sputum, lavage) Culture, Routine with Gram stain. Aerobic Bacteria Identification and S
Исследуемый материал Мокрота, промывные воды бронхов или трахеи
Бактериологический диагноз инфекционных поражений дыхательных путей и обоснование рациональной антибиотикотерапии.
Диагностика и лечение лёгочной патологии основана на многих специальных методах исследования. Важнейшим из них является микробиологический метод. Он необходим при дифференциальной диагносте пневмоний (пневмококковая, стафилококковая, стрептококковая и др.), абсцесса лёгких, хронических обструктивных заболеваний лёгких, бронхоэктазов. Только микробиологический диагноз позволять обосновать действительно рациональную терапию и излечить больного.
Выделяемые возбудители: этиологически значимые – H. influenzae, S. pneumoniae и M. catarrhalis, грамотрицательные бактерии семейства Enterobacteriaceae, P. aeruginosa, S. aureus (включая MRSA), S. pyogenes, Acinetobacter sp., грибы рода Candida.
Мокрота, проходя через верхние дыхательные пути и полость рта, может контаминироваться вегетирующей в них микрофлорой, это могут быть зеленящие стрептококки (S. viridans group), стафилококки (S.еpidermidis), непатогенные нейссерии (Neisseria sp.), непатогенные дифтероиды (Corynebacterium sp.), Lactobacillus sp., Candida sp. и некоторые другие.
Литература
- Беркоу Р. (Ред.). Руководство по медицине, т. I М. «Мир», 1997. 1045 с.
- Приказ МЗ СССР от 22 апреля 1985 г. № 535 Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностических лабораториях лечебно-профилактических учреждений.
- Энциклопедия клинических лабораторных тестов под ред. Н.У. Тица. Издательство “Лабинформ” – М. – 1997 – 942 с.
- Nightingale C. et al./ Antimicrobial Pharmacodynamics in Theory And Clinical Practice/2006/ M.Dekker inc./ 550 ps.
| Забор крови из вены | 100 | |
| Забор материала на онкоцитологию | 150 | |
| Забор мазка из влагалища (уретры) на степень чистоты | 150 | |
| Забор мазка из носа, уха или ротоглотки | 200 | |
| Забор материала на ПЦР диагностику | 150 | |
| Забор материала на бактериологическое исследование | 150 | |
| Диагностическая пункция под контролем УЗИ (молочная железа) 1 сторона | 600 | |
| Диагностическая пункция под контролем УЗИ (мягкие ткани) | 600 | |
| Диагностическая пункция под контролем УЗИ (щитовидная железа) | 600 | |
| Диагностическая пункция под контролем УЗИ (лимфатические узлы) | 600 | |
| Биопсийный соскоб из цервикального канала | 600 | |
| Забор биопсии влагалища, шейки матки, вульвы | 450 | |
| Аспирационный забор биоптата на гистологическое исследование | 1000 | |
| Забор материала на биопсию (из носа, глотки, уха) | 1500 | |
| Биопсия при цистоскопии (без стоимости гистологического исследования) | 250 | |
| Забор секрета простаты | 350 | |
| 1515 | Клинический анализ крови: общий анализ, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов) (Clinical Blood Analysis: General Blood Analysis, Leucocyte Formula, ESR (with Microscopic Examination of Blood Smear if Presence of Pathologic Changes)) | 350 |
| 5 | Общий анализ крови (ОАК) (без лейкоцитарной формулы и СОЭ) (General Blood Analysis, without White Blood Cell (WBC) Count and ESR) | 250 |
| 119 | Лейкоцитарная формула (дифференцированный подсчет лейкоцитов, лейкоцитограмма) с микроскопией мазка крови при наличии патологических сдвигов (Leucocyte Formula (Differential White Blood Cell Count) with Microscopic Examination of Blood Smear if Presence of Pathologic Changes) | 150 |
| 150 | Ретикулоциты (Reticulocytes) | 150 |
| 15RH | Rh (C, E, c, e) Kell-фенотипирование (Rh C (E, c, e) Kell-Phenotyping) | 600 |
| 140 | Аллоиммунные антитела, включая антитела к Rh-антигену (Anti Rh) | 420 |
| 1 | Активированное частичное (парциальное) тромбопластиновое время (АЧТВ (АПТВ), кефалин-каолиновое время) (Activated Partial Thromboplastin Time, APTT) | 200 |
| 2 | Протромбин (протромбиновое время, ПВ), МНО (Международное нормализованное отношение) (Prothrombin, Рrothrombin Time, PT, International Normalized Ratio, INR) | 200 |
| 3 | Фибриноген (Fibrinogen, FG) | 175 |
| 4 | Антитромбин III, % активности (АТ III, Antithrombin III, % Activity) | 285 |
| 194 | Тромбиновое время (ТВ) (Thrombin Time, TT) | 150 |
| 164 | D-димер (D-Dimer) | 935 |
| 190 | Волчаночный антикоагулянт (ВА) (Lupus Anticoagulant, LA ) | 500 |
| 1263 | Протеин C, % активности (Protein C, % Activity) | 1 500 |
| 1264 | Протеин S свободный (Protein S, Free) | 1 500 |
| 1153 | Плазминоген (Plasminogen) | 462 |
| 1155 | Протромбиновый индекс (ПТИ) (Prothrombin Index, PTI) | 100 |
| 1ГЕМ | Комплексное исследование системы гемостаза с интерпретацией (ПТИ, МНО, ПВ, тромбиновое время, фибриноген, D-димер, АЧТВ, антитромбин III, протромбин по Квику, плазминоген, ВА (подтверждающий), лабораторное описание врача) (Hemostatic System: PTI, INR, PT, FG, D-Dimer, APTT, Antithrombin III, Plasminogen, LA (with Description)) | 3 245 |
| 3ГЕМ | Гемостазиограмма (без описания) (Coagulation (without Description)) | 2 770 |
| 139 | СОЭ (Cкорость Оседания Эритроцитов, ESR) | 200 |
| Онкомаркеры (Tumor Markers) | ||
| 103 | ПСА общий (Простатический специфический антиген общий) (Prostate-Specific Antigen Total, PSA Total) | 380 |
| 92 | Альфа-фетопротеин (АФП) (?-Fetoprotein, AFP) | 310 |
| 141 | Раково-эмбриональный антиген (РЭА, карциноэмбриональный антиген) (Carcinoembryonic Antigen, CEA) | 400 |
| 142 | СА-15-3 (Углеводный антиген 15-3) (Carbohydrate Antigen СА-15-3, Cancer Antigen СА-15-3) | 500 |
| 144 | СА-19-9 (Углеводный антиген 19-9) (Carbohydrate Antigen СА-19-9, Cancer Antigen-GI) | 480 |
| 143 | СА-125 (Углеводный антиген 125) (Carbohydrate Antigen СА-125, Cancer Antigen СА-125) | 500 |
| ОБС69 | Онкориск мужской: предстательная железа (Male oncologic risk: prostate) | 770 |
| 2113 | Оценка здоровья простаты (ПСА общ.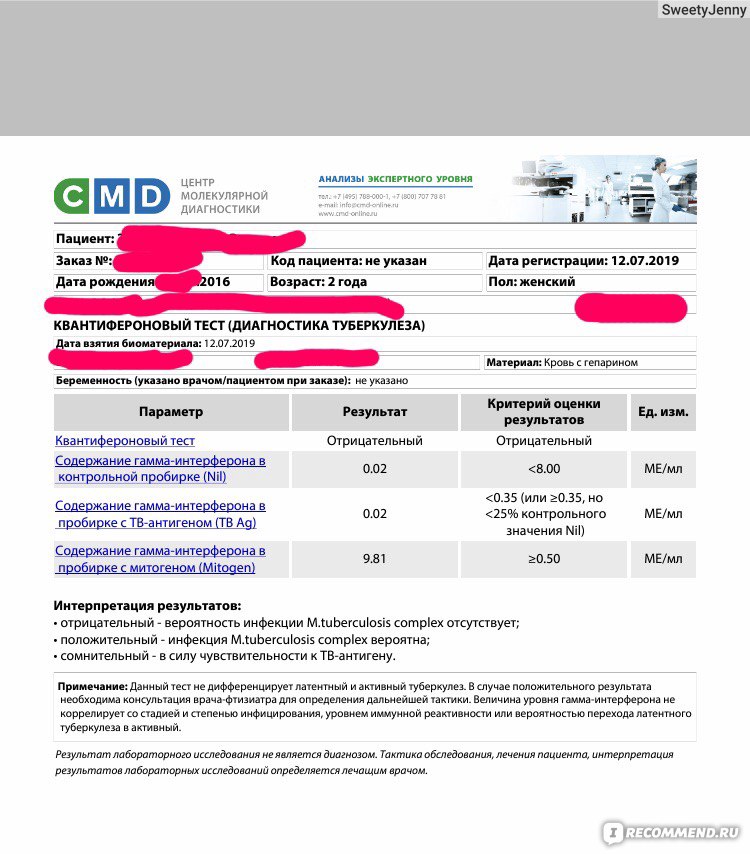 , ПСА св., -2proPSA, phi) , ПСА св., -2proPSA, phi) | 7 500 |
| 171 | Кальцитонин (Calcitonin) | 500 |
| 166 | CA-72-4 (Углеводный антиген 72-4) (Carbohydrate Antigen СА-72-4, Cancer Antigen CA-72-4) | 750 |
| 167 | Цитокератиновый фрагмент (Cyfra 21-1, фрагмент цитокератина 19) (Cytokeratin 19 Fragments, C-terminus of Cytokeratin 19, CK19 Soluble Fragments, Cyfra 21-1) | 750 |
| 141/43 | СА-125 + РЭА (Cancer Antigen СА-125 + CEA) | 950 |
| 1281 | HE4 (Белок 4 эпидидимиса человека) (Human Epididymis Protein 4, HE4) | 850 |
| 1280 | CA-242 (Углеводный антиген 242, опухолевый маркер CA-242) (Carbohydrate Antigen СА-242, Tumor Marker CA-242) | 710 |
| 208 | Бета-2-микроглобулин (?-2-микроглобулин) в сыворотке крови (Вeta-2-Microglobulin, BMG, Serum ) | 720 |
| 946 | Хромогранин А (Chromogranin A, CgA) | 4 540 |
| 1573 | Белок S100 (S100 Рrotein) | 1 900 |
| 1296 | SCC (Антиген плоскоклеточной карциномы) (Squamous Cell Carcinoma Antigen, SCCA, SCCAg) | 1 900 |
| 31 | Холестерин общий (Холестерин) (Cholesterol Total) | 150 |
| 32 | Холестерин ЛПВП (Холестерин липопротеинов высокой плотности, ЛПВП, ?-холестерин) (High-Density Lipoprotein Cholesterol, HDL Cholesterol) | 200 |
| 28 | Общий белок (Protein Total) | 130 |
| 22 | Креатинин (Creatinine) | 120 |
| 26 | Мочевина (Urea) | 120 |
| 27 | Мочевая кислота (Uric Аcid) | 120 |
| 37 | Кальций общий (Ca) (Calcium Total) | 100 |
| 165 | Кальций ионизированный (Ca2+, cвободный кальций) (Ionized Calcium, Free Calcium) | 200 |
| 40 | Магний (Мg) в сыворотке крови (Magnesium (Mg), Serum) | 140 |
| 155 | Общая железосвязывающая способность сыворотки (ОЖСС) (Total Iron Binding Capacity, TIBC) | 150 |
| 43 | С-реактивный белок (СРБ) (C-Reactive Protein, CRP) | 300 |
| 16 | Глюкоза (Glucose) | 120 |
| 17 | Фруктозамин (Fructosamine) | 220 |
| 18 | Гликированный гемоглобин HbA1С (HbA1С, Glycated Hemoglobin, GHB) | 600 |
| 215 | Лактат (Lactate) | 470 |
| ГТТ | Глюкозо-толерантный тест с определением глюкозы в венозной крови натощак и после нагрузки через 2 часа (2-Hour Oral Glucose Tolerance Test, OGTT, Glucose Concentration (Fasting and 2 Hours after Load), Venous Blood) | 450 |
| ГТГС | Глюкозо-толерантный тест с определением глюкозы и С-пептида в венозной крови натощак и после нагрузки через 2 часа (2-Hour Oral Glucose Tolerance Test, OGTT, Glucose and C-Protein Concentration (Fasting and 2 Hours after Load), Venous Blood) | 1 100 |
| 30 | Триглицериды (ТГ) (Triglycerides) | 160 |
| 33 | Холестерин ЛПНП (Холестерин липопротеинов низкой плотности, ЛПНП, ?-холестерин) (Low-Density Lipoprotein Cholesterol, LDL Cholesterol) | 100 |
| 218 | Холестерин ЛПОНП (Холестерин липопротеинов очень низкой плотности, ЛПОНП) (Very Low-Density Lipoprotein Cholesterol, VLDL Сholesterol) | 370 |
| 1071 | Липопротеин (a), ЛП (а) (Lipoprotein (a), Lp (a)) | 660 |
| 219 | Аполипопротеин А1 (Апопротеин А1, апо А1) (Apolipoprotein A1, Apo A1) | 440 |
| 220 | Аполипопротеин B (Апопротеин B, апо В) (Apolipoprotein B, Apo B) | 330 |
| 10 | Альбумин (Albumin) | 130 |
| 29 | Белковые фракции (Serum Protein Electrophoresis, SPE, SPEР) | 175 |
| 4050 | М-градиент, скрининг.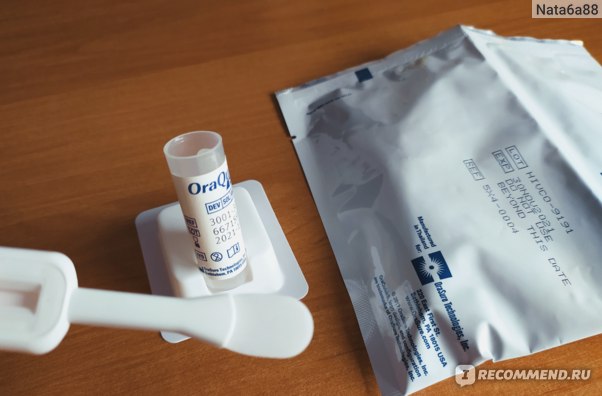 Электрофорез сыворотки крови, иммунофиксация с поливалентной антисывороткой, количественная оценка М-белка (без типирования) (M-Gradient, Screening. Serum Protein Electrophoresis (SPEP), Immunofixation with Polyvalent Antiserum, Quantification of M-Protein (without Typing)) Электрофорез сыворотки крови, иммунофиксация с поливалентной антисывороткой, количественная оценка М-белка (без типирования) (M-Gradient, Screening. Serum Protein Electrophoresis (SPEP), Immunofixation with Polyvalent Antiserum, Quantification of M-Protein (without Typing)) | 1 810 |
| 4051 | М-градиент, типирование. Электрофорез сыворотки крови, иммунофиксация с панелью антисывороток (раздельно к IgG, IgA, IgM, каппа, лямбда), количественная оценка М-белка (M-Gradient, Typing. Serum Protein Electrophoresis (SPEP), Immunofixation with Antisera (IgG, IgA, IgM, Kappa, Lambda), Quantification of M-Protein) | 3 350 |
| 1551 | Электрофорез белков мочи, определение типа протеинурии (Urine Protein Electrophoresis) | 1 420 |
| 1552 | Белок Бенс-Джонса в моче, скрининг с применением иммунофиксации и количественное определение (Bence-Jones Protein, Urine, Immunofixation, Quantification ) | 1 790 |
| 1553 | Белок Бенс-Джонса в моче: иммунофиксация, количественное определение, типирование каппа, лямбда (Bence-Jones Protein, Urine, Electrophoresis, Immunofixation, Kappa/Lambda Typing, Quantification ) | 2 850 |
| 153 | Гомоцистеин (Homocysteine) | 1 050 |
| 1526 | Клубочковая фильтрация, расчет по формуле CKD-EPIцистатин С (2012) (eGFR, Estimated Glomerular Filtration Rate, CKD-EPIcystatin C (2012) equation) | 680 |
| 1525 | Цистатин С (Cistatin C) | 640 |
| 40CKDEPI | Клубочковая фильтрация, расчет по формуле CKD-EPI – креатинин (Estimated Glomerular Filtration Rate, eGFR, CKD-EPI Creatinine Equation) | 140 |
| 13 | Билирубин общий (Bilirubin Total) | 130 |
| 11 | Альфа-амилаза (?-амилаза, диастаза) (Аlpha-Аmilase, ?-Amylase) | 175 |
| 12 | Альфа-амилаза панкреатическая (P-изофермент амилазы) (Pancreatic ?-Amylase) | 210 |
| 15 | Гамма-глутамилтранспептидаза (ГГТ, глутамилтранспептидаза) (Gamma-Glutamyl Transferase, GGT) | 120 |
| 19 | Креатинкиназа (Креатинфосфокиназа, КК, КФК) (Creatine Kinase, CK, Creatine Phosphokinase, CPK) | 200 |
| 20 | Креатинкиназа-МВ (Креатинфосфокиназа-МВ, КК-МВ, КФК-МВ) (Creatine Kinase-MB, CK-MB, Creatine Phosphokinase-MB, CPK-MB.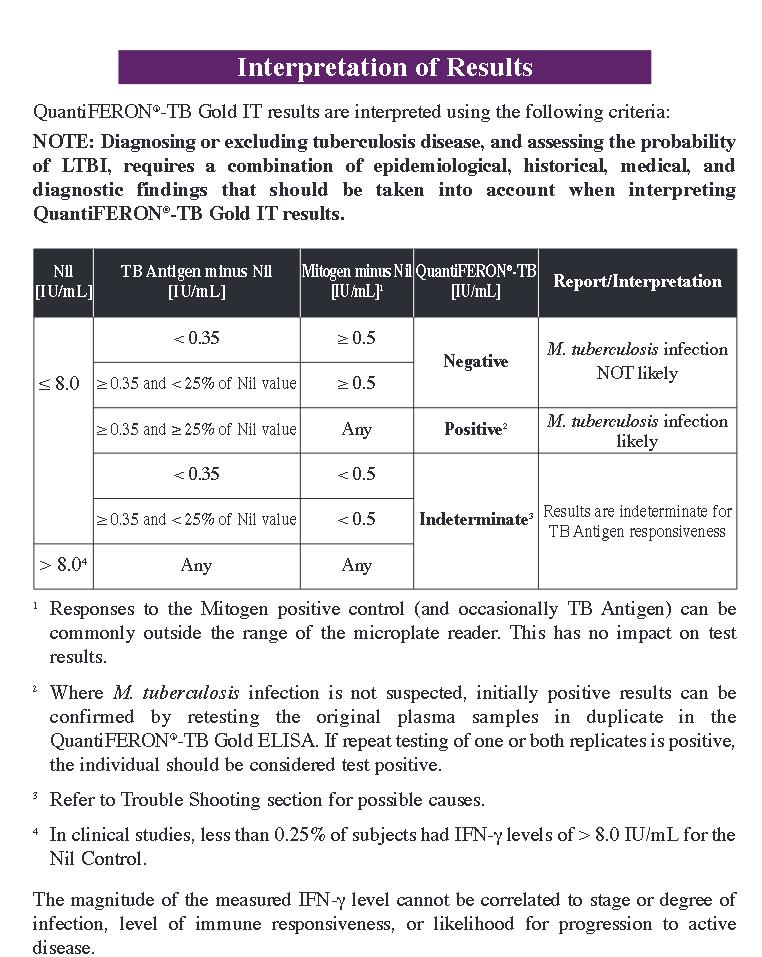 ) ) | 260 |
| 23 | Липаза (Триацилглицеролацилгидролаза) (Lipase) | 275 |
| 24 | Лактатдегидрогеназа (ЛДГ, L-лактат, НАД+Оксидоредуктаза) (Lactate Dehydrogenase, LDH) | 130 |
| 25 | ЛДГ-1 (Лактатдегидрогеназа-1, 1-й изофермент ЛДГ, альфа-гидроксибутиратдегидрогеназа) (Lactate Dehydrogenase, Isoforms 1, Lactic Acid Dehydrogenase, LDh2, Alpha-Hydroxybutyrate Dehydrogenase, Alpha-HBDH) | 210 |
| 34 | Холинэстераза (S-Псевдохолинэстераза, холинэстераза II, S-ХЭ, ацилхолингидролаза) (Cholinesterase, Pseudocholinesterase, PCHE) | 190 |
| 35 | Фосфатаза кислая (КФ) (Acid Phosphatase, ACP) | 160 |
| 36 | Фосфатаза щелочная (ЩФ) (Alkaline Phosphatase, ALP) | 180 |
| 117 | Витамин В12 (цианокобаламин, кобаламин) (Cobalamin) | 530 |
| 118 | Фолиевая кислота (Folic Acid) | 490 |
| 928 | 25-OH витамин D общий (25-OH Vitamin D Total, 25(OH)D, 25-Hydroxycalciferol) | 1 500 |
| 39 | Электролиты (Калий/Натрий/Хлор в сыворотке крови (К+/Potassium, Na+/Sodium, Сl-/Chloride, Serum) | 250 |
| 41 | Фосфор неорганический (P) (Phosphorus (P)) | 140 |
| 49 | Латентная (ненасыщенная) железосвязывающая способность сыворотки крови (ЛЖСС, НЖСС) (Unsaturated Iron Binding Capacity, UIBC) | 140 |
| 42 | Антистрептолизин-О (АСЛ-О, АСЛО) (Antistreptolysin-O, ASO) | 200 |
| 44 | Ревматоидный фактор (РФ) (Rheumatoid Factor, RF) | 200 |
| 840 | Церулоплазмин (Ceruloplasmin) | 530 |
| 841 | Гаптоглобин (Haptoglobin) | 530 |
| 1210 | Альфа-2-макроглобулин (Alpha-2-Macroglobulin, ?2-Macroglobulin, A2M) | 500 |
| 50 | Трансферрин (Сидерофилин) (Transferrin) | 385 |
| 51 | Ферритин (Ferritin) | 440 |
| 21 | Миоглобин (Myoglobin) | 530 |
| 1631 | Натрийуретического гормона (В-типа) N-концевой пропептид (NT-proBNP, N-Terminal Pro-brain Natriuretic Peptide, Pro-B-Type Natriuretic Peptide) | 2 200 |
| 157 | Тропонин-I (Troponin-I) | 495 |
| 838 | Углевод-дефицитный трансферрин (УДТ) (Carbohydrate-Deficient Trancferrin, CDT) | 2 350 |
| 14 | Билирубин прямой (Билирубин, конъюгированный, связанный)(Direct Bilirubin, DBIL, Conjugated Bilirubin) | 88 |
| 8 | Аланинаминотрасфераза (АлАТ, АЛТ, глутаминопировиноградная трансаминаза, ГПТ)(Alanine Aminotransferase, ALT, Serum Glutamic Pyruvic Transaminase, SGPT) | 88 |
| ROMA1 | Оценка риска рака яичников по алгоритму ROMA (Risk of ovarian Malignancy Algorithm, алгоритм расчета риска эпителиального рака яичников) (для женщин до менопаузы) (Risk of Ovarian Malignancy Algoritm, ROMA) (Before Menopause)) | 1 400 |
| ROMA2 | Оценка риска рака яичников по алгоритму ROMA (Risk of ovarian Malignancy Algorithm, алгоритм расчета риска эпителиального рака яичников) (для женщин после менопаузы) (Risk of Ovarian Malignancy Algoritm, ROMA) (After Menopause)) | 1 400 |
| 1198 | Белок S100 (S100 Protein) | 1 650 |
| 1595 | Растворимые рецепторы трансферрина | 1600 |
| 1604 | Витамин В1 (тиамин) | 2000 |
| 1609 | Витамин В2 (рибофлавин) | 2000 |
| 1610 | Витамин В3 (никотинамид) | 2000 |
| 1608 | Витамин В5 (пантотеновая кислота) | 2000 |
| 1605 | Витамин В6 (пиридоксальфосфат) | 2000 |
| 1611 | Витамин В7, Н (биотин) | 2000 |
| 1606 | Витамин С (аскорбиновая кислоиа) | 2000 |
| 1615 | Бета-каротин | 2000 |
| 1614 | Ретинил пальмитат | 2000 |
| 931 | Количественное определение витамина А. Сыворотка. Метод ВЭЖХ-МС/МС Сыворотка. Метод ВЭЖХ-МС/МС | 2000 |
| 932 | Количественное определение витамина Е. Сыворотка. Метод ВЭЖХ-МС/МС | 2000 |
| 877 | Количественное определение витамина К1. Сыворотка. Метод ВЭЖХ-МС/МС | 2000 |
| 1581 | Количественное определение Омега – 3 индекса. Цельная кровь. Метод ВЭЖХ-МС/МС | 3800 |
| 56 | Тиреотропный гормон (ТТГ, тиротропин) (Thyroid Stimulating Hormone, TSH) | 240 |
| 54 | Тироксин общий (T4 общий, тетрайодтиронин общий) (Total Thyroxine, TT4) | 300 |
| 55 | Тироксин свободный (Т4 свободный) (Free Thyroxine, FT4) | 240 |
| 52 | Трийодтиронин общий (Т3 общий) (Total Triiodthyronine, TT3) | 300 |
| 53 | Трийодтиронин свободный (Т3 свободный) (Free Triiodthyronine, FT3) | 240 |
| 197 | Тиреоглобулин (ТГ) (Thyroglobulin, TG) | 300 |
| 57 | Антитела к тиреоглобулину (АТ-ТГ) (Anti-Тhyroglobulin Autoantibodies, Thyroglobulin Antibodies, Tg Autoantibodies, TgAb, Anti-Tg Ab, ATG) | 500 |
| 58 | Антитела к тиреоидной пероксидазе (АТ-ТПО, микросомальные антитела) (Аnti-Тhyroid Рeroxidase Аutoantibodies, Antimicrosomal Antibodies, TPO Antibodies, TPOAb, Anti-TPO) | 300 |
| 199 | Антитела к рецепторам ТТГ (АТ к рецепторам тиреотропного гормона в сыворотке крови, Ат-рТТГ) (Thyroid-Stimulating Hormone Receptor Antibodies, TSH Receptor Antibodies, TSHRAbs, TSH binding inhibitor immunoglobulin, TBII) | 1 100 |
| 65 | Кортизол (Гидрокортизон) (Cortisol, Hydrocortisone) | 320 |
| 154 | 17-ОН-прогестерон (17-Hydroxyprogesterone, 17-OHP) | 300 |
| 59 | Фолликулостимулирующий гормон (ФСГ) (Follicle Stimulating Hormone, FSH) | 260 |
| 60 | Лютеинизирующий гормон (ЛГ) (Luteinizing Hormone, LH) | 250 |
| 61 | Пролактин (Prolactin) | 250 |
| 62 | Эстрадиол (Э2) (Estradiol, E2) | 330 |
| 63 | Прогестерон (Progesterone) | 400 |
| 66 | Хорионический гонадотропин человека (ХГЧ, бета-ХГЧ, ?-ХГЧ) (Human Chorionic Gonadotropin, HCG) | 330 |
| 189 | Свободный ?-ХГЧ (свободная ?-субъединица хорионического гонадотропина человека) (Free Human Chorionic Gonadotropin, Free HCG) | 400 |
| 172 | Инсулин (Insulin) | 380 |
| 148 | С-пептид (C-Peptide) | 400 |
| 99 | Соматотропный гормон (соматотропин, СТГ) (Growth Hormone, GH) | 450 |
| 174 | Соматомедин С (Инсулиноподобный фактор 1) (Somatomedin C, Insulin-like Growth Factor 1, IGF-1) | 600 |
| 196 | Тироксинсвязывающая способность (поглощение тиреоидных гормонов; индекс связывания тироксина; индекс свободного тироксина) (Thyroid Uptake, T-Uptake, Thyroxine-Binding Capacity,TBC, Thyroxine-Binding Index, TBI, free T4Index, fT4I) | 470 |
| 100 | Адренокортикотропный гормон (АКТГ, кортикотропин) (Adrenocorticotropic Hormone, ACTH) | 400 |
| 178 | Свободный кортизол в моче (Free Сortisol, Free Hydrocortisone, Urine) | 610 |
| 1508 | Кортизол, слюна (Cortisol, Saliva) | 530 |
| 101 | Дегидроэпиандростерон-сульфат (ДЭА-S04, ДГЭА) (Dehydroepiandrosterone Sulfate, DHEA-S) | 380 |
| 195 | Андростендион (Androstenedione) | 900 |
| 156 | 17-кетостероиды (17-КС) в моче (17-Ketosteroids, Urine) | 690 |
| 205 | Альдостерон (Aldosterone) | 400 |
| 102 | Паратиреоидный гормон (Паратгормон, паратирин, ПТГ) (Parathyroid Hormone, PTH) | 500 |
| 64 | Тестостерон (Testosterone) | 300 |
| 169 | Свободный тестостерон (Free Testosterone) | 600 |
| 168 | Дигидротестостерон (ДГТ) (Dihуdrotestosterone, DHT) | 990 |
| 170 | Андростендиол глюкуронид (Андростандиол глюкуронид) (Androstanediol Glucuronide, 3?-Androstanediol Glucuronid, 3?-diol G) | 600 |
| 101 | Дегидроэпиандростерон-сульфат (ДЭА-S04, ДГЭА) (Dehydroepiandrosterone Sulfate, DHEA-S) | 380 |
| 149 | Глобулин, связывающий половые гормоны (ГСПГ) (Sex Hormone-Binding Globulin, SHBG) | 400 |
| 1144 | Антимюллеров гормон (АМГ) (Anti-Mullerian Hormone, AMH, Mullerian Inhibiting Substance, MIS) | 1 000 |
| 1145 | Ингибин В (Inhibin B) | 1 000 |
| 207 | Плацентарный лактоген (Хорионический соматомаммотропин) (Placental Lactogen, PL, Human Placental Lactogen, hPL, Chorionic Somatomammotropin, CS, Human Chorionic Somatomammotropin, hCS) | 580 |
| 161 | Ассоциированный с беременностью протеин-А плазмы (Pregnancy-Associated Plasma Protein-A, PAPP-A) | 450 |
| 134 | Свободный эстриол (Estriol Free, Е3) | 420 |
| PRS1 | Пренатальный скрининг трисомий: I триместр (PRISСA-1) (Maternal Screen, First Trimester; Prenatal Screening I; PRISСA I (Prenatal Risk Calculation)) | 800 |
| PRS2 | Пренатальный скрининг трисомий: II триместр (PRISСA-2) (Maternal Screen, Second Trimester; Prenatal Screening II; PRISCA II (Prenatal Risk Calculation)) | 850 |
| ASTR1 | Биохимический скрининг 1-го триместра беременности для программы Астрайя (First-Trimester Biochemical Markers (Astraia)) | 3 550 |
| 173 | Проинсулин (Proinsulin) | 690 |
| 11HOMA | Оценка инсулинорезистентности: глюкоза (натощак), инсулин (натощак), расчет индекса HOMA-IR (Insulin Resistance: Fasting Glucose/Insulin, Homeostasis Model Assessment of Insulin Resistance, HOMA-IR) | 570 |
| КАТЕПЛ | Катехоламины (адреналин, норадреналин, дофамин) в плазме крови – КАТЕПЛ (Catecholamines: Epinephrine/Adrenaline, Norepinephrine/Noradrenaline, Dopamine, Plasma) | 1 800 |
| 950 | Метаболиты катехоламинов и серотонина: ванилилминдалевая кислота (ВМК), гомованилиновая кислота (ГВК), 5-оксииндолуксусная кислота (5-ОИУК) (Catecholamines and Serotonin Metabolites, 24 Hours-Urine: Vanillylmandelic Acid, VМА, Homovanillic Acid, НVА, 5-Hydroxyindoleacetic Acid, 5-НIАА) | 1 900 |
| 1166 | Метанефрины (фракции) в суточной моче: метанефрин, норметанефрин (Metanephrines, Fractinated, 24 Hours-Urine – Metanephrine, Normetanephrine) | 1 680 |
| 152 | Катехоламины (адреналин, норадреналин, дофамин) в моче (Catecholamines: Epinephrine/Adrenaline, Norepinephrine/Noradrenaline, Dopamine, Urine) | 1 800 |
| 1270 | Гистамин в плазме крови (Histamine, Plasma) | 2 300 |
| 1159 | Нефрины в плазме крови (Nephrines, Plasma) | 1 600 |
| 206 | Ренин (Ренин плазмы крови, прямое определение) (Direct Renin, Plasma) | 690 |
| 175 | Лептин (Leptin) | 700 |
| 222 | Эритропоэтин (Erythropoetin) | 650 |
| ОБС82 | Оценка андрогенного статуса (Дегидроэпиандростерон-сульфат (ДЭА-S04), Тестостерон, Глобулин, связывающий половые гормоны (ГСПГ), 17-ОН прогестерон (17-ОП), Свободный тестостерон (Free Testosterone)) | 570 |
| 993 | Серотонин в сыворотке крови (Serotonin, Serum) | 1 750 |
| ГАСТР | Гастропанель (GastroPanel) | 2 500 |
| 88 | Фенобарбитал (Люминал)(Phenobarbitalum) | 2 650 |
| 1353 | Такролимус (Адваграф, Програф, Протопик, Такросель)(FK506, Advagraf, Prograf, Protopic, Tacrosel) | 1 500 |
| 917 | Ламотриджин (Lamotrigine) | 3 300 |
| 1271 | Леветирацетам (Levetiracetam, Keppra) | 3 300 |
| 198 | Антитела к микросомальной фракции тиреоцитов (АТ к микросомальному антигену тиреоцитов, АТ-МАГ, АМАТ, тиреоидные антимикросомальные антитела) (Anti-Thyroid Microsomal Antibodies) | 470 |
| 116 | Анализ мочи общий (Анализ мочи общий с микроскопией осадка) (Complete Urinalysis, Microscopic Examination) | 220 |
| 272 | Исследование мочи по методу Нечипоренко (Nechiporenko’s Urine Test) | 180 |
| 95110 | Альбумин/креатинин-соотношение в разовой порции мочи (Отношение альбумина к креатинину в разовой порции мочи) (Urine Albumin Creatinine Ratio, UACR) | 650 |
| 109 | Глюкоза, моча (Glucose, Urine) | 110 |
| 110 | Креатинин, моча (Creatinine, Urine) | 120 |
| 111 | Мочевина, моча (Urea, Urine) | 120 |
| 112 | Мочевая кислота, моча (Uric Аcid, Urine) | 175 |
| 113 | Кальций (Ca), моча (Calcium (Ca), Urine) | 175 |
| 108 | Амилаза в моче суточной или порционной за измеренное время (Альфа-амилаза, диастаза мочи) (Amylase, 24-Hour or Timed Urine) | 150 |
| 401 | Кальций мочи, качественный тест (проба Сулковича) (Sulkowitch Urine Calcium Test) | 145 |
| 95 | Альбумин, моча (Albumin, Urine) | 480 |
| 96 | Проба Реберга (Клиренс эндогенного креатинина, скорость клубочковой фильтрации) (Glomerular Filtration Rate, GFR) | 100 |
| 110113 | Кальций-креатининовое соотношение в разовой порции мочи (Calcium-Creatinine Ratio, Random Urine) | 230 |
| 97 | Общий белок, моча (Protein Total, Urine) | 145 |
| 114 | Калий (K), Натрий (Na) (Potasium (K), Sodium (Na)) | 120 |
| 115 | Фосфор (P), моча (Phosphorus (P), Urine) | 200 |
| 1458 | Оксалаты в моче (Оxalates, Urine) | 1 160 |
| ЛМС | Наркотики и психотропные вещества ? скрининг (комплексный анализ мочи на опиаты, амфетамин, метамфетамин, кокаин, каннабиноиды и их метаболиты) (Drugs and Psychotropic Substances Screening: Opiates, Amphetamines, Methamphetamine, Cocaine, Cannabinoids, Cannabinoid Metabolites, Urine) | 2 600 |
| 902 | Каннабиноиды (марихуана) в моче (Cannabinoids (Marijuana), Urine)* | 1 000 |
| 925 | Опиаты (морфин/героин) в моче (Opiates (Morphine/Heroin), Urine)* | 1 000 |
| 898 | Барбитураты в моче (Barbiturates, Urine)* | 1 000 |
| 9950 | «Вредные привычки» (Анализ мочи на никотин, психотропные и наркотические вещества, психоактивные лекарственные препараты (никотин; психотропные и наркотические вещества, психоактивные лекарственные препараты) (Pernicious Habits: Nicotine, Drugs, Psychostimulants and Psychotropic Substances, Urine)* | 2 750 |
| 1265 | Камни почечные, анализ (Kidney Stone Analysis) | 3 150 |
| 73 | HBs-антиген вируса гепатита В (HBs-антиген, поверхностный антиген вируса гепатита B, «австралийский» антиген), качественный тест (HBsAg, Hepatitis В Surface Antigen, Qualitative) | 300 |
| 79 | Антитела классов IgM и IgG к вирусу гепатита С, суммарно (Anti-HCV Total (IgG + IgM))* | 250 |
| 122 | Антитела класса IgG к вирусу простого герпеса 1 и 2 типов (Anti-HSV-1, 2 IgG) | 350 |
| 4HSVIA | Антитела классов IgМ и IgG, определение авидности к вирусу простого герпеса 1 и 2 типов (Anti-HSV-1, 2 IgM, IgG, Avidity) | 400 |
| 267 | Антитела класса IgG к вирусу клещевого энцефалита (Anti-Tick-borne Encephalitis Virus (TBEV) IgG) | 360 |
| 268 | Антитела класса IgM к вирусу клещевого энцефалита (Anti-Tick-borne Encephalitis Virus (TBEV) IgM) | 360 |
| 2CMVIA | Антитела классов IgM и IgG к цитомегаловирусу, определение авидности (Anti-CMV IgM, IgG, Avidity) | 400 |
| 242 | Антитела класса IgA к аденовирусу (Аnti-Adenovirus IgA) | 590 |
| 241 | Антитела класса IgG к аденовирусу (Аnti-Adenovirus IgG) | 590 |
| 243 | Aнтитела класса IgG к Borrelia burgdorferi (Anti-Borrelia burgdorferi IgG) | 470 |
| 68 | Антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo) | 300 |
| 328СB | Вирус гепатита А, определение РНК (HAV-RNA) в сыворотке крови | 300 |
| 78 | Сифилис (анти-Tr. pallidum IgG/IgM) (антитела к антигенам Treponema pallidum суммарные, IgG и IgM, ИФА(EIA), Syphilis TP EIA) pallidum IgG/IgM) (антитела к антигенам Treponema pallidum суммарные, IgG и IgM, ИФА(EIA), Syphilis TP EIA) | 260 |
| 455 | Микроскопическое (бактериоскопическое) исследование мазка, окрашенного по Граму (Gram Stain. Bacterioscopic examination of different smears (vaginal, cervical, urethral, sputum, wound, etc) | 180 |
| 244 | Aнтитела класса IgM к Borrelia burgdorferi (Anti-Borrelia burgdorferi IgM) | 360 |
| 1190 | Aнтитела класса IgG к Borrelia burgdorferi, выявляемые методом иммуноблоттинга (Anti-Borrelia burgdorferi IgG, Immunoblot ) | 1 790 |
| 1191 | Aнтитела класса IgM к Borrelia burgdorferi, выявляемые методом Вестерн-блота (Anti-Borrelia burgdorferi IgM, Western Blot (WB)) | 1 790 |
| 256 | Антитела класса IgG к вирусу ветряной оспы и опоясывающего лишая (Anti-Varicella-Zoster Virus IgG, Anti-VZV IgG) | 580 |
| 257 | Антитела класса IgM к вирусу ветряной оспы и опоясывающего лишая (Anti-Varicella-Zoster Virus IgM, Anti-VZV IgM) | 650 |
| 74 | HBе-антиген вируса гепатита В (Hepatitis Be Antigen, HBeAg) | 300 |
| 75 | Антитела классов IgM и IgG к HB-core антигену вируса гепатита B, суммарно (Anti-HBc IgM, IgG, Antibodies to Hepatitis B Core Antigen; HBcAb, Total, HBV Core Total Antibodies (IgG + IgM)) | 300 |
| 76 | Антитела класса IgM к HB-core антигену вируса гепатита B (Anti-HBc IgM Antibodies to Hepatitis B Core Antigen; HBV Core Antibodies IgM) | 400 |
| 77 | Антитела к HBе-антигену вируса гепатита В (Anti-HBe, HBeAb) | 390 |
| 87 | HBs-антиген вируса гепатита В (HBs-антиген, поверхностный антиген вируса гепатита B, «австралийский» антиген), количественный тест (HBsAg, Hepatitis В Surface Antigen, Quantitative) | 1 100 |
| 2447 | Интерлейкин-28В (ИЛ-28В), генотипирование (исследование генетических маркеров, определяющих эффективность лечения хронического гепатита С интерфероном и рибавирином) (Interleukin 28 Beta IL28B, Genotyping (Study of Genetic Markers Determining Effectiveness of Treatment of Chronic Hepatitis C in Interferon and Ribavirin)) | 760 |
| 1170 | Антитела класса IgM к антигенам вируса гепатита С (Anti-HCV IgM) | 300 |
| 1171 | Антитела класса IgG к антигенам core, NS3, NS4, NS5 вируса гепатита С (Anti-HCV core, NS3, NS4, NS5 IgG) | 320 |
| 1ГЕП | Комплекс маркеров гепатитов В и C (№№ тестов: 73, 78, 75, 76, 74, 77, 79, 1170) (Markers of Hepatitis B, C ) | 2 800 |
| 1268 | Антитела класса IgM к вирусу гепатита D (Аnti-HDV IgM) | 720 |
| 1172 | Антитела к антигенам вируса гепатита D, суммарно (Аnti-HDV Total) | 300 |
| 227 | Антитела класса IgM к вирусу гепатита E (Anti-HEV IgM) | 650 |
| 228 | Антитела класса IgG к вирусу гепатита E (Anti-HEV IgG) | 650 |
| 1223 | Антитела класса IgG к вирусу простого герпеса 2 типа (Anti-HSV-2 IgG) | 726 |
| 123 | Антитела класса IgМ к вирусу простого герпеса 1 и 2 типов (Anti-HSV-1, 2 IgМ) | 342 |
| 276 | Антитела класса IgG к герпесвирусу человека 6 типа (Anti-HHV-6 IgG) | 500 |
| 277 | Антитела класса IgG к герпесвирусу человека 8 типа (Anti-HHV-8 IgG) | 580 |
| 229 | Анти-Эхинококк-IgG (антитела класса IgG к антигенам эхинококка, anti-E. granulosus) granulosus) | 660 |
| 341моч | Микобактерии туберкулеза, определение ДНК (Mycobacterium tuberculosis, DNA) в моче | 210 |
| 221 | Антитела класса IgM к Treponema pallidum (anti-Treponema pallidum IgM) | 795 |
| 352уро | Герпес-вирус человека 6 типа, определение ДНК (HHV-6, DNA) в соскобе эпителиальных клеток урогенитального тракта | 210 |
| 396уро | Бактероиды, определение ДНК (Bacteroides spp., DNA) в соскобе эпителиальных клеток урогенитального тракта | 190 |
| 1204 | Антитела к циклическому цитруллинированному пептиду (АЦЦП) (Anti-Сyclic Citrullinated Peptide, anti-CCP) | 460 |
| 1332 | Антитела класса IgG к модицифированному цитруллинированному виментину (анти-MЦВ) (Anti-Mutated Citrullinated Vimentin Antibodies, Anti-MCV, Anti-Modified Citrullinated Vimentin Antibodies, Anti-Sa Antibodies, IgG) | 1 250 |
| 71 | Антитела класса IgG к вирусу гепатита А (Anti-HAV IgG) | 630 |
| 72 | Антитела класса IgM к вирусу гепатита А (Anti-HAV IgM) | 440 |
| 1143 | Антитела класса IgG к антигенам вируса гепатита C, выявляемые методом иммуноблоттинга (Anti-HCV IgG, Immunoblot) | 4 000 |
| 93 | Группа крови (Blood Group, АВ0) | 160 |
| 94 | Резус-принадлежность (резус-фактор) (Rh-factor, Rh) | 180 |
| 1512BILE | Желчные кислоты (Bile Acids) | 2 290 |
| 1222 | Антитела класса IgG к вирусу простого герпеса 1 типа (Anti-HSV-1 IgG) | 560 |
| 1TORCH | Комплекс исследований на TORCH-инфекции IgG и IgM, определение авидности (ToRCH-Infection IgG, IgM, Avidity) | 3 000 |
| 2TORCH | Комплекс исследований на TORCH-инфекции IgG и IgM, без определения авидности (ToRCH-Infection IgG, IgM, without Avidity) | 2 000 |
| 855 | Антитела класса IgG к дифтерийному анатоксину (Anti-Diphtheria Toxoid IgG) | 750 |
| 254 | Aнтитела класса IgG к Candida albicans (Anti-Candida albicans IgG ) | 300 |
| 6617 | Плесень Candida albicans, IgG (M5) (M5 Candida albicans, IgG ) | 350 |
| 267 | Антитела класса IgG к вирусу клещевого энцефалита (Anti-Tick-borne Encephalitis Virus (TBEV) IgG) | 440 |
| 268 | Антитела класса IgM к вирусу клещевого энцефалита (Anti-Tick-borne Encephalitis Virus (TBEV) IgM) | 440 |
| 247 | Aнтитела класса IgA к Bordetella pertussis (Anti-Bordetella pertussis IgA ) | 600 |
| 245 | Aнтитела класса IgG к Bordetella pertussis (Anti-Bordetella pertussis IgG) | 600 |
| 246 | Aнтитела класса IgM к Bordetella pertussis (Anti-Bordetella pertussis IgM) | 600 |
| 1334 | Молекулярно-генетическое исследование HLA-B27 (Molecular Genetic Testing HLA-B27) | 900 |
| 808 | Кристаллы в мазке синовиальной жидкости (моноурат натрия, пирофосфат кальция) (Synovial Fluid Smear, Crystals) | 1 300 |
| 1333 | Ревматоидный фактор (РФ), выявляемый методом турбидиметрии (Rheumatoid Factor, RF, Тurbidimetry) | 940 |
| 956 | Антитела класса IgG к кератину (Антикератиновые антитела, АКА, Антифилаггриновые антитела, АФА) (Anti-Кeratin Аntibodies, AKA, Anti-Filaggrin Аntibodies, AFA, IgG) | 1 600 |
| 2500 | Антитела класса IgG к вирусу кори (Аnti-Measles IgG) | 700 |
| 251 | Антитела класса IgМ к вирусу кори (Аnti-Measles IgM) | 630 |
| 84 | Антитела класса IgG к вирусу краснухи (Аnti-Rubella IgG) | 320 |
| 3RUBIA | Антитела класса IgM и IgG к вирусу краснухи, определение авидности (Аnti-Rubella IgM, IgG, Avidity) | 460 |
| 179/80 | Антитела классов IgМ и IgG к Mycoplasma hominis (Аnti-Mycoplasma hominis IgМ, IgG) | 850 |
| 179 | Антитела класса IgМ к Mycoplasma hominis (Аnti-Mycoplasma hominis IgМ) | 850 |
| 180 | Антитела класса IgG к Mycoplasma hominis (Аnti-Mycoplasma hominis IgG) | 400 |
| 181 | Aнтитела класса IgM к Mycoplasma pneumoniae (Anti-Mycoplasma pneumoniae IgM) | 850 |
| 182 | Aнтитела класса IgG к Mycoplasma pneumoniae (Anti-Mycoplasma pneumoniae IgG) | 600 |
| 1178 | Антитела класса IgA к Mycoplasma hominis (Аnti-Mycoplasma hominis IgA) | 400 |
| 1178/180 | Антитела классов IgG и IgA к Mycoplasma hominis (Аnti-Mycoplasma hominis IgG, IgA) | 700 |
| 252 | Aнтитела класса IgG к вирусу эпидемического паротита (Anti-Mumps IgG) | 550 |
| 253 | Aнтитела класса IgM к вирусу эпидемического паротита (Anti-Mumps IgM) | 550 |
| 248 | Aнтитела класса IgG к респираторно-синцитиальному вирусу (Anti-Respiratory Syncytial Virus (RSV) IgG) | 550 |
| 249 | Aнтитела класса IgM к респираторно-синцитиальному вирусу (Anti-Respiratory Syncytial Virus (RSV) IgM) | 550 |
| 69 | Сифилис RPR – антикардиолипиновый тест (Syphilis RPR (Rapid Plasma Reagins), Аnticardiolipin Тest) | 200 |
| 70 | Aнтитела классов IgM и IgG к Treponema pallidum, суммарно (Anti-Treponema pallidum IgM, IgG, Total) | 200 |
| 1206 | Aнтитела класса IgM к Treponema pallidum, выявляемые методом иммуноблоттинга (Anti-Treponema pallidum IgM, Immunoblot ) | 2 000 |
| 1205 | Aнтитела класса IgG к Treponema pallidum, выявляемые методом иммуноблоттинга (Anti-Treponema pallidum IgG, Immunoblot ) | 2 000 |
| 1169 | Реакция Вассермана (RW) на сифилис (комплекс серологических реакций на сифилис) (Wassermann Reaction (RW), Wassermann Test) | 630 |
| 876 | Антитела класса IgG к столбнячному анатоксину (Аnti-Tetanus toxoid IgG) | 750 |
| 1208 | Антитела класса IgG к Т-лимфотропному вирусу человека типа 1 и 2 типов (Anti-HTLV-1, 2 IgG ) | 500 |
| 80 | Антитела класса IgG к Тoxoplasma gondii (Аnti-Toxoplasma gondii IgG) | 320 |
| 81 | Антитела класса IgМ к Тoxoplasma gondii (Аnti-Toxoplasma gondii IgМ) | 320 |
| 1TOXOIA | Антитела классов IgM и IgG к Тoxoplasma gondii, определение авидности (Аnti-Toxoplasma gondii IgM, IgG, Avidity) | 500 |
| 261 | Антитела класса IgG к Trichomonas vaginalis (Аnti-Trichomonas vaginalis IgG) | 320 |
| 1266 | Антитела классов IgM, IgA, IgG к Mycobacterium tuberculosis, суммарно (Аnti-Mycobacterium tuberculosis IgM, IgA, IgG, Тotal) | 1 200 |
| 264 | Антитела класса IgG к Ureaplasma urealyticum (Аnti-Ureaplasma urealyticum IgG) | 320 |
| 1151 | Антитела класса IgA к Ureaplasma urealyticum (Аnti-Ureaplasma urealyticum IgA) | 850 |
| 133 | Aнтитела класса IgG к Helicobacter рylori (Anti-Helicobacter pylori IgG) | 350 |
| 177 | Aнтитела класса IgA к Helicobacter рylori (Anti-Helicobacter pylori IgA) | 550 |
| 258 | Aнтитела класса IgG к Helicobacter pylori, выявляемые методом иммуноблоттинга (Anti-Helicobacter pylori IgG, Immunoblot) | 2 200 |
| 259 | Aнтитела класса IgA к Helicobacter pylori, выявляемые методом иммуноблоттинга (Anti-Helicobacter pylori IgA, Immunoblot) | 2 200 |
| 105 | Aнтитела класса IgA к Chlamydia trachomatis (Anti-Chlamydia trachomatis IgA) | 300 |
| 106 | Aнтитела класса IgG к Chlamydia trachomatis (Anti-Chlamydia trachomatis IgG) | 300 |
| 105/6 | Aнтитела классов IgA и IgG к Chlamydia trachomatis, раздельно (Anti-Chlamydia trachomatis IgA, IgG) | 300 |
| 188 | Aнтитела класса IgM к Chlamydia trachomatis (Anti-Chlamydia trachomatis IgM) | 450 |
| 183 | Aнтитела класса IgA к Chlamydophila pneumoniae (Anti-Chlamydophila pneumoniae IgA) | 500 |
| 1495 | Антитела класса IgG к белку теплового шока (БТШ) Chlamydia trachomatis (Anti-cHSP60 IgG) | 650 |
| 82 | Aнтитела класса IgG к цитомегаловирусу (Anti-CMV IgG) | 300 |
| 83 | Aнтитела класса IgM к цитомегаловирусу (Anti-CMV IgM) | 300 |
| 186 | Антитела класса IgМ к капсидному антигену вируса Эпштейна-Барр (Аnti-EBV Viral Capsid Antigens (VCA) IgМ ) | 400 |
| 187 | Антитела класса IgG к ядерному антигену вируса Эпштейна-Барр (Аnti-EBV Nuclear Antigen (EBNA) IgG ) | 300 |
| 255 | Антитела класса IgG к раннему антигену вируса Эпштейна-Барр (Аnti-EBV Early Antigen (EA) IgG ) | 300 |
| 275 | Антитела класса IgG к капсидному антигену вируса Эпштейна-Барр (Аnti-EBV Viral Capsid Antigens (VCA) IgG ) | 400 |
| 1180/81 | Антитела класса IgG к нуклеарному и предраннему антигену вируса Эпштейна-Барр (Epstein-Barr Virus Nuclear Antigen IgG, EBNA IgG) | 400 |
| 1195 | Вирус Эпштейна-Барр (ВЭБ), определение антител класса IgG методом иммуноблоттинга (EBV IgG, Immunoblot) | 970 |
| 1196 | Вирус Эпштейна-Барр (ВЭБ), определение антител класса IgМ методом иммуноблоттинга (EBV IgM, Immunoblot) | 970 |
| 235 | Антитела класса IgG к антигенам дизентерийной амебы (Anti-Entamoeba histolytica IgG) | 530 |
| 237 | Антитела класса IgG к антигенам аскарид (Anti-Ascaris lumbricoides IgG) | 260 |
| 234 | Антитела классов IgM, IgG, IgA к антигенам лямблий, суммарно (Аnti-Giardia lamblia IgM, IgG, IgA, Total) | 260 |
| 230 | Антитела класса IgG к антигенам описторхиса (Anti-Opisthorchis felineus IgG) | 320 |
| 1372 | Антитела класса IgG к антигенам стронгилоидоза (Anti-Strongyloides stercoralis IgG) | 920 |
| 232 | Антитела класса IgG к антигенам токсокар (Anti-Toxocara IgG) | 260 |
| 233 | Антитела класса IgG к антигенам трихинелл (Аnti-Trichinella IgG) | 410 |
| 1184 | Антитела классов IgM, IgG и циркулирующие иммунные комплексы (ЦИК) к антигенам описторхиса (Anti-Opisthorchis felineus IgM, IgG, Circulating Immune Complexes (CIC)) | 350 |
| 1185 | Антитела классов IgM и IgG к антигенам трихинелл (Anti-Trichinella IgM, IgG) | 720 |
| 1186 | Комплекс «Паразиты» (описторхис, эхинококки, токсокары, трихинеллы) (Parasites: Opisthorchis, Echinococcosis, Toxocara, Trichinella) | 350 |
| 210 | Интерлейкин-1? (ИЛ-1?) (Interleukin 1 Beta, IL-1) | 1 700 |
| 972 | Антитела классов IgA и IgG к эндомизию (антиэндомизийные антитела, АЭМА), суммарно (Anti-Еndomysial Аntibodies, Anti-EMA, IgA, IgG, Total) | 900 |
| 810 | Антитела класса IgА к эндомизию (антиэндомизийные антитела, АЭМА) (Anti-Еndomysial Аntibodies, Anti-EMA, IgА) | 940 |
| 805 | Антитела классов IgA, IgG, IgM к париетальным клеткам желудка (АПКЖ), суммарно (Gastric Parietal Cell Antibodies, GPA, Anti-Рarietal cell antibodies, APCA, IgA, IgG, IgM, Total) | 940 |
| 971 | Антитела классов IgA и IgG к ретикулину, суммарно (Anti-Reticulin Antibodies, ARA, IgA, IgG, Total) | 900 |
| 270 | Антитела класса IgG к деамидированным пептидам глиадина (Anti-Deaminated Gliadin Peptide, Anti-DGP, IgG) | 530 |
| 271 | Антитела класса IgА к деамидированным пептидам глиадина (Anti-Deaminated Gliadin Peptide, Anti-DGP, IgA) | 530 |
| 1282 | Антитела класса IgА к тканевой трансглютаминазе (Anti-Tissue Transglutaminase Antibodies, Anti-tTG, tTGA, IgA) | 750 |
| 1283 | Антитела класса IgG к тканевой трансглютаминазе (Anti-Tissue Transglutaminase Antibodies, Anti-tTG, tTGA, IgG) | 750 |
| 817 | Антитела класса IgG к внутреннему фактору Кастла (Anti-Intrinsic Factor, IFAb, Intrinsic Factor Antibodies, IgG) | 1 250 |
| 1335 | Антитела класса IgG к сахаромицетам (диагностика болезни Крона) (Anti-Sacchаromyces Cerevisiae Antibodies, ASCA, IgG ) | 940 |
| 1336 | Антитела класса IgА к сахаромицетам (диагностика болезни Крона) (Anti-Sacchаromyces Cerevisiae Antibodies, ASCA, IgA ) | 940 |
| 1337 | Антитела класса IgА к цитоплазме нейтрофилов (АНЦА) (Anti-Neutrophil Cytoplasmic Antibodies, ANCA, IgA) | 940 |
| 944 | Диагностика аутоиммунного панкреатита и других IgG4-ассоциированных заболеваний (Diagnosis of Autoimmune Pancreatitis and other IgG4-Related Diseases) | 1 400 |
| 4055 | Серодиагностика аутоиммунного гастрита и пернициозной анемии (АТ к париетальным клеткам желудка; АТ к внутреннему фактору Кастла) | 1 400 |
| 4056 | Серодиагностика болезни Крона и неспецифического язвенного колита (НЯК) (АНЦА/pANCA, cANCA, IgG; АНЦА/ANCA, IgA; ASCA, IgG, IgA) | 4 000 |
| 4057 | Целиакия, серологический скрининг (АТ к эндомизию, IgA; АТ к деамидированным пептидам глиадина, IgG; IgA общ. ) ) | 1 360 |
| 4058 | Целиакия, серологическая диагностика (АТ к эндомизию, IgA; АТ к тканевой трансглутаминазе, IgA, IgG; IgA общ.) | 2 000 |
| 1212 | Антитела классов IgG и IgA к тканевой трансглутаминазе (Anti-Tissue Transglutaminase, tTG, Anti-tTG, IgG, IgА, ) | 1 200 |
| 1584 | Антинейрональные антитела, IgG, метод непрямой иммунофлуоресценции | 2800 |
| 211 | Интерлейкин-6 (ИЛ-6) (Interleukin 6, IL-6) | 1 700 |
| 212 | Интерлейкин-8 (ИЛ-8) (Interleukin 8, IL-8) | 1 700 |
| 213 | Интерлейкин-10 (ИЛ-10) (Interleukin 10, IL-10) | 1 700 |
| 214 | Фактор некроза опухоли-? (ФНО-?) (Tumor Necrosis Factor Alpha, TNF-?, Cachectin) | 1 700 |
| 281 | РПГА с Shigella flexneri 6 (Shigella flexneri 6, IHA) | 360 |
| 282 | РПГА с Shigella sonnei (Shigella sonnei, IHA) | 360 |
| 285 | РПГА с Yersinia еnterocolitica серотипа О:9 (Yersinia enterocolitica O:9, IHA) | 360 |
| 283 | РПГА с сыпнотифозным диагностикумом риккетсий Провачека (Rickettsia prowazekii, IHA) | 360 |
| 309кр | Герпесвирус 1 и 2 типов, определение ДНК в венозной крови (HSV-1, 2 DNA, Blood)* | 250 |
| 309моч | Герпесвирус 1 и 2 типов, определение ДНК в моче (HSV-1, 2 DNA, Urine)* | 250 |
| 3090нос | Герпесвирус 1 и 2 типов, определение ДНК в соскобе эпителиальных клеток слизистой носа (HSV-1, 2 DNA, Scrape of Nasal Epithelial Cells)*, Герпесвирус 1 и 2 типов, определение ДНК в соскобе эпителиальных клеток ротоглотки (HSV-1, 2 DNA, Scrape of Faucial Epithelial Cells)* | 250 |
| 309сп | Герпесвирус 1 и 2 типов, определение ДНК в секрете простаты, эякуляте (HSV-1, 2 DNA, Prostatic Fluid, Semen)* | 250 |
| 352кр | Герпесвирус 6 типа, определение ДНК в венозной крови (HSV-6 DNA, Blood)* | 250 |
| 344уро | Кандида, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Candida albicans, DNA, Scrape of Urogenital Epithelial Cells)* | 450 |
| 3116 | Кандида (Candida albicans, Candida crusei, Candida glabrata), определение ДНК (Candida albicans, Candida crusei, Candida glabrata, DNA)* | 230 |
| 338СВ | Вирус краснухи, определение ДНК в сыворотке крови (Rubella Virus, DNA, Serum)* | 350 |
| 302моч | Микоплазма (Mycoplasma hominis), определение ДНК в моче (Mycoplasma hominis, DNA, Urine)* | 230 |
| 302сп | Микоплазма (Mycoplasma hominis), определение ДНК в секрете простаты, эякуляте (Mycoplasma hominis, DNA, Prostatic Fluid, Semen)* | 230 |
| 302уро | Микоплазма (Mycoplasma hominis), определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Mycoplasma hominis, DNA, Scrape of Urogenital Epithelial Cells)* | 230 |
| 308моч | Микоплазма (Mycoplasma genitalium), определение ДНК в моче (Mycoplasma genitalium, DNA, Urine)* | 230 |
| 308сп | Микоплазма (Mycoplasma genitalium), определение ДНК в секрете простаты, эякуляте (Mycoplasma genitalium, DNA, Prostatic Fluid, Semen)* | 230 |
| 308уро | Микоплазма (Mycoplasma genitalium), определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Mycoplasma genitalium, DNA, Scrape of Urogenital Epithelial Cells)* | 230 |
| 346отд | Бледная трепонема, определение ДНК в отделяемом (Treponema pallidum, DNA, Secretion)* | 300 |
| 346св | Бледная трепонема, определение ДНК в сыворотке крови (Treponema pallidum, DNA, Serum)* | 250 |
| 335св | Токсоплазма, определение ДНК в сыворотке крови (Toxoplasma gondii, DNA, Serum)* | 290 |
| 307уро | Трихомонада, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Trichomonas vaginalis, DNA, Scrape of Urogenital Epithelial Cells)* | 230 |
| 301сп | Хламидия (Chlamydia trachomatis), определение ДНК в секрете простаты, эякуляте (Chlamydia trachomatis, DNA, Prostatic Fluid, Semen)* | 230 |
| 301уро | Хламидия (Chlamydia trachomatis), определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Chlamydia trachomatis, DNA, Scrape of Urogenital Epithelial Cells)* | 230 |
| 310кр | Цитомегаловирус, определение ДНК в венозной крови (CMV DNA, Blood)* | 250 |
| 310моч | Цитомегаловирус, определение ДНК в моче (CMV DNA, Urine)* | 230 |
| 310сп | Цитомегаловирус, определение ДНК в секрете простаты, эякуляте (CMV DNA, Prostatic Fluid, Semen)* | 230 |
| 310уро | Цитомегаловирус, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (CMV DNA, Scrape of Urogenital Epithelial Cells)* | 230 |
| 351моч | Вирус Эпштейна-Барр, определение ДНК в моче (EBV DNA, Urine)* | 250 |
| 351сп | Вирус Эпштейна-Барр, определение ДНК в секрете простаты, эякуляте (EBV DNA, Prostatic Fluid, Semen)* | 250 |
| 351уро | Вирус Эпштейна-Барр, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (EBV DNA, Scrape of Urogenital Epithelial Cells)* | 250 |
| 377с-уро | Вирус папилломы человека высокого онкогенного риска, скрининг 14 типов: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 + КВМ, oпределение ДНК в соскобе эпителиальных клеток урогенитального тракта (HPV DNA, Scrape of Urogenital Epithelial Cells, 14 Types (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) Screening )* | 400 |
| 305уро | Гарднерелла, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Gardnerella vaginalis, DNA, Scrape of Urogenital Epithelial Cells)* | 230 |
| 351сп | Вирус Эпштейна-Барр, определение ДНК в секрете простаты, эякуляте (EBV DNA, Prostatic Fluid, Semen)* | 300 |
| 311с-уро | Вирус папилломы человека высокого онкогенного риска, скрининг 14 типов: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 + КВМ, oпределение ДНК в соскобе эпителиальных клеток урогенитального тракта (HPV DNA, Scrape of Urogenital Epithelial Cells, 14 Types (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) Screening )* | 550 |
| 312С-УРО | Вирус папилломы человека высокого онкогенного риска, oпределение ДНК 16 и 18 типов + КВМ в соскобе эпителиальных клеток урогенитального тракта (HPV DNA, Scrape of Urogenital Epithelial Cells, 2 Types (16, 18)) | 300 |
| 3090уро | Герпесвирус 1 и 2 типов, определение ДНК в соскобе эпителиальных клеток урогенитального тракта, типирование (HSV-1, 2 DNA, Scrape of Urogenital Epithelial Cells, Тyping)* | 370 |
| 309уро | Герпесвирус 1 и 2 типов, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (HSV-1, 2 DNA, Scrape of Urogenital Epithelial Cells)* | 200 |
| 391С-УРО | Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) 21 типа ( 6, 11, 16, 18, 26, 31, 33, 35, 39, 44, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82) + КВМ | 2 050 |
| 374С-УРО | Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV), 4 типа (6, 11, 16, 18 )+ КВМ в соскобе эпителиальных клеток урогенитального тракта | 500 |
| 313с-уро | Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) высокого онкогенного риска 14 типов (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) + КВМ в соскобе эпителиальных клеток урогенитального тракта | 800 |
| 309кр | Герпес-вирус человека 1 и 2 типа (вирус простого герпеса 1 и 2 типа), определение ДНК (Human herpesvirus 1, 2, Herpes simplex virus 1, 2 (HSV-1, HSV-2), DNA) в крови | 540 |
| 3112 | Боррелиоз, определение ДНК (Вorrelia burgdorferi, DNA)* | 350 |
| 328СВ | Вирус гепатита А, определение РНК в сыворотке крови (HAV RNA, Serum)* | 250 |
| 319СВ | Вирус гепатита B, определение ДНК в сыворотке крови, качественное (HBV DNA, Serum, Qualitative)* | 300 |
| 320СВ | Вирус гепатита B, определение ДНК в сыворотке крови, количественное (HBV DNA, Serum, Quantitative)* | 880 |
| 321СВ | Вирус гепатита С, определение РНК в сыворотке крови, качественное (HCV RNA, Serum, Qualitative)* | 500 |
| 350СВ | Вирус гепатита С, определение РНК в сыворотке крови методом ПЦР, количественное (HCV RNA, Serum, Quantitative, PCR)* | 1 800 |
| 325СВ | Вирус гепатита D, определение РНК в сыворотке крови (HDV RNA, Serum)* | 400 |
| 326СВ | Вирус гепатита G, определение РНК в сыворотке крови (HGV RNA, Serum)* | 500 |
| 309нос | Герпесвирус 1 и 2 типов, определение ДНК в соскобе эпителиальных клеток слизистой носа (HSV-1, 2 DNA, Scrape of Nasal Epithelial Cells)* | 150 |
| 309рот | Герпесвирус 1 и 2 типов, определение ДНК в соскобе эпителиальных клеток ротоглотки (HSV-1, 2 DNA, Scrape of Faucial Epithelial Cells)* | 150 |
| 309св | Герпесвирус 1 и 2 типов, определение ДНК в сыворотке крови (HSV-1, 2 DNA, Serum)* | 150 |
| 347мк | Микоплазма (Mycoplasma pneumoniae), определение ДНК в мокроте (Mycoplasma pneumoniae, DNA, Sputum)* | 270 |
| 347пл | Микоплазма (Mycoplasma pneumoniae), определение ДНК в плазме крови (Mycoplasma pneumoniae, DNA, Plasma)* | 270 |
| 347рот | Микоплазма (Mycoplasma pneumoniae), определение ДНК в соскобе эпителиальных клеток ротоглотки (Mycoplasma pneumoniae, DNA, Scrape of Faucial Epithelial Cells)* | 270 |
| 346моч | Бледная трепонема, определение ДНК в моче (Treponema pallidum, DNA, Urine)* | 210 |
| 346сп | Бледная трепонема, определение ДНК в секрете простаты, эякуляте (Treponema pallidum, DNA, Prostatic Fluid, Semen)* | 210 |
| 3090кр | Герпесвирус 1 и 2 типов, определение ДНК в венозной крови, типирование (HSV-1, 2 DNA, Blood, Тyping)* | 500 |
| 3090моч | Герпесвирус 1 и 2 типов, определение ДНК в моче, типирование (HSV-1, 2 DNA, Urine, Тyping)* | 370 |
| 3090рот | Герпесвирус 1 и 2 типов, определение ДНК в соскобе эпителиальных клеток ротоглотки, типирование (HSV-1, 2 DNA, Scrape of Faucial Epithelial Cells, Тyping)* | 370 |
| 3090св | Герпесвирус 1 и 2 типов, определение ДНК в сыворотке крови, типирование (HSV-1, 2 DNA, Serum, Тyping)* | 500 |
| 3090сп | Герпесвирус 1 и 2 типов, определение ДНК в секрете простаты, эякуляте, типирование (HSV-1, 2 DNA, Prostatic Fluid, Semen, Тyping)* | 370 |
| 352моч | Герпесвирус 6 типа, определение ДНК в моче (HSV-6 DNA, Urine)* | 210 |
| 352нос | Герпесвирус 6 типа, определение ДНК в соскобе эпителиальных клеток слизистой носа (HSV-6 DNA, Scrape of Nasal Epithelial Cells)* | 210 |
| 352рот | Герпесвирус 6 типа, определение ДНК в соскобе эпителиальных клеток ротоглотки (HSV-6 DNA, Scrape of Faucial Epithelial Cells)* | 210 |
| 352св | Герпесвирус 6 типа, определение ДНК в сыворотке крови (HSV-6 DNA, Serum)* | 210 |
| 352сп | Герпесвирус 6 типа, определение ДНК в секрете простаты, эякуляте (HSV-6 DNA, Prostatic Fluid, Semen)* | 210 |
| 344моч | Кандида, определение ДНК в моче (Candida albicans, DNA, Urine)* | 150 |
| 344рот | Кандида, определение ДНК в соскобе эпителиальных клеток ротоглотки (Candida albicans, DNA, Scrape of Faucial Epithelial Cells)* | 150 |
| 344сп | Кандида, определение ДНК в секрете простаты, эякуляте (Candida albicans, DNA, Prostatic Fluid, Semen)* | 150 |
| 305моч | Гарднерелла, определение ДНК в моче (Gardnerella vaginalis, DNA, Urine)* | 230 |
| 305сп | Гарднерелла, определение ДНК в секрете простаты, эякуляте (Gardnerella vaginalis, DNA, Prostatic Fluid, Semen)* | 230 |
| 3114нос | Листерии, определение ДНК в соскобе эпителиальных клеток слизистой носа (Listeria monocytogenes, DNA, Scrape of Nasal Epithelial Cells)* | 190 |
| 3114пл | Листерии, определение ДНК в плазме крови (Listeria monocytogenes, DNA, Plasma)* | 190 |
| 3114рот | Листерии, определение ДНК в соскобе эпителиальных клеток ротоглотки (Listeria monocytogenes, DNA, Scrape of Faucial Epithelial Cells)* | 190 |
| 348пл | Стрептококк, определение ДНК в плазме крови (Streptococcus spp. , DNA, Plasma)* , DNA, Plasma)* | 400 |
| 348рот | Стрептококк, определение ДНК в соскобе эпителиальных клеток ротоглотки (Streptococcus spp., DNA, Scrape of Faucial Epithelial Cells)* | 400 |
| 348слн | Стрептококк, определение ДНК в слюне (Streptococcus spp., DNA, Saliva)* | 400 |
| 345УРО | Лактобактерии, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Lactobаcillus spp., DNA, Scrape of Urogenital Epithelial Cells)* | 190 |
| 397УРО | Мобилункус, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Mobiluncus curtisii, DNA, Scrape of Urogenital Epithelial Cells) | 190 |
| 351кр | Вирус Эпштейна-Барр, определение ДНК в венозной крови (EBV DNA, Blood)* | 300 |
| 306моч | Гонококк, определение ДНК в моче (Neisseria gonorrhoeae, DNA, Urine)* | 210 |
| 311с-рот | Вирус папилломы человека высокого онкогенного риска, скрининг 14 типов: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 + КВМ, oпределение ДНК в соскобе эпителиальных клеток ротоглотки (HPV DNA, Scrape of Faucial Epithelial Cells, 14 Types (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) Screening )* | 500 |
| 399СУРО | Вирус папилломы человека низкого онкогенного риска, определение ДНК 3 типов: 6, 11, 44 + КВМ в соскобе эпителиальных клеток урогенитального тракта (HPV DNA, Scrape of Urogenital Epithelial Cells, 3 Types (6, 11, 44)) | 270 |
| 399-РОТ | Вирус папилломы человека низкого онкогенного риска, определение ДНК 3 типов: 6, 11, 44 в соскобе эпителиальных клеток ротоглотки (HPV DNA, Scrape of Faucial Epithelial Cells, 3 Types (6, 11, 44)) | 270 |
| 391-УРО | Вирус папилломы человека, oпределение ДНК 21 типа: 6, 11, 16, 18, 26, 31, 33, 35, 39, 44, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82 + КВМ в соскобе эпителиальных клеток урогенитального тракта (HPV DNA, Scrape of Urogenital Epithelial Cells, 21 Types (6, 11, 16, 18, 26, 31, 33, 35, 39, 44, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82)) | 2 000 |
| 307моч | Трихомонада, определение ДНК в моче (Trichomonas vaginalis, DNA, Urine)* | 210 |
| 307сп | Трихомонада, определение ДНК в секрете простаты, эякуляте (Trichomonas vaginalis, DNA, Prostatic Fluid, Semen)* | 210 |
| 341мк | Микобактерии туберкулеза, определение ДНК в мокроте (Mycobacterium tuberculosis, DNA, Sputum)* | 300 |
| 341св | Микобактерии туберкулеза, определение ДНК в сыворотке крови (Mycobacterium tuberculosis, DNA, Serum)* | 300 |
| 341сп | Микобактерии туберкулеза, определение ДНК в секрете простаты, эякуляте (Mycobacterium tuberculosis, DNA, Prostatic Fluid, Semen)* | 300 |
| 303моч | Уреаплазма (Ureaplasma urealyticum) (биовар Т-960), определение ДНК в моче (Ureaplasma urealyticum (T-960), DNA, Urine)* | 210 |
| 303сп | Уреаплазма (Ureaplasma urealyticum) (биовар Т-960), определение ДНК в секрете простаты, эякуляте (Ureaplasma urealyticum (T-960), DNA, Prostatic Fluid, Semen)* | 210 |
| 301моч | Хламидия (Chlamydia trachomatis), определение ДНК в моче (Chlamydia trachomatis, DNA, Urine)* | 210 |
| 349мк | Хламидия (Chlamydia pneumoniae), определение ДНК в мокроте (Chlamydophila pneumoniae, DNA, Sputum)* | 300 |
| 3113 | Коклюш (Bordetella pertussis), определение ДНК(Bordetella pertussis, DNA)* | 300 |
| 310нос | Цитомегаловирус, определение ДНК в соскобе эпителиальных клеток слизистой носа (CMV DNA, Scrape of Nasal Epithelial Cells)* | 230 |
| 310рот | Цитомегаловирус, определение ДНК в соскобе эпителиальных клеток ротоглотки (CMV DNA, Scrape of Faucial Epithelial Cells)* | 230 |
| 310св | Цитомегаловирус, определение ДНК в сыворотке крови (CMV DNA, Serum)* | 230 |
| 310слн | Цитомегаловирус, определение ДНК в слюне (CMV DNA, Saliva)* | 230 |
| 351моч | Вирус Эпштейна-Барр, определение ДНК в моче (EBV DNA, Urine)* | 300 |
| 351нос | Вирус Эпштейна-Барр, определение ДНК в соскобе эпителиальных клеток слизистой носа (EBV DNA, Scrape of Nasal Epithelial Cells)* | 300 |
| 351рот | Вирус Эпштейна-Барр, определение ДНК в соскобе эпителиальных клеток ротоглотки (EBV DNA, Scrape of Faucial Epithelial Cells)* | 300 |
| 351св | Вирус Эпштейна-Барр, определение ДНК в сыворотке крови (EBV DNA, Serum)* | 300 |
| 351уро | Вирус Эпштейна-Барр, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (EBV DNA, Scrape of Urogenital Epithelial Cells)* | 300 |
| 306рот | Гонококк, определение ДНК в соскобе эпителиальных клеток ротоглотки (Neisseria gonorrhoeae, DNA, Scrape of Faucial Epithelial Cells)* | 210 |
| 306сп | Гонококк, определение ДНК в секрете простаты, эякуляте (Neisseria gonorrhoeae, DNA, Prostatic Fluid, Semen)* | 210 |
| 306уро | Гонококк, определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Neisseria gonorrhoeae, DNA, Scrape of Urogenital Epithelial Cells)* | 210 |
| 303уро | Уреаплазма (Ureaplasma urealyticum) (биовар Т-960), определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Ureaplasma urealyticum (T-960), DNA, Scrape of Urogenital Epithelial Cells)* | 210 |
| 342МОЧ | Уреаплазма (Ureaplasma parvum), определение ДНК в моче (Ureaplasma parvum, DNA, Urine)* | 210 |
| 342сп | Уреаплазма (Ureaplasma рarvum), определение ДНК в секрете простаты, эякуляте (Ureaplasma parvum, DNA, Prostatic Fluid, Semen)* | 210 |
| 343сп | Уреаплазма (Ureaplasma urealyticum + Ureaplasma рarvum), определение ДНК в секрете простаты, эякуляте (Ureaplasma urealyticum + Ureaplasma рarvum, DNA, Prostatic Fluid, Semen)* | 230 |
| 343моч | Уреаплазма (Ureaplasma urealyticum + Ureaplasma рarvum), определение ДНК в моче (Ureaplasma urealyticum + Ureaplasma рarvum, DNA, Urine)* | 210 |
| 343уро | Уреаплазма (Ureaplasma urealyticum + Ureaplasma рarvum), определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Ureaplasma urealyticum + Ureaplasma рarvum, DNA, Scrape of Urogenital Epithelial Cells)* | 230 |
| 345сп | Уреаплазма (Ureaplasma urealyticum + Ureaplasma рarvum), определение ДНК в секрете простаты, эякуляте (Ureaplasma urealyticum + Ureaplasma рarvum, DNA, Prostatic Fluid, Semen)* | 210 |
| 343уро | Уреаплазма (Ureaplasma urealyticum + Ureaplasma рarvum), определение ДНК в соскобе эпителиальных клеток урогенитального тракта (Ureaplasma urealyticum + Ureaplasma рarvum, DNA, Scrape of Urogenital Epithelial Cells)* | 210 |
| 301рот | Хламидия (Chlamydia trachomatis), определение ДНК в соскобе эпителиальных клеток ротоглотки (Chlamydia trachomatis, DNA, Scrape of Faucial Epithelial Cells)* | 210 |
| 349пл | Хламидия (Chlamydia pneumoniae), определение ДНК в плазме крови (Chlamydophila pneumoniae, DNA, Plasma)* | 300 |
| 349рот | Хламидия (Chlamydia pneumoniae), определение ДНК в соскобе эпителиальных клеток ротоглотки (Chlamydophila pneumoniae, DNA, Scrape of Faucial Epithelial Cells)* | 300 |
| 349слн | Хламидия (Chlamydia pneumoniae), определение ДНК в слюне (Chlamydophila pneumoniae, DNA, Saliva)* | 300 |
| 3250уро | Андрофлор Скрин, исследование микрофлоры урогенитального тракта мужчин в соскобе эпителиальных клеток | 1600 |
| 223 | Антитела антиспермальные в сыворотке крови (Anti-Spermatozoa Antibodies, ASA, Serum) | 780 |
| 807 | Антитела класса IgG к базальной мембране клубочков почек (анти-БМК) (Glomerular Basement Membrane Аntibodies, Аnti-GBM, IgG) | 1 290 |
| 970 | Антитела класса IgG к цитоплазме нейтрофилов (АНЦА) (Anti-Neutrophil Сytoplasmic Аntibodies, ANCA, IgG) | 1 640 |
| 812 | Антитела классов IgG, IgA, IgM к клеткам сосудистого эндотелия (HUVEC), суммарно (Anti-Endothelial Cell Antibodies, AECA, IgG, IgA, IgM, Total) | 1 300 |
| 837 | Антитела класса IgG к C1q фактору комплемента (Anti-Complement 1q Antibodies, Anti-C1q, IgG) | 1 200 |
| 4066 | Диагностика быстропрогрессирующего гломерулонефрита (АТ к базальной мембране клубочков почек, АТ к цитоплазме нейтрофилов (АНЦА/pANCA, cANCA), IgG) | 2 790 |
| 4067 | Диагностика аутоиммунного поражения почек (антинуклеарный фактор (АНФ), АТ к базальной мембране клубочков почек, АТ к цитоплазме нейтрофилов (АНЦА/pANCA, cANCA), IgG) | 3 800 |
| ФМ-Р | ФиброМакс (FibroMax) | 10 670 |
| ФТ-Р | ФиброТест (FibroTest) | 8 140 |
| 216 | Гастрин (Gastrin) | 570 |
| 294 | Пепсиноген I (Pepsinogen I) | 420 |
| 295 | Пепсиноген II (Pepsinogen II) | 420 |
| 2111 | Пепсиногены I и II с расчетом соотношения (Пепсиноген I/Пепсиноген II) (Pepsinogen I/Pepsinogen II, PG1/PG2) | 840 |
| 146 | Остеокальцин (Костный Gla белок) (Оsteocalcin, N-Osteocalcin, Bone Gla Protein, BGP) | 580 |
| 203 | С-концевые телопептиды коллагена I типа (бета-CrossLaps, С-терминальный телопептид, СТ) (Carboxyterminal Cross-linking Telopeptide of Bone Collagen, Collagen Cross-linked C-Telopeptide, Beta-Cross Laps, ?-CrossLaps Serum, C-Telopeptide, Crosslaps, Type 1 Collagen, СТ, b-СTx Serum) | 750 |
| 204 | N-терминальный пропептид проколлагена 1 общий (Procollagen Type 1 N-terminal Propeptide, P1NP, Total) | 1 200 |
| 147 | Дезоксипиридинолин (ДПИД) в моче (Deoxypyridinolinein, DPD, Urine) | 1 090 |
| 89 | Фенитоин (Дифенин, Дилантин) (Phenytoin) | 1 000 |
| 90 | Вальпроевая кислота (Депакин, Конвулекс) (Acidum Valproicum, Depakin, Convulexs) | 700 |
| 274 | Циклоспорин (Cyclosporine, Cyclosporine A, Sandimmune) | 800 |
| 814 | Литий (Li) в сыворотке крови (Lithium (Li), serum) | 1 200 |
| 665 | Панель разные аллергены, IgE (Panel Different Allergens, IgE) | 2 900 |
| 67 | Иммуноглобулины класса E (общий IgE, иммуноглобулин Е общий) (Immunoglobulin Е Total, IgE Total) | 350 |
| 670 | Панель педиатрическая, IgE (Pediatric Panel, IgE) | 2 900 |
| 666 | Панель респираторные аллергены, IgE (Respiratory Panel, IgE) | 2 900 |
| 669 | Панель пищевые аллергены, IgE (Food Allergy Panel, IgE) | 2 900 |
| 6611 | Смесь пищевых аллергенов 2: киви, манго, банан, ананас, IgE (FP50 (F84, F91, F92, F210), Food Panel: Kiwi Fruit, Mango, Banana, Pineapple, IgE)* | 850 |
| 602 | Смесь аллергенов плесени: Penicillium notatum, Cladosporium herbarum, Aspergillus fumigatus, Candida albicans, Alternaria tenuis, IgE (MP1 (M1, M2, M3, M5, M6), Mold Panel 1: Penicillium notatum, Cladosporium herbarum, Aspergillus fumigatus, Candida albicans, Alternaria tenuis, IgE)* (общий результат по смеси аллергенов) | 820 |
| 623 | Плесень Penicillium notatum, IgE (Penicillium notatum, IgE, M1) | 380 |
| 624 | Плесень Cladosporium herbarum, IgE (Cladosporium herbarum, IgE, M2) | 380 |
| 625 | Плесень Aspergillus fumigatus, IgE (Aspergillus fumigatus, IgE, M3) | 380 |
| 626 | Плесень Candida albicans, IgE (Candida albicans, IgE, M5) | 380 |
| 627 | Плесень Alternaria tenuis, IgE (Alternaria tenuis, IgE, M6) | 380 |
| 677 | Ананас, lgE, (Pineapple, lgE, F2100) | 360 |
| 645 | Говядина, lgE (Beef, lgE, F27) | 360 |
| 6619 | Смесь аллергенов плесени: Penicillium notatum, Cladosporium herbarum, Aspergillus fumigatus, Candida albicans, Alternaria tenuis, IgG (MP1 (M1, M2, M3, M5, M6), Mold Panel 1: Penicillium notatum, Cladosporium herbarum, Aspergillus fumigatus, Candida albicans, Alternaria tenuis, IgG)* | 700 |
| 6616 | Плесень Aspergillus fumigatus (М3), аллерген-специфические IgG (Aspergillus fumigatus, IgG, M3) | 360 |
| 1070 | Смесь аллергенов домашних грызунов: эпителий морской свинки, эпителий кролика, эпителийхомяка, крысы, мыши, IgE (EP70 (E6, E82, E84, E87, E88), Animal Panel: Guinea Pig Epithelium, Rabbit Epithelium, Hamster Epithelium, Rat, Mouse, IgE)* | 810 |
| 605 | Кошка, IgE (Cat Dander-Epithelium, IgE, E1) | 220 |
| 600 | Смесь аллергенов травы: ежа сборная, овсянная луговая,рож многолетняя, тимофеевка, мятлик луговой, IgE (GP1 (G3, G4, G5, G6, G8), Grass Panel 1: Orchard Grass, Meadow Fescue, Perennial Rye Grass, Timothy Grass, June Grass (Kentucky Bluegrass), IgE)* | 700 |
| 655 | Пивные дрожжи, IgE (Brewer’s Yeast, IgE, F403) | 360 |
| 647 | Просо, IgE (Common Millet, IgE, F55) | 360 |
| 601 | Смесь аллергенов травы: колосок душистый, рож многолетняя, тимофеевка, рож культивированная, бухарних шертистый, IgE (GP3 (G1, G5, G6, G12, G13), Grass Panel: Sweet Vernal Grass, Perennial Rye Grass, Timothy Grass, Cultivated Rye Grass, Velvet Grass, IgE)* | 700 |
| 657 | Береза, пыльца, IgE (Birch, IgE, ?3) | 360 |
| 6612 | Смесь пищевых аллергенов 1: апельсин, банан, яблоко, персик, IgG (FP15 (F33, F49, F92, F95), Food Panel: Orange, Banana, Apple, Peach, IgG)* | 700 |
| 6613 | Смесь пищевых аллергенов 3: свинина, куринное мясо, баранина, IgG (FP73 (F26, F27, F83, F88), Food Panel: Pork, Beef, Chicken Meat, Lamb, IgG)* | 700 |
| ALL | Определение специфических иммуноглобулинов класса G (IgG) к пищевым аллергенам (Basic Food Profile, IgG) | 9 800 |
| 6659 | Клубника (F44), аллерген-специфические IgG (Strawberry, IgG, F44) | 360 |
| 998 | Апельсин, IgE (Orange, IgE, F33) | 360 |
| 611 | Арахис, IgE (Peanut, IgE, F13) | 360 |
| 676 | Банан, IgE (Banana, IgE, F92) | 360 |
| 673 | Баранина, IgE (Lamb, IgE, F88) | 360 |
| 649 | Бета-лактоглобулин, IgE (Beta Lactoglobulin, IgE, F77) | 360 |
| 636 | Грейпфрут, IgE (Grapefruit, IgE, F209) | 360 |
| 641 | Гречневая мука, IgE (Buckwheat, IgE, F11) | 360 |
| 650 | Казеин, IgE (Casein, IgE, F78) | 360 |
| 642 | Капуста кочанная, IgE (Cabbage, IgE, F216) | 360 |
| 646 | Картофель, IgE (Potato, IgE, F35) | 360 |
| 654 | Киви, IgE (Kiwi Fruit, IgE, F84) | 360 |
| 634 | Клубника, IgE (Strawberry, IgE, F44) | 360 |
| 608 | Коровье молоко, IgE (Milk, IgE, F2) | 360 |
| 614 | Крабы, IgE (Crab, IgE, F23) | 360 |
| 615 | Креветки, IgE (Shrimp, IgE, F24) | 360 |
| 651 | Куриное мясо, IgE (Chicken Meat, IgE, F83) | 360 |
| 635 | Лимон, IgE (Lemon, IgE, F208) | 360 |
| 675 | Манго, IgE (Mango, IgE, F91) | 360 |
| 617 | Морковь, IgE (Carrot, IgE, F31) | 360 |
| 648 | Овсяная мука, IgE (Oat, IgE, F7) | 360 |
| 632 | Пекарские дрожжи, IgE (Baker’s Yeast, IgE, F45) | 360 |
| 674 | Персик, IgE (Peach, IgE, F95) | 360 |
| 610 | Пшеничная мука, IgE (Wheat, IgE, F4) | 360 |
| 652 | Рис, IgE (Rice, IgE, F9) | 360 |
| 644 | Свинина, IgE (Pork, IgE, F26) | 360 |
| 619 | Сельдерей, IgE (Celery, IgE, F85) | 360 |
| 612 | Соевые бобы, IgE (Soybean, IgE, F14) | 360 |
| 616 | Томаты, IgE (Tomato, IgE, F25) | 360 |
| 609 | Треска, IgE (Codfish, IgE, F3) | 360 |
| 643 | Тыква, IgE (Pumpkin, IgE, F225) | 360 |
| 613 | Фундук, IgE (Hazelnut, IgE, F17) | 360 |
| 633 | Шоколад, IgE (Chocolate, IgE, F105) | 360 |
| 653 | Яблоко, IgE (Apple, IgE, F49) | 360 |
| 607 | Яичный белок, IgE (Egg White, IgE, F1) | 360 |
| 618 | Яичный желток, IgE (Egg Yolk, IgE, F75) | 360 |
| 6614 | Плесень Penicillium notatum (М1), аллерген-специфические IgG (Penicillium notatum, IgG, M1) | 360 |
| 6615 | Плесень Cladosporium herbarum (М2), аллерген-специфические IgG (Cladosporium herbarum, IgG, M2) | 360 |
| 6618 | Плесень Alternaria tenuis (М6), аллерген-специфические IgG (Alternaria tenuis, IgG, M6) | 360 |
| 631 | Домашняя пыль/h2-Greer, IgE (House Dust – Greer, IgE, h2) | 360 |
| 672 | Домашняя пыль/h3-Stier, IgE (House Dust – Hollister-Stier, IgE, h3) | 360 |
| 621 | Клещ Dermatophagoides pteronyssinus (D1), IgE (Dermatophagoides pteronyssinus, IgE, D1) | 360 |
| 622 | Клещ Dermatophagoides farinae (D2), IgE (Dermatophagoides farinae, IgE, D2) | 360 |
| 664 | Клещ Dermatophagoides microceras (D3), IgE (Dermatophagoides microceras, IgE, D3) | 360 |
| 6632 | Клещ Dermatophagoides pteronyssinus (D1), аллерген-специфические IgG (Dermatophagoides pteronyssinus, IgG, D1) | 360 |
| 6633 | Клещ Dermatophagoides farinae (D2), аллерген-специфические IgG (Dermatophagoides farinae, IgG, D2) | 360 |
| 6634 | Клещ Dermatophagoides microceras (D3), аллерген-специфические IgG (Dermatophagoides microceras, IgG, D3) | 360 |
| 6638 | Кошка, эпителий (Е1), аллерген-специфические IgG (Cat Dander-Epithelium, IgG, E1) | 360 |
| 606 | Собака, IgE (Dog Epithelium, IgE, E2) | 360 |
| 6639 | Собака, эпителий (Е2), аллерген-специфические IgG (Dog Epithelium, IgG, E2) | 360 |
| 620 | Таракан, IgE (Cockroach, IgE, I6) | 360 |
| 660 | Морская свинка, эпителий, IgE (Guinea Pig Epithelium, IgE, Е6) | 360 |
| 661 | Волнистый попугай, перо, IgE (Budgerigar Feathers, IgE, Е78) | 360 |
| 662 | Овца, эпителий, IgE (Sheep Epithelium, IgE, Е81) | 360 |
| 663 | Курица, перо, IgE (Chicken Feathers, IgE, Е85) | 360 |
| 640 | Тополь, IgE (Cottonwood, IgE, T14) | 360 |
| 656 | Тимофеевка, пыльца, IgE (Timothy Grass, IgE, G6) | 360 |
| 658 | Полынь обыкновенная, пыльца, IgE (Mugwort, IgE, W6) | 360 |
| 659 | Полынь горькая, IgE (Wormwood, IgE, W5) | 360 |
| 628 | Латекс, IgE (Latex, IgG, K82) | 360 |
| 6667 | Апельсин, IgG (Orange, IgG, F33) | 360 |
| 6645 | Арахис, IgG (Peanut, IgG, F13) | 360 |
| 6671 | Банан, IgG (Banana, IgG, F92) | 360 |
| 6668 | Баранина, IgG (Lamb, IgG, F88) | 360 |
| 6601 | Бета-лактоглобулин, IgG (Beta Lactoglobulin, IgG, F77) | 360 |
| 6654 | Говядина (F27), аллерген-специфические IgG (Beef, IgG, F27) | 360 |
| 6666 | Грейпфрут (F209), аллерген-специфические IgG (Grapefruit, IgG, F209) | 360 |
| 6664 | Гречневая мука (F11), аллерген-специфические IgG (Buckwheat, IgG, F11) | 360 |
| 6602 | Казеин (F78), аллерген-специфические IgG (Casein, IgG, F78)) | 360 |
| 6649 | Капуста кочанная (F216), аллерген-специфические IgG (Cabbage, IgG, F216) | 360 |
| 6657 | Kартофель (F35), аллерген-специфические IgG (Potato, IgG, F35) | 360 |
| 6608 | Киви (F84), аллерген-специфические IgG (Kiwi Fruit, IgG, F84) | 360 |
| 6648 | Коровье молоко (F2), аллерген-специфические IgG (Milk, IgG, F2) | 360 |
| 6652 | Креветки (F24), аллерген-специфические IgG (Shrimp, IgG, F24) | 360 |
| 6603 | Куриное мясо (F83), аллерген-специфические IgG (Chicken Meat, IgG, F83) | 360 |
| 6609 | Лимон (F208), аллерген-специфические IgG (Lemon, IgG, F208) | 360 |
| 6670 | Манго (F91), аллерген-специфические IgG (Mango, IgG, F91) | 360 |
| 6656 | Морковь (F31), аллерген-специфические IgG (Carrot, IgG, F31) | 360 |
| 6661 | Овсяная мука (F7), аллерген-специфические IgG (Oat, IgG, F7) | 360 |
| 6669 | Персик (F95), аллерген-специфические IgG (Peach, IgG, F95) | 360 |
| 6610 | Пивные дрожжи (F403), аллерген-специфические IgG (Brewer’s Yeast, IgG, F403) | 360 |
| 6660 | Просо (F55), аллерген-специфические IgG (Common Millet, IgG, F55) | 360 |
| 6658 | Пшеничная мука (F4), аллерген-специфические IgG (Wheat, IgG, F4) | 360 |
| 6605 | Рис (F9), аллерген-специфические IgG (Rice, IgG, F9) | 360 |
| 6653 | Свинина (F26), аллерген-специфические IgG (Pork, IgG, F26) | 360 |
| 6646 | Соевые бобы (F14), аллерген-специфические IgG (Soybean, IgG, F14) | 360 |
| 6607 | Томаты (F25), аллерген-специфические IgG (Tomato, IgG, F25) | 360 |
| МАРКЕРЫ ВОСПАЛИТЕЛЬНОЙ РЕАКЦИИ | ||
| 45 | Иммуноглабулины класса А (Immunoglobulin A, lgA) | 220 |
| 46 | Иммуноглабулины класса M (Immunoglobulin M, lgA) | 220 |
| 47 | Иммуноглабулины класса M (Immunoglobulin G, lgG) | 220 |
| 48 | Железо (Fe) в сыворотке крови (Iron (Fe), Serum) | 220 |
| 193 | Компоненты системы комплемента C3, C4 (Complement components C3, C4) | 640 |
| 280 | РПГА с Shigella flexneri 1-5 (Shigella flexneri 1-5, IHA) | 360 |
| 238 | Антитела класса IgA к антигенам Yersinia еnterocolitica (Аnti-Yersinia enterocolitica IgA) | 440 |
| 239 | Антитела класса IgG к антигенам Yersinia еnterocolitica (Аnti-Yersinia enterocolitica IgG) | 440 |
| 286 | РПГА с Yersinia pseudotuberculosis (Yersinia pseudotuberculosis IHA) | 440 |
| 284 | РПГА с Yersinia еnterocolitica серотипа О:3 (Yersinia enterocolitica O:3, IHA) | 360 |
| 288 | РПГА с Salmonella gr. A (Salmonella gr.A, IHA) A (Salmonella gr.A, IHA) | 360 |
| 289 | РПГА с Salmonella gr.B (Salmonella gr.B, IHA) | 360 |
| 290 | РПГА с Salmonella gr.С (Salmonella gr.C, IHA) | 360 |
| 292 | РПГА с Salmonella gr.D (Salmonella gr.D, IHA) | 360 |
| 293 | Антитела к Salmonella gr.E, РПГА (Salmonella gr.E Antibodies, IHA) | 360 |
| 273 | Антитела к Salmonella typhi, РПГА (Salmonella typhi Antibodies, IHA) | 450 |
| Комплекс анализов для оперативного лечения (Инвитро) | ||
| 78ОБС | Госпитализация в хирургический стационар | 1650 |
Какие бывают тесты ВИЧ?
Для скрининга (т.е. быстрого и массового тестирования) применяется метод ИФА или ИХЛА. Для подтверждения диагноза применяется иммуноблот.
Для выявления ВИЧ в некоторых ситуациях применяется качественный (т.е. есть или нет, без ответа на вопрос «сколько?») ПЦР РНК или провирусной ДНК ВИЧ, но данный метод является на сегодня вспомогательным и его не следует использовать для скрининга ВИЧ-инфекции.
У лиц с диагностированной ВИЧ-инфекцией применяется количественный метод ПЦР на РНК ВИЧ, он позволяет ответить на вопрос сколько вируса в крови. Его так же не следует применять для диагностики.
Когда после риска нужно сделать тест на ВИЧ?
Оптимально сделать два теста: через 6 недель и через 12 недель (3 месяца, если округлить до целых месяцев) после риска — достоверность отрицательного результата будет предельно близка к 99,9 %. Тест через любой более длительный срок тоже будет достоверен.
На любых сроках от потенциально опасной ситуации после 6-12 недель ИФА не увеличивает и не теряет своей надежности, оставаясь точным методом диагностики и через год, и через два и далее. В очень редких случаях диагностические проблемы могут возникать у очень тяжелых, фактически терминальных пациентов, с развернутой картиной СПИДа. Подробнее можно почитать об этом здесь, также там даны ответы на вопросы о т.н. поздней сероконверсии.
Подробнее можно почитать об этом здесь, также там даны ответы на вопросы о т.н. поздней сероконверсии.
Где я могу пройти тест на ВИЧ?
Существует много мест, где вы можете пройти тест на ВИЧ: в поликлинике, в кабинете частного врача, больницах, клиниках планирования семьи и в местах, специально отведенных для тестирования на ВИЧ.
Всегда старайтесь пройти тестирование там, где проводится консультирование. В некоторых местах имеются услуги по консультированию и тестированию на дому, которые могут включать консультирование пар и оказание им поддержки для безопасного раскрытия результатов после тестирования.
Какой нужно сделать тест?
ИФА или ИХЛА тест на ВИЧ. Это название технологии теста. Конкретное название оборудование будет написано на упаковке теста, например, Abbot ARCHITECT HIV Ag/Ab Combo.
Зачем делать тест через 6 недель, если всё равно нужно будет делать через 12? Можно обойтись только одним тестом через 12 недель?Да, можно. Первый тест даст уже очень высокую предварительную достоверность, что важно для диагностики, и, кроме того, при отрицательном результате позволяет легче переждать срок до финального теста через 3 месяца.
Что такое период (серонегативного) окна?
Это период между заражением ВИЧ и появлением обнаруживаемых антител к вирусу.
В течение «периода окна» в крови ВИЧ-инфицированных людей нет антител, которые можно обнаружить с помощью теста на ВИЧ. Тест на ВИЧ отрицателен. Однако, в жидкостях организма человека, таких как кровь, семенная жидкость, влагалищное отделяемое и грудное молоко, уже может отмечаться высокий уровень ВИЧ.
ВИЧ может передаваться другим людям во время периода окна, даже если тест на ВИЧ не показал, что у вас ВИЧ-инфекция.
Какова достоверность теста через 6 недель после риска?
Для тестов, определяющих и антитела и антигены — практически полная, для тестов только на антитела — примерно на уровне 95%.
Если ИФА положительный, то это означает диагноз ВИЧ-инфекции?
Нет, требуется подтверждение другим методом. Подтверждающим методом для диагностики ВИЧ-инфекции сегодня является непрямая иммунофлюоресценция (РНИФ, иммуноблот, вестерн-блот). Иммуноблот демонстрирует высокую чувствительность (99,3 — 99,7 %) и специфичность (99,7 %), но так как метод определяет иммуноглобулины класса G, то с момента инфицирования результат может быть ложноотрицательным до трех недель.
У меня первый (второй третий, сорок шестой) ИФА тест на ВИЧ положительный, а иммуноблот отрицательный. Что это значит?
Это значит, что ВИЧ у Вас нет.
У меня иммуноблот сомнительный (неопределенный). Что это значит?
Вам необходимо повторить иммуноблот через 2-3 месяца после первого. Если он будет отрицательным или останется неопределенным, то ВИЧ можно исключить. Иммуноблот может быть отрицательным или сомнительным сразу после инфицирования в пределах 4-8 недель, именно для этого его нужно повторить.
Проверочный иммуноблот оказался положительным. У меня ВИЧ? Ошибки быть не может?
Да, у вас, к сожалению, ВИЧ. Не может.
У меня отрицательный тест через 3 месяца, но у меня продолжаются непонятные симптомы, у меня ВИЧ?
ВИЧ у Вас нет. Ваши симптомы к ВИЧ отношения не имеют. С любой непонятной симптоматикой нужно обращаться к врачам очно.
Есть ли возможность узнать о наличии или отсутствии ВИЧ раньше?
Да, возможно. Первый ИФА (ИХЛА) Ат+Аг тест можно сделать уже через 3 недели после риска, его достоверность будет высокой. Если есть лишние деньги, то можно сделать тест ПЦР ДНК качественный на ВИЧ через 2 недели после риска, его результат тоже даст высокую предварительную достоверность.
Я сдавал тест через 1,2,3,4,5,6,7,8,9,10,11,12 месяцев после риска. Они все отрицательные. Но я плохо себя чувствую, у меня чешется левая пятка и зудит под левой подмышкой. У меня точно ВИЧ, я уверен, просто тесты его не показывают!
ВИЧ у Вас нет. Со СПИДофобией нужно обратится к психиатру очно.
В чем разница между ИФА и ИХЛА? Что информативнее?
Иммуноферментный анализ (ИФА) и иммунохемилюминесцентный анализ (ИХЛА) это два способа забить гвоздь, большим красным, или средним зеленым молотком. Результат один и тот же — взаимодействие антигена с антителом или отсутствие такового. Т.е. информация — забитый гвоздь — в итоге одна и та же.
Обычно указания на ИХЛА в отношении диагностики ВИЧ носит характер артефакта, и на самом деле речь идет об ИФА. Т.е. с одной стороны — разницы нет, с другой — правильнее оперировать не названием метода, а названием тест-системы.
Как узнать поколение теста, определяет ли он антиген?
Антиген определяется, если известно, что это тест 4-го поколения, если в названии теста фигурируют слова или буквы: антиген, antigen, аг, ag.
Какие поколения тестов сейчас используются? Могут ли это быть старые тесты 2-го поколения?
Все современные тесты — это тесты 3-го (без антигена) или 4-го (с антигеном). Более старые тест-системы не производятся и не используются уже как минимум лет пять. Все современные тесты дают полную достоверность через 12 недель после риска, независимо от их обозначений и поколений.
Что такое тесты 4 поколения? Чем отличается разные поколения ИФА?
Тесты 4 поколения детектируют ВИЧ-инфекцию раньше, так как «видят» не только антитела, как тесты 3 и более ранних поколений, но и антиген ВИЧ. Антитела вырабатываются организмом в ответ на ВИЧ-инфекцию, и на выработку нужно некоторое время. Антиген ВИЧ p24, это белок вирусного капсида, а именно непосредственно кусочек вируса. Понятно, что он начинает определяться в крови ранее, чем антитела — белки иммунной системы человека, которые вырабатываются в ответ на ВИЧ-инфекцию. Т.е. «период окна» для теста 4 поколения совсем небольшой. Когда начинают обнаруживаться в большом антитела против ВИЧ, антиген p24 часто уже не выявляется, вероятнее всего в результате образования комплекса между антигеном и антителами в крови. В случаях его обнаружения антиген p24 является высокоспецифическим индикатором инфекции.
Какого поколения был мой тест?
Для Российской Федерации — четвертного, иных у нас не ввозится и не используется. В названии теста обычно присутствует что-либо из: «Combo», «At/Ag», «АТ/АГ» или «p24».
Выявляет ли ИФА тест 4 поколения ВИЧ-2?
Да, все современные специализированные ИФА-системы выявляют ВИЧ-1 и ВИЧ-2.
Какой период «окна» для тестов 4 поколения (Ag/At Combo)?
Тест-системы 4 поколения способны обнаружить не только антитела к ВИЧ, которые организм вырабатывает в ответ на инфекцию, но и непосредственно ВИЧ, посредством выявления вирусного белка p24. Белок p24 может быть определен очень рано, но его уровень в крови в период после инфицирования постепенно снижается, но одновременно с этим снижением нарастает уровень антител. Все люди разные, потому назвать точный 100% минимальный срок, когда сомневаться в тесте уже нет поводов — невозможно. Однако, на сегодня есть достаточное количество исследований, которые дают нам весьма определенные ориентиры, приведем лишь несколько из них:
Итак, у нас достаточно данных считать, что лабораторные ИФА-системы 4 поколения с очень высокой вероятностью «не пропустят» ВИЧ-инфекцию уже через месяц поле инфицирования.
Так все же, с какого срока ИФА 4 поколения совершенно надежно исключает ВИЧ?
Тест 4 поколения может в отдельных случаях выявлять ВИЧ-инфекцию уже через неделю после инфицирования, но ориентироваться на это все же нельзя, потому как это скорее исключение. Как Вы видели выше — месяц вполне надежный срок для современных лабораторных тест-систем.
Я тестировался на разных сроках, в том числе и через 6-8 недель, и через 12 недель (3 месяца после возможного контакта) и не могу успокоиться, потому как наблюдаю различные симптомы, в некоторых результатах анализов есть отклонения и т.д. и т.п. Что делать? Что мне еще сдать?
Ничего, в данном случае вы имеете дело с неким иным заболеванием, и скорее всего с тревожным или тревожно-депрессивным расстройством. Получите консультацию квалифицированного инфекциониста, а затем, если инфекционная или иная природа будет исключена, то обратитесь за помощью к психотерапевту или психиатру.
Что такое специфичность и чувствительность?
Специфичность диагностического теста – это доля верно определенных тестом заведомо отрицательных образцов.
Иначе говоря, для определения специфичности теста необходимо взять несколько тысяч заведомо здоровых людей и проверить их при помощи теста. Если на каждые 1000 образцов будет получено 10 ложных положительных результатов – то специфичность теста составит: (1000-10)/1000*100%=99%. Если количество ложных срабатываний больше, то специфичность становится меньше (т.е. хуже). Так, специфичность теста 99% означает примерно 10 ложных позитивных результатов на 1000 проверенных здоровых людей.
Внимательно изучите инструкцию и материалы предлагаемых на рынке тестов, найдите информацию о том, каким образом была проверена специфичность. Как правило, это данные по испытаниям нескольких тысяч образцов, полученных из разных географических регионов.
Чувствительность диагностического теста – это доля верно определенных тестом заведомо положительных образцов.
Иными словами, если мы возьмем 100 достоверно ВИЧ-инфицированных людей, проверим их тестом и получим 100 положительных результатов, то чувствительность теста будет равна 100%. Практически у всех тестов на рынке чувствительность 100%.
Нельзя путать понятия точности выявления положительных и отрицательных образцов. Точность выявления положительных образцов — это чувствительность теста, а точность выявления отрицательных образцов — это специфичность.
Чувствительный тест часто дает положительный результат при наличии заболевания (обнаруживает его). Однако, особенно информативен он, когда дает отрицательный результат, т.к. редко пропускает пациентов с заболеванием. Пример — ИФА.
Специфичный тест редко дает положительный результат при отсутствии заболевания. Особенно информативен при положительном результате, подтверждая (предположенный) диагноз. Пример — иммуноблот.
Логично использовать для скрининга (быстрого и дешевого тестирования большого числа пациентов) максимально чувствительный вид тестов, а вот для установления диагноза — максимально специфичные методы. Именно поэтому ИФА исторически является скрининговым, а иммуноблотом подтверждается ВИЧ-инфекция.
Важно понимать, что ложные положительные результаты существуют у всех тестов, никакой тест не может давать 100% специфичности! Результаты экспресс-тестов подлежат особой проверке и перепроверке в лабораторных условиях при помощи других методов. Результаты лабораторных ИФА тестов подлежат перепроверке методом иммуноблотинга.
Может ли тест быть ложноположительным?
Да, может. В этом случае в обязательном порядке необходимо сделать проверочный тест иммуноблот, который точно покажет есть у человека ВИЧ или нет.
По каким причинам тест на ВИЧ может быть ложноположительным?
Причин много и все они не известны. Самая частая причина — беременность, также такую вероятность несколько увеличивает недавние вакцинирование некоторыми иммунопрепаратами.
Может ли тест быть ложноотрицательным?
Может, если он сделан в период окна, который длится до 3-х месяцев после риска инфицирования.
Каковы причины ложноотрицательного результата в тесте на ВИЧ?
Ложноотрицательный результат, а точнее существенное удлинение «периода окна», может вызвать начатая очень рано после инфицирования антиретровирусная терапия или постконтактная профилактика, прием средств, подавляющих иммунитет (иммунодепрессантов, например, после пересадки органов и др.), а также некоторые тяжелые заболевания иммунной системы.
Но, нужно понимать, что тесты 4-го поколения определяют не только антитела, но и антиген p24, который является белком вирусной оболочки, т.е. эти тесты определят ВИЧ-инфекцию, даже если антитела по каким-то причинам задерживаются.
Алкоголь, иные психоактивные вещества, любая пища, БАДы, иммуностимуляторы, иммуномодуляторы, антибиотики и любые иные препараты, стресс, полнолуние, созерцание белого коня, усталость, общая болезненность и ослабленный иммунитет, грипп, ангина и прочие заболевания — все это не оказывает значимого влияния на риски ложноотрицательного результата теста на ВИЧ.
Чувствительность тестов на ВИЧ исследована и подтверждена в реальных условиях и на больших выборках, где люди принимают алкоголь, нервничают, принимают самые разные препараты, болеют различными заболеваниями, имеют самые разные отклонения лабораторных параметров.
Я сдавал общий анализ крови (биохимию печени, иммунограмму, липидный профиль), анализы в норме. Означает ли это, что у меня нет ВИЧ-инфекции?
Нет, не означает. Ни по каким анализам, кроме теста на ВИЧ, невозможно ни исключить ни подтвердить ВИЧ-инфекцию.
Я принимаю антибиотики (антидепрессанты, транквилизаторы, настой на мышиных хвостах), будет ли тест достоверен?
Будет. Никакие препараты, кроме препаратов АРТ в качестве постконтактной профилактики не влияют на достоверность теста на ВИЧ.
Я перед сдачей теста выпила стакан пива (бутылку водки, съела два торта, выкурила 5 пачек сигарет, косячок марихуаны), не повлияет ли это на результат теста?
Не повлияет.
Может быть так, что антиген уже связан антителами, а антител еще мало для теста?
Этот феномен описан, но это весьма короткоживущий феномен, по сути это точка пересечения двух условных кривых, никто вам не скажет, это часы или десятки минут, но точно не многие дни, скорее следует предполагать как максимум (предположение, для утверждения не достаточно данных) 1-2 суток. И в любом случае этот феномен, если и возникает, то находится там, где мы вообще из осторожности не говорим о полной достоверности тестирования, т.е. внутри первых 4-6 недель, и с очень высокой долей вероятности этот период внутри еще более короткого промежутка — в пределах первых двух недель, т.е. мы как бы укладываем оба окна одно в другое. Плюс, по всей видимости, есть некоторые условия, которые хоть сколько то значимыми делают вероятность «подловить» это самое второе окно — исходные иммунодефицитные состояния, например, связанные с возрастом.
Если бы доминирующие ИФА системы отдельно показывали срабатывание At или Ag линии, то мы бы знали (т.е. мы и так это знаем, но вот имели бы статистику по этому поводу), что за редким исключением выявление ВИЧ происходит по At линии, а если бы мы неким волшебным образом знали дату инфицирования, то мы бы знали, что за редким исключением мы выявляем довольно поздно, спустя многие месяцы и годы. В отдельных группах риска под влияем активных действий ситуация может чуть смещаться в сторону более раннего выявления, но это все не меняет погоды по большому счету. Т.е. реальных практических рисков феномен второго окна не несет — любой врач будет рекомендовать и принимать во внимание тестирование на тех сроках, когда с очень высокой вероятностью будет антитела в достаточных для детекции количествах.
А какие подтипы выявляет ИФА? Что если я заразился редким подтипом и тест его не видит?
Нет, такого не бывает. Современные скрининговые ИФА-системы выявят любой подтип из группы M и O. Представителей групп N и P зарегистрировано единичное число, их очень непросто найти даже в Камеруне, где их число чуть больше ноля, и измеряется единицами. Как только, с точки зрения эпидпроцесса, распространенность группы превысит хотя бы сотые доли процента, и будут обнаружены в за пределами африканской глуши хотя бы единичные пациенты, то и тест-системы официально подтянутся, вслед за нуждами — будут проведены широкие исследования и появятся группы и подтипы в технических характеристиках систем, то, что их нет там сегодня означает лишь то, что их нет официально. На данный момент рассматривать подобные сценарии нет смысла.
В 2006 году их было известно десять камерунцев с группой N, но спустя 5 лет, после тщательных просеиваний тысяч камерунцев нашли еще… четыре.
По разным оценкам от 400 до 800 тысяч камерунцев живут с ВИЧ, и мы знаем, что возможно до 0,1% являются носителями группы N. Т.е. от 400 до 800 человек на планете.
Важно: все редкие группы и подтипы ВИЧ были выявлены исходно обычным методом ИФА. То, что в технических характеристиках систем не указаны эти подтипы, говорит лишь об одно — число пациентов слишком мало, чтобы можно было бы провести стандартные исследования, для которых требуется не несколько случаев, а сотни, и официально утвердить у регулятора новые строчки в инструкции.
Я слышала, что методом ИФА ВИЧ-2 выявляется позднее, это так?
В данном случае это не имеет значения, антитела выходит на уровень достаточный для детекции примерно в одни и те же временные рамках, общие перестраховочные сроки 6-8 недель от опасного контакта «накрывают» и ситуации с ВИЧ-1 и с ВИЧ-2.
Аптечные ИФА экспресс-тесты достаточно надежны?
Экспресс-тесты на антитела к ВИЧ в США одобрены с 2002 года, в том числе ультрабыстрые тесты, чувствительность таких тестов от 93% и специфичность — от 99%. Одобренный и доступный в РФ экспресс-тест Alere Determine HIV ½ Ag/Ab Combo, значительно уступает по способности к обнаружению антигена р24 ВИЧ по сравнению с коммерческими лабораторными системами 4 поколения.
Следует учитывать, что экспресс-тесты значительно чаще лабораторных дают ложный положительный результат. Положительный прогностический результат для РФ у экспресс-тестов будет примерно 50 на 50, т.е. если экспресс-тест дает положительный результат, то в среднем, т.е. для групп низкого риска, вероятность в данном случае наличия ВИЧ-инфекции лишь 50%, и любой положительный результат обязательно требует перепроверки методом ИФА в условиях лаборатории.
Можно ли применять ПЦР РНК или ДНК ВИЧ для скрининга на ВИЧ?
Да, можно. но не не рекомендуется. Хотя за последнее десятилетие метод стал значительно дешевле и точнее, но все же он до сих пор и дорог, более длительный, и технически сложен, что предполагает большие риски ошибок. В России, так же впрочем, как и США, количественный метод ПЦР не рекомендован для скрининга и диагностики ВИЧ-инфекции в обычных случаях.
Чем отличается ПЦР ДНК от ПЦР РНК ВИЧ?
РНК обычно используется в количественных тестах для оценки вирусной нагрузки у диагностированных лиц, например для оценки эффективности терапии. ДНК — в мононуклеарных клетках, например для диагностики у детей, там, где антитела к ВИЧ матерей мешает использовать метод ИФА. И тот и другой тест могут быть и количественными и качественными. И тот и другой можно в узких случаях применить как диагностический, с учетом конкретных ограничений, которые накладывают технические параметры системы.
Я сдавал в коммерческой лаборатории анализ ПЦР РНК (или ДНК) ВИЧ, могу ли я исключить инфицирование?
Да, скорее всего можете, но вы делали это зря. Выше мы писали, что метод ПЦР не применяется для скрининга, а значит нужно делать ИФА.
Отвечал на частые вопросы равный консультант Erik Kivexa.
Мы ответим на те вопросы, которые у вас могли остаться.
Прежде, чем задать вопрос, посмотрите, нет ли ответа на него в тексте выше и соответствует ли он теме тестирования на ВИЧ. Если есть или не соответствует, то не стоит задавать вопрос снова — он не пройдет премодерацию.
Туберкулез можно диагностировать только по слюне
Туберкулез (ТБ) остается одной из самых смертоносных инфекций в мире. Частично проблема заключается в продолжительном периоде времени, необходимом для постановки правильного диагноза. Теперь ученые говорят, что для тестирования достаточно генетического анализа слюны подозреваемого пациента. Кроме того, этот метод позволит поставить точный диагноз в течение одного дня.
Вызывается бактериями Mycobacterium tuberculosis , болезнь поражает легкие пациентов.Поскольку бактерии распространяются по воздуху, больные туберкулезом могут легко заразить других людей, если им не поставить диагноз и не лечить должным образом.
В настоящее время для подтверждения диагноза ТБ в лаборатории может потребоваться до двух месяцев из-за медленного роста бактерий. Ученые надеются перейти к тестированию на туберкулез только с образцом мокроты, но небольшое количество ДНК бактерий туберкулеза в слюне затрудняет этот метод.
Но теперь ученые из Оксфордского университета говорят, что есть способ надежно проверить мокроту на туберкулез.Их метод основан на выделении ДНК ТБ и выполнении секвенирования генома для идентификации штамма ТБ. По их словам, с помощью этого метода можно обнаружить штаммы, которые стали устойчивыми к лекарствам. Такая информация принесет пользу пациенту, а также предупредит экспертов общественного здравоохранения, которые могут быть заинтересованы в отслеживании распространения этих штаммов в эпидемиологических целях.
Кроме того, новый метод может похвастаться моментом оборота в тот же день – подвиг, который может произвести революцию в диагностике туберкулеза. Это заявление подтверждается новой технологией секвенирования, которая стала более доступной и портативной с тех пор, как несколько лет назад произошел взрыв в области генетики.Команда ученых заявляет, что с помощью портативного устройства Oxford Nanopore MInION можно поставить надежный диагноз в течение 12,5 часов в любой точке мира.
«Одна из серьезных проблем при ведении туберкулеза – это необходимость в быстрых комплексных тестах, не требующих высокотехнологичной лаборатории. Мы показали, что можно получить всю информацию, необходимую как для клинического ведения, так и для отслеживания распространения заболевания, в течение 24 часов после взятия пробы у пациента.Кроме того, достигнув этого с помощью портативного устройства, мы открываем двери для полевых диагностических тестов на туберкулез », – сказал д-р Замин Икбал из Центра генетики человека Wellcome Trust при Оксфордском университете, который был одним из руководителей исследования.
«Конечно, предстоит еще много работы – наша цель – вернуть результаты анализов до того, как пациент покинет свою клинику, с огромным потенциалом для снижения передачи заболевания и устойчивости к лекарствам», – добавил он.
Среди быстрых результатов исследования исследователи считают способность идентифицировать лекарственно-устойчивые штаммы огромным преимуществом этого нового метода обнаружения.Это будет особенно важно в эпоху супербактерий.
Дополнительные источники: MedicalXpress, BBC
Определение биомаркеров сыворотки и слюны кандидата-хозяина для лучшей диагностики активной и латентной туберкулезной инфекции
Abstract
В нашей работе мы стремимся идентифицировать новых биомаркеров кандидатов-хозяев, чтобы различать пациентов с активным ТБ (n = 28), латентной инфекцией (LTBI; n = 27) и неинфицированными (NoTBI; n = 42) людьми. Для этого были привлечены активные больные туберкулезом и их контактные лица, сдавшие образцы сыворотки и слюны.Мультиплексный анализ был проведен для изучения концентрации различных цитокинов, хемокинов и факторов роста. Отбирали белки со значительными различиями между группами, и для оценки диагностической точности использовали логистическую регрессию и площадь под кривой ROC (AUC). Лучшими комбинациями маркеров, которые отличают активный ТБ от контактов с NoTBI, были [IP-10 + IL-7] в сыворотке и [Fractalkine + IP-10 + IL-1α + VEGF] в слюне. Лучшее различие между активным ТБ и ЛТИ было достигнуто при использовании [IP-10 + BCA-1] в сыворотке (AUC = 0.83) и IP-10 в слюне ( p = 0,0007; AUC = 0,78). Уровни TNFα ( p = 0,003; AUC = 0,73) в сыворотке и комбинация [фракталкин + IL-12p40] (AUC = 0,83) в слюне позволили дифференцировать контакты NoTBI и LTBI. В заключение, разные индивидуальные и комбинированные белковые маркеры могут помочь отличить активный туберкулез от неинфицированных и латентно инфицированных контактов. Наиболее многообещающие включают [IP-10 + IL-7], [IP-10 + BCA-1] и TNFα в сыворотке и [Fractalkine + IP-10 + IL-1α + VEGF], IP-10 и [Fractalkine + IL-12p40] в слюне.
Образец цитирования: Estévez O, Anibarro L, Garet E, Pallares Á, Pena A, Villaverde C, et al. (2020) Определение биомаркеров сыворотки и слюны кандидата-хозяина для лучшей диагностики активной и латентной туберкулезной инфекции. PLoS ONE 15 (7): e0235859. https://doi.org/10.1371/journal.pone.0235859
Редактор: Olivier Neyrolles, Institut de Pharmacologie et de Biologie Structurale, Франция
Поступила: 24 марта 2020 г .; Принят в печать: 23 июня 2020 г .; Опубликовано: 20 июля 2020 г.
Авторские права: © 2020 Estévez et al.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в документе и его файлах с вспомогательной информацией.
Финансирование: Эта работа была поддержана проектом EU Horizon2020 Eliciting Mucosal Immunity in Tuberculosis (EMI-TB) [номер гранта 643558] (https: // ec.europa.eu/programmes/horizon2020/en) и Xunta de Galicia «Grupo de Referencia Competitiva 2016» [номер гранта ED431C 2016/041] (https://www.edu.xunta.gal/portal/es/node/26897 ). О. выражает признательность за стипендию Министерства образования Испании [номер гранта FPU 13/03026] (http://www.educacionyfp.gob.es/servicios-al-ciudadano/catalogo/general/99/998758/ficha/998758-2019. html). Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Гонсалес-Фернандес является со-промотором компании NanoImmunoTech. Авторы не имеют других соответствующих аффилированных или финансовых отношений с какой-либо организацией или организацией, имеющей финансовый интерес или финансовый конфликт с предметом или материалами, обсуждаемыми в рукописи, кроме тех, которые раскрыты. Это не влияет на нашу приверженность политике PLOS ONE в отношении обмена данными и материалами.
Введение
Туберкулез (ТБ) остается одной из основных причин смерти во всем мире, на него приходится 1.5 миллионов смертей в 2018 году [1]. Точная диагностика туберкулеза и лечение людей, инфицированных Mycobacterium tuberculosis ( Mtb ), является ключом к предотвращению ежегодной смерти миллионов людей. Однако в диагностике туберкулеза все еще существуют большие ограничения.
Активная диагностика туберкулеза путем обнаружения кислотоустойчивых бацилл в мокроте имеет низкую чувствительность [2], а посев мокроты требует длительного периода времени до получения окончательного результата; ex vivo M . Тест амплификации гена tuberculosis (GeneXpert MTB / RIF) дает быстрые результаты с высокой чувствительностью [3].Однако это относительно дорогой тест, требующий специализированной инфраструктуры, которая не всегда доступна в районах с низким уровнем дохода [4]. Более того, ни один из этих тестов не позволяет выявить скрытую туберкулезную инфекцию (ЛТИ) [5]. В настоящее время не существует золотого стандарта теста для выявления ЛТИ, поэтому для этой цели используются туберкулиновая кожная проба (TST) или анализ высвобождения гамма-интерферона (IGRA). Оба этих теста выявляют иммунологическую память против антигенов Mtb , и ни один из них не может отличить активный ТБ от ЛТИ [6].
Принимая во внимание все ограничения, упомянутые выше, очевидна необходимость новых диагностических инструментов, позволяющих различать активных больных ТБ, скрытую инфекцию ТБ и неинфицированных людей. Желательны прямые анализы ex vivo , которые можно было бы адаптировать для доступного тестирования в местах оказания медицинской помощи. Кроме того, в этих тестах должны использоваться легкодоступные биологические образцы, которые можно получить от всех людей. Образцы сыворотки и слюны обладают несколькими качествами, которые делают их привлекательными кандидатами для этой цели.Образцы сыворотки легко собирать специализированный персонал и требуют минимальной обработки образцов [7]. Однако одним из его ограничений является инвазивность и потребность в квалифицированных специалистах для сбора. С другой стороны, образцы слюны неинвазивны, экономичны, их легко хранить и легко получить неспециализированный персонал [8,9]. Кроме того, слюна представляет собой образец слизистой оболочки, связанной с дыхательными путями, основным путем заражения Mtb . По этой причине мы считаем, что слюна может быть не только потенциальным инструментом для диагностики туберкулеза, но и источником информации о событиях, происходящих на уровне слизистой оболочки, что имеет большое значение в контексте легочного туберкулеза.
Идентификация биомаркеров хозяина в сыворотке и слюне, которые помогают различать группы, является ключом к разработке улучшенных диагностических инструментов. Предыдущие исследования были проведены с использованием образцов сыворотки, плазмы [10–19] и слюны [16,20,21], которые выявили некоторые кандидаты в биомаркеры ТБ. Однако до сих пор отсутствует консенсус относительно того, какие из них являются наиболее действенными для различения активной и латентной инфекции ТБ или между здоровыми людьми с инфекцией или без нее. По этой причине мы провели исследование, в котором проанализировали некоторые из маркеров, наиболее широко изучаемых в контексте туберкулеза, таких как IFNγ или IFN-индуцируемый белок 10 (IP-10), а также другие цитокины, хемокины и факторы роста, которые могут вносить свой вклад в инфекцию и, следовательно, являются отличительной чертой различных исследовательских групп.Наше исследование предоставляет информацию о новых биомаркерах-кандидатах в образцах сыворотки и слюны, которые могут помочь в улучшении диагностических инструментов, доступных на сегодняшний день.
Материалы и методы
Участники исследования
участников, включенных в настоящее исследование, были отобраны в рамках проекта h3020 «Выявление иммунитета слизистой оболочки к туберкулезу» (EMI-TB; h3020-EU.3.1: Социальные проблемы; «Здоровье, демографические изменения и благополучие». Ссылка 643558 ).Набор проводился в период с сентября 2015 г. по июль 2017 г. в противотуберкулезном отделении комплекса «Complexo Hospitalario Universitario de Pontevedra» (Галисия, северо-запад Испании).
В исследование были включены микробиологически подтвержденные пациенты с активным туберкулезом легких и их контактные лица, классифицированные как неинфицированные (NoTBI) или с латентной туберкулезной инфекцией (LTBI). Участники имели право на участие в исследовании, если они были готовы дать письменное информированное согласие. Люди были исключены из исследования, если они были моложе 18 лет; они были беременны; ранее получала противотуберкулезное лечение; TST проводился за последние 3 месяца до приема на работу; были одновременно инфицированы ВИЧ или проходили какое-либо иммуносупрессивное лечение, включая ингаляционные кортикостероиды.Мы также исключили людей с диабетом, терминальной стадией почечной недостаточности, алкоголизмом или любым аутоиммунным заболеванием и, в целом, любым другим иммуносупрессивным состоянием, по мнению лечащего врача. Кроме того, исключались контакты, соответствующие любому из следующих условий: предыдущий диагноз ТБ или подтвержденный TST / IGRA; наличие давно зажившего очага на груди на рентгенограмме; недавняя вакцинация (<3 месяцев) живыми ослабленными штаммами и наличие любой другой активной инфекции в течение предыдущего месяца.Исследование было одобрено Галицким этическим комитетом (регистрационный номер: 2014/492), и от всех участников было получено письменное информированное согласие.
Диагностические тесты
Диагностика лиц, контактировавших с больными туберкулезом, была основана на TST и, при наличии показаний, с помощью теста IGRA в соответствии с консенсусом в отношении диагностики ТБ в Испании [22].
TST выполняли по методу Манту с использованием двух единиц туберкулина RT-23 (PPD, Statens Serum Institute, Копенгаген, Дания). Через 48–72 часа измеряли диаметр уплотнения.Пациенты с площадью уплотнения ≥ 5 мм считались TST-положительными. Набор Quantiferon TM -TB Gold In-Tube Kit (Cellestis Ltd, Карнеги, Австралия) использовался для измерения продукции гамма-интерферона в антиген-стимулированных Т-клетках крови после инкубации с антигенами ESAT-6, CFP10 и TB7.7. следуя инструкциям производителя. Пороговое значение для положительного результата IGRA составляло 0,35 МЕ / мл. «Период окна» рассматривался в контактах с отрицательным TST / IGRA во время их первого визита.В этих случаях второй тест проводился через 8–10 недель после последнего возможного контакта с индексным случаем [23].
Пациенты с активным туберкулезом легких были микробиологически подтверждены с помощью посева и / или амплификации нуклеиновых кислот в респираторных образцах. Контактным лицам больных туберкулезом с положительным результатом TST / IGRA, у которых не было никаких симптомов и не было доказательств клинических и радиологических заболеваний, был окончательно диагностирован латентный туберкулез.
Сбор и обработка проб
Всего было набрано 97 участников, включая 28 больных туберкулезом в активной форме, 42 неинфицированных контакта и 27 лиц, контактировавших с ЛТИ.Все пациенты сдали 10 мл периферической венозной крови, собранной в пробирки с сепаратором сыворотки SST II Advance (Vacutainer, BD; Плимут, Великобритания). Пробирки центрифугировали при 1300 g в течение 10 мин при комнатной температуре, фракцию сыворотки собирали, делили на аликвоты и хранили при -80 ° C до их использования.
Образцы слюны собирали в полипропиленовые пробирки объемом 15 мл до объема 7–10 мл на участника и хранили при 4 ° C во время обработки образцов. Пробирки центрифугировали при 300 g в течение 5 минут, и супернатант собирали и обрабатывали ингибитором протеазы (Complete Tablet Mini, Roche; Mannheim, Germany), чтобы избежать деградации белка.Надосадочные жидкости слюны очищали путем механического разрушения на устройстве BeadBeater (Mini BeadBeater-16, BioSpec Products; Бартлсвилл, штат Оклахома, США) с применением трех импульсов перемешивания по 20 с в присутствии шариков из диоксида циркония 0,1 мм (BioSpec Products; Bartlesville, США). ОК, США). Супернатант собирали после центрифугирования и фильтровали через клеточный фильтр 0,22 мкм. Обработанные образцы слюны хранили при -80 ° C и постепенно оттаивали на льду в день проведения анализа.
Мультиплексный иммуноферментный анализ
Индивидуальные наборы Milliplex (модифицированные из « Human Cytokine / Chemokine Panel I » (HCYTOMAG-60K), « Human Cytokine / Chemokine Panel II » (HCYP2MAG-62K) и « Human Th27 » (HTh27MAG-14K) ) панели) были использованы для оценки различных белков иммунного ответа.Несколько белковых маркеров были изучены в образцах сыворотки и слюны, включая интерферон (IFN) -γ и -α2, фактор некроза опухоли (TNF) -α и -β, IL-1α, IL-1β, IL-2, IL-3, IL-7, IL-12p40, IL-12p70, IL-15, IL-16, IL-17A, IL-17F, IL-21, IL-22, IL-23, IL-32, IL-1Ra, IL-4 , IL-5, IL-9, IL-10, IL-13, IL-6, IL-27, IL-33, растворимая форма лиганда CD40 (sCD40L), трансформирующий фактор роста (TGF) -α, IL -8 (CXCL-8), привлекающий В-клетки хемокин 1 (BCA-1 или CXCL-13), эотаксин (CCL-11), фактор роста фибробластов-2 (FGF-2), FMS-родственный лиганд тирозинкиназы 3 ( FLT-3L), фракталкин (CX3CL1), GRO (CXCL1), интерферон-индуцируемый белок 10 (IP-10 или CXCL-10), хемоаттрактантный белок моноцитов 1 (MCP-1 или CCL-2) и 3 (MCP-3 или CCL-7), хемокин, полученный из макрофагов (MDC или CCL-22), воспалительный белок макрофагов (MIP) -α и -β (или CCL-3 и CCL-4, соответственно), RANTES (CCL5), эпидермальный фактор роста ( EGF), гранулоцитарно-колониестимулирующий фактор (G-CSF), гранулоцит-макрофагальный колониестимулирующий фактор (GM-CSF ), Фактор роста тромбоцитов (PDGF) -AA и -AB / BB и фактор роста эндотелия сосудов (VEGF).Образцы сыворотки использовали без дополнительных разведений после оттаивания, а образцы слюны разбавляли на 1/2 стерильным PBS. Образцы сыворотки и слюны оценивали на отдельных планшетах. Образцы из всех трех групп были помещены в один планшет. Образцы анализировали с помощью устройства MagPix (Luminex; Остин, Техас, США) с программным обеспечением xPonent 4.2. Образцы контроля качества для всех аналитов находились в ожидаемом диапазоне. Калибровочная кривая была построена на основе концентрации и средней интенсивности флуоресценции стандартов, которые использовались для расчета концентрации каждого образца.
Статистический анализ
Различия между группами оценивали с помощью теста Краскела-Уоллиса для выявления общих различий между тремя группами (NoTBI, LTBI и TB), а затем с помощью теста Данна, скорректированного для множественных сравнений. Различия со значением p ≤ 0,05 считались достоверными. Диагностическая точность маркеров со значительными различиями между группами оценивалась с помощью анализа кривой характеристик оператора приемника (ROC). Пороговые значения для каждого параметра определялись по наивысшему индексу Юдена [24], чтобы максимизировать чувствительность и специфичность теста.Отдельные маркеры с площадью под кривой ROC (AUC)> 0,7 использовали для изучения возможностей классификации комбинаций маркеров. Для расчета прогнозируемой вероятности комбинированных биомаркеров для различения между каждыми двумя группами применялась бинарная логистическая регрессия. Прогнозируемая вероятность была использована для построения кривых ROC и расчета AUC. Диагностическая эффективность комбинаций маркеров и отдельных маркеров сравнивалась на основании различий соответствующих AUC с использованием метода Делонга.Статистический анализ и представление графиков были выполнены с использованием GraphPad Prism версии 6.00 для Windows (GraphPad Software; Калифорния, США), IBM SPSS версии 23 для Windows (SPSS Inc., Чикаго, Иллинойс, США) и бесплатного программного обеспечения R (версия 3.4. 3).
Результаты
Всего было набрано 97 пациентов: 28 микробиологически подтвержденных больных активным ТБ, 42 неинфицированных контакта и 27 контактов с ЛТИ. В таблице 1 приведены данные об участниках исследования в отношении возраста, пола и предыдущей вакцинации БЦЖ с более высокой долей мужчин, особенно в группе больных туберкулезом.
Скрининг маркеров хозяина в образцах сыворотки
Первоначальный скрининг был проведен с анализом концентрации 46 различных белков в сыворотке 49 участников из трех групп. Среди них 18 маркеров (IL-21, IL-27, BCA-1, EGF, FGF-2, Eotaxin, TGFγ, IFNγ, GRO, MDC, IL-17A, IL-8, IP-10, MCP-1, MIP -1γ, MIP-1β, TNFγ и VEGF) были обнаружены в 90–100% образцов, два белка были обнаружены в 70–90% образцов (GM-CSF и IL-7), пять – в 60–70% образцов. из них (IL-17, G-CSF, IL-1Ra, IL-1β и IL-6), а остальные были ниже минимально обнаруживаемого уровня более чем в половине образцов, поэтому они не рассматривались для дальнейшего анализа.Среди тех, у которых уровни обнаруживались в большинстве образцов, мы применили тест Краскела-Уоллиса, и только шесть (IL-6, IL-7, IP-10, TGFα, TNFα и BCA-1) показали достоверные (p <0,05) различия. между группами или тренд (p <0,1), предполагающий различное распределение. Затем эти кандидаты в маркеры были проанализированы у остальных участников, и были дополнительно изучены различия между группами.
Индивидуальные маркеры хозяина в сыворотке
Исходная концентрация выбранных цитокинов, включая IL-6, IL-7, IP-10, TGFα, TNFα и BCA-1, показала более высокие концентрации в сыворотке от пациентов с активным ТБ, чем у их неинфицированных контактов ( p значения в диапазоне от 0 .05–0,0001) и, в случае IP-10, TGFα и BCA-1, также по сравнению с контактами с LTBI (p <0,05 –p <0,01). Не было обнаружено значительных различий между двумя контактными группами, за исключением TNFα, где контакты LTBI показали значительно более высокую концентрацию этого цитокина, чем в контактах NoTBI (p <0,005) (рис. 1, таблица 2 и таблица S1). Во всех случаях у больных ТБ наблюдались более высокие концентрации исследуемых цитокинов, но у лиц, контактировавших с ЛТИ, наблюдались промежуточные уровни между неинфицированными контактами и больными ТБ.
Рис. 1. Концентрация белковых маркеров, обнаруженных в образцах сыворотки крови.
Горизонтальные полосы представляют собой медианное значение и межквартильный размах. Различия между исследуемыми группами рассчитывались с использованием теста Краскела-Уоллиса, за которым следовал тест Данна с поправкой на множественные сравнения. Значимые различия между группами выражаются как: * p <0,05; ** р <0,01; *** p <0,001; **** p <0,0001.
https://doi.org/10.1371/journal.pone.0235859.g001
Анализ кривой ROC был проведен для оценки диагностической точности отдельных маркеров хозяина, выполняющих попарные сравнения. Этот анализ показал, что шесть маркеров дают многообещающие результаты (AUC> 0,7), дифференцируя контакты с активным ТБ и NoTBI, причем TNFα, IL-7 и IP-10 обладают наилучшей дискриминационной способностью (таблица S1).
Для различения пациентов с ЛТИ и активным ТБ тремя лучшими белковыми маркерами были IL-7, IP-10 и BCA-1, тогда как для контактов NoTBI и LTBI только TNFα показал значительные статистические различия (таблица S1).
Комбинация маркеров хозяина в сыворотке
Эти индивидуальные маркеры хозяев, которые показали значительные различия между группами, были дополнительно исследованы с использованием различных комбинаций на основе бинарной логистической регрессии. Лучшая комбинация с использованием минимального количества маркеров была выбрана с помощью пошагового выбора в обратном направлении. Для различения контактов активного туберкулеза и контактов NoTBI комбинация с наивысшей AUC (0,87) и точностью (80,1%) составила IP10 + IL7 (таблица 3), что продемонстрировало лучшую эффективность, чем отдельные цитокины, хотя и без значительных различий (таблица S1. ) были найдены (Z = 1.0926, p- значение = 0,2746 и Z = 1,5859, p- значение = 0,1128 соответственно). Включение TNFα и / или TGFα (оба с AUC> 0,8) не улучшило комбинацию IP10 + IL17.
Для различения между ЛТИ и пациентами с активной формой ТБ три маркера IP-10, BCA-1 и IL-7, которые по отдельности показали хорошие результаты, были объединены с использованием логистической регрессии. Комбинация IP10 + BCA-1 (два с наивысшей AUC) показала AUC 0,83 со специфичностью 88% и чувствительностью 72% (таблица 3).Эта комбинация также показала лучшую производительность, чем только эти два маркера. Однако добавление ИЛ-7 не улучшило результатов.
В случае сравнения контактов NoTBI и LTBI мы обнаружили только различия в уровне TNFα (таблица 3 и таблица S1), поэтому комбинации с другими цитокинами не изучались.
Таким образом, исследование в сыворотке всего 4 цитокинов: IP-10, IL-7, BCA-1 и TNFα могло бы помочь идентифицировать три популяции TB. Повышение уровней IP-10 + IL-7 позволит различать активный ТБ и NoTBI; IP-10 + BCA-1 от активных контактов TB и LTBI и только TNFα для различения контактов NoTBI и LTBI.
Скрининг маркеров хозяина в образцах слюны
Первоначальный скрининг потенциальных маркеров хозяина в образцах слюны был проведен с анализом 44 различных белков у 66 участников. Шесть из 44 кандидатов (ИЛ-23, ИЛ-33, ИЛ-15, ИЛ-17A, ИЛ-2 и ИЛ-3) не были обнаружены во всех образцах, а шесть (Эотаксин, ИЛ-4, ИЛ-5, ИЛ -9, sCD40L и TNF-β) были обнаружены только в <15% образцов слюны. Все они были исключены для дальнейшего анализа. С другой стороны, 18 белковых маркеров (EGF, Fractalkine, GMCSF, GRO, GCSF, IL-1α, IL-1β, IL-1Ra, IL-7, IL-8, IFN-α2, MCP-1, MDC, PDGF -AA, PDGF-AB / BB, TGF-α, TNF-α и VEGF) были выше минимально детектируемого уровня в> 90% образцов; Девять (IL-16, FGF-2, FLT-3L, IL-13, IL-6, IL-9, IFN-γ, IP-10 и MIP-α) были обнаружены в 70–90% проб и шести (IL-10, IL-12p40, IL-12p70, MCP-3, MIP-β и RANTES) обнаруживали уровни в 50–70% образцов.Из них тринадцать маркеров (IL-16, EGF, Fractalkine, GRO, IL-12p40, IL-1α, IL-6, IFN-α2, IP-10, MCP-1, MIP-alpha, TGF-α, VEGF) показали достоверные различия между группами (р <0,05) при применении теста Краскела-Уоллиса. Они были отобраны для дальнейшего анализа с использованием оставшихся образцов слюны.
Индивидуальные маркеры хозяина в слюне
Тринадцать кандидатов в маркеры, отобранные в образцах слюны (см. Материалы и методы), были изучены в общей сложности у 89 участников из трех групп (34 NoTBI, 27 LTBI и 28 TB).Этот анализ показал, что в целом эти белковые маркеры присутствовали в более высоких концентрациях в слюне больных туберкулезом в активной форме, за исключением IL-12p40 и IL-1α, которых было больше в слюне контактов NoTBI (Таблица 4, Рис 2). . В большинстве случаев контакты с ЛТИ показали промежуточный уровень между пациентами с ЛТИ и туберкулезом.
Рис. 2. Концентрация белковых маркеров, обнаруженных в образцах слюны.
Горизонтальные полосы представляют собой медианное значение и межквартильный размах. Различия между исследуемыми группами рассчитывались с использованием теста Краскела-Уоллиса, за которым следовал тест Данна с поправкой на множественные сравнения.Значимые различия между группами выражаются как: * p <0,05; ** р <0,01; *** p <0,001; **** p <0,0001 и нс: достоверных различий нет.
https://doi.org/10.1371/journal.pone.0235859.g002
Наибольшие различия были обнаружены между контактами с активным ТБ и NoTBI с большинством маркеров (TGF-α, Fractalkine, IFN-α2, GRO, IL -6, IP-10, MCP-1, MIP-1a и VEGF), показывающие значительные различия ( p <0,05 - p <0.0001) между этими двумя группами, за исключением IL-12p40, который показал достоверные различия только между NoTBI и LTBI ( p <0,05), и IL-16 и EGF, которые не показали значимых различий между группами. Кроме того, IFN-α2 ( p <0,05), IP-10 ( p <0,001) и VEGF ( p <0,05) были значительно выше при активном ТБ по сравнению с контактами с LTBI, а фракталкин также был значительно выше ( p <0,05) в LTBI, чем в контактах NoTBI (рис.2).
Дискриминационная способность каждого маркера со значительными различиями между группами оценивалась с помощью ROC-анализа (таблица S2). Самым многообещающим маркером хозяина для различения активного TB и NoTBI в слюне был фракталкин с AUC 0,87, чувствительностью 78,57% и специфичностью 81,25% при выбранном пороге (таблица S2). Другими маркерами с хорошей производительностью (AUC> 0,7) были GRO, IL-1α, IP-10, MCP-1, MIP-1α и VEGF (таблица S2).
Что касается маркеров, которые могли различать ЛТИ и активный ТБ, мы обнаружили, что IFN-α2 и IP-10 были наиболее многообещающими (таблица S2).Значения чувствительности и специфичности составили от 58,62% до 80,77%, что свидетельствует о несколько худших характеристиках, чем маркеры из образцов сыворотки. Наконец, фракталкин (AUC = 0,73; 69,2% чувствительности и 75% специфичности) и IL-12p40 (AUC = 0,73; 74,1% чувствительности и 72% специфичности) показали лучшую эффективность при различении контактов NoTBI и LTBI (таблица S2).
Комбинация маркеров хозяина в слюне
Изученокомбинаций индивидуальных маркеров-кандидатов в слюне, в том числе с индивидуальной AUC> 0.7. Маркеры-кандидаты были включены в модели логистической регрессии для оценки эффективности их классификации. Для различения активного ТБ и NoTBI была выбрана комбинация фракталкин + IP10 + IL1α + VEGF с использованием подхода обратной элиминации, который показал AUC 0,88 (83,61% точно классифицированных образцов, 91,2% специфичности и 74% чувствительности) (Таблица 5 ). Комбинация продемонстрировала значительно лучшие характеристики, чем индивидуальный IP-10 (Z = 1,9167, p -значение = 0.05), IL1α (Z = 2,1925, p -значение = 0,02834) или VEGF (Z = 6,6681, p -значение = 2,591e-11), и, несмотря на различия с фракталкином, не были значимыми (Z = 1,1516, p -value = 0,2495), он действительно показал более высокую AUC, чем только этот хемокин.
Были оценены две различные комбинации для различения ЛТИ и активного ТБ. Во-первых, мы попытались объединить кандидатов с наивысшими индивидуальными показателями (IP-10 и IFNα2), которые показали AUC 0,67 (59.Точность 6%, специфичность 68% и чувствительность 51,9%). Вторая комбинация была оценена с использованием метода обратного исключения. Выбранная комбинация (GRO + IL6 + IP-10 + MIP1α) показала лучшие характеристики с AUC 0,77. Однако различия между кривыми ROC этих двух комбинаций существенно не различались и не улучшали индивидуальную эффективность IP-10 и IFNα2 (таблица 5).
Наконец, была оценена комбинация маркеров для различения контактов NoTBI и LTBI, объединяющая фракталкин и IL-12p40 (таблица 5).Эта комбинация показала лучшую эффективность, чем только два маркера, с AUC 0,83 и кривой ROC, значительно лучше, чем у фракталкина (Z = 2,7566, p -значение = 0,005841), и улучшенную тенденцию по сравнению с одним IL-12p40. (Z = 1,6817, p -значение = 0,09262).
Таким образом, различные маркеры в слюне показали многообещающие результаты: фракталкин + IP10 + IL1α + VEGF различают контакты активного ТБ и контактов NoTBI; Фракталкин + IL-12p40 отличает LTBI от контактов NoTBI.С другой стороны, различение между LTBI и TB с использованием комбинации маркеров не улучшило эффективность индивидуального IP-10 или IFNα2.
Обсуждение
Новые инструменты для быстрой и точной диагностики туберкулеза необходимы, чтобы идентифицировать всех Mtb инфицированных людей и дифференцировать активную и латентную туберкулезную инфекцию. Образцы слюны и сыворотки, которые относительно легко получить, являются идеальными образцами для идентификации потенциальных биомаркеров, которые могут быть использованы для разработки необходимых диагностических инструментов.В нашей работе мы проанализировали до 50 различных маркеров в сыворотке и слюне и идентифицировали шесть маркеров в сыворотке (IL-6, IL-7, IP-10, TGFα, TNFα и BCA-1) и девять в слюне (Fractalkine, GRO , IL-1α, IP-10, MCP-1, MIP-1α, VEGF, IFNα2 и IL-12p40), которые показали многообещающий потенциал для этой цели.
Как мы показали здесь, маркеры хозяина, которые лучше всего определяют сигнатуру сыворотки или слюны, различны для каждого образца, даже несмотря на то, что первоначальный скрининг включал почти одинаковый набор маркеров.Эти результаты свидетельствуют о различном составе сыворотки и слюны. Хотя в состав слюны могут входить компоненты, полученные из крови, эти аналиты обычно имеют разные концентрации в обеих жидкостях [25]. Это объясняет, почему в нашей работе некоторые белки могут быть многообещающими биомаркерами в одном образце (например, фракталкин в слюне) и все же быть ниже минимально определяемой концентрации в большой части образцов сыворотки. Фактически, предыдущие исследования по сравнению образцов сыворотки и слюны в контексте инфекции ТБ [14,16] показали разные концентрации одних и тех же белков хозяина в обоих образцах.Это поддерживает подход, использованный в настоящем исследовании, где независимый анализ и выбор маркеров были сделаны для сыворотки и слюны.
Среди кандидатов-хозяев, идентифицированных в образцах сыворотки, IP-10 обладал наилучшими характеристиками, дифференцируя активных больных ТБ от неинфицированных и контактировавших с ЛТИ, что подтверждается его площадью под кривой ROC. Эти результаты подтверждают исследования, проведенные другими группами [26–30], подтверждающие пригодность этого маркера для диагностики туберкулеза. В отличие от диагностических тестов на ТБ, основанных на концентрациях IFNγ (IGRA), которые требуют инкубационного периода с антигенами Mtb , в наших и других исследованиях [26,31–33] было показано, что IP-10 увеличивается в сыворотке, плазма и моча больных ТБ без дополнительной стимуляции.Следует отметить, что в нашей работе IFNγ был отклонен для дальнейшего анализа в предварительном скрининге, поскольку он не показал значимых различий между группами. Это указывает на низкую применимость IFNγ в качестве биомаркера туберкулеза без предшествующей стимуляции in vitro .
Более того, мы показали, что точность IP-10 как индивидуального биомаркера может быть улучшена в сочетании с IL-7 для различения активных контактов TB и NoTBI или в сочетании с BCA-1 для дифференциации активного TB и LTBI. Хотя в предыдущих исследованиях анализировался ряд биомаркеров в образцах сыворотки или плазмы для диагностики ТБ [10–16], ни одно из них ранее не предлагало IL-7 или BCA-1 в качестве потенциальных биомаркеров.Наши результаты показывают, что их можно не только использовать в сочетании с IP-10, но они показали хорошую эффективность, дифференцирующую активный ТБ от контактов как с NoTBI, так и с LTBI, при индивидуальном использовании на основе их соответствующих AUC.
С биологической точки зрения, более высокая концентрация IP-10 и BCA-1 в образцах сыворотки от больных активной формой туберкулеза может быть связана с миграцией иммунных клеток в очаг инфекции. IP-10 и BCA-1 представляют собой два хемокина с хемоаттрактантными свойствами по сравнению с клетками, экспрессирующими рецептор CXCR3 [34,35], которые включают клетки Th2, одного из основных участников клеточного иммунитета против M . туберкулез инфекция [36]. IL-7, с другой стороны, был связан с усиленными ответами воспоминаний Mtb -специфических CD4 + Т-клеток in vitro [37], что предполагает защитную роль. Однако другие исследования описали снижение чувствительности Т-клеток к ИЛ-7, снижение растворимого и мембраносвязанного рецептора ИЛ-7 и повышение концентрации ИЛ-7 в плазме при ТБ [38]. Это указывает на то, что более высокие уровни IL-7 не обязательно означают защиту у пациентов с активным туберкулезом, хотя его можно использовать в качестве потенциального биомаркера туберкулеза.
Другие индивидуальные сывороточные маркеры, идентифицированные в нашей работе, включали IL-6 и TGFα, оба из которых показали хорошую эффективность дифференцирования активного туберкулеза от неинфицированных контактов. Наши результаты согласуются с предыдущими исследованиями [12–14,16], в которых сообщалось о диагностическом потенциале IL-6, что указывает на устойчивость этого биомаркера в различных географических условиях. Однако мы не нашли в литературе предыдущих упоминаний о TGFα как о потенциальном биомаркере туберкулеза, что позволяет предположить, что для изучения этого нового кандидата необходимы дальнейшие исследования.
Также стоит упомянуть, что один из включенных в наше исследование маркеров, TNFα, показал хорошую способность дифференцировать неинфицированные контакты и контакты с ЛТИ. Это открытие представляет особый интерес, поскольку дифференциация между здоровыми людьми с латентной инфекцией или без нее обычно возможна только после антиген-специфической активации. TNFα является критическим цитокином для образования и поддержания гранулемы, играя важную роль в контроле инфекции Mtb [39]. Это могло бы объяснить, почему у пациентов с латентной инфекцией уровень TNFα выше, чем у неинфицированных контактов.
Что касается сигнатуры маркера, обнаруженной в слюне, фракталкин оказался индивидуальным маркером с лучшей производительностью, позволяющей дифференцировать контакты с активным туберкулезом и контактами с NoTBI. Более высокая концентрация фракталкина в слюне больных туберкулезом была также обнаружена Phalane et al. . [16], подтверждающие наши результаты. Кроме того, наша работа также предоставляет информацию о более высокой концентрации этого хемокина в контактах с ЛТИ и о хороших показателях дифференциации ЛТБИ от неинфицированных контактов. Эти данные указывают на интерес к этому хемокину и его потенциальную роль в качестве биомаркера туберкулеза слюны.
Наше исследование показало, что различение между активным туберкулезом и контактами NoTBI можно проводить с использованием одного фракталкина или в комбинации с IP-10, IL-1α и VEGF, что обеспечивает более высокую чувствительность и специфичность, чем любой из маркеров по отдельности. Три из этих кандидатов, IP-10, фракталкин и VEGF, были обнаружены в более высоких концентрациях в слюне пациентов с активным туберкулезом, в то время как IL-1α был более распространен у пациентов с NoTBI. Более высокая концентрация IP-10 может быть связана с активной миграцией клеток, как обсуждалось выше, что также может отражаться на слюне.В случае фракталкина и VEGF мы полагаем, что существует связь между их более высокой концентрацией в слюне больных туберкулезом в активной форме и повышенным уровнем этих хемокинов в клетках легких [40], бронхоальвеолярным лаважем [41] и плевральными выпотами [42], о которых ранее сообщалось. у больных туберкулезом легких. Эти наблюдения предполагают, что биомаркеры, обнаруженные в слюне, могут отражать события, происходящие в легких.
И фракталкин, и VEGF экспрессируются эндотелиальными клетками, опосредуя хемоаттракцию и адгезию лимфоцитов в тканях слизистой оболочки [43] и способствуя образованию новых кровеносных сосудов [44], соответственно.Хотя роль этих белков во время инфекции ТБ не установлена, предыдущие исследования на животных моделях показали, что фракталкин может опосредовать клеточную инфекцию и распространение бацилл Mtb [45], а VEGF был предложен как механизм распространения Mtb [45]. 46]. Все это говорит о том, что эндотелиальные клетки влияют на маркеры, обнаруживаемые в слюне, и могут быть косвенно связаны с распространением Mtb у пациентов с активным туберкулезом.
Помимо тех, что включены в панель с четырьмя маркерами, в слюне были обнаружены другие индивидуальные маркеры-кандидаты, которые могли различать контакты с активным туберкулезом и контактами с NoTBI.К ним относятся GRO, MCP-1 и MIP-1α, три хемокина, которые, как известно, участвуют в рекрутинге нейтрофилов [47] и в опосредованном нейтрофилами иммунном ответе против инфекции Mtb [48]. Кроме того, существуют доказательства того, что GRO может быть связан с патогенезом туберкулеза в легких [49]; MCP-1 в большей степени продуцируется моноцитами пациентов с активным туберкулезом и здоровых людей [50], и MIP-1α, как было установлено, вносит вклад в врожденный иммунный ответ на M . туберкулез инфекция [51].Все эти свидетельства предполагают, что маркеры, обнаруженные в образцах слюны, могут отражать врожденные механизмы, запущенные против инфекции Mtb .
Наше исследование также показало, что распознавание лиц, контактировавших с ЛТИ и больных туберкулезом в активной форме, с использованием слюны возможно с помощью IP-10 или IFNα2. Насколько нам известно, это первый случай, когда IFNα2 предлагается в качестве потенциального биомаркера для различения активной и латентной инфекции ТБ в образцах слюны. С другой стороны, для различения неинфицированных контактов и контактов с LTBI наиболее многообещающим кандидатом был IL-12p40.
IL-12p40 и уже упомянутый IL-1α были единственными цитокинами, идентифицированными в нашем исследовании, которые показали более высокие концентрации в контактах NoTBI. Более высокие концентрации этих маркеров в неинфицированных контактах могут коррелировать с исследованиями, предполагающими их роль в защите от инфекции Mtb на первых стадиях заболевания [52–55].
Одним из ограничений нашего исследования является относительно небольшой размер выборки. Тем не менее, это было запланировано как исследование открытия, чтобы предоставить новые кандидаты в маркеры, которые могут быть дополнительно оценены в будущих работах.Поэтому мы установили приоритет качества когорты исследования, выбрав только тех пациентов и контактных лиц без каких-либо условий, которые могут повлиять на сигнатуру иммунного ответа. Следовательно, можно без помех проводить эффективный анализ иммунных ответов. С помощью текущего анализа мы предоставили подтверждение предыдущих результатов, таких как большой потенциал IP-10 не только в образцах крови, но и в слюне, а также мы предоставили данные, подтверждающие потенциал IL-6 и фракталкина в качестве сыворотки. и биомаркеры слюны соответственно.Что еще более важно, мы предлагаем новых кандидатов для использования в сыворотке (TGFα, IL-7) или слюне (MIP1α, VEGF, GRO, MCP-1) для дифференциации различных исследуемых групп ТБ и комбинаций биомаркеров с многообещающей дискриминационной способностью, которая может установить основу для тестов в местах оказания медицинской помощи на доступных платформах.
Комбинации маркеров, предложенные для его использования в образцах сыворотки, включали IP-10 + IL-7 или / и IP-10 + BCA-1 для различения между активными больными ТБ и неинфицированными и латентно инфицированными контактами, соответственно.Что касается комбинаций маркеров, предлагаемых для его использования в слюне, фракталкин + IP-10 + IL-1α + VEGF может отличать активный ТБ от контактов NoTBI. Наконец, исследование фракталкин + IL-12p40 может различать неинфицированные контакты и контакты с ЛТИ, что представляет особый интерес, учитывая, что до сих пор никакие другие методы, кроме туберкулиновой кожной пробы или тестов высвобождения гамма-интерферона (IGRA), не могли различить эти контакты. две популяции.
Благодарности
Мы хотели бы поблагодарить специализированный персонал «Complexo Hospitalario Universitario de Pontevedra» (SERGAS) за сбор и обработку образцов, а также всех больных туберкулезом и их семейных контактов за участие в настоящем исследовании и их альтруистическое донорство образцов крови и слюны.Мы также благодарим Альберто Лема за его советы по анализу статистики и всех членов группы иммунологии за их помощь и поддержку.
Ссылки
- 1. Всемирная организация здоровья. Global Tuberculosis Report 2019. 2019. Recuperado: https://www.who.int/tb/publications/global_report/en/
- 2. Дэвис PDO, Пай М. Диагностика и неправильный диагноз туберкулеза. Int J Tuberc Lung Dis. 2008; 12: 1226–1234. Современная серия. Туберкулез. Отредактировал И.Д. Русен.pmid: 182
- 3. Беме С.К., Набета П., Хиллеманн Д., Николь М.П., Шенай С., Крапп Ф. и др. Быстрая молекулярная диагностика туберкулеза и устойчивости к рифампицину. N Engl J Med. 2010; 363: 1005–1015. pmid: 20825313
- 4. Требук А., Энарсон Д.А., Чанг С.Й., Ван Дын А., Харрис А.Д., Бойло Ф. и др. Xpert® MTB / RIF для национальных программ борьбы с туберкулезом в странах с низким уровнем дохода: когда, где и как? Int J Tuberc Lung Dis. 2011; 15: 1567–1571. pmid: 22005110
- 5.Йонг Ю.К., Тан Х.Й., Саиди А., Вонг В.Ф., Виньеш Р., Велу В. и др. Иммунные биомаркеры для диагностики и мониторинга лечения туберкулеза: текущие разработки и перспективы на будущее. Границы микробиологии. Frontiers Media S.A .; 2019; 10: 2789. pmid: 31
4 1- 6. Пай М., Сотгиу Г. Диагностика латентной инфекции ТБ: постепенный, а не преобразующий прогресс. Eur Respir J. 2016; 47: 704–706. pmid: 26
- 7. Tuck MK, Chan DW, Chia D, Godwin AK, Grizzle WE, Krueger KE и др.Стандартные рабочие процедуры для сбора сыворотки и плазмы: Рабочая группа по интеграции стандартных рабочих процедур, согласованное заявление сети исследований раннего обнаружения. J Proteome Res. 2009. 8: 113–117. pmid: 145
- 8. Нуньес ЛАС, Муссавира С, Биндху О.С. Клиническая и диагностическая ценность слюны как неинвазивной диагностической жидкости: систематический обзор. Biochemia Medica. Биохимия Медика, редакция; 2015; 25 (2): 177–192. pmid: 26110030
- 9. Малати Н., Мифили С., Васанти HR.Диагностика слюны: краткий обзор. ISRN Dent. 2014; 2014: 158786. pmid: 24616813
- 10. Чен Т, Ли З, Ю Л, Ли Х, Лин Дж, Го Х и др. Профилирование иммунного ответа человека на Mycobacterium tuberculosis с помощью массива цитокинов человека. Туберкулез. 2016; 97: 108–117. pmid: 26980502
- 11. Михрет А., Бекеле Ю., Бобоша К., Кидд М., Асеффа А., Хоу Р. и др. Плазменные цитокины и хемокины различают активное заболевание и неактивную туберкулезную инфекцию. J Infect.2013; 66: 357–365. pmid: 23178506
- 12. Равиндран Р., Кришнан В. В., Ханум А., Люцив П. А., Хан И. Х. Изучение профилей иммуномодуляторов плазмы и антител у больных туберкулезом. Clin Vaccine Immunol. 2013; 20: 1283–1290. pmid: 23761664
- 13. Фарр К., Равиндран Р., Стрнад Л., Чанг Э., Чейссон Л. Х., Юн С. и др. Диагностические характеристики маркеров воспаления крови для скрининга на туберкулез у людей, живущих с ВИЧ. Ивани Дж., Редактор. PLoS One.2018; 13: e0206119. pmid: 30352099
- 14. Намуганга А.Р., Чегу Н.Н., Мубири П., Вальцл Г., Майянджа-Кизза Х. Пригодность слюны для диагностики туберкулеза: сравнение с сывороткой. BMC Infect Dis. 2017; 17 (1): 600. pmid: 28859607
- 15. Hur YG, Kang YA, Jang SH, Hong JY, Kim A, Lee SA и др. Дополнительные биомаркеры для улучшения диагностики туберкулеза и контроля терапевтических эффектов. J Infect. 2015; 70: 346–355. pmid: 25452040
- 16. Phalane KG, Kriel M, Loxton AG, Menezes A, Stanley K, van der Spuy GD, Дифференциальная экспрессия биомаркеров хозяина в образцах слюны и сыворотки от людей с подозрением на туберкулез легких.Медиаторы Inflamm. 2013; 2013: 981984. pmid: 24327799
- 17. Матеос Дж., Эстевес О., Гонсалес-Фернандес А., Анибарро Л., Палларес А., Релхич Р. и др. Протеомика сыворотки больных активным туберкулезом и контактных лиц выявляет уникальные процессы, активируемые при инфицировании Mycobacterium tuberculosis. Sci Rep. 2020; 10: 1–12.
- 18. Агранофф Д., Фернандес-Рейес Д., Пападопулос М.С., Рохас С.А., Гербстер М., Лусмор А. и др. Идентификация диагностических маркеров туберкулеза с помощью протеомного дактилоскопирования сыворотки.Ланцет. 2006; 368: 1012–1021. pmid: 16980117
- 19. Ван С., Ли И, Шен Й, Ву Дж, Гао И, Чжан С. и др. Скрининг и идентификация биосигнатуры из шести цитокинов для выявления туберкулезной инфекции и отличия активного туберкулеза от латентного. J Transl Med. 2018; 16: 1–13.
- 20. Джейкобс Р., Чехла Э., Малхерб С., Криэль М., Локстон А.Г., Стэнли К. и др. Биомаркеры хозяина, обнаруженные в слюне, являются многообещающими маркерами для диагностики туберкулеза легких и мониторинга реакции на лечение туберкулеза.Цитокин. 2016; 81: 50–56. pmid: 26878648
- 21. Джейкобс Р., Маасдорп Э., Малхерб С., Локстон А.Г., Стэнли К., ван дер Спуй Г. и др. Диагностический потенциал новых биомаркеров слюнных хозяев как кандидатов для иммунологической диагностики туберкулеза и мониторинга ответа на лечение туберкулеза. PLoS One. 2016; 11: e0160546. pmid: 27487181
- 22. Гонсалес-Мартин Дж., Гарсия-Гарсия Дж. М., Анибарро Л., Видал Р., Эстебан Дж., Бланкер Р. и др. Documento de Consunso Sobre Diagnóstico, Tratamiento y Prevention de la tuberculosis.Enferm Infecc Microbiol Clin. 2010; 28: 297.e1–297.e20. pmid: 20435388
- 23. Anibarro L, Trigo M, Villaverde C, Pena A, Cortizo S, Sande D и др. Анализ высвобождения интерферона-γ у лиц, контактировавших с туберкулезом: есть ли период окна? Eur Respir J. 2011; 37: 215–217. pmid: 21205718
- 24. Fluss R, Faraggi D, Reiser B. Оценка индекса Юдена и связанной с ним точки отсечения. Биометрический журнал, 2005; 47: 458–472. pmid: 16161804
- 25.
Йошизава Дж. М., Шафер Калифорния, Шафер Дж. Дж., Фаррелл Дж. Дж., Пастер Б. Дж., Вонг DTW.Биомаркеры слюны: к будущим клиническим и диагностическим утилитам. Clin Microbiol Rev.2013; 26: 781–791. pmid: 240
- 26. Вергеланд I, Пуллар Н., Ассмус Дж., Уеланд Т., Тонби К., Феруглио С. и др. IP-10 различает активный и латентный туберкулез вне зависимости от ВИЧ-статуса и его снижение во время терапии. J Infect. 2015; 70: 381–391. pmid: 25597826
- 27. Замбузи Ф.А., Кардосо-Силва П.М., Эспиндола М.С., Соарес Л.С., Гальвао-Лима Л.Дж., Брауэр В.С. и др.Выявление перспективных иммунных биомаркеров плазмы для дифференциации активного туберкулеза легких. Цитокин. 2016; 88: 99–107. pmid: 275
- 28. Xiong W., Dong H, Wang J, Zou X, Wen Q, Luo W. и др. Анализ профилей цитокинов и хемокинов в плазме у пациентов с туберкулезом и без него с помощью мультиплексных иммуноанализов на основе жидких матриц. Уилкинсон К.А., редактор. PLoS One. 2016; 11: e0148885. pmid: 26881918
- 29. Ruhwald M, Aabye MG, Ravn P. Анализы высвобождения IP-10 в диагностике туберкулезной инфекции: текущее состояние и будущие направления.Эксперт Rev Mol Diagn. 2012; 12: 175–187. pmid: 22369377
- 30. Ruhwald M, Dominguez J, Latorre I, Losi M, Richeldi L, Pasticci MB, et al. Многоцентровая оценка точности и эффективности IP-10 для диагностики инфекции M. tuberculosis. Туберкулез. 2011; 91: 260–267. pmid: 21459676
- 31. Azzurri A, Sow OY, Amedei A, Bah B, Diallo S, Peri G и др. Уровни IFN-γ-индуцируемого белка 10 и пентраксина 3 в плазме являются инструментами для мониторинга воспаления и активности заболевания при инфекции Mycobacterium tuberculosis.Микробы заражают. 2005; 7: 1–8. pmid: 15716076
- 32. Ким СИ, Ким Дж., Ким Д.Р., Кан Я.А., Бонг С., Ли Дж. И др. Моча IP-10 как биомаркер терапевтического ответа у пациентов с активным туберкулезом легких. BMC Infect Dis. 2018; 18: 240. pmid: 29843631
- 33. Чжао Y, Ян X, Чжан X, Yu Q, Zhao P, Wang J и др. IP-10 и RANTES в качестве биомаркеров для диагностики и мониторинга туберкулеза легких. Туберкулез. 2018; 111: 45–53. pmid: 30029914
- 34.Лю М., Го С., Хибберт Дж. М., Джайн В., Сингх Н., Уилсон Н. О. и др. CXCL10 / IP-10 в патогенезе инфекционных заболеваний и потенциальное терапевтическое значение. Фактор роста цитокинов Ред. 2011; 22: 121–30. pmid: 21802343
- 35. Jenh C-H, Cox MA, Hipkin W., Lu T, Pugliese-Sivo C, Gonsiorek W. и др. Хемокин 1, привлекающий В-клетки человека (BCA-1; CXCL13), является агонистом рецептора CXCR3 человека. Цитокин. 2001; 15: 113–121. pmid: 11554781
- 36. Флинн Дж. Л., Чан Дж.Иммунология туберкулеза. Анну Рев Иммунол. 2001; 19: 93–129. pmid: 11244032
- 37. Терраццини Н., Мантегани П., Керн Ф., Фортис С., Мондино А., Казерта С. Интерлейкин-7 раскрывает патоген-специфические Т-клетки, усиливая ответы антиген-отзыва. J Infect Dis. 2018; 217: 1997–2007. pmid: 29506153
- 38. Lundtoft C, Afum-Adjei Awuah A, Rimpler J, Harling K, Nausch N, Kohns M, et al. Аберрантные уровни IL-7 и растворимого рецептора IL-7 в плазме указывают на нарушение Т-клеточного ответа на IL-7 при туберкулезе человека.PLoS Pathog. 2017; 13: e1006425. pmid: 28582466
- 39. Лин П.Л., Плесснер Х.Л., Войтенок Н.Н., Флинн Ж.Л. Фактор некроза опухоли и туберкулез. J Investigate Dermatology Symp Proc. 2007; 12: 22–25. pmid: 17502865
- 40. Стэнтон Л.А., Фенхоллс Дж., Лукас А., Гоф П., Гривз Д.Р., Махони Дж. А. и др. Иммунофенотипирование макрофагов при туберкулезе легких и саркоидозе человека. Int J Exp Pathol. 2004. 84: 289–304. pmid: 14748748
- 41. Лешо Э., Форестьеро Ф. Дж., Хирата М. Х., Хирата Р. Д., Секон Л., Мело Ф. Ф. и др.Транскрипционные ответы клеток периферической крови хозяина на туберкулезную инфекцию. Туберкулез (Edinb). 2011; 91: 390–399. pmid: 21835698
- 42. Джин Х., Ли К., Джин С., Ли Ю. Фактор роста эндотелия сосудов коррелирует с матриксной металлопротеиназой-9 в плевральном выпоте. Respir Med. 2004. 98: 115–122. pmid: 14971873
- 43. Muehlhoefer A, Saubermann LJ, Gu X, Luedtke-Heckenkamp K, Xavier R, Blumberg RS и др. Фракталкин представляет собой хемоаттрактант эпителиальных и эндотелиальных клеток для интраэпителиальных лимфоцитов в слизистой оболочке тонкого кишечника.J Immunol. 2000; 164: 3368–3376. pmid: 10706732
- 44. Breier G, Albrecht U, Sterrer S, Risau W. Экспрессия фактора роста эндотелия сосудов во время эмбрионального ангиогенеза и дифференцировки эндотелиальных клеток. Разработка. 1992; 114: 521–532. pmid: 15
- 45. Хингли-Уилсон С.М., Коннелл Д., Поллок К., Хсу Т., Чилиан Э., Сайкс А. и др. ESX1-зависимый фракталкин опосредует хемотаксис и инфекцию Mycobacterium tuberculosis у людей. Туберкулез (Edinb).2014; 94: 262–270. pmid: 24631198
- 46. Polena H, Boudou F, Tilleul S, Dubois-Colas N, Lecointe C, Rakotosamimanana N и др. Mycobacterium tuberculosis использует образование новых кровеносных сосудов для своего распространения. Научный доклад 2016; 6: 33162. pmid: 27616470
- 47. Савант К. В., Полури К. М., Дутта А. К., Сепуру К. М., Трошкина А., Гарофало Р. П. и др. Хемокин CXCL1 опосредованный рекрутинг нейтрофилов: роль взаимодействий гликозаминогликанов. Научный доклад 2016; 6: 33123.pmid: 27625115
- 48. Хильда Дж. Н., Нарасимхан М., Дас С. Д.. Нейтрофилы больных туберкулезом легких демонстрируют повышенные уровни хемокинов MIP-1α, IL-8 и MCP-1, которые дополнительно повышаются при заражении in vitro штаммами микобактерий. Hum Immunol. 2014; 75: 914–922. pmid: 24994463
- 49. Niazi MKK, Dhulekar N, Schmidt D, Major S, Cooper R, Abeijon C и др. Некроз легких и нейтрофилы отражают общие пути восприимчивости к Mycobacterium tuberculosis у генетически разнообразных иммунокомпетентных мышей.Dis Model Mech. 2015; 8: 1141–1153. pmid: 26204894
- 50. Линь И, Гонг Дж, Чжан М, Сюэ В., Барнс П.Ф. Продукция моноцитарного хемоаттрактантного белка 1 у больных туберкулезом. Заражение иммунной. 1998; 66: 2319–2322. pmid: 9573123
- 51. Саукконен Дж. Дж., Базидло Б., Томас М., Стритер Р. М., Кин Дж., Корнфельд Х. Бета-хемокины индуцируются Mycobacterium tuberculosis и подавляют его рост. Заражение иммунной. 2002; 70: 1684–1693. pmid: 11895930
- 52. Bourigault M-L, Segueni N, Rose S, Court N, Vacher R, Vasseur V и др.Относительный вклад IL-1α, IL-1β и TNF в ответ хозяина на Mycobacterium tuberculosis и ослабленную BCG M. bovis. Иммунитет, Воспаление Dis. 2013; 1: 47–62. pmid: 25400917
- 53. Ямада Х., Мизумо С., Хораи Р., Ивакура Ю., Сугавара И. Защитная роль интерлейкина-1 при микобактериальной инфекции у мышей с двойным нокаутом IL-1 альфа / бета. Lab Invest. 2000. 80 (5): 759–767. pmid: 10830786
- 54. Hölscher C, Atkinson RA, Arendse B, Brown N, Myburgh E, Alber G и др.Защитная и агонистическая функция IL-12p40 при микобактериальной инфекции. J Immunol. 2001. 167 (12): 6957–6966. pmid: 11739515
- 55. Khader SA, Partida-Sanchez S, Bell G, Jelley-Gibbs DM, Swain S, Pearl JE и др. Интерлейкин 12p40 необходим для миграции дендритных клеток и праймирования Т-клеток после инфицирования Mycobacterium tuberculosis. J Exp Med. 2006; 203: 1805–1815. pmid: 16818672
Быстрая диагностика туберкулеза с использованием биомаркеров хозяина ex vivo в мокроте
Редактору:
Туберкулез продолжает оставаться серьезной проблемой общественного здравоохранения в развивающихся странах [1].Одним из препятствий на пути к снижению передачи туберкулеза является отсутствие точных безлабораторных диагностических тестов, которые можно было бы использовать в местах оказания медицинской помощи. Если мы хотим ликвидировать туберкулез, нам нужен надежный, недорогой и безопасный диагностический тест в месте оказания медицинской помощи, который, в свою очередь, требует идентификации соответствующих биомаркеров [2]. Экспресс-тесты, основанные на микрофлюидике (тесты с боковым потоком), открывают большие перспективы для диагностики туберкулеза. Они просты в использовании, дешевы, дают ответ в течение нескольких минут, не требуют специального оборудования и стабильны при комнатной температуре, что делает их идеальными для использования в условиях высокого бремени туберкулеза и ограниченных ресурсов.Однако на сегодняшний день такой тест на туберкулез не разработан из-за отсутствия чувствительности, связанной с маркерами и / или типом образца. Разработка тестов на основе биомаркеров хозяина требует оценки различных типов образцов [3] – [5] и маркеров, отличных от интерферона (IFN) -γ [5], для дифференциальной диагностики активного туберкулеза, латентной инфекции и других респираторных заболеваний. Ранее мы показали, что сочетание трех факторов хозяина в плевральной жидкости привело к 96% правильной классификации туберкулеза среди других респираторных заболеваний (ОРЗ) (включая бактериальную пневмонию) независимо от ВИЧ-статуса [6].Однако этот тип образца получить непросто, и поэтому мы хотели определить, можем ли мы использовать мокроту ex vivo , которая неинвазивна и ее легко получить у взрослых пациентов с туберкулезом легких.
Субъекты были последовательно набраны из амбулаторной клиники и отделения Совета медицинских исследований, Фаджара, Гамбия. Все испытуемые были взрослыми (≥18 лет) с симптомами, указывающими на туберкулез. Впоследствии субъекты были разделены на две группы: пациенты с подтвержденным посевом туберкулеза и пациенты с ОРЗ.75% больных туберкулезом и 50% пациентов из группы ORD были положительными по тесту IFN-γ QuantiFERON (Qiagen, Hilden, Германия). Одновременно были взяты образцы у одного и того же пациента. Сыворотку собирали с использованием сывороток Vacutainers (BD, Франклин Лейкс, Нью-Джерси, США) после центрифугирования, а слюну собирали с использованием метода пассивного слюноотделения. 1 мл свежей мокроты переваривали в течение 15 мин при комнатной температуре 0,1% дитиотреитолом. Добавляли равный объем PBS, образцы центрифугировали (600 × г в течение 5 минут), супернатанты собирали и хранили при -20 ° C.Неразбавленную гепаринизированную кровь (450 мкл на лунку) стимулировали очищенным производным белка (PPD) (Statens Serum Institut, Копенгаген, Дания) или ESAT-6 (6-кДа рано секретируемый антиген) / CFP-10 (10-кДа фильтратный белок культуры. ) в конечной концентрации 10 мкг · мл -1 . После 24 ч инкубации (при 37 ° C и 5% углекислого газа) супернатанты собирали и анализировали с помощью множественного набора цитокинов. Образцы анализировали с использованием предварительно смешанных наборов цитокинов / хемокинов из 13-сплетений (стимулированная кровь) или 27-сплетений Bio-Plex (сыворотка, слюна и мокрота) в соответствии с инструкциями производителя (Bio-Rad, Nazareth-Eke, Бельгия. ).Уровни цитокинов у пациентов с туберкулезом и нетуберкулезом анализировали с использованием U-критерия Манна – Уитни. Были выполнены логистическая регрессия и анализ рабочей кривой приемника с поправкой на возраст и пол. Графики были созданы с использованием GraphPad Prism версии 6.0 (программное обеспечение MacKiev, Бостон, Массачусетс, США) и статистического анализа с помощью SPSS версии 20 (IBM, Армонк, Нью-Йорк, США). Значения p ≤0,035 считались значимыми, чтобы учесть частоту ложных открытий.
После стимуляции цельной кровью в течение ночи уровни 10-кДа IFN-γ-индуцируемого белка (IP10) и моноцитарного хемоаттрактантного белка (MCP) -1 были высокими в обеих группах после всех стимуляций, при этом трансформируя фактор роста (TGF) -α, Уровни эпидермального фактора роста и фактора роста эндотелия сосудов (VEGF) были низкими (рис.1а). IP10, лиганд CD40 (CD40L), TGF-α, фактор некроза опухоли (TNF) -α и IFN-γ были значительно выше у субъектов с подтвержденным туберкулезом по сравнению с ORD в нестимулированных образцах (p = 0,0005, p = 0,0089, p = 0,0020, p = 0,0016 и p = 0,0313 соответственно). После вычитания фона основные различия наблюдались в образцах, стимулированных PPD, с более высокими уровнями CD40L, IL-10 и TGF-α при туберкулезе по сравнению с субъектами, не страдающими туберкулезом (p = 0,0089, p = 0,0034 и p <0,0001, соответственно), но более низкие уровни IFN-γ, интерлейкина IL) -2 и воспалительного белка макрофагов (MIP) -1β (p = 0.0313, p = 0,0040 и p = 0,035 соответственно). Используя логистический регрессионный анализ, наилучшая классификация была достигнута после стимуляции PPD комбинацией CD40L, TGF-α и IL-10, что дает 89% правильную классификацию туберкулеза или ORD. Переваренная мокрота показала удивительно высокие уровни цитокинов ex vivo по сравнению как с слюной, так и с сывороткой (фиг. 1b). Уровни IL-4, IL-5, IL-10, IL-13, IL-7, IL-8, IL-12 p70 и MIP-1β были значительно выше в мокроте по сравнению как с слюной, так и с сывороткой (проиллюстрировано на рис.1b с помощью IL-7 и IL-8), в то время как IL-1β, IL-17, гранулоцитарный колониестимулирующий фактор (G-CSF), гранулоцитарно-макрофагальный колониестимулирующий фактор, MCP-1 и TNF-α были значительно выше в как слюна, так и мокрота по сравнению с сывороткой (проиллюстрировано на рис. 1b G-CSF и MCP-1). ИЛ-6 был единственным цитокином, который был ниже в слюне по сравнению как с сывороткой (p <0,01), так и с мокротой (p <0,0001), без разницы между сывороткой и мокротой (данные не показаны) и без разницы в уровнях IFN-γ. между тремя типами образцов (рис.1б).
Рисунок 1–a) Тепловая карта профилей цитокинов после стимуляции цельной крови туберкулезными антигенами в течение ночи. Представлены медианные значения. б) Сравнение уровней цитокинов в сыворотке, слюне и мокроте больных туберкулезом (n = 25, n = 20 и n = 23 соответственно). Обратите внимание, что указанные значения не скорректированы с учетом разведения цитокинов мокроты во время пищеварения (четырехкратное). Прямоугольники указывают межквартильный диапазон, горизонтальные линии указывают медианы, а усы указывают диапазон 5–95%.Данные были проанализированы с использованием теста Краскела – Уоллиса с последующим многократным сравнением Данна. Значения p ≤0,035 считались значимыми и указаны. в) Тепловая карта уровней цитокинов в мокроте ex vivo . Средние значения представлены для пациентов с туберкулезом (n = 23) и пациентов с другими респираторными заболеваниями (ORD) (n = 29). Данные были проанализированы с использованием U-критерия Манна – Уитни. Значения p ≤0,035 считались значимыми и указаны. Контроль: без антигена; ESAT-6: ранний секретируемый антиген массой 6 кДа; CFP-10: белок фильтрата культуры 10 кДа; PPD: очищенное производное белка; ТБ: туберкулез с подтвержденным посевом; CD40L: лиганд CD40; EGF: фактор роста эпидермиса; MIP: воспалительный белок макрофагов; TGF: трансформирующий фактор роста; VEGF: фактор роста эндотелия сосудов; IFN: интерферон; ИЛ: интерлейкин; IP10: IFN-γ-индуцируемый белок массой 10 кДа; МСР: хемоаттрактантный белок моноцитов; TNF: фактор некроза опухоли; нс: незначительно; G-CSF: гранулоцитарный колониестимулирующий фактор; IL-1Ra: антагонист рецептора IL-1; FGF: фактор роста фибробластов; PDGF: фактор роста тромбоцитов.
Затем мы сравнили уровни цитокинов в мокроте ex vivo от туберкулезных и нетуберкулезных субъектов (рис. 1c). Интересно, что мы не обнаружили различий в провоспалительных цитокинах (, т. Е. TNF-α, IFN-γ и IP10), но значительно более низкие уровни IL-10 (p = 0,004), IL-13 (p = 0,003) и IL- 15 (p = 0,022) были обнаружены в мокроте от туберкулеза по сравнению с пациентами, не страдающими туберкулезом (рис. 1c). Кроме того, антагонист рецептора IL-1 врожденных цитокинов, G-CSF и VEGF были значительно ниже (p = 0.005, p = 0,004 и p = 0,030 соответственно), тогда как фактор роста фибробластов (FGF) был значительно выше при туберкулезе по сравнению с субъектами, не страдающими туберкулезом (медиана (межквартильный размах) 287 (40–764) пг · мл 90 · 107 −1 90 · 108 и 2,2 (0–325) пг · мл −1 соответственно; p = 0,007) (рис. 1в). Уровни только FGF дали 74% правильную классификацию туберкулеза (чувствительность (95% ДИ) 78% (56–93%) и специфичность 67% (47–83%)). Логистическая регрессия (с корректировкой по возрасту и полу) показала, что комбинация IL-13, FGF и IFN-γ дала 96% правильную классификацию туберкулеза (чувствительность 85% и специфичность 96%).
Наряду с высокой чувствительностью и специфичностью одним из основных критериев разработки теста на туберкулез, основанного на боковом потоке, является время получения результатов [7]. Мы обнаружили, что уровни биомаркеров хозяина в мокроте ex vivo были значительно выше, чем уровни, измеренные после in vitro посевов крови, стимулированных антигеном , что сокращало время до постановки диагноза. Мокрота обычно используется для микробиологического обнаружения Mycobacteriun tuberculosis , и ее легко получить, что делает ее идеальным типом образца для разработки теста бокового потока на туберкулез.Интересно, что при использовании ex vivo типов образцов не наблюдалось различий в уровнях цитокинов Th2 между туберкулезными и нетуберкулезными субъектами. Это может быть связано с уровнем скрытой инфекции M. tuberculosis в нетуберкулезной группе (50% были положительными по результатам теста QuantiFERON). И наоборот, цитокины Th3 IL-10 и IL-13 были значительно ниже при туберкулезе по сравнению с нетуберкулезной мокротой, что указывает на предвзятость в отношении ответов Th2 у субъектов с туберкулезом.В предыдущем исследовании, проведенном в Бразилии, было показано, что уровни IFN-γ в мокроте соответствуют ответу на лечение [8], но мы не оценивали это в настоящем исследовании. G-CSF необходим для набора нейтрофилов, и в нашем исследовании было обнаружено, что его содержание в мокроте от туберкулеза значительно ниже, чем у субъектов, не страдающих туберкулезом. Это интересно, поскольку нейтрофилы являются основным компонентом защитного иммунного ответа на туберкулез [9], и было показано, что введение G-CSF увеличивает ответ на терапию туберкулеза [10].В то время как большинство факторов были ниже при туберкулезе по сравнению с образцами, не связанными с туберкулезом, FGF был значительно выше. Интересно, что фибробластов, инфицированных M. tuberculosis , теряют свою способность к презентации антигена, что позволяет предположить, что M. tuberculosis могут ускользать от иммунного надзора Т-хелперов, заражая фибробласты, что приводит к персистенции бактерий [11].
Мы проанализировали только субъектов с подтвержденным посевом туберкулеза, и только трое из них имели отрицательный мазок (14%), поэтому на данном этапе сложно определить чувствительность у субъектов с отрицательным мазком мокроты.Тем не менее, 96% правильная классификация туберкулеза с использованием комбинации FGF, IL-13 и IFN-γ из мокроты значительно выше, чем результаты, полученные на основе текущих анализов крови, дыхания или мочи [4], [7]. Таким образом, наши результаты обещают будущую разработку быстрого диагностического теста на туберкулез на основе бокового потока, который можно использовать в условиях ограниченных ресурсов. Ликвидация туберкулеза никогда не будет достигнута в развивающихся странах без синергетического подхода, включая разработку более качественных, быстрых и доступных по цене диагностических средств [2], [7], [12].
Footnotes
Заявление о поддержке: Это исследование финансировалось Европейским партнерством по клиническим исследованиям и развивающимся странам (номер гранта 09.32040.011) и Советом медицинских исследований Великобритании. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конфликт интересов: раскрытие информации можно найти вместе с онлайн-версией этой статьи на сайте www.erj.ersjournals.com
- Поступила 7 ноября 2013 г.
- Принято 28 января 2014 г.
(PDF) Пригодность слюны для диагностики туберкулеза: сравнение с активатором
сыворотки [23] и способствует Т-клеточной памяти. Предыдущие
исследований показали, что продукция ИЛ-2 снижается у
пациентов с активным ПТБ [32]. Это может объяснить низкие уровни IL-2
, полученные с учетом того, что все использованные образцы были исходными
от лиц с подозрением на туберкулез.
Требуются дополнительные исследования, включая исследования
, проведенные на биомаркерах, отличных от тех, которые исследовались в текущем исследовании
, учитывая потенциал того, что диагностический инструмент
, основанный на слюне, может способствовать лечению
туберкулеза у всех пациентов типы, особенно те, у кого
трудности с сдачей образцов мокроты, например, дети.
Такие будущие исследования должны быть сосредоточены на идентификации
биосигнатур, а не индивидуальных биомаркеров, учитывая
, что эти воспалительные биомаркеры могут быть не очень специфичными для ТБ
, особенно при использовании по отдельности. Проверенные
биосигнатурслюны затем могут быть включены в
тестов на месте для диагностики туберкулеза
(Sutherland et al. [33]).
Заключение
В заключение, слюна может быть важной альтернативой
диагностического образца для диагностики PTB и обнаружения биомаркеров.Наши результаты показывают, что биосигнатуры, содержащие
комбинаций между различными маркерами хозяина
, обнаруженными в слюне, могут быть полезны для диагностики заболевания PTB
. Мы подтвердили, что существуют очень значимые
различий в концентрациях некоторых биомаркеров
, выраженных в слюне, по сравнению с уровнями в сыворотке и
, поэтому биомаркеры, которые не проявляют потенциала в образцах сыворотки
, могут не обязательно давать то же самое re-
слюны.Таким образом, слюна требует дальнейшего исследования в качестве образца для обнаружения биомаркера
биомаркера туберкулеза, учитывая, что это очень легко доступный образец и может быть получен
у всех типов пациентов, а иммунологические оценки
на основе слюны могут быть легко переведенным в простые,
тестов без посева в местах оказания медицинской помощи. Кроме того, слюна
может быть более информативным типом образца, чем сыворотка, поскольку это образец
, связанный со слизистой оболочкой / дыхательными путями, и поэтому он ближе к
очагу заболевания, чем образцы периферической крови.Наши результаты
требуют дальнейшего изучения в будущих более крупных проспективных исследованиях
.
Сокращения
AUC: Площадь под кривой ROC; Mtb: Mycobacterium tuberculosis; ORD: Прочие
болезни органов дыхания; PTB: Легочный туберкулез
Благодарности
Авторы благодарны участникам исследования и научному персоналу из исследовательского центра
Уганда и CWRU, а также сотрудникам Центра DST / NRF
по биомедицинским исследованиям туберкулеза и Центру SAMRC за
Исследования туберкулеза, Отделение молекулярной биологии и генетики человека,
Отделение биомедицинских наук, факультет медицины и здравоохранения
Науки, Стелленбошский университет, Кейптаун, Южная Африка.
Финансирование
Эта работа финансировалась Европейским партнерством по разработке клинических испытаний
(EDCTP), номер гранта IP_2009_32040 через Африканский
Европейский туберкулезный консорциум (AE-TBC).
Наличие данных и материалов
Все данные, подтверждающие выводы этой статьи, включены в эту статью
. У нас нет дополнительных неопубликованных данных. Данные, представленные в рукописи
, доступны по запросу в ARN и HMK.
Вклад авторов
ARN; концептуализация, методология, статистический анализ и написание оригинального проекта
, NNC; концептуализация, методология, статистический анализ и обзор рукописей
, PM; анализ данных GW и HMK; составление протокола
, клиническая классификация участников исследования, предоставлены материалы для всех экспериментов
, даны рекомендации по статистическому анализу, наблюдению, привлечению финансирования
и обзору рукописи.Все авторы прочитали и одобрили окончательную рукопись.
Утверждение этических норм и согласие на участие
В этом исследовании принимали участие субъекты, которые дали информированное согласие на участие в более крупном исследовании
Африканско-европейского консорциума по борьбе с туберкулезом (AETBC). Этическое разрешение
было получено от Национального совета по науке и технологиям Уганды, Университета Макерере
, Колледжа медицинских наук и Объединенного центра клинических исследований
Институциональных наблюдательных советов.
Согласие на публикацию
Не применимо.
Конкурирующие интересы
Авторы заявляют, что у них нет конкурирующих интересов.
Примечание издателя
Springer Nature сохраняет нейтралитет в отношении юрисдикционных претензий на опубликованных картах
и институциональной принадлежности.
Сведения об авторе
1
Объединенный клинический исследовательский центр, Кампала, Уганда.
2
Отдел молекулярных исследований
Биология и генетика человека, Отдел биомедицинских наук, DST / NRF
Центр передового опыта биомедицинских исследований туберкулеза и SAMRC
Центр исследований туберкулеза, факультет медицины и здравоохранения
,
Стелленбошский университет, Кейптаун, Южная Африка.
3
Уганда – Case Western
Research Collaboration, Мулаго-Кампала, Уганда.
4
Колледж здравоохранения
Наук, Университет Макерере, Кампала, Уганда.
Получено: 29 сентября 2016 г. Принято: 16 августа 2017 г.
Список литературы
1. Всемирная организация здравоохранения. Глобальный доклад о туберкулезе, 2015 г .; 2015.
2. Парсонс Л.М., Сомоскёви Б., Гутьеррес С. и др. Лабораторная диагностика туберкулеза
в странах с ограниченными ресурсами: проблемы и возможности.Clin
Microbiol Rev.2011; 24 (2): 314–50. DOI: 10.1128 / CMR.00059-10.
3. Хатун З., Хоссейн М., Рой С. и др. Светоизлучающая диодная (LED) флуоресцентная микроскопия
: веха в обнаружении микобактерий Paucibacillary
при туберкулезе легких. Bangladesh Med J. 2012; 40 (1): 22–6.
DOI: 10.3329 / bmj.v40i1.9958.
4. Пиатек А.С., Ван Клифф М., Александр Х. и др. GeneXpert для диагностики туберкулеза:
плановое и целенаправленное внедрение.Glob Health Sci Pract.
2013; 1 (1): 18–23. DOI: 10.9745 / GHSP-D-12-00004.
5. ЛАС Н., Муссавира С., Биндху О.С. Клиническая и диагностическая ценность слюны как неинвазивной диагностической жидкости
: систематический обзор. Biochem Med.
2015; 25 (2): 177–92. DOI: 10.11613 / BM.2015.018.
6. Лима Д.П., Диниз Д.Г., Моймаз САС, Сумида Д.Х., Окамото АС. Слюна: отражение
тела. Int J Infect Dis. 2010. 14 (3): 184–8. DOI: 10.1016 / j.ijid.2009.04.022.
7.Малати Н., Мифили С., Васанти HR. Слюнная диагностика: краткий обзор.
ISRN Dent. 2014; 2014: 158786. DOI: 10,1155 / 2014/158786.
8. Менезес ГБЛ, Перейра Ф.А., Дуарте КАБ и др. Количественное определение вируса гепатита С
в сыворотке и слюне пациентов, инфицированных ВГС. Mem Inst Oswaldo Cruz.
2012; 107 (5): 680–3. DOI: 10.1590 / S0074-02762012000500016.
9. Маламуд Д. Слюна как диагностическая жидкость. Dent Clin N Am. 2011; 55 (1): 159–78.
DOI: 10.1016 / j.cden.2010.08.004.
10. Якобс Р., Маасдорп Э., Малхерб С. и др. Диагностический потенциал новых биомаркеров слюны
хозяина в качестве кандидатов для иммунологической диагностики туберкулеза
и мониторинга ответа на лечение туберкулеза.
PLoS One. 2016; 11 (8): e0160546. DOI: 10.1371 / journal.pone.0160546.
Намуганга и др. BMC Infectious Diseases (2017) 17: 600 Стр. 10 из 11
Содержимое любезно предоставлено Springer Nature, применяются условия использования.Права защищены.
Новый простой тест может улучшить диагностику туберкулеза в развивающихся странах
В развивающихся странах текущий тест для диагностики туберкулеза (ТБ) подвержен ошибкам, сложен и требует много времени. Кроме того, пациенты в этих областях с ограниченными ресурсами не могут легко вернуться в клинику позже, чтобы получить свои результаты. Чтобы сделать диагностику проще, быстрее и точнее, химики разработали быстрый и легкий диагностический инструмент. Полевые испытания нового экспериментального теста начались в июне в Южной Африке, где высока заболеваемость туберкулезом.
Исследователи представят свою работу сегодня на 252-м Национальном собрании и выставке Американского химического общества (ACS). ACS, крупнейшее в мире научное сообщество, проведет здесь собрание до четверга. Он содержит более 9000 презентаций по широкому кругу научных тем.
По данным Всемирной организации здравоохранения, во всем мире почти 10 миллионов человек заболевают туберкулезом и почти 2 миллиона умирают от этой болезни каждый год. Наиболее пострадавшие регионы – Юго-Восточная Азия и Африка.
В более богатых странах пациента с подозрением на туберкулез можно обследовать с помощью рентгена грудной клетки. Или образец мокроты или слюны пациента можно отправить в лабораторию для тестирования такими методами, как полимеразная цепная реакция (ПЦР).
Но в развивающихся странах с ограниченными ресурсами и непостоянным доступом к электричеству пациентов часто проверяют на туберкулез с помощью теста Циля-Нильсена (ZN), который был разработан в 1880-х годах. Техники, использующие эту 11-шаговую процедуру, помещают образец слюны на предметное стекло микроскопа, затем окрашивают его и несколько раз промывают.Процесс занимает несколько часов. Хуже того, «тест ZN не очень чувствителен. Он пропускает некоторые случаи туберкулеза и дает много ложных срабатываний», – сказала Кэролайн Р. Бертоцци, доктор философии. Эти ограничения побудили Бертоцци и ее команду из Стэнфордского университета разработать новый тест.Но это не было первоначальной целью исследователей, когда они начали изучать туберкулез 16 лет назад. В то время они исследовали молекулы, известные как гликолипиды, в клеточных стенках бактерий, вызывающих болезнь. Каждый гликолипид состоит из сахарной трегалозы, связанной с липидом или жиром.Исследователи обнаружили, что если они предоставят бактериям слегка модифицированные формы трегалозы, микробы будут метаболизировать молекулы сахара и интегрировать их в свои гликолипиды.
Другие исследователи показали, что бактерии могут принимать формы трегалозы, в которых каждый сахар присоединен к молекуле флуоресцентного красителя. Клетка, которая собирает эти сахара, светится зеленым. «Мы думали, что можем использовать это для обнаружения бактерий в образцах мокроты», – сказал Бертоцци. К сожалению, краситель других исследователей также прилипает к другим компонентам слюны, что затрудняет различение бактерий.
Команда Бертоцци решила эту проблему, присоединив трегалозу к «сольватохромному» красителю, который не светится, пока не войдет в клеточные стенки. В результате нет фонового свечения. Кроме того, процесс не может быть проще: техник берет образец мокроты, брызгает на него немного смеси красителей, а затем через час смотрит на него под микроскопом, чтобы увидеть, не светится ли что-нибудь.
Более того, только живые бактериальные клетки могут метаболизировать молекулы трегалозы / красителя.Однако красители в тесте ZN маркируют как живые, так и мертвые клетки. Это означает, что традиционный тест не может определить, уменьшается ли количество живых клеток, поэтому его нельзя использовать, чтобы определить, работает ли лечение пациента. Поскольку многие штаммы бактерий туберкулеза теперь устойчивы к стандартным методам лечения, «если лекарства не работают, вы хотите как можно быстрее переключить пациента на следующий курс лечения, чтобы не способствовать развитию лекарственной устойчивости», – пояснил Бертоцци. .
Сейчас группа работает с коллегой из Южной Африки, чтобы посмотреть, как новый тест работает в реальных условиях.Тем временем команда Бертоцци изучает другие флуоресцентные красители, которые могли бы работать даже лучше в тесте на туберкулез. Они также используют свою нынешнюю молекулу трегалозы / красителя для изучения молекулярной структуры и физических свойств клеточной стенки бактерий ТБ. Эти знания могут пролить свет на механизм устойчивости бактерий к лекарствам, а также на потенциальные новые способы уничтожения клеток.Тесты на основе нуклеиновых кислот | FDA
Аденовирус Аденовирус R-ген US Argene SA K121942 Анализ на аденовирус Lyra Quidel Corportation K141931 Анализ ProAdeno + Gen-Probe Prodesse, Inc. K102952 Анализ Prodesse ProAdeno + Gen-Probe Prodesse, Inc. K132159 Устойчивость к противомикробным препаратам GenePOC Carba GenePOC Inc. K1 Устойчивость к противомикробным препаратам Accelerate Pheno System, набор Accelerate PhenoTest BC Accelerate Diagnostics, Inc. K1 Bacillus Anthracis Система обнаружения сибирской язвы JBAIDS Idaho Technology, Inc. К131930, К071188, К051713 Bacillus Anthracis B. anthracis Анализ ПЦР в реальном времени Центры по контролю и профилактике заболеваний K1 Маркеры бактериального вагиноза (БВ) Анализатор Aptima BV Hologic, Inc. K1 Bordetella
ARIES Bordetella Assay; Набор файлов протокола анализа ARIES Bordetella Корпорация Люминекс K163626, K163626 / S001 АНАЛИЗ AMPLIVUE BORDETELLA КОРПОРАЦИЯ QUIDEL К143206 Great Basin Bordetella Direct Test Great Basin Scientific, Inc. К170284 ILLUMIGENE PERTUSIS DNA AMPLIFICATION ASSAY ILLUMIGENE PERTUSSIS НАБОР ВНЕШНЕГО КОНТРОЛЯ ILLUMIPRO-10 AUTOMATED ISOTHERMA MERIDIAN BIOSCIENCE, INC. К133673, К152285 SIMPLEXA BORDETELLA DIRECT, SIMPLEXA BORDETELLA POSITIVE CONTROL PACK ООО «ДИАСОРИН МОЛЕКУЛЯР» K173498 SIMPLEXA BORDETELLA DIRECT, SIMPLEXA BORDETELLA POSITIVE CONTROL PACK ООО «ДИАСОРИН МОЛЕКУЛЯР» К183223 Candida tropicalis / Candida albicans / Candida parapsilosis / Candida glabrata / Candida krusei Подтвердите тест на идентификацию микроорганизмов VPIII Microprobe Corp. К 1, К4Дрожжевой светофор PNA FISH AdvanDx, Inc. K0 , K080719 C. albicans / C. glabrata PNA FISH AdvanDx, Inc. K0 C. albicans PNA FISH AdvanDx, Inc. K0 , K062461 C. Albicans экран Carr-Scarborough Microbiologicals, Inc. K8 T2Candida 1.1 Панель T2 Biosystems, Inc. K173536 Candida glabrata / Candida
видовая группа / Trichomonas vaginalis (TV)Aptima CV / TV Assay Candida glabrata / Группа видов Candida
/ Trichomonas vaginalis (TV)K1 Clostridium difficile ОВЕН C.difficile, набор файлов протокола анализа ARIES C. difficile Люминекс К17 1441 Анализ Solana C. difficile Quidel Corporation K170491 Набор ICEPlex C. difficile PrimeraDx К132726 IMDx C. difficile для Abbott m2000 Intelligent Medical Devices, Inc. К132235 BD Diagnostics BD MAX Cdiff Assay GeneOhm Sciences Canada Inc. К130470 Quidel Molecular Direct Анализ C. difficile Quidel Corporation К123998 Verigene C. Тест на сложные нуклеиновые кислоты Nanosphere, Inc. К123197 Портрет токсигенного анализа C. difficile Great Basin Scientific, Inc. К113358 Универсальный прямой анализ Simplexa C. difficile Focus Diagnostics, Inc. K113433, K163085, K163085 / S001 Xpert C. difficile / Epi Цефеида К110203 Анализ амплификации ДНК Illumigene C. difficile Meridian Bioscience, Inc. К110012 Анализ Illumigene C. difficile Meridian Bioscience, Inc. К100818, К110012 Xpert C. difficile Цефеида K0 Анализ ProGastro Cd Prodesse Inc. K0 BD GeneOhm C. diff Assay BD Diagnostics / GeneOhm Sciences, Inc. K081920 ARTUS C. DIFFICILE QS-RGQ MDX KIT QIAGEN, GMBH К133936 АМПЛИВА C. СЛОЖНЫЙ АНАЛИЗ КОРПОРАЦИЯ QUIDEL К123355 GenePOC CDiff GenePOC Inc K172569 Тест на нуклеиновую кислоту Cobas Cdiff для использования в системе Cobas Liat Roche Molecular Systems, Inc. К171770 Clostridium difficile Материал для контроля качества Панель управления Cepheid Xpert C. Difficile / Epi Microbiologics, Inc. K1 Coxiella burnetii Совместная система идентификации и диагностики биологических агентов (JBAIDS) Комплект для обнаружения лихорадки Q Idaho Technology, Inc. К103207 Chlamydia trachomatis / Neisseria gonorrhoeae Abbott RealTime CT / NG и набор для сбора образцов Multi-Collect Abbott Molecular Inc. K0 , K080739Подтверждающий тест на культуру Accuprobe Neisseria gonorrhoeae Gen-Probe, Inc. K895583 Тест Amplicor Chlamydia trachomatis Roche Molecular Systems, Inc. K 6Тест AMPLICOR CT / NG на Chlamydia trachomatis Roche Molecular Systems, Inc. K973707 Тест AMPLICOR CT / NG на Chlamydia trachomatis Roche Diagnostics Corp. K070174 Тест AMPLICOR CT / NG на Neisseria gonorrhoeae Roche Diagnostics Corp. K070172 APTIMA Combo 2 Assay Gen-Probe, Inc. К111409 APTIMA Combo 2 Assay (система Panther) Hologic / Gen-Probe, Inc. K132251 BD MAX CT / GC / TV, BD MAX Instrument Becton, Dickinson, & Co. K151589, K151589 / S001, K151589 / S002 BD ProbeTec Chlamydia trachomatis (CT) Qx Amplified DNA Assay Becton, Dickinson, & Co. K0 , K0 , K081824 Анализ амплифицированной ДНК BD Probetec Neisseria gonorrhoeae (GC) Qx Becton, Dickinson, & Co. K0 , K0, K081825 BD ProbeTec Chlamydia trachomatis (CT) Qx Amplified DNA Assay на системе BD Viper LT Becton, Dickinson, & Co. К140446 Анализ амплифицированной ДНК BD Probetec Neisseria gonorrhoeae (GC) Qx на системе BD Viper LT Becton, Dickinson, & Co. К140048 BDProbeTec ET Анализ амплифицированной ДНК Chlamydia trachomatis и Neisseria gonorrhoeae Becton Dickinson Microbiology Systems K984631 BDProbeTec ET Анализ амплифицированной ДНК Chlamydia trachomatis и Neisseria gonorrhoeae Becton, Dickinson, & Co. K012351 Тест binx health io CT / NG binx health, Inc. K19 1352 COBAS 4800 CT / NG Test Roche Molecular Systems, Inc. К110923 Тест COBAS AMPLICOR CT / NG на Chlamydia trachomatis Roche Molecular Systems, Inc. K973718 Тест COBAS AMPLICOR CT / NG на Chlamydia trachomatis Roche Diagnostics Corp. K053287 Тест COBAS AMPLICOR CT / NG на Neisseria gonorrhoeae Roche Molecular Systems, Inc. K974342 Тест COBAS AMPLICOR CT / NG на Neisseria gonorrhoeae Roche Diagnostics Corp. K053289 COBAS CT / NG ДЛЯ ИСПОЛЬЗОВАНИЯ В СИСТЕМАХ COBAS 6800/8800 Roche Molecular Systems, Inc. K173887 cobas CT / NG v2.0 Тест Roche Molecular Systems, Inc. К132270, К140887, К163184 cobas CTNG для использования в системах cobas 6800/8800 Roche Molecular Systems, Inc. K202408 GEN-PROBE AMPLIFIED Chlamydia trachomatis Assay Kit Gen-Probe, Inc. К962217 Анализ GEN-PROBE APTIMA на Neisseria gonorrhoeae Gen-Probe, Inc. K063664, K062440, K043144 Анализ GEN-PROBE APTIMA на Chlamydia trachomatis Gen-Probe, Inc. K063451, K053446, K043072 GEN-PROBE APTIMA Combo 2 Assay Gen-Probe, Inc. K043224, K032554, K003395 Система GEN-PROBE PACE 2C для Chlamydia trachomatis и Neisseria gonorrhoeae Gen-Probe, Inc. K9 Тест подтверждения культуры ДНК зонда GONOSPOT Орто Диагностические Системы, Инк. K872628 GONOSTAT Набор для выявления гонококков Sierra Diagnostics, Inc. K9 Hybrid Capture II CT / GC Test Digene Corp. К981567, К010891 Тест Hybrid Capture II CT-ID Digene Corp. К9, К010892 Тест Hybrid Capture II GC-ID Digene Corp. К981485, К010893 Анализ LCx Chlamydia trachomatis Abbott Laboratories K 2 Анализ LCx Neisseria gonorrhoeae Abbott Laboratories K 3Подтверждающий анализ зонда PACE 2 Chlamydia trachomatis Gen-Probe, Inc. K 2 Подтверждающий анализ зонда PACE 2 Neisseria gonorrhoeae Gen-Probe, Inc. K 1 Система PACE 2 для Chlamydia trachomatis Gen-Probe, Inc. K 8Система GEN-PROBE PACE для Chlamydia trachomatis Gen-Probe, Inc. K874878 Система GEN-PROBE для Neisseria gonorrhoeae Gen-Probe, Inc. K874620 Система PACE для Neisseria gonorrhoeae Gen-Probe, Inc. К88 1277 Система быстрой диагностики Chlamydia trachomatis Gen-Probe, Inc. K871878 Тест Roche AMPLICOR CT / NG на Neisseria gonorrhoeae Roche Molecular Systems, Inc. K974503 Тест Roche COBAS AMPLICOR Chlamydia trachomatis Roche Molecular Systems, Inc. K964507 TIGRIS DTS Автоматический анализатор APTIMA Assay for Chlamydia trachomatis Gen-Probe, Inc. K061413 Анализ TIGRIS DTS GEN-PROBE APTIMA на Neisseria gonorrhoeae Gen-Probe, Inc. K061509 TIGRIS DTS GEN-PROBE APTIMA COMBO 2 Assay Gen-Probe, Inc. K060652 Xpert CT / NG Цефеида К121710 Xpert CT / NG Цефеида K1 Aptima Combo 2 Assay (система Panther) Hologic, Inc. K1 Aptima Combo 2® Assay (система Panther®)
Aptima Combo 2® Assay (система Tigris® DTS®)
Hologic, Inc. K200866 binx io CT / NG Assay и binx io CT / NG System binx Health Inc K200533 CT / GC / TV QC материал ПАНЕЛЬ КК на 20 дней BD MAX CT / GC / TV MICROBIOLOGICS, INC. К18 1683 CT / GC QC материал Панель управления Cepheid Xpert CT / NG Microbiologics, Inc. K1 Цитомегаловирус Abbott RealTime CMV Abbott Molecular P160044 Комплект ARTUS CMV RGQ MDX QIAGEN P130027 S001-S002 Тест COBAS CMV Рош Молекулярные системы P160041 S001 Тест COBAS AmpliPrep / COBAS TaqMan CMV Рош Молекулярные системы P110037 S001-S031 NucliSens CMV pp67 Органон Корпорация Текника K983762 Вирус денге CDC DENV-1-4 Анализ ОТ-ПЦР в реальном времени Центры по контролю и профилактике заболеваний K113336 ДНК ядерного антигена-1 ВЭБ / Вирусы, ассоциированные с раком головы и шеи NP Экран Advance Sentry Corporation DEN1 EBV / BKV cobas BKV, контрольный набор cobas EBV / BKV, набор cobas Buffer Negative Control Kit Roche Molecular Systems, Inc K202215 BKV / Количественный тест на вирусную нуклеиновую кислоту для ведения пациентов после трансплантации cobas BKV Roche Molecular Systems, Inc. K203220 EBV / Количественный тест на вирусную нуклеиновую кислоту для ведения пациентов после трансплантации cobas EBV Roche Molecular Systems, Inc. DEN200015 Энтеркокк IMDx Van R для Abbott m2000 Intelligent Medical Devices, Inc. К123753 Анализ BD GeneOhm VanR BD Diagnostics (GeneOhm Sciences, Inc.) К102416 Анализ Xpert vanA Цефеида K0 E. faecalis / OE PNA AdvanDx, Inc. K083074 GBS PNA FISH AdvanDx, Inc. K082612 Набор для идентификации культур E. faecalis PNA FISH AdvanDx, Inc. K063127 Материал для контроля качества кишечных паразитов ПАНЕЛЬ УПРАВЛЕНИЯ BD MAX ENTERIC PARASITE, ПАНЕЛЬ BD MAX ENTERIC PARASITE 20-DAY QC MICROBIOLOGICS, INC. К181711 Энтеровирус Анализ NucliSens EasyQ Enterovirus vl.1 bioMérieux, Inc. K0 , K063261Escherichia coli / Klebsiella pneumoniae / Pseudomonas aeroginosa GNR Светофор PNA FISH AdvanDx, Inc. К101558 E. coli / P. aeruginosa PNA FISH AdvanDx, Inc. K0 , K081309 EK / P aeruginosa PNA FISH AdvanDx, Inc. K0 , K081433 E. coli PNA FISH AdvanDx, Inc. K082068 Francisella tularensis Набор для обнаружения туляремии JBAIDS Idaho Technology, Inc. K072547 Панель по грибковым патогенам ПАНЕЛЬ ИДЕНТИФИКАЦИИ КУЛЬТУРЫ EPLEX ПАНЕЛЬ ГРИБОВЫХ ПАТОГЕНОВ (BCID-FP) GENMARK DIAGNOSTICS, INCORPORATED К182690 грамположительные / грамотрицательные бактерии Accelerate Pheno System, комплект Acceleraet Phenotest BC Ускоренная диагностика DEN160032, DEN160032 / S001 Панель культуры крови Great Basin Staph ID / R Great Basin Scientific, Inc. K152470, K152470 / S001 hemoFISH Masterpanel Miacom Диагностика GMBH K150031, K150031 / S001 Анализ IC-GPC для использования в системе IC (положительные посевы крови) iCubate, Inc. K163390, K163390 / S001 Тест на нуклеиновую кислоту для грамположительной культуры крови Verigene (BC-GP) Nanosphere, Inc. К122514, К113450 Xpert Carba-R (GNR) Цефеида K152614, K152614 / S001, K160901 (Ректальные мазки) ПАНЕЛЬ ИДЕНТИФИКАЦИИ КУЛЬТУРЫ EPLEX – ПАНЕЛЬ ПОЛОЖИТЕЛЬНОЙ ГРАММЫ (BCID-GP) GENMARK DIAGNOSTICS, INCORPORATED К181663 Панель для определения грамотрицательной культуры крови EPlex (BCID-GN) GenMark Diagnostics, Incorporated K182619 IC-GN Кассета IC для использования в системе IC ICubate, Inc. K1 грамположительные / грамотрицательные бактерии (устойчивость к противомикробным препаратам) XPERT CARBA-R CEPHEID К173263 Вирус простого герпеса Aptima Herpes Simpex Viruses 1 и 2 Hologic, Inc. K162673, K162673 / S001 Кассеты для анализа ARIES HSV 1 и 2 – Коробка из 24 (IVD), ARIES HSV 1 и 2 Набор протоколов анализа Корпорация Люминекс K151906 ОВЕН Система Корпорация Люминекс K160517, K160517 / S001 Система ARIES MI, кассеты для анализа ARIES HSV 1 и 2 – коробка 24 шт. (IVD) Корпорация Люминекс К16 1495 Анализ IsoAmp HSV Корпорация BioHelix K111951 Набор MultiCode-RTx Herpes Simplex Virus 1 и 2 EraGen Biosciences, Inc. К111527, К100336 BD ProbeTec Herpes Simplex Viruses (HSV I & 2) QX Amplified DNA Assays BD Diagnostic Systems K103798 SIMPLEXA HSV 1 и 2 ПРЯМОЙ ДИАГНОСТИКА ФОКУСА K133621 (DEN130049) АНАЛИЗ AMIPLIVUE HSV 1 и 2 КОРПОРАЦИЯ QUIDEL K140029 IMDX HSV-1/2 ДЛЯ ABBOTT M2000 INTELLIGENT MEDICAL, INC. К140198 SIMPLEXA HSV 1 & 2 КОМПЛЕКТ ПРЯМОГО / ПОЛОЖИТЕЛЬНОГО УПРАВЛЕНИЯ ДИАГНОСТИКА ФОКУСА K141458, K151565, K151565 / S001 SIMPLEXA HSV 1 и 2 DIRECT, SIMPLEXA HSV 1 и 2 Положительный контроль, пакет ООО «ДИАСОРИН МОЛЕКУЛЯР» K173798 Анализ Solana HSV 1 + 2 / VZV Quidel Corporation K162451 ARTUS HSV-1/2 QS-RGQ MDx НАБОР QIAGEN K142738 SEEGENE ANYPLEX II HSV-1/2 АНАЛИЗ SEEGENE К142156 QUIDEL MOLECULAR DIRECT HSV 1 + 2 / VZV АНАЛИЗ DIAGNOSTIC HYBRIDS INC. K133448 (DEN140004) SENTOSA SA201 HSV 1/2 КАЧЕСТВЕННЫЙ ПЦР-ТЕСТ VELA DIAGNOSTICS USA INC. К172509 HSV 1 & 2 ELITE MGB KIT; ЭЛИТА INGENIUS ELITECHGROUP K180559 Вирус гепатита Abbott RealTime HCV Genotype II Abbott Molecular, Inc. P120012 S001-S0016 Анализ Abbott Realtime HCV Abbott Molecular, Inc. P100017 S001-S006, S007-S012, S014-S019 Alinity m HCV Abbott Molecular, Inc. P1 Abbott Realtime HBV Assay Abbott Molecular, Inc. P080026 S001-S004, S005-S014, S016-S020 Анализ Aptima HCV Quant Dx Hologic, Inc. P160023 Тест COBAS HBV Рош Молекулярные системы P150014 S001-S008 Alinity m HBV Abbott Molecular, Inc. P200013 Тест COBAS HCV Рош Молекулярные системы P160016 Тест COBAS HCV Рош Молекулярные системы P150015 S001-S007 Тест COBAS AmpliPrep / COBAS TaqMan HCV Рош Молекулярные системы P060030 S001-S032, S033-S047, S048-S058 Тест COBAS Taqman HBV Roche Molecular Systems, Inc. P050028 S001-S027, S028-S047, S048, S050-S057 Versant HCV 3.0 Assay (бДНК) Siemens Healthcare Diagnostics P020022 Versant Качественный анализ РНК HCV Gen-Probe, Inc. P020011 S001-S007, S008, S009 COBAS AMPLICOR Тест на вирус гепатита C (HCV) Roche Molecular Systems, Inc. P000012 S001-S043, S044-S053, S054-S056 AMPLICOR HCV Test, v2.0 Roche Molecular Systems, Inc. P000010 S001-S024 КОЛИЧЕСТВЕННЫЙ АНАЛИЗ APTIMA HBV HOLOGIC, INC P170025 Метапневмовирус человека Pro hMPV + Анализ Gen-Probe Prodesse, Inc. К132200, К082688, К123838 Quidel Molecular hMPV Assay Quidel Corporation К112490 Quidel Molecular RSV + hMPV Assay Quidel Corporation К131813, К122189 Вирус папилломы человека Анализ генотипа APTIMA HPV 16 18/45 Gen-Probe, Inc. P120007 S001-S010 Анализ APTIMA HPV Gen-Probe, Inc. P100042 S001-S012 BD ONCLARITY HPV ASSAY БЕКТОН, ДИКИНСОН И КОМПАНИЯ P160037 cobas HPV для использования в системах cobas 6800/8800 Рош Молекулярные Системы, Инк. P1 Cervista HPV 16/18 Hologic, Inc. P080015; S001-S012 Набор для экстракции ДНК Cervista HPV HR и Genfind Hologic, Inc. P080014 S001-S018 Тест COBAS HPV Roche Molecular Systems, Inc. P100020 S001-S024 Digene Hybrid Capture 2 Тест ДНК ВПЧ высокого риска Digene Corporation P8 S001-S034 Вирусы гриппа и респираторных заболеваний Анализ на грипп PLEX-ID Abbott Laboratories К121003 Alere i Influenza A & B ALERE SCARBOROUGH, INC D / B / A BINAX, INC К141520, К151464, К151690, К163266 Alere i RSV Alere Scarborough, Inc. К16 1375 ARIES Flu A / B & RSV Assay Корпорация Люминекс К161220 artus Infl A / B RG RT-PCR Kit Qiagen GmbH К113323 CDC Панель обнаружения и характеристики ОТ-ПЦР вируса гриппа человека в реальном времени Центры по контролю и профилактике заболеваний K080570 Панель диагностики РТ-ПЦР вируса гриппа человека КДК в реальном времени Центры по контролю и профилактике заболеваний К133869, К132508, К130551, К123905, К111507, К161556 CDC Диагностическая панель RT-PCR вируса гриппа человека в реальном времени, набор для определения подтипа гриппа A Центры по контролю и профилактике заболеваний К161556 CDC Диагностическая панель RT-PCR вируса гриппа человека в реальном времени, набор для набора текста A / B гриппа Центры по контролю и профилактике заболеваний К17 2091 CDC Панель диагностики вируса гриппа человека ОТ-ПЦР в реальном времени, набор для типирования вируса гриппа A / B, панель диагностики вируса гриппа человека CDC в режиме реального времени, набор подтипов гриппа A, ОТ-ПЦР вируса гриппа человека в режиме реального времени ПЦР, набор для определения подтипа вируса гриппа A / H5 Центры по контролю и профилактике заболеваний K200370 CDC ВИРУС ГРИППА ЧЕЛОВЕКА ОТ-ПЦР в реальном времени ДИАГНОСТИЧЕСКАЯ ПАНЕЛЬ ГРИППА A / H5 ПОДТИПИРОВАНИЕ ЦЕНТРЫ КОНТРОЛЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ К141859, К153148 CDC Influenza 2009 A (h2N1) pdm Панель ОТ-ПЦР в реальном времени Центры по контролю и профилактике заболеваний К101564 CDC Вирус гриппа человека RT-PCR Диагностическая панель в реальном времени Набор для генотипирования линии гриппа B Центры по контролю и профилактике заболеваний К181736 XPERT XPRESS FLU / RSV, XPERT Назофарингральный набор образцов, XPERT назальный набор образцов, GENEXPERT XPRESS II, GENEXPERT XPRESS IV Цефеида К180218 ТЕСТ ACCULA RSV MESA BIOTECH, INC. К18 1443 Панель биокодирования респираторных патогенов (RPP) Applied BioCode, Inc K1 cobas Liat Influenza A / B и RSV Iquum, Inc. K153544, K153544 / S001 Молекулярная среда для сбора и сохранения eNAT Copan Italia S.p.A. K201849 Пробирка для сбора ДНК / РНК Shield Zymo Research K202641 Панель респираторных патогенов ePlex GenMark Diagnostics, Inc K163636, K163636 / S001 eSensor Respiratory Viral Panel (RVP) Clinical Micro Sensors, Inc. K113731 FilmArray Респираторная панель (RP) Idaho Technology, Inc. К120267, К110764, К103175 FilmArray Респираторная панель (RP) ООО «БиоФайр Диагностика» К123620, К143080, К160068 FilmArray Респираторная панель 2 (RP2) ООО «БиоФайр Диагностика» К170604 FilmArray Респираторная панель EZ (RP EZ) ООО «БиоФайр Диагностика» K152579, K152579 / S001, K152579 / S002 FilmArray RP EZ Control Panel M265 Maine Molecular Quality Controls, Inc. К16 1573 Idylla Respiratory (IFV-RSV) Панель Янссен Фармацевтика NV К163628, К163629, К163630 IMDx Flu A / B и RSV для Abbott m2000 Intelligent Medical Devices, Inc. К131584 НАБОР ДЛЯ ПОДТИПОВ ГРИППА CDC ВИРУС ГРИППА ЧЕЛОВЕКА ОТ-ПЦР ДИАГНОСТИКА В РЕАЛЬНОМ ВРЕМЕНИ ЦЕНТРЫ КОНТРОЛЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ К140851 Вирус гриппа A / H5 (азиатская линия) Набор праймеров и зондов для ОТ-ПЦР в реальном времени Центры по контролю и профилактике заболеваний K060159 НАБОР ГЕНОТИПОВ ЛИНИИ ГРИППА B CDC ВИРУС ГРИППА ЧЕЛОВЕКА ОТ-ПЦР в реальном времени ДИАГНОСТИЧЕСКАЯ ПАНЕЛЬ ЦЕНТРЫ КОНТРОЛЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ К140857 Набор для определения подтипа гриппа A JBAIDS U.S. Деятельность по разработке медицинского оборудования армии К111778 Набор для обнаружения гриппа A&B JBAIDS Деятельность по разработке медицинского оборудования армии США К111775, К152523 Набор для обнаружения гриппа JBAIDS A / H5 (азиатская линия) Деятельность по разработке медицинского оборудования армии США К100287 Анализ Liat Influenza A / B IQuum, Inc. К111387 АНАЛИЗ ВИРУСА LYRA PARAINFLUENZA КОРПОРАЦИЯ QUIDEL К141927 Панель респираторных патогенов NxTAG Luminex Molecular Diagnostics, Inc. K152386, K152386 / S001 Панель респираторных патогенов NxTAG, файлы панели респираторных патогенов NxTAG, программное обеспечение SYNCT Luminex Molecular Diagnostics, Inc. K1 Prodesse ProFAST Assay Gen-Probe Prodesse, Inc. К132237 Анализ Prodesse ProFlu + Gen-Probe Prodesse, Inc. К132129 Prodesse ProParaflu Assay Gen-Probe Prodesse, Inc. К132238, К0 Prodesse ProParaflu Assay Hologic / Gen-Probe Prodesse, Inc. К153223, К132238 Анализ ProFlu + Hologic / Gen-Probe Prodesse, Inc. K153219, K110968, K0 , K081030, K073029 Анализ ProParaFlu + Prodesse, Inc. K0 Quidel Molecular Influenza A + B Assay Quidel Corporation К131728, К113777, К112172 Simplexa Flu A / B и RSV Focus Diagnostics, Inc. К102170 Simplexa Flu A / B и RSV Direct Focus Diagnostics, Inc. К120413, К142365, К152408 Simplexa Influenza A h2N1 (2009) Focus Diagnostics, Inc. К100148 Анализ Solana Influenza A + B Quidel Corporation К16 1814 Verigene Respiratory Pathogens Flex Nucleic Acid Test (RP Flex) Nanosphere, Inc. K143653, K143653 / S001 Verigene Respiratory Virus Plus Nucleic Acid Test (RV +) Nanosphere, Inc. K103209, K0 , K0, K0, K083088Xpert Xpress Flu Цефеида K162456, K162456 / S001, K171552 Xpert Flu + RSV Xpress Цефеида K151226, K162331, K162331 / S001 Анализ Xpert Flu Цефеида К123191, К120911, К103766 АНАЛИЗ XPERT FLU / RSV XC Цефеида К142045 XPERT XPRESS FLU, XPERT NASOPHARYNGEAL НАБОР ДЛЯ СБОРА ОБРАЗЦОВ, НАБОР ДЛЯ СБОРА НАСАЛЬНЫХ ОБРАЗЦОВ XPERT, СИСТЕМЫ GENEXPERT DX (GX-I, GX-II, GX-IV, GX-XVI), GENEXPERT INFINITY-48S SYSTEM СИСТЕМА Цефеида К181289 Панель респираторных вирусов xTAG (RVP) Luminex Molecular Diagnostics, Inc. K112781, K112199, K0 , K081483, K063765xTAG Respiratory Viral Panel Fast (RVP FAST) Luminex Molecular Diagnostics, Inc. K103776 ТЕСТ ACCULA FLU A / FLU B MESA BIOTECH, INC. К171641 Alere I Influenza A & B 2, Alere I Instrument, Alere I Набор контрольных мазков для гриппа A и B Alere Scarborough, Inc. К1792 Панель управления FilmArray RP2 / RP2plus Maine Molecular Quality Controls, Inc. K173171 ДЫХАТЕЛЬНАЯ ПАНЕЛЬ FILMARRAY 2 PLUS (RP2PLUS) БИОЖАРНАЯ ДИАГНОСТИКА, ООО DEN170017 Анализ Panther Fusion AdV / HMPV / RV Hologic, Inc. K172629 Анализ Panther Fusion Paraflu Hologic, Inc. K172282 Анализ Panther Fusion Flu A / B / RSV, универсальный набор жидкостей Panther Fusion, Panther Hologic, Inc. К17 1963 Анализ Solana RSV + HMPV Quidel Corporation K171974 ID СЕЙЧАС Грипп A и B 2 Alere Scarborough, Inc. K1 ID СЕЙЧАС Грипп A и B 2 Abbott Diagnostics Scarborough, Inc. K19 1534 Тест на нуклеиновую кислоту Cobas Influenza A / B для использования в системе Cobas Liat Roche Molecular Systems, Inc K1 ТЕСТ НА ЯДЕРНУЮ КИСЛОТУ COBAS INFLUENZA A / B и RSV ДЛЯ ИСПОЛЬЗОВАНИЯ В СИСТЕМЕ COBAS LIAT Roche Molecular Systems, Inc К210234 FluChip-8G Анализ гриппа A + B InDevR, Inc К182513 Cdc Панель диагностики вируса гриппа человека в реальном времени Rt-Pcr, набор для набора текста A / B, панель диагностики вируса гриппа человека Cdc в реальном времени Rt-Pcr, набор подтипов гриппа A, Cdc вирус гриппа человека в режиме реального времени Rt- Pcr, Набор для генотипирования линии гриппа B, Cdc Human Influenza Virus Real-Time Rt-Pcr, Центры по контролю и профилактике заболеваний K1 Тест на нуклеиновую кислоту cobas Influenza A / B для использования в системе Cobas Liat, тест на нуклеиновую кислоту cobas Influenza A / B и RSV для использования в системе Cobas Liat, тест на нуклеиновую кислоту cobas Strep A для использования в системе Cobas Liat Roche Molecular Systems, Inc К200065 Simplexa Flu A / B & RSV Direct Gen II, Simplexa Flu A / B & RSV Positive Control Pack ООО «ДиаСорин Молекуляр» K201505 Вирусы гриппа и респираторных заболеваний
Грипп A и B, Strep A, RSVУЖЕ I INFLUENZA A & B, ALERE I STREP A, ALERE I RSV, ALERE I INFLUENZA A & B 2 Alere Scarborough, Inc. K173932 ALERE I INFLUENZA A & B, ALERE I STREP A, ALERE I RSV, ALERE I INFLUENZA A & B 4 Alere Scarborough, Inc. K173932 ALERE I STREP A 2, ALERE I INSTRUMENT, ALERE I STREP A 2 CONTROL SWAB KIT Alere Scarborough, Inc. К173653 Контрольный материал респираторной панели Панель управления респираторной системой Cepheid Xpert Microbiologics, Inc. K1 Респираторная панель Респираторная панель QIAstat-Dx; Анализатор QIAstat-Dx QIAGEN GmbH Виды лейшмании SMART Leish Деятельность по разработке медицинского оборудования армии США K081868 Менингит / энцефалит FilmArray Meningitis / Encephalitis (ME) Panel ООО «БиоФайр Диагностика» DEN150013, DEN150013 / S001, K160462 Mycobacterium tuberculosis Анализ Xpert MTB / RIF Цефеида К131706 BDProbetec ET Набор для идентификации комплекса микобактерий туберкулеза Becton, Dickinson, & Co. К000884 Прямой тест на усиленные микобактерии туберкулеза Gen-Probe, Inc. P4 Тест на Amplicor Mycobacterium tuberculosis Roche Molecular Systems, Inc. P 0
SNAP M.tuberculosis complex Syngene, Inc. K2 Accuprobe Mycobacterium tuberculosis complex Тест Gen-Probe, Inc. К896493 Система быстрой диагностики Mycobacterium tuberculosis Gen-Probe, Inc. K871795 Тест быстрой идентификации Mycobacterium tuberculosis complex Gen-Probe, Inc. K862614 Виды Mycobacterium Accuprobe Mycobacterium avium комплексная культура Gen-Probe, Inc. К 5, К896494, К897078 Идентификационный тест Accuprobe Mycobacterium kansasii Gen-Probe, Inc. К3 Комплекс SNAP Mycobacterium avium Syngene, Inc. K 2
Accuprobe Mycobacterium intracellulare Тест идентификации культуры Gen-Probe, Inc. K897077 Тест для идентификации культур Accuprobe Mycobacterium gordonae Gen-Probe, Inc. К896492 Система быстрой диагностики Mycobacterium gordonae Gen-Probe, Inc. K8 Система быстрой диагностики микобактерий Gen-Probe, Inc. K864597 Тест быстрой идентификации Mycobacterium avium Gen-Probe, Inc. K862613 Система быстрого подтверждения Gen-Probe Mycobacterium Gen-Probe, Inc. K860782 Mycoplasma Genitalium Анализ Aptima Mycoplasma Genitalium Hologic, Inc. DEN180047 Mycoplasma genitalium (MG) и Trichomonas vaginalis (TV) Cobas TV / MG для использования в системах Cobas 6800/8800, набор для положительного контроля Cobas TV / MG, набор для отрицательного контроля Cobas Buffer Roche Molecular Systems, Inc. K1 Mycoplasma pneumoniae Illumigene Mycoplasma Direct Анализ амплификации ДНК Meridian Bioscience, Inc. К160829 illumigene Mycoplasma DNA Amplification Assay Meridian Bioscience, Inc. К152800, К123423 Мультиплексная панель Вагинальная панель BD Max, BD MAX Instrument GeneOhm Sciences Canada DEN160001 / DEN160001 / S001 ПАНЕЛЬ ПАТОГЕНОВ ЖЕЛУДОЧНО-КИШЕЧНОГО БИОКОДА (GPP) APPLIED BIOCODE, INC. К180041 Панель идентификации культуры крови BioFire 2 (BCID2) ООО «БиоФайр Диагностика» K1 Панель управления FilmArray BCID2 M416 Maine Molecular Quality Controls, Inc. К200010 Приложение Curetis Unyvero LRT Curetis GmbH DEN170047 Приложение Unyvero LRT BAL Curetis GmbH K1 Прибор ePlex (мультиплекс) GenMark Diagnostics, Inc K163652, K163652 / S001 Панель BCID FilmArray BioFire Defense, LLC К143171, К160457 FilmArray NGDS Warrior Panel BioFire Defense, LLC K170883, DEN160048 Панель управления FilmArray Warrior Maine Molecular Quality Controls, Inc. K163522 NEUMODX GBS АНАЛИЗ NEUMODX MOLECULAR, INC. K173725 ТЕСТ PANNAT STEC МИКРОНИКС, ИНК К173330 Анализ ProGastro SSCS Gen-Probe Prodesse, Inc. К123274 Панель биокодирования желудочно-кишечных патогенов (GPP) Applied Biocode, Inc. K1 Анализ EntericBio Dx Серосеп, ООО К182703 xTAG Панель по патогенам желудочно-кишечного тракта (GPP) Luminex Molecular Diagnostics, Inc. К121894, К121454 BD MAX Extended Enteric Bacterial Panel, BD MAX System Бектон Дикинсон и компания К170308 BD MAX ENTERIC ВИРУСНАЯ ПАНЕЛЬ, BD MAX INSTRUMENT Бектон Дикинсон и компания К18 1427 FILMARRAY GASTROINTESTINAL (GI) PANEL БИОПОГНЕННАЯ ДИАГНОСТИКА K140407, K160459, K160459 / S001 Панель xTAG Gastrointestinal Pathogen Panel (GPP), Программное обеспечение для анализа данных xTAG (TDAS GPP) Luminex Molecular Diagnostics, Inc. К1 xTAG Панель по патогенам желудочно-кишечного тракта (GPP) Luminex Molecular Diagnostics, Inc. K1 T2BACTERIA ПАНЕЛЬ T2 BIOSYSTEMS, INC. К172708 Панель xTAG Gastrointestinal Pathogen Panel (GPP), Программное обеспечение для анализа данных xTAG (TDAS GPP) Luminex Molecular Diagnostics, Inc. К1 xTAG Панель по патогенам желудочно-кишечного тракта (GPP) Luminex Molecular Diagnostics, Inc. K1 Панель бактериальных патогенов стула Большого бассейна Great Basin Scientific, Inc. K163571, K163571 / S001 XTAG ПАНЕЛЬ ПАТОГЕНОВ ЖИВОТНОВОДСТВА (GPP) / АНАЛИЗ ДАННЫХ XTAG LUMINEX MOLECULAR DIAGNOSTICS INC. К140377, К140647 ТЕСТ НА ЯДЕРНУЮ КИСЛОТУ НА ВЕРИГЕННЫЙ ПАТОГЕН ВВЕРХ (EP) НАНОСФЕРА, INC К140083, К142033 ПАНЕЛЬ FILMARRAY PNEUMONIA ООО «БиоФайр Диагностика» K180966 FILMARRAY PNEUMONIA PANEL PLUS ООО «БиоФайр Диагностика» К181324 Multiplex Panel (Пневмония) Материал для контроля качества FilmArray Pneumonia / Pneumoniaplus Control Maine Molecular Quality Controls, Inc.(MMQCI) K1 Ортопоксвирус, не связанный с натуральной оспой НАБОР ПРАЙМЕРА И ЗОНДОВ ДЛЯ ПЦР В РЕАЛЬНОМ ВРЕМЕНИ НЕВАРИОЛОВОГО ОРТОПОКСВИРУСА Центры по контролю и профилактике заболеваний К181205 НАБОР ПРАЙМЕРА И ЗОНДОВ ДЛЯ ПЦР В РЕАЛЬНОМ ВРЕМЕНИ НОВАРИОЛЫ ОРТОПОКСВИРУСА Центры по контролю и профилактике заболеваний DEN070001 Норовирус RIDA GENE Nororvirus GI / GII Р-Биофарм AB K171511 XPERT NOROVIRUS GENEXPERT Dx SYSTEMS (GX-I GX-11 GX-IV GX-XVI) СИСТЕМА GENEXPERT INFINITY-48, СИСТЕМА GENEXPERT INFINITY-48S, СИСТЕМА GENEXPERT INFINITY-80 CEPHEID К142501 Плазмодий ID-FISH Набор для анализа рода Plasmodium, ID-FISh P.falciparum и P. vivax Combo Test ID-FISH Technology, Inc. DEN160025, DEN160025 / S001 Риккетсия Анализ ПЦР в реальном времени на Rickettsia Центры по контролю и профилактике заболеваний К170940 Сепсис SeptiCyte LAB Иммунэкспресс, Инк. К163260 Стафилококк Анализ BD Max MRSA BD Diagnostics (GeneOhm Sciences Canada, Inc.) K120138 Стафилококк QuickFISH BC AdvanDx, Inc. K113371 MRSA / SA ELITe MGB EliTechGroup Epoch Biosciences. К112937, К132468 Тест на нуклеиновую кислоту Verigene Staphylococcus Blood Culture (BC-S) Nanosphere, Inc. К112424 Анализ NucliSENS EasyQ MRSA bioMerieux, Inc. К102740 Анализ культуры крови Xpert MRSA / SA Цефеида К101879, К082140 Полный назальный анализ Xpert MRSA / SA Цефеида K100822 Расширенный тест LightCycler MRSA Roche Molecular Systems, Inc K0 Анализ BD GeneOhm MRSA ACP BD Diagnostics (GeneOhm Sciences Canada, Inc.) K0 S. aureus и / или другие виды стафилококков PNA FISH Культура AdvanDx, Inc. K0 Анализ Xpert MRSA / SA SSTI Цефеида K080837 Анализ BD GeneOhM StaphSR Assay BD Diagnostics (GeneOhm Sciences Canada, Inc.) K071026 S. aureus PNA FISH AdvanDx, Inc. К0 , К060099 Xpert MRSA Цефеида K070462 Анализ IDI-MRSA Infectio Diagnostic, Inc. К042357, К033415 MECA XPRESSFISH ADVANDX INC. К140619 COBAS MRSA / SA ТЕСТ ROCHE MOLECULAR SYSTEMS INC. К142721 Xpert MRSA NxG Цефеида K162444 Культура крови Xpert MRSA / SA, система GeneXpert Dx, система GeneXpert Infinity-48s, система GeneXpert Infinity-80 Цефеида K1 Контрольный материал по стафилококку / MRSA Панель управления Cepheid Xpert MRSA NxG Microbiologics, Inc. K19 1172 Cepheid Xpert SA Назальная полная панель управления Microbiologics, Inc. K1 Стрептококки ARIES GBS Assay Корпорация Люминекс K162772 Анализ Xpert GBS LB Цефеида К121539 illumigene Анализ амплификации ДНК стрептококка группы A (GBS) Meridian Bioscience, Inc. K122019 Иллюмиген Streptococcus группы B (GBS) Анализ амплификации ДНК Meridian Bioscience, Inc. К121044 BD Max GBS Assay Becton, Dickinson, & Co. К111860 Анализ Cepheid Smart GBS Цефеида K062948 Xpert GBS Цефеида K060540 Анализ IDI-Strep B Infectio Diagnostic, Inc. K022504 Gen-Probe Accuprobe Набор для идентификации культур стрептококков группы B Chugai Pharmaceuticals Co, Ltd. K974572 Подтверждение посева Accuprobe Streptococcus pneumoniae Gen-Probe, Inc. K 8
ИЛЛЮМИГЕН ГРУППА B STREPTOCOCCUS (GBS) АНАЛИЗ АМПЛИФИКАЦИИ ДНК MERIDIAN BIOSCIENCE, INC. К112125 АНАЛИЗ AMPLIVUE GBS КОРПОРАЦИЯ QUIDEL К133503 LYRA DIRECT STREP ASSAY КОРПОРАЦИЯ QUIDEL K133883 (DEN140005) АНАЛИЗ АМПЛИВНОГО ГАЗА КОРПОРАЦИЯ QUIDEL К141173 LIAT STREP A ASSAY IQUUM INC К141338 ревоген GenePOC Inc. K170558 GenePOC GBS LB GenePOC Inc. K170557 Полный анализ Solana Strep Quidel Corporation К162274 ARIES Group A Strep Assay, ARIES Group A Strep Assay Protocol File Kit Корпорация Люминекс К172402 Xpert Xpress Strep A Цефеида K172126; K173398 GenePOC Strep A GenePOC Inc. К183366 Стрептококки / контрольный материал GBS Панель управления Cepheid Xpert GBS LB Microbiologics, Inc. К182472 Токсин Шига Прямой тест на токсин шига Большого бассейна Great Basin Scientific, Inc. K152955, K152955 / S001, K152955 / S002 Trichomonas vaginalis Affirm VP Тест на определение микробов Gardnerella vaginalis и Trichomonas vaginalis Microprobe Corp. K 3 Amplivue Trichomonas Assay Quidel Corporation K143329 Анализ APTIMA Trichomonas vaginalis (ATV) Gen-Probe, Inc. К102911 Анализ APTIMA Trichomonas vaginalis (система PANTHER) Gen-Probe, Inc. К122062 BD ProbeTec Trichomonas vaginalis (TV) QX Amplified DNA Assay Becton, Dickinson & Co. К130268 Анализ трихомонад Solana Quidel Corporation K161182, K161182 / S001 Xpert TV Цефеида K151565, K151565 / S001, K161619 Aptima Combo 2 Assay (Panther) – набор тестов 250, Aptima Combo 2 Assay (Tigris) – набор тестов 250, Aptima Trichomonas Vaginalis (Panther) – набор тестов 250, Aptima Trichomonas Vaginalis (Tigris) – набор тестов 250 Hologic, Inc. К200436 Транспортные средства PRIMESTORE MTM Longhorn Vaccines and Diagnostics LLC DEN170029 Вагинальная панель (Бактериальный вагиноз, вагинит) Вагинальная панель BD MAX GeneOhm Sciences Canada, Inc. (BD Diagnostics) DEN160001 Вирусы ветряной оспы Simplexa VZV Direct, Simplexa VZV Positive Control Pack DiaSorin K1 Вариола Анализ ПЦР в реальном времени на вирус натуральной оспы Центры по контролю и профилактике заболеваний DEN160016, DEN160016 / S001 Yersinia pestis Комплект для обнаружения чумы JBAIDS Idaho Technology, Inc. K072631 Дифференциальная экспрессия биомаркеров хозяина в образцах слюны и сыворотки от лиц с подозрением на туберкулез легких Академический исследовательский доклад на тему «Биологические науки»
Издательство Hindawi Publishing Corporation, том 2013 г., номер статьи 981984, 10 страниц http://dx.doi.org/10.1155/2013/981984
Исследовательская статья
Дифференциальная экспрессия биомаркеров хозяина в образцах слюны и сыворотки от лиц с подозрением на туберкулез легких
Хуцо Г.Фалан, Магдалена Криэль, Андре Г. Локстон, Анджела Менезес, Ким Стэнли, Джан Д. ван дер Спуй, Герхард Вальцль и Роман Н. Чегу
DST / NRF Центр передового опыта в области биомедицинских исследований туберкулеза и Центр молекулярной и клеточной биологии MRC, Отделение молекулярной биологии и генетики человека, Отделение биомедицинских наук, Факультет медицины и наук о здоровье, Стелленбошский университет, P.O. Box 19063, Francie van Zijl Drive, Tygerberg 7505, Южная Африка
Переписку следует направлять Роману Н.Чегоу; [email protected]
Поступило 4 августа 2013 г .; Принята в печать 18 сентября 2013 г.
Академический редактор: Ив Денизо
Авторские права © 2013 Хуцо Г. Фалане и др. Это статья в открытом доступе, распространяемая по лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Диагностика туберкулеза остается сложной задачей у людей, которым трудно получить образцы мокроты хорошего качества, например у детей.В таких случаях могут быть полезны биосигнатуры маркеров воспаления хозяина, особенно если они основаны на более легко доступных образцах, таких как слюна. Чтобы изучить потенциал слюны в качестве альтернативного образца для диагностики / исследования биомаркеров туберкулеза, мы оценили уровни 33 маркеров хозяина в образцах слюны людей с симптомами туберкулеза легких и сравнили их с полученными в сыворотке крови. Из 38 человек, включенных в исследование, туберкулез был подтвержден у 11 (28.9%) посевом мокроты. Как в случаях туберкулеза, так и в других случаях уровни большинства маркеров были выше минимально обнаруживаемого предела в обоих типах образцов, но не было стабильной картины в отношении соотношения маркеров в сыворотке / слюне. Уровни фракталкина, IL-17, IL-6, IL-9, MIP-10, CRP, VEGF и IL-5 в слюне, а также уровни IL-6, IL-2, SAP и SAA в сыворотке были значительно выше при туберкулезе. пациенты (P <0,05). Эти предварительные данные показывают, что существуют значительные различия в уровнях маркеров хозяина, экспрессируемых в слюне, по сравнению с уровнями, экспрессируемыми в сыворотке, и что воспалительные маркеры в обоих типах образцов являются потенциальными кандидатами для диагностики туберкулеза.
1. Введение
Туберкулез (ТБ) остается глобальной проблемой здравоохранения. По оценкам, в 2011 г. в результате этого заболевания возникло 8,7 миллиона новых случаев заболевания и 1,4 миллиона случаев смерти [1]. Задержка или неудача в диагностике заболевания приводит к отсрочке лечения с последующим увеличением возможности передачи, при этом ежегодно на каждый нелеченый случай потенциально заражаются десять человек [2]. Широко известна низкая чувствительность микроскопии мазка мазка, наиболее часто используемого диагностического теста на туберкулез в условиях ограниченных ресурсов [3, 4].Помещения для культивирования Mycobacterium tuberculosis (M.tb) не так широко доступны в условиях ограниченных ресурсов, и для получения результатов посева может потребоваться до 42 дней [5]. Разработка теста Xpert MTB / RIF (Cepheid Inc., Калифорния, США) явилась самым важным достижением в этой области, поскольку тест дает результаты в течение 2 часов вместе
с обнаружением устойчивости к рифампицину [6]. Общая чувствительность теста у взрослых составляет 67–98%, а специфичность – около 98% [7].Однако ограничения, в том числе высокая стоимость и требование стабильного электроснабжения и короткого срока хранения расходных материалов [8], препятствуют массовому развертыванию теста в условиях ограниченных ресурсов и часто с высокими нагрузками. Кроме того, диагностические тесты, основанные на мокроте, не подходят для людей, которым трудно получить образцы мокроты хорошего качества, например у детей [9] и лиц с внелегочным туберкулезом. В таких случаях могут быть полезны методы иммунодиагностики, использующие биосигнатуры маркеров воспаления хозяина [10,11], особенно если они основаны на более легко доступных образцах, таких как слюна, и превращены в быстрые тесты в месте оказания медицинской помощи.
Слюна в основном выделяется через околоушные, поднижнечелюстные и подъязычные железы. Состоит на 98%
воды и содержит другие вещества, включая электролиты, слизь, антибактериальные соединения и различные ферменты [12]. Он в изобилии вырабатывается людьми всех возрастных групп, и средний человек производит от 0,3 до 7 мл слюны в минуту и всегда имеет около 1 мл в полости рта [12]. Сбор слюны прост, неинвазивен и не несет в себе неудобств или рисков, связанных с забором крови [13].
В последнее время появился интерес к изучению слюны на предмет потенциально полезных воспалительных биомаркеров [13]. Диагностические тесты на основе слюны, такие как быстрые тесты на ВИЧ [14], имеются в продаже. Несмотря на большое количество исследований по обнаружению биомаркеров ТБ, доступных в литературе, большинство из которых основано на сыворотке или, в меньшей степени, моче [15-18] (обзор в [19-21]), слюне, относительно легкодоступный и обильный тип образца, пока не вызвал большого интереса в этой области.В настоящем исследовании мы оценили уровни 33 маркеров хозяина в слюне людей с симптомами, указывающими на туберкулез легких, и сравнили их с уровнями, обнаруженными в сыворотке. Мы показываем, что существуют большие различия в уровнях маркеров, экспрессируемых в слюне по сравнению с сывороткой, и что некоторые из маркеров слюны могут иметь потенциал в диагностике туберкулеза.
2. Материалы и методы
2.1. Участники исследования. Лица с подозрением на заболевание туберкулезом легких были набраны из сообщества Фисантекраал на окраине Кейптауна, Южная Африка, в рамках продолжающегося исследования Африканского европейского консорциума по борьбе с туберкулезом (AE-TBC), финансируемого EDCTP (http: // www.ae-tbc.eu/). Набор участников исследования начался в октябре 2010 года. На момент проведения этого пилотного исследования в исследовательском центре было зарегистрировано 50 участников, а заболевание легочным туберкулезом было подтверждено у 11 (22%). В это предварительное исследование были включены образцы от всех 11 человек с подтвержденным заболеванием ТБ и 27 человек без ТБ, которые были случайным образом отобраны из нашего банка образцов. Все люди, включенные в исследование, предоставили пару образцов (слюна и сыворотка).
Все участники обратились в сельское учреждение здравоохранения с симптомами, указывающими на туберкулез легких.Вкратце, у участников был постоянный кашель продолжительностью более 2 недель и по крайней мере одно из следующего: лихорадка, недомогание, недавняя потеря веса, ночная потливость, знание тесного контакта с больным туберкулезом, кровохарканье, боль в груди или потеря аппетита. Участники имели право на участие в исследовании, если они были 18 лет и старше, желающие дать письменное информированное согласие на участие в исследовании, в том числе на тестирование на ВИЧ. Пациенты были исключены из исследования, если они не проживали в районе исследования более 3 месяцев, страдали тяжелой анемией (HB <10 г / л), получали противотуберкулезное лечение, получали противотуберкулезное лечение в предыдущий период. 90 дней или принимали хинолоновые или аминогликозидные антибиотики в течение последних 60 дней.При включении в исследование для каждого участника заполнялась форма отчета о болезни, а затем были собраны образцы крови и слюны, а также другие образцы, включая мочу и мокроту, необходимые для основного исследования. Исследование было одобрено Комитетом по исследованиям в области здравоохранения
.Стелленбошского университета (номер ссылки N10 / 08/274) и города Кейптауна.
2.2. Сбор образцов и диагностические тесты. Кровь собирали в простые пробирки BD vacutainer объемом 4 мл (BD Biosciences) и транспортировали в лабораторию в условиях окружающей среды.Затем пробирки центрифугировали при 2500 об / мин в течение 10 минут, после чего сыворотку собирали, разделяли на аликвоты и замораживали (-80 ° C) до использования. Слюну собирали у всех участников в пробирки для слюны (Sarstedt, Numbrecht, Германия) в соответствии с инструкциями производителя. Затем образцы слюны транспортировали на льду (4 ° C) в лабораторию, после чего пробирки для слюны центрифугировали в течение 2 минут (1000 г), слюну собирали, аликвотировали в промаркированные пробирки и хранили при -80 ° C до анализа.
образцов мокроты, собранных у всех участников, были культивированы методом MGIT (BD Biosciences). Положительные образцы MGIT были исследованы на AFB с использованием метода Циля-Нильсена для проверки на загрязнение, после чего были проведены эксперименты с ПЦР для подтверждения выделения комплексных организмов M.tb. Все люди, классифицированные как больные туберкулезом в этом исследовании, имели положительные микробиологические посевы мокроты по комплексу M.tb и другие клинические признаки, соответствующие туберкулезу, включая типичный рентген грудной клетки., растворимый лиганд CD40 (sCD40L), трансформирующий фактор роста (TGF) -a, фактор роста эндотелия сосудов (VEGF), фактор, стимулирующий колонии гранулоцитов (G-CSF), CXCL1 (GRO), C-реактивный белок (CRP), амилоид сыворотки протеин A (SAA), сывороточный амилоидный протеин P (SAP), матриксная металлопротеиназа (MMP) -2 и MMP-9 оценивались в образцах сыворотки и слюны всех участников исследования. Это было сделано с использованием индивидуальных наборов Milliplex (Merck Millipore, Сент-Чарльз, Миссури, США) на платформе Bio-Plex (Bio-Rad Laboratories, Геркулес, Калифорния, США).Все образцы анализировали в неразбавленном виде (за исключением образцов на MMP-2, MMP-9, CRP, SAA и SAP) слепым методом в соответствии с инструкциями производителя (Merck Millipore). Образцы для MMP-2 и MMP-9 были предварительно разведены 1: 100, а образцы для CRP, SAA и SAP были предварительно представлены как 1: 8000, после экспериментов по оптимизации (проведенных на сыворотке). Образцы сыворотки и слюны одного и того же человека оценивались на одном планшете. Уровни всех аналитов в реагентах для контроля качества были в пределах ожидаемых
.Рисунок 1: Уровни маркеров хозяина, обнаруженных в образцах слюны и сыворотки всех участников исследования («= 38).Уровень каждого маркера хозяина, обнаруженного в слюне, был сопоставлен с уровнем, полученным в образце сыворотки от того же участника исследования. Показаны репрезентативные графики для маркеров, более выраженных в слюне.
диапазонов. Программное обеспечение Bio-Plex Manager 6.0 использовалось для сбора гранул и анализа средней интенсивности флуоресценции.
2.4. Статистический анализ. Различия в уровнях аналитов между больными ТБ и участниками, не страдающими ТБ, или между уровнями маркеров, обнаруженных в слюне и сыворотке, оценивали с помощью U-критерия Манна-Уитни для непараметрического анализа данных.Диагностическая точность маркеров была исследована с помощью анализа кривой характеристик оператора приемника (ROC). Оптимальные пороговые значения и связанные с ними чувствительность и специфичность были выбраны на основе отношения наибольшего правдоподобия. Прогностические способности комбинаций аналитов оценивались путем выполнения общего дискриминантного анализа лучших подмножеств (GDA) с перекрестной проверкой исключения по одному. Перед процедурой GDA данные с нестандартным распределением были преобразованы в логарифм. Различия между группами считались значимыми, если значения P были <0.05. Данные анализировали с помощью GraphPad Prism, версия 5.00 (GraphPad Software, Сан-Диего, Калифорния, США) и STATISTICA (StatSoft, Огайо, США).
3. Результаты
Из 38 участников, включенных в это исследование, 27 (71%) были женщинами. Средний возраст всех участников исследования составил 38,0 ± 10,2 года. Из 28 участников исследования с доступными результатами Quantiferon In-Tube 67,9% были положительными при использовании рекомендованного производителем порогового значения (> 0,35 МЕ / мл). Восемь (21%) участников исследования были ВИЧ-инфицированными (таблица 1).
3.1. Маркеры хозяина, обнаруженные в слюне по сравнению с сывороткой. Мы оценили уровни маркеров хозяина выше минимально определяемой концентрации (MDC; получено из вкладыша производителя) в слюне и сыворотке, а затем сравнили уровни маркеров, обнаруженных в слюне, с уровнями, полученными в
.Таблица 1: Демографические и клинические характеристики участников исследования.
Все случаи ТБ Случай без ТБ
Количество участников 38 11 27
Средний возраст (лет) ± стандартное отклонение 38., MCP-1 и sCD40L) были выше, чем MDC, как в сыворотке, так и в образцах слюны всех (100%) участников исследования. Уровни шести (IL-8, G-CSF, TGF-a, EGF, VEGF и GRO) были выше MDC в обоих типах образцов по крайней мере у 90% участников исследования, в то время как уровни IL-4 и IL-9 не обнаруживался или едва обнаруживался в обоих типах образцов у всех участников исследования (таблица 2).
В слюне уровни IFN-γ, IL-1a, IL-12 (p70), IL-13, IL-15, IL-17, фракталкина, GM-CSF и EGF были в среднем в 6 раз выше. образцы от всех участников исследования по сравнению с уровнями сыворотки., GRO и CRP, обнаруженные в образцах сыворотки всех участников исследования по сравнению с уровнями в слюне. Уровни SAA, SAP, sIL-2Ra, sCD40L, MCP-1 и MMP-2 также были значительно выше в сыворотке (таблица 2, рисунок 2). Когда уровни маркеров, полученные в сыворотке, сравнивались с уровнями, полученными в слюне только у больных туберкулезом или не больных туберкулезом, то же выражение
Таблица 2: Доля участников исследования с маркерами хозяина выше минимально определяемой концентрации (MDC) и различиями между слюной и сывороткой.
Маркер MDC (пг / мл) Слюна%> Медиана MDC (IQR)%> Медиана сыворотки MDC (IQR) Значение P
(A) Маркеры хозяина более интенсивно экспрессируются в слюне
Ил-1 «1,5 100,0 4618,9 (1956,3-10000,0) 21,0 0,0 (0,0-0,0) <0,0001
ИЛ-1ß 0,7 95,0 24,6 (12,23-54,7) 18,0 0,0 (0,0-0,2) <0,0001
Ил-2 0,4 97,0 6,5 (2,3-14,4) 32,0 0,0 (0,0-0,6) <0,0001
Ил-5 0.1 32,0 0,0 (0,0-1,1) 0,0 0,0 (0,0-0,0) <0,0001
Ил-7 1,0 45,0 0,0 (0,0-19,0) 16,0 0,0 (0,0-0,0) <0,0001
Ил-8 0,3 100,0 145,2 (78,6-237,3) 97,0 13,6 (6,2-27,7) <0,0001
Ил-10 0,3 39,5 0,0 (0,0-16,8) 2,6 0,0 (0,0-0,0) <0,0001
Ил-12п70 0,9 89,0 9,8 (3,7-16,9) 16,0 0,0 (0,0-0,3) <0,0001
Ил-13 0,3 92,0 20,7 (11,4-34,1) 0,0 0,0 (0,0-0,0) <0,0001
Ил-15 0.6 45,0 0,0 (0,0-8,4) 5,0 0,0 (0,0-0,0) <0,0001
Ил-17 0,4 97,0 13,0 (8,6-18,9) 16,0 0,0 (0,0-0,0) <0,0001
IFN-y 0,4 82,0 4,1 (0,6-10,4) 42,0 0,0 (0,0-5,0) <0,0001
G-CSF 3,9 100,0 1348,0 (842,0-2263,2) 97,0 90,7 (45,3-114,4) <0,0001
GM-CSF 2,3 100,0 100,5 (65,3-137,9) 8,0 0,0 (0,0-0,0) <0,0001
ТГФ- «1,4 100,0 9,5 (6,7-16,6) 92,0 6,9 (3,2-20.8) 0,08
EGF 5,3 100,0 5717,0 (3991,9-7964,4) 97,0 98,6 (45,5-185,1) <0,0001
VEGF 10,1 100,0 618,2 (457,3-802,6) 95,0 303,5 (145,7-493,2) <0,0001
Фракталкин 7,6 97,0 451,8 (137,9-699,9) 10,0 0,0 (0,0-0,0) <0,0001
ММП-9 1,0 100,0 164631,4 (105484,3-348292,9) 100,0 2673,0 (1795,9-3951,6) <0,0001
(B) Маркеры более интенсивно экспрессируются в сыворотке
СИЛ-2Ра 7.5 8,0 0,0 (0,0-0,0) 29,0 0,0 (0,0-10,4) 0,01
GRO 11,4 97,0 132,5 (74,1-204,0) 100,0 1209,1 (856,0-2099,6) <0,0001
ИП-10 1,3 100,0 102,6 (67,4-213,3) 100,0 408,0 (307,4-710,0) <0,0001
MIP-1ß 3,2 100,0 12,0 (8,4-17,0) 100,0 47,7 (22,2-81,3) <0,0001
ГЦН-1 1,2 100,0 124,5 (29,5-204,0) 100,0 473,4 (314,3-644,6) <0,0001
CRP 0,0012 * 71,0 88,2 (0,0-232.0) 100,0 27668,5 (9213,7-127253,2) <0,0001
SAA 0,21 * 50,0 119,5 (0,0-848,8) 97,0 11408,9 (2519,1-95050,4) <0,0001
SAP 0,055 * 21,0 0,0 (0,0-0,0) 100,0 46954,9 (37567,1-60894,8) <0,0001
ММП-2 48 13,0 0,0 (0,0-0,0) 100,0 1148,8 (971,1-1333,0) <0,0001
sCD40L 5,2 100,0 353,8 (166,9-779,2) 100,0 * 705911 (307862-1039000) <0,0001
(C) Нет разницы в уровнях экспрессии между сывороткой и слюной
Ил-4 0.6 0,0 0,0 (0,0-0,0) 0,0 0,0 (0,0-0,0) –
Ил-6 0,4 45,0 0,0 (0,0-37,3) 32,0 0,0 (0,0-11,5) 0,12
Ил-9 1,1 15,8 0,0 (0,0-0,0) 5,3 0,0 (0,0-0,0) 0,14
TNF- «0,2 87,0 10,6 (6,9-20,6) 95,0 11,1 (6,5-13,0) 0,23
Показаны средние уровни биомаркеров, обнаруженных в образцах слюны и сыворотки от всех участников исследования (n = 38), и доля участников, у которых каждый маркер был> MDC., фракталкин , IL-17 и VEGF) значительно различались или демонстрировали тенденции различий между двумя группами (таблица 3)., а уровни фракталкина выявили заболевание туберкулезом со специфичностью> 93% (таблица 3, рисунок 3).
Когда данные, полученные по слюне, были подогнаны к моделям общего дискриминантного анализа (GDA), оптимальный прогноз
Рисунок 2: Уровни маркеров хозяина, обнаруженных в образцах слюны и сыворотки всех участников исследования (n = 38). Уровень каждого маркера хозяина, обнаруженного в слюне, был сопоставлен с уровнем, полученным в образце сыворотки от того же участника исследования.Показаны репрезентативные графики для маркеров, более интенсивно экспрессируемых в сыворотке.
случаев туберкулеза или отсутствия туберкулеза было достигнуто, когда маркеры использовались в комбинации из пяти. Комбинация IL-5, IL-6, IL-15, TNF-a и CRP точно предсказала 81,8% случаев туберкулеза и 81,4% других случаев после перекрестной проверки с исключением одного случая. Наиболее часто встречающиеся аналиты в 20 наиболее точных дискриминирующих моделях включали IL-5, IL-6, IL-15, CRP, TNF-a и GRO (рис. 4).
3.3. Точность маркеров, обнаруживаемых в сыворотке крови при диагностике туберкулеза. Когда уровни сывороточных маркеров, полученные в случаях ТБ, сравнивались с уровнями, полученными в случаях, не являющихся больными, значимые различия были получены для четырех маркеров (IL-6, IL-2, SAP и SAA). Уровни IL-6, IL-2 и SAP были значительно выше в случаях ТБ (P <0,03), в то время как уровни SAA были выше в других случаях (Таблица 4).
Когда диагностическая точность маркеров, обнаруженных в сыворотке, была исследована с помощью анализа кривой ROC, AUC для всех четырех маркеров, которые показали значительные различия (IL-2, IL-6, SAP и SAP), была> 0.70 (таблица 4, рисунок 4). Из четырех маркеров только SAP выявлял заболевание ТБ с чувствительностью до 55%, но специфичность была между 85,2% и 96,3% для всех четырех маркеров на уровнях отсечения, соответствующих наивысшему отношению правдоподобия (таблица 4, рисунок 5). могла предсказать только 54.6% случаев ТБ и 81,5% других случаев после перекрестной проверки исключения по одному. Когда процедура GDA была повторена с объединением данных, полученных из сыворотки и слюны, точность прогнозов моделей увеличилась. Уровни ИЛ-5 и ИЛ-6 в слюне + Г-КСФ, ИЛ-12p70 и ИЛ-6 в сыворотке точно классифицировали все (100%) случаев ТБ и 85,2% всех случаев ТБ после одноразовой перекрестной проверки . Наиболее часто встречающиеся аналиты в прогнозных моделях
, состоящий из маркеров, полученных как из сыворотки, так и из слюны, включает сывороточные IL-6, G-CSF и IL-12p70, а также IL-5, IL-6 и IL-7 из слюны (фиг. 4).
4. Обсуждение
Мы оценили уровни 33 иммунологических биомаркеров хозяина в образцах слюны и сыворотки людей с подозрением на туберкулез легких. Основным выводом нашего исследования была неодинаковая экспрессия маркеров хозяина, которые были обнаружены в обоих типах образцов, с до 6 раз более высокими уровнями некоторых маркеров, экспрессируемых в слюне. Таким образом, мы показали, что слюна, образец которой относительно легко получить, может быть очень ценным образцом в исследованиях по обнаружению биомаркеров туберкулеза.фракталкин, CRP, SAA и SAP в сыворотке или слюне показали потенциал в качестве диагностических кандидатов на ТБ, что подтверждается площадью под кривой ROC.
IL-2 (обзор приведен в [22]) является важным иммуномодулирующим цитокином, который продуцируется несколькими типами клеток, включая активированные Т-клетки, дендритные клетки и NK-клетки, и имеет решающее значение как для иммунных ответов против многих инфекционных заболеваний, так и для для поддержания толерантности [22]. IL-2 широко изучался, особенно в исследованиях на основе Т-клеток, и показал потенциал в качестве диагностического маркера для
Таблица 3: Полезность маркеров хозяина, обнаруженных в слюне, в диагностике туберкулеза.
Маркер ТБ Нет заболевания ТБ Значение P AUC (95% ДИ) Пороговое значение Чувствительность% (95% ДИ) Специфичность% (95% ДИ)
ИЛ-6 37,3 (0,0-52,2) 0,0 (0,0-13,2) 0,019 0,72 (0,54-0,91)> 25,8 63,6 (30,8-89,0) 81,5 (61,9-93,7)
CRP 246,5 (22,0-353,9) 45,9 (0,0-122,0) 0,024 0,74 (0,53-0,94)> 271,7 45,5 (16,8-76,6) 92,6 (75,7-99,0)
ИЛ-9 0,0 (0,0-11,0) 0,0 (0,0-0,0) 0,027 0,65 (0,44-0,86)> 10.3 27,3 (6,0-60,9) 96,3 (81,0-99,9)
Ил-5 0,9 (0,0-9,2) 0,0 (0,0-0,0) 0,033 0,68 (0,48-0,88)> 7,8 27,3 (6,0-61,0) 96,3 (81,0-99,9)
MIP-1j3 17,0 (11,3-22,2) 11,3 (8,4-15,6) 0,039 0,72 (0,54-0,90)> 18,7 45,5 (16,8-76,6) 92,6 (75,7-99,1)
Фракталкин 772,9 (225,8-1148,3) 338,2 (104,3-565,5) 0,041 0,72 (0,52-0,91)> 912,2 36,4 (10,9-69,2) 96,3 (81,0-99,9)
Ил-17 18,9 (7,6-37,0) 12,6 (8.6-16,6) 0,085 0,68 (0,46-0,90)> 29,0 45,5 (16,8-76,6) 96,3 (81,0-99,9)
VEGF 457,3 (307,7-754,9) 680,0 (512,4-802,6) 0,085 0,68 (0,47-0,90) <370,5 45,5 (16,8-76,6) 92,6 (75,7-99,1)
Показаны медианные уровни и межквартильные диапазоны (в скобках) маркеров и способности различать случаи легочного ТБ (n = 11) и лиц без активной формы ТБ (n = 27). Показаны только маркеры, для которых значения UP Манна-Уитни были <0,09.AUC: площадь под кривой характеристик оператора приемника (ROC); 95% ДИ: 95% доверительный интервал. Пороговые значения предназначены для чувствительности и специфичности заболевания ТБ и были выбраны на основе самого высокого отношения правдоподобия. Уровни маркеров указаны в пг / мл, за исключением CRP (нг / мл).
2500 2000 1500 1000 500 0
Значение P | 0,0408
** iS * »
i 150 §100 3 50 0
Значение P | 0.(слюна): кривая ROC
0,0 0,2 0,4 0,6 0,8 1,0 1 – специфичность
0,0 0,1 0,2 0,3 0,4 1 – специфичность
0,0 0,2 0,4 0,6 0,8 1,0 1 – специфичность
CRP (слюна): кривая ROC
0 0,2 0,4 0,6 0,8 1 – специфичность
Рисунок 3: Уровни маркеров, обнаруженных в образцах слюны больных туберкулезом легких и лиц без заболевания туберкулезом, и графики характеристик оператора приемника (ROC), показывающие точность этих маркеров при диагностике заболевания туберкулезом.Столбики ошибок на графиках точечного рассеяния указывают на медианные уровни аналита. Показаны только маркеры, для которых площадь под кривой ROC (AUC) была> 0,70.
ТБ [23, 24]. IL-6 (обзор приведен в [25]) представляет собой плейотропный цитокин и оказывает разнообразное воздействие на регуляцию иммунных ответов, воспаления, онкогенеза и гематопоэза, среди прочего, и широко известен как индуктор острой фазы ответа. Ранее было показано, что IL-6 продуцируется в более высоких концентрациях у больных туберкулезом [26, 27] и был единственным маркером, который показал потенциал в качестве диагностического кандидата в образцах сыворотки и слюны в этом исследовании.показал потенциал в диагностике туберкулеза в слюне, но не в сыворотке крови. CRP, SAA и SAP являются белками острой фазы и составляют
секретируются во время острой фазы воспаления, когда они действуют как опсонины или в рекрутировании клеток в места воспаления [34]. Известно, что эти неспецифические воспалительные маркеры преимущественно продуцируются печенью и были исследованы при многих заболеваниях [34, 35]. Ранее считалось, что СРБ является маркером как диагноза [35, 36], так и степени заболевания туберкулезом [37, 38].SAA считается более чувствительным индикатором воспаления, чем CRP [39], а уровни сыворотки повышаются в 1000 раз в ответ на инфекцию [40]. Подобно SAA, SAP структурно подобен CRP (51% гомология последовательности), и уровни SAP, как было доказано, были высокими при TB на мышиных моделях, тогда как очищенный SAP мыши ингибировал рост M.tb в альвеолярных макрофагах [41]. Наши наблюдения о том, что эти маркеры обладают диагностическим потенциалом для туберкулеза, согласуются с этими предыдущими выводами.
Одним из наиболее заметных наблюдений нашего исследования были заметные различия в уровнях обнаруженных маркеров
Таблица 4: Полезность маркеров хозяина, обнаруженных в сыворотке крови, при диагностике туберкулеза.
Маркерные случаи ТБ Случаи без ТБ Значение P
Ил-6 11,5 (0,0-28,1) 0,0 (0,0-0,0) 0,01
Ил-2 0,6 (0,0-1,3) 0,0 (0,0-0,0) 0,01
SAP 60894,8 (45131,4-65623,2) 42251,4 (36985,9-53804,8) 0,03
SAA 239,1 (0,0-848,8) 6133,8 (2012,1-40010,2) 0,05
Чувствительность отсечки AUC,% Специфичность,%
Значение(95% ДИ) (95% ДИ) (95% ДИ)
21.3 (6,0–61,0) 96,3 (81,0–99,9) 45,5 (16,8–16,6) 92,6 (15,1–99,1)
0,13 (0,54-0,92)> 21,54
0,13 (0,53-0,92)> 0,95
0,12 (0,54-0,90)> 58914 54,6 (23,4-83,3) 85,2 (66,3-95,8)
0,10 (0,52-0,88)> 94 1894 18,2 (2,3-51,8) 96,3 (81,0-99,9)
Показаны медианные уровни (пг / мл) и межквартильные диапазоны (в скобках) маркеров и способности различать случаи легочного ТБ (n = 11) и лиц без активного ТБ (n = 27).• OpH o ‘W N
«В <№ 60 тд
о <»-
футов 1 G 60
‘ю.ш. 60 o
фут
футов ком ftT *
Рис. 4: Частота аналитов в 20 лучших прогностических моделях GDA, которые наиболее точно классифицируют участников исследования как туберкулез или нет. Столбцы представляют, сколько раз каждый аналит был включен в 20 лучших дискриминационных моделей.
♦♦♦♦♦
150000 -,
а 100000-
ди-джей 50000–
Значение P | 0,0350
5000000 -, 4000000 -3000000-2000000 -1000000 -0
Значение P | 0,0575
0,8 0,6 0,4 0,2 0,0
IL-6 (сыворотка): кривая ROC
SAP (сыворотка): кривая ROC
SAA (сыворотка): кривая ROC
‘Площадь | 0.7340
0,00 0,05 0,10 0,15 0,20 1 – специфичность
0,0 0,2 0,4 0,6 0,8 1,0 1 – специфичность
0,0 0,2 0,4 0,6 0,8 1,0 1 – специфичность
Рисунок 5: Уровни маркеров, обнаруженных в образцах сыворотки больных туберкулезом легких и лиц без заболевания туберкулезом, и графики характеристик оператора приемника (ROC), показывающие точность этих маркеров при диагностике заболевания туберкулезом. Столбики ошибок на графиках точечного рассеяния указывают на медианные уровни аналита.Показаны только маркеры, для которых площадь под кривой ROC (AUC) была> 0,70.
в слюне и сыворотке и что более высокие уровни большинства маркеров были получены в слюне. Большинство маркеров, которые в большей степени экспрессировались в сыворотке крови, были хемокинами (IP-10, MIP-1 £ и MCP-1), белками острой фазы (CRP, SAA, SAP), а также sIL-2R и sCD40L, оба являются лигандами для молекулы, необходимые для активации и дифференцировки Т-клеток, и GRO является медиатором ангиогенеза. Более высокие уровни наиболее часто исследуемых провоспалительных цитокинов и факторов роста были получены в слюне.Наши наблюдения согласуются с выводами о том, что слюнная железа является резервуаром многих факторов роста у грызунов [42]. У людей EGF, основной фактор роста фибробластов, инсулин и члены семейства инсулиноподобных факторов роста были обнаружены в слюнных железах, хотя их физиологическая роль остается неясной [42].
Хотя исследования слюны в области биомаркеров туберкулеза ограничены, слюна широко изучалась при других заболеваниях, в частности, при лейкемии, раке полости рта, красном плоском лишае полости рта и пародонтите [43, 44].FDA США одобрило существующие коммерческие экспресс-тесты на ВИЧ на основе слюны [45]. Многие преимущества использования слюны в качестве диагностического образца обсуждались в другом месте [44]. Наши наблюдения подтверждают потенциальную пользу слюны для исследования биомаркеров туберкулеза. Высокие уровни маркеров хозяина в слюне подразумевают, что эти маркеры можно более надежно измерить даже с помощью устройств с боковым потоком, которые обычно просты в использовании и подходят даже для удаленных настроек, но часто имеют низкие пределы обнаружения.Хотя диагностические тесты, основанные на воспалительных маркерах слюны, могут быть недостаточно специфичными, поскольку уровни этих маркеров могут быть высокими и при других заболеваниях, эти маркеры могут быть полезны в сочетании с клинической информацией. Такие тесты будут очень полезны в области диагностики туберкулеза, учитывая трудности, возникающие при диагностике туберкулеза при получении недостаточного количества мокроты и невозможности отхаркивания, как у маленьких детей [9], и в случаях внелегочного туберкулеза. Все больные туберкулезом, оцениваемые в этом исследовании, были взрослыми, и у всех был диагностирован туберкулез легких.На основании данных, представленных в этом исследовании, мы не можем установить, будут ли эти маркеры полезными для детей и для пациентов с внелегочным туберкулезом. Следовательно, необходимы дальнейшие исследования у детей, больных внелегочным туберкулезом и других заболеваний легких. Дети и, в частности, больные внелегочным туберкулезом получат наибольшую пользу от новых, простых в выполнении диагностических тестов, не основанных на выделении спермы. Хотя использование биосигнатуры, содержащей воспалительные цитокины, очень желательно и необходимо в диагностической области ТБ, важно предупредить, что большинство маркеров, идентифицированных в этом исследовании (например,g., белки острой фазы) будут повышены при других инфекционных заболеваниях. Следовательно, данные, полученные с помощью таких диагностических методов, необходимо будет интерпретировать с учетом клинической картины пациента.
Это исследование было проведено в качестве пилотного для более крупного, продолжающегося исследования и, как таковое, было ограничено небольшим размером выборки и отсутствием людей с другими легочными инфекциями. Однако наши наблюдения послужат подтверждением концепции для дальнейших исследований в этой области, учитывая тот факт, что диагностические тесты, основанные на легко доступных образцах, таких как слюна, произведут революцию в диагностике туберкулеза, особенно если таких маркеров
.встроен в устройства с боковым потоком.Мы не исследовали влияние факторов, таких как потребление пищи или напитков, до отбора проб на уровни биомаркеров слюны. Возможное влияние таких факторов может потребовать дальнейшего изучения.
5. Выводы
В заключение, данные, представленные в этом исследовании, указывают на то, что существует много различий в уровнях маркеров хозяина, экспрессируемых в слюне, по сравнению с уровнями сыворотки, и некоторые маркеры, обнаруженные в обоих типах образцов, имеют потенциал в диагностике туберкулеза.Наши результаты показывают, что слюна может быть лучшей альтернативой сыворотке в исследованиях по обнаружению биомаркеров туберкулеза. Наши результаты требуют дальнейшего изучения в более крупных исследованиях.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов относительно публикации данной статьи.
Благодарности
Авторы благодарны участникам исследования, нашим медсестрам-исследователям, особенно г-же Ширли Маканда, и членам исследовательской группы SUN-Immunology за их различные роли в обеспечении доступности данных, необходимых для этой статьи.Эта работа финансировалась EDCTP через Африканско-европейский туберкулезный консорциум (AE-TBC, грант № IP_2009_32040) и Испытания передового опыта в Южной Африке (TESA, код проекта CG_cb_07_41700), главный исследователь: профессор Герхард Вальцл. NN Chegou был поддержан докторскими стипендиями Фонда Клода Леона и Южноафриканского MRC.
Список литературы
[1] Всемирная организация здравоохранения, «Глобальный отчет по туберкулезу 2012», Tech.Реп., 2012.
[2] C. J. L. Murray, E. DeJonghe, H. J. Chum, D. S. Nyangulu, A. Salomao и K. Styblo, «Экономическая эффективность химиотерапии туберкулеза легких в трех странах Африки к югу от Сахары», The Lancet, vol. 338, нет. 8778, pp. 1305-1308, 1991.
[3] Л. Аперс, Дж. Муцвангва, Дж. Магвензи и др., «Сравнение прямой микроскопии, метода концентрации и пробирки индикатора роста микобактерий для исследования мокроты на кислотоустойчивые бациллы», Международный журнал Туберкулез и болезни легких, т.7, вып. 4. С. 376-381, 2003.
.[4] Н. Н. Чегу, К. Г. Хук, М. Криэль, Р. М. Уоррен, Т. К. Виктор и Г. Вальцл, «Тесты на туберкулез: прошлое, настоящее и будущее», Expert Review of Anti-Infective Therapy, vol. 9, вып. 4. С. 457469, 2011.
.[5] Б. А. Ханна, А. Эбрагимзаде, Л. Б. Эллиотт и др., «Многоцентровая оценка системы BACTEC MGIT 960 для восстановления микобактерий», Журнал клинической микробиологии, вып. 37, нет. 3. С. 748-752, 1999.
[6] C. C. Boehme, P. Nabeta, D. Hillemann et al., «Быстрое молекулярное обнаружение туберкулеза и устойчивости к рифампицину», Медицинский журнал Новой Англии, вып. 363, нет. 11. С. 1005-1015, 2010.
[7] К. Р. Стейнгарт, Х. Зон, И. Шиллер и др., «Анализ Xpert (R) MTB / RIF для выявления туберкулеза легких и устойчивости к рифампицину у взрослых», Кокрановская база данных систематических обзоров, том. 1, Код статьи CD009593, 2013.
[8] А.Требук, Д. А. Энарсон, К. Ю. Чианг и др., «Xpert MTB / RIF для национальных программ борьбы с туберкулезом в странах с низким уровнем дохода: когда, где и как?» Международный журнал туберкулеза и болезней легких, вып. 15, вып. 12. С. 1567-1572, 2011.
.[9] Б. Дж. Марэ и М. Пай, «Новые подходы и появляющиеся технологии в диагностике детского туберкулеза», Pediatric Respiratory Reviews, vol. 8, вып. 2. С. 124-133, 2007.
.[10] Н. Н. Чегу, Г. Вальцл, К.Т. Боллигер, А. Х. Диакон и М. М. ван ден Хеувел, “Оценка адаптированных тестов высвобождения интерферона цельной крови для диагностики туберкулеза плевры”, Дыхание, т. 76, нет. 2. С. 131-138, 2008.
.[11] М. Э. Мунк, С. М. Аренд, И. Брок, Т. Х. М. Оттенхофф и П. Андерсен, «Использование антигенов ESAT-6 и CFP-10 для диагностики внелегочного туберкулеза», Journal of Infectious Diseases, vol. 183, нет. 1. С. 175-176, 2001.
.[12] Р.Г. Шиппер, Э. Силлетти и М. Х. Вингерхоедс, “Слюна как материал исследования: биохимические, физико-химические и практические аспекты”, Archives of Oral Biology, vol. 52, нет. 12. С. 1114-1135, 2007.
.[13] A. Gustafsson, V Ajeti и L. Ljunggren, «Обнаружение suPAR в слюне здоровых молодых людей: сравнение с уровнями в плазме», Biomarker Insights, vol. 6. С. 119-125, 2011.
.[14] Н. Пант Пай, Р. Джоши, С. Догра и др., «Оценка диагностической точности, осуществимости и предпочтений клиентов для быстрой диагностики ВИЧ-инфекции на основе жидкостей полости рта в сельских районах Индии», PLoS ONE, vol.2, вып. 4, статья е367, 2007.
[15] К. Беме, Е. Молокова, Ф. Минья и др., «Обнаружение микобактериального липоарабиноманнана с помощью ELISA с захватом антигена в необработанной моче танзанийских пациентов с подозрением на туберкулез», Труды Королевского общества тропической медицины и Гигиена, т. 99, нет. 12. С. 893-900, 2005.
.[16] С. Ф. Кингсмор, “Мультиплексное измерение белков: технологии и применение массивов белков и антител”, Nature Reviews Drug Discovery, vol.5, вып. 4. С. 310-320, 2006.
.[17] J. L. Luque-Garcia и T. A. Neubert, «Подготовка образцов для анализа профиля сыворотки / плазмы и идентификации биомаркеров с помощью масс-спектрометрии», Journal of Chromatography A, vol. 1153, нет. 1-2, стр. 259-276, 2007.
[18] R. Mutetwa, C. Boehme, M. Dimairo et al., «Диагностическая точность коммерческого обнаружения липоарабиноманнана в моче у подозреваемых на туберкулез и пациентов в Африке», International Journal of Tuberculosis and Lung Disease, vol.13, вып. 10. С. 1253-1259, 2009.
.[19] A. Thakur, L.E. Pedersen и G. Jungersen, “Иммунные маркеры и корреляты защиты для иммунных ответов, индуцированных вакциной”, Vaccine, vol. 30, стр. 4907-4920, 2012.
[20] Р. С. Уоллис, П. Ким, С. Коул и др., «Открытие биомаркеров туберкулеза: разработки, потребности и проблемы», The Lancet Infectious Diseases, vol. 13, стр. 362-372, 2013.
[21] Г. Вальцль, К. Ронахер, В.Ханеком, Т. Дж. Скриба и А. Зумла, “Иммунологические биомаркеры туберкулеза”, Nature Reviews Immunology, vol. 11, вып. 5. С. 343-354, 2011.
.[22] Т. Р. Малек, “Биология интерлейкина-2”, Ежегодный обзор иммунологии, вып. 26, стр. 453-479, 2008.
[23] Р. Бизелли, С. Мариотти, В. Саргентини и др., «Обнаружение интерлейкина-2 в дополнение к интерферону-γ позволяет различать пациентов с активным туберкулезом, лиц с латентной инфекцией и контрольную группу», «Клиническая микробиология и инфекция, т. .16, нет. 8. С. 1282-1284, 2010.
.[24] С. Ван, Н. Диао, К. Лу и др., «Оценка диагностического потенциала IP-10 и IL-2 в качестве биомаркеров для диагностики активного и латентного туберкулеза в популяции, вакцинированной БЦЖ». “PLoS ONE, vol. 7, код статьи e51338, 2012.
[25] Т. Кишимото, “IL-6: от его открытия до клинического применения”, Международная иммунология, вып. 22, нет. 5. С. 347-352, 2010.
.[26] Дж. Ф. Джоба Сиавая, Н.Бейерс, П. ван Хелден и Г. Вальцл, “Дифференциальная секреция цитокинов и ранний ответ на лечение у пациентов с туберкулезом легких”, Клиническая и экспериментальная иммунология, вып. 156, нет. 1. С. 69-77, 2009.
[27] R. Hussain, A. Kaleem, F. Shahid et al., «Профили цитокинов с использованием анализов цельной крови могут различать пациентов с туберкулезом и здоровых эндемичных контрольных групп в популяции, вакцинированной БЦЖ», Journal ofImmunological Methods, vol. 264, нет. 1-2, с. 95-108, 2002.
[28] П. Фратичелли, М. Сирони, Г. Бьянки и др., «Фракталкин (CX3CL1) как схема усиления поляризованных ответов Th2», Журнал клинических исследований, т. 107, нет. 9. С. 1173-1181, 2001.
.[29] T. Lehner, Y. Wang, T. Whittall и T. Seidl, “Врожденный иммунитет и инфекция ВИЧ-1”, “Достижения в стоматологических исследованиях”, вып. 23, нет. 1. С. 19-22, 2011.
.[30] М. Маурер и Э. фон Стебут, «Макрофагальный воспалительный белок-1», Международный журнал биохимии и клеточной биологии, вып.36, нет. 10. С. 1882–1886, 2004.
.[31] Н. Н. Чегу, Г. Ф. Блэк, М. Кидд, П. Д. ван Хелден и Г. Вальцл, «Маркеры хозяина в супернатантах Quantiferon позволяют дифференцировать активный ТБ от латентной ТБ-инфекции: предварительный отчет», BMC Pulmonary Medicine, vol. 9, статья 21, 2009.
[32] К. Л. Келлар, Дж. Герке, С. Е. Вайс и др., «Множественные цитокины высвобождаются, когда кровь больных туберкулезом стимулируется антигенами Mycobacterium tuberculosis», PLoS ONE, vol.6, вып. 11, Идентификатор статьи e26545, 2011.
[33] Н. Н. Чегу, А. К. Детжен, Л. Тиарт и др., «Полезность маркеров хозяина, обнаруженных в супернатантах квантиферона, для диагностики туберкулеза у детей в условиях тяжелого бремени», PLoS ONE, vol. 8, код статьи e64226, 2013.
[34] Э. Грюс, М. Дж. М. Туссен, Т. А. Невольд и С. Дж. Купманс, «Реакция острой фазы и белки острой фазы», Журнал Чжэцзянского университета, вып. 6, вып. 11. С. 1045-1056, 2005.
[35] М. К. Шейх, Дж. А. Само, Б. Р. Девраджани, С. З. А. Шах, С. Шейх и И. Шейх, «С-реактивный белок у пациентов с туберкулезом легких», журнал World Applied Sciences Journal, вып. 17, нет. 2. С. 140–144, 2012.
.[36] Д. Уилсон, М. Бадри и Г. Маартенс, «Эффективность сывороточного c-реактивного белка в качестве скринингового теста на туберкулез с отрицательным мазком мокроты в амбулаторной популяции с высокой распространенностью ВИЧ», PLoS ONE, vol. 6, вып. 1, идентификатор статьи e15248, 2011 г.
[37] L. Haghighi и J. Y. Doust, “C-реактивный белок при туберкулезе легких”, Diseases of the Chest, vol. 50, нет. 6. С. 624-626, 1966.
.[38] С. Рао и В. Бернхардт, “С-реактивный белок сыворотки при туберкулезе легких: корреляция с бактериологической нагрузкой и степенью заболевания”, Инфекционные заболевания в клинической практике, вып. 17, нет. 5. С. 314-316, 2009.
.[39] Дж. Г. Рейнс и Э. Х. Купер, «Сравнение сывороточных концентраций амилоидного белка А и С-реактивного белка при раке и незлокачественных заболеваниях», Журнал клинической патологии, вып.36, нет. 7. С. 798-803, 1983.
[40] Н. Эриксен, «Семейство липопротеинов амилоидного протеина А сыворотки», в Acute Phase Proteins: Molecular Biology Biochemistry and Clinical Applications, A. Mackewicz, I. Kushner, and H. Boumann, Eds., Pp. 93- 106, CRC Press, Бока-Ратон, Флорида, США, 1993.
[41] П. П. Сингх и С. Каур, “Амилоидный Р-компонент сыворотки при туберкулезе мышей: индукционная кинетика и внутримакрофагальное ингибирование роста Mycobacterium tuberculosis in vitro”, Microbes and Infection, vol.ala, S. Warnakulasuriya и др., “Оценка окислительного стресса и антиоксидантного профиля у пациентов с красным плоским лишаем полости рта”, Journal of Oral Pathology and Medicine, vol. 40, нет. 4. С. 286-293, 2011.
.[44] Э. Кауфман и И. Б. Ламстер, «Диагностические применения слюны – обзор», Critical Reviews in Oral Biology and Medicine, vol. 13, вып. 2. С. 197-212, 2002.
.[45] Б. М. Брэнсон, “FDA одобряет OraQuick для использования в слюне.

 Чувствительность ПЦР так высока, что в некоторых случаях этот анализ позволяет обнаружить туберкулез даже тогда, когда все другие методики показывают отрицательный результат.
Чувствительность ПЦР так высока, что в некоторых случаях этот анализ позволяет обнаружить туберкулез даже тогда, когда все другие методики показывают отрицательный результат.