Мастопатия и профилактика рака молочной железы как междисциплинарная проблема | Керчелаева С.Б., Сметник А.А., Беспалов В.Г.
В статье освещена междисциплинарная проблема мастопатии и профилактики рака молочной железы
Проблема заболеваний молочной железы (МЖ) остается актуальной не только в России, но и во всем мире, поскольку распространенность как доброкачественных, так и злокачественных поражений МЖ растет повсеместно. Частота мастопатии в популяции российских женщин достигает 50–60%. Нельзя недооценивать роль мастопатии в развитии рака молочной железы (РМЖ), хотя в целом она не рассматривается как предрак или стадия онкологического процесса в МЖ, однако многие ее формы существенно повышают риск развития РМЖ. Не вызывает сомнений междисциплинарность мастопатии как проблемы. Так, согласно приказу МЗ РФ № 572н от 2012 г., медицинскую помощь женщинам с целью выявления заболеваний МЖ оказывает врач акушер-гинеколог. Патогенетическое же лечение мастопатии должно быть направлено на нормализацию гормонального баланса в организме женщины, прежде всего баланса половых гормонов, что является сферой интересов эндокринологов. При подозрении на очаговую или злокачественную патологию МЖ необходима консультация онколога-маммолога. Также порой требуется вмешательство других специалистов для коррекции заболеваний, которые повлекли развитие мастопатии, например, заболеваний печени, нервной системы и т. д. Таким образом, одну пациентку могут вести сразу несколько специалистов, взаимодействуя и дискутируя между собой. Поэтому в данной публикации мы обсудим мастопатию с позиции трех экспертов: акушера-гинеколога, гинеколога-эндокринолога и онколога, которые выскажут свои взгляды на патогенез и лечение мастопатии, ее роль в развитии РМЖ и тактику ведения пациенток с данной патологией.Профессор С.Б. Керчелаева
ГБОУ ВО «РНИМУ им.
 Н.И. Пирогова» МЗ РФ, Москва
Н.И. Пирогова» МЗ РФ, Москва Эпидемиология. Известно, что в разных странах популяционные риски развития РМЖ неодинаковы. В России в 2013 г. заболеваемость РМЖ составила 320 на 100 тыс. населения, т. е. примерно 0,008% женской популяции ежегодно. Из 741 пациентки, жительниц Ганы, обратившихся за маммологической помощью, масталгия была основным симптомом в 50,2% случаев. РМЖ был диагностирован у 7,8% пациенток, рецидивирующий рак – у 0,8% пациенток. В остальных случаях (около 88%) масталгия не была ассоциирована со злокачественной трансформацией тканей МЖ [1, 2]. В ходе изучения связи между циклической масталгией и РМЖ с участием 5463 женщин 28% (1529 пациенток) сообщили о боли в груди. При этом у 15,8% был диагностирован РМЖ [3]. Таким образом, надо понимать, что масталгия не является маркером раковой трансформации, но ее следует признать значимым фактором риска.
В общей популяции фиброзно-кистозная болезнь встречается у 60–80% женщин, причем пациентки репродуктивного возраста с гинекологическими заболеваниями в анамнезе обеспечивают самый высокий процент. Клинические проявления мастопатии не только ухудшают качество жизни пациенток, но и повышают риск развития РМЖ в десятки раз [4]. Со стороны акушеров-гинекологов незаслуженно мало внимания уделяется доброкачественным заболеваниям МЖ. Клинические симптомы мастопатии приравнивают к норме, хотя это, как правило, свидетельствует о патологическом процессе.
 д., у 10,9% пациенток причиной была боязнь идти к врачу, в 6,5% случаев женщины занимались самолечением, что приводило к резкому прогрессированию заболевания. Однако в 32,5% случаев запущенность заболевания лежит на совести врачей общей лечебной сети ввиду их низкой онкологической грамотности и отсутствия онкологической настороженности. У 51,7% больных от момента появления клинических признаков РМЖ до постановки диагноза проходило от 1 до 6 мес. [5].
д., у 10,9% пациенток причиной была боязнь идти к врачу, в 6,5% случаев женщины занимались самолечением, что приводило к резкому прогрессированию заболевания. Однако в 32,5% случаев запущенность заболевания лежит на совести врачей общей лечебной сети ввиду их низкой онкологической грамотности и отсутствия онкологической настороженности. У 51,7% больных от момента появления клинических признаков РМЖ до постановки диагноза проходило от 1 до 6 мес. [5]. В любом современном государстве основу профилактики составляют скрининговые программы, причисленные по значимости к государственным программам, а борьба с раковыми опухолями на мировом уровне включена в глобальные задачи человечества.
С 2009 г. на основании приказа № 808 МЗ РФ выявление и терапия заболеваний МЖ входят в сферу ответственности акушеров-гинекологов, тогда как ранее этими вопросами занимались исключительно маммологи и хирурги.
Анатомия и физиология. МЖ – это гормонозависимые органы, входящие в репродуктивную систему женщины, которые развиваются и начинают функционировать под влиянием целого комплекса гормонов: рилизинг-факторов гипоталамуса, гонадотропных гормонов гипофиза (фолликулостимулирующего и лютеинизирующего), хорионического гонадотропина, пролактина, тиреотропного гормона, кортикостероидов, инсулина, эстрогенов, прогестерона, андрогенов. МЖ в своем развитии проходят несколько этапов. После рождения МЖ представляют собой рудиментарные образования. В период полового созревания, когда у девочек начинают функционировать яичники, МЖ начинают увеличиваться в объеме, и с наступлением менструальной функции ткань МЖ подвергается ежемесячным циклическим изменениям в соответствии с фазами менструального цикла.
 С прекращением менструальной функции ткань МЖ подвергается инволютивным изменениям, а именно жировому перерождению. Паренхима МЖ представлена сложными альвеолотрубчатыми железами, собранными в мелкие дольки, из которых формируются крупные доли. В МЖ имеется от 6 до 24 долей. Каждая из них имеет свой выводной проток, некоторые протоки могут сливаться перед выходом на поверхность соска.
С прекращением менструальной функции ткань МЖ подвергается инволютивным изменениям, а именно жировому перерождению. Паренхима МЖ представлена сложными альвеолотрубчатыми железами, собранными в мелкие дольки, из которых формируются крупные доли. В МЖ имеется от 6 до 24 долей. Каждая из них имеет свой выводной проток, некоторые протоки могут сливаться перед выходом на поверхность соска.Кровоснабжение МЖ осуществляется за счет внутренней грудной и подмышечной артерий и ветвей межреберных артерий. Вены МЖ сопровождают артерии и широко анастамозируют с венами окружающих областей.
Патогенез. По определению ВОЗ, мастопатия – это фиброзно-кистозная болезнь с нарушением соотношения эпителиального и соединительнотканного компонента, с разнообразными пролиферативными и регрессивными изменениями в тканях МЖ. У термина «мастопатия» имеется множество синонимов, наиболее часто используют такие как «фиброзно-кистозная болезнь», «доброкачественная дисплазия молочных желез», однако обобщающим считают термин «нераковые заболевания молочных желез».
В России для диагностики нераковых заболеваний МЖ применяют клинико-рентгенологическую классификацию мастопатии Н.И. Рожковой [6], согласно которой выделяют 5 форм диффузной мастопатии:
с преобладанием:
– железистого компонента;
– фиброзного компонента;
– кистозного компонента;
– смешанную форму диффузной фиброзно-кистозной мастопатии;
– склерозирующий аденоз.
Кроме того, по результатам биопсии устанавливают диагноз в соответствии с гистологической классификацией опухолей МЖ (ВОЗ, 1995).
Различают морфологически непролиферативную и пролиферативную формы доброкачественной дисплазии.
 При этом риск малигнизации при непролиферативной форме составляет 0,86%, при умеренной пролиферации – 2,34%, при резко выраженной пролиферации – 31,4% наблюдений. По данным гистологических исследований операционного материала, РМЖ сочетается с фиброзно-кистозной болезнью в 46% случаев [7].
При этом риск малигнизации при непролиферативной форме составляет 0,86%, при умеренной пролиферации – 2,34%, при резко выраженной пролиферации – 31,4% наблюдений. По данным гистологических исследований операционного материала, РМЖ сочетается с фиброзно-кистозной болезнью в 46% случаев [7]. Из вышеизложенного следует, что в противораковой борьбе большое значение имеют своевременное выявление и лечение нераковых заболеваний МЖ.
Диагностика заболеваний молочной железы основывается на осмотре МЖ, их пальпации, что должно проводиться с особой тщательностью и онкологической настороженностью. Физикальное обследование включает пальпацию МЖ, регионарных лимфоузлов (подключичных, надключичных, подмышечных).
Из дополнительных методов используются маммография, УЗИ, пункции узловых образований и подозрительных участков и цитологическое исследование пунктата.
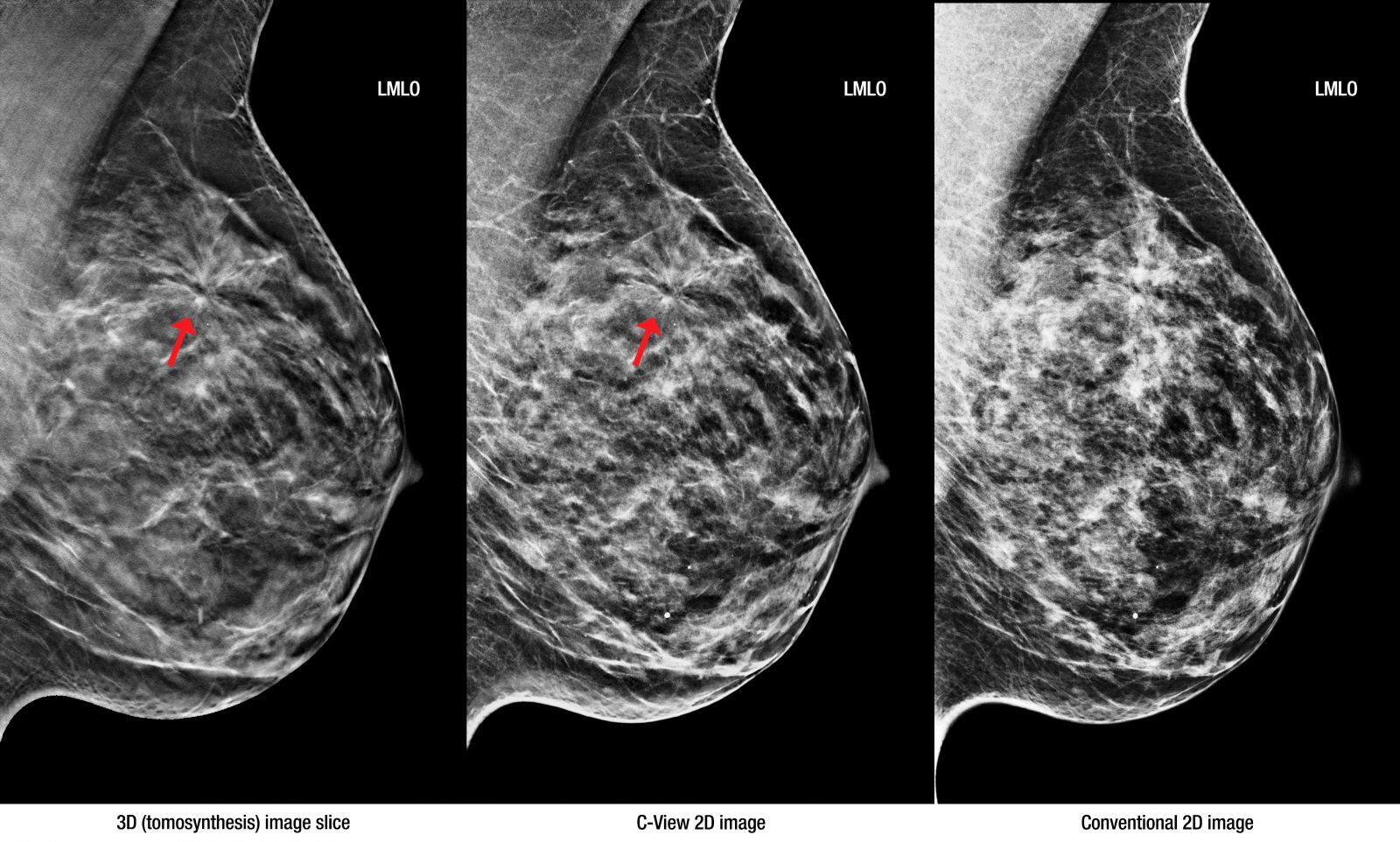 Кроме того, необходимо руководствоваться приказом № 572н, который регламентирует обязательное скрининговое обследование женщин старше 35 лет.
Кроме того, необходимо руководствоваться приказом № 572н, который регламентирует обязательное скрининговое обследование женщин старше 35 лет. Международная ассоциация специалистов репродуктивной медицины, Российская ассоциация маммологов предложила Правила маммологического скрининга для акушера-гинеколога: каждую женщину моложе 35 лет необходимо опрашивать для выявления прогностических факторов РМЖ (разница между ростом в сантиметрах и массой тела в килограммах более 110, возраст начала менструации – до 13 лет, гинекологические заболевания в анамнезе (миома матки, полип матки, эндометриоз, кисты яичников, дисфункция яичников, бесплодие и др.), отсутствие родов, первые роды в возрасте старше 30 лет, стрессовые ситуации, ушибы, маститы, операции на МЖ, онкологические заболевания у близких родственников). Мануальное обследование проводить всем; при наличии факторов риска РМЖ, но при отсутствии изменений молочных желез направлять на УЗИ. При наличии пальпаторных изменений направлять не только на УЗИ, но и на маммографию.
Главная цель первичных диагностических мероприятий – определить характер процесса. При обнаружении узлового очага пациентку нужно направить к рентгеномаммологу, который выполнит биопсию с цитологическим и гистологическим исследованием пунктата. С учетом результата пациентка будет направлена к маммологу-онкологу, который будет заниматься ее лечением. При диффузном процессе пациенткой должен заниматься акушер-гинеколог, который проведет полное обследование, в т. ч. и гормонального статуса, для дальнейшего консервативного лечения и мониторинга. При обнаружении галактореи (вне беременности и лактации) необходимо определить концентрацию гормона пролактина и тиреотропного гормона, а также взять отпечаток-мазок отделяемого для цитологического исследования.
 В зависимости от его результатов решается вопрос о дальнейшем ведении пациентки. Гиперпролактинемия – одна из причин эстроген-прогестеронового дисбаланса, именно пролактин стимулирует рост числа эстрогеновых рецепторов в тканях МЖ, повышает чувствительность клеток к действию эстрадиола и ускоряет пролиферацию эпителиальных клеток.
В зависимости от его результатов решается вопрос о дальнейшем ведении пациентки. Гиперпролактинемия – одна из причин эстроген-прогестеронового дисбаланса, именно пролактин стимулирует рост числа эстрогеновых рецепторов в тканях МЖ, повышает чувствительность клеток к действию эстрадиола и ускоряет пролиферацию эпителиальных клеток.Профилактика заболеваний молочной железы. Основная задача акушера-гинеколога – вести среди женского населения пропаганду против абортов, проводить своевременное лечение воспалительных заболеваний органов малого таза, коррекцию нарушений менструального цикла на всех этапах жизни женщины, коррекцию хронической ановуляции, лечение эндометриоза, миомы матки, полипов матки, опухоли яичников. Перечисленные состояния характеризуются гормональным дисбалансом и дефицитом прогестерона, все это приводит к отеку и гипертрофии внутридольковой соединительной ткани, пролиферации протокового эпителия, что является причиной обтурации протоков и образования кист. Гиперэстрогенизм вследствие недостаточной лютеиновой фазы цикла обусловливает развитие дисгормональных дисплазий МЖ у женщин репродуктивного возраста.
Негормональная базовая терапия диффузной формы нераковых заболеваний МЖ включает: коррекцию диеты, психологическую коррекцию, нормализацию функционального состояния печени, желудочно-кишечного тракта, использование мочегонных средств, препаратов, улучшающих кровоснабжение, использование арсенала фитотерапии.
Многие специалисты сегодня задаются вопросом: есть ли возможности прогнозирования РМЖ? На основании исследовательских работ результаты экспериментов показали, что большая часть канцерогенного влияния эстрогенов связана с образованием агонистических метаболитов эстрогенов, преимущественно 16-гидроксиэстрогена (16-ОНЕı). Другие метаболиты, такие как 2-гидроксиэстрон (2-ОНЕı) и 2-гидроксиэстрадиол, обеспечивают протективное действие, выступая как антагонисты 16-гидроксиэстрогена [9, 10].
 Установлено, что при нормальном соотношении стероидных гормонов в организме женщины концентрация метаболита 2-ОНЕı превышает концентрацию 16-ОНЕı не менее чем в 2 раза. Уменьшение этого соотношения признано фактором риска РМЖ. Таким образом, соотношение 2-ОНЕı к 16-ОНЕı менее 2,0 можно считать адекватным универсальным биомаркером и надежным диагностическим критерием для определения риска и прогноза развития эстрогензависимых опухолей [8, 11].
Установлено, что при нормальном соотношении стероидных гормонов в организме женщины концентрация метаболита 2-ОНЕı превышает концентрацию 16-ОНЕı не менее чем в 2 раза. Уменьшение этого соотношения признано фактором риска РМЖ. Таким образом, соотношение 2-ОНЕı к 16-ОНЕı менее 2,0 можно считать адекватным универсальным биомаркером и надежным диагностическим критерием для определения риска и прогноза развития эстрогензависимых опухолей [8, 11].Заключение. Долгое время считали, что мастопатия – это не заболевание, поскольку очаги фиброза и кисты в МЖ очень распространены, а потому не требуют лечения. Однако сегодня, изучая данную проблему, мы пришли к выводу, что указанные изменения нельзя считать вариантом нормы. Сегодня нераковые заболевания МЖ следует рассматривать как маркер гормонального и тканевого неблагополучия МЖ, а также как фактор онкологической настороженности. Нераковые заболевания МЖ необходимо активно выявлять и лечить, тем самым обеспечить женщине приемлемое качество жизни и проведение онкопрофилактики.
Риск рака молочной железы и половые гормоны
К.м.н. А.А. Сметник
ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» МЗ РФ, Москва
Молочная железа является органом-мишенью для большого количества гормонов и факторов роста, среди которых одну из ведущих ролей играют половые гормоны и экспрессия соответствующих рецепторов [12].
Клетки МЖ, экспрессирующие эстрогеновые рецепторы (ЭР), пролиферируют медленно, в отличие от ЭР-негативных клеток, которые митотически активны. Пролиферация здорового эпителия, не содержащего ЭР или прогестероновые рецепторы (ПР), происходит за счет паракринных эффектов от рядом расположенных покоящихся ЭР-позитивных клеток. В отличие от этого в опухолевых рецептор-позитивных клетках митозы регулируются аутокринными механизмами. В менструальном цикле в МЖ происходят последовательные волнообразные процессы пролиферации и апоптоза. Эндогенный прогестерон в синергизме с эстрадиолом способны стимулировать процессы пролиферации и апоптоза в МЖ, васкуляризацию, выработку протеогликанов, аккумуляцию жидкости в ткани МЖ, что приводит к субъективным ощущениям нагрубания МЖ и повышению маммографической плотности в лютеиновую фазу менструального цикла [13]. Именно в лютеиновую фазу в МЖ наблюдается максимальная частота митозов [14].
Эндогенный прогестерон в синергизме с эстрадиолом способны стимулировать процессы пролиферации и апоптоза в МЖ, васкуляризацию, выработку протеогликанов, аккумуляцию жидкости в ткани МЖ, что приводит к субъективным ощущениям нагрубания МЖ и повышению маммографической плотности в лютеиновую фазу менструального цикла [13]. Именно в лютеиновую фазу в МЖ наблюдается максимальная частота митозов [14].
МЖ является местом локального биосинтеза и метаболизма половых гормонов. К ферментам, участвующим в локальном синтезе и метаболизме эстрогенов, относятся ароматаза (переход андрогенов в эстрогены), сульфатаза (переход неактивных сульфатных форм эстрогенов в активные), 17-дигидрогеназа I и II (из эстрона в эстрадиол и наоборот), сульфотрансфераза (образование сульфатных форм) [15]. Возможно, высокая распространенность гормонально зависимого рака в период низкой продукции половых гормонов яичниками (в постменопаузе) обусловлена отчасти ролью данных ферментных систем. Активность эстронсульфатазы в опухолевой ткани МЖ в 10–500 раз выше активности ароматазы. Также важную роль играют гидроксиметаболиты эстрогенов и ряд метаболитов прогестерона, которые оказывают пролиферативные либо антипролиферативные эффекты [16].
Клинические и экспериментальные данные о роли гормонов в развитии мастопатии зачастую противоречивы. Тем не менее, мастопатия является гормонозависимым заболеванием, обусловленным дисбалансом в гипоталамо-гипофизарно-яичниковой системе.
Если говорить о развитии РМЖ, то переход в гормонозависимой регуляции с паракринного на аутокринный механизм – важная часть опухолевого процесса [12, 17]. Андрогеновые рецепторы присутствуют в 70–80% случаев РМЖ (экспрессируются чаще, чем ЭР или ПР). В случае коэкспрессии андрогеновых рецепторов при ЭР-позитивных раках прогноз обычно лучше. Однако при ЭР-негативном раке андрогеновые рецепторы часто служат компенсаторным механизмом для роста опухоли [18]. Факторы риска РМЖ приведены в таблице 1 [19].
На приеме гинеколога-эндокринолога одним из самых частых вопросов со стороны пациенток является вопрос о возможности назначения им, в зависимости от возраста, комбинированных оральных контрацептивов (КОК) или менопаузальной гормонотерапии (МГТ). Врачу же приходится оценивать безопасность гормональной терапии в каждом конкретном случае, в т. ч. с позиций возможного влияния на риск РМЖ. Общепринятым является положение о том, что изменения синтеза и метаболизма эстрогенов и прогестерона имеют фундаментальное значение для риска развития РМЖ [21].
В случае сочетания мастопатии с гинекологическими заболеваниями, требующими гормональной коррекции, назначение последней возможно.
Метаанализ 13 проспективных когортных исследований КОК не выявил значимого повышения риска РМЖ. Однако различные типы гестагенов в составе КОК также по-разному влияют на различные прогестероновые рецепторы [22]. Например, согласно данным Ruan X. et al. (2012), следующие гестагены, входящие в состав КОК, повышали пролиферацию в культуре клеток РМЖ (MCF-7) при высоких концентрациях: дроспиренон, левоноргестрел, дезогестрел. В отличие от этого, пролиферативный эффект отсутствовал в случае хлормадинона ацетата и номегестрола ацетата [23].
В постменопаузе в опухолевой ткани МЖ концентрация локального эстрадиола в 20–50 раз выше, чем в плазме (результат локальной конверсии из андрогенов, эстрона и эстрона сульфата). При этом не наблюдаются значимые различия в концентрациях эстрадиола: в крови при РМЖ и в норме; в самой МЖ при раке в репродуктивном возрасте и постменопаузе; локально при РМЖ в постменопаузе на фоне приема МГТ и без МГТ. Таким образом, опухолевая концентрация эстрадиола не зависит от уровня в плазме [24].
Согласно рекомендациям Всемирной ассоциации по менопаузе (International Menopause Society) от 2016 г., возможное повышение риска РМЖ, связанное с МГТ, невелико и оценивается менее чем в 0,1% в год, или менее 1,0 случая на 1000 женщин на год использования [25]. Этот уровень схож или ниже, чем повышение риска, связанное с такими частыми факторами образа жизни, как сниженная физическая активность, ожирение и употребление алкоголя. Данные, полученные в исследовании WHI (Women’s Health Initiative – «Инициатива во имя здоровья женщин»), не показали повышения риска РМЖ у женщин, впервые применяющих МГТ в течение 5–7 лет после начала терапии [20]. Исследование WHI также показало, что монотерапия конъюгированными эквин-эстрогенами в течение 7,1 года снижала риск диагностирования РМЖ и смертности у женщин с удаленной маткой [26].
Этот уровень схож или ниже, чем повышение риска, связанное с такими частыми факторами образа жизни, как сниженная физическая активность, ожирение и употребление алкоголя. Данные, полученные в исследовании WHI (Women’s Health Initiative – «Инициатива во имя здоровья женщин»), не показали повышения риска РМЖ у женщин, впервые применяющих МГТ в течение 5–7 лет после начала терапии [20]. Исследование WHI также показало, что монотерапия конъюгированными эквин-эстрогенами в течение 7,1 года снижала риск диагностирования РМЖ и смертности у женщин с удаленной маткой [26].
В 3-х исследованиях было высказано предположение, что микронизированный прогестерон или дидрогестерон могут быть связаны с более низким риском, чем синтетический прогестаген [27–29]. Доступные в настоящее время данные не позволяют предположить различия в риске между пероральным и трансдермальным путями применения эстрадиола [30]. Тем не менее в настоящее время недостаточно данных клинических исследований адекватной мощности для полной оценки возможной разницы в частоте развития РМЖ при использовании разных типов, доз и путей введения эстрогенов, типа прогестагена и применения андрогенов.
На сегодняшний день в мировую практику лечения расстройств, связанных с менопаузой, активно внедряется комбинация селективного модулятора эстрогеновых рецепторов – базедоксифена (который блокирует эстрогеновые рецепторы в МЖ и эндометрии) и конъюгированных эквин-эстрогенов [31]. Данный препарат способствует уменьшению плотности МЖ, но требуются дополнительные данные для подтверждения ее влияния на заболеваемость РМЖ [32].
Таким образом, можно сделать вывод, что с точки зрения любого увеличения риска РМЖ более значим именно прогестагенный компонент МГТ и КОК, а не эстроген. Риск может быть ниже при применении микронизированного прогестерона или дидрогестерона, чем при использовании синтетического прогестагена в составе МГТ. Риск РМЖ, связанный с применением МГТ, невелик, зависит от ее длительности и неуклонно снижается после ее прекращения. Имеющихся в настоящее время данных о безопасности недостаточно для поддержки назначения МГТ женщинам, перенесшим РМЖ. До назначения МГТ следует оценить соответствующий риск. Возможное увеличение риска РМЖ, связанное с МГТ, может быть частично снижено путем отбора женщин с исходно более низким индивидуальным риском, включая низкую плотность МЖ, а также путем образования по вопросам превентивных мер, направленных на коррекцию образа жизни (снижение массы тела, приема алкоголя и увеличение физической активности). У женщин, принимающих МГТ, следует проводить ежегодную маммографию [25]. Современные прогестагены, натуральный прогестерон и селективный модулятор эстрогеновых рецепторов оптимизируют влияние гормонотерапии на МЖ. Эти данные следует учитывать гинекологам-эндокринологам при ведении пациенток с мастопатией.
Имеющихся в настоящее время данных о безопасности недостаточно для поддержки назначения МГТ женщинам, перенесшим РМЖ. До назначения МГТ следует оценить соответствующий риск. Возможное увеличение риска РМЖ, связанное с МГТ, может быть частично снижено путем отбора женщин с исходно более низким индивидуальным риском, включая низкую плотность МЖ, а также путем образования по вопросам превентивных мер, направленных на коррекцию образа жизни (снижение массы тела, приема алкоголя и увеличение физической активности). У женщин, принимающих МГТ, следует проводить ежегодную маммографию [25]. Современные прогестагены, натуральный прогестерон и селективный модулятор эстрогеновых рецепторов оптимизируют влияние гормонотерапии на МЖ. Эти данные следует учитывать гинекологам-эндокринологам при ведении пациенток с мастопатией.
Мастопатия как фактор риска РМЖ: вопросы этиопатогенеза и лечения
Д.м.н. В.Г. Беспалов
ФГБУ «НИИ онкологии им. Н.Н. Петрова» МЗ РФ, Санкт-Петербург
Мастопатия (фиброзно-кистозная болезнь) – распространенная патология, ее частота в женской популяции составляет до 50% [33]. В целом мастопатия не является предраком или стадией онкологического процесса в МЖ. Однако нельзя недооценивать роль мастопатии в развитии РМЖ. Рост заболеваемости РМЖ в XX в. во многих странах сопровождался параллельным ростом частоты мастопатии. В 2014 г. в России зарегистрировано 65 088 новых случаев РМЖ, 21,2% (1-е место) в структуре заболеваемости женщин раком; за 10 лет стандартизованный показатель заболеваемости вырос на 19,79%, рост на 1,78% в год [34]. При этом мастопатия имеется у 50–60% российских женщин [35]. Выделяют более 50 доброкачественных заболеваний МЖ или форм мастопатии, среди которых многие существенно повышают риск РМЖ.
Взаимосвязь этиологии и патогенеза мастопатии и РМЖ
Существует 4 группы доказательств связи мастопатии с РМЖ: 1) у мастопатии и РМЖ общие факторы риска; 2) патогенез мастопатии и РМЖ имеет общие черты, ключевую роль играет относительная или абсолютная хроническая гиперэстрогения; 3) при мастэктомии в связи с РМЖ в тканях МЖ часто обнаруживают морфологические проявления мастопатии и предраковые изменения; 4) у больных РМЖ чаще была предшествующая мастопатия [36].
РМЖ – полиэтиологическое заболевание, идентифицировано более 80 факторов риска РМЖ, которые можно разделить на 5 групп: половые и возрастные, генетические, репродуктивные, гормональные и обменные, внешней среды и стиля жизни. Мастопатия – также полиэтиологическое заболевание, а основные факторы риска РМЖ и мастопатии совпадают [37]. Если РМЖ в большинстве случаев развивается в постменопаузальном возрасте, то пик заболеваемости мастопатии приходится на возраст 30–50 лет, т. е. данная патология предшествует развитию РМЖ. Кровные родственники, больные РМЖ; носительство мутантных генов, отвечающих за репарацию ДНК и биосинтез половых гормонов, являются одновременно факторами риска и РМЖ, и мастопатии. Большинство репродуктивных факторов риска одинаковы для РМЖ и мастопатии: раннее менархе, низкая частота родов, поздние первые роды, отсутствие или короткий период грудного вскармливания, искусственные аборты, высокая рентгеновская плотность маммограмм в позднем репродуктивном возрасте. Гормональные и обменные факторы риска в большинстве одинаковы для РМЖ и мастопатии: гиперэстрогения, гиперпролактинемия, гипотиреоз; гиперпластические заболевания гениталий и гинекологические заболевания, связанные с нарушениями гормонального баланса; ожирение, сахарный диабет, болезни печени. Из факторов внешней среды и стиля жизни одинаковы для РМЖ и мастопатии нарушения питания в виде избытка жиров, калорий, животных белков, алкоголя, недостатка овощей и фруктов, пищевых волокон, витаминов и минералов; депрессия, нарушения сна, работа в ночные смены; сниженная физическая активность.
Мастопатию можно считать биомаркером гормонального неблагополучия на уровне организма и локального неблагополучия в ткани МЖ. Множественные факторы риска нарушают гормональный баланс в организме женщины, вызывают гиперэстрогению и гиперпролиферацию эпителия в ткани МЖ, что приводит к развитию мастопатии, а при наличии врожденных или приобретенных повреждений генов – РМЖ.
Риск РМЖ у больных мастопатией
Мастопатия является и самостоятельным фактором риска РМЖ. В эпидемиологических когортных исследованиях при сроках наблюдения за женщинами от 6 до 20 лет установлено, что относительный риск РМЖ (в сравнении с частотой РМЖ в общей популяции, с женщинами без мастопатии, с непролиферативной мастопатией) при мастопатии без пролиферации эпителия статистически недостоверно, но в некоторых исследованиях и статистически достоверно, повышается в 1,27–2,23 раза; при мастопатии с гиперплазией без атипии достоверно повышается в 1,53–3,58 раза; при мастопатии с атипичной гиперплазией достоверно повышается в 2,03–10,35 раза [38]. Dyrstad S.W. et al. провели метаанализ 32 эпидемиологических ретроспективных и проспективных исследований о связи мастопатии с риском РМЖ; относительный риск РМЖ при непролиферативных формах мастопатии статистически недостоверно повышался до 1,17, при пролиферативных формах без атипии – достоверно повышался до 1,76, при пролиферативных формах с атипией – до 3,93 [39].
В эпидемиологических когортных исследованиях при сроках наблюдения за женщинами от 6 до 20 лет установлено, что относительный риск РМЖ (в сравнении с частотой РМЖ в общей популяции, с женщинами без мастопатии, с непролиферативной мастопатией) при мастопатии без пролиферации эпителия статистически недостоверно, но в некоторых исследованиях и статистически достоверно, повышается в 1,27–2,23 раза; при мастопатии с гиперплазией без атипии достоверно повышается в 1,53–3,58 раза; при мастопатии с атипичной гиперплазией достоверно повышается в 2,03–10,35 раза [38]. Dyrstad S.W. et al. провели метаанализ 32 эпидемиологических ретроспективных и проспективных исследований о связи мастопатии с риском РМЖ; относительный риск РМЖ при непролиферативных формах мастопатии статистически недостоверно повышался до 1,17, при пролиферативных формах без атипии – достоверно повышался до 1,76, при пролиферативных формах с атипией – до 3,93 [39].
К предраковым изменениям МЖ относят протоковую атипичную гиперплазию и карциному in situ, дольковую атипичную гиперплазию и карциному in situ, склерозирующий аденоз, радиальный рубец [40]. Основные формы предрака МЖ приведены на рисунке 1.
В таблице 2 указывается степень риска РМЖ при мастопатии по данным R.J. Santen и R. Mansel [40].
Коллегия американских патологов рекомендовала подразделять женщин с мастопатией на 3 категории в зависимости от выявленных при биопсии МЖ морфологических изменений: 1) непролиферативная – риск РМЖ не повышен и равен популяционному; 2) пролиферативная без атипии – риск РМЖ повышен в 1,5–2 раза по сравнению с популяцией; 3) пролиферативная с атипией – риск РМЖ повышен в 4–5 раз по сравнению с популяцией [41]. При биопсии МЖ и морфологическом обследовании примерно у 5% женщин с мастопатией выявляется атипическая гиперплазия [42].
Лечение мастопатии и профилактика РМЖ
Стандартов лечения мастопатии на сегодняшний день нет. К общим недостаткам большинства применяемых сегодня средств можно отнести невысокую эффективность, побочное и токсическое действие, необходимость применения в виде комплекса с другими средствами, нацеленность только на облегчение патологической симптоматики, а не на более серьезную задачу – профилактику РМЖ. Поэтому актуальной является проблема создания специальных лекарственных средств для лечения мастопатии. С учетом характера данной патологии такие средства должны быть эффективными, безопасными, пригодными для длительного применения, направленными на профилактику РМЖ. Патогенетическое лечение мастопатии относят к первичной и вторичной профилактике РМЖ [43, 44].
Поэтому актуальной является проблема создания специальных лекарственных средств для лечения мастопатии. С учетом характера данной патологии такие средства должны быть эффективными, безопасными, пригодными для длительного применения, направленными на профилактику РМЖ. Патогенетическое лечение мастопатии относят к первичной и вторичной профилактике РМЖ [43, 44].
В настоящее время для патогенетического лечения мастопатии существуют лишь единичные препараты. Например, лекарственный препарат Мамоклам, который производят из липидной фракции бурой морской водоросли Laminaria; действующими веществами Мамоклама являются органический йод, полиненасыщенные жирные кислоты омега-3 типа, хлорофилл. Мамоклам разрешен для медицинского применения в качестве лекарственного средства для лечения мастопатии. В эпидемиологических исследованиях показано, что все 3 действующих вещества Мамоклама снижают риск развития РМЖ. В клинических исследованиях доказано, что Мамоклам вызывает регрессию масталгии, ослабляет предменструальное нагрубание МЖ, вызывает регрессию уплотнений и кист в МЖ, снижает маммографическую плотность, нормализует процессы пролиферации эпителия МЖ, нормализует менструальный цикл и баланс тиреоидных и половых гормонов [45–47].
Патогенетическое лечение мастопатии должно быть направлено на нормализацию гормонального баланса в организме женщины, прежде всего баланса половых гормонов; на уменьшение гиперэстрогении как на системном уровне, так и на уровне рецепторного аппарата клеток в ткани МЖ; на подавление процессов гиперпролиферации железистого эпителия МЖ. Основным действующим веществом Мамоклама является йод в органически связанной форме (в составе аминокислот). При поступлении в организм в дозах, превышающих суточную потребность, йод накапливается в тканях МЖ и оказывает прямое действие на патогенетические пути развития мастопатии: подавляет пролиферацию эпителия, индуцирует апоптоз и дифференцировку клеток, снижает чувствительность ткани МЖ к эстрогенам; в щитовидной железе формируются йодолипиды, которые оказывают антиоксидантное действие и контролируют клеточную пролиферацию в МЖ; йод также опосредованно влияет на состояние МЖ, нормализуя баланс тиреоидных и половых гормонов, уменьшая местную гиперэстрогению в тканях МЖ [48–50]. Показано, что при лечении мастопатии йодом в дозах, превышающих суточную потребность, нормализуется архитектоника тканей МЖ [51]. Длительный прием йода в дозах, превышающих суточную потребность, возможен только для органического йода, который содержится в Мамокламе. Другой компонент Мамоклама – полиненасыщенные жирные кислоты омега-3 типа также влияют на патогенетические пути развития мастопатии: формируют структуру и определяют вязкость клеточных мембран, регулируют клеточные сигналы, нормализуют баланс эстрогенов, в результате чего уменьшают гиперэстрогению и ослабляют пролиферацию клеток в ткани МЖ [52].
Показано, что при лечении мастопатии йодом в дозах, превышающих суточную потребность, нормализуется архитектоника тканей МЖ [51]. Длительный прием йода в дозах, превышающих суточную потребность, возможен только для органического йода, который содержится в Мамокламе. Другой компонент Мамоклама – полиненасыщенные жирные кислоты омега-3 типа также влияют на патогенетические пути развития мастопатии: формируют структуру и определяют вязкость клеточных мембран, регулируют клеточные сигналы, нормализуют баланс эстрогенов, в результате чего уменьшают гиперэстрогению и ослабляют пролиферацию клеток в ткани МЖ [52].
Выводы
1. К группе повышенного онкологического риска женщины, страдающие мастопатией, могут быть отнесены после оценки всех индивидуальных факторов риска и морфологического анализа тканей МЖ.
2. Решающим в оценке степени риска развития РМЖ у больных мастопатией является морфологическое исследование ткани МЖ, полученной при биопсии. Риск РМЖ не повышается или является минимальным при непролиферативных формах мастопатии, при пролиферативной форме без атипии риск возрастает в 2 раза, при пролиферативной с атипией – в 4 раза и достигает наиболее высоких цифр (до 12 раз) при протоковой или дольковой карциноме in situ.
3. Своевременная диагностика и патогенетическое лечение мастопатии не только улучшают качество жизни, но и должны быть направлены на профилактику РМЖ. Мамоклам – эффективный и безопасный лекарственный препарат для патогенетического лечения мастопатии, при длительном применении Мамоклам снижает риск РМЖ.
.
ЛЕЧЕНИЕ МАСТОПАТИИ МОЛОЧНОЙ ЖЕЛЕЗЫ МЕТОДОМ ПРОФЕССОРА С.Н.ПАЩЕНКО
Мастопатия молочной железы – это доброкачественное заболевание, которое проявляется разрастаниями тканей молочной железы и появлением одиночных или множественных уплотнений (узлов). Мастопатии подвержены в основном женщины, однако редко заболевание встречается и у мужчин.В клинике «Лекарь» уже много лет успешно проводят диагностику и лечение мастопатий.
 Прием ведет доктор медицинских наук, онколог-маммолог, профессор Пащенко Сергей Николаевич.
Прием ведет доктор медицинских наук, онколог-маммолог, профессор Пащенко Сергей Николаевич.
Мастопатия довольно распространенное заболевание: у молодых женщин встречаемость патологии достигает 30% и существенно повышается после 40 лет.
Различают следующие виды мастопатий:
- Очаговая мастопатия (присутствуют только единичные узлы)
- Диффузная мастопатия (множественные уплотнения в молочной железе)
- Фиброзно-кистозная мастопатия (формируются кисты, внутрипротоковые папилломы и фиброаденомы)
При мастопатии, вне зависимости от формы, женщин часто беспокоят боли, что является показанием к назначению анальгетиков.
Почему возникает мастопатия?В женском организме есть так называемые органы-мишени, которые зависят от обмена половых гормонов: матка, яичники и молочные железы. Из-за нарушения обмена половых гормонов и повышенной продукции эстрогенов в этих органах происходит патологическое разрастание слизистой. В молочной железе разрастается не только слизистая, но и протоки, соединительная, а также железистая ткани.
Эстрогены выделяются в первой половине менструального цикла, прогестероны — во второй. Нарушение эстрогено-прогестеронового баланса — это основное условие для развития мастопатии, фиброаденомы матки и эндометриоза.
Важно! Применение только лекарственных средств неспособно полностью нормализовать нарушения гормонального обмена. Однако правильное использование естественных методов оздоровления позволяют нормализовать работу эндокринной системы. Особенностью лечения больных по методу профессора С.Н.Пащенко является использование в комплексе традиционных лечебных средств и методов нормализации обмена веществ с помощью природного регулятора – двуокиси углерода.
ДиагностикаВ выявлении мастопатии очень важную роль играет самодиагностика. Именно самостоятельное обследование позволяет выявить патологические изменения уже на ранних стадиях.![]() Проводится обследование в спокойной обстановке в первой половине менструального цикла.
Проводится обследование в спокойной обстановке в первой половине менструального цикла.
Следует обратить внимание на следующие моменты: кожу железы, наличие выпуклых и втянутых мест, форму и ореол соска.
Признаками заболевания могут служить следующие симптомы:
- выделения из сосков,
- изменение цвета кожи,
- наличие уплотнений,
- боли различного характера и продолжительности
При появлении одного или нескольких симптомов необходимо незамедлительно обратиться к врачу.
Узловая мастопатия
Заболевание проявляется в виде фиброаденом, липом, внутрипротоковых папиллом и кист. Различают фиброзную, железистую и фиброзно-кистозную мастопатии, в зависимости от изменений в железе. Главный признак мастопатии — уплотнения в груди с четкими границами в одной или обеих железах.
Очаговая мастопатия требует дополнительной диагностики, так как её симптоматика очень схожа со злокачественными новообразованиями. В клинике «Лекарь» разработана и внедрена оригинальная методика оценки озлокачествления образований молочной железы .Эта методика не требует затрат и обеспечивает высокую точность прогнозирования риска развития рака молочной железы. Это позволяет уменьшить количество неоправданных операций в онкологических и хирургических стационарах с одной стороны, а также индивидуализировать профилактические операции в зависимости от характера перестройки железы.
Диффузная мастопатия молочных желез
При диффузной мастопатии границы патологических изменений не выражены (в отличие от узловой формы). А проявление клинических признаков связанно с изменением менструального цикла.
Лечение диффузной мастопатии молочной железы требует сочетания медикаментозного лечения и метода ликвидации дефицита кислорода в тканях, предложенного профессором Пащенко для профилактики рака.
У больных с высоким риском развития рака молочной железы в клинике «Лекарь» осуществляется персонификация хирургических методов профилактики: удаления фиброаденом молочной железы, профилактические секторальные резекции, квандранэктомии. У больных с крайне высоким риском развития рака молочной железы проводится профилактическая мастэктомия.
У больных с крайне высоким риском развития рака молочной железы проводится профилактическая мастэктомия.
Риски развития рака молочной железы в клинике «Лекарь» рассчитываются на основании инструментальных, морфологических и молекулярно-биологических методов исследования с учетом состояния противоопухолевой защиты организма.
Для записи на консультацию звоните по телефону: +380664301009.
ЛЕЧЕНИЕ МАСТОПАТИИ МОЛОЧНОЙ ЖЕЛЕЗЫ МЕТОДОМ ПРОФЕССОРА С.Н.ПАЩЕНКО обновлено: Октябрь 25, 2019 автором: CL Administrator
Фиброаденоматоз – Клиника СМТ
Фиброаденоматоз молочных желез или мастопатия – это группа доброкачественных заболеваний, которые характеризуются избыточным разрастанием железистой или опорной соединительной ткани.
Различают диффузные, узловые и смешанные формы мастопатии:
- При диффузных формах изменения затрагивают всю молочную железу. Это наиболее благоприятное течение заболевания.
- При узловой мастопатии в молочной железе появляются доброкачественные опухоли – фиброаденомы, крупные жидкостные образования – солитарные кисты или папилломатозные разрастания внутри протоков.
Мастопатией страдают около 80% женщин репродуктивного периода и 60% женщин менопаузального возраста.
Мастопатия стремительно «молодеет». Еще 10 лет назад дебют фиброаденоматоза приходился, в основном, на возраст 35-37 лет. В настоящее время подавляющее большинство 25-летних женщин имеют признаки мастопатии.
Симптомы заболевания
Диффузный фиброаденоматоз – заболевание, протекающее стадийно. И в разные возрастные периоды проявляется по-разному.
Первоначальная жалоба – это незначительные боли в молочных железах перед менструацией. Большая часть женщин считают этот симптом совершенно безобидным.
Большая часть женщин считают этот симптом совершенно безобидным.
В дальнейшем боли в молочных железах приобретают более выраженный характер и начитаются после овуляции, а в ряде случаев не проходят и после наступления менструации.
Молочная железа в этот период может значительно увеличиваться в размерах, при пальпации прощупываются крупные болезненные уплотненные участки, а из сосков появляются светлые или зеленоватые выделения. Значительно ухудшается качество жизни. Женщины ограничивают физическую нагрузку, дабы не сотрясать молочную железу, отказываются от привычных бюстгальтеров, не могут спать на животе. В дальнейшем появляется тревожность за свое здоровье, что еще больше усугубляет ситуацию.
Максимальная выраженность болевого синдрома приходится на возраст 37-45лет. В дальнейшем боли стихают и носят нерегулярный характер.
В периоде менопаузы в большинстве случаев жалобы отсутствуют или встречаются эпизодически. Но это вовсе не значит, что болезнь прошла. Длительное увеличение железистого слоя молочной железы приводит к разрастанию соединительной ткани, а в ряде случаев, к ее склерозированию. Такая молочная железа наощупь плотная с множеством мелких болезненных уплотненных участков.
Женщины старшего возраста, в связи с отсутствием жалоб, редко посещают врача маммолога. А ведь максимальные риски заболеть раком молочной железы приходятся на возраст 60-64 года и остаются стабильно высокими до 70-75 лет. Немногие знают, что скрытый период рака молочной железы от 1 опухолевой клетки до 1см составляет 5-10 лет.
Все женщины, начиная с 18 лет, должны ежегодно проходить осмотр у врача маммолога. А при появлении боли или дискомфорта в молочной железе, выделений из сосков, шелушения или трещин сосков и ареол, уплотнений или образований молочных желез, асимметрии или деформаций молочных желез, покраснения или отека молочных желез визит к врачу откладывать недопустимо!
Причины заболевания
Здоровье женской груди в руках мужчины
Главный маммолог Беларуси, доктор медицинских наук, профессор Леонид ПУТЫРСКИЙ.
Мастопатия жизни не угрожает
– Леонид Алексеевич. Звоню из Копыля. Моей дочке 19 лет, ей поставили диагноз «мастопатия». И грудь у нее очень болит. Как ей можно помочь?
– Не волнуйтесь, мастопатия не опасна для жизни.
– Нам очень страшно.
– Мастопатия чаще всего жизнь не укорачивает. Это обменные нарушения в молочной железе в результате разных причин. Среди них, во-первых, – стресс, нервные нагрузки, напряженный умственный труд. Во-вторых, гормональные нарушения могут вызвать мастопатию. Влияет все – сколько женщина рожала, сколько кормила ребенка грудью, были ли аборты, воспалительные заболевания, отношения с мужем… Третья группа причин возникновения мастопатии – экология. Все это сказывается на женском организме. Мастопатия – это когда ткань железы замещается грубой фиброзной тканью, в ней могут разрастаться фиброзные тяжи и появляться кисты, наполненные жидкостью. Две третьи всех мастопатий относятся к подобной фибрознокистозной форме.
– Но она лечится?
– Конечно. Но назначить лечение должен врач после осмотра.
– Мне лечение назначили. Но УЗИ сказали можно делать только после менструации.
– Грудь лучше всего смотреть первые 10 дней после месячных.
– Татьяна беспокоит. Мне 34 года. Грудь всегда болела перед месячными, обратилась к гинекологу, она выписала гомеопатические капли и дала направление на маммографию.
– Сразу вам скажу, что в вашем возрасте маммографию делать рано, она будет мало информативна. Вам нужно сделать УЗИ молочных желез. А маммограмму делают ближе к 45 годам.
– А я уже сделала.
– Ну, учтите мои слова на будущее.
– Написали диффузная фиброзно-кистозная мастопатия.
– Живите с ней совершенно спокойно.
– Леонид Алексеевич, врач сказал, что у моей дочери узловая мастопатия. Что это такое?
– Мастопатия бывает диффузная, бывает узловая, или очаговая. При диффузной мелкая зернистость по всей молочной железе, она иногда покалывает, побаливает, отдает в подмышку, в сосок. Могут быть выделения из соска, но не кровянистые. А при очаговой мастопатии есть более-менее четкое образование, которое можно прощупать руками, увидеть на УЗИ. Очаговую мастопатию чаще всего удаляют хирургически, чтобы убедиться в том, что в ней нет ничего плохого. Ведь в 6% всех внешне доброкачественных опухолей после удаления находят злокачественные клетки.
УЗИ молочных желез – раз в год
– Беспокоит Эдуард Константинович. У супруги были две операции по поводу фиброаденомы. Как сейчас ей себя вести, как питаться? Ей 36 лет.
– В таком возрасте редко бывают повторные фиброаденомы. Как любой здоровой женщине ей нужно побольше овощей, фруктов, держать постоянный вес, ежемесячно осматривать свои молочные железы. Чтобы не было воспалительных гинекологических заболеваний, абортов…
В мире нет препарата, который можно было бы назначить и знать, что он убережет от всех проблем. Поэтому не надо ничего ждать, не надо думать, что может что-нибудь появиться. Но УЗИ раз в год делать необходимо. А вам стоит побольше ласковых слов говорить супруге, здоровье груди женщины во многом зависит от отношений с мужем. Она должна быть уверенной, спокойной, что ее любят. Счастливые женщины меньше болеют раком молочной железы и мастопатией. Важно, чтобы муж тоже следил за молочными железами своей жены, потому что, к примеру, в Италии до 80% опухоль первой стадии (до двух сантиметров) находили именно мужчины. А у нас это бывает очень редко.
– Недавно прочел о том, что в грейпфруте обнаружили компонент, который позволяет избежать рака молочной железы.
– Все фрукты содержат витамины, поэтому они полезны и для молочной железы. Но вы должны понимать, что тем мизерным количеством полезных веществ, которые есть в том же грейпфруте, нельзя вылечить мастопатию или рак. Не будете же вы их есть тоннами. Но здоровье груди зависит от множества факторов, в том числе и от питания.
Фиброаденому нужно удалять
– Леонид Алексеевич, хочу проконсультироваться по поводу своей жены. У нее в одной груди нашли кисту, а в другой – фиброаденому. Врач говорит, что нужно делать операцию. А можно обойтись без нее? Или обязательно удалять фиброаденому?
– До 20 лет можно назначить лечение фиброаденомы. А вашей супруге сколько лет?
– 48.
– В 48 лет уплотнение оставлять в груди нельзя. Потому что фиброаденома может перерождаться в злокачественную опухоль. Не стоит вам этого ждать. Удалять однозначно.
– Но этот диагноз у нее стоит под вопросом.
– Я еще раз вам повторю, что в 48 лет оставлять любое уплотнение в груди нельзя. Кисту можно шприцем отпунктировать – и все лечение. А фиброаденому обязательно удаляют и отправляют на исследование. После того как ее посмотрят под микроскопом, вам окончательно скажут результат. Но хирург даже во время операции увидит, какая это опухоль. Поэтому не занимайтесь самолечением, не рискуйте. Кстати, сама операция длится не больше 30 минут.
– У меня в груди было сначала покалывание, потом появились светлые выделения, а теперь красноватые. Куда мне можно обратиться?
– У здоровой женщины выделений из груди, как правило, не бывает. Иногда даже в норме может выделяться капелька в сутки. Но если выделения появились впервые или стали кровянистыми, необходимо обратиться или к гинекологу, или онкологу-маммологу.
– Я обращалась к маммологу, у меня брали мазок этих выделений.
– И убедились, что опухолевых клеток нет? Прекрасно. Но если выделения сейчас стали кровянистыми, вам нужно еще раз сдать мазок. Если в нем много крови, вам можно назначить лечение на несколько недель. Если в течение двух-трех недель все пройдет, на УЗИ тоже все будет в порядке, можно просто наблюдаться. Если кровянистые выделения будут продолжаться, скорее всего ту область возле соска, при надавливании на которую появляются выделения, придется удалить. Не пугайтесь, такое может быть и при доброкачественных процессах, а если это опухоль, то она микроскопических размеров, и после удаления жизни ничто не угрожает. Но решать это должен онколог.
– Но я никаких уплотнений не нащупываю.
– Эта опухоль может быть такой мизерной, что ее можно рассмотреть только под микроскопом.
– Мне 39 лет, в 35 поставили диагноз «ранний климакс». Назначили лечение. Но у моей мамы был рак молочной железы. Сейчас, слава Богу, все в порядке. А у меня мастопатия. Скажите, велик риск того, что я тоже не избегу рака?
– Наследственный рак существует. Но для того, чтобы это узнать, нужно делать генетический анализ. Если рак не наследственный, то ваш риск такой же, как у любой женщины. Если наследственность есть, женщины заболевают в более молодом возрасте – до 40 лет. Если мама болела, риск у дочери в 3 – 5 раз повышается. Только не нужно этого ждать. А стоит принять меры, чтобы было меньше рисковых факторов. И, кстати, риск рака молочной железы снижается при раннем климаксе. Отчасти природа вас спасает.
НЕ ЗАГОРАЙТЕ ТОПЛЕС
– У меня на УЗИ обнаружили мастопатию, но в нашей поликлинике нет маммолога. К какому специалисту я могу обратиться?
– К онкологу, гинекологу. Любая женщина имеет право на направление в онкологический диспансер, если в ее поликлинике нет онколога, а в груди нашли уплотнение.
– Леонид Алексеевич, у меня мастопатия уже 18 лет, сначала не принимала никаких лекарств, а последние три года чувствую себя не очень хорошо. Что вы можете посоветовать?
Без осмотра никакое лечение назначать нельзя. Идите к доктору.
– Леонид Алексеевич! Мне уже 40 лет. Хотела бы узнать, какие витамины полезны для молочной железы?
– Все витамины необходимы и полезны. Ведь мы с пищей недополучаем витаминов, а для нормальной жизнедеятельности мы должны их восполнять. Существует всего 13 витаминов, поэтому лучше принимать поливитамины. Можно чередовать антиоксидантные комплексы с другими поливитаминами, где их количество больше. Витамины нужно пить не натощак, а после или во время еды, не сезонно, а регулярно в течение всего года.
Если побаливает грудь надо принимать успокаивающие средства: валериану, пустырник дней десять перед месячными.
Очень важны для женщины роды. Двое, трое родов снижают риск опухоли молочной железы. Важно первого ребенка родить около 20 лет. В Скандинавских странах, Америке, где женщины рожают первого ребенка после 35 лет, случаев рака молочной железы в два раза больше, чем в Беларуси. Важно также кормить грудью ребенка не меньше полугода. Это не только для ребеночка важно – убережет его от аллергий и других проблем, но и мамино здоровье сбережет. У тех, кто кормит не меньше полугода, риск рака молочной железы снижается в полтора-два раза.
– А загорать можно?
– Можно, но в разумных пределах, не до черноты. Не советую загорать топлес, для груди это не очень хорошо.
ГРУДЬ МОЖЕТ БОЛЕТЬ ОТ ЗИМНЕЙ ТОСКИ
– Мне 35 лет, в осенне-зимний период перед месячными очень болит под правой рукой. Что это может быть?
– Во-первых, это может быть так называемый синдром предменструального нагрубания. В осенне-зимний период организм больше страдает от нехватки витаминов, солнечной энергии, от зимней тоски. Это нормально, потому что перед месячными у женщины изменяется гормональный фон, грудь отекает и побаливает. Принимайте успокаивающие средства, может быть, даже мочегонное.
Во-вторых, такое может быть при диффузной фиброзно-кистозной мастопатии. Ничего страшного нет. Но если беспокоит, покажитесь врачу.
– А почему боль бывает только с одной стороны?
– Возможно, с правой стороны у вас больше гормональных рецепторов. Может быть больше болевых рецепторов, или долек больше, и они отекают сильнее. Такое бывает и не говорит о том, что это плохо.
– Леонид Алексеевич, несколько дней назад на меня упала коробка тяжелая. Она грудь очень сильно ударила, сейчас пятно темное и припухлость остается.
– Молочная железа не любит, когда ее ударяют. По разным данным, от 5 до 40% опухолей оказываются результатом травм. Но не пугайтесь, не обязательно каждая травма заканчивается опухолью. Сразу после удара нужно было приложить лед. А сейчас вам нужны рассасывающие средства. Главное, чтобы не образовалось никаких уплотнений. И осматривайте себя регулярно.
– А как это правильно делать?
– Каждый месяц в первые 10 дней после менструаций. Убедитесь, что на коже нет никаких выпячиваний, втяжений, покраснений, отека в виде лимонной корочки. Посмотрите, чтобы из соска не было никаких выделений, чтобы он не был отклонен в какую-нибудь сторону. После этого нужно осмотреть подмышечную область – правой рукой левую, левой правую. Потом осматриваете молочную железу, сначала в вертикальном положении, пальцы прижать плотно к молочной железе и убедиться, что между ними и грудной клеткой нет никаких уплотнений. А потом лежа правую руку под голову, а левой рукой от периферии к центру по кругу всю грудь осмотреть. И снова ничего новенького не найти. До сорока лет я рекомендую раз в год показываться гинекологу, маммологу или онкологу. Иногда раз в год можно делать УЗИ. Если через месяц после вашей травмы останется уплотнение, обязательно покажитесь врачу.
— Здравствуйте, Леонид Алексеевич. Меня оперировали в вашем институте в 1988 году, будет уже двадцать лет.
— Это очень здорово, что вы позвонили. Это важно для тех женщин, которые сегодня только начинают лечение. Им важно видеть на вашем примере, что можно жить и двадцать лет, и больше.
— Десять месяцев назад я обнаружила в груди уплотнение, как палочки сантиметра 4-5. Обратилась к маммологу, он сказал, что это жировые дольки. У меня в семье была онкология, поэтому я обратилась к онкологам. Они тоже сказали, чтобы я не волновалась. Что для моего возраста, мне 69 лет, это нормально. Вчера я сходила на УЗИ, там тоже сказали, что можно не беспокоиться. Но меня все-таки волнует, насколько опасно наличие этих жировых долек?
— Не опасно. Молочная железа имеет свойство с возрастом замещаться жировой тканью. И это позволяет стать ей мягче, в некоторых местах образуются более заметные жировые дольки. Это совершенно нормальные собственные ткани и естественное состояние для женщины в менопаузе. Жизни это не угрожает. Но смотреть за собой, конечно, нужно.
— А как же! Спасибо!
— У моей мамы втянут сосок и сейчас начались какие-то выделения. Надо срочно проверяться?
— Сколько маме лет.
— Уже 82.
— Ей бы сделать маммограмму. У нее может быть внутрипротоковая папиллома, воспаление, но может быть и опухоль.
— Здравствуйте, Леонид Алексеевич. У меня удалены яичники. После операции стала очень болеть грудь, раз в месяц точно. Никакое лечение не помогает, хотя толком ничего не находят.
— У вас наступила искусственная менопауза, в организме идет гормональная перестройка, и молочные железы на это реагируют.
— Леонид Алексеевич, я много лет наблюдалась онкодиспансере с мастопатией. А теперь меня, как и многих других женщин, сняли с учета в диспансере. Что теперь делать?
— Это очень неприятная ситуация. Для меня, как для маммолога, такое решение было неожиданностью. Онкологи оказались очень перегружены. И эту нагрузку переложили на обычных гинекологов, которые не обучены лечению мастопатий. Теперь страдают женщины, страдают гинекологи… Их сначала надо было обучить, подготовить. Я и мои коллеги теперь проводим в поликлиниках Минска и других городов семинары для врачей-гинекологов.
СПАСИБО, ДОКТОР!
– Леонид Алексеевич, хочу поблагодарить вас за все, что вы сделали для моей дочери. Сегодня ровно месяц, как вы прооперировали мою Наташу. Вы согрели нас своим безграничным вниманием и теплом, подарили надежду на выздоровление. Мы во всем следуем вашим советам, живем и дышим вами и вашими стихами. У вас огромная душа. Спасибо вам огромное. Победа над этой болезнью будет за нами!
Мастопатия – Лечение в Киеве
Мастопатия — одно из самых распространенных заболеваний молочных желез. Мастопатия объединяет группу заболеваний, к которым относится фиброз, кисты, смешанные фиброзно-кистозные изменения как диффузного, так и очагового характера.
Причины возникновения
Мастопатия возникает как следствие нарушения гормонального баланса. Причин нарушения много:
- прерывание беременности,
- нарушение /отсутствия половой жизни,
- нарушение режима грудного вскармливания,
- травмы молочных желез,
- психических расстройств и т.д.
- следствие заболеваний либо нарушений функции яичников, печени или щитовидной железы.
Проявления
Проявления мастопатии могут быть различными:
- появление в молочных железах болезненных образований различной величины
- болевые ощущения в молочных железах за несколько дней перед менструацией
По характеру поражения тканей молочной железы различают диффузную и узловую формы мастопатии. При очаговой мастопатии в молочной железе появляются подвижные, единичные уплотнения круглой или бляшковидной формы, крупных размеров, при этом ткань молочной железы остается не измененной.
Симптомы
В начальной стадии заболевание дает о себе знать болями в груди, которые появляются перед началом менструации.
При развитии заболевания появляются следующие симптомы:
- увеличиваются грудные железы
- появляется ощущение дискомфорта
- появляется тяжесть
- сильные боли в груди
- боли при пальпации
- выделения из сосков, напоминающие по консистенции молозиво.
Диагностика
Для диагностирования мастопатии проводится ряд исследований.
Основным способом диагностировать мастопатию является маммография. Выполняется маммография в первой фазе менструального цикла. Если возникает подозрение, что появилось злокачественное новообразование – день цикла не имеет значения.
Также применяется дуктография – рентгенологическое исследование с введение контраста в млечные протоки.
УЗИ, как и маммография, проводится в первой фазе менструального цикла. Также проводится цитологическое исследование молочной железы. Дополнительно проводят КТ и МРТ.
Лечение
Если мастопатия была обнаружена случайно, а пациентка не имеет жалоб на физическое состояние, то лечения может не требоваться. В таком случае проводят комплексное обследование. Также требуется ежегодное обследование у мамолога и гинеколога.
В случае, когда болезненность молочной железы сопровождается наличием диффузных кистозно-фиброзных изменений в тканях то назначается диета и медикаментозная коррекция гормонального состояния пациентки.
MEDISON.RU – Ультразвуковая диагностика узловой мастопатии
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
Одним из наиболее распространённых проявлений дисгормональных расстройств у женщин является развитие фиброзно-кистозной мастопатии [10]. Как известно, фиброзно-кистозной мастопатия может выражаться в виде диффузной, диффузно-узловой и узловой (локализованной) форм. Узловая мастопатия – сложное и малоизученное заболевание молочной железы [11]. Следует разделить диагностику этой формы мастопатии на клиническую и инструментальную части. Выявленная клинически узловая мастопатия при проведении инструментальных исследований может оказаться локальным фиброзом, кистой, фиброаденомой, интрамаммарным лимфоузлом, липомой [14]. В то же время описаны признаки локализованной формы фиброзно-кистозной мастопатии в рентгенологическом и ультразвуковом изображении [2, 6].
Имеющиеся в литературе данные о малигнизации локализованной мастопатии и тактике её лечения противоречивы. Так, В. П. Харченко и соавт. [13] указывают на ошибочность трактовки узловой мастопатии как предракового состояния с обязательным хирургическим лечением. Однако ряд авторов придерживаются противоположного мнения [4, 5, 18]. Все авторы, между тем, сходятся во мнении о необходимости комплексного обследования пациенток с целью установления наличия истинной локализованной фиброзно-кистозной мастопатии.
В настоящее время для инструментального исследования молочных желёз чаще применяют следующие методы диагностики: рентгеновскую маммографию и ультразвуковое исследование.
Рентгеновская маммография длительное время считалась “золотым стандартом” в диагностике различных заболеваний молочных желёз [8]. Большинство маммологов используют метод на первом этапе диагностики [1]. Истинную природу образования рентгеновская маммография выявляет в 75-91 % случаев [11]. Следует отметить, что некоторые авторы отмечают невысокую специфичность и точность этого метода (46-56 %) при проведении дифференциального диагноза между доброкачественным и злокачественным процессом [12].
Роль и место ультразвукового исследования в маммологии на протяжении последних лет является предметом дискуссий. Отношение к методу меняется соответственно уровню используемой техники. В 80-е гг. ультрасонография рассматривалась лишь как дополнение к клиническому осмотру и рентгеновской маммографии [17,19]. Однако совершенствование диагностических аппаратов с применением сложных ультразвуковых датчиков и сосудистой эхографии позволили повысить информативность УЗИ молочных желёз [2, 16]. С.А. Берзин и С.Д. Лисьева (1997) полагают, что этот факт в сочетании с приемлемой стоимостью ультрасонографии позволяют рекомендовать метод на первом этапе инструментального исследования молочной железы, а во многих случаях – и вместо маммографии [1]. Эхография предшествует другим инструментальным диагностическим процедурам у молодых, при отчётливо пальпируемом образовании и при расположении опухоли в недоступных для рентгеновской маммографии участках молочной железы [3].
Мнения о возможностях УЗИ в диагностике очаговой формы мастопатии различны [2, 7, 11]. Чувствительность эхографии при узловых формах мастопатии равна, по данным различных авторов, 74-89 % [9, 15].
Приводим описание интересного случая узловой мастопатии, расцененной рентгенологически как злокачественное новообразование молочной железы.
Описание случая
Пациентка, 42 г., обратилась к маммологу по направлению гинеколога, обнаружившего уплотнение в левой молочной железе. Состоит на учёте по поводу аденомиоза. В семье имеется онконастороженность по раку молочной железы.
Женщине были проведены: осмотр маммолога, рентгеновская маммография, ультрасонография мультичастотным линейным датчиком с частотой сканирования от 6 до 12 МГц.
При осмотре изменений молочных желез не выявлено. При пальпации в верхненаружном квадранте левой молочной железы обнаружено уплотнение без чётких границ, не спаянное с кожей и с подлежащими тканями. Регионарные лимфатические узлы не изменены. Высказано предположение о наличии узловой формы мастопатии.
На рентгеновской маммограмме в верхненаружном квадранте левой железы на фоне инволютивных изменений выявлена тень узла с нечёткими бугристыми контурами размером ~ 3,0 + 2,5 см (рис. 1). Структурный рисунок железы изменен. Рентгенологическое заключение: подозрение на злокачественное поражение левой молочной железы.
Рис. 1. Маммограмма левой молочной железы.
При проведении ультразвукового исследования получены следующие данные: в обеих железах выражена преимущественно жировая ткань. Млечные протоки не расширены. В верхненаружном квадранте левой молочной железы визуализируется участок сниженной эхогенности, причудливой формы, напоминающий соты, с достаточно чёткими контурами, без дистальных акустических эффектов. Размеры образования: 1,1 х 3,0 см (рис. 2). При исследовании в режиме цветного допплеровского картирования образование аваскулярно. При применении энергетического допплера выявлен единичный интранодулярный сосуд. Использование импульсноволнового допплеровского режима позволило произвести количественную оценку показателей кровотока: максимальная систолическая скорость (PSV) = 0,08 м/с, конечная диастолическая скорость (EDV) = 0,02 м/с, индекс резистентности (RI) = 0,74. При исследовании регионарных зон лимфооттока патологии не выявлено. Ультразвуковое заключение: узловая мастопатия левой молочной железы.
Рис. 2. Эхограмма очагового образования левой молочной железы.
Пункционная аспирационная биопсия под ультразвуковым контролем осуществлена по стандартной методике с использованием иглы 0,8 х 40 мм без мандрена. При цитологическом исследовании обнаружилось малое количество клеточного субстрата во взятом материале.
Пациентка госпитализирована. Произведена секторальная резекция левой молочной железы. Гистологическое заключение: непролиферативная мастопатия.
Обсуждение
Узловая мастопатия нередко в клиническом, рентгенологическом и ультрасонографическом отношении имеет сходное проявление с опухолевыми узлами злокачественной природы [2,11]. Поэтому в приведённом наблюдении ультразвуковое заключение не повлияло на тактику ведения пациентки – образование обязательно должно иметь морфологическую верификацию. Однако случай демонстрирует широкие возможности ультрасонографии при использовании аппаратуры высокого класса. Ультразвуковая картина выявленного образования молочной железы не была типичной ни для одного варианта эхографического изображения злокачественной опухоли. Исследуемый участок был расценён как комплекс расположенных рядом и расширенных млечных протоков. Ультрасонографическое заключение базировалось в основном на данных В-режима. И хотя показатели васкуляризации указывали скорее на доброкачественный процесс, литературные данные о значимости отдельных исследуемых параметров кровотока при патологии молочных желез крайне разноречивы [12].
Постоянное совершенствование ультразвуковой диагностической техники позволит максимально приблизить эхографию к “золотому стандарту” в маммологии.
Литература
- Берзин С.А., Аисъеба С.Д. Место ультразвукового исследования в комплексном инструментальном обследовании молочных желёз // Современная лучевая диагностика и лучевая терапия.Материалы научно-практической конференции, посвящённой памяти проф. Б.К. Шарова, 31 октября 1997 г. Челябинск, 1997. С. 13-15.
- Заболотская Н.В., Заболотский B.C. Ультразвуковая маммография. М., 1997.104 с.
- Зайцев А.Н. Эхография и маммография в диагностике рака молочной железы // Дис. …канд. мед. наук. СПб., 1995.
- Кириллов B.C., Даниленко Э.Н., Литвинов В.В. Клинико-морфологическая характеристика узловой формы мастопатии // Маммология. 1995. N 2. С. 20-25.
- Кукин Н.Н. Диагностика и лечение заболеваний молочной железы // М., 1972. 239 с.
- Аинденбратен А.Д., Бурдина A.M., Пинхосевич Е.Г. Маммография. М.: Видар, 1997. 123 с.
- Аисъеба С.Д. Место УЗИ в комплексной диагностике опухолевых и предопухолевых заболеваний молочных желёз // Дис. …канд. мед. наук. Екатеринбург, 1998.
- Михайлова С.А., Скрынник Е.Б. Влияние возраста и диффузных дисгормональных гиперплазии на эффективность рентгеновской диагностики узловых новообразований молочной железы // Современная лучевая диагностика и лучевая терапия. Материалы науч.-практ. конф., посвящённой памяти проф. Б.К. Шарова, 31 октября 1997 г. Челябинск, 1997. С. 128-131.
- Озерова О.Е., Торлина В.Е. // Клин. мед. 1987. N 3. С. 105-109.
- Ошмянская А.И. Дифференциальная диагностика и лечебная тактика при дисгормональных дисплазиях молочных желёз // Маммология. 1993. N 2. С. 22-28.
- Рожкова Н.И., Харченко В.П., Якобе А.В. Современный взгляд на диагностику узловой мастопатии // Вестник рентгенологии и радиологии. 1995. N 6. С. 15-18.
- Трофимова Е.Ю. Ультразвуковая диагностика заболеваний молочной железы // Визуализация в клинике. 2002. N 6. С. 44-50.
- Харченко В.П., Рожкова Н.И., Якобе А.В. Комплексный подход к диагностике узловой мастопатии. Обзор // Маммология. 1995. N 1. С. 22-28.
- Якобе А.В. Комплексная лучевая диагностика узловой мастопатии// Дис. …канд. мед. наук. М., 1996.
- GuyerP.B., Dewbury K.C., Rubin CM. et al. // Clin. Radiol. 1992. Vol. 45. N 3. P. 175-178.
- Jamamoto Т., IrijamaK., Araki T. Male inflammatory breast cancer// Surg. Today. 1997. Vol. 27 (7). P. 669-671.
- Mushlin Alvin]. Diagnostic tests in breast cancer // Ann. Intern. Med. 1985.103. N 1. P. 79-85.
- Sciarra]. Грудное кормление и негенетические факторы риска рака молочной железы // Проблемы гинекологии. Материалы международного семинара по гинекологическим проблемам заболеваний молочной железы. 1998. С. 243-244.
- Sickles E.A., Filly R.A., Callen P.W. Breast cancer detection with sonography and mammography: comparison usung state of the art equipment // Amer. J. Radiol. 1983. Vol. 140. P. 843-845.
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Живите полной грудью!
По статистике, в мире 80% женщин в возрасте от 25 до 45 лет страдают мастопатией. При этом четкого понимания того, что такое мастопатия, у большинства представительниц прекрасного пола нет до сих пор. Для многих из нас любое уплотнение в груди ‑ это повод удариться в панику, поскольку широко распространено мнение, что «мастопатия ‑ предраковое состояние». А рака мы все боимся, как огня.
– Мастопатия ‑ однозначно не предраковое состояние, – говорит Олег Канаев, один из самых известных и уважаемых онкологов города Владимира. – Это фиброзно-кистозная болезнь в молочной железе. Думаю, миф, связывающий мастопатию с раком молочной железы, возник из-за определенных сложностей в диагностике. Просто очаговая мастопатия и начинающий развиваться рак иногда очень похожи. Поэтому на фоне узловых образований несколько труднее диагностировать рак.
– Надо ли женщине, вдруг обнаружившей в груди уплотнение, паниковать?
– Ни в коем случае. Во-первых, никакой стресс не пойдет на пользу здоровью. Во-вторых, уплотнение в молочной железе может оказаться чем угодно. Мастопатия бывает даже у совсем молоденьких. Это может быть и не диагноз даже, а симптом гормональных нарушений при перестройке организма. Вы говорите «вдруг обнаружила». Это не должно быть «вдруг». Каждой женщине надо ежемесячно себя осматривать. Причем в строго определенные дни: все обследования груди проводятся с 5 по 12 день цикла. Если женщина делает это регулярно, то она сразу поймет, если что-то не так. Но и это не повод для паники. А повод обратиться к специалисту. Большинство уплотнений в молочной железе ‑ это не рак, а проявление той или иной формы мастопатии.
– Мне говорили, что причины мастопатии нужно искать в нарушениях работы либо щитовидной железы, либо яичников…
– Правильно. Но и гипофиза тоже. На самом деле мастопатия ‑ это проблема внутреннего гомеостаза, то есть общего баланса внутри организма. Как гормонального, так и работы всех других органов и систем. Все же связано! Молочная железа ‑ орган, подверженный влиянию многих гормонов, поэтому мастопатия – частое заболевание. И от работы желудочно-кишечного тракта многое зависит. Даже, например, если нет сбоев в гормональной системе, а печень или желчный пузырь не работают или работают плохо, то циркулирующие в организме гормоны не выводятся со шлаками, накапливаются. В частности, у женщин таким депо гормонов является жировая ткань. То есть чем больше вес, тем хуже. В организме все должно работать, как часы. Если где-то сбой, то организм сам на начальных этапах все компенсирует благодаря своим восстановительным резервам. Но когда мы уже начинаем чувствовать какой-то орган, это говорит о том, что организм не справляется, и ему нужна помощь. Либо лечение, либо ‑ в легких случаях ‑ достаточно восстановить режим здорового питания, труда и отдыха.
– Так мастопатия излечима?
– Она даже сама может проходить. Если гормональный фон нормализовался, мастопатия проходит безо всякого лечения. Иногда вопрос так и ставится: а надо ли лечить? Есть ли там мастопатия или это просто гормональное нарушение, ПМС? Поэтому очень важна правильная диагностика.
– Что женщина сама может сделать, чтобы уберечься от мастопатии?
– Стандартные рекомендации ‑ ведите здоровый образ жизни. С дозированными физическими нагрузками. Прогулками на свежем воздухе. Правильно питайтесь, чтобы печень не зашлаковывать.
– Каковы основные факторы риска заболеваний молочной железы ‑ кроме лишнего веса?
– Поздние первые роды ‑ после 25 лет. Хотя сейчас это тенденция. Отсутствие беременностей. Отсутствие кормления грудью после родов. Аборты ‑ они резко обрубают гормональную цепочку в организме. Триада связанных между собой заболеваний «гипертония, ожирение, сахарный диабет», по официальным научным данным, повышает риск развития рака груди в три раза. Также среди факторов риска зашлакованность печени. Проблемы с желудочно-кишечным трактом. Слабая стрессоустойчивость. Потому что любое психо-эмоциональное перенапряжение приводит к выделению большого количества гормонов коры надпочечников ‑ адреналина, глюкокортикоидов, которые напрямую влияют на яичники. Поэтому я рекомендую всем женщинам стараться реагировать на стрессы спокойно ‑ буквально, как удавы. Все плохое в конце концов проходит, так что не надо нервничать. Лучше поберечь себя и тем самым сохранить здоровье. Это гораздо важнее.
Прямая речь
Олег Канаев, врач-онколог высшей категории:
– После 30 лет даже тем женщинам, кто никакого дискомфорта в груди не ощущает, рекомендуется УЗИ молочных желез раз в год. После 40 лет ‑ маммография раз в два года. И осмотр специалиста. При наличии проблемы ‑ то есть признаков мастопатии – в первую очередь надо идти искать проблему не к маммологу-онкологу, а к гинекологу и эндокринологу. Это же гормональное нарушение. Мастопатия может быть лишь сопровождающим симптомом кист яичников, миомы матки и т.д. Но, конечно, даже в этом случае маммолог дифференцирует онкологию или просто мастопатию и, сообразно рекомендациям гинеколога, что-то добавит к лечению или будет достаточно наблюдения за состоянием молочных желез.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Диабетическая мастопатия: отчет о 5 случаях и обзор литературы | Онкология | JAMA Surgery
Фон Диабетическая мастопатия – это необычное фибровоспалительное поражение груди, которое характерно для женщин в пременопаузе с длительным сахарным диабетом 1 типа с множественными микрососудистыми осложнениями.Считается, что патогенез этого состояния включает аутоиммунную реакцию на накопление аномального матрикса, вызванное гипергликемией. Клинико-патологические признаки включают развитие плотных келоидоподобных образований груди, которые часто рецидивируют, являются двусторонними или и тем, и другим. Клиническое отличие от злокачественного новообразования может быть затруднено. Однако доброкачественный характер этого поражения легко распознать при гистологическом исследовании, и он не связан с увеличением частоты эпителиальной или стромальной неоплазии.
Гипотеза Для постановки диагноза диабетической мастопатии необходимо сочетание гистопатологических и клинических признаков. При клиническом наблюдении пациентов с множественными, двусторонними и рецидивирующими поражениями можно избежать ненужного хирургического вмешательства.
Дизайн Серия кейсов.
Пациенты и методы В период с декабря 1993 г. по декабрь 1998 г. у 5 женщин в пременопаузе с сахарным диабетом 1 типа продолжительностью от 18 до 23 лет были обнаружены безболезненные, пальпируемые, твердые или твердые образования в груди.На сегодняшний день прогрессирование опухолевидных разрастаний было двусторонним и повторяющимся у 2 пациентов, двусторонним у третьего пациента и рецидивирующим у четвертого. У пятого пациента не было ни двусторонних, ни рецидивирующих поражений. Визуализирующие исследования ни у одного пациента не продемонстрировали очагового поражения. Все поражения лечили с помощью эксцизионной (4 пациента) или основной (1 пациент) биопсии. Резецированные препараты исследовали гистопатологически.
Результаты Общий осмотр образцов показал твердые массы с однородными желтовато-белыми поверхностями среза.Их максимальный диаметр составлял от 3,0 до 6,0 см. При микроскопическом исследовании выявлен келоидный фиброз с дуктитом, лобулитом и васкулитом. Клинический профиль в сочетании с этими патологическими особенностями характерен для диабетической мастопатии.
Выводы При лечении у женщин в пременопаузе врачи должны знать о связи длительного сахарного диабета с развитием доброкачественных фибровоспалительных поражений молочной железы. Мы описываем совокупность результатов клинического обследования, истории болезни, визуализационных исследований и гистопатологического исследования, которые необходимы для постановки диагноза диабетической мастопатии.Хотя эти образования в груди могут повторяться, они не являются предраковыми. В соответствующих условиях диагноз может быть поставлен с помощью центральной биопсии, что позволяет избежать ненужных операций у пациентов с множественными, двусторонними или рецидивирующими поражениями.
РАЗЛИЧНЫЕ МЕДИЦИНСКИЕ состояния связаны с доброкачественными заболеваниями груди, и врачи, ухаживающие за этими пациентами, должны сохранять высокий индекс подозрительности. Выявлена необычная мастопатия в сочетании с сахарным диабетом, которая может имитировать злокачественное новообразование при физикальном обследовании.Диабетическая мастопатия, 1 или диабетическая фиброзная болезнь молочной железы, 2 была впервые описана Soler и Khardori в 1984 году как плотное фиброзное разрастание стромы, которое происходит у женщин с длительным сахарным диабетом 1 типа и множественными микрососудистыми осложнениями. С тех пор дальнейшие исследования выявили гистопатологические особенности этого необычного фибровоспалительного поражения, которое составляет менее 1% доброкачественных поражений молочной железы. 3 -10 Описаны клинико-патологические особенности 5 случаев диабетической мастопатии.
В период с декабря 1993 г. по декабрь 1998 г. 5 женщин с сахарным диабетом 1 типа обратились в общий хирургический кабинет одной из нас (T.P.). Их клинические файлы были проанализированы на предмет типа, терапии и возраста начала диабета; история других эндокринных аномалий; возраст начала первого поражения груди; результаты физикального обследования новообразования груди; результаты визуализационных исследований, включая маммографию и ультрасонографию; и интраоперационные результаты.
У 4 из 5 пациентов было выполнено девять эксцизионных биопсий и две тонкоигольной аспирации. Пятому пациенту были выполнены 2 стержневые биопсии и 1 тонкоигольная аспирация. Были рассмотрены общие описания всех экземпляров. Гистологическое исследование всех препаратов биопсий и аспираций было интерпретировано одним из нас (P.M.C.).
Возраст 5 женщин на момент появления первого новообразования груди был от 30 до 36 лет (в среднем 34 года) (Таблица 1).При первичном обращении все пациенты страдали сахарным диабетом 1 типа в течение 18–23 лет (в среднем 20,4 года), и все получали длительную инсулиновую терапию. У всех, кроме 1, были вторичные осложнения диабета: у 3 пациентов была ретинопатия, у 1 из которых также была невропатия, а у четвертого была почечная недостаточность, гипертензия и перенесенный инсульт. Только у 1 пациента было вторичное эндокринное заболевание, гипотиреоз неустановленной этиологии.
При физикальном обследовании пациенток были обнаружены безболезненные, неподвижные, локализованные неправильные области на одной или обеих грудях, которые были твердыми, грубыми и часто плоскими.Они не были ни дискретными, ни круглыми, и их текстура отличалась от остальной части груди. Подмышечная аденопатия не была обнаружена ни у одного пациента, и никто не сообщил о травмах в этой области.
Все 5 пациентов прошли маммографию и ультрасонографию. Во всех случаях оба исследования изображений не смогли продемонстрировать какое-либо очаговое поражение, которое могло бы объяснить пальпируемую аномалию. Маммограмма показала плотную фиброгландулярную ткань без очаговой массы или искажения. Точно так же ультрасонограммы не показали кистозных или твердых образований.Во время операции было обнаружено, что поражения являются весьма доброкачественными, но явно отличаются от окружающей ткани груди.
При макроскопическом осмотре образования были твердыми с однородными желтовато-белыми поверхностями на разрезе. Максимальный диаметр образцов варьировался от 3,0 до 6,0 см, включая образец биопсии, который оценивался примерно в 3 см. Микроскопическое исследование всех образцов показало плотный келоидоподобный фиброз, связанный с периваскулярными, перидуктальными и перилобулярными лимфоцитарными инфильтратами (Рисунок 1 и Рисунок 2).Эпителиоидные фибробласты были обнаружены в 1 случае (рис. 2, вставка). Во всех случаях кистозных или гиперпластических изменений не отмечалось. Образцов тонкоигольной аспирации оказалось недостаточно для постановки диагноза.
Пациенты находились под наблюдением от 1 до 6 лет (в среднем 3,4 года). В анамнезе были выявлены двусторонние поражения у 3 пациентов, у 1 во время первичного обращения и у 2 через 7 месяцев и 3 года после первой биопсии. Рецидив произошел в 3 случаях, 2 из которых также были двусторонними. Один рецидив произошел через 1 год с 3 новообразованиями в том же месте.В другом случае наблюдались множественные двусторонние рецидивы через 11 месяцев после первоначальной биопсии левой груди, через 4 месяца после первоначальной биопсии правой груди и через 13 месяцев после второй биопсии обеих молочных желез. За это время массы увеличились в максимальном диаметре заполнителя с 2,5 до 7,0 см. Микроскопически поражения имели те же гистологические характеристики, что и те, что изображены на рисунках 1 и 2.
Диабетическая мастопатия – это необычное опухолевидное фиброзное разрастание груди.Диагноз требует соотнесения конкретного клинического профиля с отличительными патологическими признаками. 11 В большинстве опубликованных сообщений о диабетической мастопатии участвовали женщины в пременопаузе с длительным анамнезом сахарного диабета 1 типа, осложненного диабетической ретинопатией, невропатией или нефропатией. Сводка клинических признаков, описанных в литературе, приведена в таблице 2. 1 -10 Средний возраст пациентов на момент постановки диагноза первичного поражения груди составлял от 32 лет.От 2 до 62,0 лет, при длительности сахарного диабета от 4 до 43 лет. Это состояние также наблюдалось у пациентов с сахарным диабетом 2 типа, которые были инсулинозависимыми 7 , 8 и у пациентов с другими эндокринными нарушениями, особенно с заболеваниями щитовидной железы. 1 , 7 , 8 Были редкие сообщения об этом состоянии у мужчин. 7
Клинические данные включали единичные или множественные неточно очерченные, безболезненные, пальпируемые, твердые и твердые образования в одной или обеих молочных железах, которые вызывали подозрение на карциному.Маммограммы обычно выявляли локализованное увеличение плотности железистого рисунка без отчетливых образований, спикуляций или кальцификатов. Однако один исследователь сообщил об единичных случаях, когда результаты маммографии указывали на карциному или лимфому. 3 Результаты ультразвукового исследования поражений включали сильную акустическую тень позади узелков, которая предположительно коррелировала с количеством фиброзной ткани. 4 , 10 Однако никаких отдельных твердых или кистозных образований не было выявлено ни с помощью одного из методов визуализации.
Гистопатологическое исследование этих поражений показало плотные однородные образования диаметром от 2 до 6 см. Микроскопически они характеризуются келоидным фиброзом и вариабельной перидуктальной, перилобулярной или периваскулярной лимфоцитарной инфильтрацией, которая состоит в основном из В-клеток. Было обнаружено, что эти особенности являются уникальными для диабетической мастопатии, в отличие от пациентов с маститом и фиброзом, вторичными по отношению к другому процессу. 7 , 8 В некоторых случаях были описаны эпителиоидные фибробласты, характеризуемые как округлые клетки с обильной цитоплазмой и овальными ядрами, встроенными в плотный коллаген. 7 , 12 Тонкоигольная аспирация всех этих поражений обычно дает редкие элементы соединительной ткани. 7
Патогенез диабетической мастопатии до конца не изучен и, скорее всего, имеет многофакторный характер. Многие исследователи предполагают роль вторичной аутоиммунной реакции на аномальное накопление внеклеточного матрикса, которое является проявлением эффектов гипергликемии на соединительную ткань. Гипергликемия вызывает гликозилирование, повышенное межмолекулярное сшивание и расширение матрикса, количество и качество которого изменяется и становится устойчивым к деградации.Накопление аномального матрикса и продвинутых гликозилированных конечных продуктов создает «неоантиген», который запускает вторичную аутоиммунную реакцию с пролиферацией B-клеток и образованием аутоантител. 13 Последующее опосредованное макрофагами удаление конечного продукта гликозилирования и высвобождение цитокинов могут действовать как факторы роста и вызывать дополнительное расширение матрикса и пролиферацию коллагена. 7 , 8
Диабетическая мастопатия не связана с последующим развитием карциномы молочной железы или стромальной неоплазии.Для односторонних поражений достаточно лечения эксцизионной биопсией. Однако сводка данных в литературе показывает, что примерно 63% поражений являются двусторонними или рецидивирующими, или и тем, и другим, что имело место у 4 (80%) из 5 наших пациентов в течение среднего периода наблюдения 3,4 года. Это говорит о том, что естественная история этого состояния включает в себя многоцентровое полевое воздействие диабета на ткань молочной железы. Поскольку рецидивы, как правило, происходят в одном и том же месте и затрагивают больше ткани груди, чем предыдущее поражение, возможно, мастопатия влияет на процесс заживления, а сама операция усугубляет состояние.
Чтобы правильно консультировать и вести таких пациентов, хирурги должны знать о связи длительного сахарного диабета с развитием характерных фибровоспалительных поражений груди у женщин в пременопаузе. В соответствии с ранее процитированными рекомендациями, 4 , мы предлагаем, что диагноз диабетической мастопатии может быть установлен при соблюдении следующего набора результатов:
1. Пациентка в пременопаузе страдает хроническим сахарным диабетом 1 типа, который обычно сопровождается микрососудистыми осложнениями.Пациент может иметь или не иметь в анамнезе другие эндокринные или аутоиммунные заболевания.
2. При физикальном осмотре выявляется пальпируемое образование в груди, твердое, безболезненное и клинически подозрительное на карциному.
3. Маммографические исследования показывают повышенную плотность, но не подтверждают наличие локализованного образования. Ультрасонография также не позволяет выявить твердые или кистозные образования.
4. Эксцизионная или стержневая биопсия показывает плотный келоидный фиброз, связанный с периваскулярным, перидуктальным или перилобулярным лимфоцитарным инфильтратом.Эпителиоидные фибробласты могут присутствовать, а могут и не присутствовать. Поскольку образцы тонкоигольной аспирации обычно «не подходят для цитологического диагноза», мы не считаем это адекватным средством для диагностики или наблюдения за этими пациентами.
Рекомендуется минимальное плановое ежегодное наблюдение за пациентами с диабетической мастопатией, как и наша практика для всех пациентов с отклонениями от нормы при обследовании груди. Женщинам с диабетом с подозрительной массой груди или маммограмме, у которых нет патологических данных, соответствующих диабетической мастопатии при основной биопсии, требуется эксцизионная биопсия, чтобы исключить неоплазию.Однако при высоком индексе подозрительности в надлежащих клинических условиях диагноз диабетической мастопатии обычно можно поставить на основе стержневой биопсии, избегая ненужных хирургических процедур, которые могут фактически усугубить состояние.
Мы благодарим М. Гамбарделла, М. Смит, Д. Чепмен и П. Билински за помощь в подготовке рукописи.
Отпечатки: Тереза Понн, доктор медицины, ассоциация общей хирургии, 330 Орчард-стрит, апартаменты 305, Нью-Хейвен, Коннектикут 06511.
1.Soler Н.Г.Хардори R Фиброзная болезнь груди, тиреоидит и хироартропатия при сахарном диабете I типа. Ланцет. 1984; 1193-195Google ScholarCrossref 2.Pluchinotta AMTalenti ЕЛодовичетти грамм и другие. Диабетическая фиброзная болезнь молочной железы: клиническое заболевание, имитирующее рак. Eur J Surg Oncol. 1995; 21207-209Google ScholarCrossref 3.Byrd BFHartmann WHGraham LSHogle HH Мастопатия у инсулинозависимых диабетиков. Ann Surg. 1987; 205529-532Google ScholarCrossref 4.Logan WWHoffman Нью-Йорк Диабетическая фиброзная болезнь груди. Радиология. 1989; 172667-670Google Scholar5.Foschini MPCavazza AMacedo Pinto IMEusebi V Диабетическая фиброзная мастопатия: сообщение о двух случаях. Арка Вирхова Патол Анат Гистопатол. 1990; 417529-532Google ScholarCrossref 6. Гарстин WIHKaufman ZMichell MJBaum M Фиброзная мастопатия у инсулинозависимых диабетиков. Clin Radiol. 1991; 4489-91Google ScholarCrossref 7.Tomaszewski Дж. Э. Брукс JSJHicks DLiVolsi В.А. Диабетическая мастопатия: своеобразное клинико-патологическое образование. Hum Pathol. 1992; 23780-786Google ScholarCrossref 8.Seidman JDSchnaper LAPhillips Л.Е. Мастопатия при инсулинозависимом сахарном диабете. Hum Pathol. 1994; 25819-824Google ScholarCrossref 9. Морган MCWeaver MGCrowe JPAbdul-Karim FW Диабетическая мастопатия: клинико-патологическое исследование при пальпируемых и непальпируемых поражениях груди. Mod Pathol. 1995; 8349-354Google Scholar 10.Rode SFavre CThivolet C Диабетическая мастопатия: частый источник путаницы с лобулярной карциномой груди [письмо]. Уход за диабетом. 1998; 21322Google Scholar11.Bloomgarden ZT Эндотелиальная дисфункция, нейропатия и диабетическая стопа, диабетическая мастопатия и эректильная дисфункция. Уход за диабетом. 1998; 21183-189Google Scholar 12.Розен Патология груди П.П. Розена.Нью-Йорк, Нью-Йорк Липпинкотт-Рэйвен Паблишерс, 1997; 46-49
13. Шварц ISStrauchen JA Лимфоцитарная мастопатия: аутоиммунное заболевание груди? Am J Clin Pathol. 1990; 93725-730Google ScholarДоброкачественные воспалительные заболевания груди
Кейс-презентация
54-летняя афроамериканка обратилась с жалобой на постоянное пальпируемое уплотнение, боль и периодический генерализованный отек левой груди в течение примерно 7 месяцев.Она не заметила выделений из сосков или инверсии сосков, а также предыдущей биопсии в анамнезе не было. У нее не было ни личного, ни семейного анамнеза рака груди. Соответствующий акушерский анамнез включал одну предшествующую беременность с годом кормления грудью. В прошлом у нее не было серьезной истории болезни. При поступлении осмотр включал двустороннюю маммографию и УЗИ (, рисунки 1-3, ). Был получен аспират, который не показал роста через 5 дней. В конечном итоге была проведена биопсия под ультразвуковым контролем, а затем двусторонняя МРТ молочной железы (, рис. 4, ).
Ключевые клинические результаты
Односторонняя или двусторонняя боль и эритема в груди, часто с пальпируемым образованием
Ключевые результаты визуализации
Неспецифические маммографические находки, нерегулярные образования или скопления жидкости на УЗИ, а также новообразования, немассовые улучшения, ходы носовых пазух и скопления жидкости на МРТ
Дифференциальная диагностика
Идиопатический гранулематозный мастит
Абсцесс
Диабетическая мастопатия
Послеоперационный некроз жира
Волчаночный мастит
Саркоид
Mondor’s
Обсуждение
Воспалительные состояния груди включают широкий спектр причин, которые в целом делятся на 3 категории: инфекционный мастит, неинфекционный воспалительный мастит и воспаление, вторичное по отношению к лежащему в основе раку груди (воспалительный рак груди, IBC).Клинические и рентгенологические признаки доброкачественного мастита и ИБК в значительной степени совпадают, что часто задерживает диагностику и лечение.
Мастит – это воспаление паренхимы груди. Наиболее частые клинические проявления мастита включают боль, покраснение, тепло, подкожный отек и утолщение кожи. Рентгенологические признаки часто неспецифичны и могут имитировать IBC. В центре внимания этой статьи – доброкачественные воспалительные заболевания груди.
Дифференциальная диагностика
Идиопатический гранулематозный мастит
Идиопатический гранулематозный мастит (IGM) или гранулематозный лобулярный мастит – это необычное доброкачественное хроническое воспалительное состояние, впервые описанное в литературе Кесслером и Воллоком в 1972 году. 1 Окончательная причина неизвестна, но наиболее постулируемая этиология – аутоиммунная реакция, возможно, возникающая в результате начального поражения эпителиальных клеток протока с утечкой секреции люминального белка в дольчатую строму молочной железы. 2 IGM – это диагноз исключения, поскольку определенные типы рака груди включены в злокачественную дифференциацию. IGM обычно проявляется рецидивирующим или стойким течением болезни, что приводит к значительной заболеваемости пациентов. Чаще всего поражает рожавших в пременопаузе репродуктивного возраста с лактацией в анамнезе.Есть данные, указывающие на клиническую связь с гиперпролактинемией. 2 Это в основном одностороннее и обычно поражает периферию груди.
Визуализация IGM варьируется с фокальной асимметрией, как типичная маммографическая находка. 3 Другие менее распространенные маммографические находки включают неправильную массу и глобальную асимметрию. Также можно увидеть утолщение кожи и трабекул. На УЗИ наиболее частым проявлением является нерегулярное гипоэхогенное образование с сопутствующими изменениями протоков.Иногда сонографические особенности IGM могут имитировать внутрипротоковую папиллому, особенно если они расположены в ретроареолярной области. Результаты МРТ IGM чаще всего включают усиление кластерного кольца и немассовое усиление кластера (NME). Второй наиболее описываемый результат – это увеличение массы, причем наиболее распространенным образцом улучшения является усиление обода. Сообщалось также о дополнительных связанных признаках архитектурных искажений, очагового улучшения кожи, утолщения кожи, ходов носовых пазух, изъязвлений кожи, втягивания сосков и подмышечной лимфаденопатии. 4
Окончательный диагноз обычно ставится на основании гистопатологии, поскольку клинические и визуальные признаки неспецифичны. Центральная биопсия под ультразвуковым контролем имеет более высокую диагностическую эффективность по сравнению с тонкоигольной аспирацией (FNA), особенно в случаях абсцесса и некроза жира. По гистопатологии IGM характеризуется наличием неказеозных гранулем с различной степенью фиброза вокруг долек груди.
Окончательного лечения IGM не существует; поэтому лечение следует подбирать с учетом клинических проявлений каждого пациента.Варианты лечения включают консервативные меры, такие как тщательное клиническое наблюдение и визуализацию, медикаментозную терапию антибиотиками, кортикостероидами и / или иммунодепрессантами, такими как метотрексат. Более агрессивный хирургический подход – широкое местное иссечение.
Абсцесс (послеродовой, непухожильный)
Одной из частых причин болезненного уплотнения в груди является скопление инфицированной жидкости или абсцесс. Большинство абсцессов груди являются осложнениями инфекционного мастита. Обычно они возникают в первые 3 месяца после родов или при отлучении от груди; Таким образом, назвали послеродовые абсцессы. 5 Они вызываются бактериями, чаще всего Staphylococcus aureus, , которые проникают через небольшие разрывы кожи в застойные молочные протоки. Хотя и реже, непарперальные абсцессы молочной железы возникают из-за застоя молочной железы из-за закупорки протоков кератиновыми пробками. Факторы риска развития непарперальных абсцессов молочной железы, особенно в центральной части груди, включают чернокожую расу, ожирение и курение табака. Периферические абсцессы связаны с хроническими заболеваниями, приемом стероидов или недавними вмешательствами на груди. 5 Ультразвук и маммография обычно выполняются при обследовании пациентов старше 30 лет; однако ультразвук обычно является методом первой линии, поскольку пациенты часто испытывают боль. Типичные сонографические находки включают скопление гипоэхогенной жидкости с повышенной периферической васкуляризацией. Отек и гиперваскуляризация ткани также часто отмечаются по всей паренхиме прилегающей груди. Аспирация и дренирование под ультразвуковым контролем с антибактериальной терапией оказались эффективными при лечении как послеродовых, так и непарперальных абсцессов. 6 При отсутствии послеродового периода или при длительном клиническом течении следует учитывать лежащий в основе воспалительный рак молочной железы. 5
Послеоперационный некроз жира
Еще одна частая находка у пациентов с болезненным пальпируемым образованием – некроз жировой ткани. Гистологически некроз жира проявляется в виде пенистых гистиоцитов и гигантских клеток, окружающих липидные вакуоли и адипоциты. 7 Это может варьироваться в зависимости от времени обращения пациента, поскольку некроз жировой ткани обычно возникает в результате травмы.Это происходит после того, как повреждение сосудов вызывает воспаление в жировой ткани. В результате возникают отечные изменения, которые возникают, когда интерстиций наполняется жидкостью. Со временем может развиться фиброз, приводящий к образованию грануляционной ткани и фиброзному рубцеванию. Когда жир инкапсулируется в кальцифицированной грануляционной ткани, возникает масляная киста, которая маммографически проявляется в виде кальцификации ободка. До образования кальцинированных масляных кист некроз жира может проявляться как очаговая асимметрия, асимметрия или масса. Сонографически некроз жировой ткани следует гистологической шкале времени, первоначально наблюдаемый как отек во всех тканях.Это сопровождается повышенной эхогенностью жира или даже образованием дискретных кист с гиперэхогенными массами по всей паренхиме. Позже могут быть обнаружены кисты с периферической кальцификацией (масляная киста) или архитектурные искажения из-за фиброза. Т2-взвешенные изображения МРТ могут демонстрировать гиперинтенсивный сигнал от отека, а позже Т1-взвешенные изображения без жирового насыщения часто демонстрируют центральный гиперинтенсивный сигнал. 8
Диабетическая мастопатия
Диабетическая мастопатия – это необычное доброкачественное воспалительное заболевание, которое преимущественно наблюдается у женщин в пременопаузе с длительным инсулинозависимым диабетом.Типичное проявление – одно или несколько пальпируемых образований груди, твердых, но подвижных. Пациенты обычно имеют другие диабетические осложнения, такие как ретинопатия или невропатия. Хотя патофизиология не ясна, предполагаемый механизм представляет собой локализованную аутоиммунную реакцию. Воспалительная реакция приводит к инфильтрации лимфоцитами перидуктального, перилобулярного и периваскулярного пространств, что приводит к плотному келоидоподобному фиброзу, который выявляется при гистопатологии. 9,10 Из-за типичных клинических проявлений диабетическая мастопатия обычно оценивается с помощью маммографии и ультразвука.Маммография может демонстрировать различные типы асимметрии или, что менее вероятно, образование высокой плотности. Ультразвук покажет несосудистое, нерегулярное, гипоэхогенное образование с не ограниченными границами. Характерно выраженное заднее акустическое затемнение. Результаты МРТ плохо установлены и, как правило, не помогают в диагностике. Как клинические, так и визуальные признаки диабетической мастопатии имитируют таковые при раке груди, и для постановки диагноза необходима биопсия стержневой иглой. 10,11
Волчаночный мастит
Некоторые аутоиммунные процессы могут также проявляться симптомами со стороны груди.Редким феноменом молочной железы, проявляющимся у пациентов с системной красной волчанкой (СКВ), является волчаночный мастит, который может проявляться в виде болезненного пальпируемого уплотнения или одностороннего отека. Волчаночный мастит должен оставаться в дифференциальной диагностике пациентов с СКВ; тем не менее, это должен быть диагноз исключения, и забор ткани должен исключать другие, более распространенные этиологии. Пациенты с волчаночным маститом могут заметить один или несколько отдельных пальпируемых бугорков, которые увеличиваются и ослабевают, а иногда даже изъязвляются на коже.Другие клинические проявления включают общую асимметричную, увеличенную и болезненную пораженную грудь. Гистологически волчаночный мастит включает некроз гиалинового жира с промежуточными лимфоидными клетками. В конечном итоге наступают фибротические изменения. Иммунофлуоресценция может показывать IgG и C3 вдоль базальных мембран сосудов и на стыке дермы и эпидермиса. 12 Маммографические находки варьируются от дискретных масс до глобальной асимметрии. Сонографически неправильные образования неотличимы от злокачественных новообразований.Во многих случаях происходит скопление жидкости, иногда имитирующей абсцессы. МРТ неспецифична, чаще всего встречаются скопления жидкости и немассовое улучшение. 13
Саркоид
Редкий дифференциальный диагноз болезненного уплотнения груди включает вовлечение груди при саркоидозе. Саркоидоз – системное воспалительное заболевание неизвестной этиологии, которое приводит к образованию ненекротических гранулем в пораженных органах. 14 Обычно проявляется в третьем и четвертом десятилетиях жизни.Поражение груди саркоидозом встречается редко, а первичный саркоид груди встречается еще реже. При гистопатологическом исследовании паренхимные гранулемы можно увидеть среди долек груди и протоков. Подобный патологический процесс может поражать лимфатические узлы, вызывая их увеличение. 15 Результаты визуализации саркоидоза груди часто указывают на злокачественность. Маммография обычно выявляет нерегулярные образования с шипами. Ультразвуковые корреляты часто представляют собой нерегулярные гипоэхогенные образования. Также были описаны маленькие, ограниченные, круглые массы.Кальцификации в паренхиме груди обычно отсутствуют. 15 Для постановки диагноза необходимо исключить другие причины, включая биопсию с отрицательными окрасками и посевы на бактерии, микобактерии и грибки. Клинические доказательства саркоидоза в других частях тела наиболее полезны для постановки этого диагноза. 14
Болезнь Мондора
Болезнь Мондора – это острый тромбофлебит одной или нескольких поверхностных вен груди, который чаще всего встречается у женщин среднего возраста.Типичное проявление – пальпируемый тяж или новообразование, сопровождающееся очаговой болью и покраснением груди. Хотя во многих случаях заболевание носит идиопатический характер, заболевание часто связано с предшествующей травмой, например хирургическим вмешательством. 16 Ультразвук почти всегда является диагностическим, но из-за типичных симптомов обычно выполняется и маммография, и УЗИ. На маммографии тромбированная вена может быть видна как очаговая асимметрия трубчатой формы на поверхности груди. Ультразвук покажет расширенный поверхностный сосуд с недостаточной сжимаемостью и отсутствием внутрипросветного кровотока на допплеровском изображении. 10
Диагностика
Идиопатический гранулематозный мастит
Сводка
Гранулематозный лобулярный мастит – доброкачественное редкое хроническое воспалительное заболевание груди с неспецифической клинической картиной. Существует значительное совпадение характеристик визуализации IGM, других доброкачественных воспалительных образований и злокачественных новообразований. Это совпадение может привести к неправильной диагностике; однако дополнительная визуализация и отбор образцов тканей помогают исключить основные дифференциальные объекты.В конечном итоге цель состоит в том, чтобы поставить правильный диагноз и предотвратить отсрочку лечения. Может быть полезна корреляция с клиническими проявлениями и факторами риска. Окончательный диагноз основан на исключении других причин и соответствующих патологических данных биопсии.
Список литературы
- Kessler E, Wolloch Y. Гранулематозный мастит: поражение, клинически имитирующее карциному. Am J Clin Pathol 1972; 58 (6): 642-646.
- Pluguez-Turull CW, Nanyes JE, Quintero CJ, et al. Идиопатический гранулематозный мастит: проявления при мультимодальной визуализации и подводные камни.РадиоГрафика 2018; 38 (2): 330-356.
- Yilmaz E, Lebe B, Usal C, Balci P. Результаты маммографии и сонографии в диагностике идиопатического гранулематозного мастита. Евро Радиол 2001; 11 (11): 2236-2240.
- Чу А.Н., Зайлер С.Дж., Хейс Дж.С., Вулдридж Р., Порембка Дж. Х. Характеристики магнитно-резонансной томографии гранулематозного мастита. Clin Imaging 2017; 43: 199-201.
- Trop I, Dugas A, David J, et al. Абсцессы груди: доказательные алгоритмы диагностики, лечения и последующего наблюдения.RadioGraphics 2011; 31 (6): 1683-1699.
- Kasales CJ, Han B, Smith JS Jr и др. Непурперальный мастит и субареолярный абсцесс груди. Am J Roentgenol. 2014; 202 (2): W133-139. DOI: 10.2214 / AJR.13.10551.
- Cibas ES, Ducatman BS. Электронная книга по цитологии: диагностические принципы и клинические корреляты. 4-е изд. Elsevier Health Sciences; 2013.
- Атасой М.М., Орен Н.С., Илица А.Т. и др. Сонография жирового некроза груди: корреляция с маммографией и МРТ. J Clin Ultrasound 2013; 41 (7): 415-423.
- Tomaszewski JE, Brooks JS, Hicks D, Livolsi VA. Диабетическая мастопатия: отличительное клинико-патологическое заболевание. Хум Патол 1992; 23 (7): 780-786.
- Cao MM, Hoyt AC, Bassett LW. Маммографические признаки системного заболевания. РадиоГрафика 2011; 31 (4): 85-100.
- Dilaveri CA, MacBride MB, Sandhu и др. Грудные проявления системных заболеваний. Int J Womens Health 2012; 4: 35-43.
- Гулабчанд Р., Хафиди А., Ван де Перре П. и др. Мастит при аутоиммунных заболеваниях: обзор литературы, методы диагностики и ключевые патофизиологические факторы.Журнал J Clin Med 2020; 9 (4): 958.
- Ли SJ, Saidian L, Wahab RA, Khan S, Mahoney MC. Развитие визуализационных особенностей волчаночного мастита. Грудь J 2019; 25 (4): 753-754.
- Illman JE, Terra SB, Clapp AJ и др. Гранулематозные заболевания груди и подмышечной впадины: рентгенологические данные с патологической корреляцией. Insights Imaging 2018; 9 (1): 59-71.
- Sabate JM, Clotet M, Gomez A, et al. Радиологическая оценка необычных воспалительных и реактивных заболеваний груди. RadioGraphics 2005; 25 (2): 411-424.
- Bejanga BI. Болезнь Мондора: анализ 30 случаев. J R Coll Surg Edinb 1992; 37 (5): 322-324.
Доброкачественные новообразования молочной железы, имитирующие рак: определение радиолого-патологического соответствия
Маммография – золотой стандарт раннего выявления рака груди с чувствительностью 60-90% и общей специфичностью примерно 93%, 1 со средней степенью отзыва с просмотра 9,8%. Из тех напомним, примерно 12% женщин нуждаются в биопсии и более 60% биопсий доброкачественные, в среднем 4.8% положительный прогноз значение (PPV). 2,3,4 Хотя УЗИ является важным дополнением к маммографии и в настоящее время используется для обследования женщин с плотной тканью груди, 5 имеет относительно высокий уровень ложноположительных результатов. 6 Магнитно-резонансная томография (МРТ) рекомендуется в дополнение к маммография для женщин с повышенным риском поражения груди в течение жизни рак более 20-25%. Ежегодный скрининг с МРТ и маммографией начало в 30 лет для женщин из группы высокого риска считается эффективным. 7
Хотя рак груди относительно распространен и остается вторым ведущая причина смерти у женщин, большинство результатов было обнаружено на изображения, которые подвергаются чрескожной биопсии, являются доброкачественными. Кроме того, когда имеется несоответствие радиологии и патологии после биопсии под визуальным контролем, Впоследствии выполняется хирургическое иссечение. Дополнительная визуализация обследование и, в некоторых случаях, биопсия или даже операция по поводу этих доброкачественных поражения связаны с серьезным беспокойством пациента, потерей времени из-за работа и добавили расходы в систему здравоохранения.
На примерах случаев в этой статье обсуждаются общие и необычные благоприятные условия, которые проявляются в виде масс или архитектурных искажений на маммография, УЗИ и / или МРТ, которые могут демонстрировать особенности визуализации которые имитируют рак груди (Таблица 1). В результате радиологи будут познакомиться с доброкачественными новообразованиями груди, имитирующими рак груди. и лучше понять их управление.
Маммографические признаки, позволяющие прогнозировать злокачественные новообразования, включают опухоли с колючие края (PPV 81%) и неправильной формы (PPV 73%), в то время как массы с круглой или овальной формой, ограниченными полями и низкими или жиросодержащая плотность, вероятно, будет доброкачественной (отрицательный прогноз значение [NPV] 95%). 8,9,10 Сонографические особенности, предсказывающие злокачественные новообразования включают образования со шипами на краях (PPV 86%), нерегулярные форма (PPV 62%) и непараллельная ориентация (PPV 69%), тогда как массы с тонкой эхогенной капсулой (NPV 95%), ограниченным краем (NPV 90%), и параллельная ориентация (NPV 78%) указывают на доброкачественность. 11,12,13 На МРТ образование со спикулированными краями (PPV 88%), усиление края (PPV 79%) или кинетика вымывания (Тип III) (PPV 87%) предполагает злокачественность, в то время как дольчатая масса с не усиливающимися внутренними перегородками (NPV 95%) и стойкая (тип I) кинетика (NPV 94%) свидетельствует о доброкачественности. 14,15
Некроз жира
Некроз жира – негнойный воспалительный процесс, вторичный по отношению к случайная или хирургическая травма (например, тупая травма, биопсия, лампэктомия, уменьшение, увеличение, реконструкция, лучевая терапия) и гистологически характеризуется пенистыми гистиоцитами, насыщенными липидами макрофаги, воспалительные клетки с периферическим фиброзом и некрозом. Он может проявляться в виде безболезненного пальпируемого образования или может быть обнаружен. кстати на снимках.
Некроз жира имеет различные визуализации.Маммографический появление некроза жировой ткани варьируется от прозрачной массы, нечетко выраженной асимметрия, очаговая масса с микролобулатами, нечеткими или спикулярными края, к сгруппированным микрокальцификациям (рис. 1A, B, D). 16,17 Степень фиброза в поражении определяет его маммографический вид. Сонографически некроз жировой ткани может проявляться как киста, сложная кистозная или плотная масса с хорошо ограниченными рамками, нечеткие или заостренные края и архитектурное искажение окружающие ткани (рис. 1в, д). 18 На МРТ некроз жира характеризуется массой интенсивности жирного сигнала, часто содержащей уровень жировой жидкости с переменным увеличением после контрастирования. Другое МРТ внешний вид включает сплошную неоднородную массу с переменным сигналом интенсивность на T1- и T2-взвешенных изображениях и интенсивное усиление с Кинетика II или III типа. 19 Корреляция с историей болезни часто помогает в диагностике; однако для подтверждения диагноза может потребоваться биопсия.
Лучевой рубец / сложное склерозирующее поражение
Радиальный рубец (RS) – это псевдоинфильтративное поражение, характеризующееся фиброэластотическое ядро с захваченными протоками и окружающими излучающими протоками и дольки, демонстрирующие ряд эпителиальной гиперплазии. 20 Термин «радиальный рубец» используется для поражений <1 см, а термин «Сложное склерозирующее» поражение используется для очагов размером более 1 см. В эпителиальный компонент может проявлять различные атипии и может представлять собой nidus для развития протоковой карциномы in situ. RS обычно встречаются кстати в патологии образцы получены по другим причинам, но могут также видны как непальпируемые поражения, обнаруженные при скрининговой маммографии.
На маммографии RS обычно рассматриваются как центральная архитектурная область. искажения, и лучше видны в одной проекции, без каких-либо заметная центральная масса или втягивание вышележащей кожи. 21 Поражение имеет вид «черной звезды» с длинными тонкими, расходящимися лучами спикулами. из центральной рентгенопрозрачной области (рис. 2А). УЗИ не всегда может обнаруживают RS, но могут показать плохо очерченную гипоэхогенную область или нерегулярная гипоэхогенная масса с нечеткими шипами на краях и разная степень затенения кзади. 22 Нет специфические сонографические особенности, которые отличают RS от рака груди. МРТ обычно демонстрирует фокальную область слабого сигнала архитектурного искажение на T1- и T2-взвешенных изображениях с улучшением в диапазоне от нет / от минимального до интенсивного усиления, иногда с кинетикой III типа (Рисунок 2b). 23 Накопление доказательств указывает на связь с атипией и / или злокачественности и предполагает, что это независимый фактор риска развитие карциномы в любой груди. Следовательно, иссечение рекомендуется после диагноза лучевого рубца при биопсии стержневой иглы. 20,21
Гранулярно-клеточная опухоль
Гранулярно-клеточная опухоль молочной железы – редкая опухоль, возникающая из Шванновские клетки. Это может произойти в любом месте тела примерно в 5-8% случаев, замеченных в груди. 24 Пациенты обращаются с единичным односторонним твердым безболезненным образованием. имитирует рак и может иметь втягивание кожи и инверсию сосков. 25 Маммографические признаки варьируются от круглой ограниченной массы до нечеткая или спикулированная масса с кальцификациями или без них (Рисунок 3а). 26 На УЗИ они слабо проявляются как гипоэхогенные определенная сплошная масса с заметной задней затенением, хотя она также может представлены как четко очерченная твердая масса с переменной эхогенностью (Рисунок 3b).Также описан периферический эхогенный ореол. 26 Внешний вид МРТ неспецифичен и включает очаговую массу с переменным высокий сигнал на Т2-взвешенной последовательности и гомогенное или ободчатое усиление после введения контраста. 27 Лечение варьируется от последующего визуализации до широкого хирургического удаления. 26,27 Возможны местные рецидивы.
Поражения веретенообразных клеток
,00Поражения веретенообразных клеток включают широкий спектр пролиферативных заболевания, некоторые из которых доброкачественные.Результатом является множество повреждений веретенообразных клеток. от чрезмерного роста фибробластов и миофибробластов, которые являются нормальным часть стромы дольчатой молочной железы. 28,29 Доброкачественные разрастания фибро- и миофибробластов имеют диапазон клинических характеристик и включает псевдоангиоматозную стромальную гиперплазия (PASH), миофибробластома и фиброматоз. Это трудно различать различные типы поражения веретенообразных клеток как на визуализация и гистопатология из керна биопсии. Получение достаточного образцы тканей во время биопсии имеют решающее значение для постановки точного диагноза по пункционной биопсии и устранению необходимости в последующем хирургическом вмешательстве. иссечение.
Фиброматоз
Фиброматоз молочной железы, также известный как десмоидная опухоль, представляет собой редкую доброкачественную опухоль фибробластов и миофибробластов. 30,31 Клинически он представляет собой твердую, безболезненную, подвижную массу, хотя пациенты могут испытывать очаговую боль, если опухоль затрагивает грудную клетку. стена. Дополнительные физические данные могут включать ретракцию кожи, ямочка или втягивание соска, вызывающее подозрение на рак груди. 30,31 На маммографии фиброматоз обычно проявляется в виде спикулированной массы. тогда как на УЗИ он обычно представляет собой гипоэхогенное образование с спикулированные, нерегулярные или микролобулированные края 30 (Рис. 4а).На МРТ это обычно появляется как образование с сигналом от низкого до среднего. интенсивность на T1-взвешенных изображениях и переменная интенсивность сигнала Т2-взвешенные маги с доброкачественной кинетикой или кинетикой типа I. 32 Сундук вовлечение стенок лучше всего оценивается с помощью МРТ (рис. 4b). Широкий хирургический иссечение является предпочтительным, так как эти опухоли имеют тенденцию быть местно агрессивными. 31
Миофибробластома
Миофибробластома – это доброкачественная опухоль миофибробластов, которая чаще встречается у мужчин, чем у женщин. 33 Клинически он представляет собой единичный, медленно растущий, безболезненный и мобильный масса.На маммографии он выглядит как четко очерченный круглый или яйцевидный плотный масса от 1 до 4 см в диаметре (рис. 4в). 34 Вкл. Ультразвук, как правило, представляет собой твердую, ограниченную, однородно гипоэхогенная масса; однако он может также представлять собой нечеткое образование с затемнением сзади (рис. 4d). 35 Большинство клиницистов также рекомендуют хирургическое удаление этих поражений.
Псевдоангиоматозная гиперплазия стромы (PASH)
PASH, тип поражения веретенообразных клеток, представляет собой доброкачественный рост стромальных миофибробластов, чаще всего обнаруживаемый у женщин в пременопаузе. 36 Пациенты могут иметь безболезненное пальпируемое образование или PASH. обнаружил случайно на снимке. На маммографии PASH обычно представляет собой не кальцинированную овальную массу или развивающуюся очаговую асимметрию (Рисунок 4e). 37 На УЗИ чаще всего представляет собой хорошо очерченную овальную гипоэхогенную массу. 36,37 Гистологически PASH характеризуется щелевидными промежутками в строме. выстланы веретеновидными миофибробластами. Эти щелевидные пространства легко ошибочно принимают за сосудистые пространства (отсюда и название псевдоангиоматозный), и может быть ошибочно интерпретирован как ангиосаркома. 37 Патогенез плохо изучен, однако гормоны яичников могут играть роль. PASH может увеличиваться, но доброкачественный и не требует иссечения, хотя некоторые пациенты выбирают хирургическое удаление.
Воспалительные состояния
Мастит
Мастит – это очаговая или диффузная инфекция груди, проявляющаяся как у послеродовые и непериодические состояния. Пациенты с острым маститом обычно проявляется нежностью, покраснением, отеком и теплом грудь. Диагноз часто ставится на основании клинических симптомов и реакции на антибиотики.Хронический мастит, обычно наблюдаемый в непериодических состояниях, клинически проявляется асимметричным утолщением груди, опухолью груди, выделения из сосков и / или подмышечная лимфаденопатия без каких-либо конституциональные симптомы.
Маммография может быть затруднена из-за болезненности и груди отек и может быть отрицательным или показывать очаговое / диффузное утолщение кожи или нечеткая очаговая асимметрия. 38 Сонография демонстрирует утолщение кожи, повышенную эхогенность. жира, потери плоскостей тканей и / или расширенных протоков (более 3 мм) или лимфатические сосуды. 38 Очаговая гетерогенная гипоэхогенная масса с толстые неровные стенки и повышенная периферическая васкуляризация, представляющая также часто можно увидеть абсцесс (рис. 5а). Стремление может быть недиагностика, так как содержимое абсцесса толстое и содержит грануляции ткани и культуры часто не содержат микроорганизмов. Лечение – чрескожный дренаж и антибиотики, хотя хирургическое иногда требуется вмешательство. МРТ может показать очаговую или диффузную кожу утолщение, толстостенная очаговая масса с переменным усилением и протоковой усиление и лимфаденопатия. 39 Результаты визуализации неспецифическая, и следует выполнить стержневую биопсию, чтобы исключить воспалительная карцинома, если нет клинического улучшения антибиотики.
Гранулематозный мастит
Гранулематозный мастит – редкое заболевание, обычно встречающееся у молодых женщин и связан с беременностью, кормлением грудью и пероральным контрацепция. 40 Клинически он часто имитирует воспалительный рак и проявляется как плохо очерченные участки утолщения и подмышечной лимфаденопатии.На маммография, как правило, проявляется в виде нечеткой очаговой асимметрии, хотя он может также проявляться в виде множественных небольших нечетко очерченных масс. 40 41 На УЗИ это обычно нечеткое гипоэхогенное образование. с повышенной васкуляризацией в непосредственной близости от протоков (рис. 5b). 40 41 МРТ обычно показывает низкую массу сигнала с плохо очерченными краями, имитирующую злокачественную опухоль. 41 Диагноз ставится на основании керновой биопсии с выявлением гистологического исследования. неказеозные, неинфекционные гранулемы в долях груди.Много пациенты отвечают на лечение кортикостероидами и находятся под наблюдением тщательное клиническое наблюдение и визуализационное наблюдение, хотя некоторые в конечном итоге требуют хирургическое широкое иссечение. 42 Рецидив наблюдается у 25% пациентов.
Диабетическая мастопатия
Диабетическая мастопатия (СД) – редкое доброкачественное фибровоспалительное заболевание. состояние груди. СД обычно встречается у женщин в пременопаузе. страдает хроническим сахарным диабетом I типа, но также встречается у недиабетических пациентов с другими аутоиммунными заболеваниями. 43 Клинически и рентгенологически СД характеризуется плотной, фиброзной ткань груди, которую трудно отличить от рака груди. Клинически он проявляется как односторонний или двусторонний, однократный или множественный. твердые, пальпируемые, нерегулярные, безболезненные образования. 43 На маммографии это часто проявляется как очаговая асимметрия или масса. 44 На УЗИ обычно видны значительные задние акустические затенение с неравномерными и диффузными зонами затенения (рис. 5C). 44,45 Патогенез плохо изучен, однако современные теории предполагают что гликозилирование из-за гипергликемии может индуцировать внеклеточный матрикс расширение и аутоиммунный ответ, который приводит к дальнейшей матрице распространение. 43
Другие доброкачественные состояния
Другие доброкачественные образования, имитирующие рак груди, включают болезнь Купера. связки, саркоидоз и инфаркт груди. Связки Купера могут демонстрируют затенение на УЗИ (рис. 6А), но изображение в ортогональная плоскость не будет демонстрировать стойкую аномалию, поэтому подтверждая нормальное анатомическое строение.
Саркоидоз – доброкачественное гранулематозное системное заболевание неизвестного происхождения. этиология, которая может вторично влиять на грудь в <1% случаев 46 у пациентов с активным системным заболеванием.Чаще всего это представлено как двусторонняя подмышечная и / или интрамаммарная лимфаденопатия, лучше всего оценивается как плотно увеличенные узлы на маммографии или как аномальные увеличенные узлы с утолщенной корой на УЗИ. В редких случаях саркоидоз может проявляться как образование нерегулярной или спикулированной груди или как развитие асимметрии при маммографии или нерегулярное гипоэхогенное образование на УЗИ (рис. 6Б). На МРТ подозрительно улучшающийся нерегулярный сообщалось о массе с прогрессирующей кинетикой вымывания. 47 Практически во всех случаях показана биопсия для исключения злокачественных новообразований.
Инфаркт груди – редкое заболевание, которое обычно проявляется болезненное пальпируемое уплотнение, но также редко может быть сгруппированным кальцификаты на маммографии (рис. 6C). 48 Это связано с беременностью и кормлением грудью и может быть замечено у пациентов, принимающих системные антикоагулянты, такие как варфарин. Биопсия часто выполняется для исключения злокачественных новообразований.
Заключение
Несмотря на то, что рак груди имеет характерные особенности визуализации, он часто трудно диагностировать рак только на основании изображений и биопсии необходимо для точного диагноза.Высокая частота доброкачественной груди состояния, имитирующие злокачественное новообразование, указывают на то, что тщательная корреляция между рентгенологическими и патологическими данными. Знакомство с доброкачественными новообразованиями груди повышает уверенность рентгенологов после биопсия стержневой иглой, развеивает страхи пациента и предотвращает ненужные хирургическое иссечение. Наконец, сочетание мультимодальной визуализации и оценка факторов риска пациента и клинические проявления будут обеспечить оптимальный уход за пациентом.
Список литературы
- Carney PA, Miglioretti DL, Yankaskas BC, et al.Индивидуальные и комбинированные эффекты возраста, плотности груди и заместительной гормональной терапии использовать на точность скрининга мам мография. Энн Интерн Мед. . 2003. 138: 168–175.
- Янкаскас BC, Кливленд Р.Дж., Шелл М.Дж., Козар Р. Ассоциация процент отзыва с чувствительностью и положительной прогностической ценностью скрининговая маммография. AJR Am J Рентгенол . 2001; 177: 543-549.
- Розенберг Р.Д., Янкаскас BC, Абрахам Л.А. и др. Тесты производительности для скрининговой маммографии. Радиология. 2006; 241: 55-66.
- Sickles EA, Miglioretti DL, Ballard-Barbash R, et al. Тесты производительности диагностической маммографии. Радиология. 2005; 235: 775-790.
- Хули Р.Дж., Гринберг К.Л., Стакхаус Р.М. и др. Скрининг США в пациенты с маммографически плотной грудью: начальный опыт работы с Государственный закон Коннектикута 09-41. Радиология. 2012; 265: 59-69.
- Corsetti V, Houssami N, Ferrari A и др. Скрининг груди с УЗИ у женщин с плотной грудью, отрицательной по результатам маммографии: данные дополнительное обнаружение рака и ложноположительные результаты, а также связанные с этим расходы. Eur J Cancer. 2008; 44: 539-544.
- Lowry KP, Lee JM, Kong CY, et al. Ежегодные стратегии скрининга в Носители мутаций генов BRCA1 и BRCA2: сравнительная эффективность анализ. Рак. 2012; 15; 118: 2021-2030.
- D’Orsi CJ, Sickles EA, Mendelson EB, Morris EA, et al. ACR BI-RADS ® Атлас, Система отчетов и данных визуализации груди. Рестон, штат Вирджиния, Американский колледж радиологии; 2013.
- Либерман Л., Абрамсон А.Ф., Сквайрс Ф. Б. и др.Визуализация груди система отчетности и данных: положительная прогностическая ценность маммографических особенности и итоговые оценочные категории. AJR Am J Roentgenol. 1998; 171: 35-40.
- D’Orsi CJ, Kopans DB. Анализ маммографических признаков . Семин Рентгенол . 1993; 28: 204–230.
- Lazarus E, Mainiero MB, Schepps B и др. Лексика BI-RADS для США и маммография: вариабельность между наблюдателями и положительная прогностическая ценность. Радиология . 2006; 239: 385-391.
- Hong AS, Rosen EL, Soo MS, Baker JA. BI-RADS для сонографии: положительные и отрицательные прогностические значения сонографических характеристик. AJR Am J Рентгенол . 2005. 184: 1260–1265.
- Ставрос Т., Тикман Д., Рапп К.Л. и др. Твердые узелки груди: применение сонография для различения доброкачественных и злокачественных образований. Радиология . 1995; 196: 123–134.
- Икеда Д.М., Хилтон Н.М., Кинкель К. и др. Разработка, стандартизация, и тестирование словаря для сообщения о груди с контрастным усилением магнитно-резонансные исследования. J Magn Резонная визуализация . 2001; 13: 889-895.
- Liberman L, Morris EA, Lee, MJ, et al. Поражения груди, обнаруженные на МРТ: особенности и прогностическая ценность. AJR Am J Roentgenol. 2002; 179: 171-178.
- Хогге Дж. П., Робинсон Р. Э., Магнант С. М. и др. Маммографический спектр жирового некроза груди. RadioGraphics. , 1995; 15: 1347-1356.
- Табоада Дж. Л., Стивенс Т. В., Кришнамурти С. и др. Многоликая жировая некроза груди. AJR Am J Roentgenol. 2009; 192: 815–825.
- Soo MS, Kornguth PJ, Hertzberg BS. Некроз жира в груди: сонографические особенности. Радиология . 1998. 206: 261–269.
- Daly CP, Jaeger B, Подоконник DS. Различные проявления некроза жира на МРТ груди. AJR Am J Рентгенол . 2008; 191: 1374-1380.
- Кеннеди М., Мастерсон А.В., Крейн М., Фланаган Ф. Патология и клиническое значение лучевых рубцов: обзор. J клин патол. 2003; 56: 721–724.
- Shaheen R, Schimmelpenninck CA, Stoddart L, et al. Спектр заболевания, проявляющиеся на маммографии как архитектурные искажения: мультимодальная радиологическая визуализация с патологической корреляцией. УЗИ семин КТ MR . 2011; 3: 351–362.
- Cohen MA, Sferlazza SJ. Роль сонографии в оценке радиальных рубцов груди. AJR Am J Roentgenol. 2000; 174: 1075-1078.
- Pediconi F, Occhiato R, Venditti F и др. Радиальные рубцы грудь: внешний вид на магнитно-резонансной маммографии с контрастным усилением. Грудь J . 2005; 11: 23-28.
- Адениран А., Аль-Ахмади Х., Махони М.С., Робинсон-Смит TM. Гранулированный клеточная опухоль молочной железы: серия из 17 случаев и обзор литература. Грудь J . 2004. 10: 528–531.
- Lack EE, Worsham GF, Callihan MD, et al. Гранулярно-клеточная опухоль: клинико-патологическое исследование 110 пациентов. J Surg Oncol. 1980; 13: 301–316.
- Ян В.Т., Эдейкен-Монро Б., Снейдж Н., Форнаж Б.Д. Сонографический и маммографические проявления гранулярно-клеточных опухолей молочной железы с патологическая корреляция. J Clin Ультразвук. 2006; 34: 153–160.
- Скаранело А.М., Буханов К., Кристалл П и др. Гранулярно-клеточная опухоль молочной железы: результаты МРТ и обзор литературы . Br J Radiol. 2007; 80: 970–974.
- Броджи Э. Доброкачественные и злокачественные веретено-клеточные поражения груди . Semin Diagn Pathol. 2004; 21: 57–64.
- Schnitt SJ. Поражения веретенообразных клеток груди. Клиника хирургического тракта . 2009; 2: 375-390.
- Эргуван-Доган Б., Демпси П.Дж., Айяр Г., Гилкриз М.З.Первичная десмоидная опухоль (экстраабдоминальный фиброматоз) груди . AJR Am J Roentgenol. 2005; 185: 488–489.
- Шварц Г.С., Дротман М., Розенблатт Р., Милнер Л. и др. Фиброматоз груди: история болезни и современные концепции ведения необычное поражение. Breast J. 2006; 12: 66–71.
- Наказоно Т., Сато Т., Хамамото Т., Кудо С. Динамическая МРТ фиброматоза груди. AJR Am J Roentgenol. 2003; 181: 1718–1719.
- Mele M, Jensen V, Worenecki A, Lelkaitis G.Миофибробластома груди: описание случая и обзор литературы. Int J Surg Case Rep. 20112: 93-6.
- Dockery WD, Singh HR, Wilentz RE. Миофибробластома мужчины грудь: визуализация и диагностика стержневой биопсии под контролем УЗИ. Грудь J . 2001 май-июнь; 7: 192-4.
- Yoo EY, Shin JH, Ko EY и др. Миофибробластома женской груди Результаты маммографической, сонографической и магнитно-резонансной томографии . J Ultrasound Med. 2010; 29: 1833-1836.
- Celliers L, Wong D, Bourke A. Псевдоангиоматозная гиперплазия стромы: изучение маммографических и сонографических особенностей. Clin Radiol. 2010. 65: 145–149.
- Hargaden G. Анализ маммографических и сонографических особенностей псевдоангиоматозной гиперплазии стромы. AJR Am J Roentgenol. 2008; 191: 3593-63.
- Ferron S, Asad-Syed M, Boisserie-Lacroix M, et al. Визуализация доброкачественных воспалительных синдромов. Диагностика интервальной визуализации .2012; 93: 85–94.
- Рибер А., Томчак Р.Дж., Мерго П.Дж. и др. МРТ груди в дифференциальная диагностика мастита по сравнению с воспалительной карциномой и следовать за. J Comput Assist Tomogr . 1997; 21: 128-132.
- Ованесян Ларсен Л.Дж., Пейванди Б., Клипфель Н. и др. Гранулематозный лобулярный мастит: визуализация, диагностика и лечение. AJR Am J Roentgenol. 2009; 193: 574–581.
- Дурсун М., Йылмаз С., Яхьяев А. и др. Мультимодальная визуализация особенности идиопатического гранулематозного мастита: исход 12 лет опыт. Radiol Med. Июнь 2012 г .; 117: 529-38. DOI: 10.1007 / s11547-011-0733-2. Epub 2011 21 октября
- Тагизаде Р., Шелли О.П., Чу Б.К., Вейлер-Митхофф Э.М. Идиопатический гранулематозный мастит: хирургия, лечение, реконструкция. Breast J. 2007; 13: 509–513.
- Чан С.Л., Хо Р.С., Шек Т.В., Квонг А. Диабетическая мастопатия. Breast J. 2013; 19: 533–538.
- Neetu G, Pathmanathan R, Weng NK. Диабетическая мастопатия: отчет о болезни и обзор литературы. Корпус Rep Oncol . 2010; 3: 245–251.
- Франсиско С., Жулио С., Фонтес А.Л. и др. Диабетическая мастопатия: история болезни. Clin Imaging. 2012; 36: 829–32.
- Isley LM, Cluver AR, Leddy RJ, Baker MK. Первичный саркоид груди со случайным злокачественным новообразованием. J Clin Imaging Sci. 2012; 2: 46.
- Kenzel PP, Hadijuana J, Hosten N, et al. Саркоидоз груди: результаты маммографии, УЗИ и МРТ. J Comput Assist Tomogr .1997; 21: 439–441.
- Люси Дж. Спонтанный инфаркт груди. J Clin Pathol. 1975; 28: 937–943.
Боль в груди
% PDF-1.5 % 1 0 obj > эндобдж 2 0 obj > поток
Неизвестный случай № 5 Диагноз: лимфоцитарная мастопатия, ассоциированная с ревматоидным артритом | Журнал визуализации груди
Часть 2
История
38-летняя женщина обратилась с жалобой на пальпируемую аномалию правой груди, в анамнезе ревматоидный артрит и семейный анамнез рака груди у матери в возрасте 60 лет и тетушек в неизвестном возрасте.Пациентке была проведена диагностическая маммография (рис. 1) и последующая МРТ (рис. 2) по поводу пальпируемой аномалии в правой груди.
Рисунок 1.
Двусторонний маммографический краниокаудальный (CC) и медиолатеральный косой (MLO) виды с маркером BB (стрелка), разграничивающим пальпируемую область в правой груди на 9–10 часах. Маммограмма справа демонстрирует очаговую асимметрию в правой центральной / наружной передней глубине груди, соответствующей пальпируемой области.
Рисунок 1.
Двусторонняя маммографическая краниокаудальная (CC) и медиолатеральная косая проекции (MLO) с маркером BB (стрелка), ограничивающим пальпируемую область в правой груди на 9–10 часах. Маммограмма справа демонстрирует очаговую асимметрию в правой центральной / наружной передней глубине груди, соответствующей пальпируемой области.
Рисунок 2.
МРТ молочной железы ( A ) аксиальная Т2-взвешенная жиронасыщенная, ( B ) аксиальная Т1-взвешенная жиронасыщенная постконтрастная вычитание, ( C ) аксиальная Т1-взвешенная и ( D ) аксиальный Т1-взвешенный постконтраст, насыщенный жиром.Правая грудь демонстрирует немассовое увеличение на 3 см на глубине от 9 до 10 часов спереди (стрелки), что соответствует пальпируемой аномалии и очаговой асимметрии, наблюдаемой на маммографии.
Рисунок 2.
МРТ молочной железы ( A ) аксиальная Т2-взвешенная жиронасыщенная, ( B ) аксиальная Т1-взвешенная жиронасыщенная постконтрастная вычитание, ( C ) аксиальная Т1-взвешенная и ( D ) аксиальный Т1-взвешенный постконтраст, насыщенный жиром. Правая грудь демонстрирует немассовое увеличение на 3 см на глубине от 9 до 10 часов спереди (стрелки), что соответствует пальпируемой аномалии и очаговой асимметрии, наблюдаемой на маммографии.
Диагноз: лимфоцитарная мастопатия, ассоциированная с ревматоидным артритом
Диагностическая маммограмма (рис. 1) продемонстрировала очаговую асимметрию, соответствующую пальпируемой области правой груди на глубине от 9 до 10 часов спереди. Для маммографической находки не было сонографического коррелята. МРТ (рис. 2) была проведена с учетом семейного анамнеза. МРТ показала справа от 9 до 10 часов на глубине передней части, соответствующую 3-сантиметровую область немассового увеличения с низким центральным сигналом T1 и T2, указывающим на фиброз.
Дифференциальный диагноз по результатам визуализации включает инвазивную протоковую карциному, инвазивную лобулярную карциному, псевдоангиоматозную гиперплазию стромы (PASH) и фиброз стромы. Биопсия этой области выявила лимфоцитарную мастопатию, связанную с ревматоидным артритом. Это доброкачественное заболевание может имитировать рак груди, и оно было описано у женщин с давним системным аутоиммунным заболеванием, таким как ревматоидный артрит, тиреоидит Хашимотоса, синдром Шегрена, волчанка или диабет (1–3).Средний возраст обращения – у женщин в пременопаузе 34–47 лет (4, 5). Эта пациентка обратилась в 38-летнем возрасте, у нее длительный анамнез ревматоидного артрита, последние шесть лет она принимала гидроксихлорохин по поводу серонегативного ревматоидного артрита.
Гистопатологическая оценка демонстрирует фибровоспалительное поражение со стромальными изменениями, включая фиброз и лимфоцитарные инфильтраты вокруг дольчатых единиц (6). Пациенты часто описывают безболезненное образование, а маммография часто выявляет асимметрию (2, 3, 7).Ультразвук может выявить подозрительные признаки, такие как гипоэхогенное поражение с задней акустической затенением (2, 3, 7). МРТ может показать замедленное усиление, наводящее на мысль о фиброзе; однако нет никаких уникальных признаков, позволяющих отличить лимфоцитарную мастопатию, ассоциированную с ревматоидным артритом, от рака груди (2). Чтобы исключить злокачественные новообразования, необходимо провести центральную биопсию, поскольку тонкоигольная аспирация не рекомендуется из-за низкой клеточности этих поражений (1–3, 6). Специфической терапии проявления в молочной железе не существует, вместо этого существует постоянное ведение системного заболевания (2, 3).Рекомендуется плановое последующее наблюдение с визуализацией молочных желез без дополнительного наблюдения (3).
Радиологам важно знать об этом заболевании, потому что это системное проявление заболевания груди.
Заявление о конфликте интересов
Не объявлено.
Список литературы
1.Кампос
GC
,Castro
MV
,de Mattos
VF
,Pinto
LZ
,Boechat
MC
,Dos Santos
AA
.Лимфоцитарная мастопатия, имитирующая злокачественное новообразование груди: клинический случай
.Бюстгальтеры Radiol
2014
;47
(4
):256
–258
. 2.Sabaté
JM
,Clotet
M
,Gómez
A
,De Las Heras
P
,Torrubia
S
,Salinas
T
.Радиологическая оценка необычных воспалительных и реактивных заболеваний груди
.Радиография
2005
;25
(2
):411
–424
. 3.Декрен
Дж
,Van Ongeval
C
,Clinckemaillie
G
,Wildiers
H
.Склерозирующий лимфоцитарный лобулит, имитирующий рецидив опухоли у молодой женщины с раком груди в анамнезе
.J Belg Soc Radiol
2015
;99
(1
):72
–75
. 4.Розен
PP
.Воспалительные и реактивные опухоли
. В:Патология груди Розена
. 4-е изд.Филадельфия, Пенсильвания, Липпинкотт Уильямс и Уилкинс
,2014
:66
–68
. 5.Ламми
GA
,Bobrow
LG
,Staunton
MD
,Levison
DA
,Page
G
,Millis
RR
.Склерозирующий лимфоцитарный лобулит груди – свидетельство аутоиммунного патогенеза
.Гистопатология
1991
;19
(1
):13
–20
.6.Шварц
IS
,Strauchen
JA
.Лимфоцитарная мастопатия. Аутоиммунное заболевание груди?
Am J Clin Pathol
1990
;93
(6
):725
–730
.7.Уильямс
PH
,Рубин
CM
,Theaker
JM
.Склерозирующий лимфоцитарный лобулит груди
.Clin Radiol
1995
;50
(3
):165
–167
.© Society of Breast Imaging 2020. Все права защищены. Для получения разрешений, пожалуйста, пишите на электронную почту: журналы[email protected]
Доброкачественные заболевания груди – AMBOSS
Последнее обновление: 18 марта 2021 г.
Резюме
Существует ряд доброкачественных заболеваний, которые могут повлиять на грудь, включая врожденные аномалии (например, избыточные соски), жировой некроз, мастит, фиброзно-кистозные изменения , гинекомастия, эктазия протока молочной железы и новообразования, такие как фиброаденома, опухоль филлодий и внутрипротоковая папиллома. Фиброзно-кистозные изменения приводят к наиболее частому доброкачественному поражению груди и, как и все остальные поражения, в первую очередь поражают женщин между третьим и пятым десятилетиями жизни.Хотя доброкачественные заболевания груди могут вызывать симптомы, имитирующие рак груди, большинство этих поражений не повышают риск злокачественных заболеваний. Обычно им ставят диагноз на УЗИ и маммографии, но в некоторых случаях требуется биопсия. Из-за доброкачественного характера этих состояний лечение обычно не включает хирургическое вмешательство.
Обзор
Врожденные аномалии груди
Грудной гребень регрессирует на 7 -й –8 -й неделе эмбрионального развития.Нарушения на этой стадии развития могут приводить к следующим аномалиям:
- Амастия: отсутствие тканей груди и сосков
- Полимастия: наличие добавочной ткани молочной железы
- Ателия: отсутствие сосков
- Полителия: наличие дополнительных сосков
- Синдром Поланда [3]
- Односторонняя аплазия / гипоплазия грудных мышц и груди с ассоциированными аномалиями пальцев (например, брахисиндактилия)
- Чаще всего развивается справа
Фиброзно-кистозные изменения
- Обзор Определение: доброкачественные изменения, характеризующиеся образованием фиброзной и / или кистозной ткани [4] [5]
- Эпидемиология
- Наиболее частое доброкачественное поражение груди
- Преимущественно у женщин в пременопаузе 20–50 лет
- До 50% женщин страдают от этого заболевания в течение жизни.
- Этиология: неизвестно.
Гистологические подтипы
[6]- Непролиферативные поражения
- Кисты: расширенные протоки, заполненные жидкостью (кисты с синим куполом)
- Стромальный фиброз (без злокачественного потенциала)
- Апокринная метаплазия
- Пролиферативные поражения (возникают с атипичными клетками или без них)
Клинические особенности
Диагностика
[8]- Физический осмотр
- УЗИ и маммография (первая линия)
- Ультразвук
- Результаты варьируются от нормального внешнего вида до очаговых областей толстой паренхимы.
- Систы могут присутствовать.
- Маммограмма (не рекомендуется женщинам)
- Образования округлой или овальной формы с четкими границами
- В некоторых случаях диспергированные кальцификаты
- Ультразвук
- Тонкоигольная аспирация (после того, как визуализация подтверждает кистозное поражение): показана, если у пациента есть симптомы и / или требуется процедура
- Биопсия: подтверждает диагноз, если визуализация не дает результатов.
Лечение
[9]Прогноз
Зависит от гистологического подтипа:
- Непролиферативные поражения не увеличивают риск рака.
- Пролиферативные поражения с атипичными клетками (например, гиперплазия протокового эпителия) связаны с повышенным риском рака.
Мастит
- Определение: воспаление паренхимы груди [10]
- Эпидемиология: встречается у 10% кормящих матерей (особенно через 2–4 недели после родов).
- Этиология
- Патофизиология
- Трещины сосков способствуют проникновению бактерий, находящихся в ноздре и горле младенца или на коже матери, в молочные протоки во время кормления грудью.
- Длительное нагрубание груди; (из-за перепроизводства молока) или недостаточный дренаж молока; (например, из-за нечастого кормления, быстрого отлучения от груди, болезни ребенка или матери) приводят к застою молока, что создает благоприятные условия для роста бактерий в млечных протоках.
- Клинические особенности
- Диагностика
- Клинический диагноз
- Если нет ответа на начальное лечение, может потребоваться посев грудного молока или визуализация.
- Лечение [11] [12]
Пациентам с маститом следует продолжать грудное вскармливание, чтобы снизить риск абсцесса груди.
Абсцесс груди
[13]- Определение
- Инкапсулированное скопление гноя в ткани груди
- Основное осложнение мастита
- Клинические особенности
- Лечение
Колеблющаяся масса может указывать на абсцесс груди.
Жировой некроз груди
- Определение: доброкачественное негнойное воспалительное образование, поражающее жировую ткань груди.
- Эпидемиология
- Этиология: травма; (положительный анамнез сильно варьируется) [14]
- Клинические особенности
- Диагностика [15] [16]
- Лечение: не требуется
Эктазия протока молочной железы
- Определение: хроническое субареолярное перидуктальное хроническое воспалительное состояние, определяемое расширенными протоками молочных желез, которые в конечном итоге закупориваются [17]
- Эпидемиология
- Этиология: застой сгущенного люминального секрета, ведущий к перидуктальному воспалению и фиброзной облитерации
- Клинические особенности
- Диагностика
- Маммография и / или УЗИ: могут использоваться для определения диаметра протока молочной железы [18]
- Биопсия (при наличии подозрительных или неубедительных результатов визуализации) может показать следующее:
- Лечение
- Обычно не требуется (большинство случаев разрешается спонтанно)
- Антибактериальная терапия при инфицировании
- Хирургическое удаление стойких поражений
Эктазия протока молочной железы является наиболее частой причиной зеленоватых выделений из сосков.
Доброкачественные новообразования молочной железы
Фиброаденома
- Определение: доброкачественная опухоль молочной железы с фиброзной и железистой тканью [19]
- Эпидемиология
- Этиология: неизвестна, но гормональная связь установлена; (повышенный уровень эстрогена, например, во время беременности или перед менструацией, может стимулировать рост)
- Клинические признаки: обычно четко выраженная подвижная масса
- Диагностика [20]
- Лечение: регулярные осмотры
Прогноз [21]
Опухоль Phyllodes
[22]- Определение: редкая фиброэпителиальная опухоль с гистологией, аналогичной фиброаденоме.
- Эпидемиология
- Этиология: неизвестно
- Клинические признаки
- Безболезненная, гладкая, многоузловая опухоль в груди, со средним размером 4–7 см
- Переменная скорость роста: может расти медленно в течение многих лет, быстро или иметь двухфазный характер роста
- Диагностика
- Лечение
- Прогноз
Внутрипротоковая папиллома
- Определение: одиночные или множественные доброкачественные образования, возникающие из эпителия молочных протоков молочной железы [23]
- Эпидемиология: пик заболеваемости: 40–50 лет
- Множественные поражения: ~ 41 год
- Одиночные поражения: ∼ 48 лет
- Этиология: неизвестно
- Клинические особенности [24]
- Одиночные поражения (также известные как центральная папиллома)
- Множественные поражения (также известные как периферические папилломы)
- Обычно бессимптомные, но в редких случаях могут вызывать выделения из сосков
- Периферические поражения
- Меньшие по размеру по сравнению с одиночными поражениями
- Диагностика
- Лечение: хирургическое иссечение пораженного протока.
- Прогноз
- В целом отлично; для большинства поражений нет риска злокачественной трансформации
- Поражения с атипичной гиперплазией связаны с повышенным риском рака груди.
Внутрипротоковая папиллома является наиболее частой причиной кровянистых выделений из сосков.
Дольчатая карцинома in situ (LCIS)
[26]- Характеристики
- Микрокальцификации или образование новообразования встречаются редко (обычно при случайной биопсии).
- Более низкий риск последующей инвазивной карциномы (одинаковая предрасположенность в обеих молочных железах) по сравнению с DCIS
- Локализация: мультифокальная [27]
- Патология
- Пониженная экспрессия E-кадгерина
- Дольки, заполненные мономорфными клетками
- Интактная базальная мембрана
- Модель диффузного роста
Гинекомастия
Обзор
Типы и патофизиология
1390 [ []Гинекомастия физиологическая
- Гинекомастия новорожденных [31]
- Пубертатная гинекомастия [32]
- Эпидемиология: встречается у 50% мальчиков-подростков.
- Патофизиология: вызвано пубертатным дисбалансом эстрогенов / андрогенов.
- Клинические особенности
- Небольшие, подвижные, твердые бляшки ткани груди в субареолярной области, которые развиваются в период полового созревания.
- Может быть болезненным, односторонним / двусторонним и ассоциироваться с жировым развитием вокруг соска
- Самопроизвольно проходит к 17 годам
- Менеджмент
- Старческая гинекомастия: встречается примерно у 50% мужчин старше 50 лет.
Патологическая гинекомастия
Некоторые гормоны вызывают фульминантный кливаж: спиронолактон, гормоны, циметидин, финастерид, кетоконазол вызывают гинекомастию.
Идиопатическая гинекомастия
Клинические особенности
Диагностика
[38]Дифференциальный диагноз
Лечение
[39]- Лечите первопричину.
- Наблюдение: показан при физиологической и недавно возникшей () патологической гинекомастии.
- Медикаментозное лечение: показано некоторым пациентам при косметической или болезненной гинекомастии
- Хирургическое вмешательство (подкожная мастэктомия): показано для косметического вмешательства при стойкой гинекомастии (> 1 года).
Galactocele
Обзор
Клинические особенности
- Твердая, безболезненная масса, обычно локализованная в субареолярной области
- Боль предполагает вторичную инфекцию.
Диагностика
[40]В первую очередь клинический диагноз
Дифференциальный диагноз
| Дифференциальный диагноз галактоцеле | |||
|---|---|---|---|
| Содержание | Mamoma| Mamoma | Кистозная масса с уровнем жировой жидкости |
Псевдогамартома |
ЛечениеПрогнозСсылки |
