Консультация пульмонолога
Консультация пульмонолога необходима:
– если кашель, появляется в утреннее время и сопровождается отхаркиванием вязкой мокроты. Такой тип кашля свойственен курильщикам при развитии хронической формы бронхита (его осложнения приводят к эмфиземе легких и дыхательной недостаточности).
– при сухом или влажном кашле, длящемся несколько недель,
– если одышка возникает даже при незначительных физических нагрузках или в состоянии покоя.
– при одышке, сочетающейся с затрудненным выдохом,
– если отходящая при кашле мокрота изменила цвет или в мокроте появились сгустки крови,
– при болях в грудной клетке, возникающих при дыхательных движениях,
– в случае сильной сонливости в течение дня в сочетании с сухостью (или болью) во рту и горле после пробуждения.
Чаще всего к пульмонологу взрослые пациенты обращаются для помощи в лечении заболеваний:
– хронического бронхита.
– пневмонии (воспаления легких). В большинстве случаев пневмония – это инфекционное заболевание, вызываемое каким-то микроорганизмом при снижении иммунной защиты (например, при переохлаждении). Пневмонии отличаются и по течению заболевания, и по прогнозу, и по схемам лечения. Разобраться во всех нюансах может только такой специалист, как врач-пульмонолог.
– бронхиальной астмы. Хроническое заболевание, требующее постоянного врачебного контроля и коррекции лечения.
– плеврита, который бывает сухим и экссудативным (с накоплением избыточной жидкости в плевральной полости). Причиной плеврита могут быть инфекции, опухоли и травмы грудной клетки, иногда причина остается невыясненной.
Кроме вышеперечисленных заболеваний, существует множество более редких, но не менее грозных болезней, для диагностики и лечения которых необходимо обращаться к врачу-пульмонологу. К таким заболеваниям относятся и болезни, развившиеся под воздействием профессиональных факторов:

– силикоз. Это заболевание развивается при длительном вдыхании пыли, которая содержит свободный диоксид кремния (у горнорабочих, в литейных цехах, при производстве керамических изделий и огнеупорных материалов).
– силикатоз, который развивается при длительном вдыхании пыли силикатов.
– асбестоз, развивающийся при длительном вдыхании асбестовой пыли.
– талькоз, который провоцируется вдыханием тальковой пыли.
– антракоз, возникающий при длительном вдыхании каменно-угольной пыли.
– сидероз, который провоцирует вдыхание пыли железа.
Для более точной диагностики врачу-пульмонологу часто требуются анализы и флюорография, которые также можно пройти в центре семейной медицины «Ладамед».
“О бронхиальной астме простым языком” – беседа с врачом-пульмонологом Зоновой Юлией Александровной в эфире радио “Эхо Москвы в Кирове”
ЗВОНИТЕ, ЗАПИСЫВАЙТЕСЬ НА ПРИЕМ К ВРАЧУ-ПУЛЬМОНОЛОГУ:
(8332) 52-53-53; 22-03-03.
Methodology for Sputum Induction and Laboratory Processing
within-page=”1″>ГоряеваТипичное изображение будет показано в Рисунок 1 , которая визуализируется с использованием Горяева микроскопа. Плоскоклеточный клетки легко определить, как они гораздо больше, чем не плоскоклеточный клетки. Эти клетки плоского эпителия, эпителиальные клетки приходя от устья. Оба типа клеток являются запятнана Трипановый синий, когда мертвые. Необходимо проявлять осторожность во избежание подсчета дрожжей, бактерий и металлолома.
Рисунок 1 : Горяева рисунок (A) жизнь не-плоскоклеточный, (B) мертвый плоскоклеточный клеток и (C) плоскоклеточный клеток. Шкалы бар = 50 µm. пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Cytospin слайд: на рисунке 2 показан образ представителя cytospin слайд, полученных после обработки мокроты.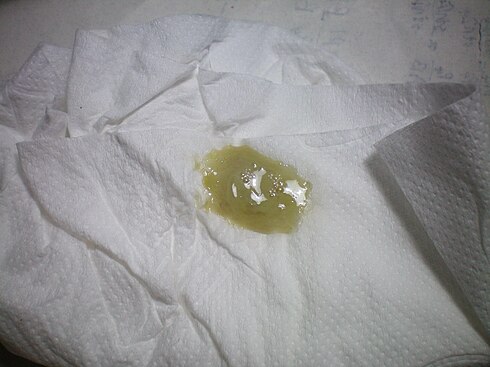 Различных типов клеток (нейтрофилов, эозинофилов, макрофагов, лимфоцитов и клеток эпителия) могут быть продифференцированы посредством их морфологии и окраской. В некоторых случаях загрязнение плоскоклеточный клетки могут быть важными и, если процент плоскоклеточный клеток больше, чем 80%, образец считается неудачным (
Различных типов клеток (нейтрофилов, эозинофилов, макрофагов, лимфоцитов и клеток эпителия) могут быть продифференцированы посредством их морфологии и окраской. В некоторых случаях загрязнение плоскоклеточный клетки могут быть важными и, если процент плоскоклеточный клеток больше, чем 80%, образец считается неудачным (
Рисунок 2 : Cytospin слайд рисунок (A) нейтрофилов, (B) макрофагов, (C) eosinophil, (D) лимфоцитов и (E) эпителиальных клеток. Шкалы бар = 20 мкм. пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Рисунок 3 : Пример cytospin слайд низкого качества с > 80% плоскоклеточный клеток. Шкалы бар = 20 мкм. пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
В нашем отделе успешность процедуры (сочетания успешных индукции и читается cytospin), основанные на выборке из 1129 больных (здоровых испытуемых, астматики или ХОБЛ), 82% (924/1129). В суб-анализ в зависимости от типа пациентов успех ставка составляет 75% (57/76) в здоровых испытуемых, 82% (827/1004) астматиков и 82% (40/49) у больных ХОБЛ.
Результаты в здоровых испытуемых
Ретроспективный анализ ряда 289 здоровых испытуемых из нашего отдела, медиана (межквартильный диапазон) мокроты вес был 3.72 g (межквартильный диапазон 2.46 g – 5.54 g) и средний всего не-плоскоклеточный фото/g мокроты был 0.59 x6 (10) межквартильный диапазон 0,37 x 106 – 1,29 х 106).
В этих здоровых испытуемых низка доля плоскоклеточный клеток на 19% (10% – 34) и жизнеспособность на 66% (54-78%). Что касается доли различных типов клеток результаты резюмируются в рисунке 4A. Мы можем наблюдать, что процент макрофагов (49% [31-68%]) является выше, чем процент нейтрофилов (34% [14% – 60%]), а процент лимфоцитов (2% [1-3]), эозинофилов (0% [0% – 0%]) и эпителиальных клеток (4% [2-11%]) является низким. Эти результаты схожи, когда данные выражены в абсолютных величинах (
Мы можем наблюдать, что процент макрофагов (49% [31-68%]) является выше, чем процент нейтрофилов (34% [14% – 60%]), а процент лимфоцитов (2% [1-3]), эозинофилов (0% [0% – 0%]) и эпителиальных клеток (4% [2-11%]) является низким. Эти результаты схожи, когда данные выражены в абсолютных величинах (
Рисунок 4 : Представитель результаты подсчета дифференциальной клеток наблюдается в здоровых испытуемых выражены в процентах (A) или (B) абсолютные значения. Результаты представлены как медиана (межквартильный диапазон). Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Важно также учитывать возраст больных. Действительно сильная корреляция между возраст пациента и доля нейтрофилов в присутствует мокроты (рис. 5). Аналогичным образом при классификации больных по 10 лет возрастных групп ( рис. 6), мы наблюдали значительное увеличение числа нейтрофилов с увеличением возраста. Таким образом эта переменная должна рассматриваться при сравнении результатов от различных когорт, и осторожность должны быть приняты в соответствующих субъектов.
6), мы наблюдали значительное увеличение числа нейтрофилов с увеличением возраста. Таким образом эта переменная должна рассматриваться при сравнении результатов от различных когорт, и осторожность должны быть приняты в соответствующих субъектов.
Рисунок 5: Корреляция между возрастом и мокроты нейтрофилов процент. Была рассчитана корреляции Спирмена тест. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Рисунок 6: Эволюция нейтрофилов процент согласно возрастная категория. P значение ANOVA был < 0.0001 для сравнения нейтрофилов процент между возрастных классов. Множественные сравнения были сделаны с Данн множественные сравнения теста. P значения представлены следующим образом: * p < 0,05, ** p < 0.01, и *** p < 0,001. Результаты представлены как медиана (межквартильный диапазон). Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Результаты у пациентов, страдающих от заболеваний органов дыхания
Метод индуцированной мокроты обычно используется для оценки профиля воспалительных клеток у больных астмой.Этот метод может применяться также для пациентов, страдающих от ХОБЛ, другой воспалительных заболеваний дыхательных путей. При сравнении здоровых испытуемых, астматиков и больных ХОБЛ (3 группы, сопоставляемой по возрасту, полу и табака привычки), мы наблюдали, что профиль воспалительных клеток отличается между этими когорты (рис. 7). Действительно астматических больных обычно характеризуются поднял мокроте эозинофилов, в то время как доля мокроты нейтрофилы обычно выше у больных ХОБЛ, по сравнению с здорового управления, который связан с тяжести заболевания.
Рисунок 7 : Мокроты воспалительных клеток профиль здоровых испытуемых (n = 45), астматическим пациентов (n = 108) и больных ХОБЛ (n = 54). Три группы были сопоставимы по полу, возрасту и табака привычки. P значения ANOVA были < 0,05, < 0,0001, и < 0.0001 для сравнения нейтрофилов, эозинофилов и макрофагов между группами, соответственно. Множественные сравнения были сделаны с Данн множественные сравнения теста. P значения представлены следующим образом: * p < 0,05 и *** p < 0,001. Результаты представлены как медиана (межквартильный диапазон). Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Три группы были сопоставимы по полу, возрасту и табака привычки. P значения ANOVA были < 0,05, < 0,0001, и < 0.0001 для сравнения нейтрофилов, эозинофилов и макрофагов между группами, соответственно. Множественные сравнения были сделаны с Данн множественные сравнения теста. P значения представлены следующим образом: * p < 0,05 и *** p < 0,001. Результаты представлены как медиана (межквартильный диапазон). Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Депздрав рассказал, как отличить грипп от ОРВИ
Осень – традиционное время сезонного всплеска острых респираторных вирусных заболеваний (ОРВИ) и гриппа. Главный специалист по первичной медицинской помощи взрослому населению ДЗМ Андрей Тяжельников назвал отличительные признаки этих заболеваний.
Некоторые люди путаются в определениях гриппа и ОРВИ, однако это не совсем верно. ОРВИ – общее название любой респираторной вирусной инфекции, а грипп только один из этих представителей.
Грипп и ОРВИ являются самыми распространенными в мире инфекционными заболеваниями. Но если большинство ОРВИ протекают относительно легко, то грипп может приводить к крайне опасным осложнениям.
«Заболевание гриппом начинается резко, быстро, в течение нескольких часов после заражения. У человека появляется сильная слабость, озноб, повышение температуры. Всего за один час лихорадка может подняться до 40°С.», – рассказал Андрей Тяжельников.
Температура при гриппе держится в течение нескольких суток, трудно сбивается. У заболевшего наблюдаются ломота в теле, головные боли. На второй день появляется сухой кашель, который переходит во влажный с выделением мокроты.
При ОРВИ температура тела обычно не повышается до 39°С и держится пару дней, затем постепенно нормализируется. Наблюдается общая слабость, но не сопровождающаяся сильными болевыми ощущениями в мышцах и суставах, как при гриппе.
«Еще один отличием является продолжительность течения болезни. ОРВИ не длится больше недели, после выздоровления человек чувствует себя хорошо, то грипп проходит за 7-10 дней и недомогания остаются еще до трех недель после выздоровления», – добавил специалист.
Ученые давно доказали, что самым эффективным способом защиты от гриппа является своевременная вакцинация. Защитный эффект наступает через 2 недели после прививки, а полученный иммунитет сохраняется в течение года.
В Москве уже не первый год проводится массовая вакцинация против гриппа. Сделать бесплатную прививку можно как во всех поликлиниках, так и в мобильных пунктах рядом со станциями метро, МЦК, ж/д станцией Крюково, в некоторых павильонах «Здоровая Москва», в двух флагманских центрах госуслуг «Мои документы».
Привиться в мобильных пунктах могут все совершеннолетние граждане России. С собой нужно взять только паспорт. Перед вакцинацией каждого обязательно осматривает врач-терапевт или инфекционист. После прививки выдают сертификат. Вся процедура занимает 10–15 минут. Детям до 18 лет сделать прививку можно только в детских поликлиниках, детских садах и школах.
Бактериальный посев мокроты – понимание теста и результатов
Мокрота – это густая слизь или мокрота, которая выделяется из нижних дыхательных путей (бронхов и легких) при кашле; это не слюна или слюна. В процессе сбора пробы необходимо соблюдать осторожность, чтобы гарантировать, что проба поступает из нижних дыхательных путей, а не из верхних дыхательных путей. Образцы мокроты могут отхаркивать или индуцировать (См. Раздел ниже, посвященный отбору образцов.)
В процессе сбора пробы необходимо соблюдать осторожность, чтобы гарантировать, что проба поступает из нижних дыхательных путей, а не из верхних дыхательных путей. Образцы мокроты могут отхаркивать или индуцировать (См. Раздел ниже, посвященный отбору образцов.)
Посев бактериальной мокроты выявляет присутствие болезнетворных бактерий (патогенов) у людей, у которых есть подозрение на бактериальную пневмонию или другие инфекции нижних дыхательных путей.Бактерии в образце идентифицируются, и проводится тестирование чувствительности для определения курса лечения антибиотиками.
Иногда респираторная инфекция вызывается патогеном, который невозможно вырастить и идентифицировать с помощью обычного бактериального посева мокроты. Другие тесты, такие как мазок и посев КУБ, посев на грибок или вирусный посев, можно заказать в дополнение к обычному посеву или вместо него.
Обычно первым этапом рутинного анализа образца мокроты является окрашивание по Граму для определения общего типа бактерий, которые могут присутствовать. Затем образец помещается на подходящую питательную среду или в нее и инкубируется. Среда стимулирует рост присутствующих бактерий, что позволяет проводить дальнейшие исследования и идентификацию.
Затем образец помещается на подходящую питательную среду или в нее и инкубируется. Среда стимулирует рост присутствующих бактерий, что позволяет проводить дальнейшие исследования и идентификацию.
Мокрота нестерильная. Это означает, что когда у человека есть бактериальная респираторная инфекция, обычно присутствуют безвредные бактерии, которые обычно присутствуют во рту, горле и т. Д. (Нормальная флора), а также присутствуют болезнетворные (патогенные) бактерии.
Квалифицированный лаборант дифференцирует нормальную флору от патогенных бактерий и определяет различные типы бактерий, присутствующих в культуре.Идентификация – это пошаговый процесс, который может включать несколько биохимических, иммунологических и / или молекулярных тестов и наблюдение за характеристиками роста организма.
Тест на чувствительность к противомикробным препаратам часто требуется для определения курса лечения и определения того, могут ли присутствующие бактерии реагировать на определенные антибиотики.
Посев мокроты, окрашивание по Граму и тестирование на чувствительность – все это вносит свой вклад в отчет, который информирует практикующего врача о том, какие патогены присутствуют и какие антибиотики могут ингибировать их рост.
Образцы мокроты могут кашлять или индуцироваться. Прокашлявшиеся образцы помещают в стерильную чашку, предоставленную лабораторией. Обычно требуется глубокий кашель, и человека следует проинформировать о том, что необходима мокрота / слизь из легких, а не слюна. Если кто-то не может получить образец мокроты, то это часто можно вызвать, следуя предоставленным инструкциям и вдыхая стерильный физиологический раствор или аэрозоль глицерина в течение нескольких минут для разжижения мокроты в легких. Вдыхание пара или горячий душ также могут быть полезны для разжижения мокроты.Иногда сбору мокроты может помочь специалист по респираторной терапии.
Все собранные образцы должны быть незамедлительно доставлены в лабораторию для обработки, пока они еще свежие. Перед обработкой образцы мокроты должны быть проанализированы и приняты лабораторией.
Перед обработкой образцы мокроты должны быть проанализированы и приняты лабораторией.
Полезные результаты посева мокроты во многом зависят от хорошего сбора образцов. Если исследование образца, окрашенного по Граму, показывает, что он содержит значительное количество нормальных клеток, выстилающих ротовую полость (клетки плоского эпителия), то образец обычно не считается подходящим для культивирования, и может потребоваться повторный сбор образца. .Если образец содержит большинство лейкоцитов, которые указывают на реакцию организма на инфекцию, то он считается подходящим образцом для культивирования.
Вас могут попросить почистить зубы и прополоскать рот водой перед взятием пробы. Вам также могут посоветовать избегать еды как минимум за 1-2 часа до взятия пробы, что обычно является первым делом с утра.
Цвет мокроты и бактерии при обострениях хронического бронхита: объединенный анализ
Реферат
Мы исследовали корреляцию между цветом мокроты и наличием потенциально патогенных бактерий при обострении хронического бронхита (AECB).
Были объединены данные шести многоцентровых исследований, сравнивающих моксифлоксацин с другими противомикробными препаратами у пациентов с ОКБ. Перед антимикробной терапией собирали мокроту, и бактерии определяли посевом и окрашиванием по Граму. Связь между цветом мокроты и бактериями определяли с помощью логистической регрессии.
Из 4089 образцов мокроты цвет был зарегистрирован в 4003; 1898 (46,4%) были положительными по культуре. В образцах мокроты зеленого или желтого цвета чаще всего обнаруживаются бактерии (58.9% и 45,5% образцов соответственно), по сравнению с 18% прозрачных и 39% образцов ржавого цвета, положительных на потенциально патогенные микроорганизмы. Факторами, предсказывающими положительный посев, были цвет мокроты (самый сильный предиктор), гнойность мокроты, усиление одышки, мужской пол и отсутствие лихорадки. Зеленый или желтый цвет по сравнению с белым цветом мокроты был связан с чувствительностью 94,7% и специфичностью 15% для наличия бактерий.
Цвет мокроты, особенно зеленый и желтый, был более сильным предиктором потенциально патогенных бактерий, чем гнойность мокроты и усиление одышки у пациентов с ОВХБ.Однако это не обязательно предсказывает необходимость лечения антибиотиками у всех пациентов с ОКБ.
Одно из самых сложных решений, с которыми ежедневно приходится сталкиваться в клинической практике первичной медико-санитарной помощи, – назначать или не назначать противомикробные препараты пациентам с обострением хронического бронхиального заболевания (, т.е. хронический бронхит, бронхоэктазия или хроническая обструктивная болезнь легких (ХОБЛ)). Такие решения принимаются эмпирически на основании клинических данных. Чрезмерное использование противомикробных препаратов в обществе явно связано с повышенным риском развития бактериальной устойчивости [1].Диагностический инструмент, который можно использовать на месте оказания медицинской помощи для выявления пациентов, которым можно безопасно лечить без противомикробных препаратов, может снизить количество случаев неправильного назначения.
Антонисен и др. . [2] сообщили, что пациенты, поступившие как минимум с двумя из них: повышенная одышка, выделение мокроты и гнойность мокроты, с большей вероятностью выздоровели при назначении противомикробного препарата по сравнению с пациентами с одним из симптомов. Однако в их исследование были включены пациенты с тяжелой и очень тяжелой ХОБЛ, и эти критерии никогда не проверялись на пациентах с необструктивным хроническим бронхитом.Совсем недавно Stockley et al. [3] заметил, что только гнойная мокрота по сравнению со слизистой мокротой в значительной степени связана с присутствием бактерий во время обострения. Изменение цвета мокроты на более темный во время обострения обнаруживается клинически и может соответствовать увеличению рекрутирования нейтрофилов, что указывает на новый или значительный бактериальный стимул. Это потемнение мокроты указывает на присутствие миелопероксидазы, фермента зеленого цвета из гранул азурофилов нейтрофилов [3].
Для получения дополнительных доказательств того, что более темный цвет мокроты указывает на присутствие бактерий во время обострений хронического бронхита (AECB), были собраны данные рандомизированного клинического исследования моксифлоксацина для лечения этого состояния. Их использовали в объединенном анализе для определения корреляции между цветом мокроты и присутствием потенциально патогенных микроорганизмов (PPM) в мокроте пациентов с AECB. Все исследования имели одинаковые критерии включения и исключения и использовали один и тот же вопросник для регистрации цвета и внешнего вида мокроты.Поскольку предыдущие исследования цвета мокроты как диагностического маркера были одноцентровыми исследованиями [3–5], эти данные из многих различных центров в Европе и Северной Америке могут дать новое понимание полезности цвета мокроты в качестве помощи при принятии решений о лечении в клинических условиях. практика у пациентов с ОВХБ разной степени тяжести.
МЕТОДЫ
Дизайн исследования
Исходные данные были объединены из шести клинических испытаний с использованием аналогичных методологий, сравнивающих моксифлоксацин с другими противомикробными препаратами у пациентов с ОКБ (таблица 1), чтобы определить взаимосвязь между инфекцией и цветом мокроты [6–10].Все клинические испытания были проспективными, рандомизированными, контролируемыми многоцентровыми исследованиями, проведенными в Европе и Северной Америке.
Таблица 1 Дизайн шести исследований, включенных в анализ мокротыПациенты
Пациенты мужского и женского пола в возрасте> 18 лет с хроническим бронхитом с клиническими симптомами обострения имели право присоединиться к исследованиям. Критерии включения включали обострения по Антонисену I типа (все исследования) или обострения по Антонисену II типа (одно исследование).Обострение типа I определялось как наличие повышенной одышки, выделения мокроты и гнойной мокроты [2]. Для постановки диагноза обострения Антонисена типа II требовалось наличие двух из этих симптомов. Хронический бронхит определялся как ежедневное выделение мокроты в течение большей части дней в течение не менее трех месяцев подряд на протяжении более двух лет подряд [11]. Лихорадку оценивали при включении во все исследования. Критерии исключения: значительная почечная или печеночная недостаточность; тяжелая инфекция дыхательных путей, требующая парентеральной антимикробной терапии или искусственной вентиляции легких; диагноз пневмонии; нерешенное злокачественное новообразование грудной клетки; туберкулез; кистозный фиброз; бронхоэктазы; в анамнезе тяжелая сердечная недостаточность; беременность или период лактации; радиологические доказательства бронхолегочных инфильтратов или необходимость сопутствующей системной противомикробной терапии с агентами, не указанными в протоколах исследования; аллергия на фторхинолоны, производные карбоксихинолона или противомикробные препараты сравнения; удлинение интервала QTc или прием лекарств для увеличения интервала QTc; тендинопатия, связанная с фторхинолонами; любое заболевание, которое может привести к смерти в течение 6 месяцев; получение системной противомикробной терапии> 24 ч в течение 7 дней с момента включения в исследование; или получение любого исследуемого препарата в течение 30 дней с момента регистрации.
Все исследования были проведены в соответствии с Хельсинкской декларацией и получили соответствующее одобрение местных комитетов по этике и регулирующих органов. Перед началом исследования каждый пациент предоставил письменное информированное согласие. Во всех исследованиях были получены индивидуальные данные пациентов.
Микробиологическая оценка
В каждом исследовании перед началом противомикробной терапии (исходный уровень) собирали мокроту. Все центры и исследователи использовали одну и ту же анкету для регистрации характеристик мокроты, включая цвет мокроты.Все образцы достаточного качества были проанализированы посевом и окраской по Граму в местной лаборатории каждого исследователя. Были включены только образцы с <10 плоскоклеточными клетками на поле низкого увеличения и> 25 полиморфноядерными лейкоцитами на поле низкого увеличения, идентифицированными с помощью окрашивания по Граму. Наличие PPM ( Haemophilus influenzae , Haemophilus parainfluenzae , Staphylococcus aureus , Streptococcus pneumoniae , Klebsiella pneumoniae , Pseudomonas aeruginosa , cat Pseudomonas aeruginosa , cat Morahalxella и др.) определяли посевом.
Статистический анализ
Все параметры, связанные с воздействием и лечением AECB, были проанализированы с использованием описательной статистики. Чтобы определить полезность использования зеленого или желтого цвета мокроты в качестве диагностического теста на наличие PPM, для каждого из шести клинических испытаний были рассчитаны следующие статистические данные диагностических тестов, включая 95% доверительные интервалы: чувствительность, специфичность, положительная прогностическая ценность. , отрицательная прогностическая ценность, положительное отношение правдоподобия и отрицательное отношение правдоподобия.Объединенные оценки были рассчитаны для чувствительности и специфичности с использованием двумерного метода [12]. В соответствии с рекомендациями Кокрановского сотрудничества [13] объединенные оценки не рассчитывались для положительных и отрицательных прогностических значений, поскольку они зависят от основной распространенности, которая несколько варьировалась в шести испытаниях. Кроме того, никакие объединенные оценки для положительных и отрицательных отношений правдоподобия не рассчитывались, как рекомендовано Zwinderman и Bossuyt [14].
Модель логистической регрессии использовалась для проверки того, является ли цвет мокроты статистически значимым предиктором присутствия микроорганизма.Сначала была выполнена пошаговая логистическая регрессия с использованием следующих возможных объясняющих переменных: пол, возрастная группа (<65 против ≥65 лет), долгосрочное использование ингаляционных бронходилататоров и / или кортикостероидов, географический регион, исследование, аспект мокроты ( гнойный, слизисто-гнойный или слизистый), количество предыдущих обострений, увеличение одышки, уровень С-реактивного белка (СРБ) до лечения и количество лейкоцитов, наличие лихорадки и длительность обострения до исследования. В этой пошаговой процедуре каждая переменная добавлялась к существующей модели по одной.Если значение p для новой переменной было <0,05 (что означает, что это, вероятно, был значимым предиктором присутствия микроорганизмов, даже с учетом других переменных, уже присутствующих в модели), оно добавлялось в модель. Если была добавлена новая переменная, общая модель запускалась снова; если какая-либо переменная в новой модели имела значение p> 0,05, то она исключалась из модели. Этот шаг был выполнен для каждой из потенциальных переменных. После завершения пошаговой процедуры была запущена окончательная модель с использованием только переменных, определенных пошаговой процедурой.p-значения, точечные оценки и 95% доверительные интервалы для отношений шансов были предоставлены для каждой переменной в окончательной модели. Основная цель модели логистической регрессии состояла в том, чтобы показать, что цвет мокроты является важным предиктором присутствия PPM, даже при корректировке других важных переменных-предикторов в модели. Модель со случайными эффектами исследования была адаптирована в качестве анализа чувствительности для подтверждения результатов модели с фиксированными эффектами исследования.
РЕЗУЛЬТАТЫ
Характеристики пациента
В общей сложности 4089 пациентов сдали образец мокроты.Пациенты в основном были мужчинами (55,0%), белыми (78,6%) и в возрасте> 45 лет (74,8%) (таблица 2). В целом у 44,5% пациентов за предыдущий год было три и более обострения. Хотя характеристики населения в целом и пациентов с положительными или отрицательными культурами были в целом схожими, одно заметное различие заключалось в том, что пациенты с положительными культурами с большей вероятностью были бывшими или нынешними курильщиками, чем пациенты с отрицательными культурами (85,8% против 75,4%, соответственно; p <0.001).
Таблица 2- Демографические данные пациентов, включенных в анализ мокротыХарактеристики и микробиология мокроты
Из 4089 образцов мокроты цвет был зарегистрирован в 4003 (97,9%) и 1898 (46,4%) были положительными на исходном уровне. У большинства пациентов была желтая (56,7%) или зеленая (29,8%) мокрота; Еще у 466 пациентов была мокрота белого (8,6%) или ржавого (2,8%) цвета (таблица 3). После культивирования из 1898 образцов было обнаружено 2331 PPM.
Таблица 3– Обычно изолированные потенциально патогенные микроорганизмы: общее количество и соотношение по цвету мокротыИнфекционные организмы чаще всего выделялись из зеленой или желтой мокроты, 58.9% и 45,5% этих проб, соответственно, были бактериологически положительными (рис. 1). Пациенты с прозрачной или белой мокротой реже имели PPM (18,4%).
Рисунок 1-Процент образцов мокроты с выявленным патогеном по цвету мокроты. Данные в столбцах представлены как n / N.
H. influenzae был наиболее часто выделяемым организмом в мокроте всех цветов (таблица 3). Зеленый или желтый цвет был наиболее часто встречающимся цветом мокроты, где присутствовали PPM, за ним следовали ржавчина или белый цвет.Цветовые узоры были одинаковыми для всех видов изолированных PPM; следовательно, конкретный цвет не может быть ассоциирован с данным микроорганизмом (рис. 2).
Фигура 2-Распределение цвета мокроты по видам-возбудителям. a) Haemophilus influenzae , b) Streptococcus pneumoniae , c) Moraxella catarrhalis , d) Haemophilus parainfluenzae , e) Staphylococcus aureus , f) Klebsiella pneumoniae , ) Haemophilus spp.
Наличие зеленой или желтой мокроты по сравнению с белой мокроты имело чувствительность к наличию PPM от 91,1% до 96,8% в исследованиях, с объединенной оценкой 94,7% и специфичностью от 4,7% до 24,4%, с объединенная оценка 15,0%. Прогнозирующая ценность положительного результата варьировала от 41,6% до 56,6%, а прогностическая ценность отрицательного результата – от 65,2% до 87,9% в разных испытаниях. Все положительные отношения правдоподобия в испытаниях были> 1, а отрицательные отношения правдоподобия были <1 (таблица 4).
Таблица 4– Параметры эффективности цвета мокроты при диагностике наличия потенциального патогенного микроорганизма путем исследованияРегрессионный анализ: прогнозирование бактериальной инфекции на основании характеристик пациента и мокроты
В логистическом регрессионном анализе факторами, предсказывающими присутствие инфекционного организма, были цвет мокроты, гнойность мокроты, усиление одышки, мужской пол и отсутствие лихорадки (таблица 5). Было обнаружено, что цвет мокроты является более сильным предиктором наличия PPM, чем другие факторы (таблица 5), хотя все факторы были значимыми.Анализ хи-квадрат нулевой гипотезы («отсутствие связи между цветом мокроты и присутствием PPM») дал значение p <0,001 (хи-квадрат 108, три степени свободы), что указывает на сильную связь между цветом мокроты и наличие бактерий. Наличие бактерий также строго прогнозировалось по гнойной мокроте (p <0,001, хи-квадрат 27, четыре степени свободы). Модель со случайными эффектами исследования подтвердила, что цвет мокроты является самым сильным предиктором наличия PPM.
Таблица 5– Регрессионный анализ значимых факторов, прогнозирующих наличие потенциально патогенных микроорганизмов в мокротеОБСУЖДЕНИЕ
Настоящее исследование показало, что цвет мокроты является лучшим маркером наличия PPM в мокроте во время AECB по сравнению с аспектом мокроты, одышкой или лихорадкой. PPM был выделен в 46,4% образцов от пациентов с обострением типа I или II, при этом почти 60% положительных образцов были получены из зеленой мокроты и только 18.4% из белой мокроты. В соответствии с другими исследованиями [15], H. influenzae был PPM, наиболее часто выделяемым в нашей большой серии, и мы не обнаружили специфического цветового рисунка для различных PPM, присутствующих в образцах мокроты.
Критерии Антонисена (, т. Е. усиление одышки, выделения мокроты и гнойности мокроты) считаются наиболее надежными предикторами бактериальной инфекции как причины обострения, требующего противомикробного лечения, в течение> 20 лет [2].Однако эти критерии были описаны для ХОБЛ: у всех пациентов объем форсированного выдоха за 1 с (ОФВ 1 ) <80% от прогнозируемого; Фактически, в исследовании Anthonisen et al. средний ОФВ 1 составлял только 33%. [2], который представляет популяцию с тяжелой и очень тяжелой ХОБЛ. Эти критерии никогда не применялись при простом, необструктивном хроническом бронхите. Более того, наиболее важным достижением в нашей способности прогнозировать участие бактерий в обострениях хронического бронхиального заболевания стало наблюдение, что не все три критерия имеют одинаковую прогностическую ценность.Стокли и др. . [3] с помощью цветовой диаграммы продемонстрировали, что изменение цвета мокроты во время обострения является чувствительным и специфическим маркером бактериального присутствия, а также позволяет прогнозировать высокую бактериальную нагрузку в бронхиальном секрете. Эти результаты были повторены другими группами [4, 5] и были подтверждены с использованием более специфичных и чувствительных методов отбора проб, таких как метод защищенной кисти для образцов у госпитализированных пациентов. Этот метод продемонстрировал, что изменение гнойности мокроты, описанное пациентом, имело чувствительность 89.5% и специфичность 76,2% для наличия PPM во время эпизода обострения [16].
Наши результаты согласуются с предыдущими наблюдениями, демонстрируя связь между более темным цветом мокроты и более высокой частотой выделения PPM. Мы расширили общее количество наблюдений, включив очень большую выборку пациентов из многих центров в Европе и Северной Америке, включая не только людей с ХОБЛ, но и пациентов с необструктивным хроническим бронхитом. Результаты показывают, что желтый и особенно зеленый цвет мокроты является хорошим маркером наличия PPM по всему спектру хронических бронхиальных заболеваний, включая острый кашель [17], стабильную ХОБЛ [18] и бронхоэктазы [19].
Одним из ограничений настоящего исследования является то, что, в отличие от предыдущих исследований [3–5], не использовалась стандартизованная цветовая диаграмма. Однако согласованность результатов в этой большой международной выборке позволяет предположить, что цвет мокроты легко распознается врачами и даже пациентами. В исследовании Soler et al . [16], образцы мокроты исследователи не видели; их цвет описывался исключительно самими пациентами и обеспечивал хорошую диагностическую точность на наличие PPM.
Также собиралась информация о гнойной мокроте. Гнойность сильно зависит от цвета, но еще более субъективна. В проспективных исследованиях слизистая мокрота обычно описывается как бесцветная или белая, а гнойная мокрота – от бледно-желтой до темно-зеленой [20]. Мы обнаружили значительную и последовательную взаимосвязь между гнойностью и наличием PPM в мокроте, хотя она имела меньшую прогностическую ценность, чем цвет образца.
Вторым ограничением настоящего исследования является то, что в исследование были включены только пациенты с обострениями типа I и II, поскольку в эту популяцию входили кандидаты на участие в испытании противомикробных препаратов в AECB.Нам удалось продемонстрировать взаимосвязь между цветом мокроты и наличием PPM, изучая только пациентов с высокой вероятностью бактериального обострения. Вероятно, что расширение исследования на пациентов с обострениями типа III, даже с той же тяжестью основного заболевания [21], покажет еще более сильную связь между цветом мокроты и бактериальной инфекцией. Это отражено в низкой специфичности, наблюдаемой в нашем исследовании (15%). Вероятно, это связано с очень низким количеством пациентов с белой мокротой в нашей выборке, потому что только в одно из испытаний были включены пациенты с обострением типа II ( i.е. пациентов, у которых потенциально могла быть белая мокрота). Наши результаты показывают большее сходство с результатами, полученными Дэниелсом и др. . [22], которые сообщили о чувствительности и специфичности 70% и 39% соответственно для сообщаемого цвета мокроты, но, в отличие от нашего исследования, до одной трети их пациентов имели слизистую мокроту. Важным следствием наших результатов является то, что белая мокрота является хорошим предиктором отрицательного посева мокроты и может помочь предотвратить использование антибиотиков у тех пациентов, которые вряд ли принесут пользу.
Результаты, полученные в выбранной нами популяции пациентов, удовлетворяющих критериям включения в клинические испытания, нельзя экстраполировать на более гетерогенную популяцию пациентов с хроническим бронхитом, получающих первичную медико-санитарную помощь. Однако наши результаты согласуются с результатами других исследований, проведенных у пациентов в обычной клинической практике, с различной степенью тяжести [3–5, 16, 18].
Информация о вирусной инфекции не собиралась. Вирусы могут быть изолированы до 45% обострений тяжелой ХОБЛ отдельно или вместе с бактериями [23].Вирусные обострения ХОБЛ чаще всего сопровождаются лихорадкой [24]. Наличие лихорадки неизменно ассоциировалось с более низкой вероятностью выделения бактерий у наших пациентов, что снова указывает на то, что обострения лихорадки с большей вероятностью связаны с вирусами. В другом исследовании лихорадочные обострения ХОБЛ не были достоверно связаны с гнойной мокротой по сравнению с обострениями без лихорадки [25].
Уровень CRP в плазме не позволяет прогнозировать присутствие PPM в мокроте.Предыдущее исследование показало, что тестирование на СРБ при инфекциях нижних дыхательных путей в учреждениях первичной медико-санитарной помощи значительно сокращает количество назначений противомикробных препаратов без ущерба для выздоровления пациента [26]. Однако пациенты имели легкое заболевание и средний возраст 50 лет, и только 7% имели диагноз ХОБЛ. У лиц с более тяжелым заболеванием Gompertz et al . [20] и Стокли и др. . [3] сообщили о значительно более высоких концентрациях CRP у пациентов с гнойными обострениями по сравнению с мукоидными обострениями; пациенты с положительным посевом мокроты в настоящем исследовании также имели более высокие (хотя и не значительно более высокие) концентрации CRP.Возможно, включение пациентов с обострениями III типа сделало бы это различие более очевидным. В многофакторном анализе СРБ не позволял предсказать присутствие PPM в мокроте; в систематическом обзоре тестирование на CRP неизменно не было ни достаточно чувствительным, чтобы исключить, ни достаточно специфичным, чтобы исключить инфильтрат на рентгенограмме грудной клетки и бактериальной этиологии инфекции нижних дыхательных путей [27]. В области биомаркеров измерение уровня прокальцитонина является многообещающим средством выявления пациентов с обострениями ХОБЛ, которым требуется лечение противомикробными препаратами [28].
Четвертым ограничением нашего исследования было использование посева мокроты в качестве маркера бактериального участия в этиологии обострения. Хорошо известно, что отрицательный посев мокроты не исключает бактериальной инфекции [29]. Фактически, исследования с использованием инвазивных методов у более тяжелых госпитализированных пациентов, таких как метод защищенной кисти для образцов, продемонстрировали высокую распространенность бактерий у пациентов с окрашенной мокротой [16], что более надежно, чем процент положительных культур.Что еще более важно, эти исследования продемонстрировали высокую точность использования слизистой мокроты для исключения бактериальной инфекции [3, 16]. Ясно, что использование инвазивных диагностических методов в рутинной клинической практике нецелесообразно, а отбор мокроты по-прежнему незаменим в диагностическом подходе к инфекциям нижних дыхательных путей в обществе. Однако следует отметить, что присутствие PPM в мокроте не подтверждает его роль в качестве причины обострения и не обязательно означает, что антибактериальная терапия будет полезна для разрешения обострения.
Заключение
Этот объединенный анализ результатов клинических испытаний AECB показал, что цвет мокроты является более сильным предиктором наличия PPM, чем другие факторы, включая гнойность мокроты и усиление одышки. Наибольшая связь между цветом мокроты и наличием бактерий была обнаружена с более темной (зеленой и желтой) мокротой. Изменение цвета мокроты в ходе обострения может быть использовано в планах самоконтроля [30, 31], что приведет к ранней антимикробной терапии, которая может сократить продолжительность обострения и улучшить результаты [32, 33].Кроме того, отказ от использования противомикробных препаратов для лечения обострений, когда мокрота имеет белый цвет, уменьшит количество случаев неправильного назначения антибиотиков в обществе и поможет замедлить развитие резистентности бактерий [1].
Сноски
Заявление о поддержке
Это исследование финансировалось Bayer Schering Pharma. Коммуникационная консалтинговая компания Highfield, финансируемая Bayer Shering Pharma, оказала редакционную помощь в подготовке этой рукописи.
Заявление о заинтересованности
Заявление о заинтересованности всех авторов и самого исследования можно найти на сайте www.erj.ersjournals.com/site/misc/statements.xhtml
- Получено 8 марта, 2011.
- Принято 3 октября 2011 г.
Посев мокроты | Cigna
Обзор теста
Мокрота – это густая жидкость, вырабатываемая в легких и в дыхательных путях, ведущих к легким.Посев мокроты – это тест для обнаружения микробов (таких как бактерии или грибок), который может вызвать инфекцию. Образец мокроты добавляется к веществу, способствующему росту микробов. Если микробы не растут, посев отрицательный. Если микробы, которые могут вызвать инфекцию, разрастаются, посев положительный. Тип микроба можно определить с помощью микроскопа или химических тестов. Иногда проводятся другие анализы, чтобы подобрать правильное лекарство от инфекции. Это называется проверкой чувствительности.
Вас могут попросить кашлять, чтобы сдать образец мокроты. Некоторые люди не могут кашлять достаточно глубоко, чтобы произвести анализ. Они могут вдыхать специальный туман, который помогает им откашляться.
Зачем это делается
Посев мокроты делается на:
- Найдите бактерии или грибки, вызывающие инфекцию легких или дыхательных путей, ведущих к легким.Примеры включают пневмония и туберкулез. Симптомы легочной инфекции могут включать затрудненное дыхание, боль при дыхании или кашель с кровянистым или зеленовато-коричневым оттенком. мокрота.
- Найди лучшее антибиотик для лечения инфекции. (Это называется проверкой чувствительности.)
- Посмотрите, работает ли лечение.
Как подготовить
Не используйте жидкость для полоскания рта до сбора образца мокроты. Некоторые виды жидкостей для полоскания рта убивают бактерии и могут повлиять на ваши результаты.
Если Бронхоскопия будет использована для сбора образца мокроты, ваш врач скажет вам, как скоро до обследования прекратить есть и пить. Точно следуйте инструкциям о том, когда прекратить есть и пить.Если вы этого не сделаете, ваша операция может быть отменена. Если врач сказал вам принимать лекарства в день операции, запивайте их только глотком воды.
Сообщите своему врачу, если вы недавно принимали антибиотики.
Как это делается
В большинстве случаев образец мокроты собирают рано утром, прежде чем вы что-нибудь съедите или выпьете. В некоторых случаях могут потребоваться три или более утренних пробы.(Это часто делают, если у вас туберкулез.)
Если вы носите зубные протезы, вам нужно будет их снять, прежде чем брать образец мокроты. Затем прополощите рот водой. Затем сделайте глубокий вдох и глубоко откашляйтесь, чтобы взять образец мокроты. Человек, берущий образец, может постучать вам по груди. Это постукивание помогает разжижить мокроту в легких перед кашлем. Если у вас по-прежнему возникают проблемы с откашливанием образца, вас могут попросить вдохнуть аэрозольный туман, чтобы облегчить кашель.
Бронхоскопия
Некоторым людям может потребоваться бронхоскопия для взятия образца мокроты. Тонкая трубка с подсветкой (бронхоскоп) вводится через рот или нос в дыхательные пути, ведущие к легким. Вы получите лекарство, которое вызывает онемение горла и носа, чтобы вы не чувствовали боли от бронхоскопа. Вы также можете получить успокоительное, чтобы вызвать сонливость во время теста. Для сбора пробы солевой раствор можно промыть в дыхательные пути, а затем отсосать в контейнер.Для взятия образца можно использовать небольшую тонкую щетку.
Всасывание
Отсасывание также можно использовать для сбора образца мокроты. Мягкая гибкая трубка (называемая назотрахеальным катетером) вводится через нос в горло. Для сбора пробы применяется отсасывание на срок до 15 секунд. Этот метод часто используется для людей, которые очень больны или без сознания.
После отбора пробы
Образец мокроты будет помещен в контейнер с питательной средой или питательной средой.Это вещества, способствующие росту бактерий или грибков. Бактериям обычно требуется 2–3 дня для роста. Для роста грибка часто требуется неделя или больше. Для роста организма, вызывающего туберкулез, может потребоваться 6 недель. Любые бактерии или грибки, которые растут, будут обнаружены под микроскопом или с помощью химических тестов. Чтобы найти лучший антибиотик, тестирование чувствительности часто занимает еще 1-2 дня.
Как это чувствуется
Если вы чувствуете боль при глубоком вдохе или кашле, сдать образец мокроты может быть неудобно.Если вам нужно вдохнуть аэрозольный туман для получения образца, вы, вероятно, почувствуете сильное желание кашлять.
Во время бронхоскопии или сбора образца мокроты с помощью катетера вы можете почувствовать сильное желание кашлять. Это может произойти, когда бронхоскоп или катетер попадают в заднюю часть горла. Вы также можете почувствовать, что не можете дышать. Попытаться расслабиться. Дышите медленно.
Если вам дадут лекарство от онемения горла и носа, вы можете почувствовать, как будто у вас опухли язык и горло.Вам может быть трудно глотать.
Риски
Ваше горло может болеть после бронхоскопии или сбора мокроты с помощью назотрахеального катетера.
Если у вас тяжелая астма или бронхит, вам может быть трудно дышать во время сбора образца мокроты с помощью назотрахеального катетера.
Результаты
Посев мокроты – это тест для обнаружения бактерий или грибки, поражающие легкие или дыхательные пути.Некоторые виды бактерий или грибов быстро растут в культуре, а некоторые – медленно. Результаты анализов могут занять от 1 дня до нескольких недель. Сколько времени займет получение результатов, зависит от типа инфекции, которое, по мнению врача, у вас может быть. Некоторые организмы не растут в стандартной культуре и нуждаются в специальной питательной среде, которую можно найти в культуре мокроты. (Примеры: Chlamydophila pneumoniae и микоплазма.)
Обычный: | Мокрота, прошедшая через рот, обычно содержит несколько типов безвредных бактерий.К ним относятся некоторые виды стрептококка ( Streptococcus ) и стафилококка ( Staphylococcus ). В культуре не должно быть никаких вредных бактерий или грибков. Нормальные результаты посева отрицательны. |
Ненормальное: | Присутствуют вредные бактерии или грибки.Наиболее распространенными вредными бактериями в посеве мокроты являются те, которые могут вызывать бронхит, пневмония или туберкулез. Если растут вредные бактерии или грибки, посев положительный. |
Если результаты теста указывают на инфекцию, можно провести тест на чувствительность. Это тестирование помогает найти лучший антибиотик для уничтожения бактерий или грибков.
Даже если в вашей культуре не растут бактерии или грибки, у вас все равно может быть инфекция.
Что влияет на тест
Возможно, вы не сможете пройти тест, или результаты могут оказаться бесполезными, если:
- Вы использовали антибиотики в последнее время. Они могут предотвратить рост бактерий или грибков в культуре.
- Образец мокроты загрязнен.
- Недостаточно образца мокроты.
- Вы слишком долго ждете, чтобы отнести образец в лабораторию.
- Вы используете жидкость для полоскания рта перед сбором мокроты.
Что думать о
- Бактерии или грибки можно обнаружить, нанеся на образец мокроты специальные красители.Это называется окраской по Граму. Окраска по Граму может помочь врачу:
- Узнайте, подходит ли образец мокроты для посева. Например, правильно ли была собрана мокрота? Достаточно ли мокроты в пробе? Содержит ли он другие бактерии, не заражающие легкие? Если образец не подходит для культивирования, можно получить другой образец.
- Поставьте диагноз до того, как результаты посева вернутся из лаборатории. В некоторых случаях результаты окрашивания по Граму можно получить в течение 30 минут.Но другие результаты посева могут быть недоступны в течение от 1 до нескольких дней. Информация, полученная при окрашивании по Граму, может помочь вашему врачу быстрее вылечить инфекцию, не дожидаясь результатов посева.
- Мокрота, полученная при кашле, чаще всего содержит бактерии изо рта. Таким образом, врач рассмотрит ваши симптомы, состояние и другие результаты анализов (например, рентген грудной клетки) вместе с результатами посева.
- Тест на чувствительность помогает врачу выбрать лучшее лекарство для уничтожения определенных типов бактерий или грибков, заражающих человека.Различия в генетическом материале ( ДНК) бактерий или грибов может сделать их устойчивыми к определенным антибиотикам. В таких случаях эти антибиотики не могут убить все бактерии. Когда выбран антибиотик, вы должны принять все лекарство, чтобы снизить вероятность того, что бактерии станут устойчивыми к антибиотику. Раннее прекращение лечения антибиотиками убивает только самые слабые бактерии. Тогда более сильные и устойчивые могут размножиться и продлить инфекцию.Более поздние инфекции также может быть труднее лечить, если они вызваны устойчивыми бактериями.
- Бронхоскопия часто проводится при наличии серьезной или повторяющейся инфекции легких. Это особенно верно, когда другие тесты точно не обнаружили причину. Чтобы узнать больше, смотрите тему Бронхоскопия.
Список литературы
Консультации по другим работам
- Chernecky CC, Berger BJ (2008).Лабораторные исследования и диагностические процедуры, 5-е изд. Сент-Луис: Сондерс.
- Fischbach FT, Dunning MB III, ред. (2009). Руководство по лабораторным и диагностическим исследованиям, 8-е изд. Филадельфия: Липпинкотт Уильямс и Уилкинс.
- Pagana KD, Pagana TJ (2010). Руководство Мосби по диагностическим и лабораторным исследованиям, 4-е изд. Сент-Луис: Мосби.
Кредиты
Текущий по состоянию на: 23 сентября 2020 г.
Автор: Healthwise Staff
Медицинский обзор:
Адам Хусни, доктор медицины, семейная медицина
Э.Грегори Томпсон, врач – внутренняя медицина
Роберт Л. Коуи, MB, FCP (SA), MD, MSc, MFOM – Pulmonology
W. David Colby IV MSc, MD, FRCPC – Инфекционные заболевания
По состоянию на: 23 сентября 2020 г.
Автор: Здоровый персонал
Медицинский обзор: Адам Хасни, доктор медицины, семейная медицина и Э.Грегори Томпсон, врач-терапевт и Роберт Л. Коуи, MB, FCP (SA), MD, MSc, MFOM – пульмонология, и W. Дэвид Колби IV, MSc, MD, FRCPC – инфекционные заболевания
Бронхоэктазий; Причины, симптомы, лечение и профилактика
Обзор
Нормальный и поврежденный бронх с бронхоэктазами.Что такое бронхоэктазия?
Бронхоэктазия – это заболевание легких, вызывающее отхаркивание слизи. Это (произносится как brong-kee- ek -t uh -sis). В легких бронхи – это проходы, через которые воздух попадает в легкие. При бронхоэктазии внутренние поверхности бронхов со временем утолщаются из-за воспаления, которое оставляет рубцы. Более толстые стенки вызывают скопление слизи в этих проходах, потому что стенки недостаточно прочны, чтобы слизь могла выйти из легких.Кроме того, разрушаются реснички (тонкие пряди, похожие на волосы и помогающие отводить слизь). Когда это происходит, инфекции могут возникать легче, и дыхание становится затруднительным. Времена, когда дыхание или кашель ухудшаются, называются обострениями.
Насколько распространены бронхоэктазы?
По оценкам, в США 500 000 человек страдают бронхоэктазами, и один человек из 150 человек в возрасте 75 лет и старше страдает бронхоэктазами. Риск заболеть этим заболеванием увеличивается с возрастом.Однако молодые люди могут заболеть бронхоэктазами. У взрослых он гораздо чаще встречается у женщин, чем у мужчин. У детей это чаще встречается у мальчиков, чем у девочек. Рождение детей с бронхоэктазами возможно, но редко.
Каковы факторы риска бронхоэктазов?
Факторами риска бронхоэктатической болезни считаются люди со следующими состояниями:
- Муковисцидоз
- Хронические воспалительные заболевания легких
- Хронические или тяжелые легочные инфекции, такие как туберкулез, нетуберкулезные микобактерии (НТМ) или пневмония
- Дефицит иммунной системы
- Повторное вдыхание (вдыхание) чего-либо, кроме воздуха, например частиц пищи, которые вызывают повреждение легких
Симптомы и причины
Что вызывает бронхоэктазы?
Бронхоэктазия может быть вызвана муковисцидозом (МВ), генетическим заболеванием, которое приводит к длительным инфекциям легких и снижению способности дышать.CF со временем ухудшается.
Причина бронхоэктазов, не связанных с МВ, не всегда известна. Это называется идиопатической бронхоэктазией. Однако в других случаях причины включают:
- Тяжелая инфекция с повреждением легких в прошлом
- Генетические заболевания, такие как первичная цилиарная дискинезия или дефицит альфа-1-антитрипсина
- Состояние иммунной системы, затрудняющее борьбу с инфекциями
- Вдыхание (вдыхание) жидкостей, желудочного сока или пищи в легкие
- Аллергический бронхолегочный аспергиллез, аллергия на определенный вид грибка
- Другие состояния, такие как ревматоидный артрит, болезнь Крона и синдром Шегрена
- Закупорка дыхательных путей (дыхательные пути заблокированы чем-то вроде опухоли или вдыхаемого предмета)
Каковы симптомы бронхоэктазии?
Некоторые из наиболее распространенных симптомов:
- Кашель с выделением большого количества слизи
- Откашливание слизи с кровью (известное как кровохарканье)
- Боль или стеснение в груди из-за того, что трудно дышать
- Свистящее дыхание или свист при дыхании
- Забивание ногтей
- Потеря веса
- Вспышки, которые обычно включают:
Диагностика и тесты
Как врач диагностирует бронхоэктазы?
Считается, что бронхоэктатическая болезнь недооценивается.Если ваши симптомы заставляют вашего врача подозревать это заболевание, вероятно, будут назначены следующие анализы:
- КТ грудной клетки или Рентгеновский снимок , визуализационные тесты, чтобы показать состояние легких.
- Анализы крови и посев мокроты , чтобы узнать, есть ли инфекции.
- Функциональные тесты легких , чтобы определить, насколько хорошо вы дышите / насколько хорошо работают ваши легкие.
- Бронхоскопия , способ заглянуть внутрь легких.В этом методе используется свет и камера на трубке, вводимой через нос или рот, а затем по трахее в легкие. В случае закупорки бронхоскопия также может найти и удалить объект, блокирующий дыхательные пути. Процедуру также можно использовать для получения секрета из легких.
Ведение и лечение
Какие методы лечения бронхоэктазов?
Бронхоэктатическая болезнь неизлечима, но поддается лечению.Ваш врач может прописать лекарства, использование определенных устройств или сочетание этих и, возможно, других методов.
Если бронхоэктатическая болезнь вызвана основным заболеванием, например аспергиллезом или заболеванием иммунной системы, то сначала необходимо вылечить это состояние.
Варианты лечения могут включать лекарства, например:
- Антибиотики, лекарства, применяемые для лечения бактериальных инфекций. К ним относятся оральные (таблетки) и ингаляционные формы (вдыхаемые с помощью небулайзера).
- Макролиды, препараты, применяемые одновременно для лечения инфекций и воспалений.
- Лекарства, влияющие на слизь и способствующие ее откашливанию.
Лечение может также включать:
- Устройства очистки дыхательных путей для разрушения слизи и помощи при ее откашливании
- Устройства положительного давления на выдохе (PEP), которые можно держать в руках
- Ударные устройства, например жилетки, которые можно носить
- Физиотерапия похожа на хлопанье по груди, чтобы помочь вывести слизь из тела
Кроме того, лечение бронхоэктазов дополнительно подразделяется на то, на какой стадии вы находитесь: есть вещи, которые вы делаете ежедневно (поддержание), и действия, которые вы делаете, когда у вас обострение (ухудшение).
Профилактика
Как предотвратить бронхоэктазы?
Невозможно предотвратить врожденный бронхоэктаз (тот, с которым вы родились). Однако есть способы избежать повреждения легких, которое приводит к бронхоэктазу.
- Обязательно вакцинируйте своих детей от таких болезней, как корь и коклюш.
- Если у вас или вашего ребенка разовьется какая-либо легочная инфекция, обратитесь за медицинской помощью.
- Помните об опасности вдыхания любого предмета. Если ваш ребенок или взрослый вдохнет какой-либо предмет, немедленно обратитесь за медицинской помощью.
- Держитесь подальше от переносимых по воздуху веществ, которые могут повредить ваши легкие, таких как дым, пары и газы.
Перспективы / Прогноз
Каков прогноз для пациентов с бронхоэктазами?
Перспективы людей с бронхоэктазами сейчас лучше, чем раньше.Люди, которых лечат, живут относительно нормальной продолжительностью жизни. Прогноз также зависит от возраста человека, общего состояния здоровья, количества обострений за определенный период времени и степени тяжести обострений.
Жить с
Какие советы можно дать при бронхоэктатической болезни?
- Не курите.Если вы курите, обратитесь к врачу за помощью.
- Важно соблюдать ежедневную поддерживающую терапию, рекомендованную врачом.
- Соблюдайте здоровую диету.
- Пейте много воды, чтобы избежать обезвоживания и предотвращения липкости слизи.
- Выполняйте регулярные упражнения.
- Обязательно делайте прививку от гриппа каждый год и вакцину от пневмонии в соответствии с указаниями врача.
Когда мне следует обратиться к врачу по поводу бронхоэктазов?
Если в какой-то момент вы обнаружите, что сильно кашляете, часто кашляете слизью, кашляете с кровью или испытываете проблемы с дыханием, вам следует проконсультироваться с врачом.
Если вам поставили диагноз бронхоэктазия, вам следует связаться с вашим лечащим врачом, если:
- У вас есть признаки инфекции, например жар или озноб
- У вас проблемы с дыханием, чем обычно
- У вас болит грудь
- Вы устали намного больше, чем обычно
- Вы непреднамеренно худеете
- Вы кашляете еще больше слизи, слизи с кровью или слизи желтого или зеленого цвета
- У вас нет аппетита
Ресурсы
Существуют ли организации, которые поддерживают людей с бронхоэктазами и лиц, ухаживающих за ними?
Вам могут быть полезны следующие организации:
Реологический анализ мокроты от пациентов с хроническими бронхиальными заболеваниями
Анализ деформации непосредственно характеризует реологию мокроты
Структурные и динамические свойства образца запрашиваются в квазистатическом и проточном режимах соответственно.Чтобы последовательно оценить и то и другое на образцах мокроты, мы применяем развертку деформации с увеличением линейной деформации от 0,9% до 3000%. На рисунке 1 для каждого из четырех рассмотренных условий представлен типичный пример эволюции модулей накопления (\ (G ‘\)) и потерь (\ (G’ ‘\)) с деформацией. Реологические свойства, напоминающие мягкие вязко-эластопластические твердые вещества (гели), качественно аналогичны независимо от тестируемого состояния. При низкой деформации (обычно, когда \ (\ gamma \ leqslant 10 \% \)), \ (G ‘\) и \ (G’ ‘\) постоянны и, таким образом, представляют квазистатические свойства материала, когда структура остается практически неизменным при деформации (LVR).В мокроте механический ответ определяется эластичностью \ (G ‘> G’ ‘\) с коэффициентом демпфирования \ (\ tan \ delta = G’ ‘/ G’ \), обычно в пределах 0,25–0,45. Частотная зависимость модулей подчиняется слабому степенному закону со сравнимыми показателями для \ (G ‘\) и \ (G’ ‘\) (см. Дополнительный материал S1, рис. S1), как недавно наблюдалось в мокроте ХОБЛ 29 как а также образцы посевов слизи 30 .
Рисунок 1Реологический ответ мокроты на деформацию. Эволюция модулей хранения (\ (G ‘, \ blacktriangle \)) и потерь (\ (G’ ‘, \ blacktriangledown \)), а также коэффициента демпфирования (\ (\ tan \ delta = G’ / G ”, \ bullet \)) с приложенной деформацией, полученной при развертке деформации в колебательном режиме (частота 0.6 Гц). Незакрашенные символы: значения, полученные при развертке частоты при деформации 5% и 10% соответственно.
При увеличении деформации более чем на 10%, \ (G ‘\) и \ (G’ ‘\) оба уменьшаются и в конечном итоге сходятся выше деформации \ (\ sim 1000 \)%. В этом режиме структура сети начинает необратимо распутываться (пластический режим). Степень, амплитуда и форма этого режима варьируются от образца к образцу, независимо от состояния пациента. В большинстве случаев \ (G ” \) уменьшается со скоростью, аналогичной \ (G ‘\), по мере увеличения сдвига, но иногда остается почти постоянным во всем диапазоне пластичности (см. Здоровый случай на рис.1) и / или повышается и превышает значение \ (G ‘\) в конце этого диапазона (см. Случай ХОБЛ на рис. 1). Это альтернативное поведение отражает постепенное разворачивание и выравнивание микроструктурных элементов вдоль направления сдвига, что приводит к увеличению рассеяния. Вследствие этой изменчивости в пластическом режиме нельзя соблюдать общее правило относительно эволюции \ (\ tan \ delta \), которое либо остается примерно постоянным, либо постепенно увеличивается. Точка перехода (когда деформация \ (\ gamma = \ gamma _c \), обычно в пределах 500–3000%) определяет начало режима с преобладанием вязкости, т.е.е., поток. Обратите внимание, что эта критическая точка не всегда может быть достигнута и / или измерена надежно, поскольку некоторые образцы имеют тенденцию выходить из измерительной ячейки при высоком сдвиге.
Помимо общего поведения, показанного на рис. 1, меньшая часть образцов демонстрирует неожиданно вязкий отклик со слабыми значениями критической деформации \ (\ gamma _c \), около 100% или ниже. Предполагается, что эти жидкообразные образцы в основном состоят из слюны и поэтому исключаются – мы устанавливаем пороговое значение \ (\ gamma _c = 500 \% \), которое находится на полпути между поведением с преобладанием слюны и с преобладанием мокроты, ниже которого образец считается загрязненным.Кроме того, некоторые образцы (особенно среди астматиков и пациентов с ХОБЛ), по-видимому, имеют кроссовер, в то время как \ (G ‘\) и \ (G’ ‘\) оба очень резко увеличиваются, превышая 1000% деформации (рис. S2). Физический смысл этого очевидного резкого перехода не определен и, вероятно, связан с инструментальным артефактом. Чтобы избежать риска ненужных сравнений, образцы с таким необычным поведением выделены отдельно от анализа и обсуждаются отдельно в дополнительном материале S2.
Подводя итог, можно однозначно выделить две характерные деформационные реакции образцов мокроты в LVR и в начале кровотока (точка кроссовера).Мы извлекаем значение \ (G ‘\) и \ (G’ ‘\) в \ (\ gamma = 5 \% \) (см. Методы), которое обычно попадает в этот первый режим (или близко к нему) и может быть измеряется с разумной точностью. Поскольку линейный отклик по существу эластичен, мы сосредотачиваемся на \ (G ‘\); \ (\ tan \ delta \) также систематически указывается как структурный маркер баланса накопления и рассеивания. В кроссовере значение модуля \ (G ‘= G’ ‘= G’_c \) позволяет нам вычислить критическое напряжение \ (\ sigma _c = \ sqrt {2} G’_c \ gamma _c \ ), что физически соответствует напряжению, необходимому для движения материала.Теперь мы проанализируем надежность этих реологических величин для характеристики состояния пациента.
Реология мокроты стабильна во времени
Перспектива использования реологии мокроты в биомедицинских или клинических исследованиях основана на предположении, что значения измеренных реологических величин зависят от пациента и, следовательно, стабильны в течение относительно короткого времени, пока пациент остается стабильным.
Рисунок 2Временная стабильность реологии мокроты.Эволюция линейного модуля накопления \ (G ‘_ {5 \%} \) и критического стресса \ (\ sigma _c \) между последовательными повторами и между последовательными визитами для отдельных пациентов с ХОБЛ (вверху) и CF ( Нижний). Каждая связанная группа символов соответствует одному образцу мокроты; символы связаны с отдельными пациентами. Горизонтальная полоса в каждой реплике представляет собой среднее геометрическое. Факторы вариации – это отношения повторностей \ (n + 1 \) и n , взятых по отдельности, и повторяющихся значений при каждом посещении (столбец: средний коэффициент вариации).Заштрихованная область ограничивает вариации (увеличение или уменьшение) менее чем в два раза.
На рис. 2 показана индивидуальная эволюция \ (G ‘_ {5 \%} \) и \ (\ sigma _c \), измеренная в последовательных измерениях, выполненных на аликвотах из одного и того же образца (репликации), с одной стороны, и на последовательных образцах, полученных с разницей в два дня одним и тем же стабильным пациентом, с другой стороны. Символы и цвета идентифицируют отдельных пациентов с ХОБЛ (вверху) и CF (внизу). В обоих случаях отдельные значения разброса в пределах до двух порядков как в линейном, так и в кроссоверном режимах.Рассматривая образцы по отдельности, рис. 2 показывает, что, за некоторыми исключениями, вариации между последовательными повторами остаются в пределах двух раз (т.е. коэффициент вариации составляет от 0,5 до 2, что ограничивается заштрихованной областью). Двухдневные вариации рассчитываются путем сравнения для каждого пациента среднего числа повторений во время визитов 1 и 2. Хотя у некоторых пациентов наблюдается увеличение или уменьшение в 4–5 раз в отдельных случаях, в подавляющем большинстве из них на самом деле стабильны (в заштрихованной области), так что типичные относительные вариации между повторностями (один и тот же образец) и между посещениями (один и тот же пациент, разные образцы) сопоставимы по амплитуде.
Амплитуда наблюдаемых вариаций во всех случаях очень мала по сравнению с ожидаемой сигнатурой основных клинических событий. Сообщалось, что в линейном режиме \ (G ‘\) постоянно увеличивается примерно в 5 раз у пациентов с МВ при обострении и симметрично снижается до исходного уровня после события 24 : это изменение реологии мокроты. намного больше, чем типичные вариации, наблюдаемые в настоящем исследовании. Таким образом, последовательные измерения можно считать стабильными как на уровне выборки, так и на уровне пациента при рассмотрении характеристики основных событий.
Чтобы оценить статистическую надежность стабильности измерений, мы выполнили тесты корреляции между последовательными повторами и посещениями, когда они были доступны. В таблице 1 собраны коэффициент корреляции Спирмена и соответствующее значение p , полученные в каждом случае (см. Также дополнительный материал S3, таблица S1). Последовательные повторы (первая строка) значимо коррелированы во всех случаях (\ (p <0,05 \)), что подтверждает высокую стабильность измерений на уровне выборки.Эта стабильность показывает, что в течение продолжительности набора измерений (до \ (\ sim \) 1 часа после отхаркивания) образцы мокроты существенно не изменяются, и повторные сравнительные измерения могут иметь значение, если можно собрать достаточное количество образца.
Между посещениями (вторая строка) значимая корреляция обнаружена только для \ (G ‘_ {5 \%} \) у пациентов с ХОБЛ. Во всех других случаях корреляции не могут быть подтверждены из-за очень небольшого размера популяции (\ (N \ leqslant 5 \)), что не позволяет нам сделать статистически надежный вывод.Однако, учитывая умеренные двухдневные вариации, наблюдаемые в большинстве образцов (рис. 2), и статистически устойчивую двухдневную корреляцию, обнаруженную в более благоприятном случае (\ (G ‘_ {5 \%} \) при ХОБЛ , с \ (N = 11 \)), разумно ожидать глобальной двухдневной стабильности реологических измерений.
Таблица 1 Результаты корреляционных тестов Спирмена между случаями (посещение 1, повторение 1), (посещение 1, повторение 2) и (посещение 2, повторение 1): коэффициент Спирмена \ (\ rho \), p -значение и объемом выборки N .Этот результат, кажется, противоречит выводам Радтке и др., Которые, скорее, пришли к выводу, что стабильность реологических измерений не может быть подтверждена статистически 25 . Однако в их исследовании оценивалась стабильность измерений в течение более длительного времени (\ (7 \ pm 1 \) дней, с промежуточным посещением), что делает клиническое развитие более вероятным. Примечательно, что медианные значения модулей упругости очень похожи в первых двух посещениях, но значительно меньше в третьем из-за плохого перекрытия распределений.Таким образом, это исследование не ставит под сомнение наш вывод о том, что мокроту можно считать стабильной в течение 2 дней.
Реологическая стабильность мокроты означает, что можно определить исходные уровни и считать их репрезентативными для стабильного пациента с данным состоянием. Конечно, надежность реологических характеристик также зависит от стандартизованных протоколов, особенно во время получения мокроты. В свете этого мы теперь оцениваем, как на реологические измерения влияет индукция предварительного сбора.
Индукция мокроты изменяет ее реологию
Возможным практическим ограничением анализов мокроты является возможность сбора достаточного количества образца. Фактически, спонтанное выделение мокроты возможно только у пациентов с избыточной секрецией. Чтобы помочь пациентам отхаркивать, обычно применяется индукция 28 , которая заключается в распылении солевых растворов с помощью мундштука; это действительно необходимо в тех случаях, когда пациенты не могут откашливаться самостоятельно. Однако, поскольку физиологические растворы являются гидраторами слизи, они, вероятно, влияют на реологию мокроты 17 .Мы количественно оценили этот эффект как на ХОБЛ, так и на мокроту при МВ, поскольку эти две группы населения могли откашливаться спонтанно.
Рисунок 3Влияние индукции на реологию мокроты. Слева: эволюция линейного модуля упругости \ (G ‘_ {5 \%} \), коэффициента демпфирования \ (\ tan \ delta _ {5 \%} \) и критического напряжения \ (\ sigma _c \ ), до (\ (t = 0 \), спонтанное отхаркивание) и после распыления 4,5% HSS для отдельных пациентов с ХОБЛ. Справа: те же реологические параметры, при сравнении спонтанной мокроты с 4.Распыление 5% HSS (10 мин) и 2,5 мл рчДНазы у пациентов с МВ. Каждая связанная группа символов соответствует последовательным образцам мокроты, собранным у одного и того же пациента; каждый символ представляет собой среднее значение для последовательных повторений, если доступно. Горизонтальные полосы: геометрическое (\ (G ‘, \ sigma _c \)) или арифметическое (\ (\ tan \ delta \)) среднее по соответствующим совокупностям. * \ (p <0,05 \); ** \ (р <0,01 \).
На левой панели рис. 3 представлена эволюция \ (G ‘_ {5 \%} \), \ (\ tan \ delta _ {5 \%} \) и \ (\ sigma _c \), измеренная на Мокрота при ХОБЛ, собранная через несколько последовательных откашливаний до (\ (t = 0 \)) и во время распыления 4.5% гипертонический солевой раствор (ГСС). И \ (G ‘_ {5 \%} \), и \ (\ sigma _c \) соответственно уменьшаются в \ (2,9 \ pm 1,8 \) (\ (p = 0,009 \)) и \ (3,4 \ pm 2,3 \) (\ (p = 0,246 \)) в течение первых 10 минут, а затем в среднем насыщаются. Первоначальная тенденция также постоянно наблюдается на уровне отдельных пациентов, за исключением пациентов, у которых в мокроте уже были низкие реологические базовые уровни. Развитие \ (\ tan \ delta _ {5 \%} \) более контрастно, хотя средний тренд показывает небольшое увеличение от 0.От 31 до 0,37 (\ (p = 0,043 \)), что может отражать легкий увлажняющий эффект. При кистозном фиброзе мокроты (рис.3, правая панель) также наблюдается уменьшение в \ (2,6 \ pm 1,1 \) (\ (p = 0,014 \)) и \ (1,9 \ pm 0,7 \) (\ (p = 0,061 \)), из \ (G ‘_ {5 \%} \) и \ (\ sigma _c \) посредством индукции HSS, и контрастные изменения в \ (\ tan \ delta _ {5 \%} \) (\ ( р = 0,836 \)). Таким образом, распыление HSS аналогичным образом приводит к значительному снижению линейных и перекрестных реологических параметров при обеих патологиях, хотя и более выражено при ХОБЛ, чем при МВ.
Для сравнения, рекомбинантная человеческая ДНКаза I (рчДНаза, Pulmozyme) вводилась пациентам с МВ во время их второго визита. RhDNase – муколитический препарат, широко используемый при лечении CF, который ослабляет гнойную слизь путем расщепления ДНК 13,15 . Как показано на правой панели рис. 3, рчДНаза влияет на реологию мокроты способом, количественно сопоставимым с HSS (\ (G ‘_ {5 \%} \) и \ (\ sigma _c \) уменьшаются в \ раз. (1.9 \ pm 1.0 \) и \ (2.2 \ pm 1.6 \) соответственно; \ (p = 0.053 \) и \ (p = 0,049 \)).
Таким образом, индукция HSS однозначно приводит к существенному ослаблению исходного реологического уровня мокроты у пациентов с ХОБЛ и МВ, что значительно превышает вариабельность измерений. Следовательно, индукцию следует рассматривать как важный параметр при сравнении реологических измерений в мокроте. Следовательно, с учетом стандартизованного протокола, даже пациенты с избыточной секрецией должны проводить индукцию, если их мокрота сравнивается со здоровыми людьми.
Реология мокроты характеризует хронические бронхиальные заболевания
Теперь вернемся к сравнению реологических свойств у пациентов с различными состояниями. Учитывая, что пациент может быть охарактеризован исходным уровнем реологии его / ее мокроты, мы теперь задаемся вопросом, определяется ли сам этот уровень заболеванием. Таким образом, мы строим для каждой реологической величины распределение уровней пациентов в каждой популяции.
Рис. 4Реологические уровни при некоторых состояниях бронхов.Вверху: графики вероятностей значений \ (G ‘_ {5 \%} \), \ (\ tan \ delta _ {5 \%} \) и \ (\ sigma _c \), измеренных у субъектов с четырьмя условиями. (здоровый, \ (\ bullet \); астма, \ (\ blacktriangle \); ХОБЛ, \ (\ blacklozenge \); CF, \ (\ blacktriangledown \)). Каждый символ соответствует среднему значению для пациента после распыления HSS; сплошная линия соответствует уравнению. (1). Внизу: ожидаемые значения и стандартные отклонения (\ (X_0 \ pm \ Sigma \)) этих реологических параметров, сравниваемые по условию, как функция соответствующего относительного FEV \ (_ 1 \) (среднее ± стандартное отклонение).Закрашенные и открытые символы обозначают HSS-индуцированную и спонтанную мокроту соответственно. ** \ (p <0,01 \); *** \ (р <0,001 \).
Учитывая стабильность реологических измерений, уровень каждого пациента определяется путем усреднения всех значений, полученных после распыления HSS. Это дает нам для каждой реологической величины единое значение для каждого пациента и позволяет избежать перегрузки наиболее продуктивных. На верхней панели рис. 4 эти данные представлены в виде графиков вероятностей \ (G ‘_ {5 \%} \), \ (\ tan \ delta _ {5 \%} \) и \ (\ sigma _c \) для четырех популяций здоровых субъектов, астматиков, пациентов с ХОБЛ и МВ.2} \ mathrm {d} t \) функция ошибок и \ (X = \ log G ‘_ {5 \%} \), \ (\ tan \ delta _ {5 \%} \) и \ (\ log \ sigma _c \) соответственно; \ (X_0 \) и \ (\ Sigma \) – соответственно ожидаемое значение и стандартное отклонение. С этими переменными функциональная форма E ( X ) подразумевает, что распределения \ (\ tan \ delta _ {5 \%} \), с одной стороны, и \ (G ‘_ {5 \% } \) и \ (\ sigma _c \), с другой стороны, являются нормальными и логнормальными соответственно. Рассчитанные ожидаемые значения (\ (X_0 \)) и стандартные отклонения (\ (\ Sigma \)) показаны на нижней панели рис.4; В таблице 2 приведены соответствующие физические величины для всего набора измеренных реологических параметров.
Рисунок 4 подтверждает, что реология мокроты позволяет различать патологии. В линейном режиме модули упругости уменьшаются по мере увеличения средних относительных значений ОФВ \ (_ 1 \) и хорошо сменяют друг друга по сравнению со здоровыми (ожидаемое значение, \ (G ‘= 0,14 ~ \ mathrm {Pa} \)), астматиками. (0,25 Па), ХОБЛ (0,43 Па) до пациентов с МВ (0,84 Па), демонстрируя постепенно более жесткую слизь. Однако существует некоторое совпадение, и только CF и здоровая мокрота статистически различны (\ (p <0.01 \)). Коэффициент демпфирования \ (\ tan \ delta \) постоянно остается около 0,35. Таким образом, даже если гелевая структура слизи, вероятно, различна в каждом состоянии, что макроскопически отражается через различные значения \ (G '\), влияние рассеивания по существу идентично. Никакое состояние не отличается "более жидкой" или "более твердой" слизью.
При кроссовере четыре условия следуют той же последовательности ранжирования, что и линейные модули, с меньшим перекрытием между популяциями.В частности, значения \ (\ sigma _c \), соответствующие пациентам с ХОБЛ и МВ, значительно выше (в 10-20 раз), чем значения, измеренные у здоровых субъектов (3,61 и 6,34 Па по сравнению с 0,27 Па; \ (p <0,01 \) и \ (p <0,001 \) соответственно). Больные астмой находятся на среднем уровне (0,75 Па), но ближе к здоровым субъектам и статистически отличаются от пациентов с МВ (\ (p <0,01 \)). Таким образом, критический стресс разительно отличает обструктивные (ХОБЛ, МВ) от необструктивных состояний (астма, здоровые), что подчеркивает роль динамических (текучести) свойств слизи в бронхиальной обструкции.Таблица 3 суммирует результаты всех сравнительных тестов Бонферрони, выполненных с помощью ANOVA, а также включает статистический анализ измерений FEV \ (_ 1 \). Эти результаты подтверждают повышенную специфичность измерений кроссовера (\ (G'_c \) и \ (\ sigma _c \)) по сравнению с линейными модулями (\ (G '\) и \ (G' '\) при 5%) и к ВРЭ \ (_ 1 \). Таким образом, реология мокроты позволяет лучше различать патологические состояния, особенно обструктивные, чем спирометрия.
Для сравнения ожидаемые значения и стандартные отклонения для спонтанной мокроты также представлены на нижней панели рис.4 (открытые символы; только пациенты с ХОБЛ и МВ) и сведены в Таблицу 2. Уровни ХОБЛ и МВ становятся поразительно похожими в линейном и перекрестном режимах.
Таблица 2 Ожидаемые и экстремальные значения, полученные из распределений для каждой измеренной реологической величины. Таблица 3 Результаты ANOVA: p – значения, полученные в результате теста сравнения всех пар Бонферрони.Бронхоэктазы – Физиопедия
Определение
Бронхоэктазия – это обструктивное заболевание легких, которое возникает в результате наличия хронических воспалительных выделений и микробов, приводящих к необратимому расширению и деформации стенок дыхательных путей, а также к рецидивирующей инфекции [1] .Это связано с частыми обострениями, которые являются независимым предиктором прогрессирующего снижения респираторной функции и ухудшают прогноз [2]
Механизм повреждения / патологического процесса
Бронхоэктазия – хроническое необратимое расширение бронхов в легких. Это следует за тяжелой инфекцией легких или аспирацией. Это чаще встречается при таких состояниях, как муковисцидоз, ревматоидный артрит, иммунодефицит, синдром Юнга и аллергический бронхолегочный аспергиллез, а также после детских болезней, таких как коклюш, туберкулез и корь.Бронхоэктатическая болезнь, не связанная с муковисцидозом, известна как брохиэктазия без муковисцидоза [2]
[3]
Клинически значимая анатомия
Бронхоэктазия включает воспаление стенок дыхательных путей, в частности стенок бронхов [4] . Стенки дыхательных путей – это «трубки», которые идут от рта и носа к легким. Основная область поражения бронхоэктазами – это бронхи [4] .Трахея разветвляется на правый и левый главные бронхи, которые затем делятся на вторичные бронхи; по одному на каждую долю легкого [5] . Затем они делятся на третичные бронхи; по одному на каждый бронхолегочный сегмент [5] . Для более подробной анатомии см. Анатомия легких.
Реснички также повреждаются при бронхоэктазии. Реснички выстилают дыхательные пути и прикрепляются к эпителию. Они похожи на волосы с крошечными крючками на кончике, которые захватывают слизистую и помогают продвигать ее к горлу [4] .
Эпидемиология
Недооценивается распространенность, заболеваемость и заболеваемость, поскольку симптомы часто приписывают курению. Исследование, проведенное Hill [6] , показало, что каждый 1000 человек в Великобритании страдает бронхоэктазами, при этом количество связанных смертей увеличивается примерно на 3% в год в Англии и Уэльсе [7] . Хотя общий уровень смертности в этих странах увеличивается, показатели в старших группах растут, тогда как показатели в более молодых группах снижаются [7] .Непропорционально большое количество случаев выявлено в развивающихся странах и среди аборигенов в богатых общинах [8] . В некоторых группах населения улучшение социально-экономического статуса, жилья и образования может улучшить общее состояние здоровья и снизить частоту респираторных инфекций и развития бронхоэктазов [8] .
Этиология
Причина неизвестна в 50% случаев, но связана с воспалительным заболеванием кишечника, ревматоидным артритом и у 29-50% пациентов с ХОБЛ [9] .Есть несколько состояний, связанных с бронхоэктазами, в том числе: муковисцидоз, первичная цилиарная дискинезия, туберкулез легких, аллергический бронхолегочный аспергиллез, ревматоидные заболевания, симптоматическая красная волчанка, иммунодефицит, тяжелая респираторная инфекция у детей и воздействие инородного тела или разъедающего вещества [4] . Это также было связано с дефицитом x1-антитрипсина [4] . Бронхоэктазы предрасполагают пациентов к приобретенным и врожденным легочным инфекциям [4] .
Патофизиология
Процесс начинается с воспалительного поражения стенок бронхов, которое затем стимулирует образование избыточной густой слизи [4] . Теплая и влажная среда легких в сочетании со слизью вызывает дальнейшее воспаление и непроходимость, создавая отличную среду для инфекции [4] . Густая слизь раздавливает реснички и вызывает дальнейшее повреждение. Иммунный ответ высвобождает токсичные воспалительные химические вещества (например, нейтрофилы), а также приводит к фиброзу и бронхоспазму, если он сохраняется [4] .
Диагностические процедуры
В настоящее время КТ высокого разрешения является золотым стандартом диагностики бронхоэктазов [4] . На сканированном изображении могут присутствовать параллельные технологические колеи и кольцевые тени, указывающие на утолщенные стенки дыхательных путей и расширенные дыхательные пути, соответственно, [4] . Также могут быть «тени пальцев перчаток», которые представляют собой выступы в виде пальцев, которые представляют расширенные бронхи, заполненные затвердевшим секретом [4] .
Спирометрия просто определяет наличие обструкции дыхательных путей, но это может указывать на многие другие заболевания [4] .
Микробиология также может использоваться для идентификации бактерий, присутствующих во время обострения [4] . Образец мокроты отправляется, и результаты возвращаются с частотой бактериальной колонизации, измеренной [4] .
Клинические проявления
Так как нежные реснички часто повреждаются из-за наличия густой слизи, большое количество образовавшейся мокроты не может быть эффективно удалено [4] . Эти выделения приводят к появлению хрипов, грубого потрескивания и писка при аускультации.Часто пациенты также проявляют мышечную дисфункцию из-за воспаления, нарушений газообмена, бездействия, недоедания, гипоксии и приема лекарств [10] . Одышка при физической нагрузке, по-видимому, является основным клиническим проявлением, поскольку ее испытывают три из четырех пациентов. Другие физические проявления включают боль в груди, храп, удары дубинками, усталость, постоянный кашель, рецидивирующую инфекцию и потерю аппетита [4] . Стрессовое недержание мочи также может быть результатом чрезмерного кашля.Бронхоэктазия также имеет психологические проявления, такие как тревога, депрессия, снижение уверенности, изменение отношений и отсутствие работы [4] .
Обострения могут возникать несколько раз в год и идентифицируются по четырем или более из следующих признаков и / или симптомов: изменение мокроты, усиление одышки, усиленный кашель, температура более 38 °, усиление хрипов, снижение переносимости физических нагрузок, утомляемость, летаргия и рентгенологические признаки новой инфекции [4] .
Физиотерапия и другое лечение
Ключом к лечению бронхоэктазов является обучение и системное лечение. В настоящее время антибиотики используются при первых признаках изменения цвета мокроты [4] , а длительный прием антибиотиков рекомендуется людям, у которых в год случаются 3 и более обострения [11] . Поскольку антибиотики не помогают при стойком воспалении дыхательных путей, ингаляционные стероиды используются как противовоспалительное средство и для уменьшения образования мокроты [4] .Броходилататоры, как правило, помогают пациентам, у которых одновременно есть ХОБЛ и астма [11] . Обзор и контролируемое исследование показали, что многие люди с бронхоэктазами также имеют дефицит витамина D, и назначение витамина D может иметь противовоспалительную и противоинфекционную роль [12] [13] .
Физиотерапия играет очень важную роль в облегчении симптомов бронхоэктазов. Поскольку мукоцилиарный клиренс снижен примерно до 15% от нормы, пациенты склонны кашлять чаще [4] .Физиотерапевтические процедуры направлены на облегчение выведения секрета, снятие усталости, вызванной усилием неэффективного очищения и учащенным кашлем. Наиболее распространенные и эффективные методы лечения:
Активный цикл дыхательной техники
(ACBT) – это широко распространенная методика, которая часто используется с постуральным дренажом и ручным дренажом [14] . Его цель – разжижить и очистить излишки легочного секрета, улучшить эффективность кашля и улучшить вентиляцию легких и их функцию.Он состоит из 3-х основных этапов:
- Контроль дыхания
- Упражнения на глубокое дыхание или упражнения на расширение грудной клетки
- Техника принудительного выдоха (FET) [15]
- Техника принудительного выдоха, иногда называемая гудком. Он является частью ACBT, но может использоваться отдельно. Вытяжка очень эффективна при очистке секрета, особенно в сочетании с другими методами очистки дыхательных путей. [16]
- Мануальная терапия – это популярный метод лечения, который часто используется, когда пациент устал или испытывает обострение симптомов.В нем описаны методы, которые включают внешние силы, воздействующие на грудную стенку для разжижения слизи, и включают любую комбинацию перкуссии, встряхивания, подпрыгивания ребер, вибраций и избыточного давления [17] . Из-за характера техники он противопоказан пациентам, принимающим антикоагулянты или страдающим остеопорозом [18] . Целью лечения является:
- Выделение секрета
- Снижение усталости
- Повысьте эффективность других методов лечения
- Постуральный дренаж (или модифицированный постуральный дренаж) – это эффективное лечение, которое включает в себя техники с использованием силы тяжести, чтобы помочь очистить выделения из определенных сегментов легких, и часто требует наклона головы вниз очистить выделения из средней и нижней долей.Болезнь Паркинсона обычно используется в сочетании с другими методами, такими как АКВТ, перкуссия, кашель или выдох. Исследования показали, что при использовании этих методов при болезни Паркинсона выделяется большее количество мокроты [19] [20] . Хотя болезнь Паркинсона эффективна для удаления секрета, она требует много времени и часто оказывается менее переносимой, чем методы, выполняемые сидя [20] . Если наклон головы вниз противопоказан или недопустим, вместо этого можно использовать позиции модифицированного постурального дренажа (МПД), а в случаях, когда гастроэзофагеальная рефлюксная болезнь присутствует и обостряется даже при использовании модифицированной болезни Паркинсона, рекомендуется использовать метод, который может выполнять сидя.
- Аутогенное дренирование – это метод, при котором используется контроль дыхания для удаления выделений из дыхательных путей. Цель состоит в том, чтобы изменить глубину, частоту и расположение объемов легких во время дыхания, чтобы переместить выделения из более мелких дыхательных путей в более крупные дыхательные пути для облегчения отхождения мокроты. Он состоит из трех этапов:
- Фаза мобилизации (отсоединения) – включает в себя выдыхание как можно большего количества воздуха из легких и подавление позывов к кашлю.На этом этапе можно услышать потрескивание.
- Фаза сбора – по мере того, как выделения становятся громче, частота и глубина вдоха меняются, скорость выдоха увеличивается (но не слишком быстро, чтобы вызвать кашель) и ощущается больше в середине грудной клетки. Это способствует перемещению секрета из более мелких дыхательных путей в более крупные.
- Фаза очищения – по мере того, как выделения становятся громче, цель теперь состоит в том, чтобы сделать полные медленные глубокие вдохи с последующим быстрым выдохом.Подавите желание кашлять и после трех глубоких вдохов выдохните, чтобы вывести выделения. Часто вздоха бывает достаточно, чтобы очистить выделения, но если они неэффективны, это стадия, на которой кашель может быть эффективным для удаления выделений.
- Положительное давление выдоха (PEP) – это метод, который описывает дыхание с сопротивлением и может выполняться либо через устройство, либо против сжатых губ. Это метод, который рекомендуется, когда другие методы неэффективны или противопоказаны; Было обнаружено, что он не оказывает неблагоприятного воздействия на ГЭРБ. [21] Повышение давления создает противодавление в дыхательных путях во время выдоха. Это может вызвать скопление газа за слизью, временно увеличивая функциональную способность и улучшая очищение от слизи. [22]
Исследования показывают лучшие результаты с комбинацией устройства Bubble PEP и ACBT в очищении от мокроты у этих пациентов [23] .
Высокочастотное колебание грудной клетки достигается за счет ношения жилета, имитирующего физиотерапию грудной клетки.Жилет подает импульсы воздуха с положительным давлением к груди, которые вызывают вибрации, которые разжижают и разжижают слизь. Это вместе с прерывистым кашлем или раздражением способствует удалению выделений. Это устройство позволяет людям проводить терапию в удобное для них время, что дает им некоторый контроль и меньшую зависимость от других людей.
Внутрилегочная перкуссионная вентиляция – это еще один метод, в котором используется устройство, способствующее удалению секрета. Внутрилегочный перкуссионный вентилятор (IPV) – это аппарат, который доставляет короткие порции воздуха через мундштук, который вызывает вибрацию стенок дыхательных путей [24] .Он показан для краткосрочного использования, когда другие методы противопоказаны или оказались неэффективными.
Прерывистое дыхание с положительным давлением (IPPB) – дорогое оборудование [25] и обычно используется только тогда, когда все другие методы зазора оказались неэффективными [11] . Это обычно наблюдается в отделениях интенсивной терапии и дает положительное давление при вдохе пациента, а во время выдоха создает отрицательное давление, делая кашель сильнее и эффективнее.
Физические упражнения рекомендуются при респираторных заболеваниях, включая бронхоэктазы, с целью улучшения аэробных возможностей, физической формы и выносливости.Исследование, проведенное Ли и соавторами, пришло к выводу, что физические упражнения привели к краткосрочным улучшениям и повлияли на одышку и утомляемость, а также привели к меньшему количеству обострений в течение 12 месяцев [26] .
Показатели результата
Для того, чтобы оценить эффективность лечения и изменения качества жизни, доступно несколько критериев оценки результатов:
- Георгиевский респираторный опросник (SGRQ) [4] . SGQ – это широко используемый опросник для измерения качества жизни, связанного со здоровьем, у пациентов с респираторными заболеваниями [27] .
- Опросник качества жизни – бронхоэктазы (QOL-B) [28]
- Лестерский опросник по поводу кашля [29]
- Опросник по хроническим респираторным заболеваниям (CRDQ) [30]
Ссылки
- ↑ Баркер А.Ф. Бронхоэктазия. Медицинский журнал Новой Англии, 2002 г .; 346: 1383-93.
- ↑ 2,0 2,1 Мартинес-Гарсия М., Солер-Каталония Дж., Перпина-Тордера М., Роман-Санчес П., Сориано Дж .: Факторы, связанные со снижением функции легких у взрослых пациентов со стабильным некистозным фиброзным бронхоэктазом.Сундук 2007, 132: 1565–1572
- ↑ саламхоссейн. Анимация бронхоэктаза – Что такое бронхоэктазия? Видео.mp4. Доступно по адресу: https://www.youtube.com/watch?v=uNeprw1rsgE [последний доступ 18.05.15]
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 905 905 905 4,1 4.16 4,17 4,18 4,19 4,20 4,21 4,22 Хью А. Физиотерапия в респираторной и кардиологической помощи: научно-обоснованный подход. 4-е изд. Хэмпшир: Cengage Learning EMEA, 2014.
- ↑ 5,0 5,1 Паластанга Н., Сомс Р. Анатомия и движения человека: структура и функции. 6-е изд. Нью-Йорк: Черчилль Ливингстон; 2012 г.
- ↑ Hill AT, Welham S, Reid K, Bucknall CE. Национальный аудит бронхоэктазов Британского торакального общества в 2010 и 2011 гг.Thorax 2012; 1: 1-3.
- ↑ 7,0 7,1 Робертс Х.Дж., Хаббард Р. Тенденции смертности от бронхоэктазов в Англии и Уэльсе. Респираторная медицина 2010; 104: 981-5.
- ↑ 8,0 8,1 Чанг А.Б., Марш Р.Л., Воан-Смит ХК, Хоффман Л.Р. Новые препараты от бронхоэктазов. Informa Healthcare 2012; 17: 361-378.
- ↑ Goeminne P, Dupont L. Бронхоэктазия без кистозного фиброза: Диагностика и лечение в 21 веке. Postgrad Med J 2010; 86: 493-501.
- ↑ Озалп О, Инал-Инче Д., Калик Э., Вардар-Яглы Н., Саглам М., Савчи С. и др. Внелегочные особенности бронхоэктазов: функция мышц, работоспособность, утомляемость и состояние здоровья. Междисциплинарная респираторная медицина 2012; 7: 1-6.
- ↑ 11,0 11,1 11,2 Хилл А.Т., Салливан А.Л., Чалмерс Д.Д., Де Сойза А., Элборн Д.С., Флото Р.А., Грилло Л., Граффид-Джонс К., Харви А., Хаворт С.С., Хискокс Е. Британское торакальное общество Руководство по бронхоэктатической болезни у взрослых.Грудная клетка. 2019, 1 января; 74 (Приложение 1): 1-69.
- ↑ Бартли Дж., Гарретт Дж., Грант СС, Камарго, Калифорния. Может ли витамин D играть потенциальную противовоспалительную и противоинфекционную роль при бронхоэктазиях? Текущие отчеты об инфекционных заболеваниях. 2013 1 апреля; 15 (2): 148-57.
- ↑ Чалмерс Дж. Д., МакХью Б. Дж., Дочерти С., Гован Дж. Р., Хилл АТ. Дефицит витамина D связан с хронической бактериальной колонизацией и серьезностью бронхоэктазов. Грудная клетка. 2013, 1 января; 68 (1): 39-47.
- ↑ О’Нил Б., Брэдли Дж. М., МакАрдл Н. и др.Текущее физиотерапевтическое лечение пациентов с бронхоэктазами: исследование в Великобритании. Int J Clin Pract 2002; 56: 34–5.
- ↑ Ларнер Э., Гейли П. Активный цикл дыхательной техники. Доступно по адресу: http://www.nnuh.nhs.uk/publication/download/active-cycle-of-breathing-technique-v3 (по состоянию на 24 марта 2019 г.)
- ↑ Van der Schans CP. Принудительные экспираторные маневры для увеличения транспорта бронхиальной слизи: механистический подход. Архивы Мональди по заболеваниям грудной клетки = Archivio Monaldi per le malattie del torace.1997 Август; 52 (4): 367.
- ↑ Сайед Н., Майя А.Г., Шива Кумар Т. Активные циклы дыхательной техники (АКВТ) по сравнению с традиционной физиотерапией грудной клетки при очистке дыхательных путей при бронхоэктазах – перекрестное испытание. Достижения в физиотерапии. 2009, 1 января; 11 (4): 193-8.
- ↑ Дил Н, Джонсон ММ. Распространенность остеопении и остеопороза у пациентов с бронхоэктазами некистозного фиброза. Саут Мед Дж. 2016; 109 (12): 779-83
- ↑ Рамос Е.М., Рамос Д., Морейра Г.Л., Маккионе М., Гимарайнш Э.Т., Родригес FM, де Соуза А.А., Сальдива PH, Жардим-младший.Вязкоупругие свойства бронхиальной слизи после респираторной физиотерапии у пациентов с бронхоэктазами. Респираторная помощь. 2015 1 мая; 60 (5): 724-30.
- ↑ 20,0 20,1 Флуд Л.Дж., агент П, Билтон Д. Методы физиотерапии грудной клетки при бронхоэктазах. Клиники грудной медицины. 2012, 1 июня; 33 (2): 351-61.
- ↑ Ли А.Л., Денехи Л., Уилсон Дж. У. и др. Терапия и упражнения с положительным давлением на выдохе: влияние на гастроэзофагеальный рефлюкс при ХОБЛ и бронхоэктазах.Respir Care 2012; 57: 1460–7.
- ↑ McIlwaine M, Button B, Dwan K. Физиотерапия положительным давлением на выдохе для очистки дыхательных путей у людей с муковисцидозом. Кокрановская база данных систематических обзоров. 2015 (6).
- ↑ Сантос, Мэриленд, Милросс, Массачусетс, Маккензи, Д.К., Элисон Дж. Пузырько-положительное устройство для измерения давления на выдохе и очистка мокроты при бронхоэктазах: рандомизированное перекрестное исследование. Международная организация физиотерапевтических исследований. 2020 29 февраля: e1836.
- ↑ Paneroni M, Clini E, Simonelli C, et al.Безопасность и эффективность кратковременной внутрилегочной перкуссионной вентиляции у пациентов с бронхоэктазами. Respir Care 2011; 56: 984–8.
- ↑ Eggertsen SC. Прерывистое дыхание с положительным давлением и лечение острой астмы. Журнал семейной практики. 1983 Май; 16 (5): 909-13.
- ↑ Ли А.Л., Хилл С.Дж., Сесинс Н. и др. Краткосрочные и долгосрочные эффекты тренировок при бронхоэктазиях без кистозного фиброза – рандомизированное контролируемое исследование. Respir Res 2014; 15:44.
- ↑ Феррер М., Миравитлес М., Вилласанте С., Алонсо Дж., Собрадилло В., Габриэль Р. и др.Интерпретация показателей качества жизни по респираторному опроснику Святого Георгия. Eur Respir J 2002; 19 (3): 405-13.
- ↑ Quittner AL, O’Donnell AE, Salathe MA, Lewis SA, Li X, Montgomery AB, O’Riordan TG, Barker AF. Опросник качества жизни – бронхоэктазы: окончательный психометрический анализ и определение минимально важных различий в баллах. Грудная клетка. 2015 1 января; 70 (1): 12-20.
- ↑ Birring SS, Prudon B, Carr AJ, Singh SJ, Morgan MD, Pavord ID. Разработка симптомно-специфического показателя состояния здоровья для пациентов с хроническим кашлем: опросник Лестера по кашлю (LCQ).Грудная клетка. 2003 г., 1 апреля; 58 (4): 339-43.
- ↑ Воданович Д.А., Бикнелл Т.Дж., Холланд А.Е., Хилл С.Дж., Сесинс Н., Дженкинс С., Макдональд С.Ф., Бердж А.Т., Томпсон П., Стирлинг Р.Г., Ли А.Л. Валидность и надежность опросника по хроническим респираторным заболеваниям у пожилых людей с легкой и средней степенью некистозно-фиброзных бронхоэктазов. Дыхание. 2015; 90 (2): 89-96.
Движущаяся слизь имеет значение для здоровья легких · Границы для молодых умов
Аннотация
Когда мы дышим, легкие обменивают кислород воздуха на углекислый газ из крови.Этот обмен жизненно необходим. Каждый вдох подвергает легкие воздействию внешней среды, содержащей загрязнения и микробы, представляющие угрозу для нашего здоровья. Первая линия защиты называется мукоцилиарным эскалатором: слизь улавливает потенциально опасный материал, а реснички выталкивают этот материал вверх и из наших дыхательных путей. Когда мукоцилиарный эскалатор не работает должным образом, у нас может развиться заболевание легких. Например, у пациентов с генетическими заболеваниями, такими как муковисцидоз (МВ) и первичная цилиарная дискинезия (ПЦД), или заболеваниями, связанными с курением, такими как хроническая обструктивная болезнь легких (ХОБЛ), слизь очень густая.Эта слизь накапливается, позволяя бактериям, грибам и вирусам процветать, вызывая повреждение легких и снижение оксигенации. Заболевания легких чрезвычайно затрудняют дыхание, и пациенты могут иметь опасные для жизни респираторные заболевания, когда мукоцилиарный эскалатор не может поддерживать здоровье легких.
Как работают легкие?
Основная функция легких – дыхание. Газообмен – это название процесса, при котором кислород попадает в кровоток (при вдыхании), а углекислый газ покидает тело (при выдохе).Структура легких эволюционировала, чтобы выполнять эту задачу очень эффективно. Основная структура легких – это серия полых трубок, называемых дыхательными путями. Дыхательные пути разветвляются и уменьшаются в размерах, заканчиваясь крошечными воздушными мешочками, называемыми альвеолами. Альвеолы покрыты небольшими кровеносными сосудами, называемыми капиллярами, которые служат для обмена газов в крови [1]. Легкие можно сравнить с деревом, у которого большой главный ствол, а ветви становятся меньше по мере удаления от ствола. Альвеолы похожи на листья.
В легком есть две основные области: проводящая зона и респираторная зона (рис. 1). Воздух попадает в легкие через проводящую зону и попадает в респираторную зону, содержащую альвеолы. Альвеолы одного человека имеют такую же площадь поверхности, как и теннисный корт, а это большая площадь для газообмена. Проводящая зона – это часть легких, через которую проходит воздух без газообмена, потому что трубки слишком толстые, чтобы газы могли проходить через них.Проводящая зона выстлана похожими на волосы структурами, называемыми ресничками, которые покрыты слизью, которая помогает задерживать потенциально опасные материалы. Реснички – это подвижные крошечные пальцеобразные выступы на поверхности клеток дыхательных путей. Реснички выстилают дыхательные пути и помогают выводить слизь вверх и из легких [5]. Реснички имеют высоту около 6–7 микрометров, что примерно в десять раз меньше ширины человеческого волоса [3, 5].
- Рисунок 1. Мукоцилиарный эскалатор у здорового человека (слева) и у человека с больным мукоцилиарным эскалатором (справа).
- Мукоцилиарный эскалатор находится в трахее, бронхах и бронхиолах, которые являются частью проводящей зоны. Газообмен происходит в альвеолах дыхательной зоны (вставка).
Частицы и микробы в воздухе – зачем легким защита
Есть много типов частиц, которые могут попасть в легкие и вызвать повреждение. Некоторые из этих частиц являются загрязняющими веществами, такими как выбросы от транспортных средств, работающих на газе, окись углерода от каминов, токсины от вейпинга или курения, а также аэрозоли, такие как лак для волос.Частицы могут попадать в различные области легких. Короткие волосы, такие как волосы на макушке, выстилают ноздри изнутри и покрыты слизью. Эти покрытые слизью волосы помогают задерживать более крупные частицы, попадающие в нос. Частицы, попадающие в проводящую зону, могут повредить клетки дыхательных путей, что может уменьшить движение их ресничек и привести к накоплению слизи, которая не может быть удалена из дыхательных путей [2]. Забитые слизью дыхательные пути могут не позволить воздуху перемещаться так же эффективно, как листья в желобе, мешающие потоку воды.Иногда более мелкие частицы могут достигать альвеол. Повреждение альвеол значительно затрудняет дыхание, потому что кислород не проникает в кровь. Эта пониженная эффективность газообмена может привести к гипоксии остального тела, что означает низкое содержание кислорода. Только проводящая зона, от трахеи до бронхиол, имеет способность перемещать слизь с помощью ресничек, поэтому альвеолы не могут полагаться на этот механизм, чтобы избавиться от этих мелких частиц [3]. Жизнь в загрязненном городе или годы курения / курения могут вызвать воспаление легочной ткани и привести к таким заболеваниям, как хроническая обструктивная болезнь легких (ХОБЛ) [4].
Что такое мукоцилиарный эскалатор?
Мукоцилиарный эскалатор находится внутри проводящих дыхательных путей и состоит из слизи и ресничек, которые перемещают слизь вверх и из легких, откуда она может быть удалена при кашле или глотании (рис. 1, 2) [5]. Как первая линия защиты, слизь в дыхательных путях состоит из различных компонентов, которые помогают ей задерживать частицы и микробы [2, 4]. Слизь представляет собой физический барьер для защиты легких и обладает свойствами, помогающими избавиться от потенциально инфекционных бактерий, грибков и вирусов [4, 5].Некоторые из важных компонентов слизи дыхательных путей – это муцины (липкие белки с сахарным покрытием), защитные белки, соль и вода. Вместе эти компоненты образуют гель, который улавливает частицы, попадающие в дыхательные пути [2].
- Рис. 2. (Слева) Реснички в здоровых дыхательных путях подвижны и способны эффективно перемещать слизь вверх по мукоцилиарному эскалатору.
- (посередине). При МВ слизь становится густой и ее трудно перемещать, в результате чего мукоцилиарный эскалатор становится менее эффективным; это позволяет задерживать микробы / частицы, что в конечном итоге приводит к повреждению легких.(Справа) При PCD реснички менее подвижны или даже неподвижны, что делает их неспособными перемещать слизь вверх по мукоцилиарному эскалатору.
Слизь в основном вырабатывается клетками, выстилающими внутреннюю часть дыхательных путей. Они называются бокаловидными ячейками. Бокальные ячейки имеют форму средневековых чаш, отсюда и название кубок. В отличие от других клеток дыхательных путей, которые имеют ресничную форму и имеют форму столбиков, бокаловидные клетки не имеют наверху ресничек. Бокаловидные клетки отсутствуют за пределами проводящей зоны, чтобы слизь не мешала газообмену.Слизь также участвует в гидратации дыхательных путей, что необходимо для правильного функционирования ресничек [3, 5].
Движение ресничек подобно движению ваших рук при плавании брассом [3]. Отдельная ресничка недостаточно сильна, чтобы самостоятельно перемещать слой слизи, но когда тысячи ресничек скоординированно бьются вместе, они могут коллективно вызывать движение слизи [2, 3]. Представьте себе толпу на концерте, когда исполнитель ныряет со сцены, чтобы заняться серфингом: исполнитель подобен сгустку слизи, который удерживается руками толпы и движется скоординированной волной.В некотором смысле реснички взаимодействуют друг с другом посредством движения, чтобы обеспечить скоординированное и эффективное движение слизи! Так работает мукоцилиарный эскалатор.
Какие заболевания могут возникнуть, если мукоцилиарный эскалатор не работает должным образом?
Некоторые люди наследуют аномальные гены от своих родителей и рождаются с заболеванием, называемым первичной цилиарной дискинезией (ПЦД) (рис. 2). PCD – это заболевание легких, которое препятствует эффективному сокращению ресничек, а в тяжелых случаях вообще не дает им двигаться [3].У пациентов с PCD дыхательные пути инфицируются из-за неэффективного транспорта слизи, который повреждает клетки дыхательных путей. Когда со временем дыхательные пути повреждаются, они становятся вялыми, как сплющенная соломка, не позволяя воздуху проходить через них и затрудняя дыхание. Представьте, что вы пьете вкусный густой молочный коктейль; При использовании соломки нормальной ширины требуется меньше усилий по сравнению с соломкой шириной с лапшу для спагетти.
Муковисцидоз (МВ) – еще одно наследственное заболевание, поражающее мукоцилиарный эскалатор [3] (рис. 2).У людей с МВ есть мутации в обеих копиях гена (одна от мамы и одна от папы), ответственных за выработку белка, называемого регулятором трансмембранной проводимости при муковисцидозе (CFTR). CFTR образует канал через мембраны клеток, который участвует в производстве пота, пищеварительной жидкости и слизи. CFTR регулирует, сколько воды попадает в эти выделения и, следовательно, насколько густой и липкой становится слизь. При неправильной работе канала слизи не хватает воды и она становится густой, как клей.Чрезвычайно густая слизь накапливается в легких, в отличие от нормальной водянистой слизи, которая легко выводится мукоцилиарным эскалатором, вызывая накопление густой слизи и в конечном итоге вызывая разрушение дыхательных путей и легочную недостаточность.
Хроническая обструктивная болезнь легких (ХОБЛ) – это заболевание, которое может возникнуть после курения сигарет или электронных сигарет. ХОБЛ может негативно повлиять на мукоцилиарный эскалатор и вызвать заболевание легких, которое во многом похоже на МВ [3]. Повреждение мукоцилиарного эскалатора может способствовать развитию других распространенных заболеваний, таких как пневмония и астма, которые имеют схожие, но иногда менее серьезные проблемы со слизью.
Заключение: почему имеют значение слизь, реснички и мукоцилиарный эскалатор
Для здоровых легких требуется правильное функционирование мукоцилиарного эскалатора. Слизь и реснички являются основным механизмом защиты легких. Если есть проблема со слизью или ресничками, дыхательные пути могут быть заблокированы, и вредные микробы и частицы могут попасть в легкие, что приведет к повреждению. Генетические заболевания, такие как PCD и CF, и приобретенные заболевания, такие как COPD, негативно влияют на мукоцилиарный эскалатор.Эти заболевания легких могут привести к снижению газообмена и вызвать гипоксию всего тела. Так что помните – когда вы дома больны простудой, слизь, которую вы откашливаете, исходит от мукоцилиарного эскалатора, и она помогает сохранить ваши легкие счастливыми и здоровыми, удаляя потенциально опасные частицы и микробы!
Авторские взносы
MW, JP, JK, TB, SP, R-JS и SR внесли свой вклад в подготовку рукописи и окончательное редактирование. Все авторы одобрили окончательный вариант рукописи перед отправкой.
Глоссарий
Газообмен : ↑ Процесс, при котором отходы углекислого газа (CO 2 ) удаляются из кровотока и заменяются вдыхаемым кислородом (O 2 ).
Альвеолы : ↑ Воздушные мешочки, составляющие наименьшую часть респираторной зоны; альвеолы и капиллярные кровеносные сосуды находятся в непосредственной близости; здесь происходит газообмен.
Проводящая зона : ↑ Часть дыхательных путей, не участвующая в газообмене; цель зоны проводимости состоит в том, чтобы перемещать воздух в зону дыхания и из нее; где находится мукоцилиарный эскалатор; обнаруживается в проксимальном отделе легкого от трахеи до бронхиол.
Дыхательная зона : ↑ Часть дыхательных путей, в которой происходит газообмен; обнаруживается в дистальном отделе легкого, где расположены альвеолы.
Реснички : ↑ Подвижные волосовидные выступы на верхней части клеток, выстилающих проводящую зону дыхательных путей; реснички перемещают слизь по мукоцилиарному эскалатору.
Слизь : ↑ Липкое гелеобразное вещество, которое находится на вершине щеточки ресничек в проводящей зоне дыхательных путей; в легких слизь вырабатывается бокаловидными клетками и железами и защищает дыхательные пути от опасных материалов; слизь состоит из воды, гликопротеинов муцина, защитных белков и соли.
Мукоцилиарный эскалатор : ↑ Срок для аппарата слизи и ресничек; отвечает за движение слизи вверх и из дыхательных путей; слизь улавливает частицы, а реснички выталкивают слизь вверх и из легких.
Заявление о конфликте интересов
SR имеет нелицензированный патент на использование микрооптической когерентной томографии в качестве диагностического устройства, которое используется для характеристики функциональной микроанатомии мукоцилиарного эскалатора.
Остальные авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Авторы хотели бы поблагодарить Джорджа Д. Филлипса (13 лет), С. Коринн Филлипс (16 лет) и Эндрю Роу (14 лет) за чтение рукописи и их вдумчивые правки и отзывы. Джереми Левер и Бэзил Боно за неоценимую поддержку в завершении этого проекта.
Список литературы
[1] ↑ West, J. B. 2012. West’s Respiratory Physiology: The Essentials . 9-е изд. Балтимор, Мэриленд: Липпинкотт Уильямс и Уилкинс.
[2] ↑ Ноулз М. Р. и Баучер Р. С. 2002. Очистка от слизи как основной врожденный механизм защиты дыхательных путей млекопитающих. J. Clin. Вкладывать деньги. 109: 571–7. DOI: 10.1172 / jci15217
[3] ↑ Пибоди, Дж. Э., Шей, Р. Дж., Бермингем, Б. М., Филлипс, С. Е., Тернер, Б., Роу, С. М. и др. 2018. Видение ресничек: методы визуализации движения ресничек и клинических связей. Am. J. Physiol. Легочная клетка. Мол. Physiol. 314: L909–21.DOI: 10.1152 / ajplung.00556.2017
[4] ↑ Чжан П., Саммер В. Р., Бэгби Г. Дж. И Нельсон С. 2000. Врожденный иммунитет и легочная защита хозяина. Immunol. Rev. 173: 39–51. DOI: 10.1034 / j.1600-065X.2000.917306.x
[5] ↑ Бустаманте-Марин, X. М., и Островски, Л. Е. 2017. Реснички и мукоцилиарный клиренс.
