УЗИ вилочковой железы у детей: диагностика и норма
Вилочковая железа: что это такое? Этот орган важен для обеспечения правильной работы всего организма и находится в груди. Нарушиться работа железы может при наличии разных заболеваний у человека, что негативно скажется на иммунитете.
В результате этого у человека снижается иммунитет, и он становится подвержен вирусным заболеваниям. Все нарушения в работе железы можно определить при помощи проведения УЗИ. После получения результата такого тестирования врач ставит диагноз и назначает терапию.
Строение железы
Тимус принадлежит к ЖВС и располагается в груди. Состоит он из двух частей, которые могут отличаться по своим габаритам. Соединяются между собой доли при помощи мышечных тканей.
Роль данной железы состоит в том, что она способствует производству гормонов, принимающей участие в работе иммунитета, а также способствует образованию антител, которые помогают убивать микробов. Также задача железы состоит и в том, чтобы контролировать количество и распределение кровяных телец.
При ультразвуковом тестировании органов, в том числе и вилочковой железы, врач может увидеть состояние секрета, определить в нем патологии у ребенка. Этот способ тестирования также позволяет оценить общее развитие и работу органа у ребёнка.
УЗИ вилочковой железы у детей, как метод точной диагностики
Врачи отмечают, что узи вилочковой железы является на сегодня наиболее информативным и точным методом тестирования. При помощи него может быть выявлена норма структуры тканей или отклонения от нее в органе. Назначен такой метод диагностирования может быть в любом возрасте независимо от пола больного.
При помощи УЗИ врач может определить состояние таких органов:
- Почек.
- Мозга.
- Миокарда.
- Органов ЖКТ.
- Щитовидки и прочих.
УЗИ тимуса у детей дает возможность определить размер органа, что позволяет специалисту выяснить нарушения и отклонения от нормы.
Показания
Не каждый малыш может проходить такое обследование. Для этого у него должны быть определенные показания, а потому врач перед исследованием должен провести тщательный осмотр ребенка.
Для этого у него должны быть определенные показания, а потому врач перед исследованием должен провести тщательный осмотр ребенка.
Если ребенку не исполнилось года, то показанием для процедуры может стать:
- Дисбактериоз.
- Диатез.
- Нарушения иммунитета.
После одного года ребенку могут провести такое исследование при:
- Простудном заболевании тяжелой формы.
- Увеличении лимфатических узлов.
- Аллергических проявлениях в острой форме.
- При неприятной симптоматике в груди.
Достоинства тестирования
У такого метода диагностирования есть много преимуществ. Среди таких выделяют следующие:
- Не облучается организм радиацией.
- Нет надобности использовать красители.
- Приемлемая стоимость процедуры.
- Быстрые результаты обследования.
При этом отмечается, что противопоказаний к данной процедуре не существует. Иногда человек при диагностировании может ощущать холод. Но тут нет ничего страшного, так как давление на организм может оказывать датчик ультразвука.
Но тут нет ничего страшного, так как давление на организм может оказывать датчик ультразвука.
Также могут возникать у пациента неприятные ощущения при процедуре, когда у него повышенная чувствительность эпидермиса. Но для здоровья в целом УЗИ не представляет опасности.
Подготовка
УЗИ вилочковой железы проводится в определенное время, которое назначает доктор. Человеку для проведения такой процедуры не требуется подготовка. Но нужно учесть некоторые моменты, а именно при назначении процедуры малышу, он в это время должен быть спокойным, так как это может повлиять на точность результатов.
Мать в это время должна успокоить ребенка. Для этого можно использовать игрушки или применять другие методы.
Также важно на тестирование одевать одежду. Которую можно быстро снять или расстегнуть. С собой надо взять полотенце, чтобы вытирать смазку.
Проведение процедуры
УЗИ проводится при использовании специального агрегата, который излучает ультразвуковые волны. Чтобы проверить состояние органа, датчик от аппарата размещают напротив него.
Чтобы проверить состояние органа, датчик от аппарата размещают напротив него.
При такой процедуре можно определить общее состояние органа, оценить его размеры и степень поражения недугом. Обычно на проведение такого обследования понадобиться не более 10 минут.
УЗИ новорожденным
Вилочковая железа у плода начинает формироваться с первых дней после беременности. В конце срока обычно такой орган полностью сформирован. Работать он начинает в теле малыша еще до его появления из утробы матери.
Сразу после рождения определенным категориям малышей может проводиться УЗИ тимуса для выявления патологий. Это может делаться в том случае, когда беременность протекала с определенными осложнениями.
Показания для новорожденных
Иногда при проведении обследования ребенка при помощи других методов, врач может заметить определенные патологии, например, тимус не соответствует норме по размерам. При таком диагнозе для его подтверждения потребуется сделать УЗИ.
Также тестирование назначают, когда происходят сбои в работе иммунитета. Это может быть большая температура при отсутствии признаков какого-либо заболевания. При помощи УЗИ определяется, что вызвало такую патологию.
Это может быть большая температура при отсутствии признаков какого-либо заболевания. При помощи УЗИ определяется, что вызвало такую патологию.
Особенности тестирования
Новорожденного при проведении теста надо положить на кушетку и под голову подложить валик. Когда ребенку больше 5 лет, то обследование проводится в положении стоя. Когда малыш нервничает, надо матери взять его на руки, чтобы лицом он был расположен к доктору.
Нормы тестирования
В здорового человека железа имеет среднюю эхогенность. Края органа ровные, а его структура однородная. Также на железе должно быть ограниченное количество тканей иных структур.
При тестировании определяются габариты органа. Для расчета показателей врач использует формулы. Полученный индекс он сравнивает с данными из таблицы. После этого делает заключение.
Нормы показателей и отклонений
У ребенка такая патология может быть диагностирована на фоне снижения иммунитета. У взрослого патология обычно выявляется случайно при проведении обследования других органов.
При тестировании орган в норме имеет небольшие размеры. Когда человек взрослеет, то на железе могут откладываться другие ткани. После 55 лет уже нельзя рассмотреть железу при проведении УЗИ. Это считается нормой.
Патологии
При нарушении в работе тимуса могут возникать и другие патологии. Самой опасной из них является тимомегалия. Ученым на сегодняшний день не известно до конца, почему такое осложнение может возникать у людей. Предполагается, что на это могут влиять внешние факторы: неправильное питание, травмы или недоразвитие плода.
Тимомегалия может проявляться такими симптомами:
- Продолжительными инфекционными заболеваниями, так как организм не сможет эффективно бороться с ними из-за нарушения иммунитета.
- Кашлем и одышкой.
- Уменьшением аппетита.
Врачам довольно сложно диагностировать тимомелагию, так как этому при УЗИ будут препятствовать другие ткани. Тем не менее, такое тестирование обычно назначается.
Когда врач выявляет увеличение органа, то он может диагностировать тимомелагию.
При УЗИ врачи могут выявлять опухоли на железе. Такие образования достаточно хорошо видно на экране, но для получения более точной картины, для определения типа опухоли обычно используется КТ.
Последствия обследования
Когда у пациента будет обнаружено незначительное увеличение железы, то лечение ему не назначается. Для предотвращения развития патологии больной должен правильно питаться и избегать стрессов. Ребенок на первых порах после рождения должен питаться молоком матери.
Когда орган будет увеличен достаточно сильно, то назначается прием медикаментов. Это витамины, иммуномодуляторы и гистаминные средства. Когда увеличенные размеры железы будут влиять на развитие других тканей и сдавливать их, то могут быть назначены гормоны или операция.
Заключение
Врачи говорят, что обследование железы можно проводить при помощи разных методов тестирования. Это может быть КТ или рентген. Но самый информативный и безопасный из них – УЗИ. Врач может при таком обследовании визуально рассмотреть орган и патологии на нем.
Это может быть КТ или рентген. Но самый информативный и безопасный из них – УЗИ. Врач может при таком обследовании визуально рассмотреть орган и патологии на нем.
На основании сказанного можно сделать вывод, что вилочковая железа играет важную роль в обеспечения жизнедеятельности человека, а потому за ее состоянием надо постоянно наблюдать, так как нарушения в работе органа могут стать причинами ухудшения здоровья в целом.
Для этого надо регулярно посещать врача и проводить у него полное обследование. При необходимости стоит незамедлительно осуществлять терапию, что поможет избежать осложнений и проявления иных патологий.
УЗИ тимуса у детей – что это такое фото и видео
Тимус или вилочковая железа – центральный орган иммунной системы, расположенный в верхней части грудной клетки. Именно в нем происходит созревание и развитие клеток иммунной системы (т-лимфоцитов). Состоит из двух долей, очень плотно прилегающих друг к другу, иногда сращенных. Нижние части обеих долей широкие, а верхние узкие – поэтому орган напоминает двузубую вилку, отсюда и произошло его название. Тимус растет и формируется до наступления периода полового созревания, потом начинает уменьшаться в размерах, и к преклонному возрасту весит всего 6-7 граммов.
Состоит из двух долей, очень плотно прилегающих друг к другу, иногда сращенных. Нижние части обеих долей широкие, а верхние узкие – поэтому орган напоминает двузубую вилку, отсюда и произошло его название. Тимус растет и формируется до наступления периода полового созревания, потом начинает уменьшаться в размерах, и к преклонному возрасту весит всего 6-7 граммов.
Вилочковая железа отвечает за выработку таких гормонов как тимозин, тимпоэтин, тималин, инсулиноподобный фактор роста – 1.
Главная функция – иммунная защита.
Поскольку она активна в детском возрасте, обследование этого органа назначают младенцам в качестве плановой процедуры, а деткам постарше – в профилактических целях или при жалобах на снижение иммунитета.
До недавнего времени самым полным методом обследования считался рентген грудной клетки. Но на сегодняшний день самым информативным и безопасным способом исследования этого органа является УЗИ. Обычно его назначают в сочетании с анализами крови и мочи. Именно УЗИ позволяет отметить индивидуальные особенности органа у детей, а также в полной мере оценить ее структуру.
Именно УЗИ позволяет отметить индивидуальные особенности органа у детей, а также в полной мере оценить ее структуру.
Показания к проведению обследования
- избыточный вес у ребенка в сочетании с малой подвижностью и раздражительностью;
- подверженность респираторным инфекциям;
- потливость, бледность, проявления сосудистого рисунка в области грудной клетки, мраморность;
- повышение температуры тела до субфебрильной (37,0 – 37,3) без явных причин;
- продолжительный кашель, лечение которого проходит неэффективно; одышка;
- увеличение лимфатических узлов и аденоидов;
- частые дерматиты и аллергические реакции.
УЗИ тимуса входит в комплекс УЗИ деток до года вместе с нейросонографией, УЗИ почек, надпочечников, брюшной полости и ТБС.
Что выявляет УЗИ тимуса у детей?
В первую очередь врач оценивает размеры железы. Для этого перед проведением исследования малыша могут поставить на весы – чтобы определить массу тела и сопоставить ее с размерами и весом органа. В норме вес органа у детей должен составлять до 0,3% от массы тела. При значениях веса сверх нормы врач может указать в заключении диагноз «тимомегалия».
В норме вес органа у детей должен составлять до 0,3% от массы тела. При значениях веса сверх нормы врач может указать в заключении диагноз «тимомегалия».
Кроме того, на УЗИ определяется структура органа – она должна быть в норме однородной и эхогенной.
УЗИ тимуса у детей не требует специальной подготовки. Детям в возрасте до 9 месяцев обследование проводят в положении лежа, от 9 месяцев и до полутора лет – в положении сидя, после полутора – стоя.
Основные заболевания и патологии тимуса:
- синдром увеличенной вилочковой железы;
- тимомегалия – выраженное увеличение железы;
- Т-клеточная лимфома;
- тимома;
- миастения;
- синдром MEDAC и др.
Самая часто встречающаяся патология тимуса – его увеличение или тимомегалия.
Что такое тимомегалия и нужно ли ее лечить?
Для начала нужно признать, что до конца механизмы работы не изучены. Ученые выдвигают гипотезы, но с течением времени сами их и опровергают.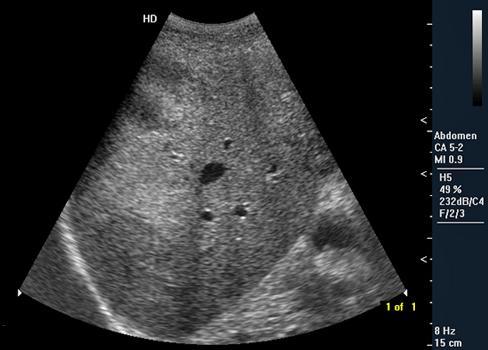
Однако как показывают исследования, у большинства детей тимус приходит в норму к шести годам без дополнительного лечения. В норме после 12 лет тимус на УЗИ не определяется.
Почему же важно знать о том, есть у ребенка тимомегалия или нет. Дело в том, что малыша с такой патологией нужно больше беречь от различных инфекционных болезней, избегать вместе с ним скоплений людей в период сезонных вспышек заболеваний. Деток нельзя закаливать популярными способами типа обливаний или стояния босыми ногами на снегу, а также их нужно беречь от стрессов и нервного перенапряжения.
Однако важно помнить, что даже на кратковременную простуду тимус может ответить изменением (увеличением) размеров.
Тимус – что это? Роль тимуса на первому году жизни ребенка
Тимус (вилочковая железа) – важный орган иммунной системы детей. Он расположен в верхнем отделе грудной клетки и состоит из двух долей, соединяющихся в передней части трахеи. Железа растет до наступления половой зрелости, достигая массы 30–40 грамм, затем постепенно уменьшается (обратное развитие).
Она играет доминирующую роль в иммунной, эндокринной системе. Тимус продуцирует тимозин, тимопоэтин, стимулирующие выработку антител, а также производит Т-лимфоциты – белые клетки крови, уничтожающие аномальные клетки с чужеродными антигенами. Другая функция вилочковой железы – предотвращение патологического роста клеток и предупреждение рака. Следует отметить, что тимус играет ведущую роль в иммунитете ребенка до трех лет.
Тимус продуцирует тимозин, тимопоэтин, стимулирующие выработку антител, а также производит Т-лимфоциты – белые клетки крови, уничтожающие аномальные клетки с чужеродными антигенами. Другая функция вилочковой железы – предотвращение патологического роста клеток и предупреждение рака. Следует отметить, что тимус играет ведущую роль в иммунитете ребенка до трех лет.
Роль тимуса в жизни ребёнка
До рождения и в детстве тимус ответственен за производство плюс созревание Т-лимфоцитов, защищающих организм от определенных угроз, включая вирусы, бактерии. Тимус является крупнейшим лимфоидным органом у новорожденных, так как активнее других тканей продуцирует лимфоциты. Железа выступает «первой скрипкой» в развитии и улучшении иммунной системы ребенка.
Тимус производит и секретирует тимозин – гормон, необходимый для выработки Т-клеток. После «созревания» в железе они поступают в кровь и мигрируют в лимфоузлы и селезенку, где помогают иммунной системе бороться с болезнью.
В некоторых случаях функции вилочковой железы снижены, что ослабляет иммунную систему, увеличивая склонность к инфекциям и аллергии. Ребенок страдает затяжными ОРВИ, патология легко переходит в хроническую. Недостаток Т-лимфоцитов в организме может привести к иммунодефицитным заболеваниям, характеризующимися сильной потливостью, отечностью и/или болезненностью горла, припухлостью лимфатических узлов, депрессией.
Недоедание и дефицит белка в раннем возрасте обусловливает медленный или ограниченный рост тимуса, «подрывая» тем самым нормальное функционирование лимфоцитов. Вот почему важно сбалансированное питание с достаточным количеством белка.
Доктора данного направления
Патология тимуса
Основные виды патологии тимуса:
- Аплазия – отсутствие или недоразвитие вилочковой железы
- Гипо- и дисплазия – недоразвитие тимуса
- Акцидентальная инволюция – уменьшение вилочковой железы, под влиянием гормонального дисбаланса, стресса, инфекции
- Атрофия – уменьшение, замещение железистой ткани соединительной, прекращение функционирования
- Тимомегалия – увеличение массы и объема паренхимы вилочковой железы выше возрастной нормы при сохранении ее нормального строения
- Гиперплазия – увеличение железистой ткани, с нарушением выработки иммунных клеток и функционирования тимуса.

- Тимома – опухоль вилочковой железы.
- Киста тимуса – жидкостное образование вилочковой железы.
- Патология тимуса (вилочковой железы) может вызывать: развитие ряда иммунодефицитных синдромов, аутоиммунных заболеваний и некоторых эндокринных нарушений.
Увеличение тимуса у детей
Отклонение в размере тимуса в большую сторону и снижение его функции обозначают термином «синдром увеличенной вилочковой железы» (СУВЖ) у детей. Проблему увеличенного тимуса чаще рассматривают в свете дифференциальной диагностики с плевритом, перикардитом, опухолями средостения, другими патологиями.
Ошибочно считают, что увеличенный тимус у детей грудного или раннего возраста является физиологическим состоянием. Особенности протекания инфекционных заболеваний у маленьких пациентов с СУВЖ заставляют классифицировать синдром, как патологию. Дети с СУВЖ имеют большую вероятность развития дисбаланса нейроэндокринной плюс иммунной систем. Поэтому пациенты с выявленным увеличением тимуса требуют полного обследования и диспансерного наблюдения у эндокринолога, иммунолога.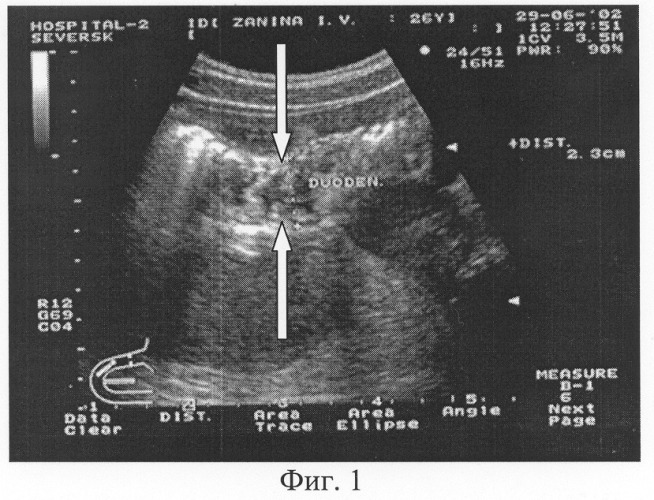
Симптомы заболевания или нарушения развития вилочкой железы
Для того, что бы вовремя выявить патологию тимуса, родителям стоит обратить внимание на отклонения, имеющие различную степень выраженности, которые могут свидетельствовать о заболевании или нарушении развития вилочковой железы:
- Частая заболеваемость ребенка простудными заболеваниями.
- Затяжное течение различных заболеваний, с частыми осложнениями.
- Увеличение лимфоидной ткани – лимфатических узлов, миндалин, аденоидов, ткани на задней поверхности глотки.
- Бледность и/или мраморный рисунок на коже ребёнка.
- Большой вес ребёнка при рождении.
- Ребёнок быстро теряет и быстро набирает вес.
- Кашель вне простудного заболевания, который усиливается в положении ребёнка горизонтально.
- Потливость, субфебрильная температура длительное время вне простудных заболеваний.
- Гипергидроз, холодные конечности.
- Видимая венозная сеточка на груди малыша.

- Цианоз (посинение) носогубного треугольника при нагрузках (плач, бег)
- Частые срыгивания, икоты, отрыжки
- Одышка
- Нарушение сердечного ритма
При возникновении подозрений на патологию тимуса, врач может назначить дополнительные методы обследования:
- УЗИ вилочковой железы,
- КТ,
- МРТ,
- рентген,
- общий анализ крови,
- иммунограмму,
- биохимический анализ крови,
- кровь на гормоны.
Тимическая недостаточность поддается иммунокорекции, которая индивидуально подбирается врачом аллергологом-иммунологом. Стоит обратить внимание, что своевременная диагностика патологии вилочковой железы особенно актуальна на первом году жизни ребенка, когда ребенку начинают проводить вакцинацию.
Для получения подробных консультаций о роли тимуса в жизни ребёнка на первом году жизни обращайтесь к педиатрам медицинских центров «Президент-Мед»
Автор: Лаврова Нина Авенировна
Заместитель генерального директора по медицинской части
Окончила Ярославский государственный медицинский институт по специальности «Лечебное дело»
Медицинский опыт работы – 25 лет
Записаться к врачу
Вилочковая железа увеличена у ребенка: что это значит и стоит ли беспокоиться
Иммунитет ребенка начинает свое формирование еще задолго до рождения в период внутриутробного развития. На 6 неделе беременности у плода уже появляется тимус главный орган иммуногенеза. По форме он схож с вилкой, поэтому ему дали второе название вилочковая железа.
На 6 неделе беременности у плода уже появляется тимус главный орган иммуногенеза. По форме он схож с вилкой, поэтому ему дали второе название вилочковая железа.
Чем младше ребенок, тем больше он подвергается различным заболеваниям. Иммунная система интенсивнее включается в процесс борьбы с вирусами и тимус работает более интенсивно. Это вызывает его соответствующий рост. В норме к 12 годам рост ВЖ притормаживается, иммунную систему можно считать уже сформированной. Если у ребенка наблюдается увеличение тимуса, значит, его иммунная система испытывает усиленные нагрузки, поэтому требуется тщательное обследование ребенка, чтобы выяснить причины патологического состояния.
Функции вилочковой железы
Где находится вилочковая железа и за что она отвечает? Тимус это орган, расположенный в передней части грудины и непосредственно участвующий в формировании иммунной системы человека. Он начинает функционировать уже в эмбриональном периоде. Максимум своего развития тимус достигает в первый год жизни, тогда же защищая хрупкий организм от воздействия различных патогенных факторов. Вилочковая железа может увеличиваться определенное время, что считается физиологической нормой. В норме, к 5-летнему возрасту орган должен прекратить свой рост.
Вилочковая железа может увеличиваться определенное время, что считается физиологической нормой. В норме, к 5-летнему возрасту орган должен прекратить свой рост.
Главная функция тимуса обучать Т-лимфоциты убирать инородные агенты, попадающие в организм (бактерии, вирусы, грибки, аллергены) и обеззараживать их. До определенного возраста железа усиленно работает, формирует иммунитет ребенка. После этого надобность в ней отпадает и она постепенно атрофируется. Тимомегалия может существенно повлиять на функциональность тимуса. Очень важно знать все предпосылки разрастания тимуса, чтобы своевременно предотвратить развитие этого процесса или правильно провести лечение.
Пpичины увeличeния ВЖ у детей
У ребенка тимус не должен быть выше КТТИ 0,33 (кардиотимикоторакальный индекс). Если показатель выше, диагностируют тимомегалию.
Гипертрофия КТТИ тимуса бывает 3 степеней:
- 0,33-0,37,
- 0,37-0,42,
- больше 0,42.
Как внутренние, так и внешние факторы сказываются на работе органов ребенка, включая вилочковую железу. Проблемы с тимусом носят чаще всего наследственный характер и относятся к эндокринным. Проявляются они в привычных для многих и часто повторяющихся ОРВИ, заболеваниям ЛОР органов. Но, в то же время, частые инфекционные заболевания могут быть связаны с нарушениями в самой вилочковой железе. Если работа тимуса нарушена, орган не помогает организму справляться с нашествием инфекционных агентов, иммунная система страдает.
Проблемы с тимусом носят чаще всего наследственный характер и относятся к эндокринным. Проявляются они в привычных для многих и часто повторяющихся ОРВИ, заболеваниям ЛОР органов. Но, в то же время, частые инфекционные заболевания могут быть связаны с нарушениями в самой вилочковой железе. Если работа тимуса нарушена, орган не помогает организму справляться с нашествием инфекционных агентов, иммунная система страдает.
Узнайте о симптомах эндокринной офтальмопатии и о лечении аутоиммунной патологии щитовидной железы.Чем и как лечить кисту яичника при беременности на ранних сроках? Действенные варианты терапии собраны в этой статье.
Точные причины увеличения вилочковой железы (тимомегалии) еще не изучены. Специалисты выделяют несколько вероятных факторов развития патологического состояния:
- инфекции у женщины в период беременности,
- злоупотребление наркотиками и алкоголем беременной,
- воздействие радиационного облучения на плод,
- преждевременные роды,
- прием антибиотиков в период гестации,
- разные резус-факторы у матери и ребенка,
- чрезмерные стресс во время беременности,
- склонность у аллергии у грудничков,
- недостаточность питательных веществ в рационе ребенка,
- поздняя беременность,
- родовые травмы.

Если увеличение вилочковой железы выявляется у детей старшего возраста, она может быть спровоцирована:
- дефицитом белковой пищи,
- снижением уровня лейкоцитов,
- лимфатическом диатезе,
- воспалительными процессами,
- склонностью к аллергии.
Симптоматика
У маленьких детей родители могут распознать увеличение ВЖ по определенным признакам:
- резкие скачки веса (как увеличение, так и снижение),
- повышенная потливость,
- нарушение сердечного ритма,
- синюшность кожи во время плача,
- частые ОРВИ,
- склонность к регулярным дерматитам и аллергическим реакциям,
- мраморный оттенок кожи, ее бледность,
- увеличение аденоидов и миндалин.
Важно! При увеличении тимуса у детей категорически запрещено принимать Аспирин (ацетилсалициловую кислоту). Лекарственный препарат может стать пусковым механизмом развития астмы.
Диагностика
При подозрении на тимомегалию ребенка необходимо комплексно обследовать. Сначала назначается УЗИ вилочковой железы. Исследование определяет размеры органа, его состояние. Также УЗИ помогает рассчитать КТТИ. Измеряются расширения и размеры тени тимуса в районах верхней, cpeдней, нижней трети грудины. Согласно показателю индекса определяют степень увеличения железы.
Если УЗИ не дает полной картины патологии или ее опровержения, проводится рентген грудной клетки в прямой проекции. Он дает возможность подробно описать структуру вилочковой железы, несоответствие ее размеров норме. Структуру тканей тимуса определяют с помощью КТ. Дополнительно у ребенка берут общий анализ крови и мочи, назначают иммунограмму.
Методы лечения
Тимомегалия у ребенка в редких случаях требует серьезного медицинского вмешательства. К 5-6 годам размеры органа должны прийти в физиологическую норму. Если гиперплазия вилочковой железы несущественная, медикаментозная терапия не назначается. Если это груднички, то им рекомендуется как можно дольше поддерживать грудное вскармливание. Более старшим детям рекомендуется обогащать рацион продуктами, способствующими укреплению иммунитета (шиповник, смородина, цитрусы).
Если это груднички, то им рекомендуется как можно дольше поддерживать грудное вскармливание. Более старшим детям рекомендуется обогащать рацион продуктами, способствующими укреплению иммунитета (шиповник, смородина, цитрусы).
При 3 степени тимомегалии требуется лечение. Схему терапии врач подбирает, исходя из возраста больного, состояние иммунной системы, степени тяжести патологии. Таким детям делают отвод от вакцинации на определенное время (исключение прививка от полиомиелита). Если состояние ребенка ухудшается, возникает надпочечниковая недостаточность, появляется дефицит синтеза кортикостероидов, назначается прием их синтетических аналогов. Дозировку врач определяет индивидуально.
Узнайте о вреде и пользе фруктозы для диабетиков, а также об особенностях употребления сахарозаменителя.О первых признаках проблем с поджелудочной железой и о лечении заболеваний органа написано на этой странице.
Перейдите по адресу https://fr-dc.ru/zabolevaniya/diabet/retinopatiya.
html и прочтите о том, что такое диабетическая ретинопатия и как лечить осложнение эндокринной патологии.
Рекомендуется применение адаптогенов:
- лимонник,
- женьшень.
Очень важно проводить профилактические мероприятия по защите от вирусных инфекций, обеспечить правильное питание, адекватные физические нагрузки, прогулки на свежем воздухе все это стимуляторы укрепления защитных сил организма.
Вилочковая железа может усиленно расти в первые годы жизни малыша, что является свидетельством ее активной работы в борьбе с патогенными факторами. В норме ее рост должен прекратиться к 5-6 годам. В любом случае выявление тимомегалии должно быть под пристальным вниманием специалистов. Существенная гиперплазия тимуса сигнализирует о неполадках в иммунной системе ребенка, требует более тщательной диагностики и коррекции состояния.
В следующем видео доктор Комаровский доступно расскажет, что такое вилочковая железа (тимус) и для чего она нужна в организме человека, а также проинструктирует, что делать, если врач говорит об увеличенном тимусе у ребенка:
youtube.com/embed/8toE1MGRKUQ” frameborder=”0″ allowfullscreen=”allowfullscreen”/>узи вилочковой железы у детей — 25 рекомендаций на Babyblog.ru
Процесс оплодотворения происходит в верхней части маточной трубы. Движение оплодотворенной яйцеклетки в полость матки продолжается трое суток. Еще трое суток зародыш «идет» до места имплантации уже в полости матки. Первые шесть дней зародыш как бы не связан с матерью, он питается за счет веществ, накопленных в яйцеклетке. Седьмой день беременности является одним из самых критических. Имплантация происходит путем растворения ферментами трофобласта слизистой оболочки матки, с этого момента питание эмбриона осуществляется за счет белков и гликогена материнского организма.
3–4-я недели. Организм женщины побуждается к перестройке. Появляются ранние признаки наступившей беременности: лабильность психики, тошнота по утрам, учащенное мочеиспускание, болезненность молочных желез… На этом сроке идет закладка органов и систем будущего ребенка. У эмбриона уже бьется сердце. На 21-й день после зачатия формируется головной и спинной мозг. К концу первого месяца устанавливается циркуляция эмбриональной крови, сформировалась пуповина. Появились глазные впадины, зачатки рук и ног. Эмбрион напоминает маленькую ушную раковину размером 4 мм, окруженную небольшим количеством околоплодных вод.
У эмбриона уже бьется сердце. На 21-й день после зачатия формируется головной и спинной мозг. К концу первого месяца устанавливается циркуляция эмбриональной крови, сформировалась пуповина. Появились глазные впадины, зачатки рук и ног. Эмбрион напоминает маленькую ушную раковину размером 4 мм, окруженную небольшим количеством околоплодных вод.
5–6-я недели. На этом сроке женщина уже не сомневается, что беременна. Усиливаются тошнота, рвота, потливость, бывают обморочные состояния. Матка начинает интенсивно расти, что позволяет врачу точно определить срок беременности. В 5 недель начинается образование эритроцитарных антигенов, которые определяют группу крови плода. На 6-й неделе у ребенка продолжается формирование конечностей, уже образовалась вилочковая железа – тимус, важнейший орган иммунной системы. Продолжается формирование лица: глаз, носа, верхней и нижней челюсти.
7–8-я недели. С cеми недель начинается спад гормональной продукции желтого тела, его функцию берет на себя развивающаяся плацента. Это один из самых сложных периодов; если формирование плаценты было нарушено на ранних этапах (пороки развития матки, аборты, воспалительные заболевания половых органов, перенесенные в эти недели инфекционные заболевания – ОРВИ и т.п.), есть опасность самопроизвольного прерывания беременности. На этом этапе сердце эмбриона становится четырехкамерным, формируются крупные кровеносные сосуды. В печени уже появились желчные протоки. Сформировались ушные раковины, на конечностях появились пальчики. Эмбрион уже двигается, но он слишком мал, чтобы мать почувствовала его движение. На 8-й неделе под влиянием У-хромосомы происходит формирование мужских гонад.
Это один из самых сложных периодов; если формирование плаценты было нарушено на ранних этапах (пороки развития матки, аборты, воспалительные заболевания половых органов, перенесенные в эти недели инфекционные заболевания – ОРВИ и т.п.), есть опасность самопроизвольного прерывания беременности. На этом этапе сердце эмбриона становится четырехкамерным, формируются крупные кровеносные сосуды. В печени уже появились желчные протоки. Сформировались ушные раковины, на конечностях появились пальчики. Эмбрион уже двигается, но он слишком мал, чтобы мать почувствовала его движение. На 8-й неделе под влиянием У-хромосомы происходит формирование мужских гонад.
9–10-я недели. Плацента берет на себя функцию управления обменом веществ материнского организма, приспосабливая его к нуждам развивающегося плода. В этот период субъективные симптомы беременности могут принимать более тяжелый характер, и развивается токсикоз первой половины беременности. Сахарный диабет может дебютировать именно в это время беременности, и женщинам с отягощенной наследственностью надо быть особенно внимательными к своему состоянию. Страдающим сахарным диабетом нужн заново подбирать дозу препаратов. А плод тем временем уже научился… глотать! На 1 неделе заканчивается развитие полости рта, кишечника, желчных протоков. Полушария мозг уже сформированы, и начинается развитие мозжечка.
Страдающим сахарным диабетом нужн заново подбирать дозу препаратов. А плод тем временем уже научился… глотать! На 1 неделе заканчивается развитие полости рта, кишечника, желчных протоков. Полушария мозг уже сформированы, и начинается развитие мозжечка.
11–12-я недели. Завершается первый триместр. К этому времени исчезают тошнота, рвота, слюнотечение. Женщина обычно отмечает, что грудь стала тяжелой, но прикосновение к ней перестало быть болезненным. Дно матки определяется над лоном, она имеет размер женского кулака. В 12 недель истекает последний срок, когда беременность можно прервать по желанию женщины. Может, от этого шага кого-то удержит известие, что будущий ребенок уже начинает свое эмоциональное развитие. Удалось заснять состояние плода в момент произведения аборта: он пятился от инструментов, и его лицо искажала гримаса ужаса…
13–14-я недели. По внешнему виду плод напоминает маленького человека. Конечно, не все взаимосвязи сформированы, но уже все на своих местах. Этот срок опасен для женщин с дисфункцией коры надпочечников, если они носят мальчика: беременность может прерваться. Следует проверить уровень 17КС в моче для подбора адекватной терапии.
Этот срок опасен для женщин с дисфункцией коры надпочечников, если они носят мальчика: беременность может прерваться. Следует проверить уровень 17КС в моче для подбора адекватной терапии.
15–16-я недели. Закончился эмбриогенез и формирование плаценты. Определив уровень эстриола в моче, можно оценить работу системы «плацента – плод». В этот период проведение амниоцентеза наиболее безопасно, т.к. матка обычно инертна.
17–18-я недели. Повторнородящие ощущают первые шевеления плода. У него к этому времени заканчивается формирование собственной иммунной системы. Он способен синтезировать интерферон и иммуноглобулины.
19–20-я недели. Завершается первая половина беременности. В организме женщины произошли большие изменения: сердечный выброс увеличился на 40%, немного повысилось артериальное давление, объем циркулирующей крови увеличился на 500 мл (а к концу беременности – на 1000 мл), СОЭ может достигать 20 мм/ч. Растущая матка, придавливая мочевой пузырь и устья мочеточников, может нарушать пассаж мочи (что грозит развитием пиелонефрита), вызывать частые болезненные мочеиспускания. На этом сроке масса плода – 300–350 г, он научился сосать и глотает околоплодные воды. У него чуть-чуть приоткрываются глаза!
На этом сроке масса плода – 300–350 г, он научился сосать и глотает околоплодные воды. У него чуть-чуть приоткрываются глаза!
21–22-я недели. Плод имеет массу 400–450 г. И у него быстрыми темпами развиваются мышцы и костная система, для чего необходим кальций. Если женщина не хочет лишиться белозубой улыбки, ей надо принимать препараты кальция или внести изменения в рацион.
23–24-я недели. Масса плода составляет 500–600 г, он считается жизнеспособным, хотя его легкие только начинают созревать. Матка начинает «подготовку к родам»: появляются схватки Брестона–Хикса. Они мало болезненны и могут продолжаться 1–2 мин до 10–15 раз в день. Это не предвещает скорых родов и не должно вызывать опасений, если схватки не приобретают интенсивность и регулярность.
25–26-я недели. Плод уже весит 700–750 г. Совершенствуется эндокринная система. А маме самое время начинать готовить грудь к будущему кормлению.
27–28-я недели. Завершается второй триместр. К этому моменту плод весит до 1000 г и имеет длину до 35 см. Его движения становятся более активными. При УЗИ видно, что он уже умеет сосать палец и даже улыбаться! Дно матки стоит на высоте 27–28 см над лоном, матка «подпирает» диафрагму, женщине становится трудно дышать. В связи с возросшей нагрузкой следует принять меры, предупреждающие варикозное расширение вен на ногах.
К этому моменту плод весит до 1000 г и имеет длину до 35 см. Его движения становятся более активными. При УЗИ видно, что он уже умеет сосать палец и даже улыбаться! Дно матки стоит на высоте 27–28 см над лоном, матка «подпирает» диафрагму, женщине становится трудно дышать. В связи с возросшей нагрузкой следует принять меры, предупреждающие варикозное расширение вен на ногах.
29–30-я недели. На этом сроке часто развивается токсикоз второй половины беременности. Маме следует строго контролировать еженедельную прибавку веса (не более 300 г) и цифры артериального давления, ограничить жидкость и соль в рационе.
31–32-я недели. Пора определить положение и предлежание плода. При головном предлежании надо носить бандаж, при тазовом – начинать гимнастику по Диканю (подробнее – позже). Беременным с 0(1) группой и резус-отрицательной кровью необходимы исследования крови на резус и групповые антитела, чтобы при необходимости провести очередной курс десенсибилизирующей терапии. Плод в это время весит 1500–1800 г.
Плод в это время весит 1500–1800 г.
33–34-я недели. Плод весит 1800–2100 г, его длина 40–41 см. В случае преждевременных родов ребенок сможет дышать самостоятельно, хотя и будет еще нуждаться в инкубаторе или грелке.
35–36-я недели. Дно матки поднялось на самую высокую точку за всю беременность. Из-за этого – изжога после приема пищи, одышка, усиливающаяся в положении лежа, синдром нижней полой вены, который проявляется обмороками, когда женщина лежит на спине, ведь вес плода уже превышает 2 кг, плюс околоплодные воды, сама матка с плацентой…
37–38-я недели. Беременность считается доношенной. Развитие ребенка полностью завершилось, он весит 2700–3000 г, рост 49–50 см, его легкие готовы к самостоятельному дыханию, терморегуляция достаточна для нормального жизнеобеспечения. Головка плода прижимается к входу в малый таз, и женщине (от этого радостного известия?) становится легче дышать. Учащаются схватки Брестона–Хикса, появляются небольшие тянущие боли в пояснице. Пора готовить обменную карту и сумку для роддома…
Пора готовить обменную карту и сумку для роддома…
39–40-я недели. Плод имеет все признаки зрелости, его масса более 3000 г, рост более 50 см. Родовая деятельность начнется с отхождения слизистой пробки, потом появятся регулярные, нарастающие по продолжительности и интенсивности схватки, интервалы между ними будут сокращаться, возможно излитие околоплодных вод. Остается вызвать машину «скорой помощи» и пожелать будущей маме удачи!
3.Если до ЭКО вы не все антитела сдали, то надо их досдать, сдать биохимию, гемостазиограмму, анализ мочи и крови, все свободны до 10 недель, можно к врачам не ходить, вы уже все, что могли сделали. В 11,5-12 недель на УЗИ смотреть патологии (т.е., Стыгар, Воеводин и т.д.) не в 13 недель!!! а в 11-12, потом ничего не видно!!!
4.Если все с масиком нормально, нет ЗБ, то стоит посмотреть шейку на кресле и подумать о враче для ведения (Зверева на Севастопольском, Тарасова в Сеченовке, понравились)
5.Дальше спокойненько сдаем еще раз биохимию, анализ крови и мочи, можно по желанию гемостазиограмму и ждем 18 недель, сдаем тройной тест, потом в 22 и 31 неделю смотрим у хорошего узиста патологии.
6.С этого момента можно заключить контракт с роддомом, до этого уже многие вещи можно делать просто в ЖК, а важные моменты делать у платных врачей.
Написала это не для того, чтобы вы не ходили к врачам, а понимали какие этапы надо отслеживать, тк у всех врачей разные подходы и сохранить наших детей прежде всего наша задача.
ЧТО еще важно!!!
1. Эстрофем и прочие отменяются постепенно по 0,5 таблетки в 4 дня и прекращают в 10 недель.
Утрожестан отменяют по таблетке в неделю с 10 недель, заканчивают в 16 недель. Если ваш врач говорит про резкую отмену проверьте указания у другого врача.
2. Витамины начинаются в 10-12 недель, раньше не надо, до этого фолиевая кислота. Стоит вне зависимости от функции щитовидки пить Йодомарин или аналоги.
Еще информация: тут расписаны максимальные обследования во время беременности (29, 30, 31) – www.invitro.ru/profiles.htm
и обследования до беременности – www.invitro.ru/mat_31.htm
Беременность после ЭКО – www. probirka.org/pregneco.htm –
probirka.org/pregneco.htm –
Комплексная оценка течения беременности после ЭКО – cps.org.ru/rarch_2004.php?art=48
Ультразвуковая техника – Startradiology
Общий
Техника
– Преобразователи
– Частота
– Различные плоскости
– Отражение / отклонение / поглощение / рассеяние
– Цветной допплер
– Дуплексный доплерАртефакты
Общие
УЗИ – удобный и доступный инструмент для обследования. Это относительно дешево и быстро. Кроме того, пациенты не подвергаются воздействию ионизирующего излучения.
Рисунок 1 дает некоторое представление о многих применениях ультразвуковой технологии. В список входят только тесты, выполненные радиологом; Например, пренатальные ультразвуковые исследования беременных женщин проводят специализированные акушеры.
Рис. 1. Общий вид ультразвуковых показаний.
Существенным преимуществом ультразвука является то, что в некоторых случаях клиническая картина, например местная боль при надавливании или пальпируемая припухлость могут быть немедленно сопоставлены с результатами ультразвукового исследования. Кроме того, это динамическая процедура с движущимися изображениями. Это может быть полезно, например, для демонстрации паховой грыжи во время Вальсавы или оценки сжимаемости желчного пузыря или сосудов (рис. 2).
Кроме того, это динамическая процедура с движущимися изображениями. Это может быть полезно, например, для демонстрации паховой грыжи во время Вальсавы или оценки сжимаемости желчного пузыря или сосудов (рис. 2).
Рис. 2. Паховая грыжа (выполняется во время Вальсавы с последующей компрессией).
К сожалению, у ультразвука есть свои недостатки. Не всем пациентам подходит УЗИ. У пациентов, страдающих ожирением, может быть трудно все четко представить (рис.3). Кроме того, качество обследования во многом зависит от опыта человека, проводящего УЗИ.
Рис. 3. Разница в качестве изображения у худых и страдающих ожирением пациентов.
Для получения дополнительных сведений о конкретных ультразвуковых исследованиях см. Соответствующие курсы, например Общее УЗИ брюшной полости (= в процессе).
Техника
Ультразвук использует звуковые волны. Они отражаются, отклоняются или поглощаются телом. Отраженные звуковые волны создают ультразвуковое изображение. Чем больше звуковых волн отражается, тем более гиперэхогенная (= более белая) ткань отображается. С уменьшенным отражением изображение будет более гипоэхогенным и анэхогенным, если нет отражения (= черный).
Отраженные звуковые волны создают ультразвуковое изображение. Чем больше звуковых волн отражается, тем более гиперэхогенная (= более белая) ткань отображается. С уменьшенным отражением изображение будет более гипоэхогенным и анэхогенным, если нет отражения (= черный).
И скорость звука, проходящего через ткань, и плотность ткани влияют на качество ультразвукового изображения. Ткань высокой плотности генерирует множественные отражения эха (например, костные / известковые структуры), создавая гиперэхогенные изображения.Жидкость не отражает звуковые волны и поэтому является анэхогенной (= черная). Мягкие ткани (например, органы) находятся где-то между гиперэхогенными и анэхогенными. Изоэхогенный – это когда ткань имеет ту же эхогенность, что и окружающая ткань (рис. 4/5).
Рисунок 4. Эхогенность с соответствующими условиями.
Рисунок 5. Пример ультразвукового исследования брюшной полости. Обратите внимание на разную эхогенность различных структур.
Преобразователи
Обычно используются три разных преобразователя (рис.6): секторный, линейный и выпуклый. Секторный преобразователь излучает звуковые волны веерообразным лучом. Головка преобразователя мала, а луч рядом с преобразователем узкий. По мере того, как луч удаляется от преобразователя, он расширяется, визуализируя более глубокие структуры. Этот датчик используется, в частности, при УЗИ черепа новорожденных. Маленькая головка датчика позволяет видеть паренхиму головного мозга через незакрепленные швы черепа. Линейный преобразователь излучает параллельные звуковые волны, обеспечивая высокое разрешение поверхностных структур (включая поражения кожи).Выпуклый преобразователь излучает параллельные звуковые волны с выпуклой поверхности. Звуковые волны излучаются веерообразным лучом, как и в большом выпуклом преобразователе, только между звуковыми волнами больше места рядом с преобразователем. Этот датчик обычно используется при УЗИ брюшной полости.
Рис. 6. Выпуклый, линейный и секторный преобразователи с различными звуковыми лучами.
На рис. 7 показано ультразвуковое исследование правой почки с использованием конвексного датчика.
Рисунок 7. Ультразвуковое исследование правой почки (конвексный датчик). Обратите внимание на движение почек при расслабленном дыхании. Проходящие черные (гипоэхогенные) вертикальные полосы – это ребра.
Частота
Помимо формы преобразователя, частота также влияет на качество изображения. Частоты от 2,5 до 7,5 МГц используются для ультразвуковой диагностики. Высокая частота обеспечивает более высокое разрешение изображения, но уменьшается глубина (= меньшая глубина проникновения).Низкая частота снижает разрешение, но увеличивает глубину проникновения.
Самолеты разные
Датчик используется для поперечной и сагиттальной оценки. Перемещая датчик по коже, получается параллельная серия ультразвуковых изображений, позволяющая систематически оценивать каждую часть тела. Другой способ – наклонить датчик. Датчик остается на месте, но поворачивается на девяносто градусов; только звуковой луч меняет направление. Таким образом, конструкции можно оценивать по двум направлениям.
Другой способ – наклонить датчик. Датчик остается на месте, но поворачивается на девяносто градусов; только звуковой луч меняет направление. Таким образом, конструкции можно оценивать по двум направлениям.
Например, в краниокаудальном направлении (= поперечная плоскость) и влево-вправо (= сагиттальная плоскость).
Важно: расположение и направление датчика на коже пациента определяют на полученном изображении спереди / сзади и слева / справа.
Как правило, в поперечной плоскости (рис. 8):
- верхняя часть ультразвукового изображения – это передняя сторона, а нижняя – задняя сторона.
- слева на изображении на самом деле справа и наоборот.Тело видно как бы снизу (как на поперечном срезе КТ).
Рис. 8. Левая почка в поперечной плоскости.
Как правило, в сагиттальной плоскости (рис.9):
- верхняя часть ультразвукового изображения – это передняя сторона, а нижняя – задняя сторона.

- справа на изображении направлен к стопам (= хвостовой), а слева – к голове (= черепной).
Изображения можно читать с экрана во время обследования.
Совет по ориентации при обследовании в реальном времени: верхняя часть изображения – это место, где звуковые волны попадают в пациента первыми. Итак, независимо от положения и наклона, верх – это сторона кожи.
Рисунок 9. Левая почка в сагиттальной плоскости.
Отражение / отклонение / поглощение / рассеяние
Когда звуковые волны движутся по граничной поверхности между двумя средами с разной плотностью, часть луча отражается на датчик.Это явление называется отражением. Остальная часть луча продолжается в ткани, но под другим углом. Это называется прогибом. Когда звуковые волны проникают в ткань, часть энергии преобразуется в тепло. Эта потеря энергии называется абсорбцией. Наконец, часть звуковых волн теряется в рассеянии. Это происходит, когда звуковые волны проходят через неоднородную ткань или «твердую» граничную поверхность (= большая разница в плотности между двумя средами). Часть звуковых волн отражается в случайных направлениях, небольшая часть – в сторону преобразователя.Для сводки см. Рисунок 10.
Часть звуковых волн отражается в случайных направлениях, небольшая часть – в сторону преобразователя.Для сводки см. Рисунок 10.
Рис. 10. Передача, отражение, отклонение, поглощение и рассеяние звуковых волн на граничной поверхности между двумя средами.
Цветной допплер
Шаблоны кровотока можно оценить с помощью эхо-допплера. Одним из применений эхо-допплера является цветной допплер. Этот метод можно использовать для оценки наличия и направления потока в кровеносном сосуде.
Звуковые отражения от движущегося объекта претерпевают изменения частоты.При обследовании измеряется разница между излучаемой и принимаемой частотами; частотный сдвиг / доплеровский сдвиг (рис. 11).
Рисунок 11. Доплеровский сдвиг; разница между излучаемой и принимаемой частотами.
Затем вычисляются доплеровский сдвиг и доплеровский угол (рис. 12), что позволяет определить характер кровообращения. Примечание: конкретные расчеты Доплера в этом курсе не рассматриваются.
Примечание: конкретные расчеты Доплера в этом курсе не рассматриваются.
Рисунок 12.Звуковая волна Доплера, распространяющаяся под углом через текущую кровь в кровеносном сосуде; угол Доплера.
Как объяснялось выше, частота движущихся объектов меняется. В цветном доплеровском режиме изменения частоты преобразуются в цвет на экране. Синий означает, что кровь отводится от датчика; красный означает, что кровь движется к датчику (примечание: синий и красный не обязательно означают кровь с низким и высоким содержанием кислорода соответственно). Объяснение: когда кровь движется к датчику, длина звуковой волны укорачивается, частота звука увеличивается (положительный доплеровский сдвиг).Противоположное происходит при движении крови от датчика (= отрицательный доплеровский сдвиг). См. Также рисунок 13.
Рис. 13. Различные частоты и длины волн в текущей крови.
Дуплексный допплер
Сигнал потока кровеносного сосуда также может быть представлен в виде спектра.
Доплеровский сдвиг показан вертикальной линией, время – горизонтальной линией (рис. 14/15). Кровь, текущая к датчику, имеет положительный доплеровский сдвиг и отображается над линией.Поток под линией имеет отрицательное доплеровское смещение (= поток от датчика).
Рис. 14. Изображение без и с цветным доплеровским потоком аорты (сагиттальное направление).
Рисунок 15. Дуплексный допплер аорты (сагиттальное направление).
Артефакты
Ультразвуковые исследования связаны с разнообразными ультразвуковыми артефактами и могут быть обнаружены во время исследования. К сожалению, не все эти артефакты можно обсудить в этом курсе.
Здесь объясняются два важных артефакта: акустическая тень и передача звука сзади. Хотя это артефакты, они ценны на практике.
Акустическая тень
Акустическое затенение вызывается двумя различными явлениями: полным отражением или поглощением. Полное отражение происходит на граничной поверхности между газом и тканью из-за большой разницы в плотности между газом и тканью. Полное поглощение происходит, когда звуковые волны поглощаются известковыми структурами (= включая камни, кости).Звуковые волны (практически) все отражаются / поглощаются; звуковые волны не достигают области за этими структурами, что делает эту часть ультразвукового изображения полностью анэхогенной (= черной). Это называется акустической тенью (рис. 16).
Полное отражение происходит на граничной поверхности между газом и тканью из-за большой разницы в плотности между газом и тканью. Полное поглощение происходит, когда звуковые волны поглощаются известковыми структурами (= включая камни, кости).Звуковые волны (практически) все отражаются / поглощаются; звуковые волны не достигают области за этими структурами, что делает эту часть ультразвукового изображения полностью анэхогенной (= черной). Это называется акустической тенью (рис. 16).
Рис. 16. Акустическое затенение, вызванное отражением кишечного газа.
Акустическое затемнение важно для выявления заболеваний, включая кальцификацию сухожилий, камни или свободный воздух. Артефакт также используется для различения твердых и кальцинированных масс, например.грамм. полип желчного пузыря (рис. 17) из желчных камней.
Рис. 17. Акустическое затенение желчным камнем, вызванное поглощением звуковых волн известковым камнем.
Передача заднего звука
Чтобы отличить кисту от твердого поражения, используются два артефакта: усиление задней стенки и повышенная передача звука. Эти явления возникают, когда звуковые волны проходят через анэхогенную структуру, обычно кисту. Звуковая волна теряет мало энергии, проходя через жидкость в кисте.Вот почему в звуковой волне в задней стенке и позади конструкции остается больше энергии, чем на том же уровне в окружающей области (примечание: окружающая ткань более плотная). Таким образом, для отражения преобразователя останется больше энергии. Это приводит к эхогенной задней стенке и эхогенной области позади кисты (рис. 18).
Рис. 18. Киста почки с усилением задней стенки и повышенной звукопередачей.
Передняя передача звука – хороший инструмент, чтобы отличить кисту от твердого поражения (рис.19).
Рис. 19. Киста печени с усилением задней стенки и передачей звука в сравнении с твердым поражением печени.
Обратите внимание, что киста анэхогенная, в отличие от эхогенного твердого поражения печени (твердое поражение было показано на КТ-сканировании как гемангиома).
Источники
- Б. Блок. УЗИ брюшной полости: шаг за шагом (2004).
- W.D. Middleton et al. Реквизиты – Ультразвук (2004).
- Дж. Бейтс. УЗИ брюшной полости: как, почему и когда (2011).
Авторы
Текст:
др. F.Y. Цзян (резидент-радиолог LUMC)
др. Р. ван ден Боом (абдоминальный рентгенолог и координатор образования LUMC)
Редактирование изображений:
др. А. ван дер Плас (радиолог MSK Maastricht UMC +)
20.02.2016 (переведено 09.11.2016)
Авторское право
Все работы (текст, иллюстрации, визуальные элементы), представленные на этом веб-сайте, являются собственностью Аннелис ван дер Плас.
Запрещается использовать его без письменного разрешения Аннелис ван дер Плас.
Как работают ультразвуки?
Ультразвук, также называемый сонографией, – это неинвазивный метод, используемый для получения внутренних изображений тела, включая кровеносные сосуды, мышцы, органы и другие мягкие ткани. Ультразвук может проводиться для наблюдения за развитием растущего плода в матке матери, для обнаружения аномалий или признаков заболевания или даже для визуальной помощи при операциях и биопсии.
Ультразвук не использует излучение, такое как рентгеновские лучи или компьютерная томография.Вместо этого он полагается на звуковые волны, генерируемые на таких высоких частотах, что они не могут быть услышаны человеческим ухом. По словам доктора Крейга К. Фройденриха, ультразвук похож на эхолокацию, форму общения, используемую летучими мышами и дельфинами, при которой они издают звуки и прислушиваются к эхо, чтобы определить местонахождение предметов или организмов в своей среде.
Основы
Ультразвуковой аппарат состоит из датчика (типа датчика) и центрального процессора или компьютера, подключенного к дисплею (монитору), клавиатуре и принтеру.
Как работает ультразвук?
Преобразователь проходит над той частью тела, которая покрывает внутренние структуры, которые необходимо отобразить. Это преобразователь, который излучает звуковые волны с частотами от 1 до 10 МГц (мегагерц). В свою очередь, звуковые волны отражаются обратно к датчику после того, как отразятся от структур, являющихся фокусом ультразвука. Центральный процессор измеряет интенсивность и скорость эха. Эти измерения преобразуются в электронные изображения, которые отображаются на мониторе машины.
Техник УЗИ использует клавиатуру для ввода данных пациента и информации, связанной с процедурой. Печатные копии ультразвуковых изображений могут быть распечатаны для представления членам диагностической или медицинской бригады.
Так же, как и непрерывная эволюция компьютеров и персональных устройств связи, ультразвуковые технологии продолжают развиваться. Изначально ультразвуковая технология позволяла получать только одно- и двухмерные изображения. Теперь есть машины, способные генерировать трехмерные изображения.Первый трехмерный ультразвуковой аппарат появился в середине 1980-х годов; Кадзунори Баба из Токийского университета использовал эту инновационную технологию для получения трехмерных изображений плода. Сейчас есть даже четырехмерные ультразвуковые аппараты, которые генерируют 3D-сканирование в реальном времени.
В последнее время произошла революционная волна, направленная на то, чтобы сделать ультразвуковые аппараты более портативными и компактными, полезными в экстренных ситуациях и во временных медицинских учреждениях и более удобными в любой клинике или больнице.По данным Klein Biomedical Consultants, в 2007 году спрос на портативные ультразвуковые устройства увеличился на 42% (Источник: «Дизайн недорогих портативных ультразвуковых систем» Джонатана М. Барана). Например, в 2009 году General Electric выпустила карманное ультразвуковое устройство V-scan. В начале 2011 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило последнее изобретение Mobisante: нечто среднее между смартфоном и ультразвуковым сканером.
Достижения в области применения ультразвука постоянно развиваются, и дополнительную информацию можно найти в этой недавно опубликованной статье.
Чем отличается ультразвуковая технология?
Помимо медицинских специалистов по диагностической ультразвуковой диагностике, также называемых специалистами по ультразвуковой диагностике, есть и другие специалисты в области здравоохранения, использующие технологию медицинской визуализации. Радиологи-технологи используют аппараты рентгена, МРТ (магнитно-резонансная томография) и КТ (компьютерная томография). В отличие от ультразвуковых аппаратов, в этих технологиях используется излучение. Технологи ядерной медицины также используют сканирующее оборудование для получения внутренних изображений тела.В этом случае они вводят своим пациентам радиоактивные соединения с целью обнаружения аномалий среди структур, которые отображаются. Узнайте больше о различиях между этими технологиями в нашей недавно опубликованной статье.
Ультразвуковое руководство и терапия | IntechOpen
1. Введение
Минимально инвазивная и неинвазивная терапия под визуальным контролем может уменьшить хирургические травмы и улучшить исход для пациентов, страдающих от самых разных заболеваний.Это также может сократить сроки пребывания в больнице и расходы. Ультразвук – важный метод интраоперационной визуализации для руководства и мониторинга этих терапевтических методов. Ультразвук стал одним из основных методов медицинской визуализации в здравоохранении, основной причиной которого является его способность отображать мягкие ткани, кровоток, функции органов и физиологию со значительно улучшенным качеством изображения. Кроме того, ультразвук обладает уникальными преимуществами визуализации в реальном времени, портативности оборудования, безопасности и низкой стоимости.В ближайшие 10 лет ультразвук столкнется с изменением парадигмы в технологии и клиническом применении. Будущий потенциал будет высвобожден за счет исследования в области знаний и инноваций в массивах датчиков, ультразвуковой электронике, программном формировании луча, параллельной визуализации и сжатых измерениях, визуализации с минимальной дифракционной волной, получении изображений с использованием модели и новых технологиях для широкого спектра методов, связанных с физиологией. , свойства тканей и функции органов в реальном времени и на месте.Высокочастотная ультразвуковая визуализация позволяет получить значительно улучшенное пространственное разрешение, однако с ограничениями, связанными с тем, насколько глубоко в ткани может быть выполнено визуализация. Во многих хирургических и терапевтических операциях с визуализацией ультразвуковое исследование выполняется с помощью датчиков, помещаемых непосредственно на интересующую ткань и орган (например, внутрисосудистое ультразвуковое исследование, кардиохирургия открытой грудной клетки, датчики пищевода для визуализации сердца, датчики, предназначенные для хирургии гипофиза). Эти приложения ограничивают размер головки ультразвукового зонда и, следовательно, качество изображений.Однако с помощью миниатюризации на основе наноматериалов и технологии наноэлектроники можно добиться значительного улучшения качества изображения. Кроме того, новая ультразвуковая технология может значительно улучшить обнаружение контрастных веществ и носителей лекарств в тканях. Интеграция визуализации с навигационными технологиями упростит интерпретацию изображений и еще больше повысит точность и точность терапевтической процедуры. Ультразвуковая техника также может использоваться в терапевтических целях. Сфокусированный ультразвук высокой интенсивности (HIFU) для удаления опухолевой ткани уже является коммерческим продуктом.Также было показано, что ультразвук может улучшить доставку и распределение наночастиц и местную доставку лекарств за счет усиления местного высвобождения, улучшения проникновения через стенку капилляров и через внеклеточный матрикс, а также за счет увеличения клеточного поглощения. Основные механизмы – кавитация, радиационная сила и нагрев. Временное увеличение пористости и проницаемости клеточных мембран, индуцированное ультразвуком, может потенциально усилить поглощение лекарств через тканевые барьеры (также гематоэнцефалический барьер) и улучшить местную доставку лекарств.
Терапевтическое использование ультразвука будет рассмотрено в конце этой главы, которая в основном посвящена безопасному вводу инструментов в тело с помощью ультразвука, а также технологических решениях, связанных с расширением ультразвука в сочетании с другими методами и методами. Ультразвук уже давно используется для ввода интервенционных инструментов в тело. Использовались разные подходы. От ручного 2D-наведения через «игольчатые» направляющие, установленные на обычных ультразвуковых датчиках, до ультразвуковой навигации с использованием технологии отслеживания и трехмерного ультразвука (см. Рисунок 1).Хирургическая навигация будет в центре внимания этой главы, и аналогия с GPS-навигацией в автомобиле очевидна; вместо нанесения положения автомобиля на электронные карты местности с помощью спутников и GPS-приемников, положение важных хирургических инструментов отображается на медицинских изображениях пациента с использованием высокоточных систем слежения. Системы для хирургии под визуальным контролем теперь хорошо зарекомендовали себя во многих клинических дисциплинах. Хирургические инструменты можно отслеживать с помощью систем позиционирования, и хирург может точно вводить инструменты в пациента с высокой точностью только на основе информации об изображении.Показано, что интраоперационная визуализация важна для улучшения резекции опухоли и увеличения выживаемости онкологических больных, перенесших операцию. Интеграция интраоперационной визуализации с навигационной технологией, предоставляющая хирургу обновленную информацию об изображении , важна для борьбы со сдвигами и деформациями тканей, которые происходят во время операции. МРТ, КТ и УЗИ были представлены как альтернативные методы интраоперационной визуализации, показывающие дополнительную информацию и имеющие различные преимущества и недостатки.Сообщается, что эти методы интраоперационной визуализации полезны для точной навигации хирургических инструментов, отслеживания прогресса операции и решения проблемы смены. Интраоперационная визуализация использовалась для обновления предоперационных изображений, что может быть важно для точного руководства. В последние годы УЗИ привлекло повышенное внимание как полезный метод интраоперационной визуализации (см. Рисунок 2) из-за улучшенного качества изображения и относительно низкой цены. Кроме того, были представлены более интегрированные решения, делающие технологию удобной и гибкой.В эволюции следующего поколения мультимодальных навигационных систем на основе ультразвука важными составляющими являются достижения в области ультразвуковой визуализации, алгоритмов регистрации, методов визуализации и отображения, а также точности навигации. Поэтому мы начнем с изучения технологии, которая необходима для того, чтобы сделать навигацию на основе ультразвука реальностью, а затем покажем ключевые приложения этой технологии. Последние достижения в области ультразвуковой визуализации будут полезны также для интраоперационной визуализации.Кроме того, ультразвук должен быть интегрирован с технологией отслеживания, чтобы создать навигационную систему с возможностями интраоперационной визуализации. Кроме того, такая система может использовать предоперационные данные КТ / МРТ, обновлять эти данные для соответствия текущей анатомии пациента с помощью интраоперационного ультразвука, извлекать важные структуры из различных наборов данных, оптимальным образом представлять доступную мультимодальную информацию хирургу. и иметь возможность отслеживать все хирургические инструменты. И последнее, но не менее важное: нам необходимо убедиться, что система навигации имеет высокую точность, чтобы мы знали, что сцена навигации, представленная хирургу на экране компьютера, является реалистичным представлением того, что на самом деле происходит внутри пациента.
Рис. 1.
Ультразвуковое сопровождение: A) Направление от руки: задача иметь длинную ось инструмента в 2D ультразвуковой плоскости. Б) Направляющие для иглы: адаптер, установленный на датчике, обеспечивает нахождение инструмента в плоскости 2D ультразвукового исследования. C) Навигация: технология отслеживания и трехмерные данные от таких методов, как КТ, МРТ и ультразвук, используются для направления соответствующих хирургических инструментов на место. Здесь ультразвуковой зонд направляется магнитно-резонансным датчиком во время ультразвукового исследования от руки в 3D.
Рис. 2.
A) Рабочий процесс: важные шаги в хирургии под визуальным контролем. B) Пример навигации на основе ультразвука из нейрохирургии: планирование с использованием предоперационной МРТ. Сделайте интраоперационное 3D-УЗИ. Контроль навигации и резекции на основе обновленных ультразвуковых изображений. При необходимости получите дополнительные данные УЗИ.
2. Последние достижения в области ультразвуковой визуализации
Звук в диапазоне слышимости человека имеет частоты от 20 до 20 000 Гц. Ультразвук определяется как звук с частотами выше 20 кГц.В медицинской визуализации частоты ультразвука обычно составляют от 2 до 40 МГц, при этом самые высокие частоты в настоящее время используются при внутрисосудистом ультразвуковом исследовании (ВСУЗИ).
Генерация ультразвукового изображения основана на передаче звуковых импульсов и приеме эхо-сигналов, отраженных от границ тканей или рассеянных от более мелких объектов. В большинстве современных сканеров узкий ультразвуковой луч передается от ультразвукового преобразователя. Когда переданный импульс давления встречает препятствие в виде границы между различными мягкими тканями или точек рассеяния в ткани с различными акустическими свойствами, часть энергии переданного звукового импульса отражается обратно на датчик.Этот принцип эхо-импульса лежит в основе всех методов ультразвуковой визуализации, таких как визуализация органов в обычном режиме яркости (B-режим), визуализация кровотока с использованием допплеровских методов и исследование механических свойств тканей с использованием методов ультразвуковой эластографии.
2.1. Достижения в ультразвуковом оборудовании и технологиях датчиков
Ультразвуковые аппараты и ультразвуковые датчики претерпели значительные улучшения за последнее десятилетие. Общее увеличение мощности компьютеров открывает новые возможности для реализации сложных методов формирования луча.Это может привести к более высокому разрешению и лучшему качеству изображения, чем существующие решения [1]. Общая тенденция к миниатюризации компонентов также сильно повлияла на размер систем ультразвуковой визуализации. Были разработаны небольшие портативные ультразвуковые устройства, которые делают ультразвук чрезвычайно портативной технологией визуализации. Одним из примеров такого карманного ультразвукового устройства является Vscan от GE Healthcare (рис. 3), который был исследован для использования в эхокардиографии [2]. Технология ультразвуковых преобразователей за последнее десятилетие достигла огромного прогресса.Количество элементов, используемых преобразователем, увеличивается, и наблюдается тенденция перехода от однорядных элементов (1D) к многострочным массивам (1,25D / 1,5D) и двумерным матричным массивам. Последний предоставляет возможность выполнять 4-мерное ультразвуковое изображение, при котором объемный объем трехмерного ультразвукового исследования регистрируется и отображается в реальном времени. Ультразвуковое изображение 4D также может использоваться для мониторинга лечения, например радиочастотная абляция [3].
Рис. 3.
Карманный ультразвуковой сканер (Vscan от GE Healthcare)
Сегодня ультразвуковые матрицы в основном основаны на пьезоэлектрических материалах.Исследования в области технологии MUT (микромашинных ультразвуковых преобразователей) и, возможно, особенно преобразователей CMUT (емкостные преобразователи частоты) открывают путь для кремниевых решеток [4]. Это может привести к появлению более дешевых, более настраиваемых датчиков с более высокими частотами и полосой пропускания по сравнению с пьезоэлектрическими преобразователями. В сочетании с непрекращающейся тенденцией к миниатюризации, CMUT в долгосрочной перспективе могут позволить полностью интегрировать ультразвуковые системы с хирургическими инструментами.Вполне возможно, что будущий хирургический инструмент будет иметь ультразвуковой преобразователь, встроенный в наконечник, и блок отображения, встроенный в ручку.
2.2. Ультразвуковая эластография
Понятие ультразвуковой визуализации деформации или эластичности тканей часто называют ультразвуковой эластографией, а соответствующие 2D-изображения часто называют эластограммами. Технику визуализации часто объясняют как аналог пальпации, когда врач слегка надавливает пальцами, чтобы исследовать жесткость ткани.Если орган вибрирует или возбужден, методы ультразвуковой эластографии можно аналогичным образом использовать для картирования областей с различиями в деформации (рис. 4).
Рисунок 4.
Эластография. A) Ультразвуковое изображение небольшой менингиомы в B-режиме и B) Ультразвуковая эластограмма опухоли, отображаемая на сканере Ultrasonix MDP.
Теоретическая основа для изучения поведения вибрирующих мягких тканей была создана в начале 1950-х годов. Von Gierke et al. опубликовал, например, «Физика колебаний в живых тканях » в 1952 г. [5].Однако только 30 лет спустя движение тканей было впервые измерено в клинических целях с помощью ультразвука при исследовании движения тканей в печени, вызванного пульсацией сосудов [6, 7]. В конце 80-х годов прошлого века были разработаны методы визуализации вибрационной эластографии, также известные как соноэластография с амплитудой вибрации или просто визуализация соноупругости [8]. В этой методике низкочастотная вибрация (20-1000 Гц) применяется снаружи к поверхности кожи для исследования подкожных структур.Внутреннее движение ткани исследуется с помощью метода импульсного допплера. Жесткая ткань по-другому реагирует на вибрации, чем более мягкая ткань, и поэтому ее можно различить на изображениях в реальном времени.
В начале 1990-х годов началось развитие компрессионной эластографии, также называемой квазистатической визуализацией эластичности. Офир опубликовал статью в 1991 году, в которой данные ультразвуковых радиочастот (RF) до и после применения сжатия сравнивались и обрабатывались с использованием взаимной корреляции для получения временных сдвигов эхо-сигналов.Это позволило в последующем рассчитать эластограммы [9]. Квазистатическая эластичность подразумевает, что сила прикладывается в течение достаточно длительного времени для стабилизации деформации ткани, и можно рассчитать результирующую разницу во времени прохождения эхо-сигнала между ультразвуковыми данными, полученными до и после сжатия. Ткань также может быть возбуждена путем приложения сил на поверхности (вручную или с помощью электромеханических устройств) или физиологических процессов внутри органа, таких как, например, пульсация артерий.Сгенерированные эластограммы обычно отображаются в виде наложения с цветовой кодировкой на обычное изображение в режиме яркости ультразвука. Цветовое отображение может охватывать диапазон значений деформации без единицы измерения в процентах от минимальной (отрицательной) деформации до максимальной (положительной) деформации. В качестве альтернативы, это также может быть отображено от «мягкой» к «твердой» ткани, тем самым не определяя отображаемый диапазон деформации. Квазистатическая визуализация эластичности оценивалась в широком спектре клинических приложений. Сообщалось о его применении для диагностики опухолей, например, груди, простаты, печени, щитовидной железы и головного мозга (рис. 4) [10-15].Квазистатическая визуализация эластичности – это развивающийся метод ультразвуковой визуализации, который в настоящее время становится все более доступным в качестве опции для коммерческих ультразвуковых систем.
Как объяснялось ранее, методы эластографии требуют возбуждения ткани. Движение ткани может быть вызвано физиологическими процессами внутри органа, такими как пульсация артерий. Ткань также можно возбуждать извне, толкая ткань вручную или используя электромеханическое вибрирующее устройство.Альтернативный подход заключается в использовании силы акустического излучения сфокусированного ультразвукового луча для создания смещений в ткани с последующим определением механических свойств. Одним из примеров такого подхода является метод Acoustic Radiation Force Impulse (ARFI), разработанный в Университете Дьюка [16]. В этом методе короткие акустические импульсы (толкающие импульсы) используются для создания небольших локализованных смещений глубоко в ткани. Эти смещения отслеживаются с помощью ультразвуковой кросс-корреляции аналогично тому, как это делается при квазистатической визуализации упругости.Метод был исследован для визуализации очаговых поражений печени, простаты и груди [17-19].
Другим примером является инновационный метод визуализации сверхзвукового сдвига (SSI), разработанный исследовательской группой Laboratoire Ondes et Acoustique [20]. В SSI сила акустического излучения используется для создания низкочастотных поперечных волн (50-500 Гц) удаленно в ткани. Модуль сдвига ткани может быть определен количественно путем визуализации распространения волны в ткани с использованием частоты кадров ультразвука в несколько кГц.Метод был исследован для диагностики фиброза печени, поражений груди и роговицы [21-23].
Для более подробного обзора методов ультразвуковой визуализации эластичности и их клинического применения мы рекомендуем прочитать обзорные статьи Wells и Liang [24] и Parker, Doyley и Rubens [25].
2.3. Нелинейная акустика и контрастные вещества
В 1980 году Карстенсен и Мьюир опубликовали две статьи, описывающие важность нелинейной акустики в области медицинской ультразвуковой визуализации [26, 27].В этих статьях были предсказаны и продемонстрированы нелинейные акустические эффекты, относящиеся к интенсивностям и частотам, обычным для биомедицинской визуализации. За последние 30 лет наблюдается возрастающий интерес к нелинейной биомедицинской акустике. Этот интерес был дополнительно усилен введением ультразвуковых контрастных агентов в форме микропузырьков, и изучение этих микропузырьков стало основным стимулом для внедрения техники гармонической визуализации тканей.
Нелинейные эффекты могут быть важны при распространении прямой волны.Уровни давления обратного рассеяния эхо-сигналов обычно слишком низки, чтобы вызвать какие-либо существенные нелинейные эффекты. Одним из источников нелинейных членов является деформация элементов объема ткани во время сжатия и расширения с сильно искривленными фазовыми фронтами. Однако обычно используют передающие лучи с относительно гладкими фазовыми фронтами. Следовательно, этот нелинейный источник обычно не самый доминирующий. Другой важный нелинейный источник – это нелинейные составляющие эластичности ткани и, следовательно, отношения между акустическим давлением и сжатием / расширением ткани.Нелинейные члены эластичности ткани ответственны за то, что ткань становится более жесткой при сжатии и более мягкой при расширении. Сжатие также увеличивает массовую плотность ткани, но этот эффект уступает повышенной жесткости и скорости распространения и, следовательно, будет зависеть от давления и будет увеличиваться с увеличением сжатия и, следовательно, с увеличением давления. Возникающее в результате искажение поля передаваемого давления создает гармонические составляющие, которые сегодня используются в гармонической визуализации тканей, особенно при чрескожной визуализации сердца и брюшной полости для подавления множественного рассеяния [28-31].
Ультразвуковая визуализация основана на нескольких предположениях, и одно важное предположение заключается в том, что многократным рассеянием пренебрегают. Для многих органов это приближение справедливо. Однако для стенки корпуса, где часто встречаются большие вариации параметров материала, это предположение может быть неадекватным. Интерфейсы между компонентами мягких тканей со значительными различиями в параметрах материалов дают настолько сильные эхо-сигналы от передаваемых акустических импульсов, что многократное рассеяние может иметь значительные амплитуды.Такое многократное рассеяние принято называть реверберацией импульсов [32, 33]. Эти реверберации уменьшают отношение самого сильного рассеивателя к самому слабому, которое может быть обнаружено в непосредственной близости друг от друга, что определяется как контрастное разрешение изображения. Снижение контрастного разрешения, в частности, является проблемой при визуализации гипоэхогенных структур, таких как камеры сердца, просвет крупных кровеносных сосудов, некоторых атеросклеротических поражений, кист, некоторых опухолей, желчного пузыря, а также при визуализации плода.Контактная поверхность между самим ультразвуковым преобразователем и мягкими тканями также является сильным отражателем, усугубляющим проблему многократного рассеяния.
Контрастные вещества для ультразвука представляют собой суспензию газовых микропузырьков, заключенных в тонкие стабилизирующие оболочки из липидов или альбумина. Типичный размер пузырьков находится в диапазоне 1-5 мкм, и контрастные пузырьки вводятся внутривенно, чтобы увеличить рассеяние от крови, которое является слабым по сравнению с рассеянием от мягких тканей.Коммерчески доступные контрастные пузырьки стабильны и достаточно малы, чтобы обеспечить транспульмональный проход, а период полувыведения из крови обычно находится в диапазоне 1-10 минут. Рассеяние от микропузырьков, возникающих внутри жидкости, является резонансным благодаря взаимодействию между совместно колеблющейся жидкой массой вокруг пузырька и упругостью сжатия пузырька [34] с типичными резонансными частотами 1-7 МГц. При достаточно гибких оболочках пузырек газа имеет очень высокую податливость по сравнению с окружающей кровью, и при возбуждении ультразвуковыми импульсами на частотах ниже или около резонансной частоты пузыря достигаются большие отклонения радиуса пузыря порядка одного микрометра, главным образом, за счет сдвига. деформация и ограниченное объемное сжатие крови, окружающей пузырь.Это смещение радиуса пузырька на один-два порядка больше, чем типичное смещение частиц, получаемое в мягких тканях. Радиус колебаний пузырька может быть получен из уравнения Рэлея-Плессета [35, 36]:
ρaa¨ + 32a˙2 = -Ba, a˙- pi (t) E1
где ρ – массовая плотность окружающая жидкость, a – радиус пузырька (где зависимость от времени для удобства опущена), B – давление, создаваемое газом и герметизирующей оболочкой, pi – падающее давление привода, а точки представляют дифференциацию по времени, так что a˙ и a¨ представляют скорость и ускорение стенки пузырька соответственно.Члены в левой части представляют собой силы ускорения массы совместно колеблющейся жидкости, тогда как члены в правой части представляют термины давления из-за упругости газа и оболочки в дополнение к давлению привода. Давление в пузырьке B можно записать в виде
Ba, a˙ = – p0 + 2σa0a0a3κ- Sa0, a + p0 + 2σa + μa˙aE2
, где первый член – это давление газа, а κ – показатель политропы газа, а a0 – равновесный пузырь. радиус. Второй член S представляет собой вклад давления со стороны герметизирующей оболочки, а p0 представляет собой гидростатическое давление окружающей среды.Четвертый член учитывает поверхностное натяжение из-за границы раздела газ-жидкость, а последний член учитывает эффекты демпфирования. Когда контрастный пузырек озвучивается частотами ниже или около его резонансной частоты, локальное нелинейное рассеяние от контрастного пузыря обычно намного больше, чем от мягких тканей [37, 38]. Это привело к появлению нескольких методов нелинейного ультразвукового обнаружения контрастного вещества с целью подавления линейной части принятого сигнала при сохранении как можно большей нелинейной части принимаемого сигнала.Затем это используется для низких уровней давления передачи. Распространение прямой волны близко к линейному, тогда как рассеяние на микропузырьках может быть сильно нелинейным. Сегодня широко используются методы импульсной инверсии, которые обнаруживают четные гармонические составляющие [39, 40]. Также используются методы амплитудной модуляции [41], часто в сочетании с методами импульсной инверсии [42-44].
Рис. 5.
Численное моделирование колебаний пузырька с равновесным радиусом 2 мкм и резонансной частотой 2.5 МГц. Верхние панели показывают импульс возбуждения, средние панели показывают результирующие колебания радиуса пузырька, а нижние панели показывают компоненту дальнего поля рассеянного давления от пузырька. На левой панели отображаются импульсы во временной области, тогда как модуль преобразования Фурье отображается на правой панели.
Уравнения, описывающие колебания пузырька, можно решить численно. Пример пузырька с равновесным радиусом 2 мкм показан на рисунке 5. Падающий импульс возбуждения с центральной частотой около 2 МГц отображается во временной и частотной области на верхней панели.На средней панели изображены результирующие колебания радиуса пузырька, а на нижней панели отображается результирующая нормализованная компонента дальнего поля рассеянного давления пузырька. Видно, что отклик сильно нелинейный, и в рассеянном давлении пузыря присутствует несколько гармонических составляющих. Этот отклик получается при падающем управляющем импульсе, имеющем механический индекс, равный 0,07, что очень мало по сравнению с тем, что используется для обычного изображения ткани.При таких низких уровнях давления передачи прямое распространение волны будет близко к линейному, и искажение поля передачи из-за нелинейной эластичности ткани, таким образом, будет очень низким. Затем гармонические составляющие можно использовать для дифференциации пузырьковых эхо-сигналов от тканевых эхо-сигналов с помощью импульсных схем с импульсной инверсией и амплитудной модуляцией. В большинстве клинических применений контрастных агентов для ультразвука желательно оценить микроциркуляцию или перфузию тканей, что невозможно сделать без использования контрастных агентов и что часто связано с различными заболеваниями.Затем необходимо получить сильное подавление сигнала ткани для обнаружения сигнала контрастного пузырька.
Примером использования контрастных агентов для ультразвука в отношении минимально инвазивных вмешательств является радиочастотная абляция опухолей печени, при которой ультразвук с контрастным усилением используется для улучшенного обнаружения и визуализации поражений, для планирования и наведения нескольких игольчатых электродов и, наконец, для немедленная оценка лечения [45].
SURF (Ультразвуковое поле второго порядка) визуализация – это метод нелинейной ультразвуковой визуализации, разрабатываемый в Тронхейме [46-50].Он основан на передаче двухчастотных импульсных комплексов, состоящих из низкочастотного управляющего импульса и высокочастотного импульса формирования изображения, которые распространяются совместно. Два комплекса импульсов передачи, которые могут использоваться с техникой SURF, показаны на рисунке 6. При использовании обычных импульсов передачи с одной полосой частот нелинейные эффекты в основном ограничиваются генерацией гармонических составляющих импульса формирования изображения. При использовании импульсов передачи в двух частотных диапазонах в игру вступают и другие нелинейные эффекты.Визуализация SURF направлена на дальнейшее использование нелинейной акустики для улучшения визуализации различных тканей и ультразвуковых контрастных веществ.
Рис. 6.
Пример комплексов импульсов передачи SURF, где низкочастотный импульс манипулирования на 1 МГц распространяется вместе с высокочастотным импульсом формирования изображения на частоте 10 МГц. Импульс высокочастотной визуализации находится на левой и правой панели при низком и высоком давлении манипуляции соответственно.
Для визуализации ультразвуковых микропузырьков традиционные методы основаны на приведении пузырька в сильные нелинейные колебания с помощью импульса визуализации с относительно низкими механическими показателями.Это обычно возможно, когда частота визуализации ниже или около резонансной частоты пузырька (как в примере на рисунке 5), а обычные контрастные вещества обычно имеют резонансные частоты ниже 7 МГц. Однако, когда частота формирования изображения выше резонансной частоты пузырька, требуется гораздо более высокий механический индекс для получения значительного нелинейного обратного рассеяния от пузырька. При более высоких механических индексах ткань также будет реагировать нелинейно, и тогда становится трудно отличить сигнал ткани от сигнала пузыря.Для получения контрастных изображений на высоких частотах, таких как 10–30 МГц, которые могут использоваться при минимально инвазивных вмешательствах, когда зонд может быть расположен близко к объекту, который визуализируется, традиционные методы контрастного изображения часто имеют ограничения. Двухполосная технология SURF имеет некоторые преимущества, поскольку низкочастотный импульс манипуляции может быть настроен для соответствия резонансной частоте пузырька (обычно около 2–3 МГц), тогда как высокочастотный импульс визуализации может быть оптимизирован для объекта, на котором создается изображение, и может, например, быть 20 МГц.Затем низкая частота управляет колебаниями пузырьков и обратным рассеянием, которые запрашиваются высокочастотным импульсом. Таким образом, высокочастотный импульс формирования изображения не связан с резонансными свойствами контрастных пузырьков.
3. Навигация на основе ультразвука – Технологии поддержки
Современная ультразвуковая визуализация имеет решающее значение для проведения вмешательства. Но в отличие от руководства от руки и руководства, основанного на ультразвуковых шаблонах (рис. 1), оптимального изображения на ультразвуковом сканере недостаточно для обеспечения хирургической навигации.Чтобы использовать навигацию на основе ультразвука для проведения таких процедур, мы обычно должны:
Получить изображения из ультразвукового сканера в навигационное программное обеспечение в режиме реального времени.
Постоянно отслеживайте положение и ориентацию ультразвукового датчика.
Синхронизируйте потоки изображения и отслеживания (временная калибровка) и найдите преобразование между датчиком отслеживания, установленным на ультразвуковом датчике, и плоскостью ультразвукового сканирования (пространственная калибровка), которая представляет собой интересную часть для отслеживания.
Восстановите все ультразвуковые кадры с позиционной меткой из обычного ультразвукового датчика 2D в обычный трехмерный объем, который можно использовать так же, как предоперационную МРТ или КТ.
3.1. Потоковая передача ультразвуковых данных
Для удобной навигации хирургических инструментов на основе ультразвука требуется доступ в реальном времени к ультразвуковым данным в навигационном программном обеспечении (рис. 7). Это требуется для того, чтобы пометить ультразвуковые кадры данными о положении и ориентации из системы отслеживания (в качестве альтернативы данные отслеживания могут быть направлены непосредственно в сканер, а ультразвуковые кадры могут использоваться в автономном режиме, например.грамм. для создания 3D-объема из помеченных 2D-кадров). Традиционный способ получения доступа к ультразвуковым кадрам в реальном времени – это подключить аналоговый выход (например, композитное видео, S-video) ультразвукового сканера к карте захвата кадров на навигационном компьютере. Использование аналогового выхода может повлиять на качество изображения из-за двойного цифро-аналогово-цифрового преобразования, а метаданные (например, глубина) не следуют за ультразвуковыми изображениями. В качестве альтернативы цифровые данные можно передавать прямо с ультразвукового сканера в навигационный компьютер.Традиционно для этого требовалось какое-то исследовательское сотрудничество между производителем ультразвуковых устройств и пользователем, но становятся доступными открытые ультразвуковые сканеры (например, сканер Ultrasonix). Эти системы обычно предоставляют только односторонний потоковый интерфейс, но существуют протоколы двусторонней связи, в которых сканер может контролироваться (например, глубиной) с помощью навигационной системы, что делает возможными более интегрированные решения (рисунок 7). В любом случае используемый протокол (или интерфейс / API) обычно является проприетарным, хотя предложения по стандартам реального времени начинают появляться (например,грамм. OpenIGTLink, DICOM в хирургии (WG24)). Когда связь между ультразвуковым сканером и навигационной системой является цифровой, ультразвуковые данные на разных этапах цепочки обработки на сканере могут передаваться (например, преобразованные при сканировании, строковые и RF-данные). Кроме того, потребуется интерфейс цифровой потоковой передачи, чтобы использовать 3D-сканеры в реальном времени, которые теперь становятся доступными также для навигации. Сложно захватить трехмерный контент на дисплее сканера с помощью фреймграббера, поэтому данные необходимо передавать в режиме реального времени или маркировать с помощью ссылки отслеживания на ультразвуковом сканере.
Рис. 7.
Передача ультразвуковых данных в навигационную систему. Интерфейс может быть аналоговым с использованием фреймграббера или цифровым с использованием прямого канала и собственного протокола. Цифровой интерфейс может быть односторонним (т. Е. Потоковым) или двусторонним (т. Е. Можно также управлять сканером из навигационной системы). В любом случае поток изображения должен быть помечен данными отслеживания, и для этого необходимо синхронизировать два потока.
3.2. Отслеживание ультразвуковых датчиков
Чтобы использовать ультразвук для управления хирургическими процедурами, необходимо отслеживать ультразвуковой датчик.На протяжении многих лет было предложено несколько технологий слежения (механическое, акустическое, оптическое и электромагнитное), но в настоящее время наиболее широко используемыми решениями являются оптические или электромагнитные системы (см. Рисунок 8). Выбор наилучшей технологии отслеживания зависит от конкретного приложения и используемых ультразвуковых датчиков. По возможности следует отдавать предпочтение системам оптического слежения, поскольку магнитное слежение в операционной может быть затруднено из-за помех от металлических предметов, а точность близка, но не так хороша, как оптические системы при благоприятных условиях.Для гибких us-зондов или зондов, которые вставляются в тело, требуется магнитное отслеживание, поскольку преобразование между датчиком и плоскостью сканирования должно быть жестким, а оптическое отслеживание требует прямой видимости для камер. Кроме того, магнитные датчики очень малы и имеют решающее значение для встраивания в инструменты и установки в тело. Когда ультразвуковой датчик отслеживается, он становится одним из нескольких инструментов, и потоковые ультразвуковые данные могут отображаться в реальном времени в нужном месте пациента или преобразовываться в трехмерный объем и показываться хирургу вместе с другими изображениями.Краткое описание двух основных технологий слежения можно найти ниже [51, 52]:
Системы оптического слежения : Основная идея состоит в использовании одной или нескольких камер с маркерами, распределенными на жесткой конструкции, геометрия которой указано заранее (рисунок 8А). Для определения положения и ориентации твердого тела в пространстве необходимо не менее трех маркеров. Дополнительные маркеры обеспечивают лучшую видимость отслеживаемого объекта камерой и повышают точность измерения.Маркеры могут представлять собой инфракрасные светодиоды (активные маркеры), отражатели инфракрасного света (пассивные маркеры) или какой-либо узор (обычно шахматная доска), который можно идентифицировать с помощью визуального света и анализа изображения.
Системы электромагнитного слежения : Приемник (датчик) помещается на ультразвуковой датчик, и система измеряет индуцированные электрические токи, когда датчик перемещается в магнитном поле, создаваемом переменным или постоянным током. (DC) передатчик / генератор (рисунок 8B).Устройства переменного и постоянного тока чувствительны к некоторым типам металлических предметов, размещенных слишком близко к передатчику или приемнику, а также к магнитным полям, создаваемым источниками питания и устройствами, такими как мониторы с электронно-лучевой трубкой. Следовательно, оба типа электромагнитных систем сложно использовать в такой среде, как операционная, где различные металлические объекты перемещаются в поле [53]. Два связанных с металлом явления, которые влияют на характеристики электромагнитных систем слежения, – это ферромагнетизм и вихревые токи [54].Ферромагнитные материалы (например, железо, сталь) влияют на системы как переменного, так и постоянного тока, поскольку они изменяют однородность магнитного поля, создаваемого трекером, хотя системы постоянного тока могут быть более чувствительными к этим эффектам. Напротив, технология переменного тока больше зависит от наличия проводников, таких как медь и алюминий, из-за искажений, вызванных вихревыми токами [53, 55]. Системы постоянного тока минимизируют искажения, связанные с вихревыми токами, путем измерения поля после затухания вихревых токов.
Сравнение оптических и магнитных систем слежения – за и против: Основными преимуществами оптических систем слежения являются их надежность и высокая точность, а проблемами являются проблемы с прямой видимостью и относительно большие корпуса датчиков.Для электромагнитной системы слежения все наоборот.
Рисунок 8.
Оптическое (A) и электромагнитное (B) слежение за ультразвуковыми датчиками.
3.3. Калибровка ультразвукового датчика
После потоковой передачи ультразвуковых данных в навигационное программное обеспечение и отслеживания ультразвукового датчика необходима калибровка для интеграции потока изображения с потоком отслеживания. Калибровка ультразвукового датчика – важная тема, так как это основной источник ошибок для ультразвуковой навигации (см. Раздел о точности).Необходимы два типа калибровки; временная калибровка для поиска запаздывания между потоками изображения и отслеживания и пространственная калибровка [56, 57] для обнаружения преобразования между плоскостью ультразвукового сканирования и датчиком отслеживания, установленным на ультразвуковом датчике (см. рисунок 9):
Временная калибровка (найдите временную задержку между потоком изображения и потоком отслеживания, см. Рисунок 9A) : Наиболее распространенный способ сделать это – перемещать ультразвуковой датчик вверх и вниз в водяной бане и извлекать некоторые особенности из созданного нами -изображения (или сопоставьте изображения и измерьте смещение).Это дает нам две синусоидальные кривые, одну для вертикального положения извлеченного объекта на изображениях и одну для вертикального компонента в данных отслеживания. Две кривые сравниваются, и одна из них подгоняется к другой, чтобы определить временную задержку между двумя потоками.
Пространственная калибровка (найдите преобразование между изображением и датчиком, см. Рисунок 9B) : Значительные усилия были потрачены на калибровку датчика за последнее десятилетие, и это все еще кажется горячей темой исследований.Может быть, потому, что сделать его точным – сложная задача, особенно если один и тот же метод / фантом должен использоваться для существенно разных зондов. Невозможно измерить это преобразование с помощью линейки, потому что ориентация плоскости сканирования относительно рамки датчика неизвестна, мы не знаем происхождение плоскости us внутри корпуса датчика, а магнитные датчики не имеют известного происхождения . Обычно используемый подход к калибровке зонда – получение двухмерных изображений фантома с известной геометрией и выявление различных деталей на изображениях.Поскольку расположение одних и тех же элементов известно в глобальной системе координат, матрицу калибровки датчика можно найти с помощью относительно простого матричного уравнения. Описанные в литературе методы калибровки зондов в основном различаются геометрией фантома, тогда как обработка полученных данных более или менее обычна для всех методов. Большинство методов калибровки датчиков можно разделить на три различных класса: одноточечные или линейные; 2-мерное выравнивание; и методы от руки.Калибровочную матрицу можно рассчитать следующим образом. Получите необходимое количество калибровочных изображений и найдите координаты всех калибровочных точек на каждом изображении. Затем мы преобразуем соответствующие физические точки из глобальных опорных координат в координаты кадра датчика, используя инверсию матрицы отслеживания. Преобразование твердого тела, которое минимизирует среднее евклидово расстояние между двумя наборами гомологичных точек, будет калибровочной матрицей датчика. Матрица может быть рассчитана с использованием метода минимизации ошибок методом наименьших квадратов [58].
Рисунок 9.
Временная (A) и пространственная (B) калибровка ультразвукового датчика.
3.4. 3D Ультразвук
Трудно направить инструмент на место с помощью только обычного 2D-ультразвука (от руки): чтобы узнать, где находится инструмент, нам нужно увидеть его на ультразвуковом изображении, а для достижения цели мы должны знать, где оттуда сложная задача на зрительно-моторную координацию. Гораздо удобнее сначала получить трехмерный ультразвуковой объем и позволить отслеживаемому инструменту извлекать срезы из объема, которые могут быть аннотированы положением и / или ориентацией инструмента (см. Раздел о визуализации).
Трехмерные ультразвуковые данные могут быть получены разными способами [59]. Обычный одномерный матричный датчик (2D + t) можно перемещать по интересующей области либо движением руки, либо двигателем. Если используется движение от руки, все ультразвуковые кадры можно объединить в объем, используя данные отслеживания (рисунок 10) или корреляцию. Двигатель внутри шланга зонда или снаружи по отношению к нему также может быть использован для покрытия области интереса путем наклона, перемещения или вращения 1D-массива (рис. 11). Кроме того, с помощью двухмерного матричного датчика ультразвуковой луч можно направлять в направлении возвышения в дополнение к боковому (азимутальному) направлению, так что область интереса может быть покрыта, пока датчик неподвижен, что делает возможным трехмерное ультразвуковое изображение в реальном времени (рис. ).
Рис. 10.
Методы реконструкции: A) Ближайший сосед вокселя (VNN), B) Ближайший сосед пикселя (PNN), этап распределения (DS) и C) Функциональные методы (FBM).
Рис. 11.
Моторизованный / механический наклон (A), поступление (B) и вращение (C). Источник: Fenster [59]
Рис. 12.
Матричные зонды. Используя двумерный массив элементов (A), луч можно направлять в двух направлениях (B), и получается усеченная пирамида данных (C).
На практике используются следующие методы:
Произвольное трехмерное ультразвуковое исследование: Это все еще наиболее широко используемый метод (в основном из-за его гибкости), и обычно метод работает следующим образом: Сканировать Область интереса с использованием обычного 2D-зонда, который отслеживается и реконструирует ультразвуковые кадры с позиционной меткой в обычный 3D-объем, который можно использовать так же, как предоперационная МРТ или КТ.Ультразвуковой датчик обычно отслеживается оптическими или электромагнитными датчиками, но были предложены другие методы. Кроме того, существуют различные методы восстановления всех 2D-кадров в обычный 3D-объем. Методы можно разделить на три основные группы [60]:
Методы на основе вокселей (VBM) : VBM пересекает каждый воксель в целевой сетке вокселей и собирает информацию из входных 2D-изображений для размещения в вокселе . Один или несколько пикселей могут вносить вклад в значение каждого вокселя.Самый простой метод в этой категории – это ближайший сосед вокселя (VNN), который проходит через каждый воксель в целевом объеме и присваивает значение ближайшему пикселю изображения (см. Рисунок 10A).
Методы на основе пикселей (PBM) : PBM обычно состоит из двух этапов: этап распределения (DS), на котором входные пиксели проходят и применяются к одному или нескольким вокселям, и этап заполнения отверстий (HFS), где воксели проходят, и пустые воксели заполняются. Самый простой метод в этой категории – ближайший сосед пикселя (PNN), который проходит через каждый пиксель во всех входных 2D-изображениях и присваивает значение пикселя ближайшему вокселю в целевом объеме (см. Рисунок 10B).
Методы на основе функций (FBM) : FBM выбирает конкретную функцию (например, полином) и определяет коэффициенты, чтобы функции проходили через входные пиксели. После этого функцию можно использовать для создания регулярного массива вокселей, оценивая функцию через равные промежутки времени (см. Рисунок 10C). Эти методы позволяют получать реконструированные объемы с высочайшим качеством, но они требуют больших вычислительных ресурсов и сегодня используются ограниченно.
Моторизованный (или механический) трехмерный ультразвук : вместо использования ручного перемещения ультразвукового датчика по интересующей области двигатель может покрывать ту же область путем наклона (рисунок 11A), перемещения (рисунок 11B) или вращая (рис. 11C) обычный ультразвуковой массив 1D.Моторизованные датчики существуют уже давно, и двигатель может быть установлен либо внутри корпуса датчика (прост в использовании, но требует специального ультразвукового датчика), либо может применяться снаружи (более гибкий, чем обычные датчики). Многие из преимуществ сканирования от руки также применимы к моторизованному сканированию, например возможность использования высокочастотных датчиков с более высоким пространственным разрешением, в том числе по углу места (датчики 1.25D / 1.5D). Моторизованное сканирование может использовать те же методы реконструкции, что и сканирование от руки, но обычно используются более оптимизированные методы, поскольку движение известно, и датчик не нужно отслеживать во время сбора данных.По сравнению с ультразвуком от руки, моторизованные датчики легче использовать в интраоперационных условиях, но, с другой стороны, в целом они не так гибки.
Трехмерное ультразвуковое исследование в реальном времени с использованием двухмерных матричных датчиков [61-65]: вместо использования обычного одномерного матричного преобразователя, который перемещается от руки или с помощью двигателя для обзора интересующей анатомии, датчики с двухмерной фазовой были разработаны массивы (рис. 12А), которые могут генерировать трехмерные изображения в реальном времени. Электроника используется для управления и направления ультразвукового луча (рис. 12B) и удаления объема, имеющего форму усеченной пирамиды (рис. 12C).Основная проблема с этой технологией – большой и тяжелый кабель, который потребуется для соединения всех элементов массива с проводом. К счастью, технологические достижения в области мультиплексирования, разреженных массивов и параллельной обработки за последнее десятилетие сделали эти системы коммерчески доступными. Они широко используются в эхокардиологии, которая требует динамической трехмерной визуализации сердца и его клапанов.
3.5. Интегрированные решения для навигации на основе ультразвука
Ультразвук и навигация могут быть интегрированы разными способами, как мы видели.Полные системы обычно можно разделить на следующие категории:
Двухстоечные системы: Где навигационный компьютер с системой слежения и т. Д. И ультразвуковой сканер – это две отдельные системы. Это наиболее распространенное явление, особенно в исследовательской среде. Основная причина этого – гибкость, в принципе любой ультразвуковой сканер с аналоговым выходом можно использовать вместе с навигационной системой, которая оснащена навигационным программным обеспечением на основе ультразвука. Примером такой конфигурации является наша собственная исследовательская система для американской навигации под названием CustusX (рисунок 13A).Система используется для различных клинических применений (например, нейрохирургии и лапароскопии), каждая навигационная стойка оснащена как оптическим, так и магнитным трекингом и может быть подключена к различным ультразвуковым сканерам с использованием аналоговых и цифровых интерфейсов.
Одностоечные системы: Здесь ультразвуковой сканер и навигационный компьютер объединены в одну систему. Эти системы удобнее использовать в операционной, но они менее гибкие. К этой категории относится большинство коммерческих решений.Существует два варианта:
Ультразвуковой сканер со встроенным навигационным программным обеспечением . Примером этого является система PercuNav от Philips, интегрированное решение для навигации и интраоперационной визуализации (рис. 13B).
Навигационная система со встроенным ультразвуковым сканером : Примером этого является система SonoWand (Тронхейм, Норвегия), в которой ультразвуковой сканер встроен в навигационную стойку (рисунок 13C).Систему можно использовать тремя различными способами: 1) в качестве навигационной системы, основанной на данных предоперационной МРТ / КТ, 2) в качестве автономного ультразвукового сканера и 3) в качестве навигационной системы на основе ультразвука с возможностями интраоперационной визуализации, ее основное применение.
Рис. 13.
Различные подходы к интеграции (3D) ультразвука и навигации. A) Решение с двумя стойками и примеры решений с одной стойкой (B и C).
4. Регистрация и сегментация в навигации на основе ультразвука
Регистрация – это процесс преобразования изображения в систему координат пациента или другого изображения.После регистрации одинаковые анатомические элементы имеют одинаковые координаты как на изображении, так и на пациенте или на обоих изображениях. Регистрация изображения пациента является одним из краеугольных камней любой навигационной системы и необходима для навигации с использованием дооперационных изображений, таких как МРТ и / или КТ. Преобразование изображения в изображение полезно для выравнивания предоперационных изображений перед регистрацией для пациента, а также для обновления дооперационных изображений во время операции, например, с использованием интраоперационного УЗИ. Только в последнем случае используется УЗИ, и он будет в центре внимания в этом разделе, но регистрация изображения пациента важна для правильной инициализации регистрации МРТ / КТ в УЗИ.Основная мотивация совмещения изображения с изображением заключается в том, что разные изображения содержат разную и дополнительную информацию о пациенте в данный момент времени. Когда мы переносим изображения в одну и ту же систему координат и в систему координат пациента, мы можем извлечь больше полезной информации из разных изображений. Такой информацией могут быть размер и расположение хирургической мишени, важные кровеносные сосуды, критические структуры, которых следует избегать и т. Д. Метод регистрации, используемый в каждом случае, сильно зависит от типа изображений, которые мы хотим зарегистрировать.Тип пространственного преобразования, то, как мы измеряем сходство между изображениями и как эта мера оптимизируется, являются ключевыми компонентами любой процедуры регистрации.
4.1. Регистрация предоперационных изображений пациенту
Регистрация изображения пациента является необходимым и решающим шагом для использования предоперационных изображений в качестве руководства. Интраоперационное ультразвуковое исследование показывает только ограниченную часть операционного поля, и для его оценки может потребоваться некоторый опыт. Таким образом, предоперационные данные можно использовать для обзора и интерпретации.Например, в нейрохирургии невозможно получить ультразвуковые изображения до вскрытия твердой мозговой оболочки. Поэтому для планирования трепанации черепа необходимы дооперационные изображения.
Один из наиболее часто используемых методов регистрации заключается в использовании самоклеящихся маркеров, также называемых реперными точками. Реперные точки приклеиваются к коже пациента перед МРТ или КТ. Маркеры могут быть идентифицированы на изображениях, а соответствующие маркеры могут быть идентифицированы на пациенте с помощью отслеживаемого указателя, как только пациент будет иммобилизован на операционном столе (рис. 14).Затем можно вычислить пространственное преобразование, преобразующее изображение в систему координат пациента. Затем хирург может указать на пациента с помощью отслеживаемого указателя и увидеть соответствующее место на изображениях на экране компьютера. Использование маркеров для регистрации изображения пациента представляет некоторые ограничения как для пациента, так и для персонала больницы. Во-первых, регистрация на основе реперных точек требует сеанса визуализации незадолго до операции, чтобы свести к минимуму риск выпадения или смещения маркеров.Во многих случаях этот сеанс визуализации проводится в дополнение к первоначальному сеансу, необходимому для диагностики. Любое смещение реперных маркеров между сеансом визуализации и операцией поставит под угрозу точность регистрации изображения пациента. Размещение реперных знаков также создает неудобства для пациентов и персонала больницы при подготовке к процедуре.
Рис. 14.
Регистрация изображения пациента с использованием соответствующих точек между пространством изображения (A) и физическим пространством (B).
Чтобы избежать использования реперных маркеров, при регистрации пациентов можно использовать естественные анатомические ориентиры. Типичными особенностями нейрохирургии являются медиальный и латеральный уголки глаз, нос и уши. Как и регистрация на основе реперных точек, структура регистрации изображения пациента с использованием естественных анатомических ориентиров требует идентификации точек на дооперационных изображениях. Обычно используемые ориентиры почти копланарны, и все они расположены на относительно небольшой площади вокруг лица и ушей.Это может поставить под угрозу точность регистрации в других частях головы и, возможно, рядом с хирургической мишенью [66]. Ряд групп представили методы согласования поверхностей для решения этой проблемы. Поверхность кожи пациента сегментируется на основе предоперационных данных и регистрируется в наборе точек поверхности, полученных в операционной. Методы получения точек на поверхности в операционной включают камеры [67, 68], лазерные сканеры поверхности [69–71] и указатели с отслеживанием [72]. Точность различных методов оценивалась и сравнивалась [71, 73-75].Регистрация ориентиров и только по поверхности менее точна, чем регистрация на основе реперных точек. Поэтому были разработаны различные подходы, сочетающие регистрацию на основе анатомических ориентиров и выравнивание поверхностей.
По мере продолжения операции ткань будет смещаться и деформироваться под действием силы тяжести, ретракции, резекции и введения лекарств. Следовательно, дооперационные изображения больше не соответствуют пациенту. В этом случае интраоперационный ультразвук можно использовать для прямого руководства и обновления местоположения дооперационных данных в соответствии с хирургической реальностью в данный момент времени.
4.2. Обновление предоперационных данных на основе ультразвука
По мере продолжения операции предоперационные изображения больше не отражают реальность, и для точной навигации необходима обновленная информация. При необходимости во время процедуры можно получить интраоперационный ультразвук и использовать его для прямого наведения и контроля резекции, а также в качестве цели регистрации для предоперационных изображений, чтобы обновить их положение. Это особенно важно для изображений, таких как функциональная МРТ (фМРТ) и диффузионно-тензорная визуализация (DTI) в нейрохирургии, потому что информацию, содержащуюся в этих изображениях, нельзя легко повторно получить во время процедуры.Выполняя регистрацию MR / CT-to-US, информация, содержащаяся в дооперационных изображениях, может быть перемещена в правильное положение в любой заданный момент времени (рисунок 15). Регистрация МРТ / КТ в УЗИ является сложной задачей из-за различий в внешнем виде изображений и шумовых характеристиках. Существующие методы можно разделить на две основные категории:
Методы на основе интенсивности : Эти методы принимают исходные изображения (MR / CT и B-режим US) в качестве входных данных, и вычисляется оптимизация параметров регистрации. прямо или косвенно (размытие, градиенты и т. д.) от интенсивности изображения.). Некоторые из существующих методов используют хорошо известные меры сходства, такие как взаимная информация и взаимная корреляция, в то время как другие разработали меры сходства, особенно адаптированные для регистрации МРТ / КТ и ультразвука [76–82].
На основе характеристик
Терапевтический ультразвук – ФИЗИЧЕСКАЯ ТЕРАПИЯ WEB
Что такое терапевтический ультразвук?
Терапевтический ультразвук – это метод, который используется физиотерапевтами с 1940-х годов.Ультразвук применяется с помощью палочки с круглой головкой или зонда, который находится в прямом контакте с кожей пациента. Ультразвуковой гель наносится на все поверхности головы, чтобы уменьшить трение и способствовать передаче ультразвуковых волн. Лечебный ультразвук находится в диапазоне частот примерно 0,8-3,0 МГц.
Волны генерируются пьезоэлектрическим эффектом, вызванным вибрацией кристаллов внутри головки палочки / зонда. Звуковые волны, проходящие через кожу, вызывают вибрацию местных тканей.Эта вибрация или кавитация могут вызвать локальный глубокий нагрев, хотя обычно пациент не ощущает тепла. В ситуациях, когда эффект нагрева нежелателен, например, свежая травма с острым воспалением, ультразвук может быть импульсным, а не непрерывным.
Ультразвук может вызывать множество эффектов, помимо потенциального теплового эффекта. Было показано, что он вызывает усиление релаксации тканей, локальный кровоток и разрушение рубцовой ткани. Эффект увеличения местного кровотока может быть использован для уменьшения местного отека и хронического воспаления, а также, согласно некоторым исследованиям, для ускорения заживления переломов костей.Интенсивность или плотность мощности ультразвука можно регулировать в зависимости от желаемого эффекта. Большая удельная мощность (измеряется в ватт / см) 2 часто используется в тех случаях, когда целью является разрушение рубцовой ткани.
Ультразвук также можно использовать для достижения фонофореза. Это неинвазивный способ введения лекарств в ткани под кожей; это идеально подходит для пациентов, которым неудобно делать инъекции. При использовании этой техники ультразвуковая энергия проталкивает лекарство через кожу.Кортизон, используемый для уменьшения воспаления, является одним из наиболее часто используемых веществ, доставляемых таким образом.
Терапевтический ультразвук на плечо
Чего мне следует ожидать от лечения ультразвуком?Обычное ультразвуковое лечение занимает от 3 до 5 минут в зависимости от размера обрабатываемой области. В случаях, когда целью является разрушение рубцовой ткани, это время лечения может быть намного больше. Во время лечения головка ультразвукового зонда находится в постоянном движении.При постоянном движении пациент не должен чувствовать дискомфорта. Если зонд удерживать в одном месте дольше нескольких секунд, это может привести к накоплению звуковой энергии, что может вызвать дискомфорт. Интересно, что при очень небольшом переломе кости в области, близкой к поверхности, может ощущаться резкая боль. Это происходит, когда звуковые волны захватываются между двумя частями разрыва и накапливаются, пока не станут болезненными. Таким образом, ультразвук часто может использоваться как довольно точный инструмент для диагностики мелких переломов, которые могут быть не видны на рентгеновском снимке.
Какие состояния можно лечить с помощью терапевтического ультразвука?Некоторые состояния, которые лечат с помощью ультразвука, включают тендинит (или тендинит, если хотите), неострый отек суставов, мышечный спазм и даже болезнь Пейрони (для разрушения рубцовой ткани).
Какие противопоказания к УЗИ?Противопоказания к ультразвуку включают местные злокачественные новообразования, металлические имплантаты ниже обрабатываемой области, местную острую инфекцию, сосудистые аномалии и непосредственно на животе беременных женщин.Также противопоказано применение ультразвука непосредственно над активными эпифизарными областями (пластинами роста) у детей, над спинным мозгом в области ламинэктомии, над глазами, черепом или яичками.
В чем разница между терапевтическим ультразвуком и диагностическим ультразвуком?Терапевтический ультразвук используется как форма лечения, помогающая заживлению тканей, в то время как диагностический ультразвук используется для получения изображений структур внутри тела.Обе формы ультразвука используют высокочастотные звуковые волны. Диагностический ультразвук также широко известен как «сонография». Хотя диагностический ультразвук можно использовать для диагностики заболеваний, одно из наиболее распространенных его применений – это обследование развивающегося ребенка в утробе матери.
Видео: терапевтическое ультразвуковое исследование
Нравится:
Нравится Загрузка …
Ультразвуковое сканирование – NHS
Ультразвуковое сканирование, иногда называемое сонограммой, – это процедура, при которой используются высокочастотные звуковые волны для создания изображения части внутренней части тела.
Ультразвуковое сканирование можно использовать для наблюдения за нерожденным ребенком, диагностики состояния или руководства хирурга во время определенных процедур.
Как работают ультразвуковые исследования
Используется небольшое устройство, называемое ультразвуковым датчиком, которое излучает высокочастотные звуковые волны.
Эти звуковые волны не слышны, но когда они отражаются от разных частей тела, они создают «эхо», которое улавливается зондом и превращается в движущееся изображение.
Это изображение отображается на мониторе во время сканирования.
Подготовка к УЗИ
Перед проведением некоторых видов ультразвукового сканирования вас могут попросить выполнить определенные инструкции, которые помогут улучшить качество получаемых изображений.
Например, вам могут посоветовать:
- пейте воду и не ходите в туалет до завершения сканирования – это может потребоваться перед сканированием вашего будущего ребенка или области вашего таза
- воздержитесь от еды и питья в течение нескольких часов перед сканированием – это может потребоваться перед сканированием вашей пищеварительной системы, включая печень и желчный пузырь
В зависимости от исследуемой области вашего тела в больнице могут попросить вас снять одежду и надеть больничную одежду.
Если вам нужно успокоительное, чтобы расслабиться, его вводят через маленькую трубку в тыльную сторону ладони или в руку.
В некоторых случаях вам также могут сделать инъекцию безвредного вещества, называемого контрастным веществом, перед сканированием, так как это может сделать изображения более четкими.
Что происходит во время ультразвукового сканирования
Большинство ультразвуковых сканирований длится от 15 до 45 минут. Обычно они проводятся в радиологическом отделении больницы и выполняются радиологом или сонографистом.
Они также могут проводиться в общественных местах, таких как врачи общей практики, и могут выполняться другими медицинскими работниками, такими как акушерки или физиотерапевты, которые прошли специальную подготовку в области ультразвуковой диагностики.
Существуют разные виды ультразвукового сканирования, в зависимости от того, какая часть тела сканируется и почему.
3 основных типа:
- внешнее ультразвуковое сканирование – зонд перемещается по коже
- внутреннее ультразвуковое сканирование – зонд вставлен в тело
- эндоскопическое ультразвуковое сканирование – зонд прикрепляется к длинной тонкой гибкой трубке (эндоскоп) и продвигается дальше в тело
Эти методы описаны ниже.
Наружное ультразвуковое исследование
Кредит:Peter Widmann / Alamy Stock Photo
https://www.alamy.com/stock-photo-pregnant-woman-getting-an-ultrasound-checkup-13287915.html?pv=1&stamp=2&imageid=858EDDE9-62F3-4E6F-9888-BE3E856C8DF9&p=28858&n = 0 & pn = 1 & searchtype = 0 & IsFromSearch = 1 & srch = foo% 3dbar% 26st% 3d0% 26pn% 3d1% 26ps% 3d100% 26sortby% 3d2% 26resultview% 3dsortbyPopular% 26npgs% 3d0% 26qt% 3dAD321G% 26qADt321G % 3d0% 26pr% 3d0% 26ot% 3d0% 26creative% 3d% 26ag% 3d0% 26hc% 3d0% 26pc% 3d% 26blackwhite% 3d% 26cutout% 3d% 26tbar% 3d1% 26et% 3d0x000000000000000000000% 26vp% 3d0% 26loc% 3d0 % 26imgt% 3d0% 26dtfr% 3d% 26dtto% 3d% 26size% 3d0xFF% 26archive% 3d1% 26groupid% 3d% 26pseudoid% 3d731695% 26a% 3d% 26cdid% 3d% 26cdsrt% 3d% 26name% 3d% 26qn% 3d% 26apalib % 3d% 26apalic% 3d% 26lightbox% 3d% 26gname% 3d% 26gtype% 3d% 26xstx% 3d0% 26simid% 3d% 26saveQry% 3d% 26editorial% 3d1% 26nu% 3d% 26t% 3d% 26edoptin% 3d% 26customgeoip% 3d % 26cap% 3d1% 26cbstore% 3d1% 26vd% 3d0% 26lb% 3d% 26fi% 3d2% 26edrf% 3d0% 26ispremium% 3d1% 26flip% 3d0% 26pl% 3d
Наружное ультразвуковое сканирование чаще всего используется для исследования вашего сердца или еще не родившегося ребенка в утробе матери.
Его также можно использовать для исследования печени, почек и других органов в области живота и таза, а также других органов или тканей, которые можно оценить через кожу, например, мышц и суставов.
Небольшой портативный зонд помещается на вашу кожу и перемещается по исследуемой части тела.
Смазывающий гель наносится на кожу, чтобы датчик двигался плавно. Это также обеспечивает постоянный контакт между датчиком и кожей.
Вы не должны ощущать на коже ничего, кроме датчика и геля (которая часто бывает холодной).
Если вам проводят сканирование матки или области таза, возможно, у вас полный мочевой пузырь, что вызывает у вас небольшой дискомфорт.
Рядом будет туалет, где можно опорожнить мочевой пузырь после завершения сканирования.
Внутреннее или трансвагинальное ультразвуковое исследование
Кредит:A. NOOR / BSIP / НАУЧНАЯ ФОТОБИБЛИОТЕКА
https://www.sciencephoto.com/media/865228/view
Внутренний осмотр позволяет врачу более внимательно изучить такие органы, как предстательная железа, яичники или матка.
«Трансвагинальное» УЗИ означает «через влагалище». Во время процедуры вас попросят лечь на спину или на бок, подтянув колени к груди.
Небольшой ультразвуковой зонд со стерильным покрытием, не намного шире пальца, затем осторожно вводится во влагалище или прямую кишку, и изображения передаются на монитор.
Внутреннее обследование может вызвать некоторый дискомфорт, но обычно не вызывает боли и не занимает много времени.
Эндоскопическое УЗИ
Кредит:LA LOUVIERE / ASTIER / НАУЧНАЯ ФОТОБИБЛИОТЕКА
https://www.sciencephoto.com/media/104779/view
Во время эндоскопического ультразвукового сканирования эндоскоп вводится в ваше тело, обычно через рот, чтобы исследовать такие области, как желудок или пищевод (пищевод).
Обычно вас просят лечь на бок, когда эндоскоп осторожно прижимают к вашему животу.
Эндоскоп имеет на конце светильник и ультразвуковое устройство. После того, как он вставлен в тело, звуковые волны используются для создания изображений так же, как и внешний ультразвук.
Обычно вам дают успокаивающее средство и спрей для местной анестезии, чтобы обезболить горло, поскольку эндоскопическое ультразвуковое сканирование может быть неудобным и вызывать тошноту.
Вам также могут дать капу, чтобы держать рот открытым и защитить зубы на случай, если вы прикусите эндоскоп.
После УЗИ
В большинстве случаев последствия отсутствуют, и вы можете вернуться домой вскоре после завершения сканирования.
Если успокаивающее средство не использовалось, вы можете водить машину, есть, пить и сразу же возвращаться к своим обычным занятиям.
Если вам сделали эндоскопическое ультразвуковое исследование и вам дали успокаивающее средство, чтобы помочь вам расслабиться, вам обычно рекомендуется оставаться в больнице на несколько часов, пока действие лекарства не прекратится.
Вам нужно будет попросить кого-нибудь забрать вас из больницы и остаться с вами в течение следующих 24 часов.
В это время нельзя водить машину, употреблять алкоголь и работать с механизмами.
Вам могут сообщить результаты сканирования вскоре после его проведения, но в большинстве случаев изображения необходимо будет проанализировать, и отчет будет отправлен врачу, который направил вас на сканирование.
Они обсудят с вами результаты через несколько дней или на следующей встрече, если она будет назначена.
Есть ли риски или побочные эффекты?
Звуковые волны, используемые при ультразвуковом сканировании, не представляют опасности. В отличие от некоторых других сканирований, таких как компьютерная томография, ультразвуковое сканирование не требует воздействия радиации.
Наружное и внутреннее ультразвуковое сканирование не имеет побочных эффектов и, как правило, безболезненно, хотя вы можете испытывать некоторый дискомфорт, когда датчик прижимается к вашей коже или вводится в ваше тело.
Если у вас есть внутреннее сканирование и у вас аллергия на латекс, важно сообщить об этом специалисту по сонографии или врачу, проводящему сканирование, чтобы они могли использовать крышку зонда без латекса.
Эндоскопическое ультразвуковое исследование может быть немного более неудобным и может вызвать временные побочные эффекты, такие как боль в горле или вздутие живота.
Также существует небольшой риск более серьезных осложнений, таких как внутреннее кровотечение.
Последняя проверка страницы: 25 мая 2018 г.
Срок следующей проверки: 25 мая 2021 г.
Новый метод позволяет ультразвуку проникать в кость и металл – ScienceDaily
Исследователи из Университета штата Северная Каролина разработали метод, который позволяет ультразвуку проникать в кости или металл, используя индивидуальные структуры, которые компенсируют искажения, обычно вызываемые этими так называемыми «аберрациями». слои.«
«Мы разработали дополнительные метаматериалы, которые упростят для медицинских работников использование ультразвука для диагностических или терапевтических целей, таких как мониторинг кровотока в головном мозге или для лечения опухолей головного мозга», – говорит Тарри Чен Шен, доктор философии. студент NC State и ведущий автор статьи о работе. «Раньше это было сложно, потому что череп искажает акустическое поле ультразвука».
«Эти метаматериалы также могут быть использованы в промышленных условиях», – говорит д-р.Юнь Цзин, доцент кафедры машиностроения и аэрокосмической техники в штате Северная Каролина и старший автор статьи. «Например, это позволит вам использовать ультразвук для обнаружения трещин в крыльях самолета под металлической« обшивкой »крыла».
Ультразвуковая визуализация основана на излучении высокочастотных акустических волн. Когда эти волны отражаются от объекта, они возвращаются к ультразвуковому оборудованию, которое преобразует волны в изображение.
Но некоторые материалы, такие как кость или металл, обладают физическими характеристиками, которые блокируют или искажают акустические волны ультразвука.Эти материалы называются аберрирующими слоями.
Исследователи решили эту проблему, разработав индивидуальные структуры метаматериалов, которые учитывают акустические свойства аберрирующего слоя и компенсируют их. В структуре из метаматериала используется серия мембран и небольших трубок для достижения желаемых акустических характеристик.
Исследователи протестировали эту технику с помощью компьютерного моделирования и находятся в процессе разработки и тестирования физического прототипа.
При моделировании только 28 процентов энергии ультразвуковой волны проходит через аберрирующий слой кости, когда структура метаматериала не на месте. Но для структуры метаматериала моделирование показывает, что 88 процентов энергии ультразвуковой волны проходит через аберрирующий слой.
«Фактически, аберрирующего слоя даже нет», – говорит Цзин.
Этот метод можно использовать для ультразвуковой визуализации, а также в терапевтических целях – например, использование ультразвука для подачи энергии на опухоли головного мозга, чтобы сжечь их.
История Источник:
Материалы предоставлены Государственным университетом Северной Каролины .

 Когда врач выявляет увеличение органа, то он может диагностировать тимомелагию.
Когда врач выявляет увеличение органа, то он может диагностировать тимомелагию.

 html и прочтите о том, что такое диабетическая ретинопатия и как лечить осложнение эндокринной патологии.
html и прочтите о том, что такое диабетическая ретинопатия и как лечить осложнение эндокринной патологии.


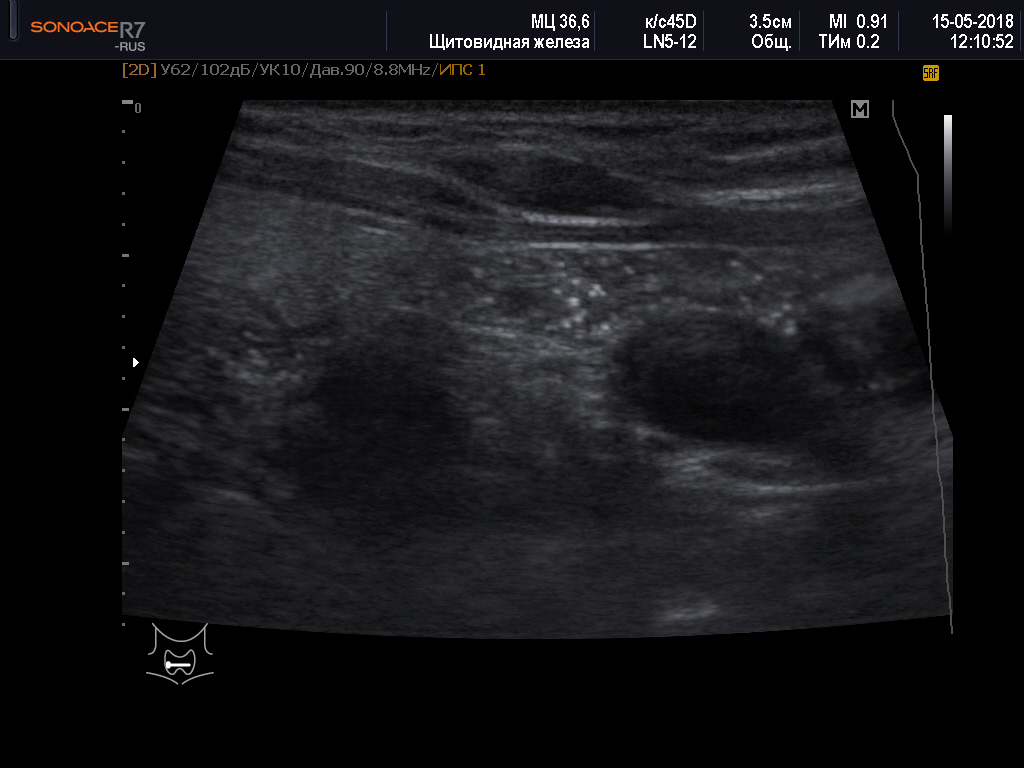 Обратите внимание, что киста анэхогенная, в отличие от эхогенного твердого поражения печени (твердое поражение было показано на КТ-сканировании как гемангиома).
Обратите внимание, что киста анэхогенная, в отличие от эхогенного твердого поражения печени (твердое поражение было показано на КТ-сканировании как гемангиома).