Чем отличаются симптомы ОРВИ (простуда) и гриппа: основные отличия
Организм человека устроен таким образом, что в определённые периоды его защитные свойства существенно ослабевают. С наступлением холодов, функционирование иммунной системы организма заметно снижается, в результате чего человек часто болеет. Вследствие продолжительного пребывания в условиях низкой температуры, существенно возрастает риск заболеть.
Осенне-весенний период является идеальным временем для активной деятельности различных патогенов, вызывающих у большинства населения всевозможные недомогания. В лучшем человека может беспокоить банальный насморк с лёгким першением в горле, но, а в худшем грипп, с последующими осложнениями.
ОРВИ и грипп — это болезни, которые заметно снижают качественный уровень жизни и могут существенно выбить из привычного ритма, причиняя человеку ряд неудобств. Клиническую картину гриппа и ОРВИ часто путают. Сходство симптомов этих заболеваний во многом обусловлено тем фактом, что в основе их развития лежат вирусные организмы, похожие по своему строению, функционированию и размножению.
ОРВИ
В связи с распространённостью данного заболевания, вполне логичным является вопрос, задаваемым пациентами: «Чем отличается грипп от ОРВИ?». При постановке диагноза ОРВИ, необходимо помнить, что эта патология считается собирательным термином, который используют врачи в отношении болезней, поражающих дыхательную систему человека и имеющих вирусное происхождение. К этой группе относятся — вирус гриппа и парагриппа, возбудитель аденовирусной и риновирусной инфекции.
Большинство людей, ОРВИ именуют обычной простудой, подразумевая, что вследствие переохлаждения, человек заболел. Однако необходимо помнить, что холод – это всего лишь фактор, благоприятствующий недомоганию, а причиной болезней являются вирусы и бактерии. Для болезней, объединённых в группу ОРВИ характерны воспалительные симптомы, проявляющиеся стремительным образом.
Буквально в течение нескольких часов на фоне общей слабости организма возникают:
- высокая температура;
- лихорадочное состояние;
- интенсивное потоотделение.

Заражение вирусными заболеваниями происходит в результате контакта здорового человека с носителем вирусной инфекции.
Основной путь передачи – воздушно-капельный. Характерной особенностью респираторных патологий является их быстрое распространение и высокий уровень заразности. Согласно медицинским наблюдениям у 85% людей, имевших контакт с возбудителем заболевания, спустя короткое время, проявляются симптомы воспалительного характера. Подобные статистические данные во многом обуславливаются тем фактом, что по причине постоянной мутации и видоизменения вируса, организм человека не успевает выработать антитела к новому штамму. Поэтому от респираторных недугов никто не застрахован.
Грипп
По причине легкомысленного отношения к гриппу, многие люди подвергают свою жизнь серьёзной опасности. Необходимо помнить, что грипп, без преувеличения, считается одним из наиболее грозных недугов, вызываемых патогенной активностью вируса.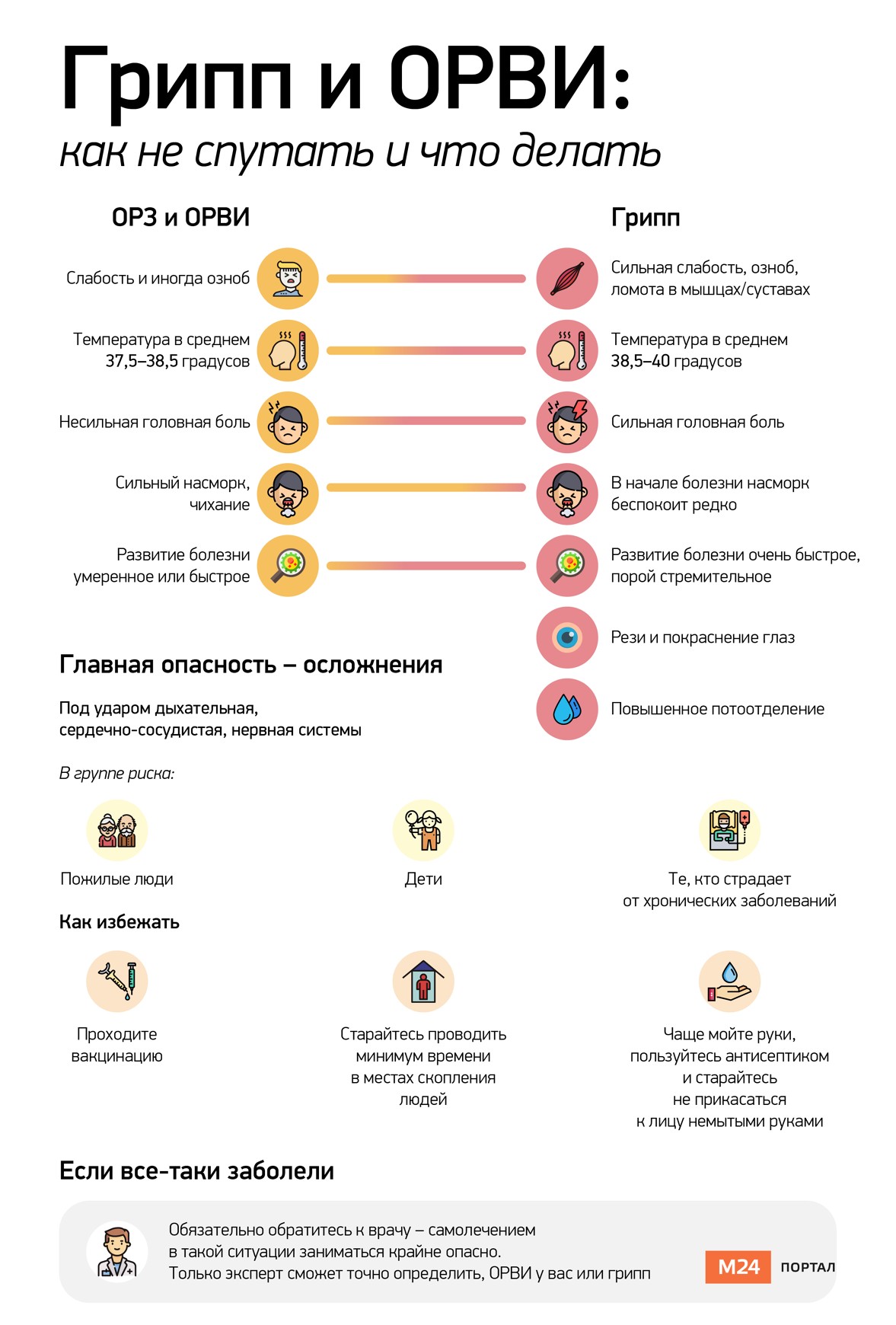 Практически каждый год, глобальные пандемии и эпидемии, приводят к тому, что около 400 тыс. от общего количества заболевших людей умирают. В связи с этим принципиально важно понимать отличие гриппа от ОРВИ на раннем этапе болезни, чтобы своевременно подобрать действенную схему лечения.
Практически каждый год, глобальные пандемии и эпидемии, приводят к тому, что около 400 тыс. от общего количества заболевших людей умирают. В связи с этим принципиально важно понимать отличие гриппа от ОРВИ на раннем этапе болезни, чтобы своевременно подобрать действенную схему лечения.
Будучи самой древней формой жизни на земле, вирусы часто видоизменяются, приспосабливаясь, таким образом, к новым условиям своего обитания. Не удивительно, что на сегодняшний день различают около 1,5 тыс. разновидностей вируса.
Самыми грозными представителями являются возбудители испанского, свиного и птичьего гриппа. Подобно остальным представителям ОРВИ, грипп распространяется воздушно-капельным путём и обладает высокой степенью инфицирования. Это свойство во многом обусловлено инкубационным периодом гриппа и ОРВИ, который в среднем составляет 3 дня. Этого времени вполне достаточно для того, чтобы инфицированный человек заразил как можно больше людей.У людей с хорошим иммунитетом симптомы гриппа проходят в средней форме тяжести.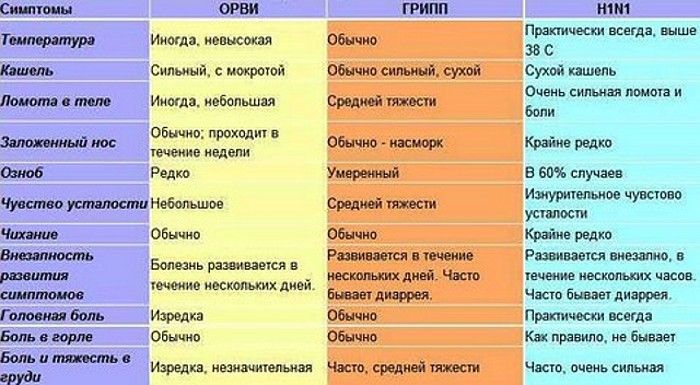 Тяжёлый ход болезни, отмечается преимущественно у детей, чья иммунная система ещё не сформировалась, или у пожилых людей, у которых защитные свойства организма ослаблены в силу возрастных причин.
Тяжёлый ход болезни, отмечается преимущественно у детей, чья иммунная система ещё не сформировалась, или у пожилых людей, у которых защитные свойства организма ослаблены в силу возрастных причин.
Клиническая картина данного недуга проявляется в виде:
- головных болей;
- болезненности глаз;
- общей слабости;
- лихорадочного состояния.
Вследствие сильной интоксикации мышцы тела начинают болеть, а суставы крутить. Симптомы общего воспаления сопровождаются высокой температурой, в некоторых случаях, достигающей отметки 40 градусов. Лихорадочное состояние может длиться от 5 до 7 дней. К 4 дню, пациент жалуется на приступы сухого кашля, першение в горле и обильные слизистые выделения в результате насморка. Прогрессирование патологии проявляется симптомами бронхита.
Опасность вирусного недуга состоит в том, что у людей с ослабленным иммунитетом могут возникнуть осложнения в виде пневмонии или недостаточности сердечно сосудистой системы.
Для того чтобы понять как отличить грипп от простуды необходимо иметь представление о других респираторных заболеваниях, объединённых под общим названием ОРВИ.
Парагрипп
Такое название во многом обусловлено схожестью клинической картины гриппа и парагриппа. Прежде всего, человек жалуется на сухой кашель, дискомфортный насморк, боль в глазном яблоке и лихорадку. Во многих случаях отмечается присоединение вторичного инфекционного процесса, поражающего глаза. Отличительной особенностью парагриппа от гриппа является меньшая степень выраженности клинических симптомов. Температура тела колеблется от 37,5 до 38 градусов и на 3 день снижается. Воспаление гортани может привести к потере голоса или появлению характерной хриплости в комплексе с мучительным сухим кашлем.
Аденовирусная инфекция
Подобно гриппу, этот недуг проявляется стремительно. Высокая температура тела сохраняется в течение 8 дней. Существенным отличием этого заболевания от гриппа считается наличие сильно выраженных катаральных явлений (боль в горле, резь в глазах, насморк). К аденовирусному конъюнктивиту может присоединиться бактериальная инфекция, в результате чего слизистые выделения приобретают
К аденовирусному конъюнктивиту может присоединиться бактериальная инфекция, в результате чего слизистые выделения приобретают
Как поставить диагноз?
Чтобы поставить диагноз ОРВИ, врач проводит, визуальный осмотр. В большинстве случаев этого вполне достаточно. Но чтобы узнать, каким именно патогеном вызвана простуда, одного поверхностного обследования будет недостаточно, потому что клиническая картина гриппа от ОРВИ практически не отличается. В таком случае актуальным будет проведение более глубоких диагностических мероприятий с помощью лабораторных исследований. Именно обнаружение вируса в крови пациента позволит специалисту, с высокой степенью вероятности, понять, какой именно респираторной патологией заболел человек.
К каждому вирусу иммунная система вырабатывает определённые, свойственные только ему, антитела.
В редких случаях лишь первые пациенты проходят лабораторное обследование, а последующие получают диагноз автоматически. Как раз именно это является основной причиной того, что терапия вирусной простуды часто не приводит к положительной динамике, а даже наоборот, может стать причиной серьёзных осложнений. В связи с этим крайне важно, людям неискушённым в тонкостях медицины, знать, как отличить простуду от вируса гриппа.
Начало заболевания
Невзирая на то, что ОРВИ, именуемое в народе простудой, имеет схожую симптоматику с гриппом, между ними имеются отличия, которые помогут человеку определить, чем он заболел.
Грипп отличается от простуды
- Начальный этап ОРВИ слегка затянут, и составляет в среднем 48 часов.

- Симптомы простуды выражены слабо, однако, они причиняют человеку неудобства.
- Незначительный насморк и лёгкая болезненность в горле сопровождаются небольшим повышением температуры на фоне общей слабости.
Вирус гриппа отличается от простуды, способностью за считаные часы, после попадания в организм, вызвать его серьёзную интоксикацию. Внезапно возникшая высокая температура и полная потеря работоспособности – результат первых часов патологической активности гриппа. Резкое и молниеносное начало – вот что отличает грипп от ОРВИ.
Температура
Любая простуда сопровождается повышением температуры тела и это тот момент, который объединяет все респираторные недуги. Однако есть и отличие. Для гриппа характерен быстрый прыжок температуры, буквально в течение 1,5 часа, от 37 до 40 градусов. Применение лекарственных препаратов с жаропонижающим действием желаемого результата не дают. Только инъекции могут привести к непродолжительному снижению температуры, которая, спустя несколько часов, вновь устремляется вверх.
ОРВИ отличается относительно невысокими показателями, которые не превышают 38,5 градусов. В большинстве случаев достаточно употребить парацетамол, чтобы температура отступила. Многие терапевты рекомендуют даже воздержаться от использования жаропонижающих препаратов при простуде, чтобы иммунная система без посторонней помощи поборола заболевание. Такие эксперименты актуальны только в отношении взрослых людей, касательно детей, то самолечение категорически запрещено. При появлении у малыша первых симптомов простуды необходимо отправиться за консультацией к педиатру. От того, как быстро маленького пациента осмотрит врач, зависит здоровье ребёнка.
Общая интоксикация
Простуда и грипп, в равной степени, вызывают общее ослабление организма, что приводит к дискомфортному состоянию. В этом случае простуда отличается от гриппа тем, что симптомы общего недомогания хоть и присутствуют в течение всего заболевания, но выражены слабее. Интенсивность мышечных и головных болей при простуде практически не доставляет проблем больному. Болезнетворная деятельность вируса гриппа приводит к сильной ломоте в теле, приступообразной боли в височной области и сильному лихорадочному состоянию.
Болезнетворная деятельность вируса гриппа приводит к сильной ломоте в теле, приступообразной боли в височной области и сильному лихорадочному состоянию.
Заложенный нос
При простуде происходит поражение верхних дыхательных путей. Любая форма ОРВИ проявляется кашлем и насморком. Грипп отличается тем, что воспалительные явления на слизистой оболочке носа отмечаются в исключительных случаях. В среднем, при наличии таковых, уже на 3 день, эти симптомы проходят. Эта характерная особенность даёт возможность отличать грипп от ОРВИ, так как при респираторной простуде к концу дня закладывается нос. По мере прогрессирования респираторного вируса человека начинает беспокоить интенсивный насморк на фоне обильного слезоотделения.
Горло
Чтобы отличить ОРВИ от гриппа, необходимо присмотреться к состоянию слизистой оболочки горла. Воспалительные процессы, вызванные вирусом гриппа, отличаются выраженной гиперемией мягкого нёба и горла. То же самое, можно увидеть, обследовав пациента, болеющего ОРВИ, но присутствие налёта на слизистой оболочке свойственно исключительно в отношении респираторных недугов.
То же самое, можно увидеть, обследовав пациента, болеющего ОРВИ, но присутствие налёта на слизистой оболочке свойственно исключительно в отношении респираторных недугов.
Бронхи
Важным признаком недомогания является кашель. ОРВИ отличается тем, что этот симптом проявляется на раннем этапе патологического процесса, а уже после дополняется насморком и температурой. Относительно гриппа ситуация несколько другая, изначально, больного беспокоит высокая температура в комплексе с головной болью и мышечной ломотой, а лишь на второй день проявляется кашель.
Длительность заболевания
Прежде всего, респираторная инфекция при эффективном лечении существенно ослабевает на 4 день. Строгое следование курсу терапии приводит к полному выздоровлению в течение недели. Восстановления организма проходит быстро и без осложнений. Все респираторно-вирусные инфекции имеют приблизительно одинаковый инкубационный период. Однако при гриппе течение патологического процесса существенно растянуто во времени. Одна только температура может удерживаться на высоких отметках на протяжении целой недели, а первые признаки выздоровления, в среднем, наступают к 12 дню.
Одна только температура может удерживаться на высоких отметках на протяжении целой недели, а первые признаки выздоровления, в среднем, наступают к 12 дню.
Но в любом случае отличие гриппа от ОРВИ достаточно заметно, поэтому проблем с определением недуга, скорее всего, не возникнет.
Грипп, ОРЗ и ОРВИ у ребенка
Грипп, ОРЗ, ОРВИ – это три болезни с похожими симптомами.
В чем разница между ними?Прежде всего, она заключается в продолжительности и возможных последствиях заболеваний.
Видео: Как отличить ОРЗ, ОРВИ и ГРИПП
Клиническая картина ОРЗ, ОРВИ и гриппа
Ответить на вопрос, чем отличается грипп от ОРВИ и ОРЗ, нельзя без знания возбудителей и симптоматики заболеваний.
Грипп
Грипп – это тип ОРВИ, вызываемый вирусом гриппа. Существует много разных штаммов этих вирусов, путем мутаций создаются новые штаммы. Грипп поражает взрослых людей чаще, чем детей, распространяется капельным путем (кашель, чихание).
Существует много разных штаммов этих вирусов, путем мутаций создаются новые штаммы. Грипп поражает взрослых людей чаще, чем детей, распространяется капельным путем (кашель, чихание).
Инкубационный период гриппа – приблизительно 1-2 дня. Симптомы развиваются в течение 24 часов. Типичным для болезни является внезапное вспыхивание, человек резко ощущает слабость, сильную лихорадку с ознобом, головными, мышечными суставными болями. Через несколько дней возникает кашель. Грипп у детей характеризуется потерей аппетита, иногда рвотой, диареей. Симптомы гриппа более серьезны, чем признаки ОРЗ.
Относительно эффективная профилактика гриппа – вакцина. Но вакцинация не обеспечивает 100% защиты, особенно если эпидемия порождает новый неизвестный вирус. Из-за высокой мутагенной способности, отдельные вакцины против гриппа эффективны только на один год.
ОРЗ
Основное отличие гриппа и ОРЗ – возбудители.
Что такое ОРЗ?
ОРЗ – это заболевание дыхательных путей, вызываемое риновирусами.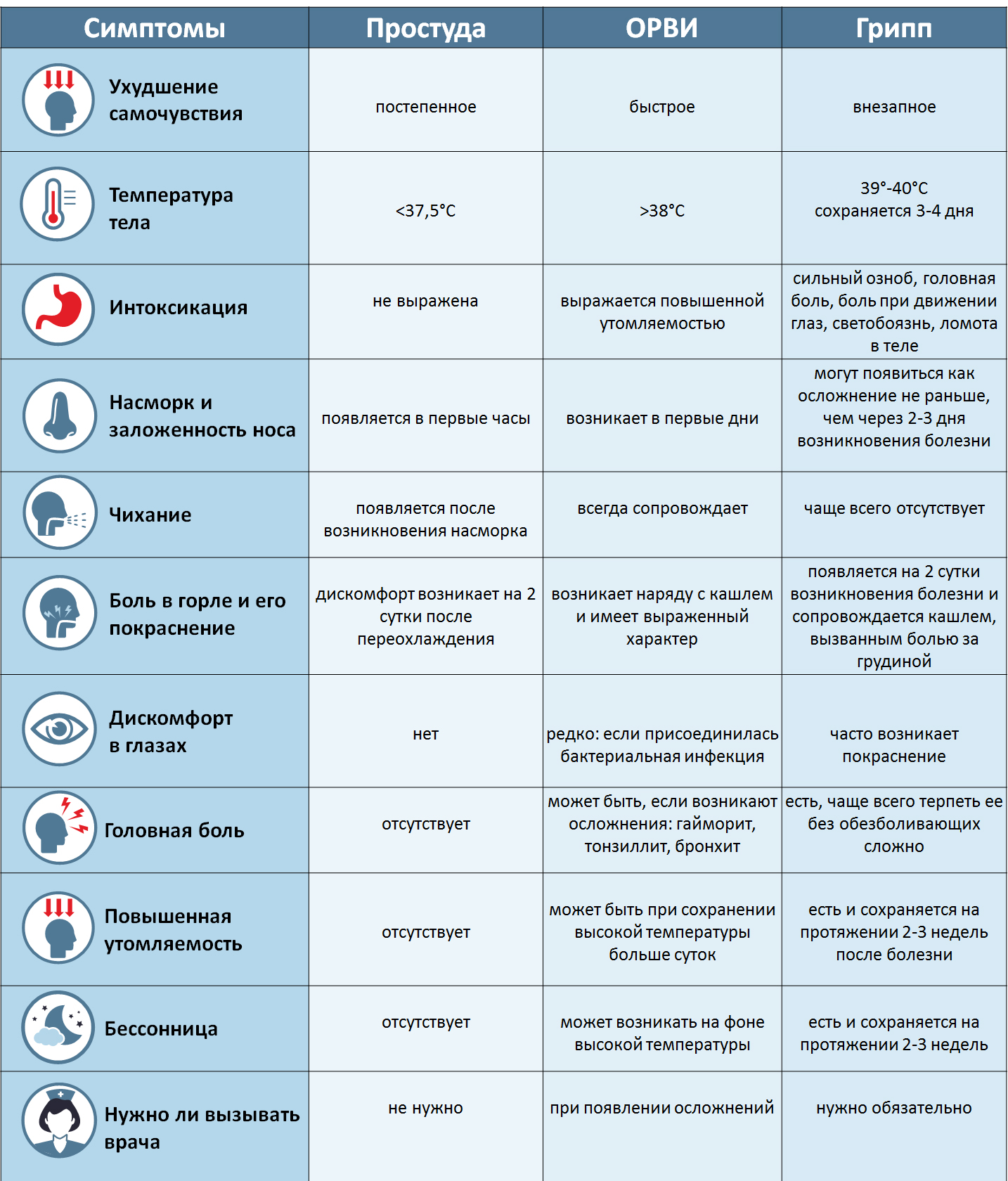
Воспаление поражает слизистую оболочку носовой полости, горла, гортани. Инфекция распространяется капельным путем.
Это — наиболее распространенное инфекционное заболевание, с которыми большинство людей встречается 1-2 раза в год.
Симптомы болезни обычно включают повышенную температуру, чихание, насморк, охриплость, кашель. Признаки проявляются в течение нескольких дней после заражения, стихают до 10 дней.
Существует более 100 различных типов риновирусов, поэтому разработка эффективной вакцины сегодня невозможна.
ОРВИ
Симптомы ОРЗ и ОРВИ очень похожи, часто 2-е заболевание развивается вследствие 1-й болезни.
Вирус присутствует в теле задолго до проявления. Он ждет подходящего момента, т.е. ослабления организма, например, вследствие простуды.
Возбудители ОРВИ
В этиологии ОРВИ участвует целый ряд вирусов. Наиболее часто болезнь вызывается коронавирусами и аденовирусами.
Но патогенов, способных вызвать острое воспаление верхних дыхательных путей и связанные с ними осложнения, очень много.
ОРВИ, аналогично гриппу и ОРЗ, распространяется капельным путем.
Видео: Грипп и ОРЗ. Какая разница и как лечить?
В чем разница между гриппом, ОРЗ, ОРВИ?
Чем грипп отличается от ОРЗ и ОРВИ?
В то время, как ОРЗ и ОРВИ вызывают около 200 различных типов вирусов, из-за чего они являются самыми распространенными заболеваниями, в развитии гриппа участвует только несколько различных вирусов. Они делятся на 3 типа: A, B, C.
Наиболее опасный тип A – самый мутагенный, имеет несколько подтипов. Именно этот тип, обычно, несет ответственность за эпидемию или даже пандемию.
Отличие гриппа от ОРВИ и ОРЗ – тяжесть течения.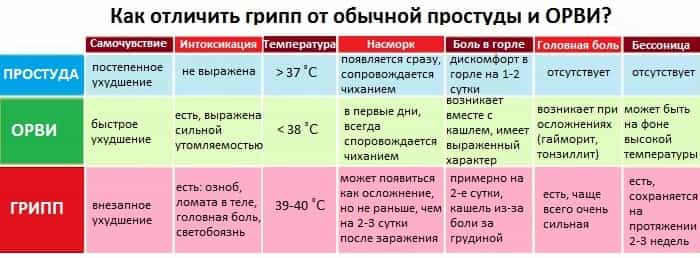 Его нельзя спокойно «переходить».
Его нельзя спокойно «переходить».
Группы риска, склонные к осложнениям, включают детей в возрасте до 2 лет, взрослых старше 65 лет, беременных женщин, людей с диабетом, болезнями сердца, почек или других органов, ослабленной иммунной системой.
ОРЗ характеризует кашель, легкое царапанье в горле, слегка повышенная температура. Это — неприятные признаки, но с ними можно нормально работать, общаться без риска серьезных осложнений.
Но — ничего не следует преувеличивать. Чрезмерное перенапряжение может сильно ослабить тело, ухудшить состояние — или, как минимум, затянуть выздоровление.
Не пренебрегайте лечением, рекомендованным врачом!
В случае ОРВИ ситуация более серьезная. Многие люди склонны переносить болезнь на ногах, ходить на работу, пребывать в обществе.Хотя этот подход иногда действенный, и симптомы исчезают через неделю -существует риск возвращения заболевания в гораздо худшей форме. Кроме того, он приводит к чрезмерному обременению организма, подвергая риску сердце и другие важные органы.
Кроме того, он приводит к чрезмерному обременению организма, подвергая риску сердце и другие важные органы.
Как определить болезнь?
Отличить заболевания можно относительно легко.
Достаточно обратить внимание на некоторые характерные черты:
- Скорость. Основной фактор, чем отличается ОРЗ от ОРВИ и гриппа, – это скорость начала болезни. ОРЗ развивается постепенно, симптомы медленно ухудшаются, грипп обычно атакует быстро, период его инкубации не превышает 24 часов. Развитие ОРВИ преимущественно подобно гриппа, зависит от конкретного возбудителя.
- Лихорадка. Другая отличительная особенность – лихорадка. При ОРЗ и ОРВИ повышенная температура, как правило, является сопутствующим симптомом, она достигает максимум 38ºС. Для гриппа типична лихорадка, превышающая 38ºС (часто до 40ºС).
- Кашель. При ОРВИ и ОРЗ кашель умеренный, к концу заболевания изменяется в продуктивный.
 Грипп характеризуется сухим кашлем с самого начала.
Грипп характеризуется сухим кашлем с самого начала. - Продолжительность. В то время, как ОРЗ длится 7-10 дней, грипп и ОРВИ продолжаются до 2 недель.
ОРЗ, ОРВИ, грипп – таблица различий в клинической картине:
Симптомы | ОРЗ | ОРВИ | Грипп |
| Повышение температуры | У детей часто, у взрослых температура слегка повышена | До 38ºС | Как правило, лихорадка, часто выше 38ºС |
| Насморк, заложенность носа | Почти всегда | Присутствует, примерно, в 70% случаев, в зависимости от типа вируса | Никогда |
| Боль в горле | Почти всегда | Зависит от типа вируса | Никогда |
| Хрипота | Почти всегда | Зависит от типа вируса | Как правило, отсутствует |
| Кашель | Сначала сухой, позже продуктивный | Сначала сухой, позже продуктивный | Преимущественно, сильный |
| Усталость, слабость | Умеренная | Умеренная | Сильная, длительная, продолжительностью до 2 недель; вначале болезни – экстремальное истощение |
Различия в возбудителях, течении, осложнениях, лечении ОРЗ, ОРВИ, гриппа:
Характеристика | ОРЗ | ОРВИ | Грипп |
| Возбудитель болезни | Риновирусы | Коронавирусы, аденовирусы | Вирусы гриппа |
| Инкубационный период | 2-5 дней | 1-4 дня | 1-2 дня |
| Проявление симптомов | Постепенное начало, медленное ухудшение состояния | Не настолько быстрое начало, как при гриппе, зависит от конкретного вируса | Быстрое начало, иногда болезнь развивается в течение ночи |
| Продолжительность болезни (при соблюдении режимных мер) | 7-10 дней | 7-14 дней | 7-14 дней |
| Инфекционность | Первые 3 дня | 10 дней | 10 дней |
| Осложнения | Отит, синусит | Пневмония, воспаление гортани, синуситы | Острое воспаление гортани, пневмония, миозит, миокардит, менингит, энцефалит |
| Перенос инфекции | Капельный путь | Капельный путь | Капельный путь |
| Постельный режим | Первые 2-3 дня | На протяжении всего периода болезни | На протяжении всего периода болезни |
| Вакцинация | Нет | Нет | Есть |
| Профилактика | Усиление иммунитета, частое мытье рук, ЗОЖ, избегание контакта с больными | Усиление иммунитета, частое мытье рук, ЗОЖ, избегание контакта с больными | Усиление иммунитета, частое мытье рук, ЗОЖ, избегание контакта с больными |
| Антибиотики | Неэффективны | Неэффективны | Неэффективны |
Видео: Чем отличаются ОРВИ и ОРЗ?
youtube.com/embed/Sj5qIGvDTXg” frameborder=”0″ allowfullscreen=”allowfullscreen”>
Различия в лечении гриппа, ОРЗ и ОРВИ
Ни при одном заболевании не существует специального лечения. Преимущественно рекомендуется постельный режим в теплой, хорошо проветриваемой комнате до устранения симптомов (как правило, не менее 1 недели).
Грипп
С гриппом организм, обычно, справляется самостоятельно.
Если инфекция возникает с осложнениями, или у пациентов с высоким риском — назначаются противовирусные препараты.
Обычное лечение:
- Снижение температуры (при превышении 38°C).
- Постельный режим.
- Потребление жидкости.
- Прием витаминов.
- Применение назальных капель.
- Прием средств от кашля, в том числе — сиропов.
Для снижения температуры и облегчения боли назначается Аспирин (не предназначен до 12 лет, ввиду риска синдрома Рейе), Парацетамол, Нурофен.
ОРЗ
В дополнение к обезболивающим препаратам, рекомендуются паровые ингаляции, облегчающие заложенность носа.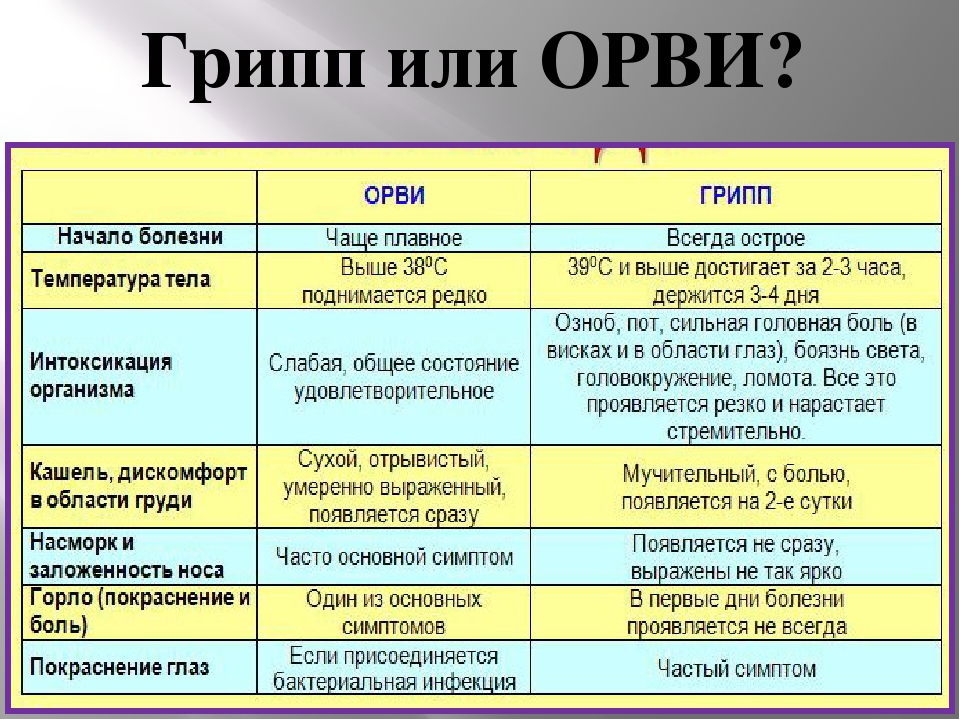
При развитии вторичных инфекций (отит, бронхит, синусит), необходимы антибиотики.
ОРВИ
При нормальном течении заболевания, знать точную причину (возбудителя) нет необходимости. Для пациента эта информация не имеет практического значения.
Распространенные респираторные вирусы лечатся симптоматично.
Терапия включает:
- Покой.
- Постельный режим.
- Прием лекарств, устраняющих симптомы продолжающейся инфекции.
Часть лечения ОРВИ – ограничение контакта с окружающими.
Несмотря на некоторые различия в развитии, течении, лечении и последствиях всех 3-х заболеваний, они имеют много общих черт, среди которых – соблюдение постельного режима, избегание контакта с окружающими в целях предотвращения распространения инфекции и усугубления состояния здоровья.
Чем отличается грипп от орви и орз таблица лечение
Даже человек с крепким здоровьем время от времени сталкивается с симптомами простудных заболеваний. Обратившись к терапевту он слышит диагноз — ОРЗ. Простые обыватели часто путаются в аббревиатурах ОРЗ или ОРВИ, поэтому хотели бы разобраться, чем отличается диагноз грипп от ОРВИ и ОРЗ. Беспокойство пациентов обосновано — от конкретного диагноза напрямую зависит тактика последующей терапии.
Краткое содержание статьи
Основные отличия
Острое респираторное заболевание (ОРЗ) — это общее понятие. Оно применяется медиками для обозначения различных, но схожих между собой заболеваний. Они вызваны разными вредными микроорганизмами:
- бактериями;
- вирусами;
- грибками либо простейшими.
Такой диагноз терапевты ставят в случаях, когда им еще точно не известно о возбудителе, хотя симптоматика болезни внешне уже проявилась. Более конкретные выводы по поводу возбудителя ОРЗ дают специальные лабораторные анализы или характерные симптомы, особенно, в период массовых эпидемий.
Более конкретные выводы по поводу возбудителя ОРЗ дают специальные лабораторные анализы или характерные симптомы, особенно, в период массовых эпидемий.
ВАЖНО! Практика показывает, что более 90% всех случаев ОРЗ имеют вирусное происхождение.
Острая респираторная вирусная инфекция (ОРВИ) имеет более конкретный характер. К категории ОРВИ относят такие инфекции, как:
- грипп;
- парагрипп;
- аденовирусная и риновирусная инфекции;
- а также множество других вирусных инфекций, которых насчитывается более 200.
В какое время можно заразиться ОРЗ
Каждым из видов ОРВИ можно заразиться в любое время года. Но в отличие от холодных сезонов, летом иммунитет человека более устойчив к различным неблагоприятным погодным условиям. В разгар морозной зимы концентрация вирусов гриппа и ОРВИ в воздухе также не является высокой. Пик заболеваемости традиционно приходится на неустойчивый температурный период декабря и февраля, поздней осени и марта.
В чем отличие гриппа от обширной группы ОРВИ (таблица)
Существуют ли отличия между течением гриппа и ОРВИ, которую часто в народе называют простудой? Начало гриппа отличается внезапной симптоматикой. У заразившегося человека быстро поднимается высокая температура тела, которая держится в течение 3-4 дней.
- Сильная головная боль.
- Дискомфорт в области глаз.
- Ломота в суставах, костях и мышцах.
- Слабость и лихорадка отличают грипп от других ОРВИ.
Восстановительный период даже после относительного выздоровления пациента затягивается еще на 7-15 дней. Человек ощущает слабость, отсутствие аппетита, перепады давления, нарушение сна, повышенную утомляемость даже после небольшой физической нагрузки.
ВАЖНО! Это называется «астеническим синдромом»: пациенту следует продлить постельный режим, а то вторая волна вирусной инфекции не заставит себя ждать.
Еще одно характерное отличие поражения организма вирусами гриппа — больного в первые дни болезни практически не беспокоят кашель, заложенность носа и воспаление горла. Эти симптомы присоединяются только через 2-3 дня после начала болезни. Если грипп начинается с кашля, то он существенно отличается от кашля при ОРВИ. Гриппозный кашель сухой и изматывающий, нередко дополняется болями за грудиной, которая возникает из-за того, что вирусы успели размножиться в слизистой трахеи и бронхов.
Эти симптомы присоединяются только через 2-3 дня после начала болезни. Если грипп начинается с кашля, то он существенно отличается от кашля при ОРВИ. Гриппозный кашель сухой и изматывающий, нередко дополняется болями за грудиной, которая возникает из-за того, что вирусы успели размножиться в слизистой трахеи и бронхов.
Также грипп протекает значительно тяжелее, чем другие ОРЗ, а также чаще вызывает различные осложнения, вплоть до летального исхода. Во время гриппозной инфекции сильно выражена интоксикация. Главная причина — распад вирусов, а также клеток иммунной системы человека, которые защищают организм.
Из наблюдений терапевтов
Как отмечают терапевты, одно из основных отличий гриппа от ОРВИ в следующем. При обычной простуде температура тела больного не повышается более 38,5 градуса и на первый план выходят проявления катаральных симптомов простуды:
- сильный насморк;
- дискомфорт в области горла;
- влажный кашель.
Любая другая вирусная инфекция всегда начинается с насморка, болей в горле, воспаления верхних, а затем и нижних дыхательных путей.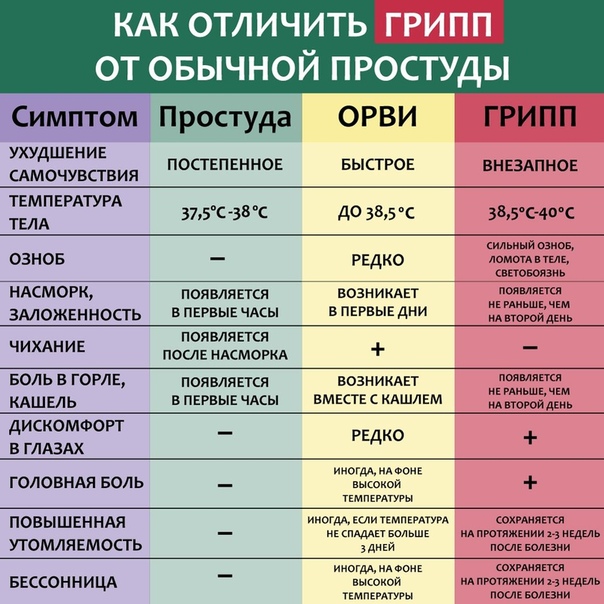
Во время гриппа у пациентов часто наблюдается покраснение глаз. При ОРВИ данный симптом не проявляется, за исключением тех случаев, когда к заболеванию уже присоединилась бактериальная инфекция.
ВАЖНО! Еще одна существенная разница заключается в том, что вирус гриппа имеет очень изменчивый характер. Через небольшой промежуток времени — от 1 года до 3 лет — образуется новый подвид, к которому человек не имеет иммунитета.
Появление осложнений — одно из главных отличий гриппа от ОРВИ
При ослабленном иммунитете человека либо недостаточном лечении гриппа к нему нередко присоединяются бактериальные осложнения. Одним из самых распространенных бактериальных осложнений является бронхит. При ослабленном иммунитете бронхит нередко превращается в пневмонию.
Другое бактериальное осложнение вирусной инфекции — это синусит, острый воспалительный процесс околоносовых пазух. К самым распространенным относятся гайморит и фронтит. Сильная боль в ухе также является осложнением вирусной инфекции в виде отита.
Лечение вирусных инфекций: есть ли разница
При заражении вирусами не стоит пускать все на самотек или разводить панику. Необходимо просто придерживаться грамотной тактики лечения на основе рекомендаций врача. Все вирусы при ОРЗ передаются воздушно-капельным путем и поражают органы дыхательной системы, поэтому подход к ним один и тот же.
ВАЖНО! Схема исцеления практически одинакова: покой и постельный режим в период острого периода болезни, обильное питье, при необходимости — симптоматическая терапия (прием жаропонижающих препаратов, капли в нос или средства для лечения кашля)
Профилактические меры против ОРЗ
Для профилактики вирусных болезней рекомендуется не допускать переохлаждение организма, придерживаться здорового образа жизни. Уделять сну и отдыху достаточное количество времени, а также правильно и сбалансированно питаться. При вынужденном контакте с пациентом с ОРЗ лучше пройти курс лечения иммуностимулирующими средствами.
Отличие короновируса COVID-19 от ОРВИ и ГРИППа, как не перепутать?
В первое время, на самых ранних этапах течения болезни очень сложно отличить коронавирус от обычного ОРВИ или гриппа. Первую неделю коварный Covid-19 может показывать те же симптомы, что и уже более привычные населению простудные заболевания или грипп. Но все же некоторые открытия иностранных специалистов, сводки и опросы от болеющих коронавирусом дали информацию о тех симптомах, которые позволяют отличить Covid-19 от других респираторных заболеваний.
Инкубационный период
Принципиальное отличие коронавируса от ОРВИ или гриппа – это инкубационный период, то есть промежуток времени от заражения до проявления симптомов болезни.
Вирусы ОРВИ, а также грипп размножаются очень быстро. Симптомы могут появиться в 1-4 дни заражения. В среднем инкубационный период по этим заболеваниям составляет 2-3 дня.
Коронавирусу для этого нужно больше времени. Инкубационный период длится до 14 дней. В среднем симптомы проявляются на пятый день, но могут появиться и куда позже.
То есть, если вы можете хотя бы предположить, когда произошло заражение (ехали на общественном транспорте; были в месте скопления народа; общались с человеком, у которого наблюдались признаки ОРВИ) – сможете отсчитать и количество дней, когда начали проявляться первые симптомы, а значит сделать предварительный вывод о том, что за болезнь вы встретили. Раннее проявление недомоганий – скорей всего ОРЗ, грипп; позднее проявление недомоганий может быть признаком коронавируса.
Одинаковые и очевидные симптомы у всех трех болезней
У всех этих заболеваний (ОРВИ, грипп, коронавирус) присутствуют абсолютно одинаковые проявления, а именно: температура, кашель, слабость, усталость, насморк, боль в суставах, боль в горле, головная боль, диарея. Вопрос только в том, на сколько часто встречается тот или иной симптом при каждом заболевании.
Вопрос только в том, на сколько часто встречается тот или иной симптом при каждом заболевании.
Температура: при коронавирусе температура обычно поднимается от 37,3 градусов и выше; при гриппе температура чаще всего достаточно высокая от 38 градусов, появляется резко, больной вплоть до точного времени может сказать, когда наступил жар; при ОРВИ – высокая температура наблюдается редко.
Кашель: при коронавирусе коронный симптом – именно кашель, так как вирус поражает горло и дыхательные пути, часто сухой кашель; при гриппе сухой кашель, также, встречается достаточно часто; а вот при ОРВИ он весьма редко наблюдается, если и встречается – чаще “мокрый”, не сухой.
Слабость и усталость: при короновирусе иногда наблюдается вялость, “поламывания” тела и усталость; при гриппе – “разбитое” состояние не редкость, при ОРВИ – слабость присутствует иногда.
Насморк: при коронавирусе влажный нос и насморк наблюдаются редко; при гриппе встречается в некоторых случаях, при ОРВИ – такое проявление присутствует достаточно часто.
Боль в суставах: при короновирусе иногда встречается боль суставов; при гриппе и ОРВИ – очень часто есть такие боли.
Боль в горле: при коронавирусе и гриппе иногда першение и боли в горле наблюдаются, при ОРВИ – боль в горле – частый и типичный симптом.
Головная боль: при коронавирусе присутствует иногда, при гриппе – очень часто, при ОРВИ – редко.
Диарея: при коронавирусе и гриппе расстройства кишечника в виде “жидкого стула” иногда случаются, при ОРВИ – они достаточно редки или отсутствуют вовсе.
Как видите, даже среди таких типичных и одинаковых для все трех видов болезней есть несущественные отличия, которые способны подсказать , с чем вы имеете дело.
Симптомы, характерные только коронавирусу
Важный симптом, который проявляется при коронавирусе – это сухой кашель.
Кашель может быть сильным и долго не останавливаться. В сутки может быть три или более приступов, которые могут длиться по часу. Причем каждый новый приступ может быть куда сильнее прежнего.
На пятый-седьмой день болезни – может появиться еще один неприятный симптом, свойственный для Covid-19 – одышка и затрудненное дыхание.
У пациентов с более тяжелой формой заболевания может развиваться пневмония, которая представляет опасность для жизни.
На восьмой день и далее у самых критичных форм заболевания может начаться процесс накапливания жидкости в легких. Это чревато нарушением дыхания, при таком исходе используют интенсивную терапию и искусственную вентиляцию легких. К сожалению, в этом случае многие заболевшие погибают или остаются с серьезными повреждениями.
Итак, основные симптомы коронавируса, типичные для всех респираторных заболеваний и характерные только Covid-19 таковы:
- сухой кашель
- температура
- боль в мышцах
- боль в горле
- одышка
- затрудненное дыхание
- диарея, тошнота
Парочка новых интересных симптомов Covid-19
Помимо вышеперечисленных симптомов, некоторые отоларингологи отмечают и еще одно интересное проявление коронавируса – потеря вкуса и обоняния. Однако другие специалисты не спешат делать поспешных выводов о взаимосвязи нового вируса и отсутствия вкуса и обоняния.
16 апреля итальянские и испанские медики сообщили об еще одном симптоме Covid-19. Признаком инфекции может быть сыпь на ногах. У каждого пятого итальянца, госпитализированного с тревожным вирусом, наблюдались проблемы с кожей в виде сыпи, часто сыпь встречалась и у детей.
Иностранные специалисты отмечают, что сыпь похожа на ту, что бывает и при кори или оспе. Обычно она выступает на пальцах ног, после болезни может бесследно проходить!
Итак, все симптомы коронавируса вместе с типичными и схожими с другими заболеваниями и теми, что характерны только этому вирусу:
- сухой кашель
- температура
- боль в мышцах
- одышка
- затрудненное дыхание
- боль в горле
- диарея, тошнота
- потеря вкуса и обоняния
- сыпь на ногах
Бессимптомное течение Covid-19
Удивительно, но переболеть коронавирусом можно даже не заметив этого. То есть вирус может совсем никак себя не проявлять, протекать бессимптомно.
Британские исследования показали, что свыше 70% людей зараженных коронавирусом, не чувствовали никаких признаков болезни, либо инфекция протекала в очень легкой форме.
В эпицентре эпидемии – Италии, исследователи утверждают , что больше половины болеющих Covid-19, также не испытывали никаких симптомов, но при этом являлись носителем вируса и представляли угрозу заражения для окружающих.
В Исландии огромное количество пациентов с положительным результатом коронавируса не замечали, что болеют.
В Ухане многие, зараженные вирусом пациенты, тоже утверждают, что не испытывали никаких тревожных отклонений в здоровье. При этом не было никакого кашля и повышенной температуры.
Как видите, вирус коварен, проявляет себя по-разному, а иногда не проявляет себя вовсе. Точным методом его диагностики является метод ПЦР. Для теста на короновирус берется соскоб из горла и носоглотки. Тест можно сделать по желанию платно во многих лабораториях по регионам России. А делать самостоятельно в лаборатории его нужно только при отсутствии симптомов, но при основании полагать, что у вас потенциально может быть заражение (ездили на общественном транспорте, были в местах скопления народа, прочее). Если же у вас имеются какие-либо симптомы – вызовите врача на дом. Далее тест вам сделают по решению доктора. Самостоятельно выезжать и подвергать других опасности не нужно.
Будьте здоровы! Все будет хорошо!
Чем отличается грипп от ОРВИ
АнвиМаксЭксперт + Эксперт в лечении ОРВИ, гриппа
23 подписчика
Хотя грипп и входит в группу острых респираторных вирусных инфекций (ОРВИ), симптомы его несколько отличаются. Поэтому опытный врач обычно может с уверенностью поставить правильный диагноз. Последний необходим для того, чтобы помочь организму легче и быстрее перенести попавший в него вирус.
Инструкция
ОРВИ на сегодняшний известно несколько групп (вирус гриппа, парагриппа, аденовирус, риновирус и др.), которые подразделяются на более чем 300 подтипов. Вирус гриппа может относиться к роду А, В или С. Последний никогда не изменяется, поэтому человек, переболевший им, приобретает иммунитет к нему на всю жизнь. Вирус В изменяется гораздо реже, им чаще всего болеют дети. А вот вирус А может вызывать целые эпидемии, так как он меняет свою антигенную структуру каждые 3-5 лет.
Помимо разных вирусов, установить которые можно лишь с помощью лабораторных исследований, ОРВИ и грипп отличаются между собой симптомами. Так, простуду человек переносит гораздо легче, она обычно начинается очень медленно, в течение нескольких дней. В некоторых случаях ярко выраженные симптомы могут появиться спустя неделю после попадания вируса в организм. Отличительной особенностью ОРВИ является синдром поражения респираторного тракта – насморк, боль и першение в горле, кашель. Температура тела редко поднимается выше 38,5оС.
В отличие от простуды, грипп развивается очень быстро, буквально спустя несколько часов после попадания вируса гриппа на слизистую верхних дыхательных путей. Температура тела за 2-3 часа может подняться до 39-40оС, будут ощущаться озноб или лихорадка, головная боль, слабость и боль в мышцах, потеря аппетита, возможна рвота. При гриппе редко бывает насморк, чаще всего больные отмечают сухость в носу и горле. Спустя сутки может появиться сухой кашель.
Немного отличается и схема лечения ОРВИ и гриппа. С простудой человеческий организм обычно справляется самостоятельно. Врачи рекомендуют принимать средства, устраняющие такие симптомы, как насморк, боль в горле, кашель. Если при ОРВИ прием противовирусных и иммуно-стимулирующих препаратов, которые помогут организму быстрее справиться с болезнью, желателен, то при гриппе он строго обязателен. Без них перенести его будет гораздо сложнее, да и могут возникнуть осложнения.
Как при гриппе, так и при ОРВИ можно принимать такой комбинированный препарат, как «АнвиМакс». Он оказывает жаропонижающее, обезболивающее, антигистаминное и интерфероногенное действие, устраняет симптомы простуды. А при гриппе – предотвращает распространение вируса типа А в клетки организма. В его состав входит ремантадин, парацетамол, аскорбиновая кислота, глюконат кальция, рутозид и лоратадин, который предотвращает развитие отека тканей.При возникновении гриппа к лечению следует подходить более основательно. Чем раньше оно будет начато, тем меньше вероятность развития серьезных осложнений, таких как пневмония, бронхит и другие. Лучше всего обратиться за консультацией к врачу. Как при ОРВИ, так и при гриппе сбивать температуру ниже 38,5оС не рекомендуется, так как подобным образом организм борется с наличием вируса в организме.
Видео по теме
Совет полезен?
Статьи медицинского характера на Сайте предоставляются исключительно в качестве справочных материалов и не считаются достаточной консультацией, диагностикой или назначенным врачом методом лечения. Контент Сайта не заменяет профессиональную медицинскую консультацию, осмотр врача, диагностику или лечение. Информация на Сайте не предназначена для самостоятельной постановки диагноза, назначения медикаментозного или иного лечения. При любых обстоятельствах Администрация или авторы указанных материалов не несут ответственности за любые убытки, возникшие у Пользователей в результате использования таких материалов.
Похожие советы
Общие сведения о птичьем гриппе
ГЛАВА 2
Текущее состояние знаний о высокопатогенном птичьем гриппе
В этой главе представлена справочная информация о вирусах птичьего гриппа и факторах, которые привели к появлению, распространению и сохранению вирусов HPAI. В качестве руководства он использует опыт до и после появления вирусов H5N1 HPAI азиатского происхождения.
2.1 Вирусы птичьего гриппа
Водные птицы являются естественными хозяевами вирусов гриппа типа А.Вирусы гриппа классифицируются по шипам гликопротеина на их поверхности – «HA» или белок гемагглютинин (на данный момент идентифицировано 16 различных подтипов) и «NA» или белок нейраминидазы (девять подтипов). Все 16 подтипов НА и девять подтипов НА (см. Вставку по терминологии) были обнаружены в различных комбинациях у водных диких птиц, и по большей части эти вирусы живут в гармонии со своими естественными хозяевами, вызывая недолговечную субклиническую кишечную инфекцию (Webster and Hulse). , 2004).Иногда вирусы переходят от водных диких птиц к домашней птице или млекопитающим, и у этих неприродных или вторичных хозяев могут закрепиться новые генотипы вируса. После адаптации к нептичьим хозяевам эти вирусы могут потерять способность размножаться в кишечнике водных птиц (Kobasa et al , 2001).Из вирусов гриппа, передаваемых наземным домашним птицам, наиболее важными являются вирусы H5. и подтипы H7. Они обладают способностью мутировать в вирусы HPAI, которые системно размножаются у кур, часто вызывая очень высокую смертность в инфицированных стадах (Alexander, 2000).
Другие подтипы вируса гриппа также скрестились с наземными домашними птицами и прижились у этих птиц. Среди них наиболее часто обнаруживается подтип H9N2, который распространился по Азии и на Ближний Восток за последние 15 лет (Alexander, 2000). Этот подтип является вирусом с низкой патогенностью, но в сочетании с другими патогенами может вызывать тяжелые респираторные заболевания у домашних птиц (Kishida et al , 2004). Вирусы H9N2 в настоящее время циркулируют в популяциях свиней в Китае (Chen et al , 2006b) и связаны со случаями клинических заболеваний у этого вида (Peiris et al , 2001).Они также вызывают несмертельные инфекции у людей (Butt et al , 2005).
| Терминология В этом документе термин «H5N1 HPAI азиатского происхождения» используется для описания высокопатогенных вирусов птичьего гриппа подтипа H5N1, связанных с линией вирусов, впервые обнаруженных у гусей в провинции Гуандун в Китае в 1996. «H5N1 HPAI» используется для описания болезни, вызываемой этими вирусами. Хотя появилось множество генетических вариантов этих вирусов, они по-прежнему образуют линию, отличную от других вирусов H5N1.Все вирусы HPAI подтипа H5N1, обнаруженные за последние 11 лет, принадлежат к этой линии. Термин HPAI имеет очень специфическое значение и относится к способности вируса вызывать заболевание у экспериментально инокулированных цыплят (т.е. его вирулентность). Это не отражает способности этих вирусов вызывать болезни у других видов. Термин «H5N1 HPAI» используется, а не просто «H5N1», чтобы избежать путаницы с неродственными низкопатогенными вирусами птичьего гриппа (LPAI) подтипа H5N1, обнаруженными у домашних и диких птиц. Вирусы гриппа имеют сегментированный геном и способность подвергаться реассортации генов. Теоретически этот процесс может происходить, когда два разных вируса гриппа одновременно заражают одну и ту же клетку. Кроме того, относительно часто происходят незначительные изменения в отдельных генах, что со временем приводит к изменениям в этих генах. Также имели место некоторые случаи рекомбинации генов, в первую очередь во время вспышек HPAI в Чили (2002 г.) и Канаде (2004 г.). Вирусы птичьего гриппа названы в соответствии с их типом (все вирусы птичьего гриппа относятся к типу A), подтипу (i.е. гликопротеинами HA и NA, которыми они обладают, что обозначается как H5N1, H7N7 и т. д.), видами животных, от которых они изолированы, географическим положением, из которого они были изолированы (часто на уровне страны, провинции или штата) , а также по номеру лаборатории и году изоляции. (например, A / Goose / Guangdong / 1/96 [H5N1]). Дополнительная номенклатура не полностью стандартизирована; не использовалась международно согласованная система для наименования различных генетических вариантов внутри подтипов.Например, в результате пересортировки появилось множество новых генотипов вирусов H5NI HPAI азиатского происхождения. Хотя все эти вирусы сохраняют версию «родительского» гена H5, они изначально были подразделены на основе состава других генов, кодирующих внутренние белки. Он впервые сообщил о вирусе H5N1 HPAI азиатского происхождения – A / Goose / Guangdong // 1/96 – используется в качестве отправной точки для сравнения генотипов (Chen et al , 2004; Guan et al , 2004) . По мере развития этих (или подобных) вирусов они приобретали гены от других вирусов гриппа, и сформированные генотипы были названы с использованием букв.Исследователи из Гонконгского университета были очень активны в этой области, и используемые ими буквы (например, генотип «Z») получили широкое распространение. К сожалению, эта система не применялась последовательно всеми исследователями. Эта вариация генотипа не обязательно отражает информацию об вариациях генов НА. Это охвачено другой системой номенклатуры, в которой были идентифицированы множественные клады (клоны) и субклады (субклады) генов гемагглютинина вируса H5N1.Всемирная организация здравоохранения (ВОЗ) первоначально предложила стандартизировать номенклатуру (с использованием кладов и субкладов для группировки этих вирусов) в 2005 и 2006 годах (ВОЗ, 2005; ВОЗ, 2006). С тех пор это было дополнительно пересмотрено (ВОЗ, 2007), и в настоящее время признано по крайней мере десять клад и множество субкладов среди вирусов H5N1 HPAI азиатского происхождения. Поскольку клады и субклады основаны на генетических отношениях между генами НА, отдельные клады могут содержать разные генотипы (последний определяется совокупностью генов, кодирующих внутренние белки, а не геном НА).Следовательно, использование какой-либо данной системы номенклатуры не включает всю информацию о происходящих изменениях. Это может затруднить сравнение молекулярных данных, особенно если разные метки используются разными исследовательскими группами для описания похожих вирусов или даже одних и тех же штаммов вирусов. |
2.1.1 Справочная информация о HPAI Ранние случаи HPAI
HPAI не новое заболевание (Alexander, 1987).Его появление предшествовало индустриализации птицеводства.
Хотя интерпретация исторических данных о HPAI (до так называемой «вирусологической эры») осложняется возможностью спутать это заболевание с другими болезнями, такими как болезнь Ньюкасла, HPAI впервые был идентифицирован в конце 19 века и, вероятно, имел место. ранее (Александр, 1987). По крайней мере, одна ранняя вспышка в 1901 году распространилась через международные границы в результате перемещения домашней птицы (Wilkinson and Waterson, 1975), предупредив о проблемах, с которыми придется столкнуться, когда торговля домашней птицей и птицепродуктами станет глобализованной позже в 20 веке.В Соединенных Штатах Америки в 1920-х годах вирусы HPAI, по-видимому, распространялись через перевозку домашней птицы по железной дороге и через рынки живой птицы (Alexander, 1987).
Точное происхождение этих ранних вирусов и события, которые способствовали мутации причинных вирусов с низкой патогенности на высокую, неизвестны (см. Раздел 2.1.2). Было высказано предположение, что инфекция HPAI была эндемической в Германии, Италии и Египте в течение ряда лет в конце 19-го и / или в первой половине 20-го века (Alexander, 1987).Это указывает на то, что в прошлом не все вспышки болезни сдерживались быстро, в отличие от вспышек с 1950-х по 1970-е годы, которые, как правило, были изолированными случаями, которые быстро контролировались. Например, вспышка 1959 г. в Соединенном Королевстве произошла на изолированной ферме и привела к гибели практически всей домашней птицы, что снизило вероятность распространения (Alexander, 1987). Недавние исследования в области моделирования подтверждают предположение, что низкая плотность фермерских хозяйств может привести к ограниченному или даже отсутствию дальнейшей передачи инфекции (Truscott et al , 2007).
Рост числа случаев HPAI
За последние восемь лет увеличилось количество зарегистрированных вспышек HPAI (Capua and Alexander, 2004), даже если исключить недавние вспышки H5N1 HPAI в Азии и в других местах. Связанные с вирусами HPAI (кроме подтипа H5N1) были обнаружены в Северной и Южной Америке (Соединенные Штаты Америки, Чили и Канада), Европе (Италия и Нидерланды) и Пакистане.
До сих пор не совсем понятно, почему произошло это увеличение.Был предложен ряд факторов, включая увеличение популяции домашней птицы в мире, усиление интенсификации птицеводства с одновременным увеличением производства на свободном выгуле и даже изменение климата, ведущее к изменению путей миграции диких птиц (Капуя и Александр, 2004). Ни один из этих факторов не является причиной такого увеличения, которое, вероятно, будет многофакторным.
Отчасти этому увеличению могли способствовать улучшенные диагностические возможности и наблюдение.Усиленный эпиднадзор позволил выявить случаи, которые в противном случае могли бы остаться недиагностированными, например, клинически легкая «вспышка» в Техасе в 2004 г. (Lee et al , 2005).
Во многом повышение важности HPAI связано с тяжелыми последствиями тех случаев, которые действительно имели место. Три крупных вспышки в Италии (1999 г.), Нидерландах (2003 г.) и Канаде (2004 г.), охватившие районы с высокой плотностью домашней птицы, привели к уничтожению десятков миллионов домашних птиц, в том числе многих здоровых птиц (Capua et al , 2003; Power , 2005; Стегемен и др. , 2004).
Источник вирусов для вспышек HPAI
Учитывая уровень внимания, уделяемого HPAI в последнее время, отрезвляюще думать о том, как мало было продемонстрировано способов заноса и распространения болезни. Дикие водные птицы были предложены в качестве наиболее вероятного источника вирусов LPAI, которые преобразовались в вирусы HPAI во многих вспышках HPAI (за исключением, на данный момент, тех, которые вызваны вирусами HPAI азиатского происхождения) (см., Например, Alexander, 2007), но доказательства, в большинстве случаев, косвенные.В таблице 1 представлена сводная информация о некоторых из этих вспышек HPAI и содержится информация как о возможном источнике вируса, так и о факторах, способствующих появлению высокопатогенного штамма. Эти случаи демонстрируют, что точный источник инфекции во время большинства вспышек не был установлен.
Отсутствие информации об источнике (источниках) также относится к вспышкам, связанным с вирусами H5N1 HPAI азиатского происхождения. Было проведено мало углубленных исследований вспышек заболеваний, вызываемых этими вирусами, особенно в развивающихся странах, и даже когда они были выполнены, путь проникновения или источник вируса не были доказаны.Например, отслеживание контактов и перемещений проводилось в Японии (Nishiguchi et al , 2005) и Республике Корея (Wee et al , 2006) после вспышек в 2003-04 гг., Но даже после этих подробных исследований Авторы могли только предполагать, как вирус попал в эти страны. Аналогичным образом недавние эпидемиологические исследования вспышек в Израиле (2006 г.) и Соединенном Королевстве (2007 г.) не смогли доказать, как был занесен вирус (Balicer et al , 2007; Defra, 2007).
Таблица 1. Отдельные вспышки HPAI – возможные источники и факторы окружающей среды
Вспышка | Подтип вируса | Источник | Возможные факторы |
Австралия 1975-76 | H7N7 | Неизвестно | Плотина на ферме привлекла диких птиц |
Австралия 1985 | H7N7 | Неизвестно | Плотина на ферме привлекла диких птиц |
Австралия 1992 | H7N3 | Неизвестно | Рядом с утиной фермой на свободном выгуле |
Австралия 1994 | H7N3 | Неизвестно | Много диких птиц на водотоке из-за засухи |
Австралия 1997 | H7N4 | Неизвестно | Дикие птицы в окрестностях |
Канада 2004 | H7N3 | Неизвестно | Перелетные птицы в районе до вспышки (Power, 2005) |
Италия 1997-98 | H5N2 | Неизвестно | Сбыт зараженной птицы |
Италия 1999-2000 | H7N1 | Первоисточник неизвестен – предположительно дикая птица | Широко распространенная инфекция вирусом низкой патогенности до появления высокопатогенного штамма (Capua et al , 2003) |
Мексика 1994 | H5N2 | Неизвестно | Широкое распространение вирусов низкой патогенности до появления высокопатогенного штамма (Вильярреал, 2006) |
Нидерланды 2003 | H7N7 | Неизвестно, но, вероятно, интродукция диких птиц | Вирус LPAI, похожий на вирус HPAI, обнаруженный у диких крякв (Munster et al , 2005) |
США 1983-84 | H5N2 | Неизвестно, но, вероятно, интродукция диких птиц | Заражение птицы вирусами низкой патогенности |
США 2004 | H5N2 | Ссылка на рынок живой птицы | Подобные вирусы LPAI, циркулирующие в течение некоторого времени до появления штамма HPAI (Lee et al , 2005) |
В Италии вирусы H7N3 LPAI, практически идентичные вирусам, обнаруженным у диких птиц в 2001 году, впоследствии были обнаружены у выращиваемых на фермах индеек в 2002–2003 годах (Campitelli et al , 2004). Была продемонстрирована тесная взаимосвязь между вирусами LPAI H5 и H7, выделенными из диких крякв, и вирусами из вспышек HPAI в Европе, включая вспышку H7N7 в Нидерландах в 2003 г. (Munster et al , 2005).Причина вспышки ВППГ в Канаде в 2004 г. неизвестна, но этот и другие случаи возникли на птицефабриках, расположенных в районах с сезонно высокой популяцией мигрирующих диких птиц.
Вспышки HPAI в Австралии с 1970-х по 1990-е годы происходили на фермах, которые не принимали адекватных мер биобезопасности. Это включало несколько случаев, когда необработанная питьевая вода из прудов или рек, часто посещаемых дикими водоплавающими птицами, подавалась домашним птицам (Westbury, 1997). Уместно отметить, что за последние десять лет в Австралии не было диагностировано ни одного нового случая HPAI, что, вероятно, связано (по крайней мере частично) с внедрением усиленных мер биобезопасности на коммерческих фермах.Они были введены в ответ на более ранние случаи HPAI и крупную вспышку болезни Ньюкасла на крупных интенсивных фермах. Это также может отражать сокращение количества диких птиц из-за продолжительной засухи (Turner, 2004).
2.1. Мутация вируса LPAI в вирус HPAI
Ключевым событием в генезе всех вирусов HPAI является преобразование (мутация) вируса LPAI H5 или H7 в вирус HPAI. Это происходило в прошлом после размножения вирусов LPAI этих подтипов у кур, но неизвестно, является ли это необходимым предварительным условием.Вирулентность вирусов птичьего гриппа – это полигенный признак (Suarez et al , 2004), который обычно возникает в результате вставки или замены нескольких основных аминокислот в сайте расщепления белка НА. Обычно они не присутствуют в вирусах LPAI. Эта мутация позволяет белку НА расщепляться широким спектром протеаз, позволяя вирусам системно размножаться (Alexander, 2000). Другие новые механизмы превращения вирусов LPAI в вирусы HPAI были описаны во время вспышек HPAI в Чили (2002 г.) и Канаде (2004 г.).Они возникли в результате рекомбинации между геном HA и другим геном, кодирующим внутренний белок, что привело к встраиванию дополнительных аминокислот в сайт расщепления HA (Suarez et al , 2004; Pasick et al , 2005). Модификация сайта расщепления, по-видимому, является важным условием, но не единственным фактором, определяющим вирулентность (Londt et al , 2007).
Несмотря на то, что молекулярные события, связанные с мутацией вируса LPAI в вирус HPAI, известны, факторы, которые приводят к этой мутации, не ясны для многих вспышек вирусов птичьего гриппа H5 и H7, включая первый вирус H5N1 азиатского происхождения. Вирусы HPAI.
Вирус HPAI был создан экспериментально путем повторного прохождения вируса LPAI через цыплят воздушным мешком и внутримозговым заражением (Ito et al , 2001), но точные триггеры этого изменения в естественных условиях неизвестны. В некоторых более ранних вспышках HPAI было очевидно, что переход от LPAI-вируса к HPAI-вирусу произошел после введения вируса LPAI в большие стада коммерческих домашних птиц. Это изменение, по-видимому, произошло в течение нескольких дней в некоторых вспышках (как в случае вспышки в Канаде в 2004 г. [Bowes et al , 2004]).С другой стороны, в некоторых странах Центральной Америки низкопатогенные штаммы H5N2 циркулировали среди домашних птиц в течение ряда лет, не превращаясь в высокопатогенные штаммы. Даже в Мексике, где в 1994 г. произошла мутация вируса LPAI H5N2 в вирус HPAI и этот штамм вируса HPAI был впоследствии ликвидирован, вирусы LPAI H5N2 продолжают циркулировать (Villarreal, 2006), но не вернулись к высокой патогенности.
Вирусы H5N1 HPAI азиатского происхождения несколько отличаются от вирусов HPAI более ранних вспышек тем, что вирусы HPAI, впервые обнаруженные в 1996 г., не были уничтожены и циркулировали в высокопатогенной форме более 11 лет (Sims et al , 2005). .Эти вирусы значительно эволюционировали за это время, но не было выделено близкородственных низкопатогенных штаммов-предшественников подтипа H5 (Duan et al , 2007; Mukhtar et al , 2007). Предположительно, такой вирус существовал до 1996 года, но никогда не обнаруживался и не регистрировался (Sims et al , 2005). Гены HA и NA в вирусах LPAI, наиболее близких к генам вирусов Goose / Guangdong / 1/96, были экспериментально выделены у водных птиц в Японии (Mukhtar et al , 2007).
Все последующие вирусы птичьего гриппа H5N1 азиатского происхождения остались высокопатогенными, и их происхождение можно проследить до вирусов, подобных тем, которые были обнаружены у гусей в провинции Гуандун в 1996 году (Sims et al , 2005). Даже те вирусы, которые инфицировали домашних уток субклинически во многих частях Азии, сохраняют множество основных аминокислот в сайте расщепления и являются высокопатогенными для наземных птиц (Chen et al , 2004).
Не было предоставлено никаких доказательств того, что первый вирус H5N1 HPAI азиатского происхождения появился на птицефабрике с интенсивным выращиванием.Если бы это преобразование из LPAI в HPAI произошло у гусей (тот вид домашней птицы, от которых он был впервые выделен), это не повлекло бы за собой промышленно развитые производственные мощности, потому что гуси на юге Китая в то время выращивались в основном небольшими стаями с лишь несколькими крупными полу- единицы интенсивного производства.
Отсутствие маркеров адаптации к цыплятам (например, делеция в стебле гликопротеина NA (Matrosovich et al , 1999) в исходных штаммах 1996 г. вируса H5N1 HPAI также предполагает, но не доказывает, что ограниченная циркуляция этого вируса встречались у кур до 1997 г.Делеция стебля в NA не обнаруживалась у вирусов этой линии до марта 1997 г., когда она была обнаружена в вирусе, изолированном от мертвой курицы на ферме в Специальном административном районе Гонконга (SAR) (Bender et al , 1999).
Эти наблюдения в сочетании с доказательствами того, что другие вирусы HPAI возникли в начале 20 века до интенсификации птицеводства, указывают на то, что циркуляция вируса LPAI в промышленно развитых системах птицеводства, хотя и считается важным фактором появления некоторых Штаммы HPAI не являются обязательной предпосылкой для возникновения вируса HPAI.
| Скачать (бесплатно) PDF, 225 страниц, 2,8 МБ ISBN 3-924774-51-X 25 € Опубликуйте эту книгу под своим именем | Птичий грипп Тимм К. Хардер и Ортруд Вернер Введение (Зеленые ссылки: бесплатные полнотекстовые статьи) Высокопатогенный грипп птиц, или, как первоначально это называлось, ‘птица чума », первоначально была признана инфекционное заболевание птиц в Италии, 1878 г. (Perroncito 1878).Из-за бывшей горячей точки в итальянской долине Верхнего По ее также называли «ломбардской болезнью». Хотя Чентанни и Савонуцци в 1901 году определили фильтрующий агент, вызывающий заболевание, Шефер только в 1955 г. охарактеризовал эти агенты как вирусы гриппа А (Schäfer 1955). В естественном водоеме хозяева вирусов птичьего гриппа, дикие водоплавающие птицы, инфекция обычно протекает полностью бессимптомное течение, поскольку биотипы вируса гриппа А низкой патогенности сосуществуют практически в идеальных условиях. баланс с этими хозяевами (Webster 1992, Alexander 2000).Когда штаммы низкопатогенного вируса птичьего гриппа (LPAIV) передаются от птичий резервуар является хозяином высокочувствительных видов домашней птицы, таких как куры и индейки (т. е. стадия трансвидовой передачи!), как правило, индуцируются только легкие симптомы. Однако в случаях, когда вид домашней птицы поддерживает несколько циклов заражения, эти штаммы могут пройти ряд события мутации, приводящие к адаптации к их новым хозяевам. Вирусы гриппа А подтипа H5 и H7 не только проходят фазу адаптации хозяина, но могут иметь способность скачкообразно переход путем инсерционных мутаций в высокопатогенную форму (высокопатогенный птичий грипп вирусы HPAIV), вызывающие тяжелое системное заболевание с быстрым смертельным исходом.Такие вирусы HPAI могут возникают непредсказуемо de novo у домашней птицы, инфицированной предшественниками LPAI H5 и H7 подтипы. HPAI у домашних птиц характеризуется внезапным началом, тяжелым заболеванием короткого продолжительность и смертность уязвимых видов приближается практически к 100%. Из-за чрезмерного экономические потери для птицеводства, HPAI получает огромное внимание в ветеринарном мире и во всем мире рассматривается как болезнь, о которой при подозрении немедленно уведомить власти.Так как их способности вызывать HPAIV, LPAI, вызываемые подтипами H5 и H7, также рассматривается подлежащий уведомлению (МЭБ 2005). К счастью, до 1997 года ВПГП был редким заболеванием. только 24 зарегистрированные первичные вспышки в мире с 1950-х годов (Таблица 1). Однако недавно птичий грипп привлек внимание всего мира, когда патогенный штамм подтипа H5N1, который, вероятно, возник до 1997 г. в Южном Китае, приобрел энзоотический статус домашней птицы по всей Юго-Восточной Азии и неожиданный переход между классами барьеры »(Perkins and Swayne, 2003), когда передается от птиц млекопитающим (кошкам, свиньям, людям).Хотя не совсем беспрецедентный (Koopmans 2004, Hayden and Croisier 2005), значительное количество задокументированных случаев в люди, связанные с тяжелым заболеванием и несколькими смертельными случаями, вызвали серьезную обеспокоенность по поводу пандемический потенциал штамма H5N1 (Klempner and Shapiro 2004; Webster 2006). Есть еще несколько доказательств, которые будет обсуждаться ниже – это предполагает, что вирус H5N1 приобрел повышенную патогенную активность для нескольких видов млекопитающих. По праву, это вызвало обеспокоенность мировой общественности (Кэй и Прингл 2005).
1 Изменено из Capua and Mutinelli, 2001* Вспышки со значительным распространением на многочисленные фермы, приводящие к большим экономическим потерям.Наиболее другие вспышки были связаны только с ограниченным распространением или отсутствием распространения на фермах-индексах. Вирусы Вирусы гриппа имеют сферическую или продольные частицы с оболочкой, содержащие до восьми сегментов одноцепочечной РНК геном отрицательной полярности. Вирусы гриппа имеют общий статус в списке Orthomyxoviridae семейства и классифицируются на типы A, B или C на основании антигенных различий их нуклео- и матричные белки.Вирусы птичьего гриппа (AIV) относятся к типу А. Отличные отзывы о структура и стратегия репликации вирусов гриппа были недавно опубликованы (например, Сидоронко и Reichl 2005). Основными антигенными детерминантами вирусов гриппа A и B являются гемагглютинин (H или HA) и нейраминидаза (N или NA) трансмембранные гликопротеины, способные к вызывание специфических подтипов и иммунных ответов, которые являются полностью защитными внутри, но только частично защитные поперек, разные подтипы.На основании антигенности этих гликопротеины, вирусы гриппа A в настоящее время группируются в шестнадцать H (h2 – h26) и девять N (N1 – N9) подтипы. Эти кластеры подтверждаются при филогенетическом анализе нуклеотидных и выведены аминокислотные последовательности генов HA и NA соответственно (Fouchier 2005). Стандартная номенклатура изолятов вируса гриппа требует коннотации типа вируса гриппа, вид хозяина (опущено в случае человеческого происхождения), географическое положение, серийный номер и год изоляции.Для вируса гриппа типа А Подтипы гемагглютинина и нейраминидазы добавлены в скобки. Один из родительских штаммов птиц из текущих вспышек H5N1 азиатского происхождения был изолирован от гуся в китайской провинции, Гуандун: соответственно, он обозначен как A / goose / Guangdong / 1/96 (H5N1) (Xu 1999), а изолят происходит от первого задокументированного случая инфекции H5N1 азиатского происхождения у человека из Гонконга. Kong (Claas 1998) обозначается как A / HK / 156/97 (H5N1). Гемагглютинин, гликозилированный и ацилированный белок, состоящий из 562 – 566 аминокислоты, включены в вирусную оболочку.Шаровидная головка ее перепончато-дистальной, узелковидный внешний домен связан со связыванием с клеточными рецепторами, состоящими из олигосахариды, которые на концах несут производные нейраминовой кислоты (Watowich 1994). Экзодомен второго трансмембранного гликопротеина, нейраминидазы (NA), оказывает сиалолитический ферментативный активности и высвобождает потомство вируса, захваченное на поверхности инфицированных клеток во время выхода. Этот функция предотвращает агрегацию вирусов во время выхода и, возможно, также способствует перемещению вирус через слои слизи целевых эпителиальных тканей, что приводит к прикреплению вируса ( Матросович 2004а).Это делает нейраминидазу интересной мишенью. противовирусных агентов (Гарман и Лейвер 2004). Взаимно согласованные и согласованные действия антагонистические виды гликопротеинов HA и NA вирусного штамма имеют решающее значение для эффективного прикрепления и процессы высвобождения вирионов (Wagner 2002).Достигнуто прикрепление к белкам клеточной поверхности вирионов гриппа А. через зрелые тримеризованные вирусные гликопротеины НА. Привязанность стратифицируется признанием отдельные концевые разновидности сиаловой кислоты (N-ацетил- или N-гликолилнейраминовая кислота), тип гликозидная связь с предпоследней галактозой ( α2-3 или α2-6) и состав дальнейших внутренних фрагменты сиалилолигосахаридов, присутствующие на поверхности клетки (Herrler 1995, Gambaryan 2005).А множество различных сиалилолигосахаридов экспрессируется с ограничением тканями и видами происхождение вирусов гриппа от разных хозяев. Адаптация как вирусной НА, так и НА. гликопротеина к конкретному типу (-ам) рецептора определенного вида-хозяина является предпосылкой для эффективное воспроизведение (Ито 1999, Банки 2001, Матросович 1999 + 2001, Сузуки 2000, Гамбарян 2004). Это подразумевает изменение формы рецепторные связывающие единицы белка НА после межвидовой передачи (Гамбарян, 2006).А Механистический обзор различных типов рецепторов представлен на рисунке 1. Птичий грипп вирусы обычно показывают самое высокое сродство к α2-3 связанной сиаловой кислоте, так как это доминирующий тип рецептора в эпителиальных тканях энтодермического происхождения (кишечник, легкие) у тех птиц, которые являются мишенью этих вирусов (Гамбарян 2005a, Kim 2005). Вирусы гриппа, адаптированные к человеку, в Напротив, в первую очередь обращаются к 2-6 связанным остаткам, которые преобладают на не реснитчатых эпителиальных клетках дыхательные пути человека. Эти рецепторные пристрастия определяют часть видового барьера, предотвращающего беспроблемная передача птичьих вирусов человеку (Suzuki 2000, Сузуки 2005).Еще недавно было показано, что в трахее человека имеется популяция мерцательных эпителиальных клеток, которые также несут птичий рецептороподобные гликоконъюгаты с более низкой плотностью (Matrosovitch 2004b), а также куриные клетки несут сиалильные рецепторы человеческого типа в низких концентрациях (Kim 2005). Это может объяснить, почему люди не полностью невосприимчив к заражению некоторыми видами птиц (Beare and Webster 1991). У свиней а также у перепелов оба типа рецепторовприсутствуют с более высокой плотностью, что делает эти виды предполагаемыми сосудами для смешивания для линий птиц и человека (Kida 1994, Ito 1998, Scholtissek 1998, Peiris 2001, Перес 2003, Ван и Перес 2005). Рисунок 1. Обзор рецепторных предрасположенностей вируса гриппа A вирусов (по данным Гамбаряна 2005) После успешного присоединения к подходящему рецептору вирион интернализуется в эндосомный компартмент с помощью клатрин-зависимых и -независимых механизмов (Rust 2004). В вирус ускользает от деградации в этом компартменте за счет слияния вирусных и эндолисомальных мембран: опосредовано транспорт протонов через туннельный белок вирусной матрицы-2 (M2) при значениях pH в эндосоме около 5.0, каскад стерических перестроек в белках матрицы-1 (M1) и начинается гомотримерный гликопротеиновый комплекс НА. В результате Высоко липофильный, слитый домен каждого мономера HA экспонируется, который внедряется в эндолизосомальная мембрана, тем самым инициируя слияние вирусной и лизосомальной мембран (Haque 2005, Вагнер 2005). В свою очередь, восемь сегментов вирусной геномной РНК, заключенные в защитный слой нуклеокапсидных (N) белков (рибонуклеопротеидный комплекс, РНП) попадает в цитоплазму.Здесь они транспортируются в ядро для транскрипции вирусных мРНК и репликация геномной РНК в сложном процессе, который тонко регулируется вирусными и клеточные факторы (Whittaker 1996). РНК-зависимая РНК-полимераза (RdRp) образована комплексом белки PB1, PB2 и PA, и для этой задачи требуется инкапсидированная РНК (РНП). На трансляция вирусных белков и сборка нуклеокапсидов, несущих реплицированную геномную РНК, дочерние вирионы отпочковываются от клеточной мембраны, в которую вирусные гликопротеины ранее проникли был вставлен.Связи между спиральными нуклеокапсидами и белками вирусной оболочки опосредованы белком вирусного матрикса-1 (M1), который образует структуру, подобную оболочке, прямо под вирусным конверт. Вирусное размножение в полностью пермиссивных клетках происходит быстро (менее десяти часов) и эффективный процесс при наличии «оптимальной» генной группы (Ротт 1979, Нойман 2004).Из-за подверженной ошибкам активности вирусного RdRp, высокая частота мутаций ≥ 5 x 10 -5 нуклеотидных изменений на нуклеотид и репликацию цикл, приближающийся почти к одному обмену нуклеотида на геном за репликацию, наблюдается среди вирусы гриппа (Drake 1993).В случае селективного давления (например, нейтрализующие антитела, неоптимальное связывание рецепторов или химические противовирусные препараты) действуют во время репликации вируса в масштабе хозяина или популяции мутанты с соответствующими селективными преимущества (например, уход от нейтрализации, видоизмененные рецептор-связывающие единицы) могут быть выделены и становятся доминирующим вариантом среди квазивидов вируса в этом хозяине или популяции. Если антигенный на детерминанты мембранных гликопротеинов НА и НА влияют механизмы, управляемые иммунитетом, такой (постепенный) процесс обозначается как антигенный дрейф (Fergusson 2003).Антигенный сдвиг, напротив, означает внезапное и глубокое изменение антигенные детерминанты, т.е. переключение подтипов H и / или N в пределах одного цикла репликации. Это происходит в клетке, которая одновременно инфицирована двумя или более вирусами гриппа А разные подтипы. Поскольку распределение реплицированных вирусных геномных сегментов в почкующемся вирусе потомство происходит независимо от подтипа ориджина каждого сегмента, репликационно-компетентное потомство несущие генетическую информацию различных родительских вирусов (так называемые реассортанты ) могут возникают (Webster and Hulse 2004, WHO 2005).В то время как пандемия вирусов гриппа человека 1957 г. (h3N2) и 1968 (h4N2) явно возникли в результате перегруппировки вирусов человека и птиц, вирус гриппа, вызывающий ‘испанский грипп ‘в 1918 г. из птичьего источника (Belshe 2005).Естественные хозяева Дикие водные птицы, особенно представители отряды Anseriformes (утки и гуси) и Charadriiformes (чайки и кулики) являются носители всего разнообразия подтипов вируса гриппа А и, таким образом, наиболее вероятно, составляют естественный резервуар всех вирусов гриппа А (Webster 1992, Fouchier 2003, Krauss 2004, Widjaja 2004 г.).Хотя все виды птиц считаются восприимчивыми, некоторые виды домашних птиц – куры, индейки, цесарки, перепела и фазаны – известны своей быть особенно уязвимым для последствий инфекции.Вирусы птичьего гриппа А обычно не вызывают болезни у их естественных хозяев. Вместо этого вирусы остаются в эволюционном застое, о чем на молекулярном уровне сигнализирует низкий N / S (несинонимичные и синонимичные) соотношения мутаций, указывающие на очищающую эволюцию (Gorman 1992, Таубенбергер 2005).Хозяин и вирус, кажется, существуют в состоянии тщательно сбалансированного взаимного толерантность, клинически продемонстрированная отсутствием заболевания и эффективной репликацией вируса. Большое количество вируса до 10 8,7 x 50% инфекционная доза яйца (EID 50 ) на грамм фекалий может выделяться (Webster 1978). При передаче в очень уязвимые виды домашних птиц, обычно легкие, если таковые имеются, следуют симптомы. Вирусы этого фенотипа называются низкопатогенными (LPAIV) и, как правило, вызывают лишь небольшое и временное снижение яйценоскость несушками или некоторое снижение привеса домашней птицы на откорме (Капуа и Мутинелли 2001).Однако штаммы подтипов H5 и H7 обладают потенциалом мутации до очень высокой степени. патогенная форма после передачи и адаптации к новым домашним птицам-хозяевам. Возникновение высокопатогенные формы H5 и H7 или других подтипов никогда не наблюдались у диких птиц ( Вебстер 1998). Поэтому можно даже взглянуть на очень патогенные формы как нечто искусственное, ставшее возможным только в результате антропогенных вмешательство в естественно сбалансированную систему.После того, как фенотипы HPAIV возникли у домашних птиц, они могут передаваться горизонтально от домашней птицы обратно в популяцию диких птиц.Уязвимость диких птиц в отношении заболевания, вызванного HPAIV, по-видимому, сильно различается в зависимости от вида, возраста и штамма вируса. До появления вирусов HPAI азиатской линии H5N1, распространение HPAIV на диких птиц популяции происходили спорадически и были ограничены на местном уровне (за единственным исключением среди крачек в Южной Африке в 1961 г. [Becker 1966]), так что дикие птицы не получили эпидемиологически важная функция в распространении HPAIV (Swayne and Suarez 2000).Это может коренным образом изменились с начала 2005 г., когда произошла крупная вспышка азиатской линии H5N1, связанной с HPAI был обнаружен среди тысяч диких водных птиц в заповеднике на озере Цинхай в г. Северо-запад Китая (Chen 2005, Liu 2005). В результате этого дальнейшее распространение этого вируса в направлении Европы в 2005 г., возможно, была создана ( МЭБ 2005 г.). В детали и последствия этого процесса описаны ниже.Рисунок 2. Схема патогенеза птичьего гриппа и эпидемиология LPAIV – вирус низкопатогенного гриппа птиц; HPAIV – высокопатогенный птичий вирус гриппа; НА – белок гемагглютинин; пунктирные линии со стрелками представляют виды шлагбаумы Патогенез HPAI Патогенность как общее вирусное свойство у вирусов гриппа A является полигенным признаком и во многом зависит от «оптимальной» комбинации генов , влияющей на тропизм хозяина и ткани, эффективность репликации и иммунную систему. механизмы уклонения, среди прочего.Кроме того, факторы, специфичные для хозяина и вида, вносят свой вклад на исход инфекции, который после межвидовой передачи непредсказуем a Априори . На сегодняшний день высокопатогенная форма птичьего гриппа вызывается гриппом А. вирусы исключительно подтипов H5 и H7. Однако лишь несколько представителей H5 и H7 на самом деле подтипы демонстрируют высокопатогенный биотип (Swayne and Suarez 2000). Обычно H5 и H7 вирусы стабильно сохраняются у своих естественных хозяев в низкопатогенной форме.Из этого водоема, вирусы могут быть занесены в птичники различными путями (см. ниже). После изменчивый и нерешительный период обращения (и, предположительно, адаптации) у восприимчивых домашних птиц В популяциях эти вирусы могут скачкообразно мутировать в высокопатогенную форму (Rohm 1995).Исследования нуклеотидного секвенирования показали, что большинство HPAIV имеют общую черту в их генах HA, которые могут служить для домашней птицы маркером вирулентности (Webster 1992, Senne 1996, Perdue 1997, Steinhauer 1999, Perdue and Suarez 2000): Чтобы получить инфекционность, вирионы гриппа A должны включать белки HA которые были эндопротеолитически обработаны из предшественника НА 0 в дисульфидно-связанный HA 1,2 димер (Chen 1998).Вновь созданный N-конец субъединицы HA 2 содержит фузогенный пептид, состоящий из высоколипофильного домена (Skehel 2001). Этот домен жизненно необходим в процессе слияния вирусной и лизосомальной мембран, потому что он инициирует процесс проникновения вирусных геномных сегментов в цитоплазму клетки-хозяина. Сайт расщепления HA низкопатогенных вирусов состоит из двух основных аминокислот в положениях -1 / -4 (H5) и -1 / -3. (H7) (Дерево, 1993). Эти сайты доступны для тканеспецифичных трипсиноподобных протеаз, которые преимущественно экспрессируются на поверхности респираторного и желудочно-кишечного эпителия.Таким образом, считается, что эффективная репликация LPAIV в основном ограничивается этими сайтами, по крайней мере, в их естественных хозяевах. Напротив, сайт расщепления вирусов HPAI обычно содержит дополнительные основные аминокислоты (аргинин и / или лизин), которые делают его пригодным для переработки субтилизин-подобные эндопротеазы, специфичные для минимальной консенсусной последовательности -R-X-K / R-R- ( Horimoto 1994, Rott 1995). Протеазы этого типа (например, фурин, пропротеин-конвертазы) активны практически во всех тканях организма.Следовательно, вирусы, несущие эти мутации, имеют преимущество в том, что они могут неограниченно реплицироваться в системным образом. Этот процесс неоднократно регистрировался в полевых условиях. В Италии для Например, вирус LPAI H7N1 циркулировал в течение нескольких месяцев в популяциях индейки и кур. раньше, в декабре 1999 г., вирус HPAI H7N1, отличавшийся от своего предшественника только по многоосновной сайт расщепления, возникший и вызвавший разрушительную болезнь (Capua 2000).Было высказано предположение, что ген HA подтипов H5 и H7 несет различные вторичные структуры РНК, которые способствуют инсерционным мутациям (дупликации кодонов) за счет механизм повторного копирования вирусной полимеразной единицы на участке богатой пуринами последовательности, кодирующей сайт эндопротеолитического расщепления этих белков НА (Garcia 1996, Perdue 1997).Это и, вероятно, и другие механизмы, такие как нуклеотидные замены или межсегментарная рекомбинация ( Suarez 2004, Pasick 2005), может привести к включению дополнительные основные аминокислотные остатки. Последнее было экспериментально доказано генерацией HPAIV из предшественников LPAIV после повторного пассирования in vitro и in vivo путем сайт-направленный мутагенез (Li 1990, Уокер и Каваока 1993, Хоримото и Каваока 1995, Ито 2001). И наоборот, удаление обратной генетикой многоосновный сайт расщепления ослабляет фенотип HPAI (Tian 2005).Однако существуют вирусные штаммы, в которых нуклеотидная последовательность, кодирующая Сайт расщепления HA и фено- / патотип не совпадают ожидаемым образом: чилийский H7N3 HPAIV которые возникли в результате межсегментарной рекомбинации, показали основные аминокислотные остатки только в положениях -1, -4 и -6 (Суарес 2004). Аналогичные примеры существуют для линии передачи H5 (Kawaoka 1984). На с другой стороны, было показано, что изолят H5N2 из Техаса несут консенсус сайта расщепления HPAIV. последовательность, но клинически классифицирована как LPAI (Lee 2005).Эти данные еще раз подчеркивают полигенный и сложный характер патогенности вируса гриппа. К счастью, появление фенотипов HPAI в полевых условиях является редким событием. За последние пятьдесят лет только 24 первичных вспышки HPAI были вызваны HPAIV, что, вероятно, возник de novo таким образом в полевых условиях, о которых сообщается во всем мире (Таблица 1). Кроме того, было показано, что HPAIV может заразить млекопитающих и людей в частности. Это особенно наблюдалось для азиатского происхождения. H5N1 ( ВОЗ, 2006 г.).Хозяин-зависимая патогенность HPAIV H5N1 для млекопитающих был изучен на нескольких модельных видах: мыши (Lu 1999, Li 2005a), хорьки (Zitzow 2002, Говоркова 2005), обезьяны-циномолги (Rimmelzwaan 2001) и свиней (Choi 2005). Исход заражения был зависит от штамма вируса и вида хозяина. По-видимому, хорьки отражают патогенность люди лучше, чем мыши (Maines 2005).Ряд генетических маркеров, которые, как считается, вовлечены в патогенность, были расположены в разных сегментах Z-генотипа H5N1 (таблица 2).Среди них механизмы вмешательство в механизмы защиты первой линии хозяина, такие как система интерферона, через продукт гена NS-1 получил заметный интерес. Экспериментально это было с помощью обратной генетики продемонстрировали, что белки NS-1 некоторых штаммов H5N1, несущие глутаминовую кислоту в положении 92 способны обойти противовирусные эффекты интерферона и некроз опухоли фактор-альфа, что в конечном итоге приводит к усилению репликации и уменьшению выведения из зараженный хост (Seo 2002 + 2004).Кроме того, иммуноопосредованное повреждение в результате NS-1-опосредованного нарушение сети цитокинов может быть причиной поражения частей легких (Cheung 2002, Lipatov 2005). Однако ни одна из мутаций (таблица 2) сама по себе представляет собой истинную предпосылку патогенности у млекопитающих (Липатов 2003 г.). Следовательно, оптимальные генные созвездия для большого степень, по-видимому, вызывает специфические патотипы у млекопитающих в зависимости от хозяина. (Липатов 2004 г.).
Клиническая презентация После инкубационного периода обычно несколько дней (но редко до 21 дня), в зависимости от характеристик изолята, доза инокулята, вид и возраст птицы, клинические проявления птичьего гриппа в Птицы изменчивы, а симптомы довольно неспецифичны (Elbers 2005).Поэтому диагноз исключительно на основании клинических проявлений невозможно. Симптомы после заражения низкопатогенным AIV могут быть столь же дискретными, как рыхлые перья, временное снижение яйценоскости или потеря веса в сочетании с незначительным респираторное заболевание (Capua and Mutinelli 2001). Некоторые штаммы LP, такие как некоторые азиатские линии H9N2, адаптирован к эффективной репликации у домашней птицы, может вызывать более заметные признаки, а также значительная смертность (Bano 2003, Li 2005). Болезнь кур и индеек является высокопатогенной. характеризуется внезапным появлением тяжелых симптомов и смертностью, которая может приближаться к 100% в течение 48 часов (Swayne and Suarez 2000).Распространение внутри пораженной плёнки зависит от форма выращивания: в стадах с подстилкой, где возможен прямой контакт и смешивание животных. возможно, инфекция распространяется быстрее, чем в клеточных хозяйствах, но все равно потребуется несколько дней для полного заражения (Capua 2000). Часто поражается только часть конюшни. Многие птицы умереть без предупреждающих признаков, поэтому иногда вначале заподозривают отравление (Накатами 2005). Стоит отметить, что конкретный изолят вируса HPAI может спровоцировать тяжелое заболевание у одного человека. видов птиц, но не в других: на рынках живой птицы в Гонконге до завершения депопуляция в 1997 г., 20% кур, но только 2.5% укрытых уток и гусей H5N1 HPAIV, в то время как все другие виды галлиформ, воробьинообразных и пситтацинов протестированы на вирус-отрицательные и только у цыплят действительно наблюдались клинические проявления болезни (Shortridge 1998). В промышленных птицеводческих хозяйствах резкий рост, за которым следует снижение потребления воды и пищи может сигнализировать о наличии системного заболевания у ок. У несушек очевидное прекращение яйценоскости. Отдельные птицы пострадавшие от HPAI часто выявляют лишь сильную апатию и неподвижность (Kwon 2005).Отек, видны на неперых участках головы, цианоз гребня, бородок и ног, зеленоватый понос и затрудненное дыхание может присутствовать непостоянно. Слоями видны яйца с мягкой скорлупой. первоначально, но любые яйцекладки быстро прекращаются по мере прогрессирования болезни (Elbers 2005). Нервные симптомы, включая тремор, необычные позы (кривошея) и проблемы с координацией. (атаксия) преобладают у менее уязвимых видов, таких как утки, гуси и ратиты (Kwon 2005). Во время вспышки HPAI в Саксонии, Германия, в 1979 г., гуси навязчиво плавали в узкие круги на пруду были одними из первых заметных знаков, ведущих к предварительному подозрение на HPAI. Клинические проявления инфекции птичьего гриппа у людей обсуждаются в подробно в главе «Клинические Презентация человеческого гриппа ».Патология LPAI Поражения различаются в зависимости от штамма вируса и вид и возраст хозяина. Как правило, только индейки и куры обнаруживают какие-либо макроскопические и микроскопические признаки. изменения, особенно со штаммами, адаптированными к этим хозяевам (Capua and Mutinelli 2001). У индюков синусит, трахеит и аэросаккулит выявлены, хотя вторичные бактериальные инфекции возможно, тоже внесли свой вклад.Описан панкреатит у индеек. У цыплят мягкий Чаще всего наблюдается поражение дыхательных путей. Кроме того, поражения концентрируются на половые органы несушек (яичники, яйцеводы, желточный перитонит). HPAI Макропатологические и гистопатологические изменения HPAI показывают зависимости, аналогичные тем, которые указаны для клинической картины. Четыре классы патологических изменений были предварительно постулированы (Perkins and Swayne 2003): (i) Сверхострый (смерть в течение 24-36 часов после заражения, в основном наблюдается у некоторых galliforme) и острые формы болезни не выявляют характерных макроскопических патологических изменения: дискретный гидроперикард, легкая кишечная непроходимость и иногда петехиальный кровотечения из серозной оболочки брыжейки и перикарда описаны непоследовательно (Mutinelli 2003a, Джонс и Суэйн 2004).У цыплят, инфицированных азиатской линией H5N1, иногда обнаруживаются геморрагические пятна и значительное количество слизи в трахее (Elbers 2004). Серозные экссудаты в полостях тела и отек легких. Точечные кровотечения в слизистой оболочке proventriculus, которые в прошлом часто описывались в учебниках, были лишь в исключительных случаях. встречается у домашней птицы, инфицированной азиатской линией H5N1 (Elbers 2004). Различные гистологические поражения вместе с вирусным антигеном можно обнаружить в разных органах (Mo 1997).В вирус впервые обнаруживается в эндотелиальных клетках. Позже инфицированные вирусом клетки обнаруживаются в миокард, надпочечники и поджелудочная железа. Нейроны, а также глиальные клетки мозга также становятся зараженный. Патогенетически можно предположить курс, сходный с течением других эндотелиотропных вирусов, где активация эндотелия и лейкоцитов приводит к системному и нескоординированному высвобождению цитокинов предрасполагающие к сердечно-легочной или полиорганной недостаточности ( Feldmann 2000, Кленк 2005).(ii) У животных с длительным появлением симптомов и продолжительным течением болезни, неврологические симптомы и, гистологически, негнойные поражения головного мозга преобладают изображение (Перкинс и Суэйн 2002a, Квон 2005).Однако вирус также можно изолировать от других органы. Этот курс был экспериментально описан на гусях, утках, эму и других видах животных. инфицированы штаммом HPAI H5N1 азиатской линии. У несушек – воспаление яичников. и яйцеводами, а после разрыва фолликула можно увидеть так называемый желточный перитонит. (iii) У уток, чаек и домашних воробьев наблюдалась только ограниченная репликация вируса. найденный. У этих птиц наблюдалась легкая интерстициальная пневмония, воздушный саккулит и иногда лимфоцитарный. и гистиоцитарный миокардит (Perkins and Swayne 2002a, 2003). (iv) В экспериментах, описанных Perkins and Swayne (2003), голуби и скворцы оказались устойчивыми к заражению H5N1. Однако Вернер и соавт. (будет опубликован) были способны вызвать длительное неврологическое заболевание из-за негнойного энцефалита (Klopeisch 2006) у 5/16 голубей с использованием недавно полученного индонезийского изолята HPAI H5N1. Дифференциальная диагностика Необходимо учитывать следующие заболевания в дифференциальной диагностике HPAI из-за их способности вызывать внезапное начало болезни сопровождается высокой смертностью или гемостазом в бородках и гребнях:
Менее тяжелые формы HPAI могут вызывать еще большее затруднение с клинической точки зрения.Быстрая лаборатория диагностическая помощь, таким образом, имеет решающее значение для всех дальнейших мер (Elbers 2005). Лабораторная диагностика Сборник образцов Образцы следует собирать из нескольких свежие туши и от больных птиц стада. В идеале адекватная выборка статистическое резервное копирование, и диагностика выполняется на постоянной основе. При отборе проб подозреваемых птиц HPAI, необходимо соблюдать стандарты безопасности, чтобы избежать воздействия на сборщики проб потенциально зооантропонозный HPAIV ( Bridges 2002).Были предложены руководящие принципы CDC (CDC 2005).Для вирусологических анализов мазки, полученные из клоаки и ротоглотки. обычно позволяют провести тщательное лабораторное исследование. Материал, собранный на тампонах, должен быть смешивают с аликвотами по 2-3 мл стерильной изотонической транспортной среды, содержащей антибиотик. добавки и источник белка (например, 0,5% [мас. / об.] бычьего сывороточного альбумина, до десяти процентов бычья сыворотка или инфузия мозг-сердце). При вскрытии, проведенном в безопасных условиях и во избежание распространения болезни (см. выше) собираются образцы содержимого головного мозга, трахеи / легкого, селезенки и кишечника без консервантов. для выделения вируса. Для серологических целей берут образцы нативной крови. Количество образцов собранные должны быть достаточно обнаружены с 95% доверительным интервалом для параметра с распространенностью 30%. Транспортировка образцов Мазки, ткани и кровь должны быть перевозятся охлажденными, но не должны замерзать. Если ожидаются задержки более 48 часов в Транзитные образцы следует замораживать и перевозить на сухом льду. Во всех случаях транспортная безопасность правила (e.грамм. Правила IATA) следует неукоснительно соблюдать во избежание распространения болезни и случайное облучение персонала при транспортировке. Настоятельно рекомендуется связаться с назначенным диагностическая лаборатория перед отправкой образцов и, в идеале, еще до их сбора. Диагностические каскады Прямое обнаружение инфекции AIV В основном есть две (параллельные) линии диагностических мер, направленных на (i) выделение и подтип вируса классическими методами (см. Руководство МЭБ 2005) и (ii) молекулярно обнаружить и охарактеризовать вирусный геном.(i) Обычно вирус гриппа гриппа выделяется путем инокуляции жидкостей мазков или гомогенаты тканей в куриные яйца с зародышем 9-11 дней, обычно хориоаллантоисом саквояжный путь (Woolcock 2001). В зависимости от патотипа эмбрионы могут погибнуть, а могут и не погибнуть. пятидневный период наблюдения и обычно нет характерных поражений, которые можно увидеть на либо эмбрион, либо аллантоисная мембрана (Mutinelli 2003b). Яйца, инокулированные HPAIV-содержащими материал обычно умирает в течение 48 часов.Наличие гемагглютинирующего агента может быть обнаружено в собранной аллантоисной жидкости. Гемагглютинация (ГК) – это нечувствительный метод, требующий как минимум 10 6,0 частиц на мл. Если в посевном материале присутствует только низкая концентрация вируса, до для некоторых штаммов LPAIV может потребоваться еще два пассажира в яйцах с зародышем, чтобы производят достаточно вируса для обнаружения HA. В случае HPAIV второй проход с использованием разбавленного инокулят может быть полезным для оптимального производства гемагглютинирования. Гемагглютинирующие изоляты антигенно характеризуются гемагглютинацией тесты на ингибирование (HI) с использованием (моно-) специфических антисывороток против подтипов 16 H и, для борьбы с различными типами птичьих парамиксовирусов, которые также проявляют гемагглютинирование деятельность. Подтип NA может быть впоследствии определен анализами ингибирования нейраминидазы, опять же требуются сыворотки, специфичные для подтипа (Aymard 2003). В случае если изоляты линий H5 или H7 являются встречаются, их индекс внутривенной патогенности (IVPI) необходимо определить, чтобы различать между биотипами LP и HP (Allan 1977).Это достигается путем в / в вакцинации десяти детей в возрасте 6 недель. цыплята с изолятом вируса, выращенного из яиц (0,1 мл аллантоисной жидкости в разведении 1: 10; с титром HA более 1 из 16). За цыплятами наблюдают в течение десяти дней на предмет клинические симптомы. Результаты интегрируются в индекс, который указывает на вирус HPAI, когда значения больше 1,2. В качестве альтернативы, изолят HPAI встречается, когда не менее семи из десяти (75%) привитых цыплят погибают в течение периода наблюдения. Описанные классические процедуры позволяют диагностировать HPAI в течение пяти дней, но может потребоваться более двух недель, чтобы исключить наличие AIV. Кроме того, высокое качество диагностические инструменты (яйца SPF, специфические антисыворотки H- и N-подтипов) и квалифицированный персонал являются предпосылка. В настоящее время не существует применения клеточных культур для выделения AIV, который может достичь чувствительности куриных яиц с эмбрионами ( Seo 2001).(ii) Более быстрый подход, особенно когда требуется исключение инфекции, использует молекулярные методы, которые также должны следовать каскадному стилю: наличие гриппа A специфическая РНК обнаруживается посредством полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) который нацелен на фрагменты гена M, наиболее консервативного сегмента генома вирусов гриппа (Fouchier 2000, Spackman 2002) или ген нуклеокапсида (Dybkaer 2004).Когда положительный результат После получения ОТ-ПЦР амплифицирующие фрагменты гена гемагглютинина подтипов H5 и H7 проводят для обнаруживать присутствие заметных AIV (Dybkaer 2004, Spackman 2002). Если снова положительный результат, молекулярная диагностика патотипа (LP по сравнению с HP) возможна после секвенирования фрагмента Ген НА, охватывающий сайт эндопротеолитического расщепления. Изоляты, содержащие несколько основных аминокислот. кислоты классифицируются как HPAI. ПЦР и другие методы ДНК-анализа разрабатываются для обнаружение штаммов H5N1 азиатского происхождения (Collins 2002, Payungporn 2004, Ng 2005).Подтипы, не относящиеся к H5 / H7, можно определить по каноническому ОТ-ПЦР и последующий анализ последовательности субъединицы HA-2 (Phipps 2004). Это также специфические праймеры для каждого подтипа NA. Полная характеристика может быть достигнута за три дней, особенно когда используются методы ПЦР в реальном времени (Perdue 2003, Lee and Suarez 2004). Однако, Чипы ДНК находятся в стадии разработки, которые должны еще больше упростить типирование вирусов AI (Li 2001, Кесслер 2005). Диагноз исключения возможен в течение одного рабочего дня.Недостатки молекулярной диагностики – это цена, за которую приходится платить закупка оборудования и расходных материалов, хотя, если таковые имеются, многие образцы могут быть проанализированы менее персонала в значительно более короткие сроки по сравнению с выделением вируса в яйцах. Однако не следует Следует держать в секрете, что каждая реакция ПЦР или гибридизации, в отличие от выделения вируса в яйцах, таит в себе внутреннюю неопределенность, связанную с наличием определенных мутаций в данном изолировать на сайтах связывания праймеров и / или зондов, которые могут сделать анализ ложным отрицательный. Таким образом, сочетание молекулярного (например, для целей скрининга) и классического методы (например, для окончательной характеристики изолятов и подтверждения диагноза индексного случая) может помочь уравновесить недостатки двух принципов. Быстрые тесты были разработаны для обнаружения вирусного антигена в тканях. мазки-слепки и срезы криостата с использованием иммунофлуоресценции или захвата антигена твердофазный иммуноферментный анализ (ELISA) и системы бокового потока с помощью щупа для мазков.Уже, эти методы были менее чувствительны, чем изоляция вируса или ПЦР, и поэтому могут быть трудно утверждать для юридически обязательного диагноза, особенно для индексного случая (Davison 1998, Селлек 2003, Каттоли 2004). В ветеринарии до сих пор не решены вопросы использования боковых тестов. младенчество и нуждается в дальнейшем развитии. Косвенное обнаружение инфекции AIV Серологический анализ на основе стада может быть полезен для в целях проверки (Beck 2003). Для обнаружения антител, специфичных к AIV, в образцах сыворотки. от птиц или в яичном желтке в случае несушек подавление гемагглютинации (HI) Анализ с использованием антигенов подтипа сравнения по-прежнему является золотым стандартом.Специально для группы антитела (вирус гриппа типа A) против белка нуклеокапсида также могут быть обнаружены с помощью агара иммунопреципитации в геле и с помощью иммуноферментных анализов (ELISA) (Meulemans 1987, Snyder 1985, Джин 2004). Конкурсные форматы ELISA позволяют исследовать сыворотки всех видов птиц, независимо от наличия видоспецифичных конъюгатов (Shafer 1998, Zhou 1998). An Сообщалось о формате ELISA для обнаружения специфичных к H7 антител (Sala 2003), но в настоящее время нет такого анализа для обнаружения специфичных к H5 антител в сыворотка птиц. Кинетика антител, специфичных к подтипу, зависит от вирусного штамма характеристик и, прежде всего, вида-хозяина. У куриных птиц, AIV-специфические антитела становятся достоверно выявляемыми в течение второй недели после контакт; антитела в яичном желтке обнаруживаются с задержкой в несколько дней (Beck 2003). В продукция и обнаружение антител у видов Anatidae гораздо более вариабельны (Suarez and Шульц-Черри 2000). Трансмиссия Передача между птицами Вирусы птичьего гриппа низкой круг патогенности генетически стабилен у диких водоплавающих птиц (Webster 1992).Инфекционный цикл среди птицы зависят от фекально-оральных цепей передачи. Помимо прямой передачи от хоста к хозяин, косвенное распространение через зараженную вирусом воду и фомиты является важным путем в отличие от инфекции вируса гриппа у млекопитающих (люди, свиньи и лошади) при передаче через аэрозоли преобладает. У птиц пиковые титры экскреции до 10 8,7 x 50% Была измерена доза заражения яиц (EID 50 ) на грамм фекалий (Webster 1978). В среднем титры будут значительно ниже.Вирусы птичьего гриппа проявляют удивительную способность сохранять инфекционность в окружающей среде и особенно в поверхностных водах, несмотря на их кажущиеся деликатная морфология (Stallknecht 1990a + b, Lu 2003). Было показано, что суспензии вирусов в воде сохраняют инфекционность более 100 дней при 17 ° C. Ниже -50С вирус может храниться бесконечно. Данные предоставлены Ito et al. (1995) и Okazaki et al. (2000) представили доказательства, что в в палеарктических регионах вирусы птичьего гриппа сохраняются в замерзшей озерной воде зимой в отсутствие мигрирующих естественных хозяев.По возвращении для разведения во время в следующем сезоне возвращающиеся птицы или их (восприимчивое) потомство повторно заражаются вирусами высвобождается случайно из-за талой окружающей воды. В соответствии с этим была выдвинута гипотеза что вирусы гриппа могут храниться во льду окружающей среды в течение длительных периодов времени (Смит 2004), и что древние вирусы и генотипы могут быть переработаны из этого резервуара (Rogers 2004 г.). Введение подтипов H5 или H7 вирусов LPAI в восприимчивую домашнюю птицу ocks является основой цепочки инфекционных событий, которые могут привести к de novo развитие высокопатогенных биотипов.Риск передачи инфекции от диких от птицы к домашней птице больше всего там, где домашние птицы свободно передвигаются, делят запас воды с диких птиц, или используйте воду или корм, которые могут быть заражены пометом инфицированных переносчики диких птиц (Capua 2003, Henzler 2003). Птицы заражаются при прямом контакте с выделяющие вирус животные и их выделения или через контакт с (абиотическими) переносчиками, которые заражены вирусосодержащим материалом. Попав в домашнее хозяйство, LPAIV может или может не зависеть от фазы адаптации к виду домашней птицы до того, как они будут выделены в больших количествах Достаточно большой, чтобы обеспечить устойчивую горизонтальную передачу внутри и между стоянками.HPAIV, как только он возник в результате заражения вирусом LPAIV, распространяется аналогичным образом. Так называемый «мокрый» рынки, где в условиях скопления людей продаются живые птицы, являются мультипликаторами распространения (Шортридж 1998, Булага 2003). Меры биобезопасности, направленные на изоляцию крупных птицеводческих хозяйств, эффективно предотвращать передачу от фермы к ферме механическими средствами, такими как зараженные оборудование, транспортные средства, корм, клетки или одежда – особенно обувь. Анализ итальянского HPAI При эпизоотии 1999/2000 г. выявлены следующие риски передачи: перемещение инфицированных fl ocks (1.0%), опосредованные контакты при транспортировке птицы на бойню (8,5%), окрестности в радиусе одного километра вокруг зараженных помещений (26,2%), грузовые автомобили, используемые для перевозки кормов, подстилок или туш (21,3%), другие косвенные контакты посредством обмена сельскохозяйственным персоналом, рабочими машинами и т. д. (9,4%) (Marangon and Capua 2005). Там не было никаких намеков на аэрогенное распространение, полученное во время итальянской эпизоотии. Однако во время вспышек в Нидерландах (2003 г.) и Канаде (2004 г.) рассматривалось распространение по воздуху (Landman and Schrier 2004, Lees 2004).Роль живых переносчиков, таких как грызуны или мухи, которые могут действовать как «механические переносчики» и сами не инфицированы, в основном неопределенный, но, конечно, не является важным фактором.До появления азиатской линии H5N1 HPAIV, повторное внедрение HPAIV из домашней птицы в популяцию диких птиц не играли существенной роли. В апреле 2005 г. однако болезнь, ассоциированная с вирусом H5N1 азиатского происхождения, обнаружена в озере Цинхай в Северо-Западном Китае. поражение тысяч гусей с головами и других мигрирующих видов уток, бакланов и чаек (Чен 2005, Лю 2005).Следовательно, передача вирусов H5N1 азиатской линии дикими птицами должна быть учтены в будущих профилактических концепциях (обсуждаемых ниже). С конца 2003 г. в Азии были обнаружены некоторые вирусы H5N1, которые высоко патогенен для кур, но не для уток ( Sturm-Ramirez 2005). Экспериментальные инфекции с использованием этих изолятов выявили гетерогенная смесь в отношении генетического анализа и способности образовывать бляшки в клетке культура (Hulse Post 2005). Было показано, что утки, пережившие заражение этими изолятами, теряют популяция вируса на 17-е сутки, утратившая свой патогенный потенциал для уток.Когда клинические признаки используемые для проверки наличия HPAIV H5N1 в полевых условиях, утки могут стать «троянским конем» этого вируса (Webster 2006).Передача человеку Передача вирусов птичьего гриппа в у людей, приводящее к развитию клинически явной болезни, является редким явлением (Таблица 3). Учитывая потенциальное заражение миллионов людей HPAIV H5N1 в Юго-Восточной Азии, фактическое количество задокументированные случаи заболевания людей, хотя и неуклонно растущие в последние годы, все же следует рассматривать как сравнительно низкая ( http: // www.who.int/csr/disease/avian_influenza/country/en).Первая ассоциация азиатской линии HPAIV H5N1 с респираторным заболеванием в Люди наблюдались в Гонконге в 1997 году, когда шесть из 18 инфицированных H5N1 людей умерли. Эти случаи были эпидемиологически связаны со вспышкой высокопатогенного H5N1 среди живых птиц. рынки (Yuen 1998, Claas 1998, Katz 1999). Риск прямой передачи вируса H5N1 от птиц к человеку, по-видимому, больше всего у людей, которые близко контактируют с живую зараженную домашнюю птицу или поверхности и предметы, сильно загрязненные их пометом.Контакт риск считается значительным во время убоя, перетира, разделки и подготовки птицы для приготовления пищи (http://www.who.int/csr/don/2005_08_18/en/). Азиатский Вирус H5N1 линии HPAI можно найти во всех тканях, включая мясо, по всей птице туша. В нескольких таких случаях сообщалось, что человек, который зарезал или приготовил заболевшая птица для употребления в пищу заболела смертельным исходом, в то время как члены семьи, принимавшие участие в трапезе не сделал (http://www.who.int/csr/don/2005_10_13/en/index.html).
* Источник: Птичий грипп – оценка угрозы пандемии.ВОЗ, http://www.who.int/csr/disease/influenza/WHO_CDS_2005_29/en/, по состоянию на 06 января 2006 г. ** Высоко патогенен для птицы Штамм H9N2 вызывал легкие, похожие на грипп симптомы, у двух детей в Гонконге SAR в 1999 г. и у одного ребенка в середине декабря 2003 г. (Saito 2001, Butt 2005). Штамм H9N2 циркулирующие в организме домашней птицы в это время вызывали значительные симптомы и летальность в очень уязвимые виды, такие как индейки и куры. На сегодняшний день нет доказательств того, что правильно приготовленное мясо птицы или продукты из птицы являются источником заражения человека азиатской линией H5N1.Как правило, ВОЗ рекомендует тщательно готовить мясо, чтобы все части мяса достигают внутренней температуры 70 C. При этой температуре вирусы гриппа инактивирован, что делает безопасным любое сырое мясо птицы, зараженное вирусом H5N1 ( ВОЗ 2005).Передача другим млекопитающим Вирусы птичьего гриппа были передается разным видам млекопитающих несколько раз. Здесь следующие циклы репликации и адаптация, могут быть созданы новые эпидемические линии.Свиньи, в частности, часто участвуют в таких «межклассовых трансверсиях ». В европейских популяциях свиней широко распространены птичьи вирусы h2N1 (Heinen 2002) и вирус h2N2, реассортантный вирус человека и птиц, впервые изолированный в Великобритании в 1992 году, постоянно набирает силу (Brown 1998). В США тройной реассортант (h4N2) между классическим h2N1, человеческим h4N2 и птичьим подтипами циркулирующие (Olsen 2002). Другие подтипы предположительно птичьего происхождения (например, h2N7, h5N6) были обнаруживается в основном у свиней (Brown 1997, Karasin 2000).Вирус H9N2 птичьего происхождения умеренно распространен в популяциях свиней на востоке Китая (Xu 2004). Помимо свиней, Было показано, что морские млекопитающие и лошади приобретают вирусы гриппа А из птичьих источников (Guo 1992, Ито 1999).Естественное заражение H5N1 было описано у тигров и других крупных кошек в зоопарке. в Таиланде после того, как животных скармливали вирус-положительными куриными тушками ( Keawcharoen 2004, Причуда 2004, Амосин 2005). Тяжелое заболевание, сопровождающееся последовала высокая смертность.Кроме того, передача от кошки к кошке, по-видимому, произошла в том же зоопарке. (Thanawongnuwech 2005). Это был Первый отчет о вирусных инфекциях гриппа в Felidae . Бытовые европейские короткие волосы кошки могут экспериментально заразиться вирусом H5N1 (Kuiken 2004).В 2004 г. было проведено 3000 образцов сыворотки, взятых от свободно бродячих свиней во Вьетнаме. протестировано серологически на предмет наличия вируса гриппа H5N1 (Choi 2005). Вирус анализ нейтрализации и вестерн-блоттинг подтвердили, что только 0.25% образцов были серопозитивный. При экспериментальных инфекциях было показано, что свиньи могут заражаться вирусами H5N1. изолирован в Азии в 2004 г. от людей и птиц. Слабый кашель и повышенная температура тела были единственными симптомами, наблюдаемыми в течение четырех дней после заражения. Вирус можно выделить из тканей верхних дыхательных путей не менее 6 дней. Пиковые вирусные титры в мазках из носа были обнаружены на на 2-й день после заражения, но ни одно из экспериментально инфицированных животных не передало инфекцию контактные свиньи.Смертельные вирусы H5N1, циркулирующие в Азии, по-видимому, способны к естественному заражение свиней. Однако частота таких инфекций, по-видимому, невысока. Ни один птичий и протестированные человеческие вирусы H5N1 легко передавались между свиньями в экспериментальных условиях. (Цой 2005). Основываясь на этих наблюдениях, свиньи, вероятно, в настоящее время не играют важной роли в эпидемиология азиатской линии H5N1. Вспышка высокопатогенного птичьего гриппа H7N7 среди домашних птиц в Нидерланды, Бельгия и Германия весной 2003 г. вызвали инфекцию и легкое заболевание, преимущественно конъюнктивит у 89 птицеводов, контактировавших с инфицированными животными и тушами (Koopmans 2004).В инфекция у одного ветеринара вызвала острый респираторный дистресс-синдром и закончилась летальным исходом ( Фушье 2004 г.). Кроме того, во время голландской вспышки инфекция H7N7 был вирусологически и серологически подтвержден в нескольких домашних контактах, четыре из которых показали конъюнктивит (Du Ry van Beest Holle 2005). Доказательства (бессимптомной) естественной инфекции О штаммах LPAIV подтипов H9, H7 и H5 у людей также сообщалось в других случаях в Италии. и Япония (Zhou 1996, Puzelli 2005, Promed 20060110.0090).В анекдотическом отчете (Promed Mail 20050826) фатальный инфекция, вызванная гриппом H5N1, у трех редких циветтовых кошек, рожденных в неволе в национальном парке в Был упомянут Вьетнам. Источник заражения оставался невыясненным. Еще 20 циветт того же виды, размещенные в соседних клетках, не заболели. Вирусы птичьего гриппа никогда не обнаруживались у крыс, кроликов и других животных. другие млекопитающие, присутствующие на рынках живых птиц в Гонконге, где были обнаружены 20% кур положительный для азиатской линии H5N1 (Shortridge 1998). Эпидемиология Птица До конца 2003 года ВПГП считался редким заболеванием. в птице. С 1959 г. во всем мире было зарегистрировано только 24 первичных вспышки (Таблица 1). В большинство произошло в Европе и Америке. Большинство вспышек были географически ограниченными, и только пять, что привело к значительному распространению на многочисленные фермы, и только одно – по всему миру. Ни одна из вспышек никогда не приближалась к размеру азиатских вспышек H5N1 в 2004 г. ( ВОЗ 2004/03/02).На сегодняшний день все вспышки высокопатогенной формы зарегистрированы. вызванные вирусами гриппа A подтипов H5 и H7.В прошлом вспышки, незаконная торговля или перемещение инфицированных живых птиц или их необработанные продукты и непреднамеренная механическая передача вируса через перемещение людей (путешественники, беженцы и т. д.) были основными факторами распространения HPAIV. Новое измерение вспышек HPAI стало очевидным в конце 2003 г. С середины декабря С 2003 г. по начало февраля 2004 г. вспышки среди домашних птиц, вызванные вирусом HPAI H5N1 азиатской линии. вирус был зарегистрирован в Республике Корея, Вьетнаме, Японии, Таиланде, Камбодже, Лаосской Народной Демократическая Республика, Индонезия и Китай.Одновременное возникновение в нескольких странах крупных Эпидемия высокопатогенного гриппа H5N1 среди домашних птиц беспрецедентна. Все усилия направленных на сдерживание болезни, пока не удалось. Несмотря на выбраковку и упреждающую уничтожение около 150 миллионов птиц, H5N1 в настоящее время считается эндемичным во многих частях Индонезия и Вьетнам, а также в некоторых частях Камбоджи, Китая, Таиланда и, возможно, также Лаоса. Народная Демократическая Республика. Первоначальный вирус, впервые обнаруженный в 1997 г., был реассортантным отцовства, включая как минимум вирус H5N1 от домашних гусей (A / goose / Guangdong / 1/96, пожертвовавший HA) и вирус H6N1, вероятно, от чирка (A / teal / Hong Kong / W312 / 97, пожертвовавший NA и сегментов для внутренних белков), которые прошли еще много циклов реассортации с другими неизвестные вирусы птичьего гриппа (Xu 1999, Hoffmann 2000, Гуань 2002b).Было обнаружено несколько различных генотипов линии H5N1. описан (Cauthen 2000, Guan 2002a + 2003). Так называемый генотип Z доминировал во вспышках с тех пор, как Декабрь 2003 г. (Li 2004).В апреле 2005 г. был достигнут очередной уровень эпизоотии, когда для Впервые штамм H5N1 получил доступ к популяциям диких птиц в более крупных масштабах (Chen 2005, Лю 2005). На озере Цинхай на северо-западе Китая несколько тысяч гусей с головами, мигрирующие виды, погибшие от инфекции.Некоторые виды чаек, а также бакланы были также затронуты в этом месте. Когда летом и в начале осени 2005 г. наблюдались вспышки гриппа H5N1. впервые сообщили из географически соседних Монголии, Казахстана и Южного В Сибири подозревали перелетных птиц в распространении вируса. Дальнейшие вспышки вдоль и поперек перекрывающиеся миграционные пути из внутренней Азии в направлении Ближнего Востока и Африки достигли Турции, Румыния, Хорватия и Крымский полуостров в конце 2005 г. Во всех случаях (кроме Монголии) и Хорватия) были обнаружены как домашние птицы, так и дикие водоплавающие птицы.Часто индексные случаи в домашние птицы оказались в непосредственной близости от озер и болот, где обитали дикие водные птицы. Хотя это кажется прямым намеком на мигрирующие водные птицы, распространяющие вирус, это Следует четко отметить, что вирус HPAI H5N1 азиатского происхождения до сих пор обнаружен только в умирающих или мертвых диких водных птиц. Истинный статус H5N1 в популяциях диких водоплавающих птиц и их роль в распространении инфекции остается загадочной. В настоящее время можно только предполагать могут ли дикие водные птицы переносить вирус на большие расстояния во время инкубационного периода, или действительно ли некоторые виды остаются мобильными, несмотря на инфекцию H5N1. Однако исследования в Китае показали наличие более новых генотипы вируса H5N1 азиатской линии у древесных воробьев (Kou 2005). Ни воробьи из какие вирусы были изолированы, ни утки, которые были экспериментально заражены этими вирусами, проявили какие-либо симптомы. Однако при передаче цыплятам был спровоцирован полноценный HPAI. поскольку разные воробьи одной и той же птицы несли несколько различных генотипов, которые, вероятно, возникла путем пересортировки с различными вирусами ИИ неизвестного происхождения, предполагалось, что Вирусы, подобные H5N1, уже передавались этим птицам некоторое время (месяцы?) Назад.Эти данные отметьте еще одну ступень обострения: воробьи в силу своих жизненных привычек являются идеальными посредниками между дикими птицами и домашней птицей и может переносить вирусы HPAI между этими популяциями. Локально ограниченная инфекция HP H5N1 у отдельных (больных или мертвых) воробьев также была Сообщается из Таиланда и Конг Конга. Эндемичность HPAIV у воробьиных птиц, таких как воробьи, скворцы или ласточки, живущие в тесной связи с человеческими поселениями, не только навяжут огромное давление на местную птицеводческую промышленность, но также увеличивает риски воздействия на человека (Несторович 1987). Люди до 30 -е декабря В 2005 г. было зарегистрировано 142 случая заболевания людей H5N1. Человеческая эпидемия в настоящее время ограничивается Камбоджа, Индонезия, Таиланд и эпицентр Вьетнама (65,5% всех случаев). 72 (50,7%) умерло человек.Подробнее см. В главе «Эпидемиология». Экономические последствия Вспышки высокопатогенных птиц грипп может иметь катастрофические последствия для фермеров-одиночек и птицеводства в пораженный регион в целом (см. Таблицу 1).Экономические потери обычно лишь частично связаны с прямыми гибель домашней птицы от инфекции HPAI. Меры, принимаемые для предотвращения дальнейшего распространения болезни. тяжелые потери. Последствия для питания могут быть столь же разрушительными в развивающихся странах, где птица – важный источник животного белка. Как только вспышки стали широко распространенными, контроль труднодостижим и может занять несколько лет ( | ||||
Основные правила // Лаборатория письма Purdue
Эта страница предоставлена вам OWL в Университете Пердью.При печати этой страницы вы должны включить полное юридическое уведомление.
Авторские права © 1995-2018, Лаборатория письма и СОВ при Университете Пердью и Пердью. Все права защищены. Этот материал нельзя публиковать, воспроизводить, транслировать, переписывать или распространять без разрешения. Использование этого сайта означает принятие наших условий добросовестного использования.
Справочный список: Основные правила
Примечание: На этой странице отражена последняя версия руководства по публикации APA (i.e., APA 7), выпущенный в октябре 2019 года. Аналогичный ресурс для более старого стиля APA 6 можно найти здесь.
Этот ресурс, отредактированный в соответствии с руководством по публикациям APA 7 -го издания , предоставляет фундаментальные рекомендации по созданию справочных страниц для исследовательских работ. Для получения дополнительной информации обратитесь к Руководству по публикациям Американской психологической ассоциации , (7 th ed.).
На этой странице приведены основные рекомендации по форматированию списка литературы в конце стандартной исследовательской работы APA.Большинство источников следуют довольно простым правилам. Однако, поскольку источников, полученных из академических журналов , имеют особый вес при написании исследований, на эти источники распространяются особые правила . Таким образом, на этой странице представлены основные рекомендации по цитированию академических журналов отдельно от «обычных» основных рекомендаций. Это различие поясняется ниже.
Примечание: Поскольку информация на этой странице относится практически ко всем цитатам, мы подчеркнули одно важное различие между APA 6 и APA 7 с помощью подчеркнутого примечания, написанного красным.
Форматирование справочного списка
Ваш список литературы должен быть в конце статьи. Он предоставляет информацию, необходимую читателю, чтобы найти и найти любой источник, который вы цитируете в основной части статьи. Каждый источник, который вы цитируете в статье, должен быть включен в ваш список литературы; аналогично, каждая запись в списке литературы должна быть процитирована в вашем тексте.
Ваши ссылки должны начинаться на новой странице отдельно от текста эссе; пометьте эту страницу «Ссылки» жирным шрифтом по центру вверху страницы (НЕ подчеркивайте и не используйте кавычки для заголовка).Весь текст должен быть разделен двойным интервалом, как и остальная часть вашего эссе.
Основные правила для большинства источников
- Все строки после первой строки каждой записи в вашем списке ссылок должны иметь отступ на полдюйма от левого поля. Это называется выступом.
- Имена всех авторов должны быть перевернуты (т.е. сначала должны быть указаны фамилии).
- Имя и отчество авторов должны быть написаны инициалами.
- Например, ссылка на источник, написанная Джейн Мари Смит, будет начинаться с «Smith, J.М. “ ”
- Если отчество недоступно, просто инициализируйте имя автора: “Smith, J.”
- Указывайте фамилии и имена / инициалы всех авторов определенной работы до 20 авторов включительно (это новое правило, так как APA 6 требует только первых шести авторов). Отделите инициалы каждого автора от следующего автора в списке запятой. Используйте амперсанд (&) перед именем последнего автора. Если есть 21 или более авторов, используйте многоточие (но без амперсанда) после 19-го автора, а затем добавьте имя последнего автора.
- Записи в списке литературы должны быть расположены в алфавитном порядке по фамилии первого автора каждой работы.
- Для нескольких статей одного автора или авторов, перечисленных в одном порядке, перечислите записи в хронологическом порядке, от самых ранних до самых последних.
- При ссылке на заголовки книг, глав, статей, отчетов, веб-страниц, или других источников используйте только первую букву первого слова заголовка и подзаголовка, первое слово после двоеточия или тире в заголовке. , и существительные собственные.
- Еще раз обратите внимание, что названия академических журналов регулируются особыми правилами. См. Раздел ниже.
- Выделите курсивом названия более длинных произведений (например, книг, отредактированных сборников, названий газет и т. Д.).
- Не выделяйте курсивом, не подчеркивайте или не ставьте кавычки названия более коротких произведений, таких как главы в книгах или эссе в отредактированных сборниках.
Основные правила для статей в академических журналах
- Привести названия журналов полностью.
- Названия журналов выделите курсивом.
- Сохраняйте нестандартные знаки пунктуации и заглавные буквы, которые используются в названии журнала.
- Например, вы должны использовать PhiloSOPHIA вместо Philosophia, или Past & Present вместо Past and Present.
- Сделайте заглавными буквами всех основных слов в названиях журналов . Обратите внимание, что это отличается от правила для названия других распространенных источников (например, книг, отчетов, веб-страниц и т. Д.), Описанного выше.
- Это различие основано на типе цитируемого источника. В названиях научных журналов все основные слова пишутся с заглавной буквы, в названиях других источников – нет.
- Сделайте с заглавной буквы первое слово заголовков и подзаголовков статей журнала , а также первое слово после двоеточия или тире в названии и любых имен собственных .
- Не выделяйте курсивом и не подчеркивайте заголовок статьи.
- Не заключайте заголовок статьи в кавычки.
- Так, например, если вам нужно процитировать статью под названием «Deep Blue: The Mysteries of the Marianas Trench», опубликованную в журнале Oceanographic Study: A Peer-Reviewed Publication, вы должны написать заголовок статьи как следует:
- Deep blue: Тайны Марианской впадины.
- … но вы бы написали название журнала следующим образом:
- Океанографическое исследование: рецензируемая публикация
- Так, например, если вам нужно процитировать статью под названием «Deep Blue: The Mysteries of the Marianas Trench», опубликованную в журнале Oceanographic Study: A Peer-Reviewed Publication, вы должны написать заголовок статьи как следует:
Обратите внимание: Хотя руководство APA предоставляет примеры того, как цитировать общие типы источников, оно не охватывает все возможные источники.Если вы должны указать источник, на который не ссылается APA, APA предлагает найти пример, похожий на ваш источник, и использовать этот формат. Для получения дополнительной информации см. Стр. 282 Руководства по публикациям Американской психологической ассоциации , 7 th ed.
определение avian_influenza и синонимов avian_influenza (английский)
- Относительно подтипа H5N1 птичьего гриппа см. Подтип вируса гриппа A H5N1.
Птичий грипп – неофициально известный как птичий грипп или птичий грипп – относится к «гриппу, вызываемому вирусами, адаптированными для птиц.” [1] [2] [3] [4] [5] [6] [7] [ необходимы разъяснения ] Наибольшую озабоченность вызывает высокопатогенный птичий грипп ( HPAI ).
«Птичий грипп» – это фраза, похожая на «свиной грипп», «собачий грипп», «конский грипп» или «человеческий грипп» в том смысле, что это относится к заболеванию, вызываемому любым из множества различных штаммов вирусов гриппа, которые адаптировались к конкретному хосту. Все известные вирусы, вызывающие грипп у птиц, относятся к вирусу гриппа A вида.Все подтипы (но не все штаммы всех подтипов) вируса гриппа А адаптированы для птиц, поэтому для многих целей вирус птичьего гриппа является вирусом гриппа А. (Обратите внимание, однако, что “A” означает , а не означает “птичий”).
Адаптация не является эксклюзивной. Адаптация к определенному виду не исключает адаптации или частичной адаптации к заражению разных видов. Таким образом, штаммы вирусов гриппа адаптируются ко многим видам, хотя могут быть предпочтительными по отношению к конкретному хозяину.Например, вирусы, вызывающие пандемии гриппа, адаптированы как для людей, так и для птиц. Недавнее исследование генов вируса испанского гриппа показало, что у него есть гены, адаптированные как к птицам, так и к людям, причем больше его генов принадлежит птицам, чем менее опасные более поздние пандемические штаммы.
В то время как его наиболее высокопатогенный штамм (H5N1) распространился по Азии с 2003 года, птичий грипп достиг Европы в 2005 году и Ближнего Востока, а также Африки в следующем году. [8] 22 января 2012 г. Китай сообщил о второй смерти от птичьего гриппа за месяц после других смертельных случаев во Вьетнаме и Камбодже. [9]
Генетика
Генетические факторы, позволяющие отличить «вирусы человеческого гриппа» от «вирусов птичьего гриппа», включают:
- PB2 : (РНК-полимераза): положение 627 аминокислоты (или остатка) в белке PB2, кодируемом геном РНК PB2. До H5N1 все известные вирусы птичьего гриппа имели Glu в позиции 627, тогда как все вирусы гриппа человека имели Lys.
- HA : (гемагглютинин): Вирусы HA птичьего гриппа связывают альфа-2-3 рецепторы сиаловой кислоты, тогда как вирусы HA человеческого гриппа связывают альфа-2-6 рецепторы сиаловой кислоты. Вирусы свиного гриппа обладают способностью связывать оба типа рецепторов сиаловой кислоты. Гемагглютинин является основным антигеном вируса, против которого вырабатываются нейтрализующие антитела, и эпидемии вируса гриппа связаны с изменениями его антигенной структуры. Первоначально он был получен от свиней и технически должен называться «свиной грипп» (см. Исх.7a) [ необходима ссылка ]
Подтипы
Существует множество подтипов вирусов птичьего гриппа, но только некоторые штаммы из четырех подтипов являются высокопатогенными для человека. Это типы H5N1, H7N3, H7N7 и H9N2. [10]
Заражение / распространение птичьего гриппа
Большинство заражений птичьим гриппом у людей происходит в результате контакта с мертвыми инфицированными птицами или контакта с инфицированными жидкостями. В то время как большинство диких птиц в основном имеют только легкую форму штамма H5N1, после заражения одомашненных птиц, таких как цыплята или индейки, он может стать гораздо более смертельным, поскольку птицы часто находятся в тесном контакте друг с другом.В настоящее время существует большая угроза заражения домашней птицы в Азии из-за низких гигиенических условий и тесноты. Хотя людям легко заразиться от птиц, гораздо труднее заразиться от человека к человеку без тесного и длительного контакта.
Распространение H5N1 из Азии в Европу гораздо более вероятно является причиной как легальной, так и незаконной торговли домашней птицей, чем распространение в результате миграций диких птиц, поскольку в недавних исследованиях не было вторичного роста инфекции в Азии, когда дикие птицы снова мигрируют на юг из их нерестилища.Вместо этого схемы заражения следовали за транспортом, таким как железные дороги, дороги и границы страны, что свидетельствует о гораздо большей вероятности торговли домашней птицей. Хотя в США существовали штаммы птичьего гриппа, например, в Техасе в 2004 году, они уже потушены, и не было известно, что они заражают людей.
Примеры штаммов вируса птичьего гриппа A: [11]
| ГА подтип обозначение | NA подтип обозначение | Вирусы птичьего гриппа A |
|---|---|---|
| h2 | N1 | А / утка / Альберта / 35/76 (h2N1) |
| h2 | N8 | А / утка / Альберта / 97/77 (h2N8) |
| h3 | N9 | А / утка / Германия / 1/72 (h3N9) |
| h4 | N8 | А / утка / Украина / 63 (h4N8) |
| h4 | N8 | А / утка / Англия / 62 (h4N8) |
| h4 | N2 | A / Турция / Англия / 69 (h4N2) |
| h5 | N6 | А / утка / Чехословакия / 56 (h5N6) |
| h5 | N3 | А / утка / Альберта / 300/77 (h5N3) |
| H5 | N3 | A / tern / South Africa / 300/77 (h5N3) |
| H5 | N4 | A / jyotichinara / Эфиопия / 300/77 (H6N6) |
| H5 | N9 | A / Турция / Онтарио / 7732/66 (H5N9) |
| H5 | N1 | A / цыпленок / Шотландия / 59 (H5N1) |
| H6 | N2 | A / Турция / Массачусетс / 3740/65 (H6N2) |
| H6 | N8 | A / Турция / Канада / 63 (H6N8) |
| H6 | N5 | A / буревестник / Австралия / 72 (H6N5) |
| H6 | N1 | А / утка / Германия / 1868/68 (H6N1) |
| H7 | N7 | A / вирус чумы птиц / голландский / 27 (H7N7) |
| H7 | N1 | A / цыпленок / Brescia / 1902 (H7N1) |
| H7 | N3 | A / Турция / Англия / 639H7N3) |
| H7 | N1 | A / вирус чумы птиц / Росток / 34 (H7N1) |
| H8 | N4 | A / Турция / Онтарио / 6118/68 (H8N4) |
| H9 | N2 | A / Турция / Висконсин / 1/66 (H9N2) |
| H9 | N6 | А / утка / Гонконг / 147/77 (H9N6) |
| H9 | N6 | А / утка / Гонконг / 147/77 (H9N6) |
| H9 | N8 | A / manishsurpur / Malawi / 149/77 (H9N8) |
| H9 | N7 | A / Турция / Шотландия / 70 (H9N7) |
| h20 | N8 | А / перепел / Италия / 1117/65 (х20Н8) |
| h21 | N6 | А / утка / Англия / 56 (х21Н6) |
| h21 | N9 | А / утка / Мемфис / 546/74 (х21Н9) |
| h22 | N5 | А / утка / Альберта / 60/76 / (х22Н5) |
| h23 | N6 | А / Чайка / Мэриленд / 704/77 (х23Н6) |
| ч24 | N4 | А / утка / Гурьев / 263/83 (h24N4) |
| h25 | N9 | A / буревестник / Австралия / 2576/83 (h25N9) |
Пандемия гриппа
Вирусы пандемического гриппа имеют некоторые гены вируса птичьего гриппа и обычно некоторые гены вируса гриппа человека.Пандемические штаммы h3N2 и h4N2 содержали гены вирусов птичьего гриппа. Новые подтипы возникли у свиней, зараженных птичьим и человеческим вирусами, и вскоре были переданы человеку. Свиньи считались первоначальным «промежуточным хозяином» для гриппа, потому что они поддерживали перегруппировку дивергентных подтипов. Однако другие хозяева, по-видимому, способны к аналогичной коинфекции (например, многие виды домашних птиц), и возможна прямая передача вирусов птиц человеку. [12] Штамм вируса испанского гриппа мог передаваться напрямую от птиц человеку. [13] Несмотря на связь с пандемией, вирусы птичьего гриппа неинфекционны для большинства видов. Когда они заразны, они обычно протекают бессимптомно, поэтому у носителя нет никаких заболеваний от него. Таким образом, при заражении вирусом птичьего гриппа животное не болеет гриппом. Обычно, когда болезнь (называемая «гриппом») от вируса птичьего гриппа действительно возникает в результате , это является результатом распространения штамма вируса птичьего гриппа, адаптированного к одному виду, к другому виду (обычно от одного вида птиц к другому виду птиц).Насколько известно, наиболее частым результатом этого является заболевание настолько незначительное, что его не стоит замечать (и поэтому мало изучено). Но с одомашниванием кур и индеек люди создали подтипы видов (домашняя птица), которые могут заразить вирус птичьего гриппа, адаптированный к водоплавающим птицам, и заставить его быстро мутировать в форму, которая убивает более 90% всего стада за несколько дней, может распространяться. к другим стадам и убить 90% из их , и остановить его можно только убив каждую домашнюю птицу в этом районе.До тех пор, пока в 1990-х годах люди не заразились вирусом H5N1, это была единственная причина, по которой птичий грипп считался важным. С тех пор вирусы птичьего гриппа интенсивно изучаются; что приведет к изменениям в представлениях о пандемиях гриппа, изменениям в птицеводстве, изменениям в исследованиях вакцинации против гриппа и изменениям в планировании пандемии гриппа.
H5N1 превратился в штамм вируса гриппа, который поражает больше видов, чем любой ранее известный штамм, является более смертоносным, чем любой ранее известный штамм, и продолжает развиваться, становясь одновременно более распространенным и более опасным.Это заставило Роберта Г. Вебстера, ведущего эксперта по птичьему гриппу, опубликовать статью под названием «Мир балансирует на грани пандемии, которая может убить большую часть населения» в журнале American Scientist . Он призвал выделить достаточные ресурсы для борьбы с тем, что он считает серьезной мировой угрозой для, возможно, миллиардов жизней. [14] С момента написания статьи мировое сообщество потратило миллиарды долларов на борьбу с этой угрозой с ограниченным успехом.
Вакцины были созданы против нескольких разновидностей птичьего гриппа H5N1.Вакцинация домашней птицы против продолжающейся эпизоотии H5N1 широко распространена в некоторых странах. Некоторые вакцины также существуют для использования на людях, а другие проходят испытания, но ни одна из них не была предоставлена гражданскому населению и не производится в количествах, достаточных для защиты более чем крошечной части населения Земли в случае вспышки пандемии H5N1. . Всемирная организация здравоохранения составила список известных клинических испытаний прототипов вакцин против пандемического гриппа, в том числе против H5N1.
H5N1
Высокопатогенный вирус гриппа A подтипа H5N1 – это новый вирус птичьего гриппа, который вызывает глобальную озабоченность как потенциальная угроза пандемии. Его часто называют просто «птичьим гриппом» или «птичьим гриппом», хотя это только один подтип вируса, вызывающего птичий грипп.
H5N1 убил миллионы домашних птиц во все большем числе стран Азии, Европы и Африки. Эксперты в области здравоохранения обеспокоены тем, что сосуществование вирусов гриппа человека и вирусов птичьего гриппа (особенно H5N1) предоставит возможность для обмена генетическим материалом между видоспецифичными вирусами, что, возможно, приведет к созданию нового вирулентного штамма гриппа, который легко передается и является смертельным для человека. . [15] Уровень смертности людей от H5N1 составляет 60%.
С момента первой вспышки H5N1, произошедшей в 1987 году, увеличилось число случаев передачи HPAI H5N1 от птицы к человеку, что привело к клинически тяжелым и смертельным инфекциям среди людей. Тем не менее, поскольку существует значительный видовой барьер между птицами и людьми, вирус не легко передается человеку, хотя некоторые случаи инфекции исследуются, чтобы определить, происходит ли передача от человека к человеку. [12] Необходимы дополнительные исследования, чтобы понять патогенез и эпидемиологию вируса H5N1 у людей. Пути воздействия и другие характеристики передачи болезней, такие как генетические и иммунологические факторы, которые могут увеличить вероятность заражения, до конца не изучены. [16]
18 января 2009 года 27-летняя женщина из восточного Китая умерла от птичьего гриппа, заявили китайские власти, что сделало ее вторым человеком, умершим от смертельного вируса на тот момент.По сообщению министерства, два теста женщины дали положительный результат на птичий грипп H5N1, но не сообщили, как она могла заразиться этим вирусом. [17]
Несмотря на то, что с момента его открытия этим вирусом заразились миллионы птиц, по данным ВОЗ на 2 февраля 2011 г., 306 человек умерли от H5N1 в двенадцати странах. [18]
Птичий грипп унес жизни не менее 300 человек в Азербайджане, Камбодже, Китае, Египте, Индонезии, Ираке, Лаосе, Нигерии, Пакистане, Таиланде, Турции и Вьетнаме.Эпидемиологи опасаются, что в следующий раз, когда такой вирус мутирует, он может перейти от человека к человеку; однако нынешний вирус A / H5N1 нелегко передается от человека к человеку. Если произойдет эта форма передачи, может возникнуть новая пандемия. Таким образом, центры по борьбе с болезнями во всем мире делают птичий грипп своим главным приоритетом. Эти организации поощряют предприятия, связанные с птицеводством, разработать превентивный план для предотвращения распространения H5N1 и его потенциально пандемических штаммов. Рекомендуемые планы сосредоточены на обеспечении рабочих защитной одеждой и изоляции стад для предотвращения распространения вируса. [19]
Вспышка птичьего гриппа в Таиланде нанесла огромный экономический ущерб, особенно птицеводам. Зараженных птиц забивали и забивали. Общественность потеряла доверие к продуктам из птицы, что привело к снижению потребления продуктов из курицы. Это также привело к запрету стран-импортеров. Однако были факторы, которые усугубили распространение вируса, в том числе миграция птиц, низкая температура (увеличивает выживаемость вируса) и несколько фестивалей в то время. [20]
У домашних животных
Несколько домашних видов были инфицированы вирусной инфекцией H5N1 и проявили симптомы, включая кошек, собак, хорьков, свиней и птиц. [21]
Птицы
В Соединенных Штатах предпринимаются попытки свести к минимуму присутствие HPAI у домашней птицы путем тщательного регулярного надзора за птичьими стадами при коммерческих птицеводческих хозяйствах. Обнаружение вируса HPAI может привести к немедленному уничтожению стада. Менее патогенные вирусы контролируются путем вакцинации, которая проводится в основном в стадах индейки (коды ATCvet: QI01AA23 для инактивированной вакцины для домашней птицы, QI01CL01 для инактивированной комбинированной вакцины для индеек). Такер Э., Янке Б. (февраль 2008 г.). «Вирус гриппа свиней: зоонозный потенциал и стратегии вакцинации для борьбы с гриппом птиц и свиней». Журнал инфекционных болезней 197 Дополнение 1 : S19–24. DOI: 10.1086 / 524988. PMID 18269323.
Орент, Венди. «Наука о птичьем гриппе, ответы на девять часто задаваемых вопросов». Обнаружить. Февраль 2006. 59-61.
Внешние ссылки
- Международный
- Координатор системы Организации Объединенных Наций по птичьему и человеческому гриппу (UNSIC).
- Всемирная организация здравоохранения (ВОЗ)
- Продовольственная и сельскохозяйственная организация ООН (ФАО)
- Всемирная организация здравоохранения животных (МЭБ)
- США
- Европа



 Грипп характеризуется сухим кашлем с самого начала.
Грипп характеризуется сухим кашлем с самого начала.