«Препараты интерферона могут предотвратить осложнения при коронавирусе»
Заведующий кафедрой клинической иммунологии и аллергологии Сеченовского Университета прокомментировал эффективные методы профилактики и лечения COVID-19
Какие препараты уже сегодня помогают справиться с болезнью и что ждет медицину в будущем, нам авторитетно объяснил Александр Викторович Караулов, доктор медицинских наук, профессор, заслуженный деятель науки РФ, академик РАН, заведующий кафедрой клинической иммунологии и аллергологии Института клинической медицины Первого МГМУ имени И.М. Сеченова, руководитель Международной лаборатории иммунопатологии института молекулярной медицины в Сеченовском Университете.
– Александр Викторович, какая терапия сегодня применяется у пациентов с COVID-19?
– В России создана уже восьмая версия временных методических рекомендаций по профилактике, диагностике и лечению новой коронавирусной инфекции.
– В чем преимущества интерферонотерапии при COVID-19, и как врачи используют препараты с интерфероном?
– Интерферон — наш естественный защитный белок, его призвание — блокировать вирусы. Однако вирус SARS-CoV-2 замедляет его выработку, подавляет защитные системы организма. Статья об этом опубликована в журнале Nature Reviews Immunology. Авторы исследования показали, что у пациентов с тяжелым COVID-19 содержание интерферона альфа в крови и легких минимально. А около 20% больных в критическом состоянии совсем не могли продуцировать интерферон. Нарушение выработки интерферона может быть связано и с индивидуальными особенностями больного, сопутствующими заболеваниями. Как выяснили наши коллеги из Франции, каждый пятый больной, у которого отсутствует необходимая концентрация интерферона, подвержен тяжелым осложнениям.
Статья об этом опубликована в журнале Nature Reviews Immunology. Авторы исследования показали, что у пациентов с тяжелым COVID-19 содержание интерферона альфа в крови и легких минимально. А около 20% больных в критическом состоянии совсем не могли продуцировать интерферон. Нарушение выработки интерферона может быть связано и с индивидуальными особенностями больного, сопутствующими заболеваниями. Как выяснили наши коллеги из Франции, каждый пятый больной, у которого отсутствует необходимая концентрация интерферона, подвержен тяжелым осложнениям.
Препараты интерферона первого типа (интерферонов альфа-2b) могут предотвращать осложнения, и чем раньше начать такую терапию, тем лучше будут результаты. Вообще, сейчас на западе большой интерес к интерферонам. Исследования идут и в Китае, и во Франции, и в Канаде, и во многих других странах. Вот еще один интересный факт: международная команда исследователей в Торонто установила, что интерферон альфа-2b ускоряет избавление организма от вируса, восстановление после перенесенного заболевания.
– Препараты интерферона давно применяются в российском здравоохранении — получается, что здесь мы вытянули «счастливый билет», ведь на Западе зарегистрированы в основном пока только инъекционные формы?
– Совершенно верно. Только не «вытянули», а заработали научным трудом, многолетними испытаниями. Есть ряд уникальных препаратов, которые уже проверены десятилетиями. Здесь российская наука опережает западную в плане опыта применения и разнообразия форм, благодаря которым экзогенный (поступающий в помощь организму извне в лекарственной форме) интерферон давно и успешно используется в нашей медицине. Есть такие уникальные препараты, как Виферон, который имеет уже более чем 20-летний опыт медицинского применения, в том числе у таких «хрупких» пациентов, как новорожденные дети и беременные женщины. Он успешно применялся при «птичьем» и «свином» гриппе, при менингитах. Важно, что в распоряжении российских медиков есть и системные формы экзогенного интерферона (свечи), которые действуют на организм в целом, и наружные формы — гели, мази и др. Они помогают защищаться от инфекции, активизируя защиту в носовых ходах — «входных воротах» для респираторной инфекции.
Есть такие уникальные препараты, как Виферон, который имеет уже более чем 20-летний опыт медицинского применения, в том числе у таких «хрупких» пациентов, как новорожденные дети и беременные женщины. Он успешно применялся при «птичьем» и «свином» гриппе, при менингитах. Важно, что в распоряжении российских медиков есть и системные формы экзогенного интерферона (свечи), которые действуют на организм в целом, и наружные формы — гели, мази и др. Они помогают защищаться от инфекции, активизируя защиту в носовых ходах — «входных воротах» для респираторной инфекции.
– Российские врачи во время эпидемии еще раз убедились в эффективности интерферонотерапии, а изменится ли отношение к интерферону за рубежом?
– Оно уже изменилось. В Китае и Австрии тоже появились наружные формы интерферона, только они используются в виде ингаляций. Система интерферона активно исследуется, появилась масса новых публикаций в крупнейших международных изданиях.
Наша команда с оптимизмом смотрит в будущее и активно участвует в создании диагностических и прогностических параметров исследования иммунной системы. Есть все основания надеяться, что все вместе мы не только справимся с этой пандемией, но и создадим мощную научно-исследовательскую базу для борьбы с другими инфекциями.
Ссылка на публикацию: kp.ru
Новое лекарство от Covid-19 резко снижает необходимость ИВЛ. Но оно пока не одобрено
- Джастин Роулэтт
- BBC News
Автор фото, Getty Images
Предварительные результаты клинического испытания нового препарата для лечения коронавируса показали, что его применение резко снижает число пациентов, которым требуется искусственная вентиляция легких, при этом время, проведенное пациентом в больнице, сокращается на треть.
Лечение, разработанное британской биотехнологической компанией Synairgen, использует белок интерферон бета, который производит организм человека для борьбы с вирусной инфекцией.
При лечении этот белок нужно вдыхать при помощи специального ингалятора – небулайзера.
Небулайзер применяется при лечении бронхиальной астмы и ряда респираторных заболеваний, с его помощью лекарство вводится в легкие в виде мелкодисперсного аэрозоля, стимулируя иммунную реакцию организма.
Предварительные результаты исследования показывают, что это лечение сокращает на 79% число пациентов, у которых в больнице развивается тяжелая форма заболевания, требующая искусственной вентиляции легких.
У пациентов в два-три раза повышаются шансы на улучшение до состояния, при котором болезнь не мешает им вести их обычную повседневную деятельность.
Интерферон бета также сокращает число пациентов, испытывающих удушье. А время, проведенное ими в больнице, уменьшается на треть – с девяти дней до шести.
Как проводилось исследование
В двойном слепом исследовании участвовал 101 доброволец из девяти британских больниц. Половина участников принимала новый препарат, другая половина – плацебо.
Никто из участников исследования не знал, каким пациентам было назначено какое лечение, пока оно не закончилось.
В настоящий момент результаты этого исследования считаются неподтверждёнными, так как компания не публиковала его результаты в рецензируемом научном журнале. Не были пока опубликованы и полные данные исследования.
Однако Том Уилкинсон, руководитель исследования, считает, что если результаты подтвердятся, новое лекарство изменит ситуацию в лечении от этой болезни. По его словам, хотя само исследование было небольшим, его результаты впечатляющи.
Исполнительный директор компании Synairgen Ричард Марсден назвал результаты крупным прорывом в стационарном лечении пациентов с Covid-19.
“Лучших результатов, чем эти, мы и ждать не могли”, – добавил он.
Интерферон бета применяется для лечения рассеянного склероза
Что будет дальше?
Компания представит свои выводы органам здравоохранения по всему миру в ближайшие пару дней, чтобы узнать, какая дополнительная информация им нужна для одобрения лечения.
Этот процесс обычно может занимать месяцы, но британское правительство, как и многие другие, заявило, что будет работать как можно быстрее, чтобы одобрить новые разработки, обещающие эффективное лечение Covid-19.
Поэтому новое лечение может быть одобрено экстренно, как это было с препаратом ремдесивир в мае.
Возможно также, что будет разрешено опробовать лечение на большем числе пациентов, и результаты будут тщательно изучаться, чтобы подтвердить его безопасность и эффективность.
Если лечение будет одобрено, лекарство и небулайзеры нужно будет производить в больших количествах.
Ричард Марсден сообщил, что дал поручение начать производство нового лекарства еще в апреле, чтобы оно уже было в запасе, если подтвердятся положительные результаты исследования.
По его словам, Synairgen сможет уже к зиме поставлять несколько сот тысяч доз лекарства в месяц.
Как работает интерферон бета?
Интерферон бета является частью первой линии защиты организма от вирусов, предупреждая его о возможной вирусной атаке.
Коронавирус, по-видимому, подавляет его производство, чтобы обойти иммунную систему.
Новый препарат представляет собой специальный состав интерферона бета, доставляемого непосредственно в дыхательные пути через небулайзер, который превращает этот белок в аэрозоль.
Идея состоит в том, что доза белка, доставленная непосредственно в легкие, вызовет более сильную противовирусную реакцию даже у тех пациентов, чья иммунная система уже ослаблена вирусом.
Интерферон бета обычно используется для лечения рассеянного склероза.
Автор фото, BBC Panorama
Подпись к фото,Корреспондент Би-би-си Джастин Роулэтт с медсестрой Сэнди Эйткен у кровати больного
Предыдущие клинические испытания, проведенные Synairgen, показали, что интерферон бета стимулирует иммунный ответ и помогает пациентам с астмой и другими хроническими заболеваниями.
Испытание препарата компании Synairgen было частью программы Accord, созданной британским правительством для ускоренного создания новых лекарств для больных Covid-19.
Разработчики считают, что этот препарат может быть еще более эффективным на ранних стадиях инфекции.
Что говорят эксперты
“Эти результаты оценить невозможно. Нам нужны полные данные и, что еще важнее, протокол испытания. Испытание должно быть зарегистрировано, а протокол доступен еще до того, как будет проведен анализ и сделаны выводы”, – сказал профессор Стив Гудэйкр из Университета Шеффилда, специализирующийся в области неотложной медицинской помощи.
Профессор Навид Саттар, специалист в области метаболической медицины из Университета Глазго, назвал результаты впечатляющими: “Хотя исследование было небольшим, всего чуть больше 100 участников, снижение возможности развития болезни в тяжелой форме на 79% могло бы изменить ситуацию”.
“Неплохо было бы ознакомиться с полными результатами исследования после того, как они будут представлены и изучены специалистами, чтобы убедиться, что они надежны, а сами испытания были проведены надлежащим образом. Кроме того, то, что испытания проводились среди небольшого числа пациентов, снижает уверенность в действительной пользе такого лечения. Нет уверенности и в том, что людям в разных группах риска оно поможет. Чтобы получить эти данные, необходимо провести более широкие испытания. Но, несмотря на это, результаты все равно впечатляют”, – говорит он.
Use of Recombinant α-2b-Interferon in the Treatment of Acute Respiratory Viral Diseases in Children
Статтю опубліковано на с. 69-73
Острые респираторные вирусные инфекции (ОРВИ) являются наиболее распространенными инфекциями у человека. На их долю, включая грипп, приходится не менее 70 % инфекционных заболеваний. Почти 90 % населения как минимум один раз в год переносят одну из респираторных инфекций вирусной этиологии, что в целом предопределяет высокую заболеваемость и даже влияет на показатель смертности.
 Экономический ущерб только от гриппа составляет около 400 000 000 гривен в год. Кроме того, лечение ОРВИ и их осложнений (риниты, фарингиты, тонзиллиты, синуситы, оти–ты, ларингиты, бронхиты, пневмонии) занимает 80 % деятельности участкового педиатра. Данные обстоятельства объясняют приоритетность проблемы заболеваемости острыми респираторными вирусными инфекциями для здравоохранения любой страны.
Экономический ущерб только от гриппа составляет около 400 000 000 гривен в год. Кроме того, лечение ОРВИ и их осложнений (риниты, фарингиты, тонзиллиты, синуситы, оти–ты, ларингиты, бронхиты, пневмонии) занимает 80 % деятельности участкового педиатра. Данные обстоятельства объясняют приоритетность проблемы заболеваемости острыми респираторными вирусными инфекциями для здравоохранения любой страны. Развитие острых респираторных вирусных заболеваний происходит в результате аэрогенного инфицирования различными возбудителями — респираторными вирусами, бактериями, атипичными микроорганизмами. У каждого третьего больного ребенка, особенно раннего возраста, встречаются формы с высоким риском развития жизнеугрожающих синдромов (синдром крупа, нейротоксикоз, судорожный синдром, бронхообструктивный синдром) и бактериальных осложнений, определяющих тяжесть, длительность и исход заболевания [7, 11, 12]. Риск развития осложнений зависит от возраста ребенка — наиболее высок он у младших детей. По мере взросления отмечается снижение вероятности их развития на 20 % каждые последующие 6 лет жизни ребенка [11, 30].
По мере взросления отмечается снижение вероятности их развития на 20 % каждые последующие 6 лет жизни ребенка [11, 30].
Наиболее часто, в 80–90 % случаев, ОРВИ у детей вызываются вирусами гриппа и парагриппа, аденовирусами, респираторно-синцитиальными вирусами [12]. Большинство возбудителей являются РНК-содержащими вирусами, исключение составляет аденовирус, в вирион которого входит ДНК.
В литературе имеется значительное количество работ, посвященных вопросам лечения и профилактики респираторных инфекций. Практика лечения вирусных заболеваний определяет две противоположные тактики, когда и врачами, и больными при самолечении в одних случаях терапия не проводится или используются симптоматические средства, в частности жаропонижающие препараты, сосудосуживающие капли в нос, спреи, в других — с первых дней заболевания применяются антибактериальные средства. Не оправдана ни одна, ни другая тактика лечения ОРВИ. Кроме того, применение антибактериальных средств при вирусных заболеваниях нередко осложняет их течение, приводит к росту бактериальной резистентности, развитию ряда побочных эффектов и аллергических реакций.
Высокая контагиозность, скорость распространения возбудителей, изменчивость антигенных свойств вирусов, смешанный характер инфекции, развивающаяся резистентность к препаратам, возникновение вторичного иммунодефицита, нерациональная фармакотерапия оставляют вопрос терапии ОРВИ открытым [1, 5, 22]. Поэтому поиск, разработка, внедрение универсальных и перспективных средств терапии и профилактики острых респираторных вирусных заболеваний представляют важную медицинскую и социальную проблему [1, 5, 19, 25, 27].
Система интерферонов (ИНФ) способна надежно защитить здорового человека от вирусных инфекций. Однако в детском возрасте возможно нарушение синтеза интерферонов, что приводит к более частым инфекционным заболеваниям, способным принимать тяжелое и затяжное течение. Также различные отклонения в системе интерферонов могут наблюдаться при нарушениях питания, техногенных загрязнениях окружающей среды, стрессах. Особенно сниженная способность вырабатывать интерфероны обнаружена у детей, находящихся на раннем искусственном вскармливании, часто и длительно болеющих, живущих в неблагоприятной экологической обстановке, подвергшихся внутриутробному инфицированию, а также в осенне-зимние месяцы, чем, возможно, определяются сезонные вспышки вирусных заболеваний. Неоправданное назначение антибиотиков в некоторых случаях также является причиной снижения собственного иммунитета, нарушает синтез интерферонов [6].
Особенно сниженная способность вырабатывать интерфероны обнаружена у детей, находящихся на раннем искусственном вскармливании, часто и длительно болеющих, живущих в неблагоприятной экологической обстановке, подвергшихся внутриутробному инфицированию, а также в осенне-зимние месяцы, чем, возможно, определяются сезонные вспышки вирусных заболеваний. Неоправданное назначение антибиотиков в некоторых случаях также является причиной снижения собственного иммунитета, нарушает синтез интерферонов [6].
Активность интерферонов многогранна и характеризуется противовирусным, иммуномодулирующим, противоопухолевым и антипролиферативным эффектами. Противовирусное действие определяется подавлением синтеза вирусной РНК, белков оболочки вируса, активацией внутриклеточных ферментов протеинкиназы (разрушает фактор инициации синтеза белка с матричной РНК, подавляющий белковый синтез) и аденилатсинтетазы (вызывает синтез веществ, разрушающих вирусную РНК). Роль интерферонов в противовирусной защите подтверждается наличием строгой корреляции между уровнем продукции эндогенного ИНФ и выздоровлением, усугублением тяжести болезни при подавлении активности эндогенного интерферона, и, наконец, профилактическое лечение интерфероном позволяет предотвратить развитие вирусной инфекции [10]. Иммуномодулирующий эффект заключается в способности интерферонов регулировать взаимодействие клеток, участвующих в иммунном ответе, регулируя экспрессию на мембранах клеток молекул главного комплекса гистосовместимости I типа, или в непосредственной активации иммунокомпетентных клеток. Способность интерферонов замедлять или подавлять рост культуры клеток, активировать противоопухолевые механизмы иммунной системы, повышать экспрессию на злокачественных клетках молекул гистосовместимости, модулировать продукцию антител, подавлять действие опухолевых ростовых факторов определяет противоопухолевый эффект. Антипролиферативное действие заключается в способности интерферонов проявлять свойства цитостатиков — подавлять рост клеток за счет ингибирования факторов, стимулирующих пролиферацию клеток [7, 10].
Иммуномодулирующий эффект заключается в способности интерферонов регулировать взаимодействие клеток, участвующих в иммунном ответе, регулируя экспрессию на мембранах клеток молекул главного комплекса гистосовместимости I типа, или в непосредственной активации иммунокомпетентных клеток. Способность интерферонов замедлять или подавлять рост культуры клеток, активировать противоопухолевые механизмы иммунной системы, повышать экспрессию на злокачественных клетках молекул гистосовместимости, модулировать продукцию антител, подавлять действие опухолевых ростовых факторов определяет противоопухолевый эффект. Антипролиферативное действие заключается в способности интерферонов проявлять свойства цитостатиков — подавлять рост клеток за счет ингибирования факторов, стимулирующих пролиферацию клеток [7, 10].
Основные классы интерферонов — интерферон альфа (α), интерферон бета (β), интерферон гамма (γ) — оказывают значимое влияние на течение РНК-вирусных инфекций. Продукция интерферонов в большинстве случаев провоцируется проникновением в организм бактерий, вирусов или продуктов их жизнедеятельности. Интерферон не только самостоятельно борется с микроорганизмами и злокачественными опухолями, но и активирует другие факторы защиты — макрофаги и естественные киллеры. Согласно исследованиям Е.И. Юлиша и соавторов, у детей, часто и длительно болеющих острыми респираторными заболеваниями на фоне персистирующего течения вирусных инфекций, имеет место значимое снижение уровня α-интерферона в крови — в 1,5 раза по сравнению с показателем здоровых детей — и многократное повышение содержания γ-интерферона [9, 20, 26, 27]. Также имеются исследования, свидетельствующие о слабой реакции эпителиальных клеток респираторного тракта на вирусную инфекцию и низкую продукцию альфа-2b-интерферона [14], дефиците его синтеза и активности при тяжелом течении ОРВИ [8, 18].
Интерферон не только самостоятельно борется с микроорганизмами и злокачественными опухолями, но и активирует другие факторы защиты — макрофаги и естественные киллеры. Согласно исследованиям Е.И. Юлиша и соавторов, у детей, часто и длительно болеющих острыми респираторными заболеваниями на фоне персистирующего течения вирусных инфекций, имеет место значимое снижение уровня α-интерферона в крови — в 1,5 раза по сравнению с показателем здоровых детей — и многократное повышение содержания γ-интерферона [9, 20, 26, 27]. Также имеются исследования, свидетельствующие о слабой реакции эпителиальных клеток респираторного тракта на вирусную инфекцию и низкую продукцию альфа-2b-интерферона [14], дефиците его синтеза и активности при тяжелом течении ОРВИ [8, 18].
Ошибочное мнение о возможности отказаться от лечения ОРВИ может привести к тому, что респираторные инфекции принимают осложненное течение, могут вызвать обострение хронических состояний, таких как бронхиальная астма, гломерулонефрит, заболевания сердца. Своевременная терапия ОРВИ способствует более быстрому выздоровлению и предупреждает развитие осложнений. Безусловно, лечение ОРВИ должно быть комплексным и строиться индивидуально в каждом конкретном случае.
Своевременная терапия ОРВИ способствует более быстрому выздоровлению и предупреждает развитие осложнений. Безусловно, лечение ОРВИ должно быть комплексным и строиться индивидуально в каждом конкретном случае.
Достаточно широкое применение при вирусных респираторных инфекциях нашли препараты интерферона, которые, как факторы защиты и средства поддержания иммунитета, обладают широким спектром профилактического и лечебного действия [6].
Одним из первых препаратов интерферона, применяемых в клинической практике, является человеческий лейкоцитарный интерферон. Наряду с целым рядом положительных качеств он имеет и недостатки. Так, даже при применении самых совершенных систем контроля не может быть 100% гарантии того, что полученный препарат не содержит вирусов иммунодефицита человека, гепатитов В, С, D, цитомегаловируса [12]. Кроме того, несмотря на высокоэффективные методы очистки получаемого сырья, невозможно полностью избавиться от балластных белков, следовательно, препараты человеческого лейкоцитарного интерферона потенциально могут являться аллергенами [5].
На смену естественным интерферонам пришли рекомбинантные формы препаратов с интраназальным, парентеральным и ректальным способом введения, такие как Лаферобион, виферон, гриппферон, назоферон, реаферон, липоферон и др. Новые биотехнологические разработки по производству безопасных и эффективных лекарственных средств позволяют синтезировать рекомбинантные интерфероны, такие как препарат Лаферобион, в бактериальных клетках кишечной палочки. Благодаря особым технологиям получают высокоочищенную субстанцию, пригодную для применения у человека, без использования донорской крови, что исключает возможность заражения вирусами гепатита, вирусом иммунодефицита человека, цитомегаловирусом [2]. Отсутствие в процессе применения препарата Лаферобион образования нейтрализующих антител и развития нежелательных эффектов позволяет назначать его при лечении новорожденных детей, в том числе недоношенных [2].
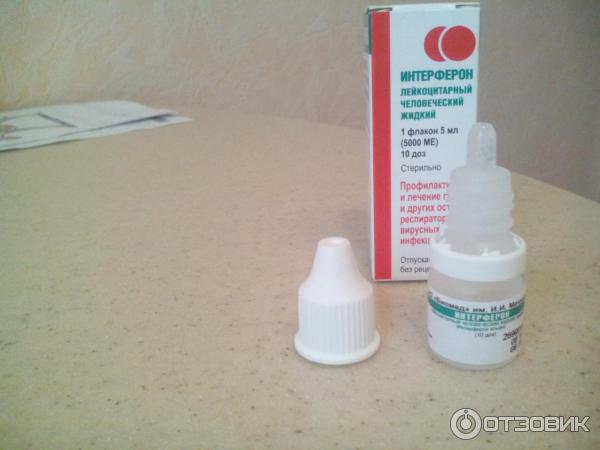
У детей при ОРВИ чаще используют препараты экзогенных рекомбинантных ИНФ для интраназального введения, имеющих специфическую активность [12, 21]. Под действием интерферонов происходят изменения топографии клеточной мембраны, что препятствует фиксации вируса и пенетрации его в середину клетки. Система интерферонов формирует защитный барьер на пути вирусов намного раньше, чем специфические защитные реакции иммунитета, путем стимуляции резистентности клеток, делая их неспособными к размножению вирусов [13]. Назальные формы препаратов рекомбинантного α-2b-интерферона целесообразно использовать для профилактики ОРВИ и при первых проявлениях заболевания [16]. Для назального применения Лаферобион выпускается в виде сухого лиофилизата для приготовления раствора в дозировке 100 тыс. МЕ во флаконах.
Под действием интерферонов происходят изменения топографии клеточной мембраны, что препятствует фиксации вируса и пенетрации его в середину клетки. Система интерферонов формирует защитный барьер на пути вирусов намного раньше, чем специфические защитные реакции иммунитета, путем стимуляции резистентности клеток, делая их неспособными к размножению вирусов [13]. Назальные формы препаратов рекомбинантного α-2b-интерферона целесообразно использовать для профилактики ОРВИ и при первых проявлениях заболевания [16]. Для назального применения Лаферобион выпускается в виде сухого лиофилизата для приготовления раствора в дозировке 100 тыс. МЕ во флаконах.
Перспективным является назначение α-2b-интерферона в виде ингаляций через небулайзер. Преимущество ингаляционной терапии заключается в том, что она может использоваться для освобождения верхних дыхательных путей от патологического содержимого, а также для доставки лекарственных препаратов к слизистой оболочке дыхательных путей. При этом возрастает интенсивность всасывания в организм лекарственного вещества, увеличивается его депонирование в подслизистом слое верхних дыхательных путей и создается высокая концентрация данного средства в очаге поражения. Лекарственное вещество распыляется и в виде аэрозоля оседает на слизистых оболочках верхних дыхательных путей. Применение небулайзерной терапии ОРВИ еще не получило широкого распространения. Однако высокая эффективность данной терапии позволяет рекомендовать ее для широкого использования в медицинской практике [23]. Для ингаляции через небулайзер Лаферобион (порошок в ампулах по 100 000 МЕ) применяется из расчета 25–30 тыс. МЕ/кг/сут на 3 приема. Содержимое ампулы предварительно необходимо растворить в 3 мл физиологического раствора хлорида натрия [15]. В последние годы появились сведения об эффективности ингаляционной коррекции интерферонового статуса препаратами ИНФ-α у новорожденных детей с синдромом полиорганной недостаточности [24], подтверждаемые достоверным повышением уровня этого цитокина в сыворотке крови на фоне лечения.
Лекарственное вещество распыляется и в виде аэрозоля оседает на слизистых оболочках верхних дыхательных путей. Применение небулайзерной терапии ОРВИ еще не получило широкого распространения. Однако высокая эффективность данной терапии позволяет рекомендовать ее для широкого использования в медицинской практике [23]. Для ингаляции через небулайзер Лаферобион (порошок в ампулах по 100 000 МЕ) применяется из расчета 25–30 тыс. МЕ/кг/сут на 3 приема. Содержимое ампулы предварительно необходимо растворить в 3 мл физиологического раствора хлорида натрия [15]. В последние годы появились сведения об эффективности ингаляционной коррекции интерферонового статуса препаратами ИНФ-α у новорожденных детей с синдромом полиорганной недостаточности [24], подтверждаемые достоверным повышением уровня этого цитокина в сыворотке крови на фоне лечения.
Таким образом, ингаляционное использование рекомбинантного α-2b-интерферона, учитывая эффективность, безопасность, удобство применения, может быть рекомендовано для клинической практики при лечении у детей острых респираторных заболеваний в первые дни, для профилактики ОРВИ — при контакте с больными вирусными инфекциями в течение всего срока угрозы инфицирования, при сезонном повышении заболеваемости, в организованных коллективах (детских и взрослых), группах риска — у медицинских работников, учителей, особенно в период эпидемии.
Еще одной формой препарата Лаферобион являются ректальные суппозитории. Применение препарата Лаферобион в форме ректальных суппозиториев позволяет свести к минимуму возможность взаимодействия с другими лекарственными препаратами [2]. В состав ректальных суппозиториев Лаферобион входят рекомбинантный α-2b-интерферон (по 150 000, 500 000 МЕ), токоферола ацетат, аскорбиновая кислота и твердый жир. Среди преимуществ суппозиториев при ОРВИ у детей — биодоступность препаратов, удобство применения, отсутствие гриппоподобного синдрома, высокий уровень абсорбции лекарственного вещества, отсутствие метаболического эффекта первого прохождения через печень [2, 16]. Наличие в комплексе препарата Лаферобион мембраностабилизирующих компонентов, цитопротекторов — токоферола ацетата и витамина С — обусловливает повышение противовирусной активности интерферона в 10–14 раз путем усиления его иммуномодулирующего действия на Т- и В-лимфоциты. Включение в состав препарата Лаферобион антиоксидантов препятствует окислительному разрушению молекул интерферона и способствует сохранности биологической активности лекарственного продукта [28].
Методика использования и дозирование ректальных суппозиториев Лаферобион:
— новорожденным, в том числе недоношенным с гестационным возрастом более 34 недель, — по 150 000 МЕ 2 раза в сутки;
— недоношенным с гестационным возрастом менее 34 недель — по 150 000 МЕ 3 раза в день 5 дней. Перерыв между курсами — 5 дней;
— детям первого года жизни — по 150 000 МЕ 2 раза в сутки;
— от 1 года до 7 лет — 500 000 МЕ 2 раза в день;
— 7–14 лет — 1 млн МЕ (2 суппозитория) 2 раза в сутки.
Курс лечения при ОРВИ — 5 дней.
В исследованиях А.П. Юрцевой и соавторов выявлено, что применение ректальных суппозиториев Лаферобион у детей, часто болеющих ОРВИ, осложненными бронхообструктивным синдромом, способствует модуляции иммунного ответа клеточным и гуморальным звеньями, происходит повышение уровня ИНФ-γ и интерлейкина-4, снижение концентрации общего IgE, отмечаются положительная динамика показателей антиоксидантной защиты, снижение продуктов перекисного окисления липидов [29]. По заключению авторов, профилактическое назначение препарата Лаферобион способствует снижению частоты ОРВИ и приступов бронхообструкции. Таким образом, использование препарата является перспективным средством профилактики бронхообструктивного синдрома у детей, протекающего на фоне ОРВИ.
По заключению авторов, профилактическое назначение препарата Лаферобион способствует снижению частоты ОРВИ и приступов бронхообструкции. Таким образом, использование препарата является перспективным средством профилактики бронхообструктивного синдрома у детей, протекающего на фоне ОРВИ.
Клиническая эффективность и безопасность ректальных суппозиториев Лаферобион при лечении ОРВИ у детей различного возраста описана в работах С.Л. Няньковского и соавторов [17].
Очень небольшой спектр противопоказаний к использованию препарата связан с индивидуальной повышенной чувствительностью к его компонентам; заболеваниями щитовидной железы, сердечно-сосудистой системы и эпилепсией; тяжелым нарушением функции почек, печени. Как правило, побочные реакции — легкие или средней тяжести, после окончания лечения исчезают [27].
Таким образом, несмотря на огромное количество препаратов для лечения ОРВИ и гриппа, представленных на современном фармацевтическом рынке, выбор лекарственного средства остается актуальной задачей для практикующего врача.
Данные исследований последних лет свидетельствуют о том, что включение α-2b-интерферона в комплексную терапию и профилактику ОРВИ способствует уменьшению выраженности воспалительного процесса, длительности заболевания, риска развития осложнений. Тактика назначения лечения и ведения больного ребенка с ОРВИ или гриппом напрямую связана с тяжестью инфекционного процесса, формой заболевания и наличием осложнений. Успех терапии зависит от правильной оценки состояния больного и раннего начала терапии. Одним из перспективных направлений не только профилактики, но и лечения вирусно-бактериальных заболеваний у детей всех возрастных групп, включая недоношенных новорожденных, является применение рекомбинантных α-2b-интерферонов, которым свойственно не только блокирование размножения инфекционных агентов, в частности вирусов, но и предотвращение инфицирования здоровых клеток, что способствует уменьшению тяжести заболевания, снижению частоты осложнений и профилактике рецидивов инфекции.
Несмотря на проводимые исследования, необходимо дальнейшее наблюдение, накопление результатов клинических исследований, касающихся обобщения сведений об эффективности действия препарата Лаферобион, различных его форм, особенностей применения у детей разного возраста с целью профилактики и лечения острых респираторных вирусных инфекций.
1. Бекетова Г.В. Интерфероны в лечении острых респираторных вирусных инфекций у детей // Ліки України. — 2011. — № 3 (149). — С. 106-109.
2. Дудник В.М. Патогенетичні особливості використання препаратів інтерферону в педіатрії // Інформаційний лист про нововедення в сфері охорони здоров’я. — № 158-2013. — Протокол № 1 від 30.04.2013.
3. Ершов Ф.И., Григорян С.С., Орлова Т.Г., Семененко Т.А., Мазанкова Л.Н., Чеботарева Т.А., Нестерина Л.Ф., Исаева Е.И. Этиопатогенетические подходы к лечению ОРВИ у детей // www.interferon.su/php/content.php?id=49.
4. Ершов Ф.И. Современная иммунопрофилактика и терапия гриппа и других острых респираторных вирусных инфекций // Consilium medicum. — 2009. — № 11. — С. 79-82.
5. Ершова И.Б., Косенко В.С., Осычнюк Л.М., Осипова Т.Ф., Мочалова А.А. Липосомные формы интерферонов в педиатрической практике при лечении ОРВИ у детей // Здоровье ребенка. — 2009. — № 2 (17). — C. 20-23.
6. Зайцева О.В. Актуальная проблема сегодняшнего дня: лечение и профилактика вирусных инфекций // http://www.interferon.su/php/content.php?id=497.
Зайцева О.В. Актуальная проблема сегодняшнего дня: лечение и профилактика вирусных инфекций // http://www.interferon.su/php/content.php?id=497.
7. Заплатников А.Л. Иммунопрофилактика и иммунотерапия острых респираторных инфекций у детей // Лечащий врач. — 2006. — № 9. — C. 50-56.
8. Казмирчук В.Е. Пособие по клинической иммунологии для практических врачей / В.Е. Казмирчук, Д.В. Мальцев. — К.: Здоров’я України, 2012. — 368 с.
9. Клинико-иммунологический статус детей, воспитывающихся в доме ребенка / Юлиш Е.И., Балычевцева И.В., Гадецкая С.Г. [и др.] // Совр. педиатрия. — 2010. — № 1 (29). — С. 63-71.
10. Колобухина Л.В. Виферон в лечении острых респираторных вирусных инфекций // РМЖ. — 2003. — № 5. — C. 306.
11. Коровина Н.А., Заплатников А.Л. Острые респираторные вирусные инфекции в амбулаторной практике врача-педиатра. — М., 2005. — 61 с.
12. Крамарев С.А. Лечение гриппа и острых респираторных вирусных инфекций у детей // Рациональная фармакотерапия. — 2008. — № 3/2. — C. 24-28.
— 2008. — № 3/2. — C. 24-28.
13. Крамарєв С.О., Євтушенко В.В. Оцінка ефективності рекомбінантного інтерферону альфа для профілактики та лікування гострих респіраторних вірусних інфекцій у дітей // Здоров’я України. — 2008. — № 18/1. — C. 49-50.
14. Лечение и профилактика острых респираторных инфекций у часто болеющих детей / Знаменская А.А., Фомина В.Л., Учайкин В.Ф. [и др.] // Лечащий врач. — 2011. — № 1.
15. Максимова С.М., Самойленко И.Г., Бухтияров Э.В., Максимова Н.В. Небулайзерная терапия в детской пульмонологии // Здоровье ребенка. — 2010. — № 5 (26). — С. 87-91.
16. Марушко Ю.В., Голубовська Ю.Є., Марушко Є.Ю. Застосування рекомбінантного інфтерферону альфа‑2b у педіатричній практиці // Здоровье ребенка. — 2016. — № 2 (70). — С. 81-86.
17. Няньковський С.Л., Няньковська О.С., Яцула М.С. Клінічні особливості використання інтерферонів при лікувані ГРВІ у дітей // Здоровье ребенка. — 2015. — № 5 (64). — С. 7-12.
18. Образцова Е. В. Препараты интерферона и его индукторы при гриппе и ОРИ у детей / Е.В. Образцова, Л.В. Осидак, Е.Г. Головачева // Детские инфекции. — 2010. — Т. 9, № 1. — С. 35-40.
В. Препараты интерферона и его индукторы при гриппе и ОРИ у детей / Е.В. Образцова, Л.В. Осидак, Е.Г. Головачева // Детские инфекции. — 2010. — Т. 9, № 1. — С. 35-40.
19. Петленко С.В., Романцов М.Г., Шульдякова О.Г., Коваленко А.Л. Снижение респираторной заболеваемости подростков в период неустойчивой эпидемической ситуации по ОРЗ и гриппу // Клинические исследования лекарственных средств: Материалы IV Международной конференции. — М., 2004. — C. 171-172.
20. Подходы к лечению и реабилитации часто и длительно болеющих респираторными заболеваниями детей, проживающих в доме ребенка / Юлиш Е.И., Балычевцева И.В., Висягин В.Б. [и др.] // Здоровье ребенка. — 2010. — № 2 (23). — С. 32-39.
21. Попов В.Ф. Лекарственные формы интерферонов. — М.: Триада-Х, 2002. — 136 с.
22. Романцов М.Г., Шульдякова О.Г., Коваленко А.Л., Ершов Ф.И. Медикаментозная профилактика респираторной заболеваемости в период неустойчивой эпидемической ситуации по гриппу // Фундаментальные исследования. — 2004. — № 4. — С. 14-16.
— 2004. — № 4. — С. 14-16.
23. Таточенко В.К. Острые респираторные заболевания (ОРЗ) у детей — лечение и профилактика // Доктор.Ру. — 2003. — № 12. — С. 12.
24. Шкурупій Д.А., Похилько В.І., Мамонтова Т.В. Інгаляційна корекція вмісту інтерферону-α в новонароджених із синдромом поліорганної недостатності // Клінічна та експериментальна патологія. — 2013. — Т. XII, № 1 (43). — С. 176-179.
25. Шульдякова О.Г. Респираторные инфекции у детей // Лекарственные средства, применяемые при вирусных заболеваниях / Под ред. М.Г. Романцова, Ф.И. Ершова. — М., 2007. — C. 233-277.
26. Юлиш Е.И. Реабилитация часто и длительно болеющих детей при различном течении персистирующих инфекций / Е.И. Юлиш, С.Я. Ярошенко // Вестн. физиотерапии и курортол. — 2010. — Т. 16, № 6. — С. 193.
27. Юлиш Е.И. Противовирусная терапия в лечении острых респираторных заболеваний у детей // Современная педиатрия. — 2013. — № 5 (53). — С. 1-4.
28. Юлиш Е.И. Цитомегаловирусная инфекция у детей. Подходы к лечению при различном течении инфекционного процесса // Здоровье ребенка. — 2015. — № 4 (64). — С. 7-14.
Подходы к лечению при различном течении инфекционного процесса // Здоровье ребенка. — 2015. — № 4 (64). — С. 7-14.
29. Юрцева А.П., Фофанова О.В., Осадець Н.Б., Боднар О.П. Ефективність застосування лаферобіону в дітей із рецидивуючим бронхообструктивним синдромом, які часто хворіють на гострі респіраторні захворювання // Здоровье ребенка. — 2014. — № 5 (56). — С. 81-86.
30. Whitley R.J., Hayden F.G., Reisinger K.S. et al. Oral oseltamivir treatment in children // Ped. Inf. Dis. — 2001. — 2. — 127-133.
Местное применение препаратов рекомбинантного интерферон А-альфа 2 в терапии рецидивирующего респираторного папилломатоза Текст научной статьи по специальности «Клиническая медицина»
Медицинская Иммунология 2006, Т. 8, № 5-6, стр 679-688 © 2006, СПб РО РААКИ
Оригинальные статьи
МЕСТНОЕ ПРИМЕНЕНИЕ ПРЕПАРАТОВ РЕКОМБИНАНТНОГО ИНТЕРФЕРОНА-АЛЬФА2 В ТЕРАПИИ РЕЦИДИВИРУЮЩЕГО РЕСПИРАТОРНОГО ПАПИЛЛОМАТОЗА
* Кафедра оториноларингологии с клиникой, Научно-практический центр стоматологии ** Научно-методический центр по молекулярной медицине СПбГМУ им. акад. И.ЛЛавлова, Санкт-Петербург
акад. И.ЛЛавлова, Санкт-Петербург
Резюме. Рецидивирующий респираторный папилломатоз (РРП) – наиболее часто встречающаяся опухоль верхних дыхательных путей, ассоциированная с вирусом папилломы человека (ВПЧ). Целью работы было выявить особенности системного и местного иммунитета при РРП, оценить клиническую и иммунологическую эффективность местной терапии рекомбинантным интерфероном-альфа (rIFNa2) и определить клинические и лабораторные показания к его назначению.
Под наблюдением находился 41 больной РРП. Обследование включало: гистологическое исследование папиллом, определение ДНК ВПЧ в папилломах методом ПЦР, определение фенотипа циркулирующих в крови лимфоцитов (СЭ3+, СЭ4+, СЭ8+, СЭ25+, ИЬА-ОК+) методом проточной цитофлюориметрии. В ларингеальном секрете определялись уровни №N7, TNFa, GM-CSF, 1Ь-2, 1Ь-4, 1Ь-5, 1Ь-10, 1Ь-12, 1Ь-13 методом мультиплексного иммуноанализа. У всех больных РРП исходно выявлены сниженная функциональная активность Т-лимфоцитов при сохранении их количественных соотношений в пределах нормы и значительно сниженные количества Т-киллеров и естественных киллеров. . В процессе лечения rIFNa2 отмечен рост уровней цитокинов, модулирующих иммунный ответ по ТЬ1-типу (№N7, 1Ь-12, 1Ь-2) и GM-CSF, снижение исходно высокого уровня 1Ь-10, снижение уровней !Ь-4 и 1Ь-13. При частичном регрессе уровни №N7 1Ь-12, 1Ь-2 и GM-CSF снижались по сравнению с ис-
. В процессе лечения rIFNa2 отмечен рост уровней цитокинов, модулирующих иммунный ответ по ТЬ1-типу (№N7, 1Ь-12, 1Ь-2) и GM-CSF, снижение исходно высокого уровня 1Ь-10, снижение уровней !Ь-4 и 1Ь-13. При частичном регрессе уровни №N7 1Ь-12, 1Ь-2 и GM-CSF снижались по сравнению с ис-
Плужников М.С.*, Катинас Е.Б.*% Рябова М.А.*, Карпищенко С.А.*, Сысоев К.А.**, Чухловин А.Б.**, Тотолян Арег А.**
Адрес для переписки:
197022, г.Санкт-Петербург, ул. Л.Толстого, д.6/8. СПб ГМУ им.акад. И.П. Павлова.
Кафедра оториноларингологии с клиникой.
К.м.н. Катинас Елена Борисовна.
E-mail: elena [email protected]
ходными значениями и на протяжении всего курса лечения колебались в пределах нормальных значений, после отмены препарата наблюдался рост уровней 1Ь-4 и 1Ь-13. Таким образом, местная терапия rIFNa2 эффективна при рецидивирующем респираторном папилломатозе с агрессивным течением. В качестве прогностического признака эффективности местной интерфероновой терапии могут служить
Таким образом, местная терапия rIFNa2 эффективна при рецидивирующем респираторном папилломатозе с агрессивным течением. В качестве прогностического признака эффективности местной интерфероновой терапии могут служить
исходно высокие значения TNFa и индекса IL-4/IFNy в ларингеальном секрете, а показателями эффективности лечения – повышение уровня IFNy IL-2 и IL-12 в сочетании со снижением (нормализацией) индекса IL-4/IFNy
Ключевые слова: рецидивирующий папилломатоз, местный иммунитет, иммунотерапия, рекомбинантный интерферон альфа2.
Plouzhnikov M., Katinas E., Ryabova M., Karpishenko S., Syssoev K., Chukhlovin A., Totolian A.
LOCAL APPLICATION OF RECOMBINANT INTERFERON-ALFA2 FOR TREATMENT
OF RECURRENT RESPIRATORY PAPILLOMATOSIS
Abstract. Recurrent respiratory papillomatosis (RRP) is the most frequently occurring tumour of the upper airways associated with a human papilloma virus (HPV). The aim of this study was to reveal some features of systemic and local immunity in RRP, to investigate clinical and immunological efficiency of local treatment with recombinant interferon-a (rIFNa), and to determine clinical and laboratory indications to it’s administration. The study included forty-one patients with confirmed RRP. Their examination included histological examination of papillomas, detection of HPV DNA in papilloma tissues using PCR technique, phenotyping of circulating lymphocytes (CD3+, CD4+, CD8+, CD25+, HLA-DR+) by means of flow cytometry. The levels of IFNy, TNFa, GM-CSF, IL-2, IL-4, IL-5, IL-10, IL-12, IL-13 in laryngeal secretions were quantified by a multiplex immunoassay. In all cases, we revealed an initially decreased functional activity of Т-lymphocytes, as well as low contents of Т-killer and NK-cells. In laryngeal secretions, increased values of Th2-type-specific cytokines (IFNy and TNFa) were found.
Recurrent respiratory papillomatosis (RRP) is the most frequently occurring tumour of the upper airways associated with a human papilloma virus (HPV). The aim of this study was to reveal some features of systemic and local immunity in RRP, to investigate clinical and immunological efficiency of local treatment with recombinant interferon-a (rIFNa), and to determine clinical and laboratory indications to it’s administration. The study included forty-one patients with confirmed RRP. Their examination included histological examination of papillomas, detection of HPV DNA in papilloma tissues using PCR technique, phenotyping of circulating lymphocytes (CD3+, CD4+, CD8+, CD25+, HLA-DR+) by means of flow cytometry. The levels of IFNy, TNFa, GM-CSF, IL-2, IL-4, IL-5, IL-10, IL-12, IL-13 in laryngeal secretions were quantified by a multiplex immunoassay. In all cases, we revealed an initially decreased functional activity of Т-lymphocytes, as well as low contents of Т-killer and NK-cells. In laryngeal secretions, increased values of Th2-type-specific cytokines (IFNy and TNFa) were found. Besides that, high levels of local IL-4 were detected thus being typical to alternative Th3-type response.
Besides that, high levels of local IL-4 were detected thus being typical to alternative Th3-type response.
Single inhalations 1000 000 ME of «Interal» or «Roferon» preparations were administered daily (a total of 1015 millions ME per therapeutic course). Thirteen patients received the treatment after surgery, as an adjuvant therapy, and eleven patients underwent monotherapy. Complete tumor regression of tumors following this monotherapy was observed in 45,5% of the patients, whereas partial regression was registered in 45%. The effect was mostly expressed in frequently recurring juvenile papillomatosis with aggressive course and histological pattern of actively proliferating papilloma. In the patients with complete tumor regression, high initial levels of TNFa and IL-4/IFNr ratios were revealed initially in laryngeal secretions. When rIFN6 was administered, an increase in Th2-type cytokines (IFNy, IL-12, IL-2) and GM-CSF were revealed, as well as decrease of initially high levels of IL-10, like as lowered levels of IL-4 and IL-13. In cases of partial tumor regression, the levels of IFNa, IL-12, IL-2 and GM-CSF were decreased against initial values, and in the course of treatment they fluctuated within normal reference values. Cancellation of the therapy was followed by increase in IL-4 and IL-13 levels.
In cases of partial tumor regression, the levels of IFNa, IL-12, IL-2 and GM-CSF were decreased against initial values, and in the course of treatment they fluctuated within normal reference values. Cancellation of the therapy was followed by increase in IL-4 and IL-13 levels.
Hence, the local rIFNa therapy is effective in controlling aggressive recurrent respiratory papillomatosis. Initial increase in TNFa and IL-4/IFNy ratios in laryngeal secretions may be considered as favorable predictor of anticipated therapy, whereas increased levels of IFNa, IL-2 and IL-12 together with decrease (normalization) of IL-4/IFNy ratio may reflect the efficiency of the treatment performed. (Med. Immunol., 2006, vol.8, № 5-6, pp 679-688)
Введение В этиопатогенезе заболевания основное зна-
Рецидивирующий респираторный папилломатоз чение имеет инфицирование вирусом папилло-
(РРП) – наиболее часто встречающаяся опухоль мы человека (ВПЧ). Основной причиной инте-
Основной причиной инте-
верхних дыхательных путей. По данным разных ав- реса к ВПЧ является его онкогенный потенциал,
торов, гортанные папилломы составляют от 15,9 до проявляющийся как в клинических наблюдени-
57,5% от всех доброкачественных образований гор- ях малигнизации респираторных папиллом [13,
тани [2]. Папиллома является доброкачественной 14, 15] так и в частом обнаружении ДНК ВПЧ в
опухолью, развивающейся из плоского или переход- плоскоклеточных карциномах головы и шеи [16].
ного эпителия. В связи с частым рецидивировани- Частота озлокачествления респираторных папил-
ем, бурным ростом и анатомической узостью про- лом, по данным разных авторов, составляет 2-3%
света гортани, растущая опухоль приводит к нару- [10].
шению голосообразовательной, а в последующем, Рецидивирование папиллом связывают с нали-при сужении ее просвета, и дыхательной функции чием латентной инфекции в морфологически здо-
органа. Выделяемые клинически, ювенильная и ровой ткани рядом с папилломами, что подтверж-
взрослая формы заболевания гистологически иден- дено обнаружением ВПЧ в неизмененном эпителии
тичны (фиброэпителиальная опухоль), однако су- [6]. Вирус длительно может существовать латент-
щественно различаются по клиническому течению: но не вызывая роста папиллом, а активизация пропри ювенильном папилломатозе отмечается высо- цесса может быть спровоцированаугнетением им-
кая степень рецидивирования и чаще встречаются мунной системы вследствие любой другой причи-
распространенные формы, а у взрослых есть риск ны: интеркуррентное заболевание, травма, инфек-
малигнизации папиллом. ция и т.д.
ция и т.д.
Подобный взгляд на патогенез РРП, а также отсутствие этиотропного лечения данного заболевания диктует основные положения тактики ведения таких больных, включающие: тщательное, часто неоднократное, удаление папиллом; гистологическое исследование удалённых папиллом на предмет возможной их малигнизации; адъювантную медикаментозную терапию с целью увеличения сроков ремиссии.
В качестве противорецидивной терапии наиболее широко используются цитостатики и препараты рекомбинантного интерферона-альфа [9, 11, 12]. Известны противорецидивные способы лечения РРП следующими препаратами интерферонов: человеческим лейкоцитарным интерфероном, эгифе-роном, реафероном, реальдироном, вифероном, ро-фероном-А, интроном-А и др. В целом, по данным различных авторов, эффективность интерфероноте-рапии составляет от 20 до 71,7%.
Системное применение препаратов интерферона имеет определенные особенности. Необходим длительный непрерывный курс лечения – до 6-12 месяцев; используются преимущественно парентеральные методы введения. Длительно вводимый больному экзогенный IFN в ряде случаев вызывает образование нейтрализующих антител.
Необходим длительный непрерывный курс лечения – до 6-12 месяцев; используются преимущественно парентеральные методы введения. Длительно вводимый больному экзогенный IFN в ряде случаев вызывает образование нейтрализующих антител.
Известны также токсические и побочные реакции на введение интерферона. Практически всегда возникает лихорадка с ознобом или без него, которая ослабевает в течение 3-5 дней. В течение первых 4 недель лечения возникает гранулоцитопения, которая иногда бывает настолько выраженной, что приходится прерывать лечение. Наконец, при длительном введении IFN могут наблюдаться изменения со стороны биохимических печеночных проб, а у некоторых больных отмечены такие симптомы, как головная боль, сухость во рту, выпадение волос, сенсорная нейропатия.
Учитывая вышеперечисленные сложности системного применения интерферонов, при лечении ограниченной локализации ВПЧ в слизистой оболочке гортани представляется оправданным использовать локальное введение препаратов интерферо-нов в виде аппликаций на слизистую оболочку, ингаляций [4], инъекций в слизистую оболочку непосредственно после удаления папиллом. Интерес представляет тот факт, что иммуномодулирующий эффект препаратов интерферона может зависеть от способа их введения [5]. Ранее нами было показано, что местное введение цитокинов, в ряде случаев, значительно эффективнее системного, так как по-
Интерес представляет тот факт, что иммуномодулирующий эффект препаратов интерферона может зависеть от способа их введения [5]. Ранее нами было показано, что местное введение цитокинов, в ряде случаев, значительно эффективнее системного, так как по-
зволяет добиться активации органоспецифических субпопуляций эффекторных клеток иммунной системы с минимальным расходом препарата и риском развития побочных эффектов [3].
Целью данной работы было выявить особенности состояния системного и местного иммунитета пациентов с рецидивирующим респираторным па-пилломатозом, оценить клиническую и иммунологическую эффективность местной терапии rIFNa2 и определить клинические и лабораторные показания к проведению местной интерфероновой терапии при рецидивирующем респираторном па-пилломатозе.
Материалы и методы
За период с 2003 по 2006 год в ЛОР клинике СПбГМУ им. акад. И.П. Павлова под наблюдением находился 41 больной часто рецидивирующим па-пилломатозом гортани в возрасте от 16 до 69 лет. Из них 26 (63,4%) мужчин и 15 (36,6%) женщины.
акад. И.П. Павлова под наблюдением находился 41 больной часто рецидивирующим па-пилломатозом гортани в возрасте от 16 до 69 лет. Из них 26 (63,4%) мужчин и 15 (36,6%) женщины.
Наиболее часто начало заболевания приходилось на ранний детский возраст (26,8%) и период полового созревания (14,6%) – ювенильный папилломатоз. В 31,9 % дебют заболевания приходился на 4050-летний возраст – папилломатоз взрослых. Такое возрастное распределение начала заболевания подтверждается данными других авторов и возможно связано с периодами конституционального иммунодефицита и гормональных перестроек в организме.
Клиническое обследование больных включало: трансназальную фиброларингоскопию с видеозаписью и покадровым воспроизведением; исследование функции внешнего дыхания у больных с большим объемом папиллом (пневмоанализатор «РИД-123»), компьютерный анализ голоса (программное обеспечение «Sound Forge 4. 5» и «Praat» спектральный анализ, сонограмма).
5» и «Praat» спектральный анализ, сонограмма).
Распространённость заболевания оценивалась по классификации И.А. Вознесенской (1968) [1], согласно которой различают ограниченную (процесс поражает одну анатомическую область гортани) и распространённую формы папилломатоза (табл.1).
Наиболее часто папилломы локализовались на истинных голосовых складках (68,9%), преимущественно в передних отделах. Среди больных с распространенной формой папилломатоза преобладали пациенты с длительным анамнезом, неоднократно перенесшие оперативные вмешательства.
Табл.1. ХАРАКТЕРИСТИКА РАСПРОСТРАНЁННОСТИ ПРОЦЕССА В ЗАВИСИМОСТИ ОТ ФОРМЫ ЗАБОЛЕВАНИЯ
Распространенность Абсолютное количество Относительное количество больных
процесса больных (%)
Ограниченный 10 24,4 %
Распространённый 31 75,6 %
Среди пациентов с распространенной формой папилломатоза у 6 больных наблюдалось сочетание папилломатоза гортани и глотки (мягкое небо, небные миндалины), у 3 больных диагностировано сочетание папилломатоза гортани, глотки и трахеи.
У 2 больных заболевание было диагностировано впервые, остальные 39 человек, перенесли до поступления в клинику от 1 до 20 операций при помощи традиционных хирургических методик под местной или общей анестезией. Длительность межре-цидивного периода составила от 3 до 6 месяцев.
Гистологическое исследование биоптатов и удаленных папиллом проводилось при окрашивании препаратов по Папаниколау.
Определение ДНК ВПЧ в удалённых папилломах или браш-биоптатах со слизистой оболочки и её типирование производилось методом полимеразной цепной реакции.
Иммунологическое обследование, включающее определение фагоцитирующей активности нейтро-филов, функциональной активности клеток методом реакции торможения миграции лейкоцитов (РТМЛ), фенотипа циркулирующих в крови лимфоцитов (CD3+, CD4+, CD8+, CD25+, HLA-DR+) методом проточной цитофлюориметрии проводилось 35 больным рецидивирующим респираторным па-пилломатозом до начала лечения.
Определение в ларингеальном секрете уровня IFNy, TNFa, GM-CSF, IL-2, IL-4, IL-5, IL-10, IL-12, IL-13 методом мультиплексного иммуноанализа с помощью анализатора белков «Bio-Plex» (Bio-Rad, США) проводилось 11 больным, получавшим ингаляции «Роферона» («Ф.Хоф-фманн-Ля Рош Лтд.», Швейцария) в качестве монотерапии 5 раз: до лечения, через сутки и через пять суток после начала терапии, после окончания курса ингаляций и через 5 дней после курса лечения (исследование выполнено при финансовой поддержке в форме гранта Правительства Санкт-Петербурга).
Для определения значений нормы изучаемых цитокинов в ларингеальном секрете была обследована контрольная группа, которую составили практически здоровые лица молодого возраста (n=6, 1830 лет), студенты 4 и 5 курсов СПбГМУ им. акад. И.П.Павлова. Критериями отбора в контрольную группу служили: отсутствие хронических соматических заболеваний и патологии ЛОР-органов, отсутствие аллергических реакций в анамнезе, а также отсутствие вредных привычек (курение, злоупотребление алкоголем). . Оценка достоверности различия полученных результатов проводилась вычислением непараметрического критерия Манна-Уитни. Различие считалось достоверным при р<0,05.
. Оценка достоверности различия полученных результатов проводилась вычислением непараметрического критерия Манна-Уитни. Различие считалось достоверным при р<0,05.
Методика лечения
В исследовании использовались препараты rINFa2: «Интераль» (ГосНИИОЧБ, Россия, регистрационный № 000697/01-2001) и «Роферон» («Ф.Хоффманн-Ля Рош Лтд.», Швейцария, регистрационный №014755/01 – 2001).
С противорецидивной целью в раннем послеоперационном периоде (на 2-3 сутки после операции) ингаляционная терапия rINFa2 проводилась 13 пациентам с рецидивирующим респираторным папил-ломатозом.
Ингаляции 1 млн. ЕД препарата «Интераль» или «Роферон», растворенного в 5 мл физиологического раствора проводились 1 раз в день с помощью компрессионного ингалятора «Бореал»(«Флаем Нуова», Италия) (размер частиц при ингаляции 0,6-
0,8 микрон). Курсовая доза составляла 10-15 млн. ЕД препарата.
Курсовая доза составляла 10-15 млн. ЕД препарата.
В качестве монотерапии без оперативного лечения курс ингаляций rINFa2 проведен 11 пациентам с рецидивирующим респираторным папилломато-зом. Эти больные получали ингаляции 1 млн. ЕД препарата «Роферон», растворенного в 5 мл физиологического раствора,1 раз в день с помощью компрессионного ингалятора «Бореал». Курсовая доза составляла 10-15 млн. ЕД препарата.
Результаты
Результаты вирусологического и гистологического обследования
При исследовании 24 препаратов удалённых папиллом и браш-биоптатов методом полимеразной цепной реакции ВПЧ 6/11 типов обнаружен в 10 случаях, 16/18 типов – 5 случаях, 6/8 типы – в 4 случаях, неидентифицированный ВПЧ в одном и ещё в четырех случаях ДНК ВПЧ обнаружено не было при гистологически подтверждённом диагнозе. При анализе данных вирусологического исследования нам не удалось провести какие-либо параллели между результатами этих исследований, клиническим течением заболевания и состоянием иммунной системы пациентов.
При анализе данных вирусологического исследования нам не удалось провести какие-либо параллели между результатами этих исследований, клиническим течением заболевания и состоянием иммунной системы пациентов.
При изучении препаратов, окрашенных по Па-паниколау, определена пролиферирующая плоскоклеточная папиллома с наличием специфического комплекса признаков, характеризующих ядро и ци-
топлазму эпителиальных клеток, обусловленных цитопатическим действием ВПЧ у всех пациентов (койлоцитарная атипия клеток). Необходимо отметить, что у больных с ювенильным папилломатозом опухоль характеризовалась как высоко пролиферирующая плоскоклеточная папиллома с наличием резко расширенных и полнокровных капилляров в строме. При папилломатозе взрослых в 12 (29,3%) случаев обнаружена плоскоклеточная папиллома с участками гиперкератоза, дисплазии 1-2 степени и низкой пролиферативной активностью.
Результаты иммунологического обследования
У всех больных РРП показатели поглотительной активности нейтрофилов, а также спонтанной миграции гранулоцитов и мононуклеаров в РТМЛ не отличались от нормальных значений.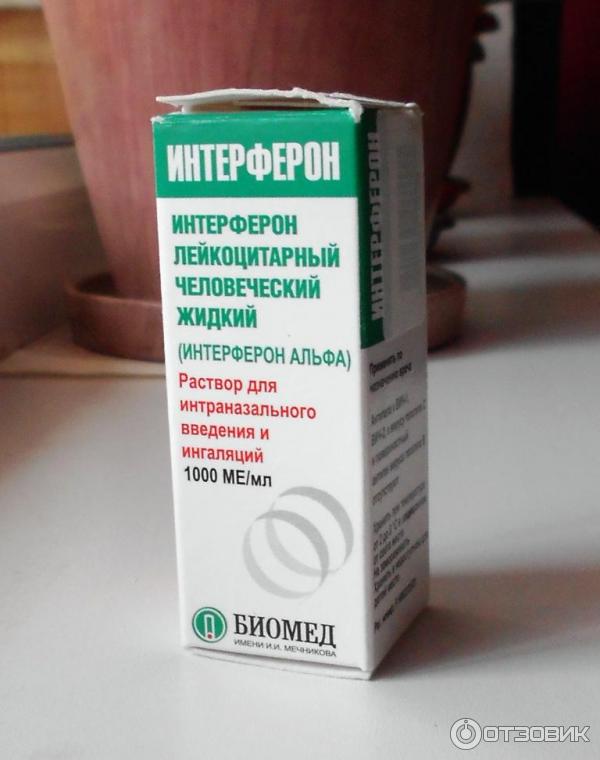
Отклонения от нормы при определении фенотипа циркулирующих в крови лимфоцитов были выявлены у 35 пациентов (85,4%). Необходимо отметить, что все эти больные характеризовались длительным и часто рецидивирующим течением патологического процесса. При анализе полученных данных не выявлено тенденции к уменьшению количества Т-лимфоцитов (СВ3+СВ19-), Т-хелперов (СВ4+СВ8-) и Т-цитотоксических лимфоцитов (СВ4-СЭ8+). Однако содержание Т-лимфоцитов, положительных по СЭ25 – «раннему маркеру активации» было значительно снижено (6,5±2,3% при норме 13-24% (р=0,042). У всех пациентов определялось достоверно сниженное количество активированных Т-лимфоцитов (СВ3+НЬА-ЭК+) – положительных по «позднему маркеру активации» (2,55±3,9% при норме 8-20 %, р=0,012).
Кроме того, отмечено значительно сниженное количество Т-киллеров (СЭ3+(16+56)+) (р=0,023) и естественных киллеров (СЭ3-(16+56)+) (р=0,035) по сравнению с нормой. -10 в ларингеальном секрете больных с ювенильной и взрослой формами респираторного па-пилломатоза (* – различия между группами больных достоверны при р<0,05, ** – различия по сравнению с нормой достоверны при р<0,05).
-10 в ларингеальном секрете больных с ювенильной и взрослой формами респираторного па-пилломатоза (* – различия между группами больных достоверны при р<0,05, ** – различия по сравнению с нормой достоверны при р<0,05).
Исходно в ларингеальном секрете у 24 обследованных больных с РРП выявлено достоверно повышенные уровни ТОТа (р=0,036) и №N7 (р=0,031) по сравнению с группой контроля. Аналогичные изменения были выявлены для 1Ь-4 (р=0,044). Средние значения уровней цитокинов в ларингеальном секрете представлены в табл. 2.
Среднее значение концентрации 1Ь-2 имело тенденцию к снижению по сравнению с группой контроля, однако отличие было статистически не достоверно. Концентрации 1Ь-5 и 1Ь-10 были близки к нулю. Отличие уровней других цитокинов от контрольной группы статистически доказаны не были.
Уровни TNFa и 1Ь-10 в группе больных с ювенильной формой папилломатоза значительно превышали таковые в ларингеальном секрете пациентов с папилломатозом взрослых и в контрольной группе (рис.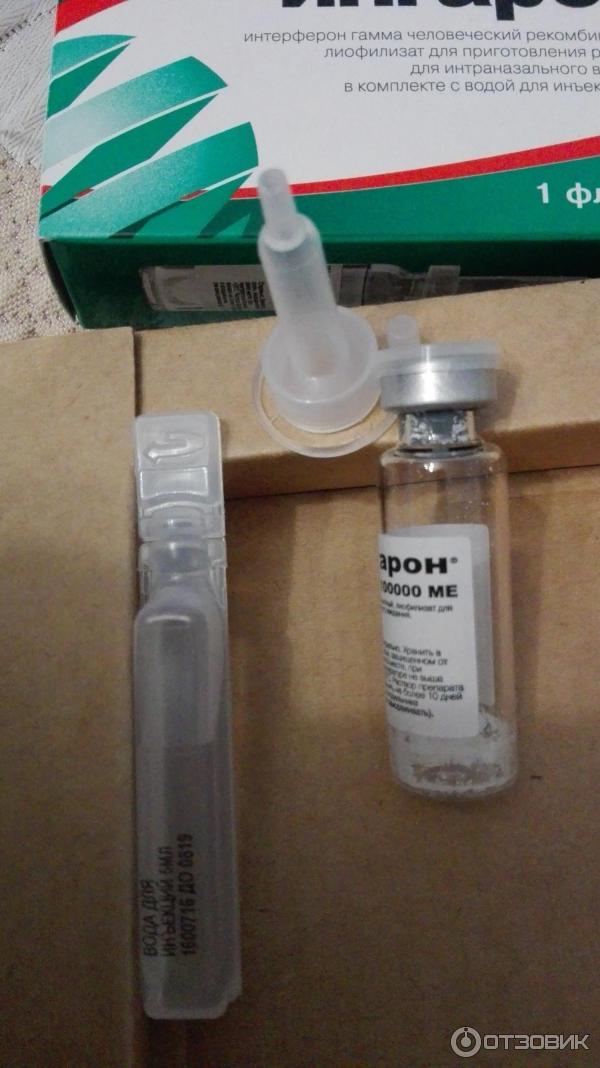 а 26,22±71,02 * 0,053±0,28
а 26,22±71,02 * 0,053±0,28
11,61±23,78 * 0,81 ±1,9
GM-CSF 50,33±90,9 9,5±8,33
!1_-2 3,42±3,97 4,5±3,2
!1_-4 4,03±6,6 * 0±0
!1_-5 0,001 ±0,004 0±0
!1_-10 0,0008±0,023 0±0
!1_-12 3,33±8,9 0,11 ±0,19
!1_-13 5,02±14,53 0,45±0,77
* – различия по сравнению со здоровыми лицами достоверны при р<0,05
7(29,2%) пациентов наблюдался «гриппоподобный» синдром, включающий субфебрильную температуру тела, умеренную головную и мышечную боль. Проявления гриппоподобного синдрома длились от 2 до 5 часов, были выражены незначительно и не требовали медикаментозной коррекции. У всех больных в первые 2-3 суток наблюдалась гиперемия и отечность слизистой оболочки гортани и глотки.
У всех больных в первые 2-3 суток наблюдалась гиперемия и отечность слизистой оболочки гортани и глотки.
В группе больных, получавших ингаляции интерферона с противорецидивной целью после оперативного удаления папиллом (13 человек), при дальнейшем наблюдении у 7 (53,8%) пациентов в течение 46 месяцев (в среднем через 4,9 месяцев) появились первые признаки рецидива роста папиллом: стелющиеся мелкозернистые папилломы в прежнем месте или продолженный рост. Необходимо отметить, что при наблюдении за данными больными до назначения терапии интерфероном средняя продолжительность межрецидивного периода составляла 3,8 месяца. Однако при проведении статистической обработки полученных результатов достоверного увеличения межрецидивного периода не наблюдалось (р= 0,12). Данным больным (7 человек) снова начинали курс ингаляционной терапии интерфероном, на фоне которого у 2 пациентов был отмечен существенный регресс папиллом с улучшением или восстановлением голосовой функции, у 6 пациентов – полное их исчезновение. У остальных 6 пациентов (47,2%) рецидива заболевания не отмечено. Период динамического наблюдения составил от 9 до 16 месяцев.
У остальных 6 пациентов (47,2%) рецидива заболевания не отмечено. Период динамического наблюдения составил от 9 до 16 месяцев.
В группе больных, получавших курс ингаляций рекомбинантного интерферона-а2 в качестве монотерапии без предварительного хирургического удаления папиллом (11 человек), у 5 (45,5%) пациентов был достигнут полный регресс папиллом и восстановление голосовой и дыхательной функции, у 5 (45,5%) наблюдалось значительное уменьшение объема папиллом с полным восстановлением дыхательной и значительным улучшением голосовой функции. После проведения курса ингаляций больные не требовали оперативного лечения. У 1 пациентки динамики не наблюда-
□ Частичный регресс ■ Полный регресс ■ Норма
Рис.2. Исходные уровни TNFa в ларингеальном секрете больных РРП в зависимости от результата лечения и здоровых лиц.(* – различия между группами больных достоверны при р<0,05). “Норма
“Норма
ОМ-СЭР
до через через 5 после через 5
лечения сутки суток курса суток
после
курса
1Ь2
1Ь-4
до
лечения
через
сутки
1Ь5
через 5 суток
после
курса
через 5 суток после курса
до через через 5 после через 5
лечения сутки суток курса суток
после
курса
1Ы2
лечения
курса
суток
после
курса
до
лечения
через
сутки
через 5 суток
после
курса
через 5 суток после
1Ы0
до
лечения
через
сутки
через 5 суток
1Ы3
после
курса
через 5 суток после курса
Рис. 3. Динамика уровней цитокинов в ларингеальном секрете (пкг/мл) больных РРП с частичным и полным регрессом папиллом в результате лечения (* – различия с исходными значениями достоверны при р<0,05 , • – различия с нормой достоверны при р<0,05).
3. Динамика уровней цитокинов в ларингеальном секрете (пкг/мл) больных РРП с частичным и полным регрессом папиллом в результате лечения (* – различия с исходными значениями достоверны при р<0,05 , • – различия с нормой достоверны при р<0,05).
до
лечения
через
сутки
через 5 суток
после
курса
через 5 суток после курса
■Частичный регресс ■ Полный регресс • Норма____________
лось, ей в дальнейшем было проведено оперативное вмешательство.
При анализе субпопуляций лимфоцитов в периферической крови после проведения местной терапии рекомбинантным интерфероном была отмечена тенденция к нормализации количества естественных киллеров (СЭ3-(16+56)+) и лимфоцитов, положительных по СЭ25, однако выявленные изменения были статистически недостоверны.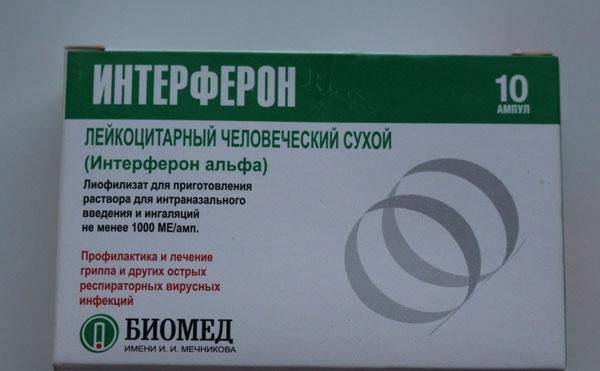
При анализе динамики уровней цитокинов в ларингеальном секрете больных РРП в процессе монотерапии интерфероном-а2 были выявлены следующие закономерности. В группе больных с полным регрессом опухоли в результате лечения выявлялись более высокие исходные уровни Т№а, чем у больных с частичным регрессом новообразования (р=0,017) (рис.2).
Динамика уровней цитокинов в ларингеальном секрете больных РРП в процессе терапии представлена на рисунке 3.
В группе больных с полным регрессом папиллом уже через сутки после начала лечения наблюдалось постепенное увеличение в ларингеальном секрете уровней 1БКу, 1Ь-12, 1Ь-2 по сравнению с исходными значениями. Максимальные значения уровней данных цитокинов достигались к пятому дню лечения, при статистической обработке наблюдались достоверные отличия от исходных показателей (р=0,023 для №N7, р=0,02 для 1Ь-12 и р=0,015 для 1Ь-2). Тенденция к росту сохранялась и через 5 суток после окончания курса лечения. Для GM-CSF отмечена та же динамика, однако изменения были статистически не достоверны. В группе больных с частичным регрессом опухоли уровни №N7, 1Ь-12, 1Ь-2 и GM-CSF через сутки снижались по сравнению с исходными значениями и на протяжении всего курса лечения колебались в пределах нормальных значений. При статистическом анализе достоверных изменений уровней данных цитокинов не наблюдалось.
Тенденция к росту сохранялась и через 5 суток после окончания курса лечения. Для GM-CSF отмечена та же динамика, однако изменения были статистически не достоверны. В группе больных с частичным регрессом опухоли уровни №N7, 1Ь-12, 1Ь-2 и GM-CSF через сутки снижались по сравнению с исходными значениями и на протяжении всего курса лечения колебались в пределах нормальных значений. При статистическом анализе достоверных изменений уровней данных цитокинов не наблюдалось.
У пациентов с полным регрессом папиллом через сутки после начала лечения выявлено достоверное снижение исходно повышенных уровней TNFa (р=0,045) до нормальных значений. В дальнейшем значения концентраций данного цитокина не отличались от нормы. В группе с частичным регрессом папиллом достоверных изменений уровня TNFa в процессе терапии не выявлено.
При анализе динамики 1Ь-4, 1Ь-10 и 1Ь-13 в обеих группах больных через сутки после начала лечения выявлено постепенное снижение уровней этих цитокинов.
До лечения В ходе лечения После отмены
Пациенты с полным регрессом папиллом
1 1,46 0 0
2 0 2,5 1,2
3 60 0 0
4 43 0 0
5 0 0 0
М±а 20,89±28,62 0,5±1,1 0,24±0,53
Пациенты с частичным регрессом папиллом
1 0,26 90 0
2 2,4 0 0
3 0 45 6,25
4 0 4 10
5 4,7 0 20
М±а 1,47±2,07 27,8±39,6 7,25±8,31
* – различия между группами больных достоверны при р<0,05, ** – различия по сравнению с нормой достоверны при р<0,05.
интенсивностью роста папиллом, зависит не столько от типа вируса, сколько от особенностей макроорганизма. В нашем исследовании у всех пациентов выявлен дефект иммунной системы, заключающийся в сниженной функциональной активности Т-лим-фоцитов при сохранении их количественных соотношений в пределах нормы. Кроме того, отмечены значительно сниженные количества Т-киллеров и естественных киллеров, которые являются основными эффекторами специфического и неспецифического звеньев противовирусной защиты соответственно. На местном уровне выявлен дисбаланс Th2/Th3 иммунных реакций. В ларингеальном секрете больных РРП обнаружены высокие уровни цитокинов, модулирующих ответ по Thl-типу (IFNy и TNFa) характерный для противовирусной иммунной защиты. Кроме того, выявлен высокий уровень IL-4, характерный для развития оппозиторного Th3-ответа. Неоднозначность местных иммунных реакций подтверждается сниженным или нормальным уровнем IL-2 и IL-12, повышение которых можно ожидать при развитии противовирусного иммунного ответа.
Учитывая изложенные выше изменения в иммунной системе больных РРП, а также наличие хорошо развитой системы местного иммунитета верхних дыхательных путей, представлялось целесообразным использовать при данной патологии локальное введение препаратов интерферонов. Так, Brandtzaeg P. и соавторы сообщают в своих исследованиях, что Т-лимфоциты выявляются в lamina propria слизистой оболочки верхних дыхательных путей как единично расположенные клетки или в виде небольших скоплений, расположенных в под-эпителиальной области, а также в эпителиальном слое между клетками эпителия, так называемые «ин-траэпителиальные лимфоциты». Применение имму-ногистохимического метода с использованием меченых моноклональных антител к различным мембранным молекулам, экспрессируемым лимфоцитами, позволило отнести их к клеткам CD3+ фенотипа и выделить среди них две основные субпопуляции: CD4+ и CD8+ Т-клетки. Небольшая часть «ин-траэпителиальных лимфоцитов» (IEL) имеет фенотип CD57+, присущий натуральным киллерам. Количественные соотношения и локализация клеток основных иммунорегуляторных субпопуляций в слизистой оболочке полости носа, по данным P.Brandtzaeg и соавторов (1996), подвержены значительным индивидуальным колебаниям [7]. Тем не менее, общей тенденцией является относительно низкое содержание Т-клеток CD8+ фенотипа среди IEL (30%) и значительное преобладание CD4+ (65%) в эпителиальном слое и lamina propria слизистой оболочки верхних дыхательных путей. Явное преобладание Т-хелперной субпопуляции клеток с фенотипом CD4+ резко отличает слизистую оболочку
Количественные соотношения и локализация клеток основных иммунорегуляторных субпопуляций в слизистой оболочке полости носа, по данным P.Brandtzaeg и соавторов (1996), подвержены значительным индивидуальным колебаниям [7]. Тем не менее, общей тенденцией является относительно низкое содержание Т-клеток CD8+ фенотипа среди IEL (30%) и значительное преобладание CD4+ (65%) в эпителиальном слое и lamina propria слизистой оболочки верхних дыхательных путей. Явное преобладание Т-хелперной субпопуляции клеток с фенотипом CD4+ резко отличает слизистую оболочку
дыхательных путей от слизистой оболочки интестинального тракта, где Т-клетки СЭ8+ фенотипа составляют подавляющее большинство 1ЕЬ [8].
В ходе местного применения rIFNa2 отмечена тенденция к росту уровней цитокинов, модулирующих иммунный ответ по ТЬ1-типу (1БКу, И.-12, 1Ь-2), максимум которых достигался к 5 суткам. Это, вероятно, связано с действием rIFNa2 на «интраэпители-альные лимфоциты» слизистой оболочки (естественные киллеры и Т-лимфоциты), а также макрофаги, их активацией и секрецией этими клетками 1БКу, 1Ь-2 и И. -12. Рост уровней 1БКу, 1Ь-2 и И.-12 и нормализация индекса 1Ь-4/1БКу в ходе лечения наблюдались только у пациентов с полным регрессом опухоли, что может свидетельствовать о том, что регресс опухоли достигается не только вследствие прямого действия rIFNa2 на репликацию ВПЧ, но и в результате иммуномодулирующего действия данного препарата, потенцирующего противовирусный иммунный ответ на местном уровне. У этой группы больных в ходе терапии также наблюдалось снижение исходно высокого уровня 1Ь-10, противовоспалительного цитокина, характерного для развития опозитор-ного гуморального иммунного ответа по ТЬ2-типу, что еще раз подтверждает сдвиг местных иммунных реакций в результате действия препаратов rIFNa2 в сторону клеточно-опосредованных. Ингаляционное введение rIFNa2 вызывало также незначительное снижение уровней других противовоспалительных цитокинов И.-4 и !Ь-13. Однако после отмены препаратов интерферона в ларингеальном секрете пациентов с частичным регрессом опухоли наблюдался рост уровней этих цитокинов.
-12. Рост уровней 1БКу, 1Ь-2 и И.-12 и нормализация индекса 1Ь-4/1БКу в ходе лечения наблюдались только у пациентов с полным регрессом опухоли, что может свидетельствовать о том, что регресс опухоли достигается не только вследствие прямого действия rIFNa2 на репликацию ВПЧ, но и в результате иммуномодулирующего действия данного препарата, потенцирующего противовирусный иммунный ответ на местном уровне. У этой группы больных в ходе терапии также наблюдалось снижение исходно высокого уровня 1Ь-10, противовоспалительного цитокина, характерного для развития опозитор-ного гуморального иммунного ответа по ТЬ2-типу, что еще раз подтверждает сдвиг местных иммунных реакций в результате действия препаратов rIFNa2 в сторону клеточно-опосредованных. Ингаляционное введение rIFNa2 вызывало также незначительное снижение уровней других противовоспалительных цитокинов И.-4 и !Ь-13. Однако после отмены препаратов интерферона в ларингеальном секрете пациентов с частичным регрессом опухоли наблюдался рост уровней этих цитокинов.
В данном исследовании нами показана эффективность местного ингаляционного применения препаратов рекомбинантного интерферона у пациентов с рецидивирующим папилломатозом гортани в качестве монотерапии (эффективность данного способа лечения составила 45,5%, при полном регрессе опухоли). Интерес представляет следующее наблюдение: при анализе результатов клинического и гистологического исследования выраженный эффект от местного применения интерферона наблюдался у пациентов с часто рецидивирующими ювенильными папилломами, агрессивным течением и гистологической картиной активно пролиферирующей папилломы с наличием расширенных и полнокровных капилляров в строме. Эти характеристики патологического процесса могут служить клиническими показаниями к ингаляционному назначению препаратов рекомбинантного интерферона. Данное наблюдение возможно объясняется механизмом действия интерферона (выраженным ан-типролиферативным действием, основанным на блокировании репликации вируса).
В качестве прогностического признака эффективности местной интерфероновой терапии могут
служить исходно высокие значения TNFa и индекса IL-4/IFNy в ларингеальном секрете, а показателями эффективности лечения – повышение уровня IFNy, IL-2 и IL-12 в сочетании со снижением (нормализацией) индекса IL-4/IFNy.
По нашему мнению, регресс быстрорастущих папиллом на фоне ингаляционной терапии интерфероном позволяет в некоторых случаях проводить консервативное лечение вместо хирургического. Сократить количество оперативных вмешательств, проводя курсы ингаляционной терапии при первых признаках рецидива с хорошим функциональным эффектом, а также сократить объем опухоли, уменьшив при этом объем оперативного вмешательства и вероятность послеоперационных осложнений (кровотечение, рубцевание). Отказ от хирургического метода лечения снижает риск иммунодепрессивных состояний, вызванных самим оперативным вмешательством, что само по себе удлиняет период клинической ремиссии.
Назначение ингаляционной интерфероновой терапии в послеоперационном периоде позволяет удлинить межрецидивный период и сократить вероятность возникновения продолженного роста папилломы.
Благодарности
Исследования были поддержаны грантом для молодых кандидатов медицинских наук вузов и академических институтов Комитета по науке и высшей школе Правительства Санкт-Петербурга (PD 06-4.0-13)
Список литературы
1. Вознесенская И.А. Папилломы верхних дыхательных путей / Л: Медгиз, 1974. – C.63-91.
2. Иванченко Г.Ф., Каримова Ф.С. Профилактика и лечение папилломатоза гортани / Заболевания голосового аппарата верхних дыхательных путей. -2001. – C.111-113.
3. Плужников М.С, Лавренова Г.В., Катинас Е.Б., Галкина О.В., Тотолян А.А. Эффективность местной иммунотерапии гнойных синуситов с использованием препаратов рекомбинантных интерлейкинов человека // Российская Ринология. – 2002. – №2.
Плужников М.С, Лавренова Г.В., Катинас Е.Б., Галкина О.В., Тотолян А.А. Эффективность местной иммунотерапии гнойных синуситов с использованием препаратов рекомбинантных интерлейкинов человека // Российская Ринология. – 2002. – №2.
– С.119-122.
4. Плужников М.С., Рябова М.А., Карпищенко С.А., Катинас Е.Б., Марфичева Н.А., Зуева Е.Е., Чух-ловин А.Б., Тотолян А.А. К вопросу о комбиниро-
ванном лечении рецидивирующего папилломатоза гортани // Болезни органов дыхания. – 2004. – №1. -C. 22-25.
5. Ющук Н.Д., Змызгова А.В., Тугутова И.В., Онуфриева Е.К., Прицкер А.Д. Иммуномодулирующие свойства лейкинферона // Сов. медицина.-1990. – №7. – С.11-14.
6. Bomholt A. Juvenile laryngeal papillomatosis. An epidemiological study from the Copenhagen region. // Acta otolaryngol. – 1988; Vol.5. – №3. -P. 367-371.
// Acta otolaryngol. – 1988; Vol.5. – №3. -P. 367-371.
7. Brandtzaeg P., Jahnsen F.L., Farstad I.N., Harald-sen G. Immunobiology and immunopathology of the upper airway mucosa // Folia Otorhinolaryngologiae et Pathologiae Respiratorae. – 1996. – Vol.2. – №1-2. -P.22-31.
8. Brandtzaeg P., Inger N. Farstad Regional specialization in the mucosal immune system: primed cells do not always home along the same track // Immunology Today. – 1999. – 20. – P.267-277.
9. Deunas L., Alcantud V., Alvares F. Use of inter-feron-a in laryngeal papillomatosis: eight years of the Cuban national programme // J. Laryngol 1997. -Vol.111. – № 2. – P.134-140.
10. Gaylis B., Hayden R.E. recurrent respiratory papillomatosis: progression to invasion and malignan-sy // Amer.J.Otolaryngol. – 1991. – Vol. 12. – №2. -P.104-112.
12. – №2. -P.104-112.
11. Kashima H.K, Leventhal B.G., Week P.W. Randomized surgical adjuvant trial of interferon alfa-nl in recurrent papillomatosis. // Arch. Otolaryngol. Head. Neck. Surg. – 1993. -Vol.114. – №2 – P.1163-1169.
12. Leventhal B.G., Kashima H.K. Randomized surgical adjuvant trial of interferon alfa-1 in recurrent papillomatosis // Arch. Otolaryngol. Head Neck surg.-1988. -Vol.114. – №10. – P.1163-1169.
13. Mahnke C., Frohlich O., Lippert B. Reccurent laryngeal papillomatosis: retrospective analysis of 95 patients and review of the literature // Otolaryngol.Pol.
– 1996. – Vol.50. – №6. -P. 567-578.
14. Ocphanidou D, Dimakou K., Latsi P. Recurrent respiratory papillomatosis with malignant transformation in a young adult // Resp. Med. – 1996. – Vol.90. -№1. – P. 53-55.
Med. – 1996. – Vol.90. -№1. – P. 53-55.
15. Shamboul K. Stomal malignant transformation of respiratory papilloma, with neck metastasis: case report // East. Afr. Med. J. -1996. -Vol.73. – №5. – P.336-338.
16. Steinberg B.M., DilorenzoT.R. A possible role for human papilloma viruses in head and neck cancer // Cancer metastasis Rev. – 1996. – Vol.5. – №1. – P.91-112.
поступила в редакцию 16.04.2006 принята к печати 21.06.2006
Ингаляции с интерфероном для детей
Чем полезен интерферон при простуде? Он повышает защитные свойства организма, обеспечивая высокую сопротивляемость к инфекциям. Ингаляции с интерфероном завоевали широкую популярность у пациентов с симптомами простуды как безопасное и действенное средство освобождения от болезни. Рассмотрим вопрос о правильном применении ингаляционного средства и дозировке препарата.
Действие интерферона
Лечение простудных заболеваний медикаментами постепенно снижает иммунитет, лишая организм природной защиты. Об этом уже давно говорят ведущие врачи мира, указывая на пользу активации иммунитета вместо его угнетения. ОРВИ и простуды — частое заболевание у людей, особенно от него страдают дети.
Постоянный прием антибиотиков и иных химических препаратов атрофирует иммунную систему, лишая ее силы. Это можно сравнить с уменьшением мышечной массы ног у парализованного человека, ведь организм угнетает невостребованные органы и системы тела по принципу разумного использования энергетических ресурсов.
Интерферон для детей — универсальное средство для борьбы с вирусами и подъема защитных функций организма. Принцип его действия заключается в создании препятствий для попадания микробов в клетки тела. То есть, интерферон блокирует развитие и размножение бактерий в организме.
То есть, интерферон блокирует развитие и размножение бактерий в организме.
Важно! Интерферон с ингаляциями в небулайзере для ребенка можно применять в профилактических целях в период эпидемий.
Как профилактическое средство ингаляции с интерфероном в небулайзере нужно применять весь период эпидемии гриппа. Делать ингаляции нужно заблаговременно, не дожидаясь заболевания. Препарат одинаково эффективно помогает и при первых симптомах простуды, и для предотвращения заболевания. Однако во время острой фазы болезни вместо ингаляторов применяют орошения и капли.
Правила применения
Как проводят ингаляции с интерфероном? Следует учитывать, что препарат утрачивает свои свойства при высоких температурах, поэтому его нельзя нагревать выше 37 градусов. Нужно разбавить в теплом растворе.
Вдыхать испарения следует только носом, так как основная активность бактерий локализуется именно там. Вирусы попадают в организм человека через нос, поэтому именно там их и нужно ликвидировать в первую очередь.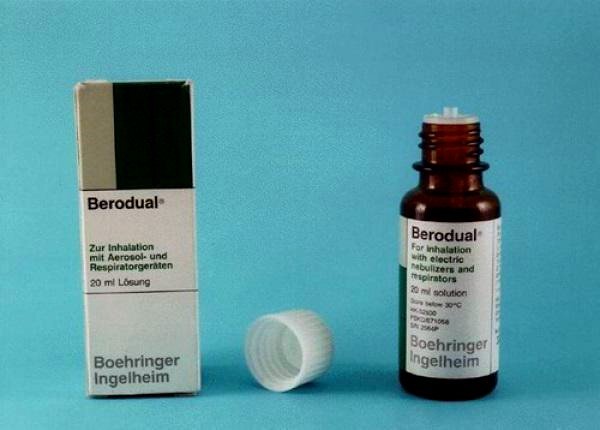 Ртом дышать нельзя.
Ртом дышать нельзя.
Ингаляции интерфероном через небулайзер — каков принцип действия? Небулайзер является прибором, распыляющим частицы вещества до микрогранул — 5 мкм или 10 мкм. По сути больной вдыхает пар, похожий на облачко. В таком состоянии лекарственные вещества быстро проникают сквозь слизистую оболочку и начинают свое лечебное действие.
Ингаляция с интерфероном — самый быстрый путь снятия симптомов простуды. Капельки лекарственных веществ равномерно распределяются по слизистой, оказывая интенсивное воздействие на больной орган.
Сколько раз можно проводить ингаляции с интерфероном в сутки? Не более четырех раз, интервал — 4 часа.
Общее правило при использовании ингаляций — за час до еды или через час после кормления. После процедуры запрещено выходить на улицу и громко разговаривать — объясните ребёнку, что нужно поиграть в тишину.
Правила приготовления раствора
Дозировка лекарственных средств определяет качество лечебной процедуры. Как правило, для ингаляции используется порошок в дозе 0,5 мг. В аптечной сети можно приобрести интерферон для ингаляций в ампулах, который следует разводить в физрастворе — тоже в ампульной расфасовке.
Как правило, для ингаляции используется порошок в дозе 0,5 мг. В аптечной сети можно приобрести интерферон для ингаляций в ампулах, который следует разводить в физрастворе — тоже в ампульной расфасовке.
Обратите внимание! Для ингаляции в небулайзере интерферон в объеме 0,5 мг нужно развести физраствором в объеме 3 мл.
Готовый лекарственный раствор нужно сразу же применять. Если вам необходимо сохранить смесь до следующего раза, ее необходимо поместить в холодильник на боковую полочку. Инструкция по применению разрешает хранить готовый раствор не более суток.
Противопоказания
Интерферон относится к безопасным препаратам, однако, противопоказания к применению существуют. Например, нельзя проводить ингалирование людям с сердечными или почечными недугами. Детям данные процедуры тоже не всегда полезны, потому что организм по-разному реагирует на ингаляции.
Запрет на проведение ингаляции ребенку:
- активная потливость после процедуры;
- изменение в стуле/мочеиспускании;
- ухудшение самочувствия;
- трудно дышать;
- нарушение сна.

Важно! Проведение ингаляций с интерфероном запрещено деткам грудного возраста.
Если вы заметили подобные отклонения в поведении малыша, прекращайте ингалирование. Никогда не проводите процедуру без ведома педиатра — он укажет необходимую дозировку для небулайзера и обозначит правильный режим проведения ингаляций.
Ингаляция интерфероном β-1a снижает смертность при COVID-19 и ускоряет выздоровление
Содержание
Общие результаты исследования
В группе плацебо шансы на выздоровление на 28 день были в 3 раза ниже, чем в группе, получавшей небулизированный рекомбинантный интерферон β-1a. В группе плацебо на 28 день было выписано 35% пациентов, а в группе, получавших интерферон – 58%.
Смертельные исходы были только в группе плацебо – 3 человека.
Побочных эффектов также было больше в группе плацебо: 60% против 54%. Наиболее частым нежелательным явлением была головная боль.
Наиболее частым нежелательным явлением была головная боль.
Методы исследования и участники
Ученые университетов Оксфорда и Саутгемптона (Великобритания) провели в 9 клиниках рандомизированное двойное слепое плацебо-контролируемое исследование. Ученые сравнивали эффективность рекомбинантного интерферона β-1a и плацебо для лечения COVID-19. Результаты исследования оценивались по состоянию пациентов на 15 и 28 день.
В исследовании участвовали 98 госпитализированных человек с подтвержденным COVID-19. Все пациенты были старше 18 лет, средний возраст – 57 лет, доля мужчин – 59%.
Доля пациентов из группы риска – 54%. Это люди с артериальной гипертензией, сердечно-сосудистыми заболеваниями, диабетом, хроническими заболеваниями легких, раком.
Средняя продолжительность симптомов COVID-19 до начала лечения составляла 10 дней (размах вариации 7 – 11 дней).
Все участники на момент начала исследования могли пользоваться небулайзером с мундштуком – эти люди не были подключены к аппаратам искусственного дыхания и не находились в отделении интенсивной терапии.
Каждый участник в течение 14 дней один раз в день получал через небулайзер плацебо или рекомбинантный интерферон β-1a в дозировке 6 млн. ЕД.
Рандомизация и маскирование
Каждому участнику был назначен уникальный идентификационный номер. Все пациенты были случайным образом разделены на 2 равных группы лечения в соответствии с графиком двойной слепой рандомизации: активное лечение интерфероном или плацебо. Простая рандомизация проводилась вручную с использованием запечатанных конвертов.
Сравниваемые препараты рекомбинантного интерферона β-1a и плацебо были идентичны по внешнему виду. Препараты были представлены в виде водных растворов, готовых к употреблению, в предварительно маркированных шприцах.
Оценка состояния пациентов
До начала исследования по всем пациентам была собрана история болезни и демографические данные.
Динамика лечения оценивалась по порядковой шкале клинического улучшения ВОЗ (Ordinal Scale for Clinical Improvement – OSCI):
- 0 – не инфицирован: нет клинических или вирусологических свидетельств инфекции;
- 1 – амбулаторно: без ограничения деятельности;
- 2 – амбулаторно: ограничение деятельности;
- 3 – легкое заболевание: без кислородной терапии;
- 4 – легкое заболевание: кислород через маску или носовые канюли;
- 5 – тяжелое заболевание: неинвазивная вентиляция или высокопоточный кислород;
- 6 – интубация и искусственная вентиляция легких;
- 7 – дополнительная поддержка жизненно важных органов;
- 8 – смерть.

Всем пациентам дважды в день оценивали OSCI, признаки спутанности сознания, анализ крови, частоту дыхания, сатурацию кислорода, проводили оценку на пневмонию, делали электрокардиограмму, проверяли наличие побочных эффектов лечения. При необходимости делали рентгенограмму грудной клетки.
Детальные исходные параметры исследования
Параметр | Группа плацебо | Группа, получавшая интерферон |
| Количество пациентов в тяжелом состоянии (OSCI ≥4) к началу исследования | 58% | 77% |
| Диабет | 33% | 12% |
| Сердечно-сосудистые заболевания | 30% | 19% |
| Гипертония | 41% | 69% |
| Хроническое заболевание легких | 44% | 42% |
| Рак | 4% | 0% |
Тяжесть заболевания на исходном уровне | ||
| Без ограничения деятельности | 2% | 0% |
| Ограничение деятельности | 2% | 0% |
| Госпитализирован без кислородной терапии | 38% | 23% |
| Кислород через маску или носовые канюли | 28% | 36% |
| Неинвазивная вентиляция | 2% | 2% |
Статус курения | ||
| В настоящее время употребляет табак | 2% | 2% |
| Бывший курильщик | 32% | 23% |
| Никогда не курил | 66% | 75% |
Детальные результаты исследования
Шансы на улучшение по шкале OSCI на 15 день были более чем в два раза выше в группе, получавшей интерферон, чем в группе плацебо (отношение шансов [OR] 2,32 [95% доверительный интервал [ДИ] 1,07 – 5,04]; p = 0,033).
Шансы на улучшение по шкале OSCI на 28 день были более чем в 3 раза выше в группе, получавшей интерферон, чем в группе плацебо (OR 3,15 [95% ДИ 1,39 – 7,14]; p = 0 · 006).
Три пациента умерли во время исследования. Все случаи смерти произошли у пациентов в группе плацебо, поэтому анализ моделирования не проводился.
В группе плацебо между первой дозой и 16-м днем у 22% пациентов развилось тяжелое заболевание или они умерли (OSCI ≥5). Причем в 10% случаев пациенты прошли интубацию или умерли (OSCI ≥6).
В группе, получавшей интерферон, в этот же период только у 13% пациентов развилась тяжелая форма коронавирусной инфекции (OSCI ≥5). Причем в 6% случаев пациентам была сделана интубация (OSCI ≥6). Ингаляции рекомбинантным интерфероном β-1a снизила вероятность развития тяжелого заболевания или смерти на 79% (OR 0,21 [95% ДИ 0,04 – 0,97]; p = 0,046).
В течение 14-дневного периода лечения вероятность выздоровления пациентов в группе, получавшей интерферон, была более чем в два раза выше, чем у пациентов в группе плацебо: 44% против 22% (соотношение рисков [HR] 2,19 [95% ДИ 1,03 – 4,69]; p = 0,043).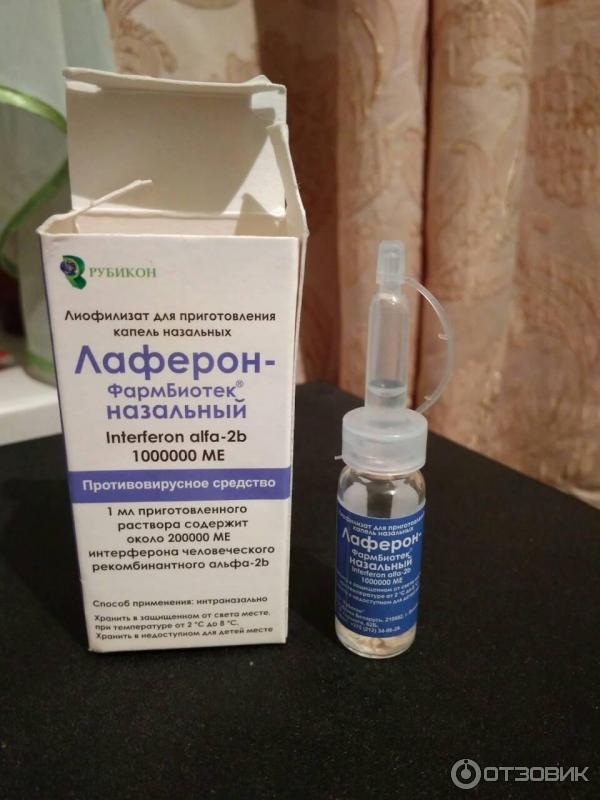
На 28 день выздоровели 58% пациентов в группе, получавшей интерферон, и 35% в группе плацебо. Шансы на выздоровление на 28 день в группе, получавшей интерферон, были более чем в три раза выше, чем в группе плацебо (OR 3,58 [95% ДИ 1,41 – 9,04]; p = 0,007).
Пациенты, получавшие интерферон, показали большее улучшение по Шкале одышки, кашля и мокроты (Breathlessness, Cough And Sputum Scale – BCSS). Уменьшение одышки было больше в группе, получавшей интерферон, чем в группе плацебо (разница –0,6 [ 95% ДИ от –1,0 до –0,2]; p = 0,007). Уменьшение кашля и выделения мокроты не были статистически значимыми в обеих группах.
Выводы
Исследование подтвердило предположение, что использование ингаляционного интерферона β-1a при коронавирусной инфекции SARS-CoV-2 улучшает противовирусный ответ и поддерживает функцию легких.
Ингаляционный способ доставки препарата позволил достичь высоких концентраций интерферона-β в легких, что привело к устойчивому локальному противовирусному ответу при ограничении системного воздействия интерферона-β.
Первоисточник
Safety and efficacy of inhaled nebulised interferon beta-1a (SNG001) for treatment of SARS-CoV-2 infection: a randomised, double-blind, placebo-controlled, phase 2 trial
Статьи по тем же ключевым словам:
| Общие характеристики | |
| Тип препарата | лекарственный препарат |
| Органы и системы | иммунная система |
| Назначение | профилактика гриппа, ОРЗ, ОРВИ, укрепление иммунитета, профилактика простудных заболеваний, лечение гриппа, профилактика ОРЗ |
| Показания к применению | Профилактика и лечение гриппа и других острых респираторных вирусных инфекций. |
| Противопоказания | Препарат не имеет противопоказаний при введении через дыхательные пути.С осторожностью:Применять с осторожностью лицам с гиперчувствительностью к антибиотикам и с повышенной чувствительностью к препаратам белкового происхождения, в том числе к мясу курицы, к куриным яйцам. С осторожностью: лицам с аллергическими заболеваниями в анамнезе. С осторожностью: лицам с аллергическими заболеваниями в анамнезе. |
| Состав | в 1 мл:активный компонент:- Интерферон альфа (интерферон лейкоцитарный человеческий) – 1 тыс. ME;вспомогательные компоненты:- натрия хлорид- 0,09 мг;- натрия дигидрофосфат дигидрат – 0,06 мг;- натрия гидрофосфат додекагидрат – 0,003 мг;- вода для инъекций-до 1 мл. |
| Действующее вещество | Интерферон альфа |
| Дозировка | 1000 МЕ/мл |
| Способ применения и дозы | Для профилактики гриппа и других острых респираторных вирусных инфекций препарат применять путем распыления или закапывания водного раствора. Введение в виде инъекций категорически запрещается.Ампулу или флакон с препаратом следует вскрывать непосредственно, перед применением. Вскрытую ампулу с препаратом можно хранить при температуре от 2 до 8 °С не более одних суток. Вскрытый флакон, аккуратно закрытый капельницей из полимерного материала, можно хранить при температуре от 2 до 8 °С до трех суток. Распыление препарата может производиться распылителями любой системы. Для детей и взрослых применяют одинаковый режим дозирования. При закапывании препарат вводить по 5 капель в каждый носовой ход 2 раза в сутки с интервалом не менее 6 часов.При лечении препарат применять путем ингаляции, распыления или закапывания. Для детей и взрослых применяют одинаковый режим дозирования. Наиболее эффективным способом является ингаляция. Для, ее проведения рекомендуются ингаляторы, оборудованные электроподогревом, либо другой системы. На одно введение используют содержимое 3 ампул препарата, к которым добавить 4 мл воды. Раствор подогреть до температуры не выше 37 °С. Ингаляционным способом препарат вводить 2 раза в сутки с интервалом не менее 6 часов. При закапывании препарат вводить по 0,25 мл (5 капель) в каждый носовой ход через 1-2 часа, не менее 5 раз в сутки, в течение2-3 дней.Меры предосторожности при применении:Категорически запрещается парентеральное введение препарата. Ингаляции рекомендуется выполнять ингаляторами, оборудованными подогревом. Распыление препарата может производиться распылителями любой системы. Для детей и взрослых применяют одинаковый режим дозирования. При закапывании препарат вводить по 5 капель в каждый носовой ход 2 раза в сутки с интервалом не менее 6 часов.При лечении препарат применять путем ингаляции, распыления или закапывания. Для детей и взрослых применяют одинаковый режим дозирования. Наиболее эффективным способом является ингаляция. Для, ее проведения рекомендуются ингаляторы, оборудованные электроподогревом, либо другой системы. На одно введение используют содержимое 3 ампул препарата, к которым добавить 4 мл воды. Раствор подогреть до температуры не выше 37 °С. Ингаляционным способом препарат вводить 2 раза в сутки с интервалом не менее 6 часов. При закапывании препарат вводить по 0,25 мл (5 капель) в каждый носовой ход через 1-2 часа, не менее 5 раз в сутки, в течение2-3 дней.Меры предосторожности при применении:Категорически запрещается парентеральное введение препарата. Ингаляции рекомендуется выполнять ингаляторами, оборудованными подогревом. |
| Побочные действия | Аллергические реакции (крапивница, полиморфная сыпь и т.д). |
| Фармакологическое действие | Противовирусное, иммуномодулирующее, противоопухолевое, антипролиферативное. Препятствует вирусному инфицированию клеток, изменяет свойства клеточной мембраны, предотвращает адгезию и проникновение вируса внутрь клетки. Инициирует синтез ряда специфических ферментов, нарушает синтез вирусной РНК и белков вируса в клетке. Изменяет цитоскелет мембраны клетки, метаболизм, предотвращая пролиферацию опухолевых (особенно) клеток. Оказывает модулирующее влияние на синтез некоторых онкогенов, приводящее к нормализации неопластической трансформации клеток и ингибированию опухолевого роста. Стимулирует процесс презентации антигена иммунокомпетентным клеткам, модулирует активность киллеров, участвующих в противовирусном иммунитете. |
| Фармакологическая группа | цитокин |
| Форма выпуска | раствор для интраназального введения и ингаляций |
| Способ применения/введения | назальный, ингалятивный |
| Минимальный возраст применения | от 18 лет |
| Дополнительно | |
| Условия хранения | Препарат хранят в соответствии с СП 3. 3.2.1248-03 при температуре от 2 до 10°С. 3.2.1248-03 при температуре от 2 до 10°С. |
| Условия отпуска из аптеки | Препарат транспортируют в соответствии с СП 3.3.2.1248-03 при температуре от 2 до 10°С. |
| Передозировка | Случаев передозировки не выявлено. |
| Применение при беременности и кормлении грудью | В период беременности и в период лактации Интерферон назначают только при условии, что ожидаемый эффект для матери превышает риск для плода. |
| Влияние на способность управлять транспортом и механизмами | Не выявлено. |
| Особые указания | С целью профилактики введение препарата следует начинать при непосредственной угрозе заражения и продолжать до тех пор, пока опасность заражения сохраняется. С целью лечения препарат следует применять на ранней стадии заболевания при появлении первых клинических симптомов. |
| Взаимодействие | В экспериментах в культуре ткани, проведенных в лаборатории антибиотиков, было установлено, что при совместном применении метилурацила с интерфероном лейкоцитарным человеческим жидким наблюдается выраженное синергидное действие. Выраженное синергидное действие наблюдается при комбинации интерферона лейкоцитарного человеческого с лизоцимом. Выраженное синергидное действие наблюдается при комбинации интерферона лейкоцитарного человеческого с лизоцимом. |
| Источник | Справочник лекарственных препаратов Видаль |
| Регистрационный номер | P N002335/01 |
| Дата государственной регистрации | 2016/03/31 00:00:00 |
| Владелец регистрационного удостоверения | Биомед им. И.И. Мечникова |
| Страна бренда | Россия |
| Страна-производитель | Россия |
| Название препарата | Интерферон человеческий лейкоцитарный |
Ингаляционный интерферон Synairgen для COVID-19 усиливает короткую, безвредную версию точки входа вируса: исследование
Прошлым летом акции Synairgen взлетели на 300% по результатам исследования, показывающего, что его ингаляционная форма интерферона бета-1a, разработанная для лечения COVID-19, уменьшилась. шанс того, что пациенты разовьются до тяжелой формы вируса.
Но на результаты нависла большая тень: известно, что интерферон увеличивает уровень белка клеточной поверхности ACE2, который служит точкой входа для SARS-CoV-2, вируса, вызывающего COVID-19. Это вызвало опасения, что лечение на основе интерферона в конечном итоге не поможет в лечении коронавируса.
Это вызвало опасения, что лечение на основе интерферона в конечном итоге не поможет в лечении коронавируса.
Теперь исследователи во главе с Саутгемптонским университетом, который сотрудничает с Synairgen в разработке своего препарата, обнаружили, что интерферон повышает уровень короткой формы ACE2, которая не позволяет SARS-CoV-2 проникать в клетки. Фактически, это может иметь защитный эффект, сообщила команда в журнале Nature Genetics.
Саммит BD&L
Выводы о сделках в отрасли наук о жизни
Собирает вместе ключевых участников сделок и служит открытым форумом для кросс-функциональных отделов развития бизнеса и юристов для обмена ценной информацией и действенными стратегиями успешного управления альянсами, лицензионными соглашениями и сделками M&A.
СВЯЗАННЫЙ: акции Synairgen растут по результатам лечения COVID-19
У короткой формы ACE2, которую обнаружили британские исследователи, отсутствует определенный сайт связывания, необходимый SARS-CoV-2 для проникновения в здоровые клетки. Поскольку эта короткая версия белка повышается в ответ на интерфероны, но не на SARS-CoV-2, исследователи полагают, что он каким-то образом участвует в естественном иммунном ответе организма на вирусы.
Поскольку эта короткая версия белка повышается в ответ на интерфероны, но не на SARS-CoV-2, исследователи полагают, что он каким-то образом участвует в естественном иммунном ответе организма на вирусы.
«Мы были взволнованы, обнаружив новую форму ACE2, и стали еще более заинтересованными, когда [осознали], что может защищать от SARS-CoV-2 в дыхательных путях, а не в месте проникновения инфекции», – сказал профессор Саутгемптонского университета. Джейн Лукас, М.D., Ph.D., в заявлении. Два соавтора исследования, Донна Дэвис, доктор философии, и Ратко Джуканович, доктор медицины, являются соучредителями и акционерами Synairgen, которая была выделена из университета.
Инвесторы приветствовали Synairgen, когда предварительные данные его исследования с участием 101 пациента показали, что его препарат интерферона, SNG001, снизил риск прогрессирования COVID-19 в тяжелую форму на 79% по сравнению с плацебо. Обновление этих результатов подняло акции компании еще на 30% в ноябре, когда компания сообщила, что 75% пациентов, принимавших SNG001, показали клиническое улучшение на 15/16 день, как измерено по ключевой шкале Всемирной организации здравоохранения.
Открытие короткого ACE2 может иметь последствия не только для Synairgen, утверждают авторы в новом исследовании. По их словам, способность исследователей различать две версии белка может породить идеи для более сложных методов лечения коронавируса.
Команда Университета Саутгемптона в настоящее время планирует дальнейшие исследования для изучения влияния короткого ACE2 на лечение COVID-19.
В декабре Synairgen объявила о начале третьей фазы испытания SNG001 в США.K. и что FDA присвоило лекарству ускоренный статус и разрешило его для исследований в США.
ингаляционных интерферонов могут помочь госпитализированным пациентам с COVID-19
Госпитализированные пациенты с COVID-19, получавшие SNG001, ингаляционный ингаляционный интерферон бета-1a, имели больше шансов показать клиническое улучшение, чем пациенты, получавшие плацебо, как показало небольшое пилотное исследование в Великобритании.
Пациенты, рандомизированные для приема SNG001 в течение 14 дней, имели больше шансов на улучшение по порядковой шкале Всемирной организации здравоохранения (ВОЗ) для клинического улучшения (OSCI; OR 2.32, 95% ДИ 1,07–5,04, P = 0,033) на 15 или 16 день по сравнению с теми, кто получал плацебо, сообщили Том Уилкинсон, доктор философии из Саутгемптонского университета в Англии, и его коллеги.
Более того, пациенты в группе вмешательства с большей вероятностью вернулись к шкале OSCI, равной 1, или к отсутствию ограничения активности на 15 или 16 день (HR 2,19, 95% CI 1,03-4,69, P = 0,043), авторы написали в журнале Lancet Respiratory Medicine .
Интерферон 1 типа является «одним из первых цитокинов, индуцированных вирусной инфекцией клетки, и является основным драйвером врожденных иммунных ответов в легких человека», – отметили исследователи.Они объяснили, что SNG001 представляет собой рецептуру рекомбинантного бета-интерферона «для ингаляционной доставки с помощью [небулайзера]», которая хорошо переносится в клинических исследованиях среди пациентов с астмой или хронической обструктивной болезнью легких.
Интересно, что в сопроводительной редакционной статье Nathan Peiffer-Smadja, MD, и Yazdan Yazdanpanah, MD, PhD, оба из Assistance-Publique Hôpitaux de Paris во Франции, отмечалось, что интерферон не дал предварительных результатов исследования SOLIDARITY ВОЗ.
Помимо различного состава двух испытаний, редакторы обнаружили еще одно ключевое различие: способ применения.В SOLIDARITY использовался подкожный бета-1а интерферон, тогда как в этом исследовании использовалась небулайзерная терапия, которая «доставляет интерферон бета-1а прямо в дыхательные пути».
«[Распыляемая] терапия позволяет направленную доставку интерферона в легкие, где он может индуцировать экспрессию стимулированных интерфероном генов, которые участвуют прямо … или опосредованно … в противовирусном ответе слизистой оболочки», Пайффер-Смаджа и Язданпанах написал.
Для нового исследования Уилкинсон и его коллеги рандомизировали взрослых, госпитализированных с симптомами COVID-19, которые дали положительный результат на SARS-CoV-2 с помощью полимеразной цепной реакции с обратной транскриптазой или теста в месте оказания помощи, чтобы получить SNG001 или ингаляционное плацебо для 14 человек. дней.Первичным результатом было изменение клинического состояния по шкале ВОЗ OSCI (9-балльная шкала, где 0 означает отсутствие инфекции, а 8 означает смерть).
С 30 марта по 30 мая в общей сложности 48 пациентов были рандомизированы в группу SNG001 и 50 – в группу плацебо в ходе анализа намерения лечиться. Средний возраст пациентов составлял 57 лет, 59% составляли мужчины и 80% были белыми. Исходные сопутствующие заболевания включали гипертонию, сердечно-сосудистые заболевания, диабет, хроническое заболевание легких и рак.
Демографические характеристики между группами были схожими, хотя группа SNG001 имела более тяжелое заболевание: 77% пациентов получали кислородную терапию по сравнению с 58% в группе плацебо.Средняя продолжительность симптомов до начала лечения составляла 10 дней.
В группе SNG001 шансы на улучшение были более чем в три раза выше на 28 день по сравнению с плацебо (OR 3,15, 95% CI 1,39-7,14, P = 0,046), отметили авторы.
Пять пациентов прошли интубацию или умерли по сравнению с тремя в группе вмешательства. За 14 дней лечения вероятность выздоровления у пациентов в группе вмешательства была более чем в два раза выше.
Не было разницы в шансах выписки из больницы или времени до выписки из больницы между группами.К 14 дню были выписаны 73% группы плацебо и 69% группы вмешательства.
Что касается безопасности, 54% пациентов в группе вмешательства и 60% в группе плацебо сообщили о побочных эффектах, возникающих в результате лечения, наиболее частым из которых была головная боль (15% и 10% соответственно). У меньшего числа пациентов в группе вмешательства были серьезные побочные эффекты по сравнению с плацебо (15% против 28%), и наиболее распространенными были дыхательная недостаточность (6% против 12%) и пневмония (по 6% каждый).
У одного пациента в группе плацебо был синдром полиорганной недостаточности, а у одного – легочная эмболия, что заставило их отказаться от участия в исследовании.Эти пациенты позже умерли вместе с третьим пациентом в группе плацебо, который умер от пневмонии COVID-19.
В своей редакционной статье Пайффер-Смаджа и Язданпанах отметили, что это исследование не способно оценить исходы смертности, и призвали к крупным рандомизированным испытаниям для изучения эффективности распыленного интерферона бета-1а, предполагая, что он может принести пользу пациентам на ранней стадии заболевание в амбулаторных условиях.
«У пациентов с тяжелой формой COVID-19 обостренная воспалительная реакция была определена как причина легочных осложнений, а интерферон бета-1a – провоспалительный цитокин – может усиливать воспалительную реакцию и быть связан с проблемами безопасности. “писали редакторы.
Они добавили, что безопасность также будет проблемой, поскольку «[распыление] интерферона еще не имеет коммерческого [разрешения] для каких-либо показаний».
Примечательно, что рекомендации по COVID-19 Национального института здоровья не рекомендуют использовать интерферон, кроме как в рамках рандомизированного клинического исследования.
Молли Уокер – помощник редактора, освещающая инфекционные заболевания в MedPage Today.У нее есть страсть к доказательствам, данным и общественному здоровью. Подписаться
Раскрытие информации
Исследование финансировалось Synairgen Research, Великобритания, дочерней компанией Саутгемптонского университета.
Wilkinson сообщил о поддержке со стороны Саутгемптонского центра биомедицинских исследований NIHR, my mhealth, GlaxoSmithKline, AstraZeneca, Boehringer Ingelheim и Synairgen Research.Несколько соавторов являются сотрудниками Synairgen Research, в том числе один, который является директором Synairgen (материнская компания Synairgen Research). Несколько соавторов также раскрыли патент на ингаляционный бета-интерферон у пациентов с SARS-CoV-2 и патенты, касающиеся противовирусной терапии респираторных заболеваний, в частности, бета-интерферона. Кроме того, один соавтор является управляющим партнером TranScrip Partners, а другие соавторы заявили о поддержке со стороны Synairgen Research, TranScrip Partners, Boehringer Ingelheim, Celgene, BioMerieux и BioFire, Roche, Janssen, Cidara Therapeutics, Randox, Qiagen, Novartis, AstraZeneca, Teva и Оксфордский центр биомедицинских исследований NIHR.
Пайффер-Смаджа и Язданпанах сообщили, что у них нет конкурирующих интересов.
Антивирусные биомаркеры активируются в клетках мокроты после введения ингаляционного интерферона бета пациентам с ХОБЛ
Резюме
Предпосылки: Интерферон бета (IFN-β) играет ключевую роль в защите хозяина от вирусов, вызывая экспрессию генов, стимулированных интерфероном. (ISG), которые ограничивают репликацию вирусов и способствуют противовирусным иммунным ответам.Ингаляционный IFN-β разрабатывается для лечения вирусных обострений заболеваний легких. В предыдущих исследованиях лечение ингаляционным IFN-β усиливало противовирусную защиту легких (экспрессию ISG клеток мокроты) и улучшало функцию легких и симптомы у «трудно поддающихся лечению» астматиков с инфекцией простуды или гриппа (Djukanović AJRCCM 2014 190 (2): 145-54). SG015 (NCT03570359) – это продолжающееся исследование на пациентах с ХОБЛ без (Часть 1) и с (Часть 2) подтвержденной респираторной вирусной инфекции, оценивающее ответ на антивирусные биомаркеры и клинические эффекты ингаляционного IFN-β по сравнению с плацебо.Представлены результаты из части 1.
Методы: 10 пациентов получали три суточные дозы IFN-β (6MIU) или плацебо (соотношение 8: 2) через небулайзер. Мокроту собирали перед дозированием (исходный уровень), через 24 часа после первой и третьей дозы и через 4-6 дней после третьей дозы. Экспрессию гена клеток мокроты (Mx1, OAS1, IFIT2, GBP1 и CXCL10) определяли с помощью RT-qPCR.
Результаты: Ингаляционный IFN-β хорошо переносился. Все противовирусные биомаркеры были значительно повышены через 24 часа после введения дозы по сравнению с исходным уровнем (p <0.05), за исключением CXCL10 после 3-й дозы (p = 0,06) (n = 5-6). Повышение экспрессии генов Mx1 и OAS1 при свертывании было аналогично тому, которое наблюдалось при той же дозе у стабильных астматиков.
Выводы: Антивирусные биомаркеры были значительно активированы в легких пациентов с ХОБЛ после введения ингаляционного IFN-β, что подтверждает предложенный механизм действия в качестве лечения вирус-индуцированных обострений.
Сноски
Цитируйте эту статью как: European Respiratory Journal 2019; 54: Дополнение.63, OA263.
Это тезисы Международного конгресса ERS. Полнотекстовая версия недоступна. Дополнительные материалы, сопровождающие этот тезис, могут быть доступны на сайте www.ers-education.org (только для членов ERS).
- Авторские права © авторы 2019
Интерферон бета-1а может помочь пациентам с COVID-19 быстрее выздороветь
The Lancet Respiratory Medicine вчера опубликовал результаты клинического исследования, показывающие, что вдыхаемый белок иммунного ответа интерферон бета-1 снизили вероятность тяжелого заболевания или смерти госпитализированных пациентов с COVID-19 от инфекции.
В двойном слепом рандомизированном контролируемом исследовании, проведенном в девяти больницах Соединенного Королевства, приняли участие 98 пациентов, набранных с 30 марта по 30 мая. Пациенты были случайным образом распределены для приема либо ингаляционного препарата интерферона бета-1а SNG001, либо препарата. плацебо один раз в день в течение 14 дней.
У пациентов, получавших SNG001, вероятность клинического улучшения на 15 или 16 день была в два раза выше, чем у пациентов, получавших плацебо (21 из 48 [44%] против 11 из 50 [22%]). В начале исследования 37 пациентам (77%) в группе SNG001 и 29 (58%) в группе плацебо требовался дополнительный кислород.
Одиннадцать из 50 пациентов, получавших плацебо (22%), серьезно заболели и потребовали искусственной вентиляции легких, или умерли между первой дозой и 15 или 16 днем, по сравнению с 6 из 48 (13%), получавших SNG001. Все пациенты в группе SNG001 выжили, а трое в группе плацебо умерли.
Шансы выписки из больницы к 28 дню существенно не различались между двумя группами: 39 из 48 (81%) в группе SNG001 и 36 из 48 (75%) в группе плацебо. Двадцать шесть (54%) пациентов, получавших SNG001, и 30 (60%) пациентов, получавших плацебо, испытали побочные эффекты во время лечения, наиболее частым из которых была головная боль.
Вторичный анализ показал, что у пациентов с SNG001 вероятность выздоровления более чем в три раза выше, чем у пациентов, получавших плацебо через 28 дней, что определяется по восстановлению способности возобновлять нормальную деятельность.
Повышение защиты легких
Интерферон бета – это белок, который координирует иммунный ответ на вирусные инфекции, такие как COVID-19, в то же время коронавирус подавляет его высвобождение. SNG001, который доставляется непосредственно в легкие после ингаляции, был протестирован при лечении астмы и хронической обструктивной болезни легких, но не был одобрен для каких-либо показаний.Инъекционная форма бета-интерферона одобрена для лечения других состояний, включая рассеянный склероз.
Соавтор Том Уилкинсон, доктор медицинских наук, магистр наук из Университета Саутгемптона, сказал в пресс-релизе Lancet, что бета-интерферон может восстановить иммунный ответ легких и ускорить восстановление после COVID-19.
«Вдыхаемый интерферон бета-1a обеспечивает высокую локальную концентрацию иммунного белка, который усиливает защитные силы легких, а не воздействует на конкретные вирусные механизмы», – сказал Уилкинсон.«Это может иметь дополнительные преимущества при лечении инфекции COVID-19, когда она возникает вместе с инфекцией другим респираторным вирусом, таким как грипп или респираторно-синцитиальный вирус (RSV), с которым вполне можно столкнуться в зимние месяцы».
В настоящее время исследовательская группа оценивает эффективность интерферона бета-1а у пациентов с коронавирусом перед госпитализацией. Авторы отметили, что исследование белка у пациентов, получающих искусственную вентиляцию легких, потребует другого метода доставки, кроме ингаляции.
Необходим профиль безопасности
В комментарии к тому же журналу Натан Пайффер-Смаджа, доктор медицинских наук, и Яздан Язданпанах, доктор медицинских наук, оба из Hopitaux de Paris, отметили, что исследования in vitro и на животных показали, что интерферон бета обладает противовирусным действием против других коронавирусов, таких как те, которые вызывают тяжелый острый респираторный синдром (SARS) и ближневосточный респираторный синдром (MERS).
Однако они предупреждают, что ранние результаты другого исследования, не прошедшего экспертную оценку, рандомизированного клинического исследования SOLIDARITY / DisCoVeRy, не показали, что подкожный инъекционный интерферон бета-1a эффективен при лечении пациентов с COVID-19, 8% кому требовалась искусственная вентиляция легких.Они сказали, что отсутствие эффективности может быть связано с тем, что подкожная доставка напрямую не нацелена на легкие, как при вдыхании.
Пайффер-Смаджа и Язданпанах также предупреждают, что интерферон бета-1а может вызвать опасную воспалительную реакцию у тяжелобольных пациентов с COVID-19. Они также сказали, что исследование не показало никакого эффекта лечения на момент выписки из больницы или смерти, а это означает, что для подтверждения результатов потребуются более крупные рандомизированные клинические испытания.
«Безопасность распыленного интерферона бета-1а будет представлять особый интерес, поскольку распыление интерферона еще не имеет разрешения на продажу для каких-либо показаний», – написали авторы комментария.«В будущих исследованиях следует оценить влияние интерферона бета-1а на воспалительные биомаркеры и проанализировать вирусологические данные, чтобы лучше охарактеризовать физиопатологию, лежащую в основе этого препарата. Также будет целесообразно изучить, влияет ли интерферон бета-1а на длительные симптомы COVID-19. , особенно легочные симптомы ».
Synairgen объявляет о включении своего лечения ингаляционным интерфероном бета в исследование US NIH ACTIV-2 у амбулаторных пациентов с COVID-19 Лондонская фондовая биржа: SNG
Пресс-релиз
Synairgen plc
(Synairgen или компания ‘)
Synairgen объявляет о включении своего лечения ингаляционным бета-интерфероном в исследование US NIH ACTIV-2 у амбулаторных пациентов с COVID-19
Партнерство ACTIV финансируется «Операцией Warp Speed», возглавляемой Департаментом правительства США. Здравоохранение и социальные услуги и предназначены для ускорения разработки наиболее перспективных методов лечения и вакцин-кандидатов от COVID-19
Саутгемптон, Великобритания – 25 января 2021 года: Synairgen plc (LSE: SNG), компания по открытию и разработке респираторных препаратов. , сегодня объявляет о соглашении о клиническом испытании, чтобы включить его ингаляционный интерферон бета-1a (SNG001) в испытание ACTIV-2 / A5401 фазы II / III в пациенте. люди с COVID-19, еще не нуждающиеся в госпитализации.Исследование спонсируется Национальным институтом аллергии и инфекционных заболеваний США (NIAID), входящим в состав Национальных институтов здравоохранения США (NIH).
NIH A ccelerating C OVID-19 T лечебный I изобретений и V accines (ACTIV) (https://www.nih.gov research-training / medical-research-Initiative / activ) – это государственно-частное партнерство, направленное на разработку стратегии скоординированных исследований для ускорения разработки наиболее многообещающих методов лечения и вакцин-кандидатов от COVID-19.ACTIV-2 – это мастер-протокол, разработанный для оценки нескольких исследуемых агентов по сравнению с плацебо у взрослых с COVID-19 от легкой до умеренной степени тяжести, не требующий госпитализации.
Исследование ACTIV-2 фазы II / III, возглавляемое группой клинических исследований СПИДа (ACTG), финансируемой NIAID, представляет собой адаптивное рандомизированное слепое плацебо-контролируемое исследование. В ходе оценки SNG001 на этапе II будет набрано до 220 участников в разных центрах США в домашних условиях, разделенных между SNG001 и плацебо, а положительный результат позволяет перейти к этапу III части исследования.
NIAID является регулирующим спонсором и держателем заявки на получение новых лекарственных препаратов для проведения исследования ACTIV-2, которое финансируется Operation Warp Speed, партнерством, возглавляемым Министерством здравоохранения и социальных служб США через NIAID, для расследования и координации разработка, производство и распространение средств диагностики, лечения и вакцин COVID-19.
Ричард Марсден, генеральный директор Synairgen, сказал: «Включение нашего лечения ингаляционным интерфероном бета-1а в финансируемое правительством США исследование ACTIV-2 отражает большой интерес, который вызвали наши данные по фазе II, и сильный интерес компании. убежденность в том, что этот препарат может сыграть жизненно важную роль в лечении COVID-19.В качестве ингаляционного лечения SNG001 предлагает простоту использования, что позволяет пациентам удобно вводить его дома, снижая риск передачи вируса во время визитов в больницу и снимая большую логистическую нагрузку на системы здравоохранения.
Лечение в домашних условиях также может применяться намного раньше в ходе болезни, предотвращая распространение вируса в нижних дыхательных путях и, в сценарии, когда больницы загружены, лечить пациентов на дому. настройка могла быть единственным вариантом.Мы надеемся получить ценные данные из этого испытания, которые помогут нам в дальнейшем одобрении SNG001 в качестве средства лечения COVID-19 ».
Кроме того, 12 января 2021 года Synairgen начал дозирование в международном исследовании фазы III для 610 пациентов, оценивающем эффективность ингаляционного бета-интерферона у госпитализированных пациентов с COVID-19.
Компания считает, что информация, содержащаяся в этом объявлении, составляет инсайдерскую информацию в соответствии с Регламентом о злоупотреблениях на рынке (ЕС) №596/2014.
Для дальнейших запросов обращайтесь:
Synairgen plc
Ричард Марсден, главный исполнительный директор
Джон Уорд, финансовый директор
Тел .: + 44 (0) 23 8051 2800
finnCap (назначенный советник и совместный Брокер)
Джефф Нэш, Джеймс Томпсон, Чарли Бисон (Корпоративные финансы)
Элис Лейн, Сунила де Сильва (ECM)
Тел .: + 44 (0) 20 7220 0500
Numis Securities Limited (Совместный брокер)
Джеймс Блэк, Фредди Барнфилд, Дункан Монтейт
Тел .: +44 (0) 20 7260 1000
Consilium Strategic Communications (Финансовые СМИ и отношения с инвесторами)
Мэри-Джейн Эллиот, Сью Стюарт, Оливия Мансер
synairgen @ consilium-comms.com
Tel: +44 (0) 20 3709 5700
Заметки для редакторов
О Synairgen
Synairgen – это компания по открытию и разработке респираторных препаратов на клинической стадии, основанная профессорами Саутгемптонского университета сэром Стивеном Холгейтом , Донна Дэвис и Ратко Джуканович. Synairgen в настоящее время полностью сосредоточен на продвижении своего ингаляционного противовирусного препарата широкого спектра действия интерферона бета1а в качестве эффективного лечения людей, страдающих инфекцией COVID-19.
Платформа BioBank по биологии человека от Synairgen и всемирно известная международная академическая сеть KOL имеют более широкое применение для защиты легких от вирусов при других респираторных заболеваниях, включая астму и ХОБЛ. Synairgen котируется на AIM (LSE: SNG). Дополнительную информацию о Synairgen см. На сайте www.synairgen.com
COVID-19
COVID-19, вызванный вирусом SARS-CoV-2, представляет собой глобальную угрозу, и существует острая необходимость в оценке новых методов лечения. для предотвращения и эффективного лечения тяжелых заболеваний нижних дыхательных путей, которые могут возникнуть при этом заболевании.Пожилые люди и люди с сопутствующими заболеваниями, такими как сердечные и легочные осложнения и диабет, подвергаются наибольшему риску развития тяжелых или смертельных заболеваний.
SNG001 (ингаляционный интерферон бета) применимость к COVID-19
Интерферон бета (IFN-бета) – это природный белок, который управляет противовирусными реакциями организма. Он широко используется системно для лечения рассеянного склероза и является безопасным и хорошо переносимым препаратом. Появляется все больше свидетельств того, что дефицит продукции IFN-бета в легких может объяснить повышенную восприимчивость групп пациентов «из группы риска» к развитию тяжелых заболеваний нижних дыхательных путей (легких) во время респираторных вирусных инфекций.Кроме того, вирусы, в том числе коронавирусы, особенно SARS-CoV-2, развили несколько механизмов для подавления эндогенной продукции IFN-бета в легких, тем самым помогая вирусу уклоняться от врожденной иммунной системы. Добавление экзогенного IFN-бета до или во время вирусной инфекции клеток легких in vitro либо предотвращает, либо значительно снижает репликацию вируса, чтобы уменьшить тяжесть инфекции и ускорить выздоровление. Признавая важность достижения высоких концентраций в легких, где SARS-CoV-2 оказывает наибольшее повреждающее действие на ткани, Synairgen SNG001 представляет собой формулировку IFN-бета-1a для прямой доставки в легкие посредством распыления.Он имеет нейтральный pH и не содержит маннита, аргинина и человеческого сывороточного альбумина, что делает его пригодным для ингаляционной доставки непосредственно к месту воздействия. Данные испытаний фазы I и II показали, что SNG001 активирует противовирусную защиту легких, измеренную в клетках мокроты, и что на сегодняшний день SNG001 хорошо переносится примерно у 280 пациентов с астмой / ХОБЛ / COVID-19.
В июле 2020 года Synairgen объявила о результатах своего двойного слепого плацебо-контролируемого исследования фазы II с участием 101 рандомизированного госпитализированного пациента с COVID-19, которое показало, что прием SNG001 в течение 14 дней был связан с более высокими шансами на улучшение по сравнению с плацебо. Порядковая шкала клинического улучшения ВОЗ и более быстрое выздоровление до точки, при которой пациенты больше не были ограничены в своей деятельности, с большей долей пациентов, выздоравливающих в течение 28-дневного периода исследования.
Результаты были опубликованы в журнале The Lancet Respiratory Medicine: «Безопасность и эффективность ингаляционного распыленного интерферона бета-1а (SNG001) для лечения инфекции SARS-CoV-2: рандомизированное двойное слепое плацебо-контролируемое исследование фазы 2». “. Monk, P D et al., 12 ноября 2020 г., доступно здесь: https://www.thelancet.com/journals/lanres/article/PIIS2213-2600(20)30511-7/fulltext .
20 января 2021 года Synairgen объявила, что завершила набор 120 пациентов с COVID-19 (старше 65 лет или старше 50 с сопутствующими заболеваниями) в домашних условиях для своего исследования SG016.Результаты этого исследования ожидаются во втором квартале 2021 года.
Synairgen начинает дозирование ингаляционного препарата COVID-19 в испытании фазы 3 –
UK biotech Synairgen продвигается вперед с испытанием фазы 3 SNG001 у госпитализированных пациентов с COVID-19 после обнадеживающие результаты исследования фазы 2, начавшегося в марте прошлого года.
Ингаляционный состав интерферона бета-1a, доставляемый с помощью небулайзера, будет протестирован на 610 госпитализированных пациентах с COVID-19, которым требуется дополнительный кислород, примерно в 20 странах, участвующих в исследовании, названном SG018.
Интерферон бета-1а уже используется в инъекционной форме при рассеянном склерозе, и до того, как пандемия разразилась, Synairgen уже тестировал свою ингаляционную версию в испытаниях с участием пациентов с астмой и хронической обструктивной болезнью легких (ХОБЛ).
Цитокин является частью реакции организма на вирусную инфекцию, и есть некоторые свидетельства того, что люди, которые серьезно заболевают после заражения вирусом SARS-CoV-2, имеют более низкие, чем обычно, уровни бета-интерферона в легких. .
Компания из Саутгемптона заявила, что назначила контрактную исследовательскую организацию (CRO) Parexel для помощи в проведении фазы 3 испытания, в настоящее время уже создано несколько британских центров, а другие в США и ЕС, как ожидается, вскоре появятся.
Первый пациент прошел лечение в Hull Royal Infirmary на этой неделе, и Synairgen надеется получить результаты летом, а это значит, что к осени можно будет получить разрешение на неотложную помощь.
Предварительные результаты исследования Synairgen на 100 пациентах фазы 2 SG016 были опубликованы в The Lancet в ноябре прошлого года и показали, что пациенты, получавшие SNG001, имели больше шансов на улучшение и быстрее выздоравливали от инфекции SARS-CoV-2, чем пациенты, получавшие плацебо.
Основной конечной точкой в исследовании была Порядковая шкала клинического улучшения (OSCI) – стандартная девятибалльная мера, разработанная Всемирной организацией здравоохранения (ВОЗ).
Пациенты, принимавшие SNG001, с большей вероятностью демонстрировали улучшение по шкале OSCI на 15 или 16 день после начала приема препарата и с большей вероятностью, чем пациенты, получавшие плацебо, вернулись к баллу OSCI, равному 1 – без ограничения их повседневной активности – во время лечения.
Было также три случая смерти в группе плацебо и ни одного случая смерти среди пациентов, принимавших SNG001, хотя испытание не было достаточно статистически мощным, чтобы оценить, было ли это реальным эффектом или случайностью.
Национальный институт исследований в области здравоохранения Великобритании (NIHR) присвоил испытанию 3 фазы статус «Срочная служба общественного здравоохранения», поэтому оно имеет право на поддержку со стороны сети клинических исследований NIHR. Между тем, FDA присвоило SNG001 статус ускоренного отслеживания COVID-19.
Ричард Марсден
В то время как развертывание вакцины поднимает настроение в разгар пандемии, исполнительный директор Synairgen Ричард Марсден сказал, что лечение все еще необходимо в «случаях, когда вакцины неэффективны, для тех, кто не прошел вакцинацию, и если вирус мутирует до такой степени, что вакцины становятся менее эффективными.«
» «Мы считаем, что это испытание представляет собой возможность для значительного научного прорыва в Великобритании, и при правильной поддержке наш препарат может быстро помочь в преодолении глобального кризиса», – добавил он.
Synairgen сообщил BBC, что курс лечения SNG001 будет стоить около 2 000 фунтов стерлингов, что, по словам Марсдена, представляет собой «хорошее соотношение цены и качества».
Ингаляционные препараты могут помочь пациентам с Covid-19, но необходимы дополнительные исследования.
Ингаляционная форма интерферона – препарата, обычно используемого для лечения рассеянного склероза с помощью инъекций, – может помочь защитить госпитализированных пациентов с Covid-19 от ухудшения, согласно данным Британский производитель лекарств.
Результаты были впервые опубликованы в июле, но были опубликованы в четверг как рецензируемое исследование в журнале The Lancet Respiratory Medicine.
Полный охват вспышки коронавируса
Организм естественным образом выделяет интерферон при столкновении с каким-либо захватчиком, например вирусом или другим патогеном. Как следует из названия, он работает, препятствуя репликации вируса. Некоторые исследователи предположили, что у пациентов с Covid-19, как правило, наблюдается дефицит интерферона, особенно в крови и легких.
Теоретически повышение уровня интерферона в организме поможет пациентам бороться с такими заболеваниями, как Covid-19.
Действительно, исследование, опубликованное в мае, показало, что коронавирус имеет тенденцию подавлять естественную реакцию организма на интерферон.
Предыдущее испытание под названием «Солидарность» показало, что введение препарата не помогло снизить смертность от Covid-19 и не помогло пациентам быстрее выздороветь.
В новом исследовании Synairgen, фармацевтической компании из Великобритании, использовался ингаляционный тип интерферона, называемый интерфероном бета-1a (SNG001).В этом случае лекарство попадает прямо в дыхательные пути.
Исследование было небольшим, в него вошли всего 98 пациентов, которые заболели прошлой весной. Около половины получали лекарство каждый день в течение двух недель. Остальные получили плацебо. Исследователи следили за их прогрессом в течение месяца.
Авторы исследования писали, что группа интерферона «имела больше шансов на улучшение и быстрее выздоравливала от инфекции SARS-CoV-2, чем пациенты, получавшие плацебо». SARS-CoV-2 – это вирус, вызывающий Covid-19.
У тех, кто принимал препарат, вероятность выздоровления к 15 или 16 дню была в два раза выше.
Интерферон «может иметь потенциал в качестве ингаляционного препарата для восстановления иммунного ответа легких и ускорения выздоровления от Covid-19», – автор исследования Том Уилкинсон. из Университета Саутгемптона в Великобритании написал в пресс-релизе. То есть лекарство может работать лучше, если оно доставляется непосредственно в легкие, а не через кровоток.
«Если я сделаю вам инъекцию интерферона, и вы получите ничтожное количество в легких, это будет похоже на то, что я вам ничего не дал.Вы не ожидаете, что это принесет пользу “, – сказал доктор Хью Кассиер, директор отделения интенсивной терапии больницы Sandra Atlas Bass Heart Hospital при университетской больнице North Shore, входящей в состав Northwell Health, на Лонг-Айленде, штат Нью-Йорк. участвовал в исследованиях вдыхаемого интерферона.
Но, добавил он, когда вы помещаете это лекарство в форму, которую можно вдыхать, «и вы получаете прямое осаждение в ткани легких, вы можете получить очень высокие уровни препарата. Если препарат подействует, можно ожидать некоторой пользы.”
Загрузите приложение NBC News для полного освещения вспышки коронавируса. k
Исследователи предупреждают, что исследование было слишком маленьким, чтобы делать какие-либо окончательные заявления о потенциальных преимуществах ингаляционного интерферона или выявлять какие-либо Возможные побочные эффекты. Ингаляционные формы интерферона не одобрены для использования в США.
В внутривенных или инъекционных формах интерферон может вызывать симптомы гриппа, боль в суставах и лихорадку.
В комментарии к исследованию, Натан Пайффер-Смаджа из Assistance Publique – Hôpitaux de Paris, Франция, указали, что время введения интерферона может иметь решающее значение.Иммунные реакции могут быть полезными на раннем этапе болезни, но также могут обострить болезнь позже.
Понятно, что гипервоспалительная реакция у некоторых пациентов с Covid-19 является пагубной и описывается как «цитокиновый шторм». Действительно, интерферон – это цитокин. Пайффер-Смаджа, который не участвовал в новом исследовании, написал, что существует необходимость «изучить, влияет ли интерферон бета-1а на пролонгированные симптомы, особенно легочные».
Связанные
Если результаты подтвердятся в более крупных испытаниях, препарат может принести большую пользу в условиях неконтролируемой пандемии, которая охватила больницы по всей стране.


