Неправильная ингаляция может убить
Зима – это разгар не только ковидной пандемии, но обычных сезонных заболеваний – ОРВИ и гриппа. В арсенале любителей самолечения – старая добрая ингаляция. Если не поможет, то уж точно не навредит, считают они. И сильно ошибаются. Об опасностях назначенной самим себе процедуры рассказывают в программе “О самом главном” на телеканале “Россия 1”.
Многие россияне до сих пор при первых признаках простуды прибегают к “бабушкиному средству” – подышать горячим паром над кастрюлей с водой, закрывшись при этом с головой полотенцем. Эта “технология” категорически противопоказана при температуре, гнойных процессах в рото- и носоглотке, склонности к кровотечениям, гипертонии и хронических заболеваниях легких, предупреждает врач-оториноларинголог, руководитель клиники лор-заболеваний, кандидат медицинских наук Эдуард Маслов. Он также напоминает, что процедура чревата опасностью ожога слизистых, а также всего тела: в его практике были случаи, когда кастрюля с кипятком опрокидывалась на простуженного ребенка.
Но даже если вышеупомянутых противопоказаний ингаляциям нет и процедура проводится специальным прибором – ингалятором или небулайзером, – она может стать причиной весьма нежелательных, а порой и опасных ситуаций.
– Ларингоспазм. Раздражение лекарством может вызвать спазм гортани, остановку дыхания и – если скорая не успеет – летальный исход.
– Дыхательная недостаточность. Если легкие заполнены слизью – а именно так проявляет себя, например, COVID-19, а мы вдыхаем вещества, которые способствуют еще большей ее выработке, – то количество дыхательной ткани, не заполненной жидкостью, сокращается до критического.
– Аллергическая реакция. Возникает чаще всего на растительные препараты или травяные отвары. Одним подышать над ромашкой – облегчения, а другим понадобится скорая помощь.
– Потеря сознания. Этим эффектом чревата как раз технология “подышать над кастрюлей”.
И еще несколько простых советов:
1. Ингаляцию можно проводить спустя час после приема пищи.
2. Использовать для нее специальные приборы, а не кастрюлю.
3. Добавлять лекарства в паровую ингаляцию можно только после консультации с врачом. Безопасен только физраствор – увлажнение слизистой всегда полезно.
Особенности использования небулайзера
Небулайзер — это аппарат, необходимый для того, чтобы проводить ингаляции. Он нашел широкое применение. С его помощью лечат заболевания дыхательных путей. При этом возраст человека не имеет значения.Аппарат годится хоть для новорожденного ребенка, хоть для пожилого человека. В настоящее время такие приборы есть у многих в доме. Особенно часто они встречаются у тех, у кого есть маленький ребенок.
Одна из проблем в использовании этого прибора заключается в том, что некоторые заправляют небулайзер любой жидкостью. Это серьезная ошибка. Вот почему цель этой статьи заключается в том, чтобы объяснить, что можно наливать в небулайзер, а что нельзя.
Что такое небулайзер?
Небулайзер — это устройство для аэрозольной терапии. Оно может преобразовать лекарственные препараты в мельчайшие частицы. В результате вещество оказывается во всех органах дыхательной системы, а потом быстро усваивается.
Небулайзер — это не обычный ингалятор. Ведь он превращает вещество в мелкую дисперсную взвесь. Причем по своей структуре она очень напоминает облако или туман.
Небулайзеры можно и нужно применять, когда необходимо осуществить точечную «доставку» медикаментов в нижние отделы органов дыхания. Аппарат создает облако целебного вещества не за счет пара, как это происходит в паровом ингаляторе.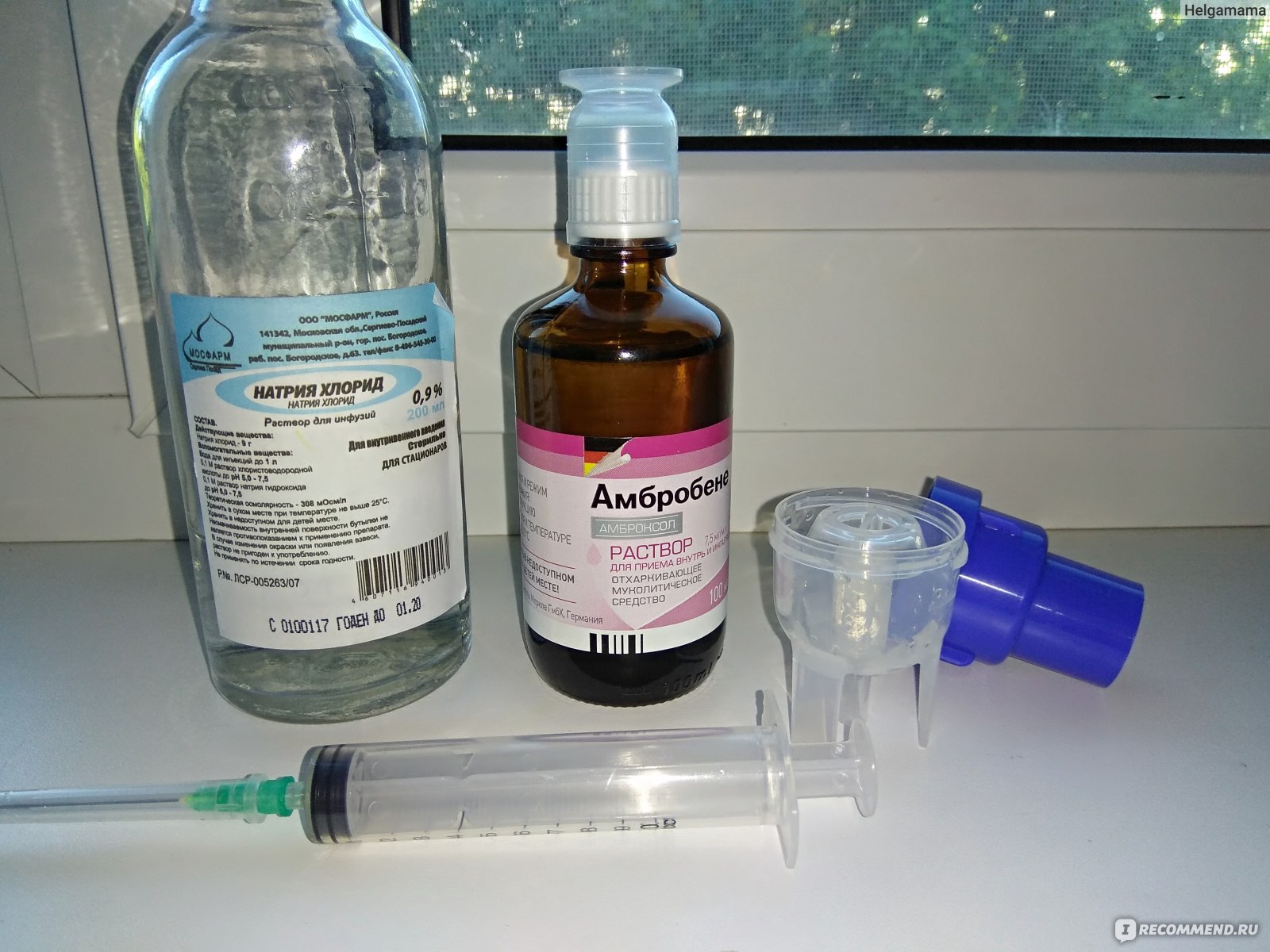
ВАЖНО! Данное устройство можно применять человеку в любом возрасте. Причем не только в стационаре, но и на дому.
Принцип работы небулайзера
Когда небулайзер несет пользу? Если есть необходимость доставить лекарство только в дыхательные пути, то лучше всего его вводить через ингалятор. В этом случае оно будет намного эффективнее. Ко всему оно будет сопровождаться меньшей частотой побочных эффектов, чем в том случае, когда прием/введение осуществляется внутрь.В составе небулайзера есть:
– компрессор,
– стаканчик для лекарства,
– маска,
– соединяющие трубки.
Образование мельчайшей воздушной взвеси осуществляется, когда воздух и лекарства силой большого давления продвигаются через крохотное отверстие.
Вместо компрессора может применяться источник ультразвука. Тогда дробление осуществляется без давления и потому бесшумно. Отметим при этом, что ультразвук способен разрушить некоторые препараты. Скажем, стероиды. Вот почему он удобен далеко не в каждом случае.
Что нельзя использовать в небулайзере?
– ВОДА
Есть среди нас такие, которые ошибочно считают, что не произойдет ничего страшного, когда добавишь в небулайзер обычную воду. Делать этого нельзя! Ведь вода, в которой много всяких примесей и ненужных микроорганизмов, направляется напрямую в наши легкие. Это ухудшает состояние здоровья. Более того, это может привести к другим заболеваниям.
– СИРОПЫ
Сиропы принимают внутрь организма. А когда они применяются в небулайзере, то попадают в легкие. Не только действующее вещество попадает на дыхательные пути, но и сахар и дополнительные вещества, которые не нужны. И потому сиропы применять в небулайзерах нельзя.
– ОТВАРЫ И НАСТОИ ТРАВ
Не наливайте в небулайзер отвары и настои трав, если в них есть взвесь любой фракции или мусор, который можно увидеть даже невооруженным глазом.
В составе любого препарата, например, ромашки, даже когда он прошел тщательную очистку, есть эфирные масла. Их много. И, если они попадут в легкие, то возможна жировая инфильтрация, пневмония и даже летальный исход.
ВАЖНО! Ко всему использованные в небулайзере настои и отвары трав, также оседают в легких и бронхах. В результате они вызывают развитие заболеваний дыхательных путей.
– ГОРЯЧИЕ ЖИДКОСТИ
Для того, что небулайзер правильно работал, жидкость не нужно нагревать. Ведь аппарат предназначен для того, чтобы преобразовать жидкое лекарство в аэрозоль. Если температура раствора повысится, то возможно, что разрушатся активные компоненты, а теплый пар распространит инфекцию. И тогда усилится воспалительный процесс, будут осложнения. Горячим воздухом можно даже обжечься, если вдохнешь пар.Медики и поныне ведут полемику о том, как нужно применять минеральную воду в небулайзере. Большинство считает, что ее нельзя использовать. С точки зрения одних, от такой процедуры просто не будет пользы. С точки зрения других, соли, которые входят в состав минеральной воды, вредны.
Нет специальной минеральной воды для ингаляций. Наливать в небулайзер физраствор или минералку – это значит то же самое, что и заправлять автомобиль овсом и сеном.
– ФИЗРАСТВОР
Немало педиатров, которые уверены, что применять физраствор в небулайзере можно. Он якобы не представляет опасности. Даже для детей. Однако с какой целью проводится такое лечение? Перевести сухой кашель во влажный? Сделать лучше отхождение мокроты? В таком случае не лучше ли просто увлажнить воздух в комнате?
ВАЖНО! Основная задача физраствора — разбавить более сложные лекарств. Ко всему, если применять медикаменты комплексно, то эффект будет максимальный.
Исключаем эфирные и косметические масла
Строго запрещено использование в небулайзерах эфирных и косметических масел. Проблема в том, что маслянистая жидкость в аппарате дробится на мельчайшие частицы, и они могут пробиваться в самые отдаленные участки дыхательных путей. Когда они попадают в бронхи, то появляется отек либо спазм легких, пневмония.
Проблема в том, что маслянистая жидкость в аппарате дробится на мельчайшие частицы, и они могут пробиваться в самые отдаленные участки дыхательных путей. Когда они попадают в бронхи, то появляется отек либо спазм легких, пневмония.
Нельзя заливать эфирное масло в небулайзер! Под давлением потока воздуха или ультразвуком масло разбивается на мелкие капли. Масло равномерно ложится на мелкие бронхи. В результате механическая закупорка, после которой бывает отек легких. Ко всему становится невозможен газообмен.
Смерь ребенка может наступить очень быстро. Так быстро, что бригады скорой медицинской помощи может и не успеть.
У масел ярко выраженный резкий запах, и потому у детей часто бывает ларингоспазм. Они же могут стать причиной развития аллергии.
ВАЖНО! Также применение масел в небулайзере может привести даже к тому, что аппарат сломается. Когда небулайзер не способен разделить основу на мелкие частицы, тогда он забивается и отказывается функционировать.
Специализированные препараты для небулайзера
Фармацевтические компании для применения в небулайзерах выпускают специальные лекарственные препараты. Они предназначены для небулайзерной терапии и стерильны, поскольку проникают глубоко в дыхательные пути.У препаратов для небулайзеров широкий спектр действия:
– муколитики и мукорегуляторы для разжижения мокроты и улучшения отхаркивания;
– М-холинолитики с бронхорасширяющим эффектом.
В небулайзерах еще применяют комбинированные лекарственные препараты:
– для терапии бронхообструктивного синдрома;
– средства противокашлевые и антигистаминные;
– препараты легочного сурфактанта;
– стимуляторы дыхания;
– средства противотуберкулезные и антимикробные.
Далеко не каждое лекарство подходит для применения с помощью небулайзеров.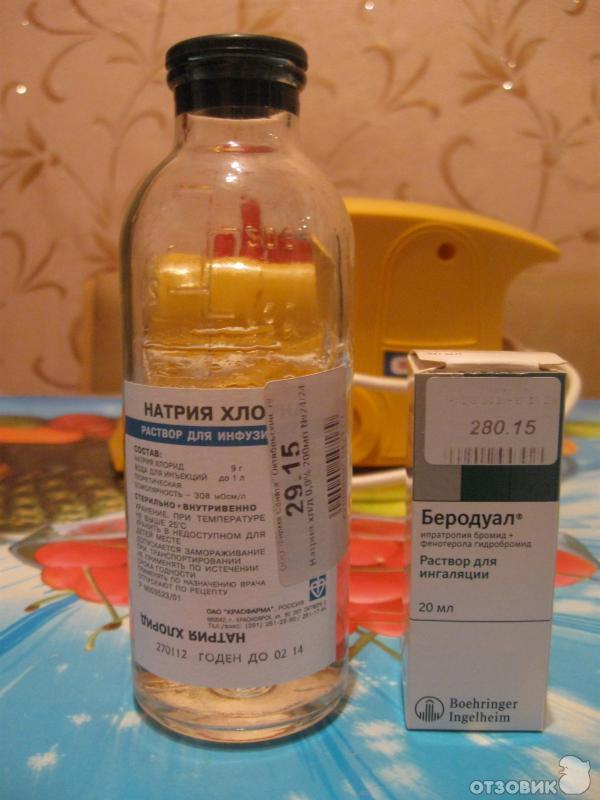 Помните, что лишь специалист может назначить соответствующую терапию и выбрать необходимый медикамент. Именно тот, который должен быть предназначен только для дыхательных путей.
Помните, что лишь специалист может назначить соответствующую терапию и выбрать необходимый медикамент. Именно тот, который должен быть предназначен только для дыхательных путей.
Как использовать небулайзер?
Сборка небулайзера осуществляется чистыми руками. Положите его на твердую поверхность. Проверяем чистоту воздушного фильтра. Если он грязный, то промойте его холодной водой. Потом просушите на воздухе. Подключаем аппарат к розетке.– Когда препарат уже упакован в нужном разведении, нужно лишь вскрыть небулу и выдавить в стаканчик содержимое. Когда препарат необходимо смешать с другим, то это делаем пипеткой или шприцем.
– Если надо, то добавляем изотонический раствор. Есть такие лекарства, которые нужно разводить. Разводят лишь физраствором, который должен быть стерильным. Приготовленный в домашних условиях солевой раствор в небулайзере использовать нельзя!
– Подсоединяем стаканчик к трубке от аппарата. Сверху прикрепляем маску. Взрослому необходимо взять трубку-мундштук в губы. Младенцу и ребенку маску прикладывают к лицу. Пока ребенок дышит ингаляторной взвесью, его нужно развлекать.
ВАЖНО! Теперь включаем аппарат. Держим стаканчик вертикально. Обычно на процедуру уходит 8-10 минут. Если пар перестанет идти, значит, препарат в стаканчике закончился. Процедура подошла к концу.
Достоинства и недостатки небулайзера
Можно смешивать разные препараты. Если надо, то их можно вводить в очень высоких дозах. Лекарства доставляются при обычном дыхании, без синхронизации с вдохом. Это очень удобно для ребенка. Таковы основные плюсы. Но!
ВАЖНО! Аппарат шумный. Ему нужен источник электроэнергии. Покупка его обходится дороже, чем покупка карманного дозированного ингалятора. В уходе он очень трудоемкий. Маску и стаканчик нужно постоянно обрабатывать.
Есть и другие минусы. Не каждое лекарство годится для применения через небулайзер. Применение небулайзера иногда раздражает дыхательные пути. Если дезинфекция недостаточная, то это может привести к бактериальному заражению и инфекции дыхательных путей.
Применение небулайзера иногда раздражает дыхательные пути. Если дезинфекция недостаточная, то это может привести к бактериальному заражению и инфекции дыхательных путей.
6 ошибок при использовании небулайзера
Что такое небулайзер? Это устройство для непосредственного введения лекарственных препаратов в дыхательные пути.
Небулайзер предназначен для людей с астмой или другими обструктивными заболеваниями легких. Такой ингалятор превращает жидкое лекарство в пар, который человек может вдыхать через маску или мундштук. Лекарство, принятое подобным образом, попадает прямо в дыхательные пути и действует там, где это необходимо.
Правильная техника ингаляций – залог успешного лечения обструктивных патологий легких. Но, используя небулайзер, пациенты нередко делают ошибки.
Разберемся, как их избежать.
⛔ Ошибка 1: использование мундштука, а не маски при ингаляции у детей младшего возрастаОчень важно использовать у детей до 5 лет именно маску. Причина в том, что малыши не всегда могут придерживаться правильной техники ингаляции и сделать вдох ртом, как того требует мундштук.
Именно маска поможет обеспечить оптимальную концентрацию лекарства для купирования у маленьких детей воспалительного процесса в нижних дыхательных путях.
⛔ Ошибка 2: маска отдельно, ребёнок отдельноПри правильной технике ингаляции маска должна плотно прилегать к лицу ребёнка. Иначе эффективность процедуры снижается.
⛔ Ошибка 3: использование растворов, не предназначенных для небулайзераКонечно, обеспечить правильную технику ингаляции у детей младшего возраста достаточно сложно, но за этим важно следить.
Раствор для небулайзерной терапии всегда выпускается формах, обеспечивающих его стерильность: в небулах или ампулах. Нестерильные растворы использовать нельзя.
Нестерильные растворы использовать нельзя.
Необходимо использовать только препараты, на которых указано, что они подходят для небулайзерной терапии. Но для ингаляции часто используют минеральную воду, в стерильности который нельзя быть уверенным.
Более того: не существует подтверждения эффективности щелочного раствора в лечении патологии лёгких, а поэтому минеральную воду не стоит использовать для ингаляций. Её нужно пить.
То же касается соды: добавление ее в воду как раз и создает щелочной раствор, эффективность действия которого научно не доказана.
Также не существует подтверждений эффективности использования для небулайзера антисептиков, например декаметоксина. Более того – они могут вызывать ожоги слизистой.
Категорически запрещено использовать для небулайзерной терапии масляные растворы, отвары трав, препараты системного действия.
В результате использования масляных растворов на стенках бронхов и альвеол оседает масло, нарушающее газообмен. Это может привести к очень тяжелым последствиям, например, масляной пневмонии или отеку легких.
Частицы трав и цветов из их отваров также могут глубоко оседать в дыхательных путях.
Помните: если дома есть небулайзер и нужно срочно его применить, лучше использовать обычный физраствор. Так шансы навредить будут минимальными.
⛔ Ошибка 4: нарушать время ингаляции и количество раствораВремя ингаляции напрямую зависит от скорости распыления раствора и скорости подачи аэрозоля, а также – от количества раствора в нем. Процедура в среднем должна длиться 10–15 минут.
Средний объем раствора, который используется за это время, – 4–6 мл. Поэтому нельзя лить в ингалятор меньше 4 мл раствора.
Для определения времени ингаляции и точного количества требуемого для одной процедуры раствора необходимо руководствоваться инструкцией к небулайзеру (или предписанием врача) и не нарушать их. Все эти параметры влияют на эффективность ингаляции.
Не рекомендуется делать ингаляцию через одну и ту же маску или мундштук всей семьей. Перед каждой процедурой маска, мундштук и другие принадлежности небулайзера должны быть продезинфицированы методом, предусмотренным в инструкции к прибору.
Оптимально, чтобы каждый член семьи имел индивидуальный набор аксессуаров к ингалятору. Ведь верхние дыхательные пути человека в норме содержат собственный микробиом, то есть комплекс микробов.
Вдыхание раствора, загрязненного микробными агентами предыдущего пользователя, способно вызвать развитие пневмонии и других заболеваний у следующего.
Особенно если речь идет об использовании одного небулайзера и насадок к нему взрослыми и детьми.
У взрослых микробиом, как правило, и более комплексный, и может содержать больше патогенной флоры. Вследствие общего использования трубки, маски, мундштука и других принадлежностей патогенная флора может передаться ребенку.
⛔ Ошибка 6: отменять ингаляции при повышенной температуре телаМелкодисперсный пар, который образовывается в компрессорном небулайзере, имеет комнатную температуру. Ингаляции с использованием прибора не повышают температуру тела, в отличие от паровых процедур.
Более того, необоснованная отмена ингаляций может привести к усилению отека слизистой и бронхоспазму и, как следствие, – к дыхательной недостаточности.
Общие представления о физрастворе, области его применения и значении
В современной медицине довольно широко применение физиологического раствора. Его используют для восполнения водного баланса, детоксикации, разведения лекарственных препаратов, промывания ран и т. д. Что же представляет из себя физиологический раствор? Какие виды физиологического раствора существуют? Как приготовить физраствор в домашних условиях? Как осуществляют ингаляции с физраствором? Ответы на данные вопросы вы сможете отыскать в настоящей статье.
д. Что же представляет из себя физиологический раствор? Какие виды физиологического раствора существуют? Как приготовить физраствор в домашних условиях? Как осуществляют ингаляции с физраствором? Ответы на данные вопросы вы сможете отыскать в настоящей статье.
Физиологический раствор
Под физиологическим раствором понимают водные растворы солей в такой концентрации, чтобы осмотическое давление раствора было равно внутриклеточному осмотическому давлению организма. Таким образом поддерживается баланс осмотического давления между раствором и тканями организма. Физиологический раствор еще называют изотоническим. В изотоническом растворе молекулы воды выделяются и поглощаются клеткой в равной мере, что обеспечивает нормальное ее функционирование. Помимо физиологического раствора существуют также гипертонический раствор с повышенным содержанием солей и гипотонический раствор с пониженным содержанием солей. Гипертонический раствор способствует выходу воды из клетки, а гипотонический раствор способствует накоплению жидкости в клетке.
Существует множество растворов, которые можно назвать физиологическими, но наиболее распространенным является раствор хлорида натрия в концентрации 0.9%. Данный раствор не содержит ничего кроме соли (хлорида натрия) и воды. Он представляет из себя бесцветную прозрачную жидкость слегка соленую на вкус.
Также в медицинской практике используют следующие физиологические растворы:
Данный раствор содержит несколько солевых компонентов, помимо дистиллированной воды в него входят хлорид натрия, хлорид калия, хлорид кальция. Благодаря многокомпонентной основе раствор Рингера более схож по электролитному составу с плазмой крови, чем простой водный раствор натрия хлорида 0.9%.
Данный раствор является модификацией раствора Рингера, к известному составу добавлены: глюкоза и гидрокарбонат натрия. Данный раствор регулирует не только водно-солевой баланс, но и кислотно-щелочное равновесие.
Данный раствор является модификацией раствора Рингера, к известному составу добавлены: дигидрофосфат натрия, хлорид магния, гидрокарбонат натрия, глюкоза. Данный раствор регулирует не только водно-солевой баланс, но и кислотно-щелочное равновесие.
Данный раствор схож по химическому составу с раствором Рингера-Локка, однако соли, входящие в его состав взяты в несколько иной концентрации.
Данные растворы имеют в своей основе водный раствор натрия хлорида, к которому добавлены некоторые виды солей: калия хлорид, гидрокарбонат натрия, натрия ацетат и др.
Все указанные солевые растворы изотоничны плазме крови человека, следовательно их можно называть физиологическими растворами.
Физраствор для детей
Как такового специфического физраствора для детей не существует. Осмотическое давление плазмы ребенка такое же, как и у взрослого, следовательно солевая концентрация физраствора для детей будет аналогична солевой концентрации физраствора для взрослых. Физраствор для детей применяется местно при насморке для осуществления промывания полости носа, глаз, ссадин, осуществления ингаляций. Внутрь физраствор для детей применяется при обезвоживании, диареи, отравлениях. Также возможно внутривенное введение физраствора в случаях, когда требуется быстро восстановить объем циркулирующей крови и при интоксикациях.
Физраствор для взрослых
Физраствор для взрослых используется при различных клинических состояниях. Местное использование физраствора для взрослых осуществляется при ингаляциях, промываниях полости носа, глаз, ссадин. Применение физраствора для взрослых внутрь используется при отравлениях, легкой степени обезвоживания, диареи. Также возможно внутривенное введение физраствора в случаях, когда требуется быстро восстановить объем циркулирующей крови и при интоксикациях. Физраствор используется как растворитель для некоторых лекарственных препаратов, приготовления капельниц, растворов для инъекций.
Физраствор пропорции
Для каждого из физиологических растворов существует индивидуальные пропорции.
Самый простой и часто используемый физраствор содержит хлорид натрия в пропорции 0.9%. Такая концентрация соли считается оптимальной для поддержания изотоничности раствора.
Физраствор Рингера имеет более сложную структуру и содержит соли в следующей пропорции (на 1 литр раствора):
- Хлорид натрия – 8.6 грамм
- Хлорид калия – 0.3 грамм
- Хлорид кальция – 0.33 грамм
Данная пропорция может видоизменяться в зависимости от добавок, входящих в физраствор. Пропорция солей в растворах на основе раствора Рингера также различна, однако итоговое осмотическое давление в готовом растворе является изотоничным.
Как приготовить физраствор в домашних условиях
Проще всего приготовить физраствор в домашних условиях на основе хлорида натрия, или поваренной соли. Для приготовления одного литра физиологического раствора нам потребуется 9 грамм соли и литр воды. Данная соль продается в любом магазине и цена ее невелика. Воду рекомендуется прокипятить перед приготовлением раствора. Соль растворяется в воде достаточно быстро. Получившийся физраствор годен только для местного применения и для приема внутрь. Для осуществления внутривенных инъекций такой раствор не годится, для этого необходимо использовать стерильный апирогенный физраствор.
В ряде случаев можно приготовить многокомпонентный физраствор. Такие растворы применяются для приема внутрь в случае легкой степени обезвоживания организма (при поносах, рвоте, отравлениях). Состав их тоже достаточно прост.
Многокомпонентный физраствор, вариант 1 (на 1 литр воды)
- Хлорид натрия (поваренная соль) – 3.5 грамм
- Бикарбонат натрия (пищевая сода) – 2.5 грамм
- Хлорид калия – 1.
 5 грамм
5 грамм - Глюкоза – 20 грамм
Многокомпонентный физраствор, вариант 2 (на 1 литр воды)
- Хлорид натрия (поваренная соль) – 2.6 грамм
- Цитрат натрия – 2.9 грамм
- Хлорид калия – 1.5 грамм
- Глюкоза – 13.5 грамм
Многокомпонентный физраствор, вариант 3 (на 1 литр воды)
- Хлорид натрия (поваренная соль) – 3 грамм
- Сахар – 18 грамм
Данные многокомпонентные физиологические растворы способствуют эффективному восполнению потерянной жидкости.
Физраствор дозировка
Физраствор не токсичен и как таковой дозировки физраствора не существует. Однако в некоторых ситуациях (тяжелые отравления, кровопотеря, обезвоживание) необходимо осуществлять массивную внутривенную инфузию физраствором. В таких случаях важно соблюдать водный баланс в организме. Для осуществления контроля водного баланса необходимо учитывать объем использованного физиологического раствора, и объем мочи, выделенный пациентом после инфузии. Контроль водного баланса особенно важен при лечении детей младшего возраста. При отрицательном водном балансе (объем потребляемой жидкости меньше объема выделяемой) происходит обезвоживание организма. При положительном водном балансе (объем потребляемой жидкости больше объема выделяемой) может возникнуть отечный синдром.
Физраствор инструкция
Итак, физраствор, инструкция к применению (на примере раствора хлорида натрия 0.9%):
Регидратация (восстановление утраченной жидкости), дезинтоксикация, восстановление дефицита натрия. Также физраствор применяется в роли растворителя для многих лекарственных препаратов.
Физраствор выпускают в виде ампул, бутилированной или пакетированной жидкости.
Физиологический раствор применяют для восстановления утраченной жидкости, при гипонатриемии, как растворитель для различных лекарственных препаратов.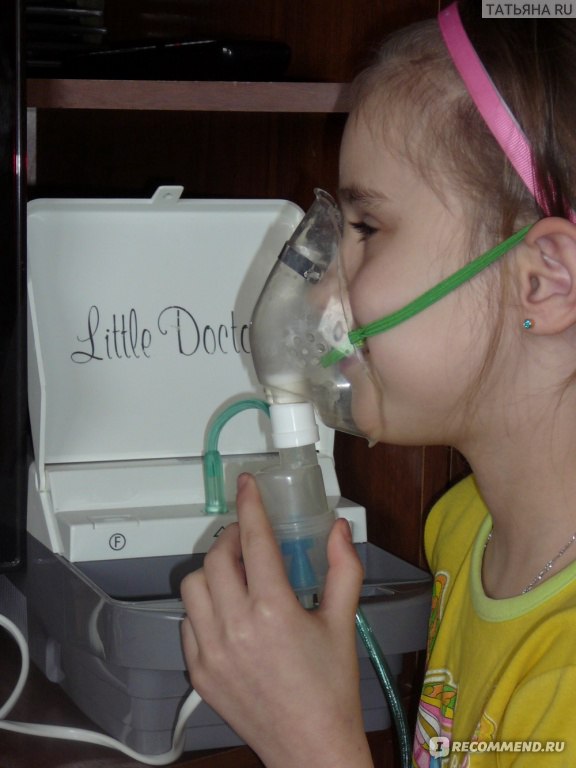
Высокий уровень натрия, хроническая сердечная недостаточность, почечная недостаточность, отек мозга, отек легких. С осторожностью физраствор применяют у больных артериальной гипертонией, отечным синдромом, лимфовенозной недостаточностью, альдостеронизмом.
Выше мы уже касались вопроса дозировки физиологического раствора. Уточним объемы внутривенных инфузий для пациентов. Физраствор для взрослых вводится в дозировке от 0.5 до 3 литров в сутки (в зависимости от показаний). Дозировка физраствора для детей рассчитывается из расчета на килограмм массы тела. Так средняя дозировка примерно равна 20-50 мл на 1 килограмм массы тела ребенка. Скорость введения физраствора определяется рядом факторов: состояния пациента, типом лекарственного препарата, растворенного в физрастворе.
Данное обстоятельство позволяет широко использовать физраствор в качестве растворителя для многих лекарственных препаратов.
-
Физраствор не оказывает побочного действия при беременности и кормлении грудью
-
Побочные явления при передозировке физраствора встречаются исключительно редко, однако могут быть явления гипергидратации (чрезмерное увеличение поступающей в организм жидкости), ацидоз, гипернатриемия.
Физраствор. Применение в медицине
Физраствор применяется в медицине повсеместно, ни одно отделение реанимации и интенсивной терапии не обходится без физраствора. Физиологический раствор является прекрасным растворителем для многих лекарственных препаратов, он используется для внутривенного, внутримышечного, подкожного, перорального введения лекарств.
Физраствор также применяют для восстановления водно-электролитного баланса организма. Дефицит жидкости (обезвоживание) в организме может наступить вследствие длительной рвоты, диареи, ожогов, интенсивного потоотделения, кровопотери, полиурии и других клинических состояний. Применение физраствора помогает компенсировать потерю жидкости и восстановить баланс электролитов.
Применение физраствора помогает компенсировать потерю жидкости и восстановить баланс электролитов.
Физраствор применяют для промывания полостей организма. При насморке и заложенности носа физраствором промывают полость носа, облегчая состояние пациента. При операциях на брюшной полости, например, при перитоните физраствор применяют для промывания брюшной полости. В ряде случаев физраствор используют для обработки раневых поверхностей. При отравлениях физраствор применяют для отмывания желудка, детоксикация осуществляется также путем внутривенного введения физраствора.
Физраствор для инъекций
Физраствор для инъекций чаще всего применяется как растворитель лекарственных препаратов. Физраствор для инъекций должен быть стерильным, о чем должна быть указана информация на упаковке. Не следует использовать физраствор для инъекций с истекшим сроком годности, с возникшим осадком или помутнением раствора, с поврежденной упаковкой.
Физраствор для инъекций производят в различных формах выпуска: пакеты, пластиковые бутылки, стеклянные банки, ампулы. Все зависит от области применения физраствора. Так, например, для массивной внутривенной инфузии используют пакеты или банки объемом 0.4-1 литр, для разовых инъекций и разведения лекарственных препаратов используют ампулы физраствора объемом 10 мл.
Физраствор для промывания носа
Использование физраствора для промывания носа является довольно эффективной процедурой, применение которой способствует разрешению различных видов насморка.
Физраствор для промывания носа не должен быть обязательно стерильным, его можно приготовить в домашних условиях, отмерив и размешав 9 грамм соли в 1 литре кипяченой воды. Используйте подогретый до 36 градусов физраствор, не следует хранить приготовленный физраствор более суток. Существуют различные способы промывания носа: при помощи шприца, особого чайничка или из собственной ладони. Смысл процедуры – достичь чистых промывных вод и облегчить носовое дыхание. Новорожденным осуществляют закапывание физраствора в нос при помощи пипетки.
Смысл процедуры – достичь чистых промывных вод и облегчить носовое дыхание. Новорожденным осуществляют закапывание физраствора в нос при помощи пипетки.
Из мер предосторожности можно рекомендовать постепенное вливание физраствора, строгое соблюдение пропорции соли при изготовлении в домашних условиях, используйте чистую кипяченую воду.
В аптеке можно приобрести готовые физрастворы для промывания носа (Аквалор, АкваМарис и др.).
Физраствор для небулайзера
В лечении заболеваний дыхательных путей высокую эффективность показывают ингаляции. Для осуществления ингаляций применяют специальный аппарат – небулайзер. Небулайзер – это специальное приспособление, которое превращает жидкость с растворенным в ней лекарством в аэрозоль, которую легко вдохнуть. Таким образом осуществляется ингаляционный способ введения лекарственных препаратов. В качестве универсальной жидкости, которая служит растворителем для многих лекарственных препаратов, выступает физиологический раствор. Небулайзер, в отличии от паровых ингаляторов, способен донести физраствор до бронхов. Паровой ингалятор преобразует физраствор в пар, который вдыхает пациент, а растворенный хлорид натрия при этом выпадает в осадок.
Физраствор для небулайзера наливают в специальную камеру, смешивая его с активным лекарственным компонентом. Иногда физраствор используют без добавления активных лекарственных веществ. При работе небулайзера образуется аэрозоль, которую вдыхает пациент. Аэрозоль при вдохе преимущественно поступает в нижние дыхательные пути (легкие и бронхи). Лечение заболеваний верхних дыхательных путей при помощи физраствора для небулайзера менее эффективно.
Физраствор для небулайзера обладает рядом полезных качеств:
- Разжижает мокроту и способствует ее выведению
- Защищает слизистую оболочку дыхательных путей от прямого воздействия лекарственных препаратов, «смягчает» их эффект
- Позволяет осуществить поступление активных лекарственных препаратов в нижние отделы дыхательных путей
В качестве активного лекарственного препарата, растворенного в физрастворе для небулайзера, могут выступать:
- Антибактериальные препараты.
 Способствуют подавлению патогенных микроорганизмов, применяются для лечения инфекционных заболеваний дыхательных путей.
Способствуют подавлению патогенных микроорганизмов, применяются для лечения инфекционных заболеваний дыхательных путей. - Расширяющие бронхи препараты, или бронхолитики. Способствуют расширению спазмированных бронхов, улучшают поступление воздуха к легким. Применяются для лечения бронхиальной астмы, обструктивных бронхитов и другой патологии дыхательных путей, сопровождающейся спазмом бронхов.
- Разжижающие мокроту, или муколитики. Способствуют разжижению и эвакуации скопившейся мокроты. Применяются в случае избыточной секреции вязкой мокроты, для разжижения и выведения мокроты.
Не следует добавлять в физраствор для небулайзера отвары из трав. В получаемом аэрозоле в таком случае будут содержаться частички растений, входящих в состав отвара, а это может повредить сам аппарат. Также в качестве добавок не следует применять масла. При вдыхании аэрозоля, содержащего масла, на слизистой оболочке может образовываться масляная пленка, препятствующая обмену кислорода между воздухом и легкими.
Физраствор при кашле
Физраствор при кашле применяют в качестве ингаляций. Нам уже известен такой прибор как небулайзер. Именно при помощи небулайзера и физраствора можно бороться с кашлем. Физраствор при помощи небулайзера преобразуется в аэрозоль, который вдыхает пациент. Аэрозоль способен проникать в нижние отделы дыхательной системы, где он оказывает лечебный эффект. Физраствор увлажняет слизистые бронхов, снижает их отечность, разжижает мокроту, облегчает дыхание.
Физраствор для небулайзера при кашле используют в педиатрической практике. При ингаляции через небулайзер не выделяется горячего пара, аэрозоль имеет комнатную температуру. Процедура проста в применении, не отнимает много времени, проводится в домашних условиях. Можно рассчитывать точную дозировку лекарственного препарата.
Физраствор при кашле используют при таких заболеваниях как:
Противопоказаниями к ингаляции физраствора при кашле могут быть:
- Кровотечение при кашле, кровь в мокроте
- Гнойный характер экссудата при воспалительных заболеваниях дыхательных путей
- Декомпенсированная легочная или сердечно-сосудистая патология
Перед использованием каких-либо лекарственных препаратов добавляемых в небулайзер, следует проконсультироваться с врачом специалистом.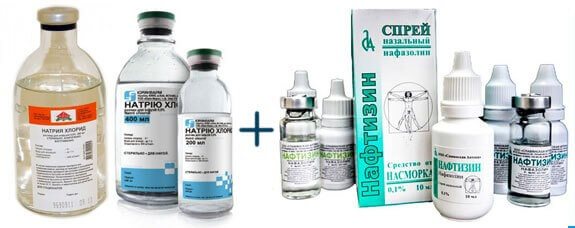 Не рекомендуется самостоятельно осуществлять лекарственные ингаляции без предварительной врачебной консультации.
Не рекомендуется самостоятельно осуществлять лекарственные ингаляции без предварительной врачебной консультации.
Лечение физраствором
Физраствор широко применяют в медицинской практике. Лечение физраствором осуществляют в случае:
Такая ситуация возникает при легкой кровопотере, рвоте, поносе и прочих состояниях, сопровождающихся обезвоживанием организма.
При отравлениях с целью снизить концентрацию токсических веществ в крови, за счет увеличения объема циркулирующей крови, применяют физраствор. Также для борьбы с интоксикацией применяют форсированный диурез. Суть метода состоит во внутривенном введении физраствора, после которого назначают диуретик. Данная процедура помогает выводить токсины с мочой. Метод эффективен только при нормальной функции почек.
Большинство капельниц и инъекций приготовляют на основе физраствра.
Физраствор применяют как нейтральную жидкость для обработки ран, в том числе во время хирургических вмешательств.
Ингаляциис физраствором способствуют выведению мокроты, увлажнению слизистых дыхательных путей, облегчению дыхания, противодействию кашлю.
Самый простой физраствор содержит ионы натрия и хлора, более сложные виды, например, раствор Рингера, содержат калий, магний и другие ионы.
Для осуществления массивных инфузий физраствора в условиях отделения реанимации может быть установлен центральный венозный катетер. При кровотечениях назначение физраствора необходимо, однако он не является средством выбора и его применение эффективно лишь при легкой степени кровопотери и в составе комплексной противошоковой терапии. Необходимо также контролировать водный баланс. Чрезмерное введение при лечении физраствора может способствовать развитию отеков, особенно это важно для пациентов с почечной патологией. Также с осторожностью следует вводить физраствор пациентам с заболеваниями сердечно-сосудистой системы, страдающим гипертонической болезнью.
Физраствор для ингаляций
Физраствор для ингаляций помогает бороться с мокротой, способствует ее эвакуации, увлажняет слизистые оболочки дыхательных путей, помогает бороться с кашлем. Для проведения ингаляций достаточно 2-4 мл физиологического раствора. Вся процедура не отнимает много времени и длится примерно 5 минут. Кратность применения физраствора для ингаляций составляет 1-2 раза в сутки. Возможно использовать физраствор в чистом виде. Данная процедура наиболее безопасна и проста в использовании. Также при различных заболеваниях в физрастворе для ингаляций возможно разведение лекарственных препаратов. Перед применением любого из лекарственных препаратов следует проконсультироваться с врачом.
Ингаляции с беродуалом и физраствором
Ингаляции с беродуалом и физраствором применяют для лечения спазма бронхов, хронической обструктивной болезни легких и бронхиальной астмы.
Беродуал является комбинированным препаратом, включающим 2 действующих компонента: фенотерол и ипратропия бромид.
Фенотерол воздействует на b2-адренорецепторы бронхов, тем самым расширяя их просвет. Ипратропия бромид также воздействует на гладкую мускулатуру бронхов, но не через адренорецепторы, а через м-холинорецепторы. Эффект ипратропия бромида также сводится к расширению бронхов. В комбинации 2 данных препарата оказывают выраженное бронхолитическое действие, воздействуя на гладкую мускулатуру бронхов с различных сторон.
Показания к применению беродуала:
- Бронхиальная астма
- Хроническая обструктивная болезнь легких
- Бронхоспазм
Противопоказания к применению беродуала:
- Аллергическая реакция на препарат
- Беременность и грудное вскармливание
- Заболевания сердечно-сосудистой системы (тахикардия, аритмии, кардиомиопатия, артериальная гипертензия)
- Закрытоугольная глаукома
- Тиреотоксикоз
Перед приемом беродуала следует проконсультироваться с врачом. Прием беродуала осуществляется при помощи небулайзера. Дозировку, которую подобрал лечащий врач, необходимо развести физиологическим раствором до 3-4 мл. Получившийся физраствор с беродуалом необходимо полностью использовать при помощи небулайзера. Разведение физраствора с беродуалом необходимо осуществлять непосредственно перед использованием и применять сразу после приготовления.
Прием беродуала осуществляется при помощи небулайзера. Дозировку, которую подобрал лечащий врач, необходимо развести физиологическим раствором до 3-4 мл. Получившийся физраствор с беродуалом необходимо полностью использовать при помощи небулайзера. Разведение физраствора с беродуалом необходимо осуществлять непосредственно перед использованием и применять сразу после приготовления.
К побочным эффектам применения физраствора с беродуалом относят:
Ингаляции с лазолваном и физраствором
Ингаляции с лазолваном и физраствором применяются для разжижения и эвакуации вязкой мокроты. Лазолван является отхаркивающим и муколитическим препаратом.
Показания к применению лазолвана:
Лазолван выпускают в виде различных форм: сироп, пастилки, таблетки, раствор для ингаляций. Действие лазолвана основано на увеличении образования железистого секрета клетками эпителия слизистой оболочки дыхательных путей, разжижении вязкой мокроты, повышении активности ресничного эпителия, способствующего ускорению эвакуации скопившейся мокроты.
Противопоказания к применению лазолвана:
- Аллергическая реакция на препарат
- Беременность и период грудного вскармливания
Лазолван также не рекомендуют принимать совместно с лекарствами, подавляющими кашель. Все дело в том, что кашлевой рефлекс способствует отхождению мокроты из дыхательных путей, подавление кашлевого рефлекса на фоне приема лазолвана может привести к нежелательным последствиям. Антибактериальные препараты лучше проникают в мокроту при совместном их назначении с лазолваном.
Передозировка лазолвана встречается довольно редко, ее симптомами могут быть тошнота, рвота, боль в животе, аллергические реакции. В случае возникновения подобных нежелательных реакций следует обратиться за медицинской помощью.
Для проведения ингаляций с лазолваном и физраствором необходимо иметь небулайзер. Пропорция разведения лазолвана с физраствором равна 1 к 1. В 1 мл раствора лазолвана содержится 7.5мг активного вещества. Осуществлять ингаляции лазолвана с физраствором необходимо в спокойной обстановке, дышать следует ровно, глубоко, желательно без кашля. Осуществлять разведение лазолвана с физраствором необходимо непосредственно перед самой процедурой ингаляции. Все емкости и сам небулайзер должны быть чистыми. Ингаляции следует проводить с периодичностью 2-3 раза в сутки. Пациентам, страдающим бронхиальной астмой перед процедурой ингаляции лазолвана с физраствором следует использовать бронхолитические препараты, чтобы избежать приступа астмы во время ингаляции.
Пропорция разведения лазолвана с физраствором равна 1 к 1. В 1 мл раствора лазолвана содержится 7.5мг активного вещества. Осуществлять ингаляции лазолвана с физраствором необходимо в спокойной обстановке, дышать следует ровно, глубоко, желательно без кашля. Осуществлять разведение лазолвана с физраствором необходимо непосредственно перед самой процедурой ингаляции. Все емкости и сам небулайзер должны быть чистыми. Ингаляции следует проводить с периодичностью 2-3 раза в сутки. Пациентам, страдающим бронхиальной астмой перед процедурой ингаляции лазолвана с физраствором следует использовать бронхолитические препараты, чтобы избежать приступа астмы во время ингаляции.
Ингаляция с физраствором для детей дозировка
Ингаляции с физраствором для детей могут применяться с раннего возраста. Перед ингаляцией следует подогреть физраствор до температуры 370С, не следует использовать холодный физраствор. Дозировка физраствора в среднем составляет 2-4 мл, он заливается в специально предназначенную камеру. Продолжительность ингаляций для детей не должна превышать 3 минут. Кратность проводимых ингаляций в среднем составляет 2-4 раза в день в зависимости от показаний. Сама процедура ингаляций с физраствором для детей подразумевает соблюдение ряда рекомендаций:
- Все используемые для ингаляции приспособления должны быть чистыми
- После ингаляции следует тщательно помыть используемые для ингаляции приспособления
- Желательно проводить ингаляции спустя час после еды
- После ингаляции желательно в течение часа не выходить на улицу
- Процедура ингаляции должна проводиться в спокойных условиях, ребенок не должен беспокоиться или бояться ингаляции
- При использовании небулайера дышать необходимо как обычно, без усилий
При использовании парового ингалятора существует ряд противопоказаний:
- Нельзя осуществлять ингаляцию посредством парового ингалятора детям до 4-х лет
- При возникновении лихорадки от ингаляций лучше воздержаться
- При возникновении гнойных осложнений воспалительных заболеваний дыхательных путей
Разведение любых лекарственных препаратов с физраствором для ингаляций допустимо только после врачебной консультации. Во всех случаях назначения лекарственного препарата дозировка и кратность приема подбирается индивидуально в зависимости от показаний.
Во всех случаях назначения лекарственного препарата дозировка и кратность приема подбирается индивидуально в зависимости от показаний.
Пропорции физраствора для ингаляции
Для ингаляций используют физраствор в чистом виде в объеме 2-4 мл. В некоторых случаях для достижения желаемого эффекта в фирастворе растворяют лекарственный препарат. Пропорции разведения лекарственных препаратов рассчитываются индивидуально. Приведем примеры некоторых препаратов, применяемых вместе с физраствором для ингаляций.
- Антибиотики могут быть использованы при воспалительных заболеваниях дыхательных путей, вызванных патогенными микроорганизмами.
- Антисептические средства применяют с целью санации при воспалительных заболеваниях дыхательных путей
- Сосудосуживающие препараты применяют при отеке слизистой оболочки и как следствие затрудненном дыхании.
- Лазолван применяют в ингаляциях для улучшения отхождения вязкой мокроты. С физраствором данный препарат разводят в равной концентрации 1 к 1. Кратность приема детям до 6 лет составляет 1 раз в сутки. Старше 6 лет кратность составляет 2 раза в сутки, используется 2 мл раствора.
- Амброгексал применяют для ингаляций пациентам старше 5 лет, на 4 мл физраствора используют 2-3 капли препарата
- Амбробене с физраствором смешивают в равной пропорции. Детям до 2 лет показан 1 мл раствора, старше 2 летнего возраста назначают по 2 мл раствора
- Беродуал разводят с физраствором исходя из индивидуальных показаний. При расчете пропорций следует помнить что 20 капель беродуала по объему равны 1 мл.
При использовании разведенного физраствора и лекарственного препарата следует помнить, что получившийся раствор всегда используют полностью. Не допускается использовать для растворов обычную или дистиллированную воду. Растворы приготовляют непосредственно перед использованием.
Пульмикорт с физраствором
Пульмикорт является препаратом из группы кортикостероидов, его применяют для лечения обструктивных бронхитов, бронхоспазмов и бронхиальной астмы.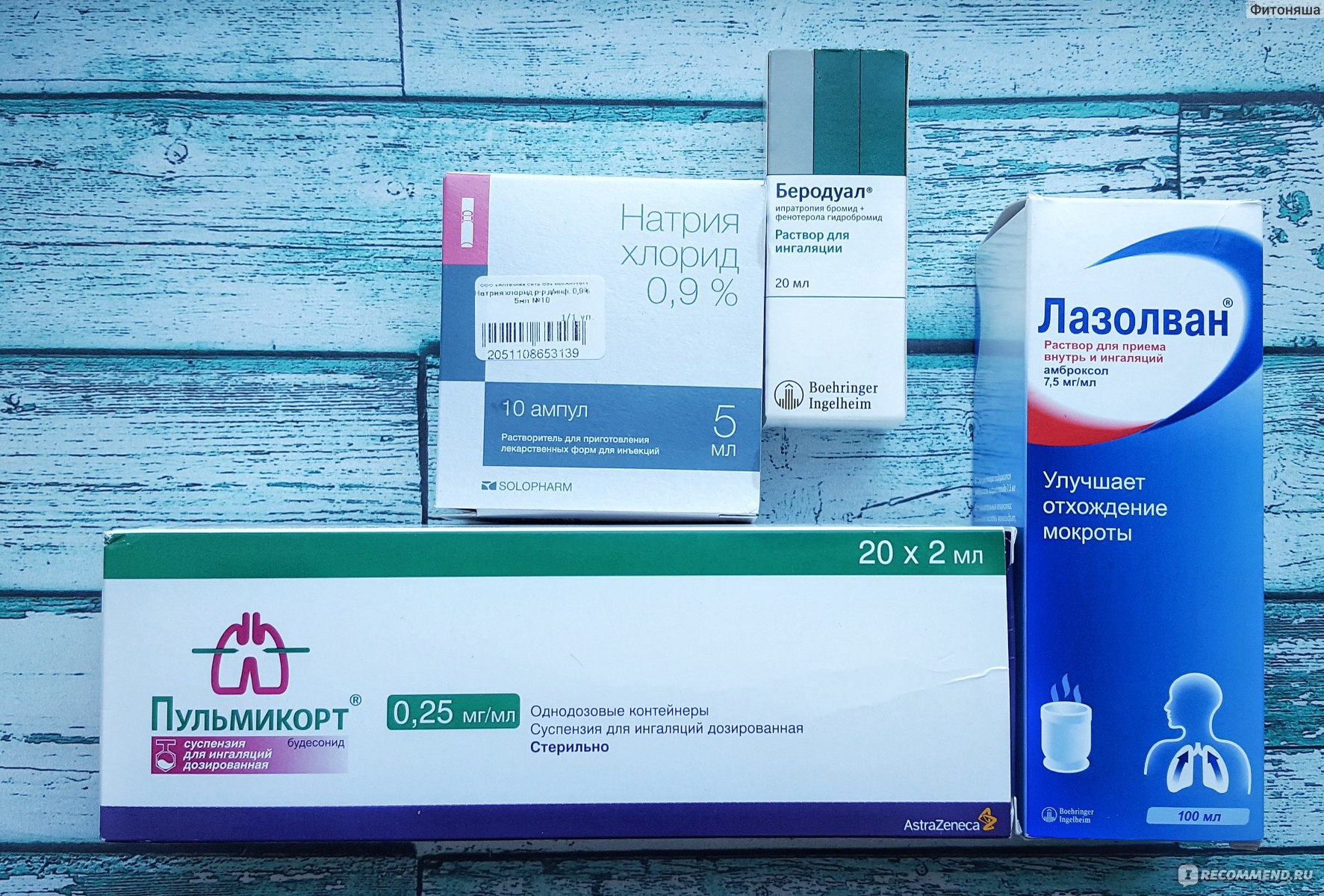 Пульмикорт расширяет бронхи, ликвидирует аллергический и воспалительный процессы.
Пульмикорт расширяет бронхи, ликвидирует аллергический и воспалительный процессы.
Показания к приему препарата пульмикорт:
- Бронхиальная астма
- Поллиноз
- Хроническая обструктивная болезнь легких
- Ларингит
Противопоказания к приему препарата пульмикорт:
- Возраст до 6 месяцев
- Туберкулез в активной форме
- Цирроз печени
- Активные грибковые и бактериальные инфекции дыхательных путей
- Непереносимость действующего вещества «будесонид»
Правила применения пульмикорта с физраствором при помощи небулайзера:
- Непосредственно перед ингаляцией производят разведение суспензии пульмикорта с физраствором, разбавленную суспензию необходимо использовать в течение получаса
- Дыхание необходимо осуществлять спокойно и ровно
- После дыхательной процедуры необходимо прополоскать рот теплой водой. Пульмикорт может подавлять местный иммунитет слизистой ротовой полости, что приводит к развитию кандидоза. Если была использована лицевая маска, то следует умыть лицо после процедуры.
- После использования небулайзер необходимо помыть и высушить.
- При приеме пульмикорта необходимо тщательно соблюдать инструкцию, прилагаемую к препарату. Перед приемом пульмикорта следует проконсультироваться с врачом.
Является ли распыленный физиологический раствор плацебо при ХОБЛ? | BMC Pulmonary Medicine
Обследовано 40 пациентов во время госпитализации по поводу обострения ХОБЛ. Пациентов набирали в то время, когда их состояние стабилизировалось перед запланированной выпиской из больницы. Клинические данные пациентов приведены в таблице 1. Шесть пациентов прошли обе конечности исследования (частичный перекрестный дизайн).
Таблица 1 Характеристики пациента Пациенты были рандомизированы для получения 4 мл 0. 9% физиологический раствор с использованием эффективной системы распылителя (активная группа) или неэффективной системы распылителя (группа плацебо). Активным небулайзером был небулайзер System 22 Acorn (Medic-Aid, Bognor Regis UK Ltd), приводимый в действие системой подачи кислорода по трубопроводу больницы со скоростью потока 9 л / мин в течение 10 минут. Было обнаружено, что эта распылительная система доставляет 95% частиц размером от 2,5 до 2,8 микрон с использованием лазерной системы Malvern. (Измерения любезно предоставлены доктором Стивом Ньюманом, главным физиком Королевской бесплатной больницы, Лондон, Великобритания).Этот небольшой размер частиц был выбран для достижения эффективной доставки в дыхательные пути. Небулайзер для плацебо представлял собой небулайзер Bard Inspiron старой модели (1980-е гг.) (Более не выпускаемый), приводимый в действие кислородом со скоростью потока 3 л / мин. Эта система распылителя доставляла 95% частиц размером от 9,5 до 9,9 микрон. Этот размер частиц был выбран для достижения эффекта плацебо с отложением в трубках системы и в глотке, но с небольшим проникновением в дыхательные пути [12]. Оба небулайзерных препарата вводились через мундштук, чтобы избежать отложения капель физиологического раствора в носу и снизить вероятность того, что пациенты заметят, что результат от системы плацебо отличается от предыдущего распыленного лечения, которое они получали.
9% физиологический раствор с использованием эффективной системы распылителя (активная группа) или неэффективной системы распылителя (группа плацебо). Активным небулайзером был небулайзер System 22 Acorn (Medic-Aid, Bognor Regis UK Ltd), приводимый в действие системой подачи кислорода по трубопроводу больницы со скоростью потока 9 л / мин в течение 10 минут. Было обнаружено, что эта распылительная система доставляет 95% частиц размером от 2,5 до 2,8 микрон с использованием лазерной системы Malvern. (Измерения любезно предоставлены доктором Стивом Ньюманом, главным физиком Королевской бесплатной больницы, Лондон, Великобритания).Этот небольшой размер частиц был выбран для достижения эффективной доставки в дыхательные пути. Небулайзер для плацебо представлял собой небулайзер Bard Inspiron старой модели (1980-е гг.) (Более не выпускаемый), приводимый в действие кислородом со скоростью потока 3 л / мин. Эта система распылителя доставляла 95% частиц размером от 9,5 до 9,9 микрон. Этот размер частиц был выбран для достижения эффекта плацебо с отложением в трубках системы и в глотке, но с небольшим проникновением в дыхательные пути [12]. Оба небулайзерных препарата вводились через мундштук, чтобы избежать отложения капель физиологического раствора в носу и снизить вероятность того, что пациенты заметят, что результат от системы плацебо отличается от предыдущего распыленного лечения, которое они получали.
Исследование проводилось слепым методом. 40 листов бумаги были помечены как «Обработка A» или «Обработка B» и помещены в непрозрачные коричневые конверты. Они были перемешаны в случайном порядке, и каждому пациенту было предложено выбрать один конверт. Затем исследователь открыл его и назначил соответствующее лечение (активный А, плацебо В). Для шести пациентов, которые принимали участие в исследовании дважды, второе лечение состояло из того лечения, которое они не получали ранее.
Пациентам сказали, что мы хотели «понаблюдать за эффектами небулайзерного лечения, которое не является новым или экспериментальным лекарством». Они не были проинформированы о точном характере лечения с помощью распыления, поскольку это могло побудить пациентов попытаться угадать, было ли полученное лечение «плацебо». Комитет по этике согласился с тем, что было бы невозможно измерить истинный эффект плацебо, если бы пациенты были осведомлены о том, что оба препарата были физиологическим раствором (не бронходилататором), а один из небулайзеров был намеренно сделан неэффективным.
Они не были проинформированы о точном характере лечения с помощью распыления, поскольку это могло побудить пациентов попытаться угадать, было ли полученное лечение «плацебо». Комитет по этике согласился с тем, что было бы невозможно измерить истинный эффект плацебо, если бы пациенты были осведомлены о том, что оба препарата были физиологическим раствором (не бронходилататором), а один из небулайзеров был намеренно сделан неэффективным.
Пациенты были набраны в респираторные отделения университетской больницы. Мы набрали пациентов, у которых диагноз ХОБЛ был подтвержден консультантом по респираторным заболеваниям (пациенты с астмой или бронхоэктазами были исключены из исследования). К пациентам обратился один из исследователей, пока они находились в относительно стабильной фазе перед выпиской из больницы после госпитализации с обострением ХОБЛ. Все тесты проводились между 12.00 и 16.00, по крайней мере, через четыре часа после лечения бронходилататорами.
Перед участием в исследовании пациенты дали информированное согласие и провели базовое измерение ОФВ1 и ФЖЕЛ, используя лучший из трех ударов на спирометре Microlab 3300 (Micro-Medical LTD, Рочестер, Великобритания. Измеряли пиковую скорость выдоха (PEF) с использованием пикового расходомера Райта. Каждый пациент также записывал оценку своего воспринимаемого уровня одышки с использованием модифицированной семибалльной шкалы Лайкерта (1 = не одышка, 2 = очень легкая одышка, 3 = легкая одышка, 4 = умеренная одышка, 5 = Сильная одышка, 6 = очень сильная одышка, 7 = наихудшая возможная одышка).
Через десять минут после завершения небулайзерной терапии были повторены измерения FEV1, FVC и PEF, а также субъективная оценка одышки. Пациенты также регистрировали субъективную оценку пользы, используя следующую модифицированную шкалу Лайкерта. (1 = Нет пользы от этого лечения, 2 = Очень незначительное улучшение, 3 = Незначительное улучшение, 4 = Умеренное улучшение, 5 = Хорошая польза, 6 = Очень хорошая польза, 7 = Максимально возможная польза).
Затем пациенты получили 4 вдоха сальбутамола (400 мкг) с использованием дозированного ингалятора и 750 мл спейсера Volumatic (Glaxo Smith Kleine UK).
Через пятнадцать минут были повторены измерения FEV1, FVC и PFR, а также баллы субъективной одышки и баллы облегчения симптомов.
Все данные были введены в статистический пакет SPSS версии 9. U-критерий Манна-Уитни использовался для сравнения тестов функции легких и оценки облегчения симптомов. Тест Wilcoxon Signed Rank использовался для сравнения изменения показателей одышки для согласованных пар до и после распыления физиологического раствора.
Исследование было одобрено Комитетом по этике исследований Салфорда и Траффорда.Все пациенты дали письменное информированное согласие на участие в исследовании и на получение однократной дозы распыленного препарата (в дополнение ко всему обычному лечению).
Небулайзерный физиологический раствор может служить активным средством лечения острого вирусного бронхиолита
8 января 2020
2 мин чтения
ДОБАВИТЬ ТЕМУ В ОПОВЕЩЕНИЯ ПО ЭЛЕКТРОННОЙ ПОЧТЕ
Получать электронное письмо, когда новые статьи публикуются на
Укажите свой адрес электронной почты, чтобы получать сообщения о публикации новых статей.Подписаться Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, обратитесь по адресу [email protected].Вернуться в Healio
Недавний метаанализ, опубликованный в JAMA Pediatrics , предполагает, что небулайзерный физиологический раствор может рассматриваться как активное лечение в отличие от плацебо в исследованиях, оценивающих методы лечения острого вирусного бронхиолита у детей младшего возраста.
«В большинстве рандомизированных клинических исследований небулайзерный физиологический раствор используется в качестве плацебо, что логично, учитывая, что физиологический раствор также используется в качестве носителя для распыления активного лечения. Однако в исследованиях бронходилататоров было отмечено последовательное улучшение показателей, превышающих ожидаемые, у пациентов, получавших плацебо », – пишут исследователи. «Растущий и убывающий характер бронхиолита может объяснить эти результаты, но, учитывая сильную тенденцию к улучшению, также возможно, что распыленный физиологический раствор действует как эффективное лечение.”
Для дальнейшего изучения этого вопроса исследователи отобрали 29 рандомизированных клинических испытаний с участием 1583 пациентов, в которых сравнивали детей в возрасте 2 лет и младше с бронхиолитами, получавших небулайзерный физиологический раствор. Исследования с группой лечения, получавшей альтернативное плацебо, также были включены для сравнения нормального физиологического раствора с другими плацебо. Затем исследователи изучили объединенные оценки связи с респираторными баллами, частотой дыхания и насыщением кислородом в течение 60 минут после лечения распыленным физиологическим раствором по сравнению с другим плацебо и изменениями до и после распыления физиологического раствора.
В метаанализе три исследования включали сравнение распыленного физиологического раствора с не распыляемым плацебо. Результаты показали, что стандартизованные средние различия в респираторных показателях благоприятствовали группе нормального физиологического раствора по сравнению с другой группой плацебо на –0,9 балла (95% ДИ, –1,2–0,6) через 60 минут после терапии, без каких-либо значительных различий в частоте дыхания или кислороде. насыщение между физиологическим раствором и другими группами плацебо.
Двадцать пять исследований предоставили данные о совокупных респираторных показателях у пациентов, получавших небулайзерный физиологический раствор. В метаанализе исследователи обнаружили, что стандартизированная средняя разница в респираторных показателях после распыления физиологического раствора составляла –0,7 (95% ДИ, –0,7–0,6; I 2 = 62%).
В метаанализе исследователи обнаружили, что стандартизированная средняя разница в респираторных показателях после распыления физиологического раствора составляла –0,7 (95% ДИ, –0,7–0,6; I 2 = 62%).
Индекс оценки респираторного дистресса (RDAI), который был наиболее часто используемым показателем и единственным показателем, который использовался достаточно часто для выполнения сохраняющей шкалы анализа подгрупп, использовался в 13 исследованиях. При анализе этих исследований средневзвешенная разница в RDAI после распыления физиологического раствора составила -1.6 баллов (95% ДИ, от –1,9 до –1,3; I 2 = 72%).
Кроме того, средневзвешенная разница после распыления физиологического раствора составила -5,5 вдохов в минуту (95% ДИ, от -6,3 до -4,6; I 2 = 24%) в 17 исследованиях, предоставляющих информацию о частоте дыхания и взвешенных Средняя разница в насыщении кислородом после распыления физиологического раствора составляла –0,4% (95% ДИ, –0,6–0,2; I 2 = 79%) в 23 исследованиях, в которых были представлены данные о насыщении кислородом.
ПЕРЕРЫВ
Анализ чувствительности, удаляющий выбросы или исследования с высоким риском систематической ошибки, существенно не изменил точечные оценки, но в некоторых случаях снизил неоднородность.
«Этот метаанализ предполагает, что распыленный физиологический раствор может быть активным средством лечения острого вирусного бронхиолита, а не инертным плацебо», – писали они. «Необходимо провести дальнейшую оценку распыления физиологического раствора по сравнению с имитацией распыления и / или пероральным плацебо, чтобы установить, является ли распыленный физиологический раствор истинным плацебо.Планы будущих исследований должны учитывать потенциальный лечебный эффект распыленного физиологического раствора на краткосрочные результаты ». – Мелисса Фостер
Раскрытие информации s : Авторы не сообщают о раскрытии соответствующей финансовой информации.
ДОБАВИТЬ ТЕМУ В ОПОВЕЩЕНИЯ ПО ЭЛЕКТРОННОЙ ПОЧТЕ
Получать электронное письмо, когда новые статьи публикуются на
Укажите свой адрес электронной почты, чтобы получать сообщения о публикации новых статей.Подписаться Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, обратитесь по адресу [email protected].Вернуться в Healio
Распыленный гипертонический раствор против физиологического раствора у младенцев с острым бронхиолитом
Согласно исследованию, у младенцев с острым бронхиолитом, получавших небулайзерный гипертонический раствор, может наблюдаться сокращение продолжительности пребывания и улучшение показателей клинической тяжести, если они госпитализированы в стационаре, и у них снижен риск необходимости госпитализации при лечении в амбулаторных условиях или в отделении неотложной помощи. опубликовано в Кокрановской базе данных систематических обзоров .
Исследователи определили 17 рандомизированных и квази-рандомизированных контролируемых испытаний в параллельных группах, которые соответствовали критериям включения, и были добавлены к 11 испытаниям, включенным в обновление 2013 года, всего 28 испытаний, состоящих из 4195 участников. Основными результатами этого исследования были продолжительность госпитализации новорожденных с диагнозом острый бронхиолит и частота госпитализации младенцев, лечившихся амбулаторно или в отделении неотложной помощи, которые лечились гипертоническим солевым раствором (≥3%) по сравнению с небулайзерами 0.9% физиологический раствор.
Младенцы были разделены на группы в соответствии с процентным содержанием гипертонического раствора, который они получали. Качество исследований оценивалось с использованием 5 факторов подхода GRADE (ограничения исследования, постоянство эффекта, неточность, косвенность и систематическая ошибка публикации). Анализ подгрупп проводился на основе доступности данных (продолжительность пребывания в больнице, вирусология, верхние возрастные пределы, концентрация гипертонического раствора, интервал приема, совместное введение с бронходилататорами, продолжительность пребывания в контрольной группе, год публикации и риск систематической ошибки отбора) для оценки на неоднородность.
Анализ подгрупп проводился на основе доступности данных (продолжительность пребывания в больнице, вирусология, верхние возрастные пределы, концентрация гипертонического раствора, интервал приема, совместное введение с бронходилататорами, продолжительность пребывания в контрольной группе, год публикации и риск систематической ошибки отбора) для оценки на неоднородность.
Результаты исследования продемонстрировали статистически значимо меньшую продолжительность пребывания у младенцев, получавших небулайзерный гипертонический раствор, по сравнению с детьми, получавшими 0,9% физиологический раствор, со средней разницей (MD) –0,41 дня (95% ДИ, –0,75 до –0,07; P = 0,02; доказательства низкого качества). У младенцев, получающих лечение в амбулаторных условиях и в отделениях неотложной помощи, лечение гипертоническим раствором снижает риск госпитализации на 14% в целом (объединенный коэффициент риска [ОР] 0,86; 95% ДИ 0.76-0,98; P = 0,02; доказательства среднего качества). Гетерогенность была значительной в изученных стационарных исследованиях и умеренной в исследованиях амбулаторных больных и отделений неотложной помощи и сохранялась, несмотря на анализ подгрупп.
Баллы после ингаляции у младенцев, получавших небулайзерный гипертонический раствор, были статистически значимо ниже, чем у детей, получавших 0,9% физиологический раствор в течение 1, 2 и 3 дней лечения (MD –0,77; 95% ДИ, от –1,18 до –0,36; P ≤.001; MD, –1,28; 95% ДИ, от –1,91 до –0,65; P <0,001; MD, –1,43; 95% ДИ, от –1,82 до –1,04; P <0,001).
Вторичные результаты этого обзора показали, что у младенцев, получавших амбулаторное лечение (n = 65), показатели клинической тяжести были статистически значимыми в первый, второй и третий дни лечения у тех, кто получал 3% гипертонический раствор по сравнению с физиологическим раствором ( MD, –1,28; 95% ДИ, от –1,92 до –0,64; P <0,001; MD, –2,0; 95% ДИ, от –2,93 до –1,07; P <.001 и MD –2,64; 95% ДИ, от –3,85 до –1,43; P <0,001 соответственно). Также наблюдалось снижение клинической степени тяжести у младенцев, находящихся в стационаре, получавших гипертонический раствор (объединенный MD, –0,82; 95% ДИ, от –1,25 до –0,38; P = 0,005; I 2 = 67%), и 2 исследования лечения в отделениях неотложной помощи продемонстрировали превосходство гипертонического раствора над физиологическим раствором.
Также наблюдалось снижение клинической степени тяжести у младенцев, находящихся в стационаре, получавших гипертонический раствор (объединенный MD, –0,82; 95% ДИ, от –1,25 до –0,38; P = 0,005; I 2 = 67%), и 2 исследования лечения в отделениях неотложной помощи продемонстрировали превосходство гипертонического раствора над физиологическим раствором.
Частота повторной госпитализации не была значительно снижена у младенцев, получавших гипертонический раствор, а также не было никаких различий в частоте дыхания, продолжительности сердечного ритма при добавлении кислорода, потребности в дополнительном лечении или радиологических показателях у детей, получавших гипертонический раствор по сравнению с физиологическим раствором.По крайней мере, одно нежелательное явление было зарегистрировано в 11 из 24 исследований, в которых были представлены данные о безопасности. Нежелательные явления были легкими и разрешились спонтанно. В других 13 испытаниях о побочных эффектах не сообщалось.
Различия между испытаниями, опубликованными до 2013 г., и текущим обзором включали уменьшение вирусологических доказательств (86% и 30% испытаний, соответственно) и увеличение зарегистрированной средней продолжительности пребывания (0% и 40% испытаний соответственно). Наконец, снижение риска госпитализации у пациентов, находящихся на амбулаторном лечении и в отделениях неотложной помощи, составило 14% (ОР, 0.86; 95% ДИ 0,76–0,98) по сравнению с 37% риском в обзоре 2013 г., что не было статистически значимым. Обзор 2013 года включал меньше испытаний и меньше данных.
Исследователи пришли к выводу, что обзор имеющихся данных поддерживает использование распыленного гипертонического раствора у младенцев, госпитализированных с острым вирусным бронхиолитом, поскольку он может сократить продолжительность пребывания в стационаре и имеет хороший профиль безопасности. Кроме того, лечение распыленным гипертоническим раствором может также снизить риск госпитализации младенцев, находящихся на амбулаторном лечении и в отделениях неотложной помощи.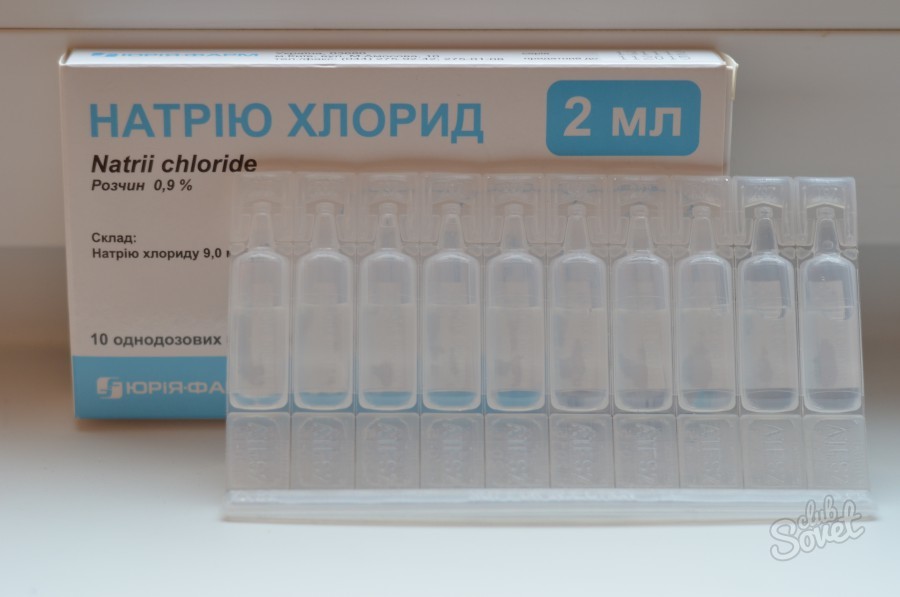
Номер ссылки
Zhang L, Mendoza-Sassi RA, Wainwright C, Klassen TP. Распыленный гипертонический солевой раствор при остром бронхиолите у младенцев. Кокрановская база данных Syst Rev. 2017; 12: CD006458.
Распыленный гипертонический солевой раствор для лечения бронхиолита – лекарства по номерам
Подробная информация для этого обзора
Группа исследователей: Дети младше 24 месяцев с бронхиолитом (3 209 участников в 24 исследованиях).В большинство испытаний не включались пациенты, которым требовалась искусственная вентиляция легких, интенсивная терапия или пациенты с сатурацией кислорода менее 85% в помещении.
Конечные точки эффективности: продолжительность пребывания в больнице, частота госпитализаций
Конечные точки вреда: тахикардия, гипертензия, бледность, тремор, тошнота, рвота, диарея и острая задержка мочи
Рассказ: Бронхиолит – наиболее распространенный респираторный тракт инфекция у младенцев, ведущей причиной которой является респираторно-синцитиальный вирус.Считается, что отек дыхательных путей и закупорка слизью являются патологическими процессами, вызывающими осложнения при вирусном бронхиолите. Поддерживающая терапия – это стандарт лечения. Кроме того, небулайзерный гипертонический раствор может облегчить симптомы.
Систематический обзор включал двойные слепые рандомизированные контролируемые клинические испытания, оценивающие эффект небулайзированного гипертонического (3% или выше) солевого раствора отдельно или в сочетании с бронходилататорами у младенцев с острым бронхиолитом по сравнению с небулайзированным нормальным (0.9%) физиологический раствор.1 Распыление гипертонического раствора привело к статистически значимому сокращению продолжительности пребывания в больнице (средняя разница: -0,45 дня; 95% доверительный интервал [ДИ], от -0,82 до -0,08). Распыленный гипертонический раствор также снижает риск госпитализации на 20% по сравнению с 0,9% физиологическим раствором (относительный риск [ОР] = 0,80; 95% ДИ от 0,67 до 0,96). Не сообщалось о каких-либо значительных побочных эффектах, связанных с ингаляцией гипертонического раствора.
Не сообщалось о каких-либо значительных побочных эффектах, связанных с ингаляцией гипертонического раствора.
Ведущий автор этого систематического обзора опубликовал Кокрановский обзор по той же теме в 2013 году.2 Этот метаанализ показал среднее сокращение продолжительности пребывания в больнице на 1,2 дня (95% ДИ, 0,8–1,5 дня) и отсутствие существенной разницы в частоте госпитализаций2. -анализ, потому что он более свежий и включает несколько недавних исследований и примерно на 2000 пациентов больше, чем Кокрановский обзор 2013 года.
В метаанализе 2014 г. сообщалось об уменьшении продолжительности пребывания в больнице примерно на один день (средневзвешенная разница = -0.96; 95% ДИ, от -1,38 до -0,54) у пациентов, получавших небулайзерный гипертонический раствор по сравнению с обычным физиологическим раствором.3 Этот метаанализ также показал значительное снижение частоты госпитализаций (ОР = 0,59; 95% ДИ, от 0,37 до 0,93) после прием небулайзерного гипертонического раствора.
Рандомизированное контролируемое исследование 2017 года с участием 777 пациентов с бронхиолитом не продемонстрировало каких-либо существенных различий в частоте госпитализации или продолжительности пребывания в больнице между группами (распыленный гипертонический раствор и распыленный физиологический раствор).4
Никаких значительных побочных эффектов, связанных с ингаляцией гипертонического солевого раствора, не наблюдалось в исследованиях, о которых сообщалось в систематических обзорах. Ни один из пациентов не выбыл из-за побочных эффектов или клинического ухудшения.
Предостережения: результаты трех крупных метаанализов рандомизированных двойных слепых клинических исследований свидетельствуют о высоком качестве доказательств и показывают некоторые преимущества использования распыленного гипертонического раствора по сравнению с обычным физиологическим раствором у детей с бронхиолитом.1–3 Однако большинство Проблема, возникающая при рассмотрении данных, заключается в том, что большинство испытаний, опубликованных после 2013 года, включая два крупных многоцентровых европейских исследования, дали отрицательные результаты. 4–8 Неоднородность испытаний и наличие модификаторов эффекта могут быть причиной этого несоответствия.
4–8 Неоднородность испытаний и наличие модификаторов эффекта могут быть причиной этого несоответствия.
Авторы обзора 2015 г. предлагают объяснение этого несоответствия между испытаниями.1 Анализ подгрупп, проведенный этими авторами, показал, что испытания, в которых было доступно вирусологическое тестирование, показали значительно больший размер эффекта распыленного гипертонического раствора (измеренный по уменьшению продолжительность пребывания в больнице и частота госпитализаций), чем в исследованиях без такого тестирования.Таким образом, точность диагностики бронхиолита может повлиять на результаты лечения.
Единственным непротиворечивым результатом всех испытаний является отсутствие каких-либо серьезных побочных эффектов, связанных с применением гипертонического раствора. Учитывая распространенность бронхиолита, а также финансовые и эмоциональные затраты на госпитализацию, возможное снижение количества госпитализаций и пребывания в больнице с минимальными побочными эффектами дает достаточно доказательств, чтобы рекомендовать это лечение острого бронхиолита.
В большинство испытаний не включались пациенты, которым требовалась искусственная вентиляция легких или интенсивная терапия, а также пациенты с сатурацией кислорода менее 85% в помещении.Следовательно, результаты этого обзора могут не относиться к младенцам с более тяжелым бронхиолитом.
Несмотря на сообщаемые преимущества, связанные с использованием гипертонического раствора при бронхиолите, мы выбрали желтую рекомендацию, потому что более поздние испытания и систематические обзоры показали либо гораздо меньший размер эффекта, либо отсутствие пользы по сравнению с более ранними испытаниями.
Авторские права 2018 Группа NNT (theNNT.com). Используется с разрешения.
Координирует эту серию Дин А.Зеехузен, доктор медицины, магистр здравоохранения, помощник медицинского редактора AFP, и Даниэль Рунде, доктор медицины, из NNT Group.
Эффект 3% и 6% физиологического раствора при вирусном бронхиолите: рандомизированное контролируемое исследование
Реферат
Бронхиолит – распространенное заболевание у маленьких детей, которое часто требует госпитализации. За исключением возможного эффекта распыленного гипертонического раствора (хлорида натрия), нет доказательной терапии. В этом исследовании изучалась эффективность распыления 3% и 6% гипертонического раствора соли по сравнению с 0.9% -ный гипертонический раствор у детей, госпитализированных с вирусным бронхиолитом.
За исключением возможного эффекта распыленного гипертонического раствора (хлорида натрия), нет доказательной терапии. В этом исследовании изучалась эффективность распыления 3% и 6% гипертонического раствора соли по сравнению с 0.9% -ный гипертонический раствор у детей, госпитализированных с вирусным бронхиолитом.
В этом многоцентровом двойном слепом рандомизированном контролируемом исследовании дети, госпитализированные с острым вирусным бронхиолитом, были рандомизированы для получения 3%, 6% гипертонического раствора или 0,9% физиологического раствора в виде небулайзера в течение всего пребывания в больнице. Сальбутамол был добавлен для предотвращения возможного сужения бронхов. Первичной конечной точкой была продолжительность пребывания в больнице. Вторичными исходами были потребность в дополнительном кислороде и зондовом питании.
Из 292 детей, включенных в исследование (средний возраст 3,4 месяца), 247 завершили исследование. Средняя продолжительность пребывания в стационаре не различалась между группами: 69 часов (межквартильный размах 57), 70 часов (IQR 69) и 53 часа (IQR 52) для 3% (n = 84) и 6% (n = 83). ) гипертонический раствор и 0,9% (n = 80) физиологический раствор соответственно (p = 0,29). Потребность в дополнительном кислороде или питании через зонд существенно не различалась. Побочные эффекты были одинаковыми в трех группах.
Распыление гипертоническим раствором (3% или 6% хлорида натрия), хотя и безопасно, не уменьшало продолжительность пребывания в больнице, продолжительность дополнительного кислорода или зондового питания у детей, госпитализированных с вирусным бронхиолитом средней и тяжелой степени тяжести.
Аннотация
Распыление гипертоническим солевым раствором не уменьшило продолжительность госпитализации детей с вирусным бронхиолитом http://ow.ly/xRVVx
Введение
Острый вирусный бронхиолит – вирусная инфекция нижних дыхательных путей у младенцев [1, 2]. Обычные вирусы, вызывающие бронхиолит, включают респираторно-синцитиальный вирус (РСВ), метапневмовирус человека, аденовирус, вирус (пара) гриппа, риновирус и коронавирус [3]. Бронхиолит является основной причиной госпитализации младенцев в течение первого года жизни и поражает миллионы младенцев во всем мире [4].Ежегодные затраты на госпитализацию по поводу бронхиолита только в США составляют более 500 миллионов долларов [5]. До сих пор было показано, что потенциально терапевтические вмешательства, такие как распыленные кортикостероиды, адреналин, бета-агонисты, антибиотики и рекомбинантная дезоксирибонуклеаза человека, неэффективны [6–10]. Следовательно, лечение бронхиолита остается поддерживающим с добавлением кислорода, поддержанием баланса жидкости и механической вентиляции, если это необходимо [11].
Бронхиолит является основной причиной госпитализации младенцев в течение первого года жизни и поражает миллионы младенцев во всем мире [4].Ежегодные затраты на госпитализацию по поводу бронхиолита только в США составляют более 500 миллионов долларов [5]. До сих пор было показано, что потенциально терапевтические вмешательства, такие как распыленные кортикостероиды, адреналин, бета-агонисты, антибиотики и рекомбинантная дезоксирибонуклеаза человека, неэффективны [6–10]. Следовательно, лечение бронхиолита остается поддерживающим с добавлением кислорода, поддержанием баланса жидкости и механической вентиляции, если это необходимо [11].
Отек дыхательных путей и закупорка слизью являются преобладающими патологическими признаками у младенцев с острым вирусным бронхиолитом [12].Распыленный гипертонический раствор (HS) с использованием хлорида натрия может иметь положительное влияние на бронхиолит, так как он может уменьшить отек подслизистой оболочки, уменьшить воспалительные медиаторы и вязкость слизи, а также улучшить клиренс слизистых оболочек [13–16]. In vitro HS улучшает реологические свойства слизи (эластичность и вязкость) и ускоряет скорость транспорта слизи [17]. Исследования последнего десятилетия показали, что легкая небулайзерная терапия HS сокращает продолжительность пребывания в больнице младенцев с легким и умеренно тяжелым бронхиолитом [4, 18–25].Все эти исследования, кроме одного, включали небольшое количество пациентов из отдельных центров и использовали плохо определенные результаты; исследовательские группы были неоднородными, а некоторые не были четко определены [4, 26–28]. Исследования на пациентах с муковисцидозом показали, что распыленный HS в концентрации 5–7% более эффективен, чем изотонический раствор, и этот эффект оказался дозозависимым [29–34]. У младенцев в возрасте 4 месяцев и старше с муковисцидозом было доказано, что HS безопасен [35]. Поэтому мы провели рандомизированное контролируемое исследование различных концентраций распыленного HS у младенцев, госпитализированных по поводу вирусного бронхиолита.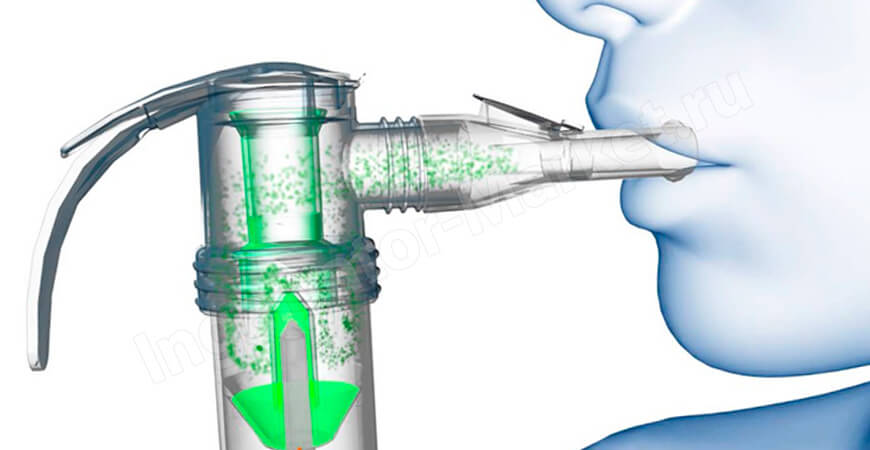 Мы предположили, что распыление HS в зависимости от дозы сократит продолжительность пребывания в больнице и продолжительность поддерживающей терапии.
Мы предположили, что распыление HS в зависимости от дозы сократит продолжительность пребывания в больнице и продолжительность поддерживающей терапии.
Методы и материалы
Настройка
Это двойное слепое рандомизированное контролируемое исследование проводилось в 11 больницах общего профиля и одном медицинском центре третичного уровня в Нидерландах. Исследование было одобрено центральным комитетом по медицинской этике Нидерландов (Голландский регистр испытаний, номер: NTR 1494) и местными комитетами по этике всех участвующих больниц.Перед началом исследования от имени каждого ребенка по крайней мере один законный опекун подписал форму информированного согласия.
Пациенты
Дети в возрасте от 0 до 24 месяцев соответствовали критериям участия в исследовании, если они были госпитализированы в одну из участвующих больниц из-за легкого или тяжелого вирусного бронхиолита и имели на момент обращения оценку Wang ≥3. Шкала клинической тяжести Wang состоит из четырех пунктов: частота дыхания, хрипы, втягивания и общее состояние (таблица 1) [36]. Клинически диагноз «бронхиолит» ставился на основании симптомов инфекции верхних дыхательных путей с хрипом, тахипноэ и одышкой [11].Чтобы снизить вероятность включения детей с атопическим хрипом, все дети получали однократную ингаляцию 2,5 мг сальбутамола перед включением в исследование. Дети были исключены, если оценка Ванга улучшилась как минимум на 2 балла после ингаляции. Другими критериями исключения были гемодинамически важные врожденные пороки сердца, хронические предсуществующие заболевания легких, Т-клеточный иммунодефицит, лечение кортикостероидами и предшествующие хрипы, (пищевая) аллергия или экзема.
Таблица 1- Система оценки клинической тяжести инфекций нижних дыхательных путей у младенцев по шкале ВангаИсследуемое лекарство
Исследуемый препарат для всех центров был подготовлен международно сертифицированным фармацевтом-исследователем (Sterop Pharmacobel, Брюссель, Бельгия). Для предотвращения возможной бронхиальной обструкции к каждой дозе добавляли 2,5 мг сальбутамола. Концентрации физиологического раствора были рассчитаны таким образом, чтобы концентрация окончательного раствора с сальбутамолом составляла 0,9%, 3% или 6% хлорида натрия, а общий объем составлял 4 мл на ингаляцию.
Для предотвращения возможной бронхиальной обструкции к каждой дозе добавляли 2,5 мг сальбутамола. Концентрации физиологического раствора были рассчитаны таким образом, чтобы концентрация окончательного раствора с сальбутамолом составляла 0,9%, 3% или 6% хлорида натрия, а общий объем составлял 4 мл на ингаляцию.
Все участники, лица, осуществляющие уход, и медицинский персонал не знали о составе исследуемых растворов, которые были идентичны по упаковке флаконов, цвету, запаху и другим физическим характеристикам. Флаконы использовались до 24 часов после открытия.Срок годности всех флаконов – 31 декабря 2011 года. Код был сдан на хранение фармацевту.
Дизайн исследования
Пациенты были набраны в период с ноября 2009 г. по май 2011 г., во время сезона бронхиолитов. При поступлении регистрировался клинический анамнез пациента, который включал продолжительность симптомов до госпитализации, прием лекарств, а также анамнез пациента и его семейный анамнез атопии. Мазок из носоглотки был взят для анализа на вирус. Если ребенок соответствовал критериям включения и было получено согласие родителей, распыление исследуемого препарата начинали в течение 12 часов после поступления.
Все отобранные пациенты были случайным образом распределены в одну из двух групп вмешательства или в контрольную группу. Рандомизация проводилась по центрам и группировалась в блоки по шесть пациентов. Каждый пациент получил последовательно рандомизированное количество, которое соответствовало идентичным пузырькам на 20 мл, которые содержали разные растворы хлорида натрия. Группы вмешательства получали ингаляции с 3% или 6% HS, а контрольная группа получала ингаляции с 0,9% хлоридом натрия (физиологический раствор (NS)).
Растворы распыляли каждые 8 ч при постоянном потоке кислорода 6–8 л · мин. –1 из настенной розетки в сочетании с небулайзером HOT Top Plus (Intersurgical, Уден, Нидерланды), масс-медианный аэродинамический диаметр ( MMAD) 4 мкм, с через , плотно прилегающую лицевую маску, и вводили до опорожнения. Распыление продолжали до выписки.
Распыление продолжали до выписки.
Всех детей обследовали дважды в день, основываясь на физикальном осмотре, шкале Ванга, частоте сердечных сокращений, сатурации, частоте дыхания, потребности в дополнительном кислороде и питании через зонд.Обследование проводил дежурный педиатр. Перед началом исследования весь медицинский персонал, участвовавший в исследовании, был обучен тому, как оценивать пациентов и классифицировать систему оценки клинической тяжести Ванга, чтобы улучшить согласие между наблюдателями.
Согласно заранее определенным критериям, дополнительное кислородное питание начиналось у младенцев с насыщением воздуха в помещении 93% или ниже в течение> 10 минут или острым раскислением <85%. Это было остановлено, когда насыщение постоянно составляло> 93%.Показанием для начала и прекращения кормления через зонд было минимальное потребление, рассчитанное как 75% от нормального. Потеря жидкости из-за обезвоживания или диареи компенсировалась добавлением потерянной жидкости к минимальному потреблению. Дополнительные лекарства и другая поддерживающая терапия были предоставлены в соответствии с рекомендациями больницы.
Все дополнительные лекарства, время и количество дополнительного кислорода и зондового питания регистрировались в карточке случая, как и частота сердечных сокращений, сатурация кислорода, температура и побочные эффекты.Побочные реакции определялись как любые наблюдаемые нежелательные эффекты, независимо от того, были ли они связаны с исследуемым лекарством или нет. Возможные известные побочные эффекты ингаляции с HS включали ринорею, беспокойство, кашель и бронхиальную обструкцию [4, 34, 37].
Первичным результатом была продолжительность пребывания в больнице, которую рассчитывали как количество часов между первой дозой исследуемого лекарства и клиническим решением о выписке. Таким образом, на первичную конечную точку не повлияло дополнительное пребывание в больнице из-за социальных или административных факторов.По словам ответственного педиатра, критерии выписки, определенные протоколом, включали отсутствие необходимости в дополнительном кислороде, питании через зонд или внутривенном введении жидкости. Вторичными исходами были переводы в педиатрическое отделение интенсивной терапии (PICU) из-за дыхательной недостаточности, необходимости и продолжительности дополнительного кислорода или зондового питания. Безопасность лечения измеряли путем регистрации нежелательных явлений.
Вторичными исходами были переводы в педиатрическое отделение интенсивной терапии (PICU) из-за дыхательной недостаточности, необходимости и продолжительности дополнительного кислорода или зондового питания. Безопасность лечения измеряли путем регистрации нежелательных явлений.
Статистические методы
Предыдущие исследования показали уменьшение продолжительности пребывания в больнице с 4 до 3 дней после ингаляции 3% HS [18].Основываясь на этом сокращении пребывания в больнице на 25%, для текущего исследования потребовался размер выборки из 65 пациентов в каждой экспериментальной группе, чтобы достичь мощности 90% при значении p <0,05. Все данные были анонимно записаны, введены в электронную таблицу Excel (Microsoft Corp, Редмонд, Вашингтон) и импортированы в программное обеспечение SPSS версии 19.0 (SPSS Inc, Чикаго, Иллинойс) для анализа. Анализы проводились в соответствии с принципами назначения лечения и протокола. Различия между включенными и исключенными пациентами в отношении характеристик пациентов оценивались с помощью независимого t-критерия (возраст) и критерия хи-квадрат (пол и вмешательство).Все непрерывные переменные (продолжительность пребывания в больнице, часы дополнительного кислорода и зондового питания) были проверены на нормальность. В случае нормального распределения различия между тремя группами были проверены с помощью ANOVA, а в случае ненормального распределения использовался тест Крускала-Уоллиса. Для категориальных переменных различия в распределении между группами вмешательства были проверены с помощью критерия хи-квадрат. Одномерные различия во времени до выписки из больницы между группами вмешательства были протестированы с помощью лог-рангового теста.
Результаты
В период с ноября 2009 г. по май 2011 г. в исследование были включены и рандомизированы 292 ранее здоровых ребенка с вирусным бронхиолитом средней и тяжелой степени тяжести (рис. 1). До включения в исследование большинство пациентов получали назальные деконгестанты: 21 – сальбутамол (спейсер), 10 – парацетамол, 4 – амоксициллин, 3 – омепразол, 3 – нистатин и 1 – вальпроевая кислота.
Включение пациентов в исследование и процедуры последующего наблюдения и анализа.
Два пациента были выписаны из-за быстрого улучшения клинического состояния и поэтому были исключены из исследования до того, как была введена первая доза исследуемого препарата. В общей сложности 290 младенцев (средний возраст 3,4 месяца, диапазон от 10 дней до 23 месяцев) были включены в исследование и проанализированы в анализе намерения лечиться. 43 (15%) пациента были исключены для анализа по протоколу, а 18 (6,2%) пациентов не завершили лечение из-за побочных эффектов. Из них девять пациентов ушли из-за кашля или возбуждения во время и после распыления, а девять других из-за клинического ухудшения, такого как повышенная потребность в кислороде, усилие дыхания или прогрессирующая обструкция дыхательных путей.Отзыв информированного согласия привел к исключению еще девяти (3,1%) пациентов. Тринадцать младенцев были исключены из исследования из-за отклонения от протокола. Трем пациентам (1,2%) потребовалась искусственная вентиляция легких в отделении интенсивной терапии интенсивной терапии в течение болезни: у одного пациента ухудшилось состояние через 5 часов после первой ингаляции с 6% HS; клиническое состояние одного пациента, рандомизированного в группу 6%, ухудшилось после 6 дней лечения и потребовалось госпитализации в реанимацию; и один пациент, получавший NS, имел респираторную недостаточность при поступлении, и это клиническое состояние не изменилось после приема одной дозы исследуемого лекарства в ожидании перевода в PICU (рис.1). Количество отказов (по причинам) существенно не различалось между группами вмешательства (p = 0,47).
Всего 247 младенцев завершили исследование и были проанализированы в соответствии с протоколом анализа; 84 получили 3% HS, 83 получили 6% HS и 80 получили NS (рис. 1). Исходные характеристики пациентов существенно не различались между тремя группами (таблица 2). Результаты анализа намерения лечиться и анализа по протоколу не различались по исходным характеристикам или по каким-либо первичным или вторичным исходам (данные не показаны).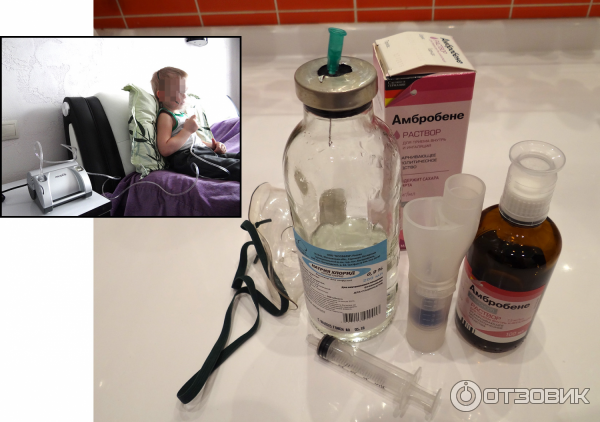 Помимо исследуемого препарата, пациенты получали: назальные деконгестанты n = 161, парацетамол n = 30, антибиотики n = 11, сальбутамол n = 6, ибупрофен n = 1, нистатин n = 1 и ранитидин n = 1. Применение назальных деконгестантов (ксилометазолина и хлорида натрия) было равномерно распределено среди исследуемых групп (данные не показаны).
Помимо исследуемого препарата, пациенты получали: назальные деконгестанты n = 161, парацетамол n = 30, антибиотики n = 11, сальбутамол n = 6, ибупрофен n = 1, нистатин n = 1 и ранитидин n = 1. Применение назальных деконгестантов (ксилометазолина и хлорида натрия) было равномерно распределено среди исследуемых групп (данные не показаны).
Средняя продолжительность пребывания в больнице составила 69 часов в группе 3% HS, 70 часов в группе 6% HS и 53 часа в группе NS (p = 0.29) (таблица 3). Различия во времени до выписки между тремя группами не были статистически значимыми (p = 0,26) (рис. 2).
Фигура 2-Процент младенцев, оставшихся в больнице, отображается в зависимости от времени до выписки в соответствии с вмешательством.
Таблица 3– Первичные и вторичные исходы для трех групп вмешательстваДополнительный кислород потребовался 50 (59,5%) младенцам в группе 3% HS, 53 (63,9%) младенцам в группе 6% HS и 51 (63,8%) младенцам в группе 0.9% группа NS (p = 0,70) со средней продолжительностью 54, 54 и 40 часов соответственно (p = 0,14).
Дополнительное зондовое питание потребовалось 29 (34,5%) младенцам в группе 3% HS, 31 (37,3%) младенцам в группе 6% HS и 22 (27,5%) младенцам в группе 0,9% NS (p = 0,39) , со средней продолжительностью 62, 52 и 54 часа соответственно (p = 0,87) (таблица 3).
Средний балл по Вангу при выписке составлял 2,0 в группе NS и в группе 3% HS и 1,0 в группе 6% HS (p = 0,53). Оценка Ванга при выписке улучшилась независимо от схемы лечения (таблицы 3 и 4) без существенных различий между группами (p = 0.80).
Таблица 4– Средний балл по Вангу через 24, 48 и 72 часа для трех групп вмешательства Значительное количество побочных эффектов было отмечено во всех группах лечения (таблица 5). За исключением кашля, который достоверно чаще возникал в группах HS (p = 0,03), различий между группами не обнаружено. Исключения из-за побочных эффектов не различались между группами (p = 0,59). Большинство нежелательных явлений, вероятно, были связаны с основным вирусным бронхиолитом.
Большинство нежелательных явлений, вероятно, были связаны с основным вирусным бронхиолитом.
Обсуждение
В этом двойном слепом рандомизированном многоцентровом исследовании мы сравнили 3% и 6% HS с NS у детей, госпитализированных с вирусным бронхиолитом.Ни 3% HS, ни 6% HS не уменьшили продолжительность пребывания в больнице, оценку тяжести клинической картины Ванга при выписке, продолжительность дополнительного кислорода или зондового питания по сравнению с NS. Эти результаты контрастируют с результатами, опубликованными в литературе [18–22]. Объединенные результаты трех небольших исследований [18–20] продемонстрировали сокращение продолжительности госпитализации на 0,9 дня в пользу группы 3% HS по сравнению с группой NS, тогда как Луо и его коллеги [21, 22] обнаружили сокращение на 0,9 дня. 1.4 и 1,6 дня, соответственно, в своих исследованиях при бронхиолите от легкой до умеренной и от умеренного до тяжелого. Однако Аль-Ансари et al. [24] сравнил распыление 3% HS и 5% HS с NS при относительно легком бронхиолите у младенцев, находящихся в отделении краткосрочного пребывания, и не показал влияния на продолжительность пребывания в больнице, которую он описал как влияющую на медицинские и социальные факторы.
Хотя критерии диагностики вирусного бронхиолита были менее четко определены в большинстве этих исследований, за исключением исследования Kuzik et al .[20], различия в исследуемых популяциях между нашим исследованием и предыдущими исследованиями вряд ли могут объяснить различия между разными результатами. Наша исследуемая популяция была сопоставима по возрасту, клинической тяжести, продолжительности заболевания до госпитализации и с преобладанием РСВ-положительных младенцев. В дополнение к критерию исключения предыдущих свистящих хрипов, атопических проявлений, таких как экзема или пищевая аллергия, мы старались избегать включения младенцев, которым может помочь сальбутамол. Действительно, недавнее исследование показало, что у детей с бронхиолитом оценка Ванга значительно улучшилась у детей с атопией, чем у детей без атопии, когда к лекарству был добавлен сальбутамол [23], что поддерживает наш подход.Принимая во внимание возможное быстрое реагирование на однократную дозу сальбутамола [12], можно утверждать, что наш протокол исследования привел к исключению быстро реагирующих людей, что, возможно, повлияло на результаты. В целом 14% всех детей, прошедших скрининг на включение, пришлось исключить из-за положительной реакции на сальбутамол. Однако, даже если бы этих младенцев включили и случайным образом распределили в исследуемые группы, их количество было бы слишком маленьким, чтобы существенно повлиять на результаты.
Действительно, недавнее исследование показало, что у детей с бронхиолитом оценка Ванга значительно улучшилась у детей с атопией, чем у детей без атопии, когда к лекарству был добавлен сальбутамол [23], что поддерживает наш подход.Принимая во внимание возможное быстрое реагирование на однократную дозу сальбутамола [12], можно утверждать, что наш протокол исследования привел к исключению быстро реагирующих людей, что, возможно, повлияло на результаты. В целом 14% всех детей, прошедших скрининг на включение, пришлось исключить из-за положительной реакции на сальбутамол. Однако, даже если бы этих младенцев включили и случайным образом распределили в исследуемые группы, их количество было бы слишком маленьким, чтобы существенно повлиять на результаты.
Метаанализ показал обратную зависимость между тяжестью заболевания и эффектом распыленного HS [4].Следовательно, различия в степени тяжести бронхиолита между исследуемыми популяциями могут объяснить разные результаты. Однако, похоже, что это не так, поскольку на исходном уровне оценка Ванга в нашем исследовании составляла 6,2 по сравнению с 5,8 в исследовании, что составляет половину веса метаанализа [21], в то время как другие исследования метаанализа в анализ были включены пациенты с более высокими оценками Ванга [18–20]. Наше исследование не было разработано для изучения подгрупп с разной степенью тяжести заболевания, и дальнейшие исследования должны выяснить, может ли HS быть особенно полезным в подгруппах младенцев с более тяжелым заболеванием.
Мы не можем исключить, что различия в типах небулайзеров и частоте небулайзеров сыграли свою роль. Мы использовали один и тот же небулайзер с MMAD 4 мкм для всех исследуемых пациентов, что привело к отложению в основном в нижних дыхательных путях [38]. Потенциально может влиять небулайзер с меньшим MMAD и другим отложением в легких [39]. Тип небулайзера и MMAD не были описаны в других исследованиях, поэтому дальнейшее сравнение невозможно. Только в двух предыдущих исследованиях участвовали участники, которым распыляли более часто, чем в нашем исследовании [20, 22].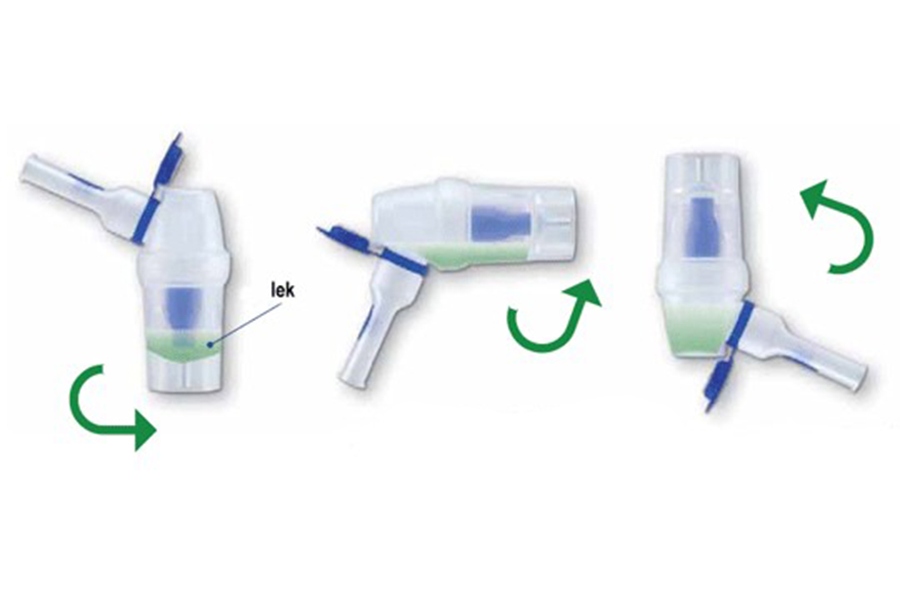 Однако не было никаких кинетических данных о периоде полураспада эффекта HS, и частое распыление не рекомендуется [20]. Следовательно, маловероятно, что различия в типе и частоте распыления могут объяснить наши выводы.
Однако не было никаких кинетических данных о периоде полураспада эффекта HS, и частое распыление не рекомендуется [20]. Следовательно, маловероятно, что различия в типе и частоте распыления могут объяснить наши выводы.
Большинство ранее опубликованных исследований были одноцентровыми исследованиями. Возможно, на результаты повлияли такие различия, как местные привычки в диагностике и лечении. Настоящее исследование представляет собой многоцентровое исследование, которое, возможно, могло бы уменьшить эти факторы.Для каждого центра была проведена рандомизация, что позволило провести анализ для каждого центра; но мы не обнаружили существенных различий между центрами.
Сильные стороны нашего исследования заключаются в использовании строгих критериев включения и выписки. Мы использовали строгое, клинически значимое определение времени выписки, на которое не влияли социальные или административные факторы [24]. Следовательно, мы ограничили продолжительность пребывания в больнице временем пребывания в больнице по медицинским показаниям. Это может объяснить нашу относительно короткую продолжительность пребывания в больнице (53, 69 и 70 часов для NS, 3% HS и 6% HS соответственно) по сравнению с 2.6–6,0 дней для 3% HS и 3,0–7,4 дня для NS в предыдущих исследованиях [18–22]. Ни в одном из этих исследований не учитывались потенциально влияющие социальные и административные факторы; в большинстве исследований использовались только клинические решения врачей.
Возможное объяснение того, почему это исследование не обнаружило разницы между группами вмешательства и контрольной группой, может заключаться в том, что NS не может быть истинным плацебо. Однако дизайн нашего исследования не может исключить положительный эффект ингаляции NS у младенцев с вирусным бронхиолитом.На этот вопрос можно было бы ответить с помощью исследования не меньшей эффективности, сравнивающего NS и HS. Физиологически адекватное количество жидкости, выстилающей дыхательные пути, имеет решающее значение для нормального функционирования мукоцилиарного клиренса дыхательных путей. Известно, что бронхиолит приводит к снижению содержания воды в жидкости слизистой оболочки дыхательных путей, вызывая уменьшение мукоцилиарного клиренса [12]. In vivo , изменение жидкости на поверхности дыхательных путей и улучшение клиренса слизи после ингаляции NS или HS, вероятно, является прямым эффектом общей массы хлорида натрия, добавленного к поверхности дыхательных путей [13].У пациентов с амбулаторным бронхиолитом распыление с большим объемом NS было так же эффективно, как и с более низким объемом 3% HS [40]. Пока это не показано для более тяжелых заболеваний. Более ранние исследования, которые показали положительный эффект 3% HS, также проводили распыление три раза в день, что дало такую же общую дозу [18, 19, 21]. Следовательно, хотя более высокая доза общего хлорида натрия может иметь влияние, это вряд ли объяснит разные результаты исследования. Наши результаты были подтверждены недавним исследованием, в котором сравнивали NS с 7% HS и использовали частоту ингаляций четыре раза в день, которое не показало положительного эффекта HS, даже при более высокой общей дозе хлорида натрия [41].Ipek et al. [23] сравнивали действие распыленных NS и HS с сальбутамолом и без него у амбулаторных пациентов с легким бронхиолитом. Все исследуемые группы показали значительное снижение клинической степени тяжести без различий между группами, что позволяет предположить, что NS может иметь некоторый терапевтический эффект также и у пациентов, не страдающих атопией. Это подтверждает наши выводы о том, что не было обнаружено значительных различий между использованием HS и NS у пациентов с бронхиолитом.
Известно, что бронхиолит приводит к снижению содержания воды в жидкости слизистой оболочки дыхательных путей, вызывая уменьшение мукоцилиарного клиренса [12]. In vivo , изменение жидкости на поверхности дыхательных путей и улучшение клиренса слизи после ингаляции NS или HS, вероятно, является прямым эффектом общей массы хлорида натрия, добавленного к поверхности дыхательных путей [13].У пациентов с амбулаторным бронхиолитом распыление с большим объемом NS было так же эффективно, как и с более низким объемом 3% HS [40]. Пока это не показано для более тяжелых заболеваний. Более ранние исследования, которые показали положительный эффект 3% HS, также проводили распыление три раза в день, что дало такую же общую дозу [18, 19, 21]. Следовательно, хотя более высокая доза общего хлорида натрия может иметь влияние, это вряд ли объяснит разные результаты исследования. Наши результаты были подтверждены недавним исследованием, в котором сравнивали NS с 7% HS и использовали частоту ингаляций четыре раза в день, которое не показало положительного эффекта HS, даже при более высокой общей дозе хлорида натрия [41].Ipek et al. [23] сравнивали действие распыленных NS и HS с сальбутамолом и без него у амбулаторных пациентов с легким бронхиолитом. Все исследуемые группы показали значительное снижение клинической степени тяжести без различий между группами, что позволяет предположить, что NS может иметь некоторый терапевтический эффект также и у пациентов, не страдающих атопией. Это подтверждает наши выводы о том, что не было обнаружено значительных различий между использованием HS и NS у пациентов с бронхиолитом.
Хотя в текущем исследовании серьезных побочных эффектов не наблюдалось, у значительного числа детей наблюдались побочные эффекты (таблица 5), которые в значительной степени могли быть вызваны самим бронхиолитом.У 6,2% всех включенных пациентов причиной отмены были побочные эффекты. Более того, кашель был более распространенным в обеих группах HS. Это требует дальнейшего внимания, поскольку предыдущие исследования не включали точного описания побочных эффектов.
Это требует дальнейшего внимания, поскольку предыдущие исследования не включали точного описания побочных эффектов.
В заключение, мы показали, что распыление 3% HS или 6% HS не уменьшало продолжительность пребывания в больнице, оценку тяжести клинической картины Ванга при выписке, потребность в дополнительном кислороде или потребность в зондовом питании у детей в возрасте до 2 лет. госпитализированных с вирусным бронхиолитом, по сравнению с применением НС.Наши результаты не подтверждают рутинное использование HS у младенцев с бронхиолитом.
Благодарности
Авторы хотели бы поблагодарить следующих участников исследования: Нико Ольденхоф (Медицинский центр VieCuri, Венло, Нидерланды) за процедуру рандомизации; Грета Велдхейс (Медицинский центр VieCuri, Венло, Нидерланды) за координацию работы сотрудников аптеки; Барт Роттьер (Университетский медицинский центр, Гронинген, Нидерланды) за промежуточный анализ; Тван Малдер (Университетский медицинский центр, Маастрихт, Нидерланды) и Бриджит ван дер Брюгген-Богартс (Медицинский центр VieCuri, Венло, Нидерланды), которые были независимыми врачами для пациентов с вопросами; Йохану де Йонгсте (Университетский медицинский центр, Роттердам, Нидерланды) за критический обзор рукописи; и Loes Janssen (Центр VieCuri, Венло, Нидерланды) за контроль статистических расчетов.
Участвовавшие центры: Медицинский центр VieCuri, Венло; Медицинский центр Маастрихтского университета, Маастрихт; Медицинский центр Орбис, Ситтард; Больница Катарины, Эйндховен; Медицинский центр Максима, Велдховен; Больница Лаврентия, Рурмонд; Больница Элькерлик, Хелмонд; Госпиталь Рейнстейт, Арнем; Больница Маасстад, Роттердам; Больница Амфия, Бреда; Госпиталь Тви Стеден, Тилбург; и больница Святой Елизаветы, Тилбург, Нидерланды.
Сноски
Редакционные комментарии см. На стр. 827.
Клиническое испытание: Испытание зарегистрировано в Голландском реестре испытаний, номер NTR1494, и в Реестре клинических испытаний ЕС, EudraCT, номер 2008-003886-17.

Заявление о поддержке: Финансовая поддержка исследования была предоставлена за счет образовательных грантов от Schering Plough BV (Маарссен, Нидерланды), Nutricia (Зутермейер, Нидерланды) и Фонда Кристин Бадер из детской больницы Ирэн (Арнем, Нидерланды) .
Конфликт интересов: раскрытие информации можно найти вместе с онлайн-версией этой статьи на сайте www.erj.ersjournals.com
- Получено 11 сентября 2013 г.
- Принято 16 мая 2014 г.
Оценка плацебо-статуса распыленного физиологического раствора у пациентов с острым вирусным бронхиолитом: систематический обзор и мета-анализ | Неотложная медицина | JAMA Педиатрия
Ключевые моментыВопрос Связан ли распыленный физиологический раствор с физиологическими показателями респираторного статуса у пациентов с острым вирусным бронхиолитом?
Выводы Этот систематический обзор и метаанализ показали, что пациенты с бронхиолитом, получавшие небулайзерный физиологический раствор, показали значительное улучшение частоты дыхания и респираторных показателей после терапии, хотя сатурация кислорода оставалась неизменной.Кроме того, по сравнению с пациентами, получавшими другие плацебо, пациенты, получавшие небулайзерный физиологический раствор, показали большее улучшение респираторных показателей после лечения.
Значение Распыленный физиологический раствор не может быть инертным плацебо для пациентов с бронхиолитом и должен быть дополнительно изучен, чтобы установить клиническую значимость любого потенциального результата лечения.
Важность В терапевтических испытаниях острого вирусного бронхиолита постоянное клиническое улучшение в группах, получавших небулайзерный физиологический раствор (НС) в качестве плацебо, поднимает вопрос о том, действуют ли распыленные НС в качестве лечения, а не плацебо.
Объектив Измерить краткосрочную связь распыленных НП с физиологическими показателями респираторного статуса у детей с бронхиолитом путем анализа изменений этих показателей между использованием небулайзированных НП и применением других плацебо, а также изменений до и после лечения небулайзерами НП.
Источники данных В течение марта 2019 г. проводился поиск в MEDLINE и Scopus, а также в библиографиях включенных исследований и соответствующих систематических обзорах для рандомизированных клинических испытаний, оценивающих небулайзерную терапию при бронхиолите.
Выбор исследования Были включены рандомизированные клинические испытания, сравнивающие детей в возрасте 2 лет и младше с бронхиолитами, получавших небулайзерные НП. Исследования с участием группы лечения, получавшей альтернативное плацебо, были включены для сравнения NS с другими плацебо.
Извлечение и синтез данных Абстракция данных была выполнена в соответствии с рекомендациями PRISMA. Использовались метааналитические модели с фиксированными и случайными эффектами, взвешенные по дисперсии.
Основные результаты и мероприятия Объединенные оценки связи с респираторными баллами, частотой дыхания и насыщением кислородом в течение 60 минут после лечения были получены для распыленных NS по сравнению с другим плацебо и для изменений до и после получения распыленных NS.
Результаты Всего было включено 29 исследований с участием 1583 пациентов. Стандартизованные средние различия респираторных баллов для распыленных NS по сравнению с другим плацебо (3 исследования) благоприятствовали небулайзированным NS на -0.9 баллов (95% ДИ, от -1,2 до -0,6 балла) через 60 минут после лечения ( P <0,001). Не было различий в частоте дыхания или насыщении кислородом при сравнении распыленных NS с другими плацебо. Стандартизированная средняя разница респираторных баллов (25 исследований) после распыления NS составила -0,7 (95% ДИ, от -0,7 до -0,6; I 2 = 62%). Средневзвешенная разница в респираторных показателях с использованием согласованной шкалы (13 исследований) после распыления NS составила -1,6 балла (95% ДИ, -1.От 9 до -1,3 балла; I 2 = 72%). Средневзвешенная разница в частоте дыхания (17 исследований) после распыления NS составила -5,5 вдохов в минуту (95% ДИ, от -6,3 до -4,6 вдохов в минуту; I 2 = 24%). Средневзвешенная разница в насыщении кислородом (23 исследования) после распыления NS составила -0,4% (95% ДИ, от -0,6% до -0,2%; I 2 = 79%).
Средневзвешенная разница в респираторных показателях с использованием согласованной шкалы (13 исследований) после распыления NS составила -1,6 балла (95% ДИ, -1.От 9 до -1,3 балла; I 2 = 72%). Средневзвешенная разница в частоте дыхания (17 исследований) после распыления NS составила -5,5 вдохов в минуту (95% ДИ, от -6,3 до -4,6 вдохов в минуту; I 2 = 24%). Средневзвешенная разница в насыщении кислородом (23 исследования) после распыления NS составила -0,4% (95% ДИ, от -0,6% до -0,2%; I 2 = 79%).
Выводы и значимость Распыленные NS могут быть активным средством лечения острого вирусного бронхиолита.Следует провести дополнительную оценку, чтобы установить, действительно ли это плацебо.
Острый вирусный бронхиолит, одно из наиболее распространенных детских болезней, насколько нам известно, не имеет надежной, научно обоснованной небулайзерной терапии. 1 -8 В большинстве рандомизированных клинических испытаний распыленный физиологический раствор (NS) используется в качестве плацебо, что логично, учитывая, что NS также используется в качестве носителя для распыления активного лечения.Однако в исследованиях бронходилататоров было отмечено последовательное улучшение показателей, превышающих ожидаемые, у пациентов, получавших плацебо. 9 Нарастающий и убывающий характер бронхиолита может объяснить эти результаты, но, учитывая сильную тенденцию к улучшению, также возможно, что распыленные НП действуют как эффективное лечение.
Распыленный NS исторически использовался в качестве плацебо и при других состояниях, как правило, в исследованиях, посвященных изучению бронхолитических препаратов и отхаркивающих средств для мокроты. 10 Существует небольшое количество доказательств того, что распыленные NS могут быть активным средством лечения взрослых с хронической обструктивной болезнью легких.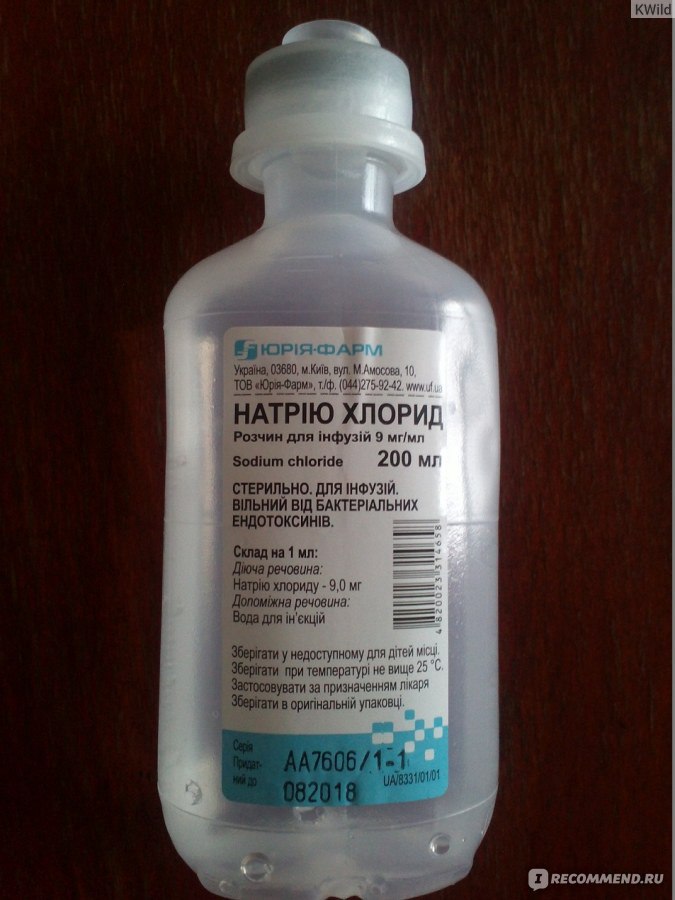 В рандомизированном клиническом исследовании 40 пациентов с хронической обструктивной болезнью легких исследователи использовали технику «неэффективного» распыления, чтобы скрыть участников от назначения лечения, и продемонстрировали значительное улучшение показателей одышки в пользу NS, распыленных через эффективный распылитель, по сравнению с неэффективным распылителем. 10 Рандомизированные клинические испытания, сравнивающие распыленные NS с ингаляционным тербуталином и с ингаляционным фуросемидом среди пациентов с одышкой, также обнаружили аналогичное улучшение показателей одышки среди групп, получающих активное лечение, и групп, получающих NS. 11 , 12 Однако в другом очень небольшом испытании лабораторно-индуцированной одышки у 5 здоровых добровольцев, которое было специально разработано для снижения ожидания облегчения одышки, только 1 из 5 пациентов испытали облегчение, которое исследователи приписали эффекту плацебо. 12
В рандомизированном клиническом исследовании 40 пациентов с хронической обструктивной болезнью легких исследователи использовали технику «неэффективного» распыления, чтобы скрыть участников от назначения лечения, и продемонстрировали значительное улучшение показателей одышки в пользу NS, распыленных через эффективный распылитель, по сравнению с неэффективным распылителем. 10 Рандомизированные клинические испытания, сравнивающие распыленные NS с ингаляционным тербуталином и с ингаляционным фуросемидом среди пациентов с одышкой, также обнаружили аналогичное улучшение показателей одышки среди групп, получающих активное лечение, и групп, получающих NS. 11 , 12 Однако в другом очень небольшом испытании лабораторно-индуцированной одышки у 5 здоровых добровольцев, которое было специально разработано для снижения ожидания облегчения одышки, только 1 из 5 пациентов испытали облегчение, которое исследователи приписали эффекту плацебо. 12
Концепция эффекта плацебо недавно подверглась пересмотру и уточнению. Статья 1955 года Бичера 13 , в которой впервые была сформулирована идея примерно равной 30% реакции на плацебо, была подвергнута критической переоценке, предполагая, что на опубликованные результаты повлияли естественные колебания изучаемых заболеваний. 14 , 15 Кроме того, 2 больших метаанализа рандомизированных клинических испытаний, сравнивающих плацебо с отсутствием лечения, не смогли выявить значительных эффектов плацебо во многих типах исследований.В частности, чем объективнее оценка результатов, тем меньше вероятность того, что будет обнаружен какой-либо измеримый эффект плацебо. 15 , 16 Меньше известно о влиянии плацебо на младенцев, у которых любое улучшение обязательно определяется внешней оценкой, а не самоотчетом.
В этом контексте мы стремились проверить гипотезу о том, что распыленные NS могут быть активным лечением, а не плацебо для пациентов с острым вирусным бронхиолитом. Мы провели систематический обзор и метаанализ рандомизированных клинических испытаний острого вирусного бронхиолита с использованием небулайзированных НП с двумя целями: сравнить небулайзированные НП с другими формами плацебо (например, ненабулизованное плацебо или имитация небулайзера) и оценить связь небулайзированных НП. с краткосрочными физиологическими измерениями респираторного статуса в рандомизированных клинических испытаниях, в которых он использовался в качестве плацебо.
Мы провели систематический обзор и метаанализ рандомизированных клинических испытаний острого вирусного бронхиолита с использованием небулайзированных НП с двумя целями: сравнить небулайзированные НП с другими формами плацебо (например, ненабулизованное плацебо или имитация небулайзера) и оценить связь небулайзированных НП. с краткосрочными физиологическими измерениями респираторного статуса в рандомизированных клинических испытаниях, в которых он использовался в качестве плацебо.
Исследования рассматривались для включения, если они сообщали о результатах клинических испытаний пациентов в возрасте 2 лет или младше с первичным диагнозом острого вирусного бронхиолита, получавших небулайзерные НП.Для испытаний, сравнивающих небулайзерные NS с другим плацебо, дополнительно требовалось включение по крайней мере 1 группы лечения, получавшей только альтернативную форму плацебо. В этом обзоре учитывались только опубликованные исследования.
Источники информации и стратегия поиска
Это исследование было проведено в соответствии с Руководством по отчетности «Предпочтительные элементы отчетности для систематических обзоров и метаанализов» (PRISMA).Мы выполняли поиск в MEDLINE с 1946 по март 2019 года и в Scopus с 1976 по март 2019 года. Условия поиска показаны на электронном рисунке 1 в Приложении. Библиографии квалификационных исследований и соответствующие систематические обзоры также были вручную изучены на предмет дополнительных исследований кандидатов. Протокол обзора не был зарегистрирован до завершения исследования.
Исследования, выявленные на основе первоначальных результатов поиска, прошли проверку заголовков и аннотаций, проведенную двумя независимыми рецензентами (S. А.Х. и С.Л.Р.). Любые разногласия относительно включения разрешались консенсусом. Затем исследования исключались посредством полнотекстового обзора, если в них не предоставлялась информация о краткосрочных физиологических показателях респираторного статуса, которые определялись как совокупный респираторный балл, частота дыхания и / или значения сатурации кислорода в течение первого часа после лечения. Дополнительными критериями исключения были включение детей старше 2 лет и получение другого небулайзерного лекарства в группу NS в течение 1 часа после включения в исследование.Для исследований с неполными данными и тех, которые были исключены из-за отсутствия отчетов о краткосрочных физиологических исходах, в которых протокол исследования предполагал, что эти данные были собраны, с соответствующими авторами связались по электронной почте, чтобы определить, доступны ли эти дополнительные данные. Исследования иностранных языков были переведены на английский язык.
А.Х. и С.Л.Р.). Любые разногласия относительно включения разрешались консенсусом. Затем исследования исключались посредством полнотекстового обзора, если в них не предоставлялась информация о краткосрочных физиологических показателях респираторного статуса, которые определялись как совокупный респираторный балл, частота дыхания и / или значения сатурации кислорода в течение первого часа после лечения. Дополнительными критериями исключения были включение детей старше 2 лет и получение другого небулайзерного лекарства в группу NS в течение 1 часа после включения в исследование.Для исследований с неполными данными и тех, которые были исключены из-за отсутствия отчетов о краткосрочных физиологических исходах, в которых протокол исследования предполагал, что эти данные были собраны, с соответствующими авторами связались по электронной почте, чтобы определить, доступны ли эти дополнительные данные. Исследования иностранных языков были переведены на английский язык.
Извлечение данных было выполнено независимо двумя исследователями (S.A.H. и S.L.R.) с использованием стандартизированного листа извлечения данных, проведена перекрестная проверка на предмет согласия и передана третьему исследователю (A.М.Г.) при любых разногласиях. Извлеченные элементы данных включали условия исследования и географическое положение, типы вмешательств, средний или средний возраст пациентов, критерии тяжести заболевания для включения в исследование, респираторные баллы, частоту дыхания и насыщение кислородом. Для всех показателей результатов были собраны среднее и стандартное отклонение исходных значений и значений после лечения, когда они были доступны, и рассчитаны или условно рассчитаны на основе представленных данных, если они не доступны напрямую, с использованием методов, представленных в Кокрановском справочнике. 17 Предпочтительно использовались 60-минутные посттерапевтические меры; Когда 60-минутные измерения были недоступны, использовались 20-30-минутные меры постобработки.
Оценка качества и риск предвзятости
Пересмотренный Кокрановский инструмент риска систематической ошибки для рандомизированных клинических испытаний использовался для скрининга общего риска систематической ошибки в каждом включенном исследовании на уровне результатов, изученных в нашем метаанализе. Два исследователя (S.A.H. и S.L.R.) оценивали каждое исследование, используя этот инструмент; расхождения были отнесены к третьему автору исследования (А.M.G.) для разрешения.
Сводные показатели и синтез данных
Для исследований, оценивающих небулайзерные NS по сравнению с другим плацебо, рассчитывались средневзвешенные различия результатов между группами лечения. Для исследований, предоставляющих данные о лечении небулайзерами NS в течение времени, были рассчитаны средневзвешенные различия результатов в течение первых 60 минут исследования по сравнению с исходным уровнем исследования.Стандартизированные средние различия использовались при объединении респираторных баллов для всей когорты исследования, потому что для баллов по конкретным исследованиям используются разные шкалы; однако шкала была сохранена при анализе исследований подгрупп с использованием согласованной оценки. Точечные оценки и 95% доверительный интервал были рассчитаны с помощью взвешенных с обратной дисперсией моделей с фиксированными и случайными эффектами с использованием Комплексного метаанализа 2.0. Неоднородность оценивалась с использованием статистики I 2 .
Предварительно запланированные анализы подгрупп проводились на основе того, была ли исследуемая популяция амбулаторными или стационарными пациентами, и в исследованиях с использованием одного и того же инструмента респираторной оценки, когда этому критерию соответствовали более 5 исследований. Анализы чувствительности были выполнены путем последовательного удаления одного исследования, удаления выбросов, как определено из-за того, что ДИ отдельного исследования не перекрывает любой конец ДИ, созданных для точечных оценок, и путем удаления исследований с высоким риском систематической ошибки на основе пересмотренного Кокрановского риска инструмент смещения для рандомизированных исследований. 18
Анализы чувствительности были выполнены путем последовательного удаления одного исследования, удаления выбросов, как определено из-за того, что ДИ отдельного исследования не перекрывает любой конец ДИ, созданных для точечных оценок, и путем удаления исследований с высоким риском систематической ошибки на основе пересмотренного Кокрановского риска инструмент смещения для рандомизированных исследований. 18
Всего в ходе первоначального поиска в базе данных было обнаружено 1084 цитаты.Обзор библиографии включенных исследований и соответствующих метаанализов привел к дополнительным 26 кандидатским исследованиям. После удаления дубликатов было проанализировано 874 исследования, 118 из которых потенциально соответствовали критериям включения после проверки заголовка и аннотации. Восемьдесят девять исследований были исключены при полнотекстовом обзоре. Наиболее частой причиной исключения исследования из полнотекстового обзора было то, что в исследовании не были представлены данные по интересующим исходам. Двадцать девять исследований соответствовали критериям включения, основанным на опубликованных результатах. 19 -47 Дополнительные данные были запрошены по электронной почте от 5 авторов, и 3 ответили неопубликованными данными по 4 включенным исследованиям. 26 , 27,46 , 47 Выбор исследования показан на электронном рисунке 1 в Приложении. Было выявлено три исследования с участием группы, получающей плацебо без ингаляции. 26 , 27,32
В таблице представлена подробная информация о включенных исследованиях.Эти 29 испытаний были проведены во многих странах и оценивали ряд активных методов лечения, включая распыленный адреналин, альбутерол, гипертонический раствор, тербуталин, ипратропиум и фуросемид. Пятнадцать исследований были проведены в условиях стационара, 20 , 22 , 23,25 , 28 -30,33 , 37 , 38,40 , 41,44 – 46 и 14 были проведены в амбулаторных условиях. 19 , 21 , 24 , 26 , 27,31 , 32,34 -36,39 , 42 , 43,47 Всего было 1477 пациентов которые получали небулайзерный NS и 106 пациентов, получавших плацебо без распыления.Индекс оценки респираторного дистресса (RDAI) 48 был наиболее часто используемой системой оценки в 14 исследованиях. 20 , 21,23 , 24,28 , 33 , 34,36 , 38 -40,44 , 46 , 47 Около половины испытаний указали минимальный уровень тяжести заболевания для включения в исследование. 21 , 25 , 29 , 30,32 -37,39 -41,43 , 45 , 47
19 , 21 , 24 , 26 , 27,31 , 32,34 -36,39 , 42 , 43,47 Всего было 1477 пациентов которые получали небулайзерный NS и 106 пациентов, получавших плацебо без распыления.Индекс оценки респираторного дистресса (RDAI) 48 был наиболее часто используемой системой оценки в 14 исследованиях. 20 , 21,23 , 24,28 , 33 , 34,36 , 38 -40,44 , 46 , 47 Около половины испытаний указали минимальный уровень тяжести заболевания для включения в исследование. 21 , 25 , 29 , 30,32 -37,39 -41,43 , 45 , 47
Большинство исследований были классифицированы как имеющие некоторую озабоченность по поводу систематической ошибки, хотя было обнаружено, что 8 исследований имеют высокий риск систематической ошибки 20 , 23 , 25 , 29 , 31 , 32,41 , 44 (см. Рисунок 2 в Приложении).
Распылители NS против другого плацебо
В трех исследованиях сравнивали небулайзированные NS с плацебо, в том числе 2 с пероральным плацебо и 1 с использованием тумана. 26 , 27,32 Стандартизованные средние различия в баллах для группы NS (n = 102) по сравнению с другой группой плацебо (n = 106) благоприятствовали NS на -0.9 баллов (95% ДИ, от -1,2 до -0,6 балла) через 60 минут после терапии ( P <,001). Протоколы исследований в двух исследованиях, сравнивающих NS с пероральным плацебо, были идентичны, потому что они были выполнены одной и той же командой исследователей в 2 разных странах; Таким образом, мы проанализировали эти данные с сохранением респираторной шкалы. 26 , 27 Средневзвешенные различия в баллах для группы NS (n = 50) и группы перорального плацебо (n = 54) благоприятствовали NS на -1,6 балла (95% ДИ, -0.От 8 до -0,03 балла) по респираторной шкале для конкретного исследования (шкала от 0 до 20) через 60 минут после терапии ( P = 0,04). Не было различий в частоте дыхания или насыщении кислородом между группой, получавшей распыленный NS, и группой, получавшей другие плацебо.
26 , 27 Средневзвешенные различия в баллах для группы NS (n = 50) и группы перорального плацебо (n = 54) благоприятствовали NS на -1,6 балла (95% ДИ, -0.От 8 до -0,03 балла) по респираторной шкале для конкретного исследования (шкала от 0 до 20) через 60 минут после терапии ( P = 0,04). Не было различий в частоте дыхания или насыщении кислородом между группой, получавшей распыленный NS, и группой, получавшей другие плацебо.
Ассоциация небулайзированных НП с респираторными оценками
Всего в 25 исследованиях сообщалось о совокупных респираторных показателях с течением времени для пациентов, получавших небулайзерные NS. 20 , 21,24 -29,31 -47 Стандартизированная средняя разница в баллах в течение 60 минут после распыления NS уменьшилась на -0,7 (95% ДИ, от -0,7 до -0,6; I 2 = 62%; P <0,001) (Рисунок 1). Моделирование случайных эффектов и анализ подгрупп по условиям исследования существенно не изменили точечные оценки; однако гетерогенность оказалась связана с несогласованностью в подгруппе стационарных пациентов (амбулаторный I 2 = 4%; стационарный I 2 = 79%).
Ассоциация небулайзированных НП с оценкой RDAI
RDAI (шкала, 0-17 баллов) была единственной оценкой, использованной в достаточном количестве исследований для выполнения анализа подгруппы с сохранением шкалы. Всего в 13 исследованиях представлены данные RDAI 20 , 21,24 , 28 , 33 , 34,36 , 38 -40,44 , 46 , 47 ; В 1 исследовании использовалась эта система баллов, но исходные баллы не могли быть установлены, и поэтому баллы не анализировались для этого исследования. 23 Средневзвешенная разница в баллах в течение 60 минут после распыления NS уменьшилась на -1,6 балла (95% ДИ, -1,9 до -1,3 балла; I 2 = 72%; P <0,001) ( Фигура 2). Анализ подгрупп продемонстрировал снижение на -2,0 балла (95% ДИ, от -2,3 до -1,6 балла) в амбулаторной подгруппе по сравнению с уменьшением на -0,9 балла (95% ДИ, от -1,4 до -0,4 балла) в подгруппе стационарных пациентов. Моделирование случайных эффектов существенно не изменило точечные оценки, в то время как неоднородность, по-видимому, была связана с несогласованностью в подгруппе стационарных пациентов (амбулаторный I 2 = 42%; стационарный I 2 = 72%).
23 Средневзвешенная разница в баллах в течение 60 минут после распыления NS уменьшилась на -1,6 балла (95% ДИ, -1,9 до -1,3 балла; I 2 = 72%; P <0,001) ( Фигура 2). Анализ подгрупп продемонстрировал снижение на -2,0 балла (95% ДИ, от -2,3 до -1,6 балла) в амбулаторной подгруппе по сравнению с уменьшением на -0,9 балла (95% ДИ, от -1,4 до -0,4 балла) в подгруппе стационарных пациентов. Моделирование случайных эффектов существенно не изменило точечные оценки, в то время как неоднородность, по-видимому, была связана с несогласованностью в подгруппе стационарных пациентов (амбулаторный I 2 = 42%; стационарный I 2 = 72%).
Связь небулайзированных НП с частотой дыхания
В 17 исследованиях, предоставляющих данные о частоте дыхания, 19 -21,23 , 24,26 -28,30 , 33 -35,38 -40,43 , 47 средневзвешенная разница в течение 60 минут после распыления NS уменьшилась на -5.5 вдохов в минуту (95% ДИ, от -6,3 до -4,6 вдохов в минуту; I 2 = 24%; P <0,001) (Рисунок 3). Моделирование фиксированных эффектов и случайных эффектов и анализ подгрупп по условиям исследования существенно не изменили точечные оценки, и неоднородность в общем анализе была низкой.
Ассоциация небулайзированных НП с насыщением кислородом
В 23 исследованиях, предоставляющих данные о насыщении кислородом, 19 -28,30 , 32 -40,42 , 43,47 средневзвешенная разница в течение 60 минут после распыления NS уменьшилась на -0. .4% (95% ДИ, от -0,6% до -0,2%; I 2 = 79%; P <0,001) (Рисунок 4). Моделирование случайных эффектов существенно изменило общую точечную оценку в сторону незначительности (средняя разница, -0,3%; P = 0,10). Анализ подгрупп также дал незначительную точечную оценку в амбулаторной подгруппе (средняя разница 0,3%; P = 0,38). Кроме того, гетерогенность была высокой в подгруппе амбулаторных пациентов ( I 2 = 83%) по сравнению с подгруппой стационарных пациентов ( I 2 = 49%).
.4% (95% ДИ, от -0,6% до -0,2%; I 2 = 79%; P <0,001) (Рисунок 4). Моделирование случайных эффектов существенно изменило общую точечную оценку в сторону незначительности (средняя разница, -0,3%; P = 0,10). Анализ подгрупп также дал незначительную точечную оценку в амбулаторной подгруппе (средняя разница 0,3%; P = 0,38). Кроме того, гетерогенность была высокой в подгруппе амбулаторных пациентов ( I 2 = 83%) по сравнению с подгруппой стационарных пациентов ( I 2 = 49%).
Анализ чувствительности с удалением одного исследования не повлиял на общие точечные оценки ни для одного из анализов. Для RDAI анализ чувствительности, удаляющий выбросы 46 , снизил неоднородность до приемлемых уровней ( I 2 = 42%) при получении аналогичной точечной оценки (средняя разница, -1,9; 95% ДИ, от -2,2 до -1,6) . Что касается частоты дыхания, анализ чувствительности, удаляющий выбросы 19 , существенно не изменил результатов.Для насыщения кислородом анализ чувствительности с удалением выбросов 23 , 32 , 35 , 47 дал общую точечную оценку -0,2%, что не было статистически значимым ( P = 0,10) с приемлемой неоднородностью. ( I 2 = 24%).
Анализ чувствительности, исключающий исследования с высоким риском систематической ошибки в анализе респираторной оценки 20 , 25 , 29 , 31 , 32,41 , 44 не изменил существенно точечную оценку, хотя она пониженная неоднородность ( I 2 = 47%).Удаление исследований с высоким риском систематической ошибки в анализе RDAI 20 , 44 существенно не изменило точечную оценку или меры неоднородности. Удаление исследований с высоким риском систематической ошибки из анализа частоты дыхания 20 , 23 существенно не изменило точечную оценку или меры неоднородности. Удаление исследований с высоким риском систематической ошибки из анализа насыщения кислородом 20 , 23 , 25 , 32 не повлияло существенно на точечные оценки, хотя и привело к небольшому снижению неоднородности ( I 2 = 60%).
Удаление исследований с высоким риском систематической ошибки из анализа насыщения кислородом 20 , 23 , 25 , 32 не повлияло существенно на точечные оценки, хотя и привело к небольшому снижению неоднородности ( I 2 = 60%).
В этом систематическом обзоре рандомизированных клинических исследований с использованием распыленных НП в качестве плацебо мы обнаружили прямые и косвенные доказательства того, что НП может быть активным лечением, а не плацебо. Прямые доказательства получены из 3 исследований с участием более 200 пациентов, в которых распыленные NS оценивались по сравнению с другими плацебо и значительно улучшили респираторные показатели. Косвенные доказательства получены из значительно улучшенных оценок респираторных показателей и частоты дыхания до и после распыления NS в нескольких рандомизированных клинических испытаниях.Хотя качество этих доказательств невысокое из-за небольшого количества исследований в первом анализе и отсутствия группы сравнения во втором, оно согласуется с широким спектром исследований и согласуется. Наконец, в метаанализе была отмечена двусмысленная связь с насыщением кислородом с высокой неоднородностью в широкой выборке; Анализ подгрупп и анализ чувствительности, разрешающий эту неоднородность, позволяют предположить, что распыленные NS не связаны с насыщением кислородом.
Есть несколько возможных объяснений наших выводов. Возможно, что распыленный NS действительно не плацебо; то есть он оказывает небольшое благотворное влияние на маленьких детей с острым вирусным бронхиолитом за счет улучшения гидратации поверхностей дыхательных путей и слизистого просвета, а также снижения сопротивления верхних дыхательных путей. Также возможно, что клиническое течение бронхиолита усиливается и ослабевает независимо от оцениваемых небулайзированных НП или других методов лечения. Пациентам могут быть назначены жаропонижающие средства или назальное отсасывание, или они могут просто успокоиться после начальной фазы оценки, таким образом улучшившись.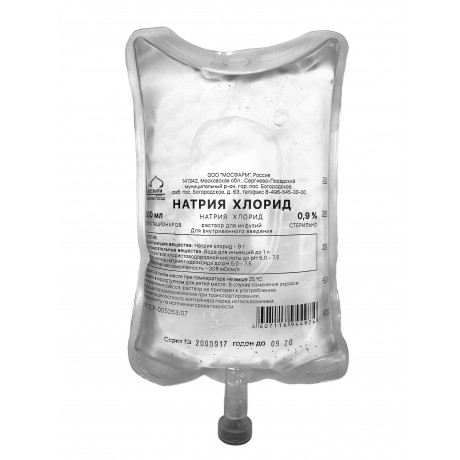 В нескольких исследованиях было отмечено, что частота дыхания и оценка дыхания коррелируют с состоянием пациента (например, бодрствование, сон или плач). 25 -27,33 Невозможно изолировать относительный эффект дополнительных симптоматических методов лечения или состояния пациента по сравнению с небулайзированным NS на результаты, оцениваемые в этом наборе данных. Третья возможность заключается в том, что основной метод оценки (респираторная оценка) является необъективным инструментом, который подвержен психологическим воздействиям на оценщика, и что эти повторяющиеся измерения имеют тенденцию регрессировать к среднему значению.Современное понимание эффекта плацебо стало более тонким, и кажется, что любой потенциально субъективный инструмент измерения симптомов (например, шкалы боли или депрессии) с большей вероятностью продемонстрирует эффект плацебо, чем объективные результаты. 15 Этот феномен также может быть связан с результатами, полученными с помощью инструментов респираторной оценки в нашем исследовании.
В нескольких исследованиях было отмечено, что частота дыхания и оценка дыхания коррелируют с состоянием пациента (например, бодрствование, сон или плач). 25 -27,33 Невозможно изолировать относительный эффект дополнительных симптоматических методов лечения или состояния пациента по сравнению с небулайзированным NS на результаты, оцениваемые в этом наборе данных. Третья возможность заключается в том, что основной метод оценки (респираторная оценка) является необъективным инструментом, который подвержен психологическим воздействиям на оценщика, и что эти повторяющиеся измерения имеют тенденцию регрессировать к среднему значению.Современное понимание эффекта плацебо стало более тонким, и кажется, что любой потенциально субъективный инструмент измерения симптомов (например, шкалы боли или депрессии) с большей вероятностью продемонстрирует эффект плацебо, чем объективные результаты. 15 Этот феномен также может быть связан с результатами, полученными с помощью инструментов респираторной оценки в нашем исследовании.
Мы не можем сделать однозначных выводов относительно лечения на основании наших результатов из-за большого количества описанных возможных объяснений и врожденной предвзятости, связанной с оценкой до и после лечения.Наши данные не должны влиять на существующее мнение о том, что активные методы лечения острого вирусного бронхиолита не изменяют течение болезни. Хотя наличие лечебного эффекта от лекарственного средства, назначенного в качестве вспомогательного средства обеим группам лечения в рандомизированном клиническом исследовании (либо в качестве плацебо-терапии, либо в качестве средства активной терапии), может усложнить анализ мощности исследования, нет никаких веских оснований полагать что это может повлиять на лечебный эффект от других активных лекарств.Как минимум, наши данные должны подчеркивать необходимость будущих рандомизированных клинических испытаний этого заболевания, чтобы учесть тот факт, что краткосрочные физиологические показатели будут иметь тенденцию к улучшению. Таким образом, анализ мощности должен будет учитывать снижение чувствительности к изменениям этих показателей.
Таким образом, анализ мощности должен будет учитывать снижение чувствительности к изменениям этих показателей.
Этот метаанализ имеет некоторые ограничения, в том числе неоднородность включенных испытаний с различными максимальными возрастами, популяциями и критериями тяжести заболевания для включения в исследование.Неоднородность исследования была чрезмерной для некоторых из наших совокупных анализов, хотя нам удалось разрешить ее до приемлемых уровней с помощью анализа подгрупп и чувствительности без изменения общих выводов. Весьма вероятно, что тяжесть заболевания будет иметь значительную связь с результатами нашего исследования, потому что пациенты с легкой формой заболевания могут иметь небольшой запас для улучшения, учитывая их относительно нормальные показатели жизнедеятельности и низкие показатели дистресса на исходном уровне. Кроме того, неясно клиническое значение краткосрочных физиологических результатов, которые мы предлагаем от лечения небулайзерами NS.Хотя снижение респираторной оценки и частоты дыхания может сигнализировать о краткосрочном клиническом улучшении, мы не оценивали другие соответствующие клинические исходы, более отражающие общее течение и тяжесть заболевания, такие как частота госпитализаций или продолжительность пребывания в больнице. Наконец, мы не приложили усилий для включения неопубликованных рефератов; таким образом, возможно, что недостающие данные могут изменить наши выводы, хотя такая возможность маловероятна, учитывая количество пациентов и включенных исследований.
Этот метаанализ предполагает, что распыленные NS могут быть активным средством лечения острого вирусного бронхиолита, а не инертным плацебо.Следует провести дополнительную оценку распыленных НП по сравнению с имитацией распыления и / или пероральным плацебо, чтобы установить, является ли распыленный НП истинным плацебо. Планы будущих исследований должны учитывать потенциальный лечебный эффект распыленных НП на краткосрочные исходы.
Принято к публикации: 9 сентября 2019 г.
Автор для корреспонденции: Шон Л. Ральстон, доктор медицины, кафедра педиатрии, Медицинская школа Джонса Хопкинса, 1800 Орлеан Авеню, Блумберг 8470, Балтимор, Мэриленд 21287 (sralsto3 @jhmi.эду).
Опубликовано онлайн: 6 января 2020 г. doi: 10.1001 / jamapediatrics.2019.5195
Вклад авторов: Доктор Хаус и Ральстон имели полный доступ ко всем данным в исследовании и несут ответственность за целостность данных и точность анализа данных.
Концепция и дизайн: Все авторы.
Сбор, анализ или интерпретация данных: Все авторы.
Составление рукописи: Все авторы.
Критический пересмотр рукописи на предмет важного интеллектуального содержания: Все авторы.
Статистический анализ: Все авторы.
Административная, техническая или материальная поддержка: House, Gadomski.
Раскрытие информации о конфликте интересов: Не сообщалось.
Дополнительные вклады: Пейдж Н. Скаддер, MLIS, биомедицинские библиотеки, Дартмутский колледж, оказала помощь в первоначальном поиске литературы.За свой вклад она не получила компенсации.
1.Хартлинг L, Бялы Л. М., Вандермейер B, и другие. Адреналин при бронхиолите. Кокрановская база данных Syst Rev . 2011; (6): CD003123.PubMedGoogle Scholar4.Gadomski AM, Скрибани МБ. Бронходилататоры при бронхиолите. Кокрановская база данных Syst Rev . 2014; (6): CD001266.PubMedGoogle Scholar8.Harrison. W, Ангулвант F, дом S, Гайдос V, Ралстон SL.Гипертонический раствор при бронхиолите и ошибке I типа: пробный последовательный анализ. Педиатрия . 2018; 142 (3): e20181144. DOI: 10.1542 / peds.2018-1144PubMedGoogle Scholar17.Higgins JPT, Green S, eds. Справочник по систематическим обзорам вмешательств . Версия 5.1.0. Кокрановское сотрудничество .. http://handbook-5-1.cochrane.org/. Обновлено в марте 2011 г. Проверено 7 июля 2018 г. 188. Хиггинс
JPT, Стерн
JAC, Савович
J,
и другие. Пересмотренный инструмент для оценки риска систематической ошибки в рандомизированных исследованиях. Кокрановская база данных Syst Rev . 2016; 10 (приложение 1): 29-31.Google Scholar20.Lines
DR, Каттампаллил
JS, Листон
P. Эффективность распыления сальбутамола при бронхиолите. Pediatric Rev Commun. 1990; 5: 121-129.Google Scholar 23.Lines
ДР, Бейтс
М.Л., Рехтман
AR, Саммартино
LP. Эффективность распыления бромида ипратропия при остром бронхиолите. Педиатрическая Революция . 1992; 6: 161-167.Google Scholar, 25, Кристьянссон.
С, Лёдруп Карлсен
KC, Веннергрен
G, Страннегард
Иллинойс, Карлсен
KH.Распыленный рацемический адреналин в лечении острого бронхиолита у младенцев и детей ясельного возраста. Арка Дис Детский . 1993; 69 (6): 650-654. DOI: 10.1136 / adc.69.6.650PubMedGoogle ScholarCrossref 27.Gadomski
AM, Лихенштейн
Р., Хортон
L, король
Джей, Кин
V, Пермутт
Т. Эффективность альбутерола при лечении бронхиолита. Педиатрия . 1994; 93 (6, pt 1): 907-912.PubMedGoogle Scholar35.Khashabi
J, Салари
S, Карамияр
М, Муссави
ЧАС.Сравнение эффективности распыленного l-адреналина, сальбутамола и физиологического раствора при остром бронхиолите: рандомизированное клиническое испытание. Med J Islam Repub Iran .
2018; 142 (3): e20181144. DOI: 10.1542 / peds.2018-1144PubMedGoogle Scholar17.Higgins JPT, Green S, eds. Справочник по систематическим обзорам вмешательств . Версия 5.1.0. Кокрановское сотрудничество .. http://handbook-5-1.cochrane.org/. Обновлено в марте 2011 г. Проверено 7 июля 2018 г. 188. Хиггинс
JPT, Стерн
JAC, Савович
J,
и другие. Пересмотренный инструмент для оценки риска систематической ошибки в рандомизированных исследованиях. Кокрановская база данных Syst Rev . 2016; 10 (приложение 1): 29-31.Google Scholar20.Lines
DR, Каттампаллил
JS, Листон
P. Эффективность распыления сальбутамола при бронхиолите. Pediatric Rev Commun. 1990; 5: 121-129.Google Scholar 23.Lines
ДР, Бейтс
М.Л., Рехтман
AR, Саммартино
LP. Эффективность распыления бромида ипратропия при остром бронхиолите. Педиатрическая Революция . 1992; 6: 161-167.Google Scholar, 25, Кристьянссон.
С, Лёдруп Карлсен
KC, Веннергрен
G, Страннегард
Иллинойс, Карлсен
KH.Распыленный рацемический адреналин в лечении острого бронхиолита у младенцев и детей ясельного возраста. Арка Дис Детский . 1993; 69 (6): 650-654. DOI: 10.1136 / adc.69.6.650PubMedGoogle ScholarCrossref 27.Gadomski
AM, Лихенштейн
Р., Хортон
L, король
Джей, Кин
V, Пермутт
Т. Эффективность альбутерола при лечении бронхиолита. Педиатрия . 1994; 93 (6, pt 1): 907-912.PubMedGoogle Scholar35.Khashabi
J, Салари
S, Карамияр
М, Муссави
ЧАС.Сравнение эффективности распыленного l-адреналина, сальбутамола и физиологического раствора при остром бронхиолите: рандомизированное клиническое испытание. Med J Islam Repub Iran . 2005; 19 (2): 119-125.Google Scholar, 36. Ralston.
S, Хартенбергер
C, Анайя
Т, Куоллс
C, Келли
HW. Рандомизированное плацебо-контролируемое исследование альбутерола и адреналина в равных дозах бета-2-агонистов при остром бронхиолите. Пульмонол Педиатр . 2005; 40 (4): 292-299. DOI: 10.1002 / ppul.20260PubMedGoogle ScholarCrossref 37.Karadag
B, Ceran
О, Гювен
ГРАММ,
и другие. Эффективность сальбутамола и ипратропия бромида в лечении острого бронхиолита – клиническое испытание. Дыхание . 2008; 76 (3): 283-287. DOI: 10.1159 / 000111817PubMedGoogle ScholarCrossref 38.Bar
А, Сруго
Я, Амирав
Я, Цверлинг
C, Нафтали
Г, Кугельман
A. Ингаляционный фуросемид у госпитализированных младенцев с вирусным бронхиолитом: рандомизированное двойное слепое плацебо-контролируемое пилотное исследование. Пульмонол Педиатр . 2008; 43 (3): 261-267. DOI: 10.1002 / ppul.20765PubMedGoogle ScholarCrossref 40.Tinsa
F, Бен Рума
А, Гаффари
ЧАС,
и другие. Рандомизированное контролируемое исследование распыленного тербуталина при первом остром бронхиолите у детей младше 12 месяцев. Тунис Мед . 2009; 87 (3): 200-203.PubMedGoogle Scholar42.Anil
AB, Анил
М, Саглам
AB, Цетин
Н, Бал
А, Аксу
N. Большой объем физиологического раствора такой же эффективен, как распыленный сальбутамол-физиологический раствор, адреналин-физиологический раствор и 3% -ный физиологический раствор при легком бронхиолите. Пульмонол Педиатр . 2010; 45 (1): 41-47. DOI: 10.1002 / ppul.21108PubMedGoogle ScholarCrossref 43.Ipek
И.О., Ялчин
ЕС, Сезер
РГ, Бозайкут
A. Эффективность распыления сальбутамола, гипертонического раствора и комбинации сальбутамол / гипертонический раствор при умеренном бронхиолите.
2005; 19 (2): 119-125.Google Scholar, 36. Ralston.
S, Хартенбергер
C, Анайя
Т, Куоллс
C, Келли
HW. Рандомизированное плацебо-контролируемое исследование альбутерола и адреналина в равных дозах бета-2-агонистов при остром бронхиолите. Пульмонол Педиатр . 2005; 40 (4): 292-299. DOI: 10.1002 / ppul.20260PubMedGoogle ScholarCrossref 37.Karadag
B, Ceran
О, Гювен
ГРАММ,
и другие. Эффективность сальбутамола и ипратропия бромида в лечении острого бронхиолита – клиническое испытание. Дыхание . 2008; 76 (3): 283-287. DOI: 10.1159 / 000111817PubMedGoogle ScholarCrossref 38.Bar
А, Сруго
Я, Амирав
Я, Цверлинг
C, Нафтали
Г, Кугельман
A. Ингаляционный фуросемид у госпитализированных младенцев с вирусным бронхиолитом: рандомизированное двойное слепое плацебо-контролируемое пилотное исследование. Пульмонол Педиатр . 2008; 43 (3): 261-267. DOI: 10.1002 / ppul.20765PubMedGoogle ScholarCrossref 40.Tinsa
F, Бен Рума
А, Гаффари
ЧАС,
и другие. Рандомизированное контролируемое исследование распыленного тербуталина при первом остром бронхиолите у детей младше 12 месяцев. Тунис Мед . 2009; 87 (3): 200-203.PubMedGoogle Scholar42.Anil
AB, Анил
М, Саглам
AB, Цетин
Н, Бал
А, Аксу
N. Большой объем физиологического раствора такой же эффективен, как распыленный сальбутамол-физиологический раствор, адреналин-физиологический раствор и 3% -ный физиологический раствор при легком бронхиолите. Пульмонол Педиатр . 2010; 45 (1): 41-47. DOI: 10.1002 / ppul.21108PubMedGoogle ScholarCrossref 43.Ipek
И.О., Ялчин
ЕС, Сезер
РГ, Бозайкут
A. Эффективность распыления сальбутамола, гипертонического раствора и комбинации сальбутамол / гипертонический раствор при умеренном бронхиолите. Пульм Фармакол Тер . 2011; 24 (6): 633-637. DOI: 10.1016 / j.pupt.2011.09.004PubMedGoogle ScholarCrossref 44.Scarlett
EE, Уокер
S, Ровителли
А, Рен
CL.Ответы приливного дыхания на альбутерол и физиологический раствор у младенцев с вирусным бронхиолитом. Детская аллергия Immunol Pulmonol . 2012; 25 (4): 220-224. DOI: 10.1089 / ped.2012.0141Google ScholarCrossref 45.Tinsa
Ф, Абделькафи
С, Бель Хадж
Я,
и другие. Рандомизированное контролируемое исследование распыленного 5% гипертонического раствора и смешанного 5% гипертонического раствора с адреналином при бронхиолите. Тунис Мед . 2014; 92 (11): 674-677.PubMedGoogle Scholar47.Angoulvant
F, Bellêttre
X, Милсент
K,
и другие; Эффективность 3% гипертонического раствора в группе исследования острого вирусного бронхиолита (ГЕРАНДИЯ).Влияние распыления гипертонического солевого раствора в отделениях неотложной помощи на частоту госпитализаций по поводу острого бронхиолита: рандомизированное клиническое исследование. Педиатр JAMA . 2017; 171 (8): e171333. DOI: 10.1001 / jamapediatrics.2017.1333PubMedGoogle Scholar48.Lowell
DI, Lister
G, фон Косс
H, Маккарти
П. Свистящее дыхание у младенцев: ответ на адреналин. Педиатрия . 1987; 79 (6): 939-945.PubMedGoogle Scholar
Пульм Фармакол Тер . 2011; 24 (6): 633-637. DOI: 10.1016 / j.pupt.2011.09.004PubMedGoogle ScholarCrossref 44.Scarlett
EE, Уокер
S, Ровителли
А, Рен
CL.Ответы приливного дыхания на альбутерол и физиологический раствор у младенцев с вирусным бронхиолитом. Детская аллергия Immunol Pulmonol . 2012; 25 (4): 220-224. DOI: 10.1089 / ped.2012.0141Google ScholarCrossref 45.Tinsa
Ф, Абделькафи
С, Бель Хадж
Я,
и другие. Рандомизированное контролируемое исследование распыленного 5% гипертонического раствора и смешанного 5% гипертонического раствора с адреналином при бронхиолите. Тунис Мед . 2014; 92 (11): 674-677.PubMedGoogle Scholar47.Angoulvant
F, Bellêttre
X, Милсент
K,
и другие; Эффективность 3% гипертонического раствора в группе исследования острого вирусного бронхиолита (ГЕРАНДИЯ).Влияние распыления гипертонического солевого раствора в отделениях неотложной помощи на частоту госпитализаций по поводу острого бронхиолита: рандомизированное клиническое исследование. Педиатр JAMA . 2017; 171 (8): e171333. DOI: 10.1001 / jamapediatrics.2017.1333PubMedGoogle Scholar48.Lowell
DI, Lister
G, фон Косс
H, Маккарти
П. Свистящее дыхание у младенцев: ответ на адреналин. Педиатрия . 1987; 79 (6): 939-945.PubMedGoogle Scholar% PDF-1.4
%
19 0 объект
>
эндобдж
xref
19 115
0000000016 00000 н.
0000002649 00000 н.
0000003112 00000 н.
0000003712 00000 н.
0000003915 00000 н.
0000004078 00000 н.
0000004471 00000 н.
0000004688 00000 п.
0000006877 00000 н.
0000007045 00000 н.
0000007610 00000 п.
0000007833 00000 н.
0000007862 00000 н.
0000008261 00000 п.
0000008493 00000 п.
0000010686 00000 п.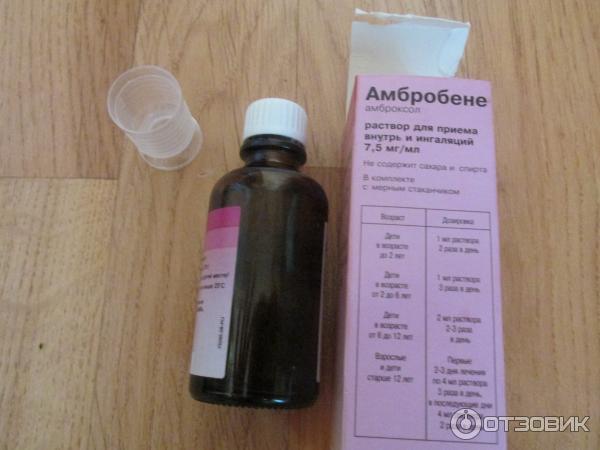 0000010760 00000 п.
0000012953 00000 п.
0000013059 00000 п.
0000013236 00000 п.
0000013265 00000 п.
0000013286 00000 п.
0000014200 00000 н.
0000016393 00000 п.
0000016623 00000 п.
0000016797 00000 п.
0000017184 00000 п.
0000017205 00000 п.
0000018064 00000 п.
0000018085 00000 п.
0000018922 00000 п.
0000019156 00000 п.
0000020379 00000 п.
0000051883 00000 п.
0000052213 00000 п.
0000052318 00000 п.
0000052339 00000 п.
0000053150 00000 п.
0000053171 00000 п.
0000054148 00000 п.
0000054223 00000 п.
0000054292 00000 п.
0000054313 00000 п.
0000055079 00000 п.
0000055100 00000 п.
0000055691 00000 п.
0000055712 00000 п.
0000056421 00000 п.
0000056981 00000 п.
0000057777 00000 п.
0000068908 00000 п.
0000068931 00000 п.
0000072321 00000 п.
0000083450 00000 п.
0000083473 00000 п.
0000083496 00000 п.
0000083519 00000 п.
0000094479 00000 п.
0000105874 00000 н.
0000105900 00000 н.
0000105926 00000 н.
0000105952 00000 н.
0000106085 00000 н.
0000106111 00000 п.
0000106137 00000 п.
0000106163 00000 п.
0000106294 00000 п.
0000106320 00000 н.
0000106346 00000 п.
0000106372 00000 п.
0000106504 00000 н.
0000106632 00000 н.
0000106658 00000 п.
0000106684 00000 п.
0000106710 00000 н.
0000106841 00000 н.
0000106867 00000 н.
0000106893 00000 п.
0000106919 00000 п.
0000107052 00000 п.
0000107078 00000 п.
0000107104 00000 п.
0000107131 00000 п.
0000107264 00000 н.
0000107291 00000 н.
0000107318 00000 н.
0000107345 00000 п.
0000107482 00000 н.
0000107509 00000 н.
0000107536 00000 п.
0000107563 00000 н.
0000107698 00000 п.
0000107725 00000 н.
0000107752 00000 н.
0000107779 00000 п.
0000107916 00000 п.
0000107943 00000 п.
0000107970 00000 п.
0000107997 00000 н.
0000108132 00000 н.
0000108159 00000 н.
0000108186 00000 п.
0000108213 00000 п.
0000108350 00000 н.
0000108377 00000 н.
0000108404 00000 н.
0000108431 00000 н.
0000108567 00000 н.
0000108673 00000 п.
0000108780 00000 н.
0000117518 00000 п.
0000139315 00000 н.
0000010760 00000 п.
0000012953 00000 п.
0000013059 00000 п.
0000013236 00000 п.
0000013265 00000 п.
0000013286 00000 п.
0000014200 00000 н.
0000016393 00000 п.
0000016623 00000 п.
0000016797 00000 п.
0000017184 00000 п.
0000017205 00000 п.
0000018064 00000 п.
0000018085 00000 п.
0000018922 00000 п.
0000019156 00000 п.
0000020379 00000 п.
0000051883 00000 п.
0000052213 00000 п.
0000052318 00000 п.
0000052339 00000 п.
0000053150 00000 п.
0000053171 00000 п.
0000054148 00000 п.
0000054223 00000 п.
0000054292 00000 п.
0000054313 00000 п.
0000055079 00000 п.
0000055100 00000 п.
0000055691 00000 п.
0000055712 00000 п.
0000056421 00000 п.
0000056981 00000 п.
0000057777 00000 п.
0000068908 00000 п.
0000068931 00000 п.
0000072321 00000 п.
0000083450 00000 п.
0000083473 00000 п.
0000083496 00000 п.
0000083519 00000 п.
0000094479 00000 п.
0000105874 00000 н.
0000105900 00000 н.
0000105926 00000 н.
0000105952 00000 н.
0000106085 00000 н.
0000106111 00000 п.
0000106137 00000 п.
0000106163 00000 п.
0000106294 00000 п.
0000106320 00000 н.
0000106346 00000 п.
0000106372 00000 п.
0000106504 00000 н.
0000106632 00000 н.
0000106658 00000 п.
0000106684 00000 п.
0000106710 00000 н.
0000106841 00000 н.
0000106867 00000 н.
0000106893 00000 п.
0000106919 00000 п.
0000107052 00000 п.
0000107078 00000 п.
0000107104 00000 п.
0000107131 00000 п.
0000107264 00000 н.
0000107291 00000 н.
0000107318 00000 н.
0000107345 00000 п.
0000107482 00000 н.
0000107509 00000 н.
0000107536 00000 п.
0000107563 00000 н.
0000107698 00000 п.
0000107725 00000 н.
0000107752 00000 н.
0000107779 00000 п.
0000107916 00000 п.
0000107943 00000 п.
0000107970 00000 п.
0000107997 00000 н.
0000108132 00000 н.
0000108159 00000 н.
0000108186 00000 п.
0000108213 00000 п.
0000108350 00000 н.
0000108377 00000 н.
0000108404 00000 н.
0000108431 00000 н.
0000108567 00000 н.
0000108673 00000 п.
0000108780 00000 н.
0000117518 00000 п.
0000139315 00000 н.

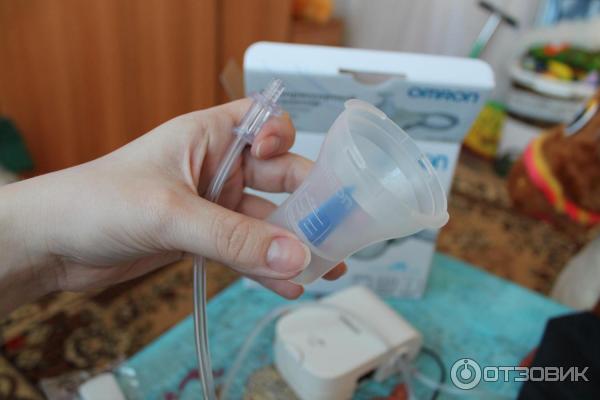 5 грамм
5 грамм Способствуют подавлению патогенных микроорганизмов, применяются для лечения инфекционных заболеваний дыхательных путей.
Способствуют подавлению патогенных микроорганизмов, применяются для лечения инфекционных заболеваний дыхательных путей.