Калия перманганат – официальная инструкция по применению, аналоги, цена, наличие в аптеках
ИНСТРУКЦИЯ
по медицинскому применению препарата
003587/01
Торговое название препарата: Калия перманганат
Международное непатентованное название препарата: Калия перманганат
Химическое название: Калий марганцевокислый
Лекарственная форма:
порошок для приготовления раствора для наружного применения.Состав:
препарат содержит не менее 99,0 % КMnО4.Описание: темно- или красно-фиолетовые кристаллы или мелкий кристаллический порошок с металлическим блеском.
Фармакотерапевтическая группа:
антисептическое средство.Код АТХ [D08AX06]
Фармакологическое действие: антисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении калия перманганата марганца оксид образует с белками комплексные соединения – альбуминаты (за счет этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах – раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв.
Образующийся при восстановлении калия перманганата марганца оксид образует с белками комплексные соединения – альбуминаты (за счет этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах – раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв.
Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях. При попадании внутрь всасывается, оказывая гематотоксическое действие (приводит к развитию метгемоглобинемии).
Показания: смазывание язвенных и ожоговых поверхностей – инфицированные раны, язвы и ожоги кожи.
Полоскание полости рта и ротоглотки – при инфекционно-воспалительных заболеваниях слизистой оболочки рта и ротоглотки (в т.ч. ангинах).
Для промывания и спринцеваний при гинекологических и урологических заболеваниях – кольпиты и уретриты.
Для промываний желудка – при отравлениях, вызванных приемом внутрь алкалоидов (морфин, аконитин, никотин), синильной кислоты, фосфором, хинином; кожи – при попадании на нее анилина; глаз – при поражении их ядовитыми насекомыми.
Противопоказания:
гиперчувствительность.Способ применения и дозы:
наружно, в водных растворах для промывания ран (0,1-0,5 %), для полоскания рта и горла (0,01-0,1 %), для смазывания язвенных и ожоговых поверхностей (2-5 %), для спринцеваний (0,02-0,1 %) в гинекологической и урологической практике, а также промывания желудка при отравлениях.Для растворения – несколько кристаллов помещают в стакан с теплой водой и перемешивают, раствор используют только свежеприготовленным.
Побочные эффекты: аллергические реакции, при использовании концентрированных растворов – ожоги и раздражения.
Передозировка:
симптомы: резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки – отечная, темно-коричневого, фиолетового цвета, возможен отек гортани, развитие механической асфиксии, ожогового шока, двигательного возбуждения, судорог, явлений паркинсонизма, геморрагического колита, нефропатии, гепатопатии.
Лечение: метиленовый синий (50 мл 1 % раствора), аскорбиновая кислота (в/в – 30 мл 5 % раствора), цианокобаламин – до 1 мг, пиридоксин (в/м – 3 мл 5 % раствора).
Взаимодействие: химически не совместим с некоторыми органическими веществами (уголь, сахар, танин) и легко окисляющимися веществами – может произойти взрыв.
Форма выпуска:
порошок по 3 г в стеклянных пробирках, флаконах, банках с инструкцией в пачку, пакетах полиэтиленовых.Срок годности:
5 лет. Не использовать позже даты, указанной на упаковке.Условия хранения:
в сухом месте, недоступном для детей.Условия отпуска из аптек:
без рецепта.Производитель:
ЗАО «Ярославская фармацевтическая фабрика» Россия 150030 г.(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Калия перманганат 3 г — инструкция по применению
Торговое наименование
Калия перманганат
Международное непатентованное наименование
Лекарственная форма
порошок для приготовления раствора для местного и наружного применения
Состав
Калия перманганат 3 г.
Описание
Тёмно- или красно-фиолетовые кристаллы или мелкий кристаллический порошок с металлическим блеском.
Фармакотерапевтическая группа
Фармакологическое действие
Антисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении калия перманганата марганца оксид образует с белками комплексные соединения — альбуминаты (за счёт этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах — раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв.
Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях и пищевых токсикоинфекциях. При попадании внутрь всасывается, оказывая гематотоксическое действие (приводит к развитию метгемоглобинемии).
Препарат относится к списку № 4 перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в РФ.
Показания
Смазывание язвенных и ожоговых поверхностей — инфицированные раны, язвы и ожоги кожи.
Полоскание полости рта и ротоглотки — при инфекционно-воспалительных заболеваниях слизистой оболочки полости рта и ротоглотки (в том числе ангинах).
Для промывания и спринцеваний при гинекологических и урологических заболеваниях — кольпиты и уретриты.
Для промываний — желудка при отравлениях, вызванных приёмом внутрь алкалоидов (морфин, аконитин, никотин), синильной кислотой, фосфором, хинином; кожи — при попадании на неё анилина; глаз — при поражении их ядовитыми насекомыми.
Способ применения и дозы
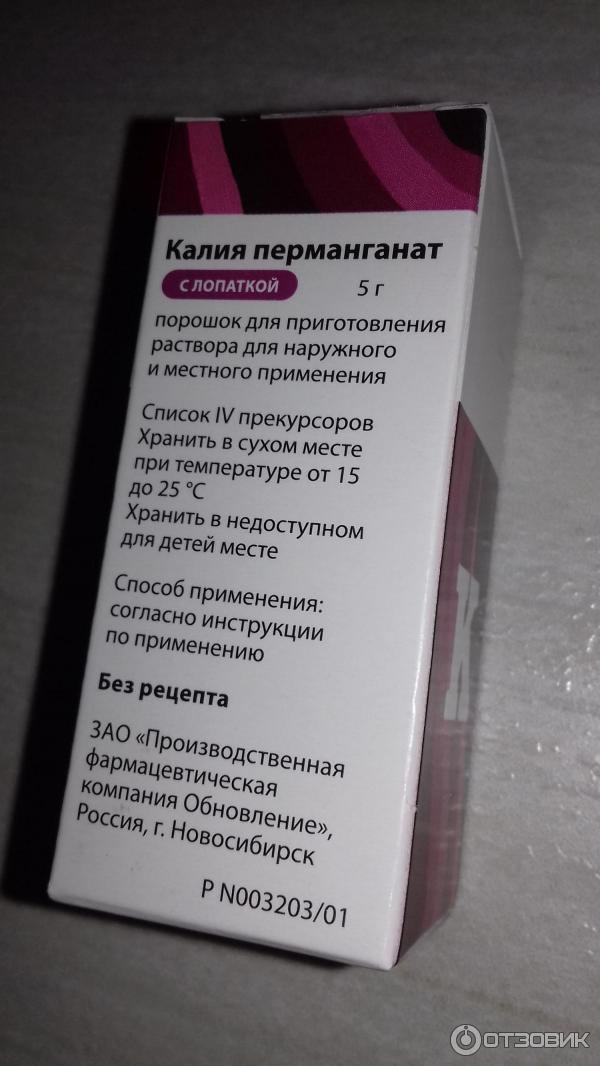 В виде водных растворах для промывания ран (0,1–0,5 %), для полоскания рта и горла (0,01-0,1 %), для смазывания язвенных и ожоговых поверхностей (2–5 %), для спринцеваний (0,02–0,1 %), в гинекологической и урологической практике, а также промывания желудка при отравлениях.
В виде водных растворах для промывания ран (0,1–0,5 %), для полоскания рта и горла (0,01-0,1 %), для смазывания язвенных и ожоговых поверхностей (2–5 %), для спринцеваний (0,02–0,1 %), в гинекологической и урологической практике, а также промывания желудка при отравлениях.Для растворения — несколько кристаллов помещают в стакан с тёплой водой и перемешивают, раствор используют только свежеприготовленным.
Передозировка
Симптомы: резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки — отёчная, темно-коричневого, фиолетового цвета, возможен отёк гортани, развитие механической асфиксии, ожогового шока, двигательного возбуждения, су
инструкция по применению, аналоги, состав, показания
Частные клиники, центры
Специализированные центры
Государственные учреждения
Детские лечебные учреждения
Экстренная медицина
Калия перманганат : Инструкция по применению : Описание препарата : Цена на EUROLAB
Действие обусловлено сильными окисляющими свойствами.
Промывание ран, язв, ожогов; спринцевание и промывание в гинекологической и урологической практике; промывание желудка при отравлениях, вызванных приемом внутрь морфина, аконитина и других алкалоидов, а также фосфора.
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;порошок для приготовления раствора для наружного применения; банка (баночка) 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 15 г;
порошок для приготовления раствора для наружного применения; пробирка 3 г;
порошок для приготовления раствора для наружного применения; пробирка 5 г;
порошок для приготовления раствора для наружного применения; пробирка 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 15 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 5 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) 15 г;
порошок для приготовления раствора для наружного применения; пробирка 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; пробирка 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г, пачка картонная 50;
порошок для приготовления раствора для наружного применения; пробирка 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; банка (баночка) 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) темного стекла 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) темного стекла 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) темного стекла 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 15 г;
порошок для приготовления раствора для наружного применения; пробирка 3 г;
порошок для приготовления раствора для наружного применения; пробирка 5 г;
порошок для приготовления раствора для наружного применения; пробирка 15 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 3 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 5 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 15 г;
Антисептическое средство. Действие обусловлено сильными окисляющими свойствами.
Действие обусловлено сильными окисляющими свойствами.
Повышенная чувствительность к калия перманганату.
Использование концентрированного раствора может вызвать повреждение окружающих тканей.
Для промывания ран используется 0.1-0.5% раствор, для полоскания горла – 0.01-0.1%, для смазывания язвенных и ожоговых поверхностей – 2-5%, для спринцеваний и промываний в гинекологической и урологической практике – 0.02-0.1%; для промывания желудка – 0.02-0.1%.
Даже при высоком разведении раствор калия перманганата при наружном применении окрашивает кожу в коричневый цвет. Симптомы интоксикации, которые могут развиться при приеме внутрь раствора калия перманганата в чрезмерно высокой концентрации: тошнота, рвота с коричневатой примесью; разъедание, отек, коричневая окраска слизистой оболочки полости рта, желудочно-кишечное кровотечение, повреждение печени и почек, угнетение деятельности сердца.
Раствор калия перманганата нельзя использовать в качестве средства для аборта, поскольку введение препарата в высоких концентрациях во влагалище вызывает глубокий ожог, тяжелое кровотечение и перфорацию стенки влагалища, что может привести к перитониту; возможен также сосудистый коллапс.
В сухом месте.
60 мес.
Калия перманганат (Kalii permanganate): описание, рецепт, инструкция
Kalii permanganate
Аналоги (дженерики, синонимы)
Калий марганцовокислый, перманганат калия, марганцовка
Действующее вещество
Калия перманганат (Kalii permanganas)
Фармакологическая группа
Антисептики и дезинфицирующие средства
Рецепт
Международный:
Rp.: Sol. Kalii permanganatis 0,1 % 500 ml
D.S. Для промывания ран
Rp.: Sol. Kalii permanganatis 1 % 20 ml
D.S. По 30 – 40 капель на стакан воды (для полоскания)
Rp.: Sol. Kalii permanganatis 5% 50 мл
DS. Для обработки ожогов
Россия:
Отпускается без рецепта
Фармакологическое действие
Антисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении препарата оксид образует с белками комплексные соединения – альбуминаты (за счет этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах – раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв.
Образующийся при восстановлении препарата оксид образует с белками комплексные соединения – альбуминаты (за счет этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах – раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв.
Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях неизвестным ядом и пищевых токсикоинфекциях.
При попадании внутрь всасывается, оказывая гематотоксическое действие (приводит к развитию метгемоглобинемии).
Способ применения
Для взрослых:
Наружно в водных растворах для промывания ран (0,1-0,5%), для полоскания полости рта и горла (0,01-0,1%), для смазываний язвенных и ожоговых поверхностей (2-5%), для спринцеваний и промываний в гинекологической и урологической практике (0,02-0,1%).
Раствор (0,02-0,1%) применяют также для промывания желудка при отравлениях, вызванных приемом внутрь морфина, аконитина и других алкалоидов, а также фосфора.
Показания
Применяют как антисептиче
Калия перманганат: инструкция по применению препарата
Промывание ран, язв, ожогов; спринцевание и промывание в гинекологической и урологической практике; промывание желудка при отравлениях, вызванных приемом внутрь морфина, аконитина и других алкалоидов, а также фосфора.
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;порошок для приготовления раствора для наружного применения; банка (баночка) 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 15 г;
порошок для приготовления раствора для наружного применения; пробирка 3 г;
порошок для приготовления раствора для наружного применения; пробирка 5 г;
порошок для приготовления раствора для наружного применения; пробирка 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 15 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 5 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) 15 г;
порошок для приготовления раствора для наружного применения; пробирка 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; пробирка 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г, пачка картонная 50;
порошок для приготовления раствора для наружного применения; пробирка 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; банка (баночка) 3 г, пачка картонная 1;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) темного стекла 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) темного стекла 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) темного стекла 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) с винтовой горловиной 15 г;
порошок для приготовления раствора для наружного применения; пробирка 3 г;
порошок для приготовления раствора для наружного применения; пробирка 5 г;
порошок для приготовления раствора для наружного применения; пробирка 15 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 3 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 5 г;
порошок для приготовления раствора для наружного применения; банка (баночка) 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 15 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 3 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 5 г;
порошок для приготовления раствора для наружного применения; пакет (пакетик) полиэтиленовый 15 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 3 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 5 г;
порошок для приготовления раствора для наружного применения; флакон (флакончик) 15 г;
Антисептическое средство. Действие обусловлено сильными окисляющими свойствами.
Действие обусловлено сильными окисляющими свойствами.
Повышенная чувствительность к калия перманганату.
Использование концентрированного раствора может вызвать повреждение окружающих тканей.
Для промывания ран используется 0.1-0.5% раствор, для полоскания горла – 0.01-0.1%, для смазывания язвенных и ожоговых поверхностей – 2-5%, для спринцеваний и промываний в гинекологической и урологической практике – 0.02-0.1%; для промывания желудка – 0.02-0.1%.
Даже при высоком разведении раствор калия перманганата при наружном применении окрашивает кожу в коричневый цвет. Симптомы интоксикации, которые могут развиться при приеме внутрь раствора калия перманганата в чрезмерно высокой концентрации: тошнота, рвота с коричневатой примесью; разъедание, отек, коричневая окраска слизистой оболочки полости рта, желудочно-кишечное кровотечение, повреждение печени и почек, угнетение деятельности сердца.
Раствор калия перманганата нельзя использовать в качестве средства для аборта, поскольку введение препарата в высоких концентрациях во влагалище вызывает глубокий ожог, тяжелое кровотечение и перфорацию стенки влагалища, что может привести к перитониту; возможен также сосудистый коллапс.
В сухом месте.
60 мес.
Перманганат калия (Kmno4) | Использование, физические и химические свойства перманганата калия
Что такое перманганат калия?
Перманганат калия – это универсальное химическое соединение пурпурного цвета.
Это калиевая соль марганцевой кислоты.
Также известный как перманганат калия, он имеет много других названий, таких как минерал хамелеон, кристаллы Конди и гипермаган.
Перманганат калия был впервые произведен немецким химиком Иоганном Рудольфом Глаубером в 1659 году, но вскоре о нем забыли.Он был заново открыт британским химиком Генри Конди, который производил дезинфицирующие средства, известные как «кристаллы Конди». Перманганат калия имел большой успех.
Обладает окислительными свойствами, поэтому нашло разнообразное применение в медицинской и химической промышленности.

Его химическая формула – KMnO4.
Физические свойства перманганата калия – KMnO4
Это химическое соединение ярко-фиолетового или бронзового цвета.
Имеет плотность 2.7 г / мл, а его молярная масса составляет 158,034 г / моль.
Соединение не имеет запаха, т.е. не имеет запаха, но имеет сладкий вкус.
Он имеет высокую температуру плавления 2400 C.
Он в основном встречается в виде порошка, кристаллов или таблеток.
Химические свойства перманганата калия
Перманганат калия растворим в ацетоне, воде, пиридине, метаноле и уксусной кислоте.
 Он также легко растворяется в неорганических растворителях.
Он также легко растворяется в неорганических растворителях.Имеет насыщенный фиолетовый цвет в концентрированном растворе и розовый цвет в разбавленном растворе.
Концентрированные и разбавленные растворы перманганата калия
Не горючий, но поддерживает горение других веществ.
При нормальных условиях это высокостабильное соединение, но при нагревании разлагается с образованием MnO2 и высвобождением кислорода.
2KMnO4 ∆ → K2MnO4 + MnO2 + O2
Это сильный окислитель (соединение, которое может легко передавать свой кислород другим веществам), образуя темно-коричневый диоксид марганца (MnO2), который окрашивает все, что есть органический.Он легко может принимать электроны от других веществ.
Он бурно реагирует с серной кислотой, приводя к взрыву.

Он немедленно вступает в реакцию с глицерином и простыми спиртами с образованием пламени и дыма.
Структура перманганата калия – KMnO4
Перманганат калия представляет собой ионное соединение, состоящее из катиона калия (K +) и перманганат-аниона (MnO4-).
В перманганат-анионе (MnO4-) атом марганца связан с четырьмя атомами кислорода тремя двойными связями и одной одинарной связью.Его структуру можно записать следующим образом.
Степень окисления марганца в этой соли +7.
Кристаллическая структура твердого KMnO4 орторомбическая. Каждая структура MnO4- присутствует в тетраэдрической геометрии.
Реакции перманганата калия (KMnO4)
Большинство реакций с перманганатом калия представляют собой окислительно-восстановительные реакции (химическая реакция, при которой одно вещество окисляется, а другое восстанавливается).
KMnO4 может окислять многие неорганические соединения.Среда раствора играет важную роль в определении продуктов реакции.
2KMnO4 + 5Na2SO3 + 3h3SO4🡪 2MnSO4 + 5Na2SO₄ + K2SO4 + 3h3O
2KMnO4 + 3K2SO3 + h3O 🡪 3K2SO4 + 2MnO2 + 2KOH
+ 3K2SO4 + 2MnO2 + 2KOH + Na2SO4 + 2KMNO4 при нагревании кристаллов 2KMNO4 .
2KMnO4 ∆ → K2MnO4 + MnO2 + O2
При разбавлении кристаллов перманганата в присутствии прямых солнечных лучей выделяется кислород.
4KMnO4 + 2h3O Солнечный свет → 4KOH + 4MnO2 + 3O2
С серной кислотой:
2KMnO4 + h3SO4 🡪 Mn2O7 + K2SO₄ + h3O
С перекисью водорода:
2KMnO2 + 3hO2 + 3h 2KMnO2 + 3h СН2 + 2KMnO4 + 2h3O 🡪 Ch3OH – Ch3OH + 2MnO2 + 2KOH (с охлаждением).
Может окислять альдегиды с образованием карбоновых кислот.
Окисляет спирты с образованием карбонилов.

Он также может окислять атомы углерода с тройными связями с образованием дионов.
Он окисляет сахар до кислот, разрушая углеродный скелет по двойным связям.
Использование перманганата калия (KMnO4)
Применение в медицине
Перманганат калия действует как дезинфицирующее средство – из-за его окислительных свойств он может действовать как дезинфицирующее средство для лечения кожных инфекций, таких как дерматит, язвы и язвы , экзема и грибковые инфекции. При нанесении на небольшие раны он атакует внешнюю клеточную мембрану микроорганизма, тем самым окисляя ее и разрушая ее структуру.При больших ранах врачи рекомендуют водные ванны с перманганатом калия с разбавленными растворами. Следует соблюдать осторожность, поскольку чрезмерное использование этого химического вещества может вызвать раздражение и ожоги.

Может использоваться для промывания ран. Влажные раны, такие как язвы и абсцессы, можно промыть раствором перманганата калия. Это лечение убивает микробы и предотвращает вторичное инфицирование. Это также помогает высушить волдыри.
Он очень эффективен при лечении грибковой инфекции, которая называется микоз.Окислительное действие раствора перманганата убивает грибок, тем самым снимая такие симптомы, как зуд и жжение.
Перманганат калия – Drugs.com
- Международный
- Перманганат калия
В некоторых странах это лекарство может быть одобрено только для ветеринарного применения.
Схема
Ph. Eur.
ATC (Анатомо-терапевтическая химическая классификация)
D08AX06, V03AB18
Регистрационный номер CAS (Chemical Abstracts Service)
0007722-64-7
Химическая формула
K-Mn-O4
Молекулярный вес Терапевтические категории
Терапевтические категории
Противоядие
Вяжущее средство
Антисептическое средство для местного применения
Химические названия
Пермангановая кислота, соль калия (USP)
Перманганат калия (USP)
Зарубежные названия Kalii
Общие наименования
- Перманганат калия (OS: JAN)
- CCRIS 5561184 (IS) Минерал хамелеон (IS)
- Кристаллы Конди (IS)
- Марганец-оксид калия (IS)
- NSC 146182 (IS)
- Перманганат калия (IS)
- UNII-00OT1QX5U4 (IS)
- Калий перманганат (PH: Ph.
 Евро. 9)
Евро. 9) - Перманганат калия (PH: BP 2018, JP XVII, USP 41)
- Перманганат калия (PH: Ph. Eur.9)
Торговые марки
- Kalii permanganas RFF
RFF, Латвия - Kalio permanganata Bakteriniai preparatai
Bakteriniai preparatai, Литва - Kalio permanganata Valentis
Valentis, Литва - Kalium hypermanganicum Galena
Galena, Польша - Koi Med Tricho-Ex [ветеринарное применение]
Fishmed, Switzerland - Permanganato de Potasio Euromed
Laboratorios Euromed Чили, Чили - Permitabs
Onelink, Новая Зеландия - Potasio Permanganato Pharma Arte
Pharma Arte, Парагвай - Potassio Permanganato
Марко Вити Фармак., Италия - Potassio Permanganato Nova Argentia
Nova Argentia, Италия - Potassio Permanganato Zeta
Zeta Farm., Италия - Перманганат калия
MidWest, Новая Зеландия - Перманганат калия Kenei
Kenei Sakai Seiyaku, Япония - Перманганат калия Nikko Seiyaku
Nikko Seiyaku, Япония - Перманганат калия Yamazen Seiyaku
Yamazen Seiyaku, Япония - Potasu nadmanganian Hasco-LEK
Hasco-Lek, Poland
Глоссарий
| Термин | Определение | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IS | Неофициальный синоним | ||||||||||||||||||
| JAN | Фармакопея Название | ||||||||||||||||||
Ph. Евро. Евро. | Европейская фармакопея | ||||||||||||||||||
| USP | Фармакопея США |
Дополнительная информация о соглашениях о наименованиях лекарств: Международные непатентованные наименования.
Важное примечание: международная база данных Drugs.com находится в стадии бета-версии. Это означает, что он все еще находится в стадии разработки и может содержать неточности. Он не предназначен для замены опыта и суждений вашего врача, фармацевта или другого медицинского работника.Его не следует толковать как указание на то, что использование каких-либо лекарств в любой стране безопасно, подходит или эффективно для вас. Проконсультируйтесь со своим лечащим врачом перед применением каких-либо медикаментов.
Дополнительная информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности
Молекулярная масса перманганата калия
Молярная масса of KMnO4 = 158. 033949 г / моль
033949 г / моль
Перевести граммы перманганата калия в моль или моль перманганата калия в граммы
Расчет молекулярной массы:
39.0983 + 54.938049 + 15.9994 * 4
| Элемент | Символ | Атомная масса | Количество атомов | Массовый процент |
| Марганец | Mn | 54.938049 | 1 | 34.763% |
| Кислород | O | 15,9994 | 4 | 40,496% |
| Калий | К | 39.0983 | 1 | 24,740% |
В химии вес формулы – это величина, вычисляемая путем умножения атомного веса (в единицах атомной массы) каждого элемента в химической формуле на количество атомов этого элемента, присутствующего в формуле, с последующим сложением всех этих продуктов вместе.
Определение молярной массы начинается с единиц граммов на моль (г / моль). При расчете молекулярной массы химического соединения он говорит нам, сколько граммов содержится в одном моль этого вещества. Вес формулы – это просто вес в атомных единицах массы всех атомов в данной формуле.
Используя химическую формулу соединения и периодическую таблицу элементов, мы можем сложить атомные веса и вычислить молекулярную массу вещества.
Если формула, используемая при расчете молярной массы, является молекулярной формулой, вычисленная формула веса является молекулярной массой.Весовой процент любого атома или группы атомов в соединении можно вычислить, разделив общий вес атома (или группы атомов) в формуле на вес формулы и умножив на 100.
Часто на этом сайте просят перевести граммы в моль. Чтобы выполнить этот расчет, вы должны знать, какое вещество вы пытаетесь преобразовать. Причина в том, что на конверсию влияет молярная масса вещества. Этот сайт объясняет, как найти молярную массу.
Формула веса особенно полезна при определении относительного веса реагентов и продуктов в химической реакции.Эти относительные веса, вычисленные по химическому уравнению, иногда называют весами по уравнениям.
Атомные веса, используемые на этом сайте, получены от Национального института стандартов и технологий NIST. Мы используем самые распространенные изотопы. Вот как рассчитывается молярная масса (средняя молекулярная масса), которая основана на изотропно взвешенных средних. Это не то же самое, что молекулярная масса, которая представляет собой массу одной молекулы четко определенных изотопов. Для объемных стехиометрических расчетов мы обычно определяем молярную массу, которую также можно назвать стандартной атомной массой или средней атомной массой.
| Дата | Код HS | Описание | Место назначения | Порт погрузки | Единица | Количество | Стоимость (INR) | 9020 ( | Ноя 22 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ ТЕХНИЧЕСКОЕ ОБОРУДОВАНИЕ МИН. 99% (ПОРОШОК) 99% (ПОРОШОК) | Германия | Нхава-Шевское море | сом | 18000 | 2,620,346 | 146 | 23 | 23 Ноя 21 год 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ ТЕХНИЧЕСКИЙ УРОВЕНЬ | США | Bombay Air Cargo | сом | 0 | 66 | 330 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ноя 19 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ УПАКОВАНО: 25 кг X 756 NOS ПЛАСТИКОВЫЕ ВЕДРО БЕЗ ПОДДОНОВ | Китай | Нхава Шевское море | кг | 18,900 | 2,596,032 9032 | Ноя 18 201630049099 | Таблетки перманганата калия (Каждая таблетка без покрытия содержит: Перманганат калия USP 500 мг | Танзания | Нхава-Шева море | NOS | 100 | 0 | 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 28416100 | [REWARDITEM] ХИМИЧЕСКИЕ ВЕЩЕСТВА СОДЕРЖАНИЕ ПЕРМАНГАНАТА КАЛИЯ (МИН 97%), NSF 60. | США | Море Нхава-Шева | сом | 18,000 | 2,994,826 | 166 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ноя 17 2016 | 28416100 | БЕСПЛАТНЫЙ ПЕРМАНГАНАТ КАЛИЯ СОРТА УПАКОВКИ: 25 КГ X 360 БЕЗ ОТКРЫТОГО ГОЛОВА ДОСТОЙНО РАЗРЕШЕНО ООН M.S. (Мягкая сталь | Бельгия | Нхава-Шева Море | сом | 9000 | 1,341,526 | 149 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ноя 17 2016 | 28416100 | БЕЗ ПЕРМАНГАНАТА КАЛИЯ СОРТА УПАКОВКИ: 25 КГ X 360 БЕЗ СИНИХ КОМПАКТНЫХ ПЛАСТИКОВ БЕЗ ВНУТРЕННЕГО ЛАЙНЕРА DULY | Бельгия | Нхава Шевское море | кг Ноя 10 2016 | 48195090 | POSTER POLY 2 ЦВЕТНАЯ НАПЕЧАТАННАЯ ПУСТЫЕ ПАМЯТНИКИ ДЛЯ КАЛИЯ ПЕРМАНГАНАТА С 3 СТОРОННЫМИ УПЛОТНЕНИЯМИ | Йемен | Bombay Air Cargo | NOS | 15000 | 6,03 | 9049 Ноя 07 201628416100 | ПЕРМАНГАНАТ КАЛИЯ ТЕХНИЧЕСКИЙ УРОВЕНЬ | Испания | Море Нхава-Шева | сом | 18,000 | 2,403,175 | 134 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ноя 05 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ AWWA FREE FLOWINGGRADE; ЧИСТОТА: 97% | США | Нхава Шевское море | сом | 18,000 | 3,005,040 | 167 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ноя 05 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ ТЕХНИЧЕСКИЙ УРОВЕНЬ 98% | Бельгия | Море Нхава-Шева | сом | 18,000 | 2,681,405 | 149 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 31 год 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ ЧИСТЫЙ СОРТА 99. 3% MIN ФОРМА ГРАНУЛЯРНЫХ КРИСТАЛЛОВ 3% MIN ФОРМА ГРАНУЛЯРНЫХ КРИСТАЛЛОВ | Южная Африка | Нхава-Шевское море | сом | 14400 | 2150976 | 149 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 29 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ КРИСТАЛЛИЧЕСКИЙ | Вьетнам | Море Нхава-Шева | сом | 2,000 | 283644 | 142 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 28 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ AWWA FREE FLOWINGGRADE; ЧИСТОТА: 97% (OIL / CHEM / XP / 35 / 16-17 DTD.14.09.2016) | США | Море Нхава-Шева | сом | 18,000 | 2,939,140 | 163 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 27 2016 | 30049099 | РАСТВОР AQ ПЕРМАНГАНАТА КАЛИЯ [РАЗМЕР УПАКОВКИ: 250 МЛ] | Восточный Тимор | Bombay Air Cargo | NOS | 1,100 | 181,252 | 165 9018 | 23 903 Октябрь 22 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ 97% СВОБОДНЫЙ РАСХОД | США | Море Нхава-Шева | сом | 18,000 | 3,208,079 | 178 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 20 2016 | 28416100 | КАЛИЯ БЕЗ ПЕРМАНГАНАТА СОРТА | Испания | Море Нхава-Шева | сом | 18,000 | 2,530,236 | 141 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 17 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ- 99.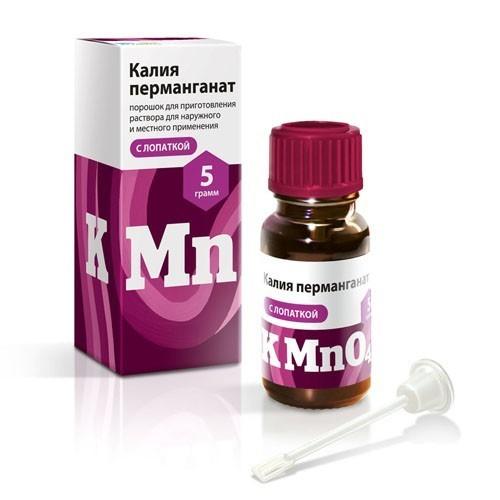 КРИСТАЛЛЫ ЧИСТОГО СОРТА 30% КРИСТАЛЛЫ ЧИСТОГО СОРТА 30% | Саудовская Аравия | Нхава Шева море | сом | 28,800 | 4,207,385 | 146 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 15 2016 | 28416100 | ПЕРМАНГАНАТ КАЛИЯ AWWA FREE FLOWINGGRADE; ЧИСТОТА: 97% | США | Нхава Шевское море | сом | 18,000 | 3,000,480 | 167 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Октябрь 14 2016 | 28416100 | КРИСТАЛЛИЧЕСКИЙ КРИСТАЛЛИЧЕСКИЙ ПЕРМАНГАНАТ КАЛИЯ В УПАКОВКЕ: 50 кг X 400 NOS NET ПОЛНОСТЬЮ ОТКРЫТАЯ ГОЛОВА МОРЕ ДОСТОЙНО РАЗРЕШЕНО ООН GALVANIS | Турция | Анклешвар | 328328 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|


 Он также легко растворяется в неорганических растворителях.
Он также легко растворяется в неорганических растворителях.


 Евро. 9)
Евро. 9) Это темно-пурпурное кристаллическое твердое вещество, растворяющееся в воде, образует насыщенный пурпурный раствор. Это стабильное соединение, но оно может вызвать пожар при контакте с горючим материалом. Ниже приведены некоторые из распространенных применений этого химического соединения.
Это темно-пурпурное кристаллическое твердое вещество, растворяющееся в воде, образует насыщенный пурпурный раствор. Это стабильное соединение, но оно может вызвать пожар при контакте с горючим материалом. Ниже приведены некоторые из распространенных применений этого химического соединения.
 01 г / мл при 25 ° C
01 г / мл при 25 ° C  Вещества, которых следует избегать, включают восстановители, сильные кислоты, органические вещества, горючие материалы, пероксиды, спирты и химически активные металлы. Сильный окислитель.
Вещества, которых следует избегать, включают восстановители, сильные кислоты, органические вещества, горючие материалы, пероксиды, спирты и химически активные металлы. Сильный окислитель. При встрече с этанолом он немедленно разлагается. В кислой среде он будет медленно разлагаться на диоксид марганца и кислород. Свет оказывает каталитическое действие на это разложение, поэтому в лаборатории его часто хранят в коричневых бутылках. Из диаграммы потенциала элемента и диаграммы степени окисления свободной энергии видно, что он оказывает сильное окислительное действие. В щелочном растворе его окислительные свойства не так сильны, как в кислой среде. В качестве окислителя продукт восстановления может быть различным в зависимости от разницы кислотно-основных свойств в разных средах.
При встрече с этанолом он немедленно разлагается. В кислой среде он будет медленно разлагаться на диоксид марганца и кислород. Свет оказывает каталитическое действие на это разложение, поэтому в лаборатории его часто хранят в коричневых бутылках. Из диаграммы потенциала элемента и диаграммы степени окисления свободной энергии видно, что он оказывает сильное окислительное действие. В щелочном растворе его окислительные свойства не так сильны, как в кислой среде. В качестве окислителя продукт восстановления может быть различным в зависимости от разницы кислотно-основных свойств в разных средах.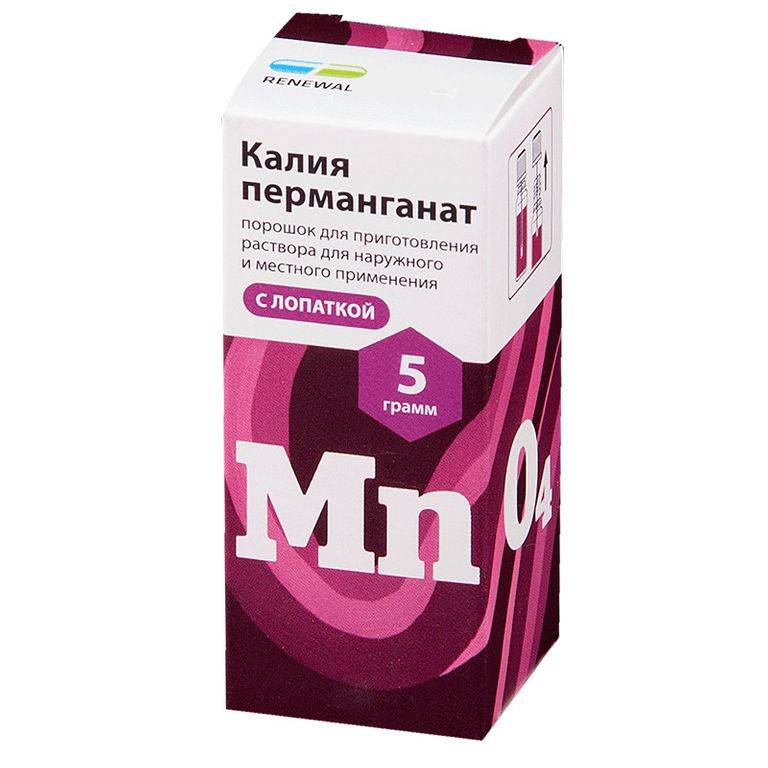 Диоксид марганца может быть объединен с белком с образованием соли с эффектом конвергенции при низкой концентрации, но с эффектом стимуляции и коррозии при высоких концентрациях.Бактерицидная сила увеличивается с концентрацией, при которой 0,1% может уничтожить большинство бактериальных пропагул, а раствор от 2% до 5% способен уничтожить бактериальные споры за 24 часа. В кислых условиях бактерицидный эффект значительно улучшается. Например, добавление 1,1% соляной кислоты к 1% раствору может убить споры сибирской язвы за 30 секунд.
Диоксид марганца может быть объединен с белком с образованием соли с эффектом конвергенции при низкой концентрации, но с эффектом стимуляции и коррозии при высоких концентрациях.Бактерицидная сила увеличивается с концентрацией, при которой 0,1% может уничтожить большинство бактериальных пропагул, а раствор от 2% до 5% способен уничтожить бактериальные споры за 24 часа. В кислых условиях бактерицидный эффект значительно улучшается. Например, добавление 1,1% соляной кислоты к 1% раствору может убить споры сибирской язвы за 30 секунд.  Применение 4 ~ 5 мг раствора перманганата калия на литр для всего разлива пруда можно использовать для лечения плесени и простейших рыб, ракообразных и других паразитов.Ванна с концентрацией 100 мг на литр в течение 30 минут может использоваться для лечения малации мембран лососевых яиц. Обычно используется 0,1% ~ 0,12% растворы для дезинфекции улья, зараженного вирусами и бактериями. Перманганат калия и формалин могут использоваться в комбинации, могут использоваться для дезинфекции воздуха фумигационной дезинфекции животноводческих (птицеводческих) домов и инкубаторов.
Применение 4 ~ 5 мг раствора перманганата калия на литр для всего разлива пруда можно использовать для лечения плесени и простейших рыб, ракообразных и других паразитов.Ванна с концентрацией 100 мг на литр в течение 30 минут может использоваться для лечения малации мембран лососевых яиц. Обычно используется 0,1% ~ 0,12% растворы для дезинфекции улья, зараженного вирусами и бактериями. Перманганат калия и формалин могут использоваться в комбинации, могут использоваться для дезинфекции воздуха фумигационной дезинфекции животноводческих (птицеводческих) домов и инкубаторов. Реакции окисления при различных условиях pH также различны. В кислом растворе он сам восстанавливается до бесцветных соединений двухвалентного марганца; в нейтральном или щелочном растворе он восстанавливается до коричневого диоксида марганца и осаждения белкового комплекса.В низкой концентрации оказывает антибактериальное, конвергентное, кровоточащее, дезодорирующее и другие эффекты. В высоких концентрациях он вызывает раздражение и разъедание, а его антибактериальный эффект сильнее, чем у перекиси водорода. В клинической практике он в основном используется для лечения острого дерматита или острой экземы (особенно при вторичной инфекции), очистки язв или абсцесса, от личинок желудка при пероральном приеме морфина, опиатов, бруцина или органических отравлений, а также для оказания первой помощи при укусах змей.Его также можно использовать для дезинфекции фруктов, посуды и прочего. Прием через рот применяется для лечения инфекции Candida albicans, некротического гингивостоматита, полоскания пародонта.
Реакции окисления при различных условиях pH также различны. В кислом растворе он сам восстанавливается до бесцветных соединений двухвалентного марганца; в нейтральном или щелочном растворе он восстанавливается до коричневого диоксида марганца и осаждения белкового комплекса.В низкой концентрации оказывает антибактериальное, конвергентное, кровоточащее, дезодорирующее и другие эффекты. В высоких концентрациях он вызывает раздражение и разъедание, а его антибактериальный эффект сильнее, чем у перекиси водорода. В клинической практике он в основном используется для лечения острого дерматита или острой экземы (особенно при вторичной инфекции), очистки язв или абсцесса, от личинок желудка при пероральном приеме морфина, опиатов, бруцина или органических отравлений, а также для оказания первой помощи при укусах змей.Его также можно использовать для дезинфекции фруктов, посуды и прочего. Прием через рот применяется для лечения инфекции Candida albicans, некротического гингивостоматита, полоскания пародонта. При контакте перманганата калия с одеждой остаются коричневые следы, которые можно удалить, добавив щавелевую кислоту в воду для очистки.
При контакте перманганата калия с одеждой остаются коричневые следы, которые можно удалить, добавив щавелевую кислоту в воду для очистки.  При попадании на органические вещества он оказывает окислительный эффект. Поэтому он может не только дезинфицировать, но и быть дезодорантом. Низкая концентрация имеет эффект конвергенции. Для поения домашнего скота и птицы его часто можно отрегулировать до 0,1% водного раствора для промывания желудка и окисления яда для детоксикации. Высокая концентрация раствора оказывает раздражающее и разъедающее действие на ткани, а 4% раствор может дезинфицировать кормушку и другие приспособления. Воспользовавшись его окислительными свойствами для ускорения испарения формалина, его можно использовать для дезинфекции воздуха, поскольку это обычно используемое дезинфицирующее средство в семье.
При попадании на органические вещества он оказывает окислительный эффект. Поэтому он может не только дезинфицировать, но и быть дезодорантом. Низкая концентрация имеет эффект конвергенции. Для поения домашнего скота и птицы его часто можно отрегулировать до 0,1% водного раствора для промывания желудка и окисления яда для детоксикации. Высокая концентрация раствора оказывает раздражающее и разъедающее действие на ткани, а 4% раствор может дезинфицировать кормушку и другие приспособления. Воспользовавшись его окислительными свойствами для ускорения испарения формалина, его можно использовать для дезинфекции воздуха, поскольку это обычно используемое дезинфицирующее средство в семье.
 Лекарства или токсиканты, оставшиеся в желудке, будут подвергаться окислению перманганатом калия и отказу.
Лекарства или токсиканты, оставшиеся в желудке, будут подвергаться окислению перманганатом калия и отказу. 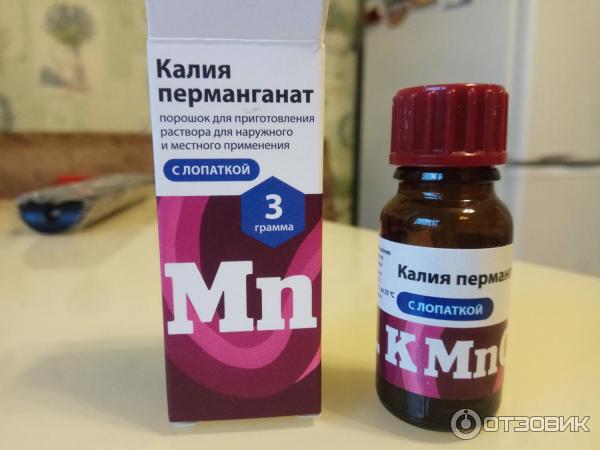 3 г (называемые квази-0,0002 г) для растворения в воде до достижения постоянного объема до 1000 мл (коричневая мерная колба), встряхните и поместите в темноте на 1 час. Взять супернатант и добавить в бюретку; Добавьте первую каплю 38 мл раствора образца в раствор оксалата натрия и нагрейте до 70 ~ 75 ℃, продолжайте понижать до тех пор, пока раствор не станет розовым без выцветания в течение 30 секунд, что можно рассматривать как конечную точку. Для исправления результатов был также проведен холостой тест.
3 г (называемые квази-0,0002 г) для растворения в воде до достижения постоянного объема до 1000 мл (коричневая мерная колба), встряхните и поместите в темноте на 1 час. Взять супернатант и добавить в бюретку; Добавьте первую каплю 38 мл раствора образца в раствор оксалата натрия и нагрейте до 70 ~ 75 ℃, продолжайте понижать до тех пор, пока раствор не станет розовым без выцветания в течение 30 секунд, что можно рассматривать как конечную точку. Для исправления результатов был также проведен холостой тест.  Его можно использовать в качестве окислителя, отбеливателя, напитка, очищенного диоксидом углерода, дезодоранта, консервантов для древесины, адсорбентов, дезинфицирующих средств, пестицидов, очистителей воды и т. Д.
Его можно использовать в качестве окислителя, отбеливателя, напитка, очищенного диоксидом углерода, дезодоранта, консервантов для древесины, адсорбентов, дезинфицирующих средств, пестицидов, очистителей воды и т. Д.