причины, симптомы, диагностика, лечение, профилактика
Представляет собой редкую, потенциально злокачественную или злокачественную опухоль, которая происходит из лимфоидной ткани, которая локализируется в стенке желудка.
ПричиныРазвитию лимфомы желудка предшествует лимфоидная ткань, расположенная в слизистой оболочке в виде отдельных лимфоцитов и скоплений клеток. При благоприятных условиях такие скопления формируют лимфоидные фолликулы, в которых могут формироваться участки атипии. Примерно у 95% больных с лимфомой желудка при проведении обследования выявляются различные штаммы Helicobacter pylori, данная инфекция рассматривается, как одна из основных причин возникновения этого новообразования.
Совместно с Helicobacter pylori, развитие различных типов лимфом желудка может провоцироваться другими факторами, в том числе влиянием канцерогенных веществ, длительным нахождением в зонах с повышенным уровнем радиации, перенесенная лучевая терапия, приемом некоторых медикаментозных средств, чрезмерным облучением ультрафиолетовым излучением, неспецифическим снижением иммунитета, иммунными нарушениями при СПИДе, аутоиммунными патологиями и искусственным ингибированием иммунитета на фоне перенесенной трансплантации органов.
Специфические признаки заболевания отсутствуют, по своим клиническим проявлениям лимфома желудка напоминает рак желудка, немного реже – язвенное поражение желудка или хронического гастрита. Самым распространенным признаком заболевания является боль в области эпигастрия, которая может усиливаться после еды. Многие больные лимфомой желудка жалуются на ощущение преждевременного насыщения. У некоторых больных развивается отвращение к определенным пищевым продуктам. Для таких больных характерно похудание, появляющееся в результате чувства переполнения желудка и снижения аппетита. Иногда возникает выраженное снижение массы тела вплоть до кахексии.
При лимфоме желудка у многих больных может выявляться тошнота и рвота, особенно – на фоне переедания, что еще больше способствует уменьшению объемов порций, а иногда сопровождается полным отказом от еды с последующим снижением массы тела. При распространении онкологического процесса иногда наблюдается развитие стеноза желудка. В отдельных случаях у больных лимфомой желудка развиваются кровотечения различной степени выраженности. При лимфоме желудка существует высокий риск развития тяжелых осложнений, таких как перфорация стенки желудка при ее прорастании опухолью и профузного кровотечения при расположении лимфомы желудка вблизи крупного сосуда. Вместе с перечисленными симптомами может возникать повышение температуры тела и обильное потоотделение, преимущественно в ночное время.
В отдельных случаях у больных лимфомой желудка развиваются кровотечения различной степени выраженности. При лимфоме желудка существует высокий риск развития тяжелых осложнений, таких как перфорация стенки желудка при ее прорастании опухолью и профузного кровотечения при расположении лимфомы желудка вблизи крупного сосуда. Вместе с перечисленными симптомами может возникать повышение температуры тела и обильное потоотделение, преимущественно в ночное время.
Диагноз устанавливается на основании жалоб, истории заболевания, физикального осмотра, пальпации живота, данных лабораторно-инструментальных исследований. В связи с неспецифичностью симптоматики возможно позднее выявление лимфомы желудка, в литературе описаны случаи, когда временной период между появлением болей в эпигастрии и постановкой диагноза составлял около 3 лет. Одним из самых достоверных и информативных методов инструментальной диагностики считается гастроскопия, позволяющая определить расположение и тип роста новообразования. Для подтверждения диагноза может потребоваться выполнение биопсии с дальнейшим гистологическим и цитологическим исследованием биоптата.
Для подтверждения диагноза может потребоваться выполнение биопсии с дальнейшим гистологическим и цитологическим исследованием биоптата.
При локализованных новообразованиях, отличающихся благоприятным течением, проводят эррадикационную антихеликобактерную терапию. Возможно использование любых схем лечения с доказанной эффективностью. При отсутствии результата после применения одной из стандартных схем больным лимфомой желудка назначают усложненную трехкомпонентную или четырехкомпонентную терапию, которая включает в себя введение ингибиторов протонного насоса и нескольких антибактериальных средств. При неэффективности усложненной схемы лечения, в зависимости от стадии лимфомы желудка может потребоваться применение химиотерапии или системной терапии.
При тяжелом течении заболевания и частым развитием осложнений может потребоваться проведение хирургического вмешательства.
ПрофилактикаНа данный момент методы профилактики данного заболевания не разработаны, однако для снижения вероятности развития лимфомы желудка следует своевременно заниматься терапией любых заболеваний, которые могу стать причиной ее развития.
Лечение лимфомы желудка в Израиле
Специалисты центра Топ Ихилов достигли поразительных результатов в терапии желудочной лимфомы. Они проводят высокоточную диагностику с помощью инновационного оборудования и применяют широчайший набор современных средств — моноклональные антитела, схемы интенсивной химиотерапии, радиологические методики и противобактериальные лекарства (последние используются в терапии одного из подтипов патологии).
Получить ценыИменно поэтому многие пациенты стараются попасть на лечение лимфомы желудка в Израиле — сюда их привлекают доступные расценки и, самое главное, опытные, высокопрофессиональные врачи. Лучшее свидетельство того, насколько эффективно ведется лечение лимфомы желудка в Израиле, — отзывы тех, кто уже избавился от данного онкологического недуга.
Методы лечения лимфомы желудка в Израиле
Хотя желудок и является наиболее характерным местом возникновения неходжкинских лимфом, лимфома желудка является достаточно атипичным видом раковых патологий ЖКТ. В большинстве случаев опухоль диагностируется на первой стадии, когда она локализована в дистальном отделе желудка. Новообразования бывают двух типов — диффузные, связанные с мутациями в В-лимфоцитах (так называемый тип DLBL), и ассоциированные с изменениями непосредственно слизистой желудка (точнее — ее лимфоидных тканей, так называемый тип MALT). В зависимости от вида опухоли выбирается способ терапии: методы лечения лимфомы желудка в Израиле в основном включают в себя применение радио- и химиотерапии (часто — в комплексе друг с другом).
В большинстве случаев опухоль диагностируется на первой стадии, когда она локализована в дистальном отделе желудка. Новообразования бывают двух типов — диффузные, связанные с мутациями в В-лимфоцитах (так называемый тип DLBL), и ассоциированные с изменениями непосредственно слизистой желудка (точнее — ее лимфоидных тканей, так называемый тип MALT). В зависимости от вида опухоли выбирается способ терапии: методы лечения лимфомы желудка в Израиле в основном включают в себя применение радио- и химиотерапии (часто — в комплексе друг с другом).
Химиотерапия применяется для лечения новообразований обоих типов. Опухоль типа DLBL лечится с использованием комбинированной схемы, в которую входят моноклональные антитела, адресно воздействующие на специфические протеины (CD20), располагающиеся на поверхности мутировавших В-лимфоцитов, а также алкилирующие цитостатические препараты, аналоги алкалоидов барвинка, кортикостероиды и противоопухолевые средства антрациклинового ряда (модификация так называемой схемы CHOP).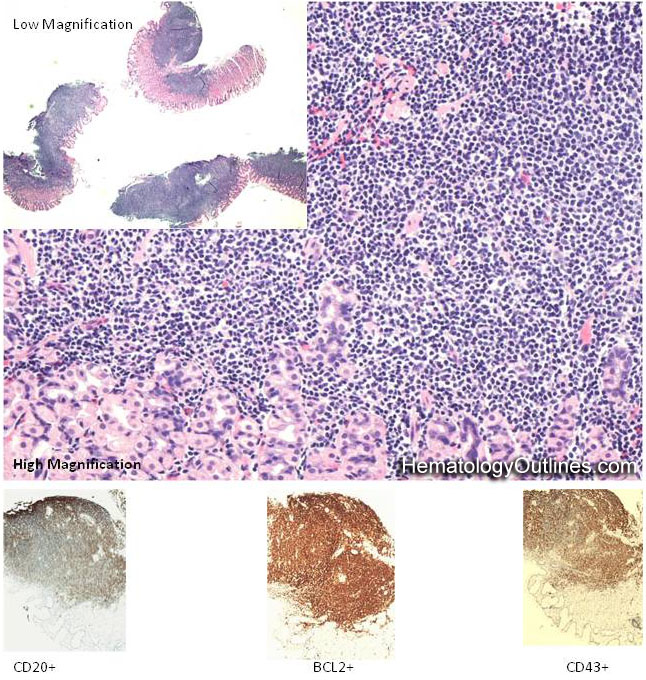 Препараты в основном вводятся внутривенно, а цикл состоит из нескольких курсов с перерывом в несколько недель (месяцев). Израильские врачи тщательно контролируют ход лечения: после двух курсов проводится ПЭТ-сканирование, а затем на основании его результатов делаются выводы о продолжении или завершении терапии.
Препараты в основном вводятся внутривенно, а цикл состоит из нескольких курсов с перерывом в несколько недель (месяцев). Израильские врачи тщательно контролируют ход лечения: после двух курсов проводится ПЭТ-сканирование, а затем на основании его результатов делаются выводы о продолжении или завершении терапии.
Лимфома типа MALT чрезвычайно чувствительна к комплексной терапии, в которой используется комбинация из моноклональных антител, действующих на белок CD20, и классических пероральных противоопухолевых средств из группы алкилирующих агентов. Успешность проводимого лечения колеблется от 60-70% в случае монотерапии до 100% при сочетании препаратов из разных групп. Пероральные алкилирующие цитостатики принимаются на протяжении примерно 12 месяцев. Лечение лимфомы желудка без операции в Израиле может осуществляться также с использованием других средств — так, хорошую активность показывают противоопухолевые препараты из группы антагонистов пуринов.
Радиотерапия – еще один метод, с помощью которого выполняется лечение лимфомы желудка без операции в Израиле. При патологиях типа DLBL она часто является частью комплексной программы, в которую входит и химиотерапия. При опухолях типа MALT радиотерапия часто служит в качестве основного метода и позволяет обеспечивать локальный контроль на ранних стадиях, достигая уровня пятилетней выживаемости в районе 100%. Как правило, используется режим облучения, при котором пациент за 15 сеансов получает дозу порядка 30 Гр — она хорошо переносится и обеспечивает желаемый терапевтический эффект.
При патологиях типа DLBL она часто является частью комплексной программы, в которую входит и химиотерапия. При опухолях типа MALT радиотерапия часто служит в качестве основного метода и позволяет обеспечивать локальный контроль на ранних стадиях, достигая уровня пятилетней выживаемости в районе 100%. Как правило, используется режим облучения, при котором пациент за 15 сеансов получает дозу порядка 30 Гр — она хорошо переносится и обеспечивает желаемый терапевтический эффект.
Рассчитать стоимость лечения
Новообразования типа MALT тесно связаны с инфицированием бактерией хеликобактер, вызывающей язву желудка. Поэтому в качестве дополнительной терапии применяются соответствующие антибактериальные препараты и лекарственные средства из группы ингибиторов протонного насоса (если тесты выявляют наличие бактерии). Как показывает практика, полная эрадикация болезнетворного микроорганизма позволяет добиться ремиссии в 50-95% случаев, особенно на ранних стадиях лимфомы типа MALT.
Диагностика лимфомы желудка в Израиле
Диагностика лимфомы желудка в Израиле проводится комплексно, с определением подтипа заболевания. На нее отводится от трех до четырех дней.
Первый день — консультация
Начальный день диагностики — вводный. Он посвящен первичной консультации у ведущего онколога, которая проводится в кратчайшие сроки после прибытия пациента в Израиль.
Второй день — исследования
На следующий день пациент проходит назначенные исследования.
- Лабораторный анализ крови.
- Эндоскопическое исследование (ключевой метод диагностики опухолей типа MALT).
- МРТ, КТ, ПЭК-КТ.
- Рентгенография.
- Множественная биопсия образцов тканей из разных участков новообразования.
- Анализ на ассоциированные с В-лимфоцитами и прочие антигены (CD19, CD22 и др.).
- Микроскопическое изучение В-лимфоцитов (используется для определения морфологических подтипов опухолей DLBL).
- Генетическая диагностика для отличия одних подтипов DLBL от других.

Третий день — комиссия
Цикл диагностики завершается на третий день, когда собирается врачебная комиссия во главе с ведущим онкологом — врачи сообща решают, какие именно терапевтические мероприятия следует включать в лечебную программу.
Лечение лимфомы желудка в Израиле — стоимость доступна широкому кругу пациентов
Как правило, когда говорят о положительных моментах, которыми отличается лечение лимфомы желудка в Израиле, цены упоминают прежде всего. Действительно, хотя медицина нашей страны и является одной из лучших в мире по уровню развития, расценки на услуги израильских клиник значительно ниже, чем в больницах Австрии, Швеции, Соединенных Штатов. В ряде случаев экономия может составить до 45-50%.
Запрос ценыПреимущества Топ Ихилов
- Специалисты экстра-класса, обладающие уникальным опытом терапии лимфом. Несмотря на свой и без того высокий уровень подготовки, наши врачи стремятся постоянно совершенствовать свои знания, внедрять в клиническую практику самые современные методы.

- Обследование больных в центре проводится с применением высокоточного оборудования, за счет чего обеспечивается непревзойденная точность дифференциальной диагностики.
- Врачи клиники лечат лимфому с использованием широкого спектра новейших методик — от современных высокоэффективных комбинированных схем химиотерапии до облучения пациентов на аппаратах дистанционной радиотерапии.
- Обращаясь к нам, пациент ничем не рискует, поскольку отсутствует предоплата, а все расчеты выполняются через кассу медицинского центра.
- Для пациентов в клинике созданы наилучшие условия — в уютных палатах имеется все необходимое, а за координацией врачей и переводом меддокументов следит личный куратор-переводчик.
- 5
- 4
- 3
- 2
- 1
MALT-ЛИМФОМА ЖЕЛУДКА (задача 15133)
MALT-ЛИМФОМА ЖЕЛУДКА
(задача 15133)
П.Г. Мальков1,2, М.А. Морозова1, В. Н. Гриневич1,
Н. Гриневич1,
Ю.В. Зорина1, Л.В. Москвина2, Н.В. Данилова2
1 Централизованная лаборатория патоморфологии и цитологии (зав. – кандидат мед. наук П.Г. Мальков) ГУЗ Консультативно-диагностический центр №6 УЗ САО г.Москвы;
2 Кафедра общей и частной патологии (зав. – член-корр. РАМН, проф. Ю.Л. Перов) факультета фундаментальной медицины МГУ имени М.В. Ломоносова.
Клиническая легенда. Женщина, 73 года. При эндоскопическом исследовании в антральном отделе желудка определяется площадка инфильтрации слизистой оболочки со сглаживанием рельефа и изъязвлением в центре до 8 мм в диаметре, при биопсии – фрагментация и повышенная кровоточивость. Эндоскопический диагноз – подозрение на новообразование желудка.
Макроскопическое описание. Получено 8 кусочков ткани.
Микрофотографии. Рис. 1 – окраска гематоксилином и эозином, об. х5; рис. 2 – окраска гематоксилином и эозином, об.х40; рис. 2а – иммуногистохимическое выявление PCK, об.20; рис. 3 – окраска гематоксилином и эозином, об.х40; рис. 4 – окраска гематоксилином и эозином, об.х63; рис. 4а – окраска гематоксилином и эозином, об.х63; рис. 5 – иммуногистохимическое выявление CD45, об.х20; рис. 5а – иммуногисто-химическое выявление CD79α; рис. 6 – иммуногистохимическое выявление CD20, об.х20; рис. 6а – иммуногистохимическое выявление CD20, об.х40.
х5; рис. 2 – окраска гематоксилином и эозином, об.х40; рис. 2а – иммуногистохимическое выявление PCK, об.20; рис. 3 – окраска гематоксилином и эозином, об.х40; рис. 4 – окраска гематоксилином и эозином, об.х63; рис. 4а – окраска гематоксилином и эозином, об.х63; рис. 5 – иммуногистохимическое выявление CD45, об.х20; рис. 5а – иммуногисто-химическое выявление CD79α; рис. 6 – иммуногистохимическое выявление CD20, об.х20; рис. 6а – иммуногистохимическое выявление CD20, об.х40.
Микроскопическое описание.
Слизистая оболочка и подслизистый слой желудка густо инфильтрированы лимфоцитоподобными клетками, среднего размера с бледной цитоплазмой и полиморфным ядром (рис. 1, 3), сходными с центроцитами лимфоидных фолликулов (рис. 4). Клетки не образуют каких-либо структур, инвазируют эпителий желез с нарушением его архитектоники (рис. 2, 2а), что обозначается как лимфо-эпителиальные повреждения. В части клеток обнаруживаются ядерные пузырьковидные включения (тельца Dutcher – рис. 4а) и оксифильные цитоплазматические включения (тельца Russel – рис. 3). Иммунофенотип: CD45 (рис. 5), CD79α (рис. 5а), CD20 (рис. 6, 6а) и CD21 – выраженная позитивная реакция в опухолевых клетках, РСК – выраженная положительная цитоплазматическая реакция в эпителиальных клетках (рис. 2а).
4а) и оксифильные цитоплазматические включения (тельца Russel – рис. 3). Иммунофенотип: CD45 (рис. 5), CD79α (рис. 5а), CD20 (рис. 6, 6а) и CD21 – выраженная позитивная реакция в опухолевых клетках, РСК – выраженная положительная цитоплазматическая реакция в эпителиальных клетках (рис. 2а).Заключение. MALT-лимфома желудка [9699/3].
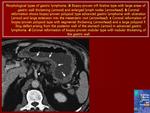 CCL клетки инфильтрируют и разрушают прилежащие железы желудка, формируя так называемые лимфоэпителиальные повреждения, типичные для MALT-лимфомы. Дифференциальный диагноз необходимо проводить с реактивным лимфоидным инфильтратом слизистой оболочки желудка и В-крупноклеточной лимфомой.
CCL клетки инфильтрируют и разрушают прилежащие железы желудка, формируя так называемые лимфоэпителиальные повреждения, типичные для MALT-лимфомы. Дифференциальный диагноз необходимо проводить с реактивным лимфоидным инфильтратом слизистой оболочки желудка и В-крупноклеточной лимфомой. Литература. Pathology & Genetics Tumours of the Digestive System / WHO Classification of Tumours.- IARC Press.-2000, p.58-61.
MALT-лимфома желудка — ЗдоровьеИнфо
Заболеваемость
Лимфома маргинальной зоны, ассоциированная со слизистыми ( MALT) составляет ~ 7 % всех неходжкинских лимфом. Процесс может возникать в любых экстранодальных зонах, но большую часть (треть всех случаев) составляют лимфомы желудка. Точная заболеваемость для Европы точно не известна по причине различия классификационных систем, используемых в разных странах.
Диагноз
Клинически MALT- лимфома желудка проявляется неспецифическими симптомами, приводящими пациента на эндоскопическое исследование. При ЭГДС как правило определяется неспецифический гастрит или язвенный дефект слизистой с нетипичными для простой пептической язвы солидными структурами.
При ЭГДС как правило определяется неспецифический гастрит или язвенный дефект слизистой с нетипичными для простой пептической язвы солидными структурами.
Диагноз устанавливается на основании иммуноморфологического исследования материала гастробиопта [III, A]. Наличие активной Helicobacter pylori инфекции должно быть подтверждено иммуногистохимияески или с помощью уреазного дыхательного теста.
Для выявления пациентов с маловероятным ответом на антибактериальную терапию в дополнение к стандартному иммуноморфологическому исследованию желательно дополнительное определение t(11;18) методом FISH [III, B].
Стадирование и факторы риска
Первичная диагностика должна включать ЭГДС с множественными биопсиями слизистых желудка, двенадцатиперстной кишки, гастроэзофагиального перехода и любых подозрительных участков.
Ультразвуковое исследование показано для исключения поражения региональных лимфоузлов и инфильтрации стенки желудка [III,A].
Комплексное обследование должно включать общий анализ крови с подсчетом формулы, биохимический анализ крови с определением уровня ЛДГ и бета2- микроглобулина, компьютерную томографию грудной клетки, брюшной полости и таза, а также исследование аспирата и трепанобиоптата костного мозга [IV,C].
Позитронно-эмиссионная томография (ПЭТ) имеет небольшую диагностическую ценность и необходимость применения метода сомнительна (IV,D).
Лечение
Эрадикационная антихеликобактерная антибиотикотерапия считается стандартом первой линии терапии локальных (ограниченных желудком) H. Pylori- позитивных MALT- лимфом [II, A]. Возможно применение любых эрадикационных режимов с доказанной эффективностью. При неудаче первичной эрадикационной антихеликобактерной терапии возможно использование усложненных трех- и четырехкомпонентных схем, включающих антибиотики и ингибиторы протонной помпы.
Эрадикация H. Pylori может способствовать регрессии лимфомы и длительному контролю болезни у большинства пациентов. Время до наступления ремиссии может колебаться от нескольких до 12 месяцев. Таким образом, у пациентов, достигших клинической и эндоскопической ремиссии, вместе с эрадикацией H. Pylori, но имеющих резидульные гистологические признаки лимфомы имеет смысл выдержать интервал как минимум 12 месяцев перед переходом на другую терапию [III, B]. Персистенция моноклональных В-лимфоцитов после полной гистологической регрессии лимфомы была показана во многих исследованиях, посвященных мониторингу пациентов после антибактериальной терапии. В подобных случаях рекомендуется тактика выжидательного наблюдения («watchful waiting»), а активная противоопухолевая терапия (см. ниже) должна быть оставлена для симптоматических или прогрессивных форм болезни.
Персистенция моноклональных В-лимфоцитов после полной гистологической регрессии лимфомы была показана во многих исследованиях, посвященных мониторингу пациентов после антибактериальной терапии. В подобных случаях рекомендуется тактика выжидательного наблюдения («watchful waiting»), а активная противоопухолевая терапия (см. ниже) должна быть оставлена для симптоматических или прогрессивных форм болезни.
В H. Pylori негативных случаях, в также при отсутствии эффекта от первичной антибактериальной терапии, в зависимости от стадии заболевания, показано применение лучевой или системной химиотерапии. Хирургический метод не показал преимуществ в сравнении с более консервативными методами в нескольких исследованиях. При I-II стадиях в H. Pylori- негативных ситуациях и при персистировании лимфомного клона после эррадикационной антибиотикотерапии высокоэффективна лучевая монотерапия (СОД 30-40 Гр, 4 недели) на область желудка и перигастрия [III, B].
Для пациентов с распространенным процессом показана системная химио- и/ или иммунотерапия терапия (с применением терапевтических анти-CD20- моноклональных антител) [III]. Только некоторые отдельные препараты и режимы были протестированы специально для MALT-лимфомы.
Только некоторые отдельные препараты и режимы были протестированы специально для MALT-лимфомы.
Оральные алкилирующие агенты (циклофосфан и хлорамбуцил), а также аналоги нуклеотидов (флударабин и кладрибин) показали высокую эффективность в контроле болезни. Противоопухолевая активность ритуксимаба была доказана в исследованиях II фазы и эффективность препарата в комбинации с хлорамбуцилом исследуется, а настоящее время в рандомизированных исследованиях. На данный момент в литературе отсутствуют достаточно доказательств преимущества того или иного препарата или режима, однако следует учитывать, что терапия пуриновыми аналогами ассоциирована с повышенным риском развития вторичных меилодисплазий. Агрессивные антрациклин- содержащие режимы рекомендуются к применению только в случаях болезни с агрессивном течением и большой опухолевой массой.
Диффузная В-клеточная лимфома желудка должна быть лечена в соответствии с рекомендациями, разработанными для первичных диффузных В-клеточных лимфом других локализаций.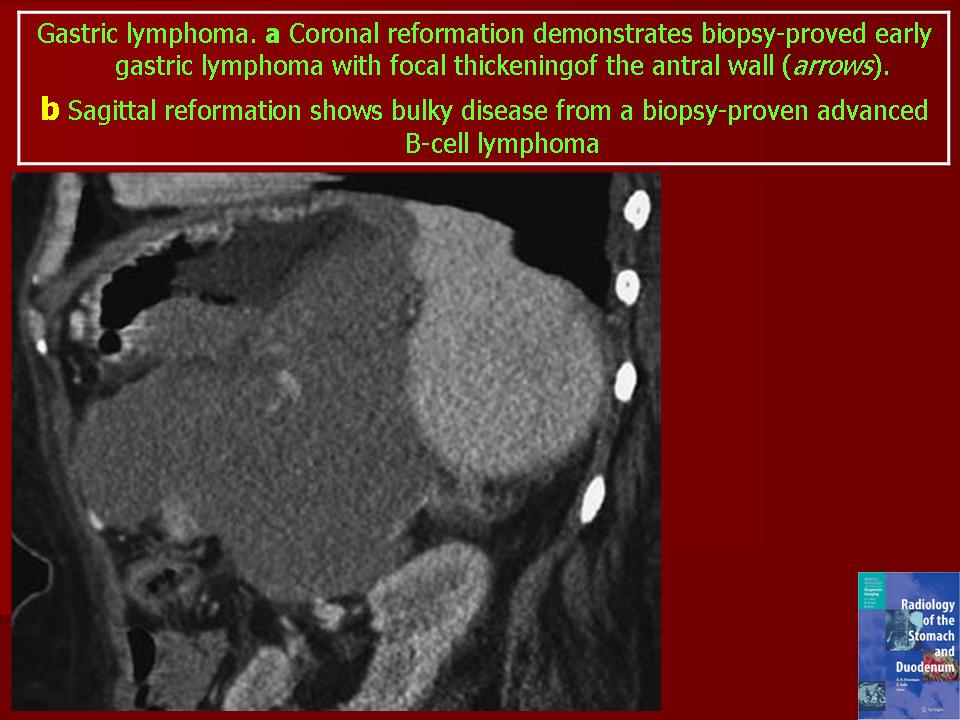
Оценка эффективности лечения и наблюдение
В основе наблюдения лежит строгое регулярное эндоскопическое исследование желудка с многократными биопсиями. К сожалению, интерпретация качества резидуальных лимфоидных инфильтратов очень сложна, поскольку четкие гистологические критерии морфологической ремиссии на настоящий момент отсутствуют. Первая ЭГДС должна быть проведена через 2-3 месяца после окончания терапии для подтверждения эррадикации H. Pylori; далее для мониторинга гистологической регрессии лимфомы исследование должно повторяться как минимум дважды в год на протяжении первых 2-х лет.
MALT-лимфома желудка отличается лимитированной способностью к дистанционному метастазированию и гистологической трансформации. Возможны транзиторные локальные рецидивы, имеющие тенденцию к самоограничению (самокупированию), особенно при отсутствии реинфицирования H. Pylori.
В случаях персистирующей, но стабильной резидуальной болезни или гистологических рецидивах (без наличия отдаленных метастазов и/или эндоскопические отчетливой опухоли) может быть применена тактика «наблюдай и жди» [IV,C]. Пациенты, однако, должны находиться под строгим контролем и регулярно проходить эндоскопическое и общее клиническое (УЗИ, рентген, исследование крови) как минимум 1 раз в год.
Пациенты, однако, должны находиться под строгим контролем и регулярно проходить эндоскопическое и общее клиническое (УЗИ, рентген, исследование крови) как минимум 1 раз в год.
Особенности эндоскопической семиотики и антихеликобактерная терапия MALT-лимфом желудка | #07/10
Лимфомы гастроинтестинального тракта охватывают от 14% до 27% всех экстранодальных поражений и составляют от 1% до 15% всех злокачественных опухолей желудочно-кишечного тракта. Чаще всего поражается желудок (50–75%), сравнительно реже тонкая кишка (20–35%). Лимфомы толстой кишки наблюдаются в 5–10% случаев. Самыми редкими признаны первичные неходжкинские лимфомы пищевода [1].
В 1983 году Brooks и Enterline [2] провели клинико-морфологическое исследование, где показали, что нодальные и экстранодальные лимфомы отличаются по биологическим свойствам и что экстранодальные варианты лимфомы имеют более благоприятный прогноз.
Brooks и Enterline впервые отметили патогенетическую связь между хроническим воспалением слизистой оболочки желудка и развитием лимфомы. Было высказано предположение, что многие типы лимфом желудка представляют собой злокачественную трансформацию доброкачественных и длительно текущих лимфоцитарных поражений желудка. Авторы пришли к тому заключению, что длительная антигенная стимуляция вместе с аутоиммунным феноменом в клетках слизистой оболочки желудка в целом приводят к появлению злокачественного клона. Эта гипотеза была подтверждена результатами клинико-морфологических исследований, проведенных при лимфомах слюнной и щитовидной желез. Было показано, что лимфомы этих желез могут возникнуть на фоне хронического тиреоидита и сиалоаденита с синдромом Шегрена или без него.
P. Isaacson и D. H. Wright [3] обратили внимание на то, что большая часть первичных лимфом желудка развивается на фоне хронических гастритов. Более того, было показано, что другие варианты экстранодальных лимфом также связаны с хроническими воспалительными процессами.
Показано, что при эрадикации этого микроорганизма симптомы хронического воспаления становятся менее интенсивными и снижается степень лимфоцитарной инфильтрации. В 1993 году были представлены доказательства, что Н. pylori играет важную роль в возникновении подгруппы лимфом желудка MALT-типа [4]. Рядом авторов [5] было высказано мнение, что Н. pylori вызывает нарушение физиологических и иммунологических процессов, окислительное повреждение ДНК и пролиферацию как гемапоэтических, так и клеток слизистой оболочки желудка. В дальнейшем было установлено, что 90% больных MALT-лимфомой инфицированы Н.
Материалы и методы исследования
Эндоскопическая картина лимфом желудка изучена нами у 250 пациентов, при этом поражение у 160 (64%) больных расценено как первичное, а у 90 (36%) — как вторичное, наблюдаемых в РОНЦ с 1995 года, из которых было 99 пациентов с MALT-лимфомой желудка. Разработаны эндоскопические и эндосонографические критерии диагноза MALT-лимфомы, ее дифференциально-диагностические признаки, проведена оценка лекарственной терапии.
Результаты и их обсуждение
При тщательном анализе развития болезни нами установлено, что в группе с первичными лимфомами желудка практически одна треть (32%) пациентов имели гастроэнтерологический анамнез: язвенную болезнь желудка, хронический атрофический, гипертрофический или смешанные гастриты, зачастую ассоциированные с инфекцией H..jpg) pylori.
pylori.
Согласно нашим наблюдениям длительность существования гастроэнтерологической патологии до установления наличия опухоли в группе с первичной лимфомой желудка весьма вариабельна: в течение первых трех месяцев диагноз установлен у 30,6% (49 больных), в течение 6 месяцев у 18,1% (29 больных), в срок от 6 до 12 месяцев у 15,6% (25 больных). Отдельно следует отметить, что практически у трети пациентов (27,5% — 44 пациента) диагноз первичной лимфомы желудка был установлен спустя год (табл. 1).
Также отдельно необходимо отметить, что диагноз первичной лимфомы желудка у 8% пациентов выявлен при плановом обследовании по поводу сопутствующей патологии и оказался диагностической находкой, так как заболевание у части больных протекало бессимптомно.
В группе пациентов со вторичным поражением желудка от момента установления диагноза первичной локализации процесса до времени выявления поражения желудка сроки были различны и представлены в табл.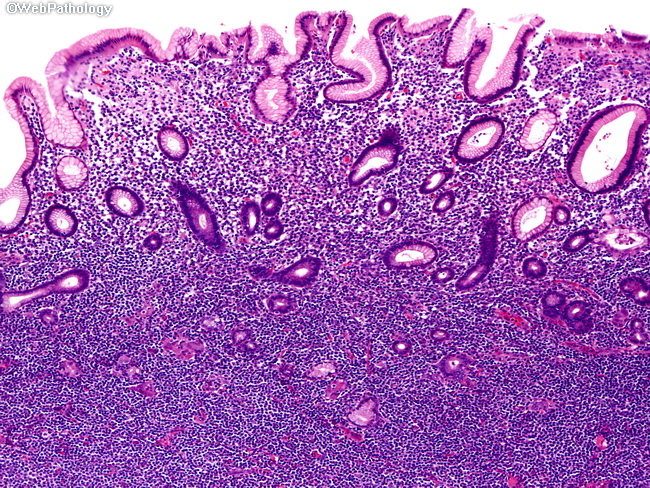 2.
2.
Как видно из представленных в таблице данных, поражение желудка в большинстве случаев развилось в первые два года от начала заболевания, что диктует нам необходимость обязательных периодических эндоскопических исследований желудка с целью своевременного выявления метастатического поражения его при лимфомах.
В нашей работе чаще всего при лимфомах желудка имело место инфильтративно-язвенное и инфильтративное его поражение — 28,4% и 21,6% соответственно, затем в 14,8% встречается язвенная форма роста опухоли. Гастритоподобный вариант опухоли отмечен в 14,4%. Реже встречались смешанная и экзофитная формы роста опухоли — 12,0% и 8,8% соответственно.
Причем, как показывает анализ наших данных, при MALT-лимфоме преобладала гастритоподобная форма роста, которая составила 34,3%.
Эндоскопическая картина гастритоподобной формы лимфомы желудка является наиболее вариабельной и по преобладанию макроскопических признаков может проявляться в виде:
антрального гастрита;
эрозивного гастрита;
локального гиперпластического гастрита;
смешанного гастрита.

Естественно, такое деление является относительно условным, и эти формы выделяются нами по преобладанию наиболее выраженных указанных признаков, симулирующих ту или иную форму гастрита (табл. 3).
Анализируя полученные данные, чаще всего, в 33,4%, отмечался поверхностный антральный гастрит, вторым по частоте стал эрозивный гастрит — 25,0%, с одинаковой частотой в 22,2% встречается очаговый гиперпластический гастрит и смешанный гастрит.
При гастритоподобной форме лимфомы желудка в виде антрального гастрита, как следует из самого определения, визуальные проявления опухоли симулируют воспалительные изменения в антральном отделе желудка, которые отмечены нами в 33,4%. При сохраненной эластичности стенок желудка отмечается пастозность, разрыхленность и очаговая гиперемия слизистой антрального отдела желудка, чередующаяся с участками белесоватого цвета, ее повышенная контактная кровоточивость. Как и при других вариантах, характерным является появление стекловидного блеска. При проведении биопсии подвижность и эластичность слизистой оболочки снижена, отмечается ее фрагментация.
Как и при других вариантах, характерным является появление стекловидного блеска. При проведении биопсии подвижность и эластичность слизистой оболочки снижена, отмечается ее фрагментация.
Изменения при лимфоме желудка в виде эрозивного гастрита отмечаются в 25,0% случаев и характеризуются наличием множественных поверхностный острых эрозий неправильной или щелевидной формы на фоне пастозной, неравномерно гиперемированной слизистой с усиленным сосудистым рисунком. Участки эрозий могут локализоваться в различных отделах желудка, чередуясь с неизмененной слизистой, либо занимать изолированную, ограниченную зону. Эластичность стенок остается, как правило, сохраненной или снижена незначительно.
Лимфома желудка в виде локального гиперпластического гастрита. Этот тип лимфомы отмечается в 22,2% случаев и характеризуется умеренным неравномерным утолщением складок на ограниченном участке чаще по большой кривизне и в проксимальном отделе желудка иногда с переходом на переднюю или заднюю стенки. Эластичность стенки сохранена, подвижность складок может быть сохраненной или сниженной. Поверхность складок покрыта вязкой стекловидной слизью, разрыхлена. При инсуффляции складки слизистой пораженного участка, как правило, не расправляются полностью.
Эластичность стенки сохранена, подвижность складок может быть сохраненной или сниженной. Поверхность складок покрыта вязкой стекловидной слизью, разрыхлена. При инсуффляции складки слизистой пораженного участка, как правило, не расправляются полностью.
В нашем исследовании инфицирование H. pylori было выявлено практически у всех больных при мелкоклеточном варианте и составило 96,7%, при промежуточном варианте MALT-лимфомы желудка — 90%, в отличие от смешанно-клеточных MALT-лимфом, при которых частота инфицирования составила только 53,8%.
При выявлении инфицирования H. pylori мы также определяли степень обсемененности. Оказалось, что при мелкоклеточных MALT-лимфомах высокая частота инфицирования сочетается с выраженной степенью обсемененности чаще (75,9%), чем при других подвариантах. Так, у больных с промежуточным вариантом наличие H. pylori-инфекции сопровождается выраженной степенью обсемененности достоверно реже и выявлено в 38,9%, при смешанных MALT-лифмомах выраженная степень обсемененности установлена у 57,1% пациентов.
Умеренная степень обсемененности при мелкоклеточных опухолях выявлена у 20,7%, при промежуточном варианте чаще — у 61,1%, а при смешанной MALT-лимфоме — у 14,3%.
Слабая степень обсемененности H. pylori встречается у больных MALT-лимфомой желудка крайне редко, она была определена лишь у трех пациентов.
Терапия больных первичной MALT-лимфомой представляет ряд особенностей. Это обусловлено тем, что в мировой практике накоплен относительно небольшой опыт использования всех видов лечебного воздействия — антихеликобактерной терапии, химиотерапии, лучевой терапии, хирургического лечения и их сочетаний.
Антихеликобактерная терапия использовалась нами только при I стадии (классификация Lugano, 1993) MALT-лимфомы желудка мелкоклеточного строения. Лечение проводилось в соответствии с рекомендациями Международного протокола LY03 по изучению MALT-лимфом желудка низкой степени злокачественности [10]. Нами применялась трехкомпонентная схема первой линии эрадикационной терапии, включающая одновременное применение в течение 10–14 дней следующих препаратов:
омепразол по 20 мг в день;
кларитромицин по 500 мг 2 раза в день;
амоксициллин по 1000 мг 2 раза в день.

В результате проведенного лечения у 14 пациентов (87,5%) из 16 больных была достигнута полная ремиссия, у 2 больных (12,5%) констатирована стабилизация заболевания.
Терапевтический эффект антибиотикотерапии реализовался постепенно. Нами установлена последовательность исчезновения проявлений болезни. Первыми ликвидировались клинические симптомы: боль, изжога, тошнота, желудочный дискомфорт.
Вслед за эрадикацией H. pylori постепенно уменьшались визуальные эндоскопические проявления опухолевого поражения: сокращались размеры опухолевого поражения, подслизистой инфильтрации, уменьшался калибр складок слизистой, происходило рубцевание специфических язвенных дефектов, затем восстанавливалась нормальная архитектоника слизистой, исчезала деформация стенок желудка.
Необходимо акцентировать внимание на том, что сроки наступления полного терапевтического эффекта весьма вариабельны. Полная ремиссия, подтвержденная гистологическим и иммунологическим исследованием гастробиоптатов, была диагностирована у больных, получавших антихеликобактерное лечение, в сроки от 2 до 10 месяцев (медиана 5,5 месяцев).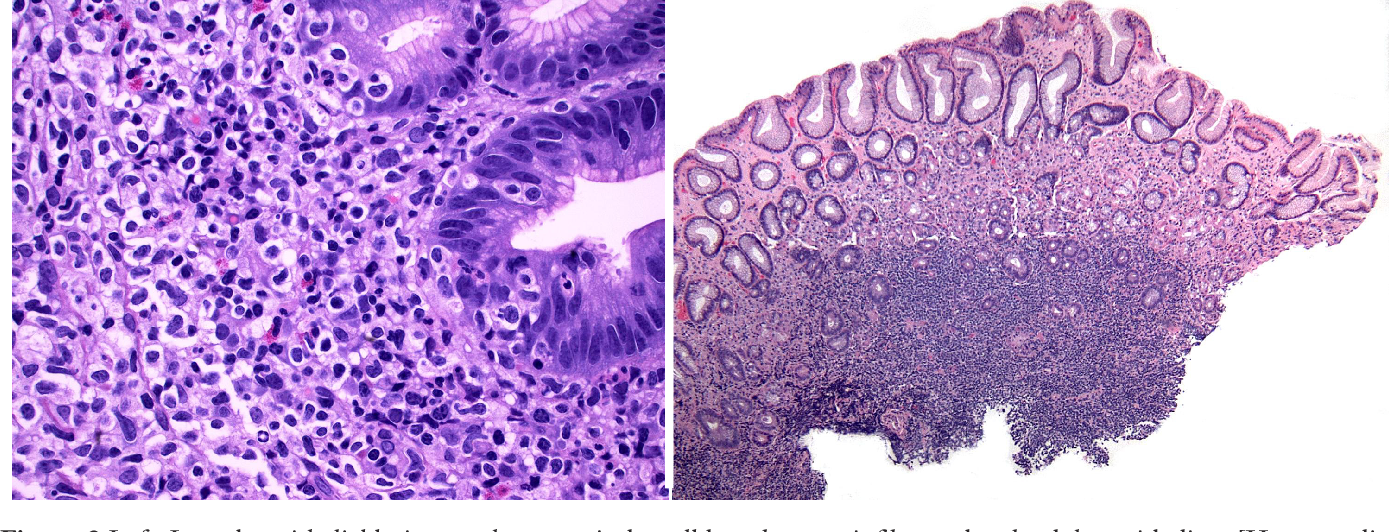
Это означает, что лечение мелкоклеточных MALT-лимфом с применением антихеликобактерных препаратов — это терапия, осуществленная всего за 10–14 дней, но требующая в последующем взвешенного динамического наблюдения и корректной оценки происходящих изменений. Темп наступления полного клинического благополучия является косвенным признаком прогнозирования терапевтического эффекта.
Из 14 больных с подтвержденной полной ремиссией вследствие антихеликобактерной терапии только у одной больной в возрасте 51 год был констатирован рецидив заболевания при контрольном обследовании через 7 месяцев после окончания лечения без каких-либо клинических проявлений. Трактовка эндоскопической картины была сложной: осуществлялась дифференциальная диагностика между эрозивным гастритом и минимальными проявлениями лимфомы. Рецидив был подтвержден иммуноморфологическими исследованиями. В последующем больная получала последовательное лечение Лейкераном (хлорамбуцил), COP с эффектом, который расценен нами как стабилизация заболевания. Учитывая клиническое благополучие, а также наличие тяжелой сопутствующей патологии, было решено хирургическое лечение не применять, а больную оставить под динамическим наблюдением. В течение последующих 36 месяцев больной проводится регулярное обследование (каждые 4–5 месяцев). За этот период наблюдения прогрессирования заболевания не наступило по настоящее время.
Учитывая клиническое благополучие, а также наличие тяжелой сопутствующей патологии, было решено хирургическое лечение не применять, а больную оставить под динамическим наблюдением. В течение последующих 36 месяцев больной проводится регулярное обследование (каждые 4–5 месяцев). За этот период наблюдения прогрессирования заболевания не наступило по настоящее время.
Это наблюдение демонстрирует особое свойство мелкоклеточной MALT-лимфомы. Сочетание клинического благополучия с объективными данными стабилизации позволяет длительно наблюдать за больными на фоне проведения регулярного полноценного обследования.
Таким образом, антихеликобактерная терапия правомочна и эффективна при первичных MALT-лимфомах желудка, но при обязательном строгом соблюдении показаний к ее использованию — I стадия процесса с небольшим локализованным поражением слизистого и подслизистого слоев при H. pylori-позитивных опухолях. Обязательным является динамическое исследование опухолевого субстрата на наличие H. pylori, эрадикация которого необходима для реализации противоопухолевого эффекта. Отсутствие эрадикации H. pylori требует использования химиотерапии с повторными курсами антибиотикотерапии.
pylori, эрадикация которого необходима для реализации противоопухолевого эффекта. Отсутствие эрадикации H. pylori требует использования химиотерапии с повторными курсами антибиотикотерапии.
Литература
Давыдов М. И., Аксель Е. М. Статистика злокачественных новообразований в России и странах СНГ в 2005 г. // Вестник РОНЦ им. Н. Н. Блохина. 2007. Т. 18. № 2 (прил. 1). 156 с.
Brooks J. J., Enterline H. T. Primary gastric lymphomas // Cancer. 1983. V. 51. P. 701–711
Isaacson P., Wright D. H. Malignant lymphoma of the mucosa associated lymphoid tissue. A distinctive type of B-cell lymphoma // Cancer. 1983. V. 52. P. 1410–1416.
Wotherspoon A. C., Doglioni C., Diss T. C. et al. Regression of primary low-grade B-cell gastric lymphoma of mucosa associated lymphoid tissue type after eradication of helicobacter pylori // Lancet. 1993.
 V. 342. P. 575–577.
V. 342. P. 575–577.Parsonnet J., Hansen S., Rodriguez L., Gelb A. B. et al. Helicobacter pylori infection and gastric lymphoma // The New England Journal of Medicine. 1994. V. 330. № 18. P. 1267–1271.
Crabtree J. E., Spencer J. Immunologic aspects of Helicobacter pylori infection and malignant transformation of B cells // Seminars in Gastrointesn. Dis. 1996. V. 7. P. 30–40.
Stolte N. M. Helicobacter pylori gastritis and gastric MALT-lymphoma // Lancet. 1992. V. 338. P. 745–746.
Wotherspoon A. C, Ortiz-Hidalgo C., Falzon M. R., Isaacson P. G. Helicobacter pylori associated gastritis and primary B-cell gastric lymphoma // Lancet. 1991. V. 338. P. 1175–1176.
Xiang Z., Bugndi M., Rappuoli R. et al. Helicobacter pylori host responses in peptic ulceration // Lancet. 1993. V. 342. P. 900–901.
Eidt S.
 , Stolte M., Fischer R. Factors influencing lymph node infiltration in primary gastric malignant lymphoma of the mucosa associated lymphoid tissue. Pathol Res Pract. 1994;190: 1077–1081.
, Stolte M., Fischer R. Factors influencing lymph node infiltration in primary gastric malignant lymphoma of the mucosa associated lymphoid tissue. Pathol Res Pract. 1994;190: 1077–1081.
О. А. Малихова*, кандидат медицинских наук
Б. К. Поддубный**, доктор медицинских наук, профессор
И. В. Поддубная*, доктор медицинских наук, профессор, член-корреспондент РАМН
О. А. Москаленко**, кандидат медицинских наук, доцент
Н. В. Кокосадзе*, кандидат медицинских наук
А. Ю. Концевая*, кандидат медицинских наук
*Учреждение Российской академии наук Российский онкологический научный центр им. Н. Н. Блохина РАМН,
**РМАПО, Москва
Контактная информация об авторах для переписки: malikhova@inbox. ru
ru
Сроки установления диагноза первичной лимфомы желудка
Сроки установления диагноза вторичной лимфомы желудка
Рая. Лимфома желудка. Держаться за волосинку, чтобы жить
Прекрасная Рыжая Женщина – именно так я зову Раечку. Её, всегда ухоженную, стильную, удивительно собранную любительницу шоколада в шоколаде, я знаю уже лет шесть. Каждый раз, когда мне нужно найти что-то интересное, эксклюзивное или просто качественное, Раечка оказывается первой, кому я звоню. И только сейчас я знаю, что именно это её умение быть стильной стало спасительной соломинкой в борьбе с раком.
9197 • • 05.02.2019– Расскажи, как ты вообще поняла, что с тобой что-то не так?
– Я долго к этому шла. Проблемы с желудком, как у всех, были. Да, думаю, гастрит. Ну, таблеточек попьём. Не обращала на это всё внимания слишком долго. А осенью меня скрючило будь здоров! Это были приступы до холодного пота по 10–15 минут, потом отпускало. Но я решила пойти к врачу только тогда, когда меня стало регулярно рвать непереваренной едой через 15 минут после того, как я её съела. Долго искала клинику. Выбрала частную, зарекомендовавшую себя мега-специалистами. Я пошла туда, меня посмотрела, пропальпировала барышня-гастроэнтеролог с кучей регалий. Как потом оказалось, она просто протыкала опухоль и поставила диагноз «рефлюкс». Но направила на любимейший зонд. После зонда врач, ничего не объяснив, сказал: “Вам срочно нужно оперироваться”. Мне нужно было ещё сделать 3D-рентген. Я тогда не понимала, что мне под вопросом поставили диагноз “карцинома”.
Но я решила пойти к врачу только тогда, когда меня стало регулярно рвать непереваренной едой через 15 минут после того, как я её съела. Долго искала клинику. Выбрала частную, зарекомендовавшую себя мега-специалистами. Я пошла туда, меня посмотрела, пропальпировала барышня-гастроэнтеролог с кучей регалий. Как потом оказалось, она просто протыкала опухоль и поставила диагноз «рефлюкс». Но направила на любимейший зонд. После зонда врач, ничего не объяснив, сказал: “Вам срочно нужно оперироваться”. Мне нужно было ещё сделать 3D-рентген. Я тогда не понимала, что мне под вопросом поставили диагноз “карцинома”.
– А когда поняла, что всё серьёзно?
– Я сделала рентген, и после него меня заведующий отделением рентгенологии привёл в кабинет, посадил и взял за руку. Рассказал мне позитивную историю о том, как к нему когда-то пришёл молодой человек с карциномой, и теперь живёт и радуется жизни уже больше 10 лет. Он сказал, что у меня диагноз не подтверждён, нужно сделать ещё кучу анализов… и вот тогда я впервые произнесла через вдохи-выдохи: “Так что вы хотите сказать? У меня…” — и пауза. — “У меня…” — и опять пауза. Не поворачивался язык произнести то, чего все боятся. Но потом я подумала, что надо же когда-то научиться говорить это слово. “У меня рак?” Он ответил: “Да, диагноз онкологический, но нужно понимать, какой. У меня есть мега-дружбан, мега-врач. Вот только к нему — и ни к кому другому”. И дальше последовала цепочка счастливых неслучайных случайностей, благодаря которой всё сложилось отлично, несмотря на диагноз.
— “У меня…” — и опять пауза. Не поворачивался язык произнести то, чего все боятся. Но потом я подумала, что надо же когда-то научиться говорить это слово. “У меня рак?” Он ответил: “Да, диагноз онкологический, но нужно понимать, какой. У меня есть мега-дружбан, мега-врач. Вот только к нему — и ни к кому другому”. И дальше последовала цепочка счастливых неслучайных случайностей, благодаря которой всё сложилось отлично, несмотря на диагноз.
– Ты поехала дообследоваться?
– Да, мы поехали к врачу, которого мне порекомендовал рентгенолог. Он такой, практически доктор Хаус. Он курит прямо в кабинете, что хоть топор вешай. Он за крепким словцом в карман не лезет… Мы пришли, я показала ему предварительный диагноз из первой клиники. Я легла на старый продавленный диван, он буквально сделал два движения пальцами, и потом долго возмущался и ругался, не подбирая выражений, о том, как можно было не прощупать то, что прощупывается двумя движениями.
Был стеноз желудка, сужение. Стеноз, вызванный чем? Это следовало из дальнейших обследований. Я пошла по медицинским рукам и в итоге мне поставили диагноз “лимфома желудка”. И показание к операции, что называется “на вчера”.
Стеноз, вызванный чем? Это следовало из дальнейших обследований. Я пошла по медицинским рукам и в итоге мне поставили диагноз “лимфома желудка”. И показание к операции, что называется “на вчера”.
– Я правильно понимаю, что тебе вырезали желудок?
– Ну, мне вырезали по максимуму, оставив только какую-то культю, из которой будет формироваться то, что потом растянется и будет называться желудком. Теперь во всех описаниях обследований, которые я прохожу, присутствует такое словосочетание, как культя желудка. Желудок удалили, но сама лимфома никуда не делась. И мне нужно было ещё сделать биопсию костного мозга, чтобы понять, понадобится ли мне в дальнейшем пересадка, и вообще на какой стадии находится всё это. И мне опять повезло. Мне с самого начала сказали, что в 90% случаев лимфома, если это не лимфома Ходжкина, прекрасно лечится и достигается полная ремиссия. Поэтому меня сразу настраивали, что никто не умирает, всё хорошо.
– Как ты вообще всё это пережила? Даже сам момент — лечь на операцию.
– Я помню, когда я вышла со снимком, была такая мерзкая погода… Конец февраля. Ветер такой паршивый, снег такой паршивый и вообще очень мерзко… А в голове — белый шум. В тот день я быстро собиралась, опаздывая на рентген… И у меня есть бзик: я никогда не оставляю разобранной постель. И я никогда ни в каком виде кроме белья или пижамы в ней не бываю. А в тот день постель оказалась разобранной. И вот я приехала домой. Я не плакала. А вот как была в свитере, в джинсах, в носках, так и закуталась в одеяло, кокон себе сделала. Организм, он хороший, он всё понимает. И он меня просто отключал. Даже не в сон, а просто куда-то в темноту проваливалась. И вот так я провела просто весь день до вечера. И вот тогда мне впервые стало жутко страшно. Самое первое, о чём я тогда подумала — это родители. Что будет с ними? (На секундочку, родители до сих пор не знают о моём диагнозе. Они знают, что у меня была операция, но диагноза они не знают. Я им наплела ТАКОГО, что они мне поверили: “Мам, да не переживай, у меня просто была язва и вот по ней надо было делать операцию. Все нормально”.) Вот только тогда я заплакала. Первый раз.
Все нормально”.) Вот только тогда я заплакала. Первый раз.
– То есть ни глубокой депрессии, ни недель рыданий? Как ты держалась?
– Сразу включаешь какую-то логику и начинаешь просто действовать: записываться в больницы, сдавать анализы. Всё на полном автомате, без эмоций, просто делать то, что нужно. Элементарно: мне нужно ложиться в больницу? Я не привыкла к домашней одежде, значит, надо купить спортивный костюм. Мне надо купить сумку, потому что у меня только огроменный чемодан. То есть это были простые бытовые вопросы, решение которых замещало всю панику и истерику. Это был список задач и работа над их выполнением.
Как-то был забавный случай. Мне говорят: операция, на вчера. И вот сидим мы с нашим старинным другом, я пью чаёк, и по телевизору идёт реклама какого-то лимитированного «Кит-Ката». И я: «М-м-м, солёная карамель, моя любимая». Друзья: «Так тебе ж нельзя!» Я отвечаю: «Так всё равно через неделю вырежут, чего ж нельзя?» И друг сидит и смеётся: «У неё через неделю операция, у неё лимфома, у неё 6 курсов химии, а она сидит и переживает, успеет или не успеет попробовать лимитированный “Кит-Кат”!» А что мне ещё делать оставалось?
– Через неделю ты легла на операцию?
– Да, госпитализировалась, прооперировалась, провела пять дней в реанимации. Но даже там меня держали маленькие радости. Вот я лежу и понимаю, что больше всего на свете мне хочется умыться и почистить зубы. И вот я пробую себя привести в порядок. Так как у меня стояло то, что называется “тефлонка” — чтоб не каждый раз вену прокалывать, в тебе оставляют иглу с крышечкой. И вот она во мне стояла, обмотанная нормальным куском бинта. И что я делаю? Отрываю кусок бинтика от этого всего, делю его на три части. Одной частью я, можно сказать, умылась: поплевала на него, протёрла себе глаза, зубы, лицо — вот и умылась, почистила зубы. А потом, глядя во фронталочку, причесалась руками, разделила волосы на две части и стала плести себе косички. Заплела косички, бинтиками перевязала. Несимметрично. Переплела. В общем, добилась симметричности. И вот лежу, красивая. Врачи, приходите, теперь я готова к осмотру!
Но даже там меня держали маленькие радости. Вот я лежу и понимаю, что больше всего на свете мне хочется умыться и почистить зубы. И вот я пробую себя привести в порядок. Так как у меня стояло то, что называется “тефлонка” — чтоб не каждый раз вену прокалывать, в тебе оставляют иглу с крышечкой. И вот она во мне стояла, обмотанная нормальным куском бинта. И что я делаю? Отрываю кусок бинтика от этого всего, делю его на три части. Одной частью я, можно сказать, умылась: поплевала на него, протёрла себе глаза, зубы, лицо — вот и умылась, почистила зубы. А потом, глядя во фронталочку, причесалась руками, разделила волосы на две части и стала плести себе косички. Заплела косички, бинтиками перевязала. Несимметрично. Переплела. В общем, добилась симметричности. И вот лежу, красивая. Врачи, приходите, теперь я готова к осмотру!
– А как прошло первое время дома после операции?
– Ну, мне надо было заново учиться кушать. Представь, что ты только что родилась и твой желудок не знает, что такое еда и как надо её есть.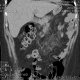 Как маленьким деткам, тебе нужен прикорм. И шесть раз в день ты обязана есть. По чуть-чуть. По полчашечки, по пол-ложечки. Немного, но 6 раз в день ты обязана. Хорошо, когда ты дома. Потом, когда мы уже стали безболезненно гулять, и я стала выходить на долгие прогулки, появился вопрос, где есть. Мы заходили в магазин и я набирала детского питания. Мой рюкзак тарахтел детским питанием, как у примерной мамаши. У меня были баночки и фруктовые, и мясные, и овощные. У меня всегда была с собой ложка. И каждые 2-3 часа мы садились на лавочке, и я ела. И, знаешь, было даже прикольно. У меня-то в детстве таких консервов не было. Если ты ко всему этому относишься с долей иронии и сарказма, то всё гораздо легче. Я была первой, кто над этим всем всегда шутил. И всё это время я ни разу не плакала. После того рентгена я плакала всего дважды.
Как маленьким деткам, тебе нужен прикорм. И шесть раз в день ты обязана есть. По чуть-чуть. По полчашечки, по пол-ложечки. Немного, но 6 раз в день ты обязана. Хорошо, когда ты дома. Потом, когда мы уже стали безболезненно гулять, и я стала выходить на долгие прогулки, появился вопрос, где есть. Мы заходили в магазин и я набирала детского питания. Мой рюкзак тарахтел детским питанием, как у примерной мамаши. У меня были баночки и фруктовые, и мясные, и овощные. У меня всегда была с собой ложка. И каждые 2-3 часа мы садились на лавочке, и я ела. И, знаешь, было даже прикольно. У меня-то в детстве таких консервов не было. Если ты ко всему этому относишься с долей иронии и сарказма, то всё гораздо легче. Я была первой, кто над этим всем всегда шутил. И всё это время я ни разу не плакала. После того рентгена я плакала всего дважды.
– Расскажешь?
– В апреле я начала проходить химию. И после первого курса я поехала к родителям, показаться, что я жива. До того, как у меня начнут выпадать волосы и они поймут, что у меня не язва. Но выпадать волосы начали именно тогда, когда я была у них. Я просыпалась, проводила рукой, и в ней оставалось прям море этих волос. А мне предстояли ещё день и ночь у родителей мужа. И вот я как завязала хвостик, я его не развязывала. Я спала сидя, потому что боялась, что если я у родителей проснусь, а у меня всё останется на подушке, то я не буду знать, что с этим делать. Я не расчесывалась всё это время, не мыла голову. Всё терпела до возвращения домой. И вот я приехала и пошла мыть голову. Я сливаю воду на голову и понимаю, что в руках у меня остаются не просто пучки, а практически всё. Волосы у меня тогда были по плечи. И вот 90% волос у меня в один момент просто осталось в ванной. И вот тогда я плакала второй раз. Это были не просто слёзы, это была истерика на грани психоза. Но! Те 10% волос, которые у меня остались, стали практически моим фетишем. Каждый для себя находит что-то типа “я сделаю себе татуировку после того, как…”. Вот так решила и я: побреюсь налысо, срежу всё это уродство и лишу себя своих последних волос только после того, как мне поставят диагноз “Ремиссия”.
Но выпадать волосы начали именно тогда, когда я была у них. Я просыпалась, проводила рукой, и в ней оставалось прям море этих волос. А мне предстояли ещё день и ночь у родителей мужа. И вот я как завязала хвостик, я его не развязывала. Я спала сидя, потому что боялась, что если я у родителей проснусь, а у меня всё останется на подушке, то я не буду знать, что с этим делать. Я не расчесывалась всё это время, не мыла голову. Всё терпела до возвращения домой. И вот я приехала и пошла мыть голову. Я сливаю воду на голову и понимаю, что в руках у меня остаются не просто пучки, а практически всё. Волосы у меня тогда были по плечи. И вот 90% волос у меня в один момент просто осталось в ванной. И вот тогда я плакала второй раз. Это были не просто слёзы, это была истерика на грани психоза. Но! Те 10% волос, которые у меня остались, стали практически моим фетишем. Каждый для себя находит что-то типа “я сделаю себе татуировку после того, как…”. Вот так решила и я: побреюсь налысо, срежу всё это уродство и лишу себя своих последних волос только после того, как мне поставят диагноз “Ремиссия”.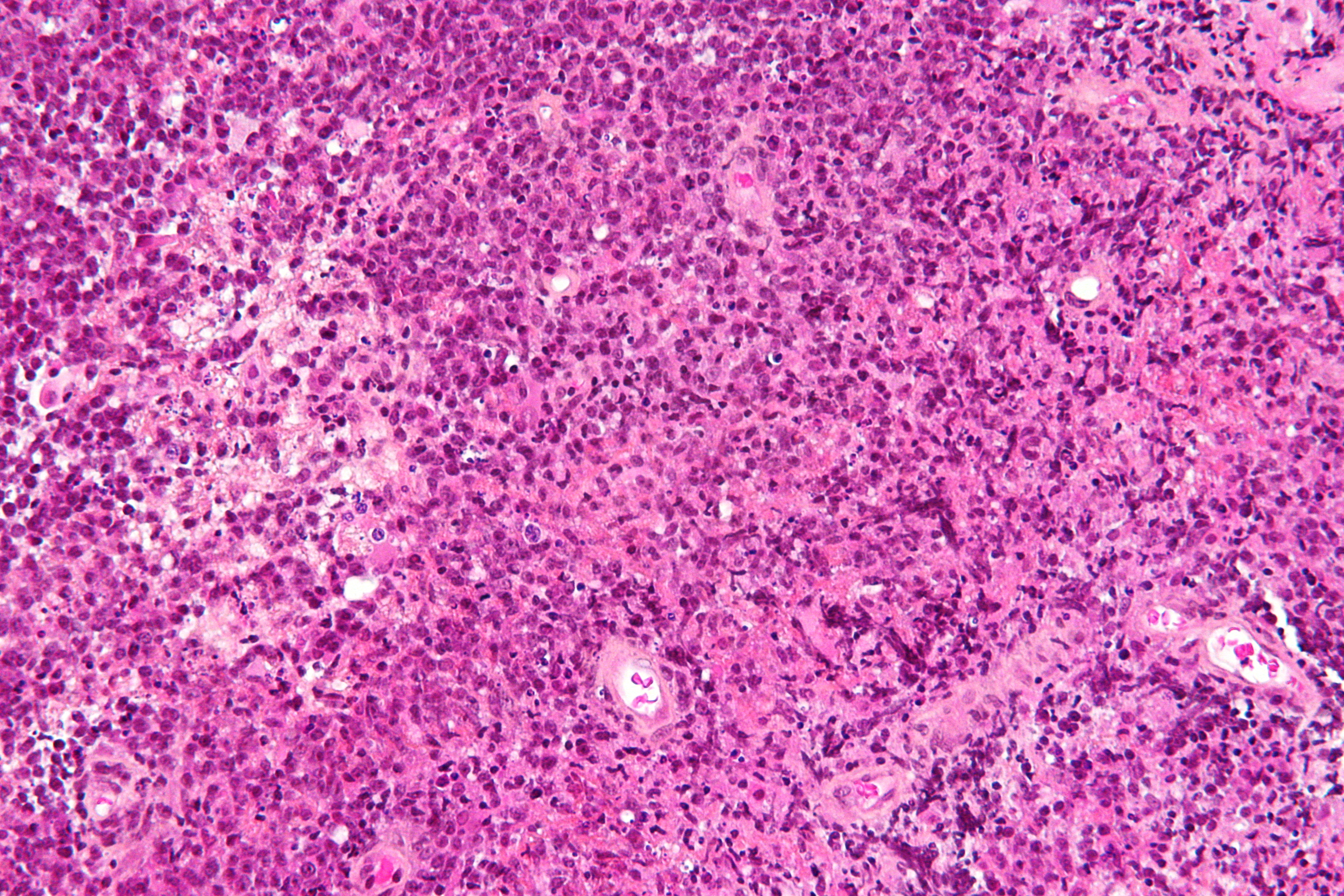 И вот то, что называется “держаться за волосинку” — для меня было в прямом смысле. Я чего только не придумывала!
И вот то, что называется “держаться за волосинку” — для меня было в прямом смысле. Я чего только не придумывала!
– А что можно придумать, если у тебя осталось три волосины?
– Ну надо же как-то лысину прятать! Пришлось постоянно что-то придумывать, как выглядеть хорошо. До какого-то момента я ходила в бейсболке, где был маленький крысиный хвостик, который я умудрялась завязать маленькой резиночкой, но он торчал. То, что у меня плешивая облысевшая башка — это одна история. Но у меня есть хвостик! А значит, у меня есть волосы! Значит, не всё потеряно, со мной всё хорошо! Я живая! В конце концов, кто сказал, что рак — это не жизнь? Особенно если не гуглить симптомы, а погуглить статистику. 10 лет назад статистика говорила, что полная ремиссия лимфомы — это 90%!
Так что я решила жить. Я стала постоянно придумывать что-то на голову. Я купила себе две шляпы, кучу платочков, где-то высмотрела, как можно носить шляпу и бандану-арафатку, какой-то рэпер-стайл. Я с этим игралась. Но, если честно, выйти на улицу в платке было непросто. Мне всё время казалось, что на меня все смотрят, все сверлят меня взглядом, все знают, что со мной. И я не могла себе позволить выглядеть плохо. То есть, если вы уж на меня смотрите, завидуйте. А что мне оставалось делать? Я не позволяла себе выйти из дома без макияжа. Ну, подумаешь, красить было особо нечего: ресницы и брови повыпадали. Я все равно нашла, что накрасить. И так прошло моё лето. В поиске новых шляп, офигенных платочков и способов их завязывать и в ожидании поездки в Москву. Потому что только в Москве на тот момент делали ПЭТ-КТ, которое должно было дать понимание, нужно ли мне ещё будет делать химию, нужна ли мне лучевая и, вообще, что со мной: я здорова или нет. У нас в Киеве такого нет.
Но, если честно, выйти на улицу в платке было непросто. Мне всё время казалось, что на меня все смотрят, все сверлят меня взглядом, все знают, что со мной. И я не могла себе позволить выглядеть плохо. То есть, если вы уж на меня смотрите, завидуйте. А что мне оставалось делать? Я не позволяла себе выйти из дома без макияжа. Ну, подумаешь, красить было особо нечего: ресницы и брови повыпадали. Я все равно нашла, что накрасить. И так прошло моё лето. В поиске новых шляп, офигенных платочков и способов их завязывать и в ожидании поездки в Москву. Потому что только в Москве на тот момент делали ПЭТ-КТ, которое должно было дать понимание, нужно ли мне ещё будет делать химию, нужна ли мне лучевая и, вообще, что со мной: я здорова или нет. У нас в Киеве такого нет.
– Что показало ПЭТ-КТ?
– Мне не понадобилось ни лучевой, ни пересадки костного мозга, к счастью. На ПЭТ-КТ сказали, что я «чистая». Когда мы с мужем приехали домой, я сказала ему, что пора. Я здорова, рака нет, соответственно, и старых волос быть не может. Мне нужно было всё обнулить. В прямом смысле. “Вань, у тебя на работе у гримеров есть машинка? Тащи! Всё! Обнуляем голову — обнуляем жизнь!” Это был третий раз, когда я плакала. Но на этот раз это была истерика с облегчением, что всё наконец закончилось. Я хохотала, плакала, сопли пузырями, и это было огромное облегчение. Мы вдвоём стояли и плакали. И первое, что я сделала — посмотрела в зеркало: “Лысая башка, дай пирожка”. И в первую ночь мы легли спать, вдруг я резко просыпаюсь, Ваня перепуганно спрашивает, что случилось, может, мне плохо? “Голова мёрзнет, — говорю. — Как вы спите с лысой головой?”
Мне нужно было всё обнулить. В прямом смысле. “Вань, у тебя на работе у гримеров есть машинка? Тащи! Всё! Обнуляем голову — обнуляем жизнь!” Это был третий раз, когда я плакала. Но на этот раз это была истерика с облегчением, что всё наконец закончилось. Я хохотала, плакала, сопли пузырями, и это было огромное облегчение. Мы вдвоём стояли и плакали. И первое, что я сделала — посмотрела в зеркало: “Лысая башка, дай пирожка”. И в первую ночь мы легли спать, вдруг я резко просыпаюсь, Ваня перепуганно спрашивает, что случилось, может, мне плохо? “Голова мёрзнет, — говорю. — Как вы спите с лысой головой?”
– Что ещё помогло тебе не свалиться в болезнь, а именно жить?
– Как ни странно, но то, что я научилась произносить слово “рак”. Это было сложно, но постепенно ты понимаешь, что чем чаще ты его произносишь, тем легче тебе становится. Мы же говорим “ангина” или “грипп”, так же и “рак”. Это просто название просто ещё одной болезни. Не надо преувеличивать и делать из неё нечто более угрожающее, чем есть. Когда меня спрашивали, я спокойно научилась говорить, да, это рак, да, это онкология.
Когда меня спрашивали, я спокойно научилась говорить, да, это рак, да, это онкология.
– Что в тебе поменяла болезнь?
– Всё это дало какую-то невероятную уверенность. На грани с самоуверенностью. Благодаря раку я поборола свои страхи настолько, что поняла, что я живу так, как хочу я, а не так, как мне пытаются навязать люди вокруг. Я стала уверенной в себе и стала чувствовать себя яркой, хотя раньше всегда была той самой “некрасивой подругой”. Если даже взять чисто женскую историю, я вдруг поняла, что никого не волнует, что у тебя сегодня не идеальная прическа, потому что дело в глазах, в том, как ты себя подаёшь, как ты эмоционируешь. И ты наконец прекращаешь себя зажимать, боясь чужих реакций.
А ещё, ты знаешь, у многих есть в жизни такой активный период, когда случаются приключения, путешествия, впечатления. У меня такого периода тогда не было. Не было ни физической, ни финансовой возможности. И я «догоняю» его теперь. Сейчас тот период, который я должна была прожить тогда. Например, прямо сейчас у меня в рюкзаке — балетки, потому что я собираюсь на свой первый урок балета для взрослых. Потому что я хочу сделать то, чем давно хотела заняться, но никогда не делала. И потому что во мне сейчас достаточно уверенности, чтобы наконец попробовать.
Например, прямо сейчас у меня в рюкзаке — балетки, потому что я собираюсь на свой первый урок балета для взрослых. Потому что я хочу сделать то, чем давно хотела заняться, но никогда не делала. И потому что во мне сейчас достаточно уверенности, чтобы наконец попробовать.
– Что бы ты хотела сказать тем, кто сейчас борется за свою жизнь?
– Даже если вам поставили диагноз “рак”, не забывайте жить! Именно сейчас делайте то, чего вы давно хотели. Не надо ждать момента, когда вы выздоровеете, чтобы начать вышивать бисером или варить борщ. Не потому что этого может не случиться, а потому что когда вы выздоровеете, вы просто станете снова откладывать. У вас тот самый момент, когда можно позволить себе жить и исполнять всё то, чего вы так давно хотели!
Авторы:Современные подходы к лечению первичных MALT-лимфом желудка Текст научной статьи по специальности «Клиническая медицина»
УДК: 616. 411-006.441 DOI: 10.12737/11201
411-006.441 DOI: 10.12737/11201
СОВРЕМЕННЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ ПЕРВИЧНЫХ MALT-ЛИМФОМ ЖЕЛУДКА
С.В. ГОЛУБ, В.А. СОЛОДКИЙ, В.М. СОТНИКОВ, Г.А. ПАНЬШИН
ФГБУ «Российский научный центр рентгенорадиологии» МЗ РФ, ул. Профсоюзная, д. 86, г. Москва, Россия, 117997
Аннотация. Основной темой статьи является освещение современных подходов к лечению MALT-лимфом желудка. На сегодняшний день, выбор тактики лечения первичной неходжкинской лим-фомы желудка, разновидностью которой является MALT-лимфома желудка, представляет собой актуальную медицинскую и социальную проблему. Отдельной проблемой, затрудняющей изучение данного заболевания, является его редкость, в среднем регистрируется 3-4 случая на 1 млн. населения. Исторически доминирующее место в лечении данной нозологии занимало хирургическое лечение. Открытие патогенетической роли H. pylori, разработка новых препаратов и схем химиотерапии, широкое использование препаратов моноклональных антител, значительно повысили эффективность лекарственной терапии. Рутинное использование компьютерной томографии, появление методик прецизионной конформной радиотерапии значительно укрепили позиции радиотерапии, особенно в сочетании с химиотерапией, позволяя добиваться результатов лечения сопоставимых с хирургическим лечением по эффективности и частоте осложнений. По этим причинам в настоящее время значительно возросла значимость консервативных, органосохраняющих методик лечения. Однако не смотря на все достижения, пока не удается достигать полной ремиссии у всех пациентов, требуется дальнейшее изучение данного заболевания, возможностей каждой методики лечения и их возможных комбинаций.
pylori, разработка новых препаратов и схем химиотерапии, широкое использование препаратов моноклональных антител, значительно повысили эффективность лекарственной терапии. Рутинное использование компьютерной томографии, появление методик прецизионной конформной радиотерапии значительно укрепили позиции радиотерапии, особенно в сочетании с химиотерапией, позволяя добиваться результатов лечения сопоставимых с хирургическим лечением по эффективности и частоте осложнений. По этим причинам в настоящее время значительно возросла значимость консервативных, органосохраняющих методик лечения. Однако не смотря на все достижения, пока не удается достигать полной ремиссии у всех пациентов, требуется дальнейшее изучение данного заболевания, возможностей каждой методики лечения и их возможных комбинаций.
Ключевые слова: певичная неходжкинская лимфома, экстраннодальная, желудок.
PRIMARY GASTRIC MALT LYMPHOMA – MODERN TREATMENT APPROACHES
S. V. GOLUB, V.A. SOLODKIY, V.M. SOTNIKOV, G.A. PANSHIN
V. GOLUB, V.A. SOLODKIY, V.M. SOTNIKOV, G.A. PANSHIN
Russian scientific center of radiology» health ministry, st. Union, d. 86, Moscow, Russia, 117997
Abstract. Main idea of this article is to make a short overview of modern MALT lymphoma treatment approaches. Historically, surgery was the leading treatment modality. Discovery of H.pylori involvement, invention of new drugs and chemotherapy protocols, wide use of monoclonal antibodies, significantly raised the effectiveness of conservative treatment. Routine use of CT scanning, invention of conformal, precise radiotherapy techniques allowed to achieve fine radiotherapy treatment results, especially in the case of combined chemo -radiotherapy protocols. That is why nowadays conservative treatment plays more significant role. However, complete remission cannot be achieved in all the cases. More research is required and thorough analyze of advantages and disadvantages of every technique and their combinations.
Key words: primary non-hodgkin gastric lymphoma, extranodal.
Желудочно-кишечный тракт (ЖКТ) является наиболее частой экстранодальной локализацией не-ходжкинских лимфом желудка. По данным мировой литературы, частота первичного поражения ЖКТ колеблется от 10 до 25%, наиболее часто поражается желудок (50-75%) [1]. Особое внимание в последние годы уделяется относительно доброкачественным клиническим формам первичных лимфом желудка. С начала 80-х годов в зарубежной литературе появились публикации, в которых из доброкачественных опухолевых процессов была выделена В-клеточная лимфома низкой степени злокачественности MALT-типа (mucosa associated lymphoid tissue), впервые описанная P.G.Isaacson. Ее характерной особенностью является антигенная зависимость от инфицирования слизистой оболочки желудка Helicobacter pylori. В 1997 г. экстранодальная MALT-лимфома низкой степени злокачественности была включена в REAL-классификацию как самостоятельный вариант В-клеточной лимфомы маргинальной зоны [2].
Исторически основу всех схем лечения неходжкинской лимфомы (НХЛ) желудка составляло хирургическое лечение. Действительно, хирургическое лечение в объеме гастрэктомии или радикальной резекции, особенно если оно дополнено лучевой и/или химиотерапией (в зависимости от стадии, степени злокачественности и распространенности опухоли), позволяет добиться хороших показателей безрецидивной выживаемости и локо-регионарного контроля [3]. Однако, в 2004 году Sam S.Yoon et al. [3] провели ретроспективный анализ результатов нескольких клинических исследований, результаты показали, что при лечении пациентов с I-II стадией НХЛ желудка, отказ от проведения хирургического лечения не снижает эффективность лечения, не приводит к увеличению частоты осложнений. В исследовании
Библиографическая ссылка:
Голуб С.В., Солодкий В.А., Сотников В.М., Паньшин Г. А. Современные подходы к лечению первичных MALT-лимфом желудка // Вестник новых медицинских технологий. Электронное издание. 2015. №2. Публикация 2-6. URL: http://www.medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
А. Современные подходы к лечению первичных MALT-лимфом желудка // Вестник новых медицинских технологий. Электронное издание. 2015. №2. Публикация 2-6. URL: http://www.medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
P.Kosch et al. [5], сравнивались 2 группы пациентов с I-II стадией НХЛ желудка (в т.ч. с MALT лимфо-мами), группа консервативного лечения (n=106) и группа хирургического лечения (n=79). Пятилетняя выживаемость составила 84.4% против 82.0%, полная ремиссия была достигнута в 95.2 и 100% случаев, среди всех 201 пациентов был зарегистрирован 1 случай желудочного кровотечения в группе консервативного лечения.
В настоящее время широко используется эрадикационная антибактериальная терапия в лечении локальных лимфом MALT-типа маргинальной зоны желудка. Результаты двух крупных клинических исследований убедительно доказывают, что возможно добиться долгосрочной полной ремиссии при использовании только эрадикационной терапии [6,7]. Медиана наблюдения в этих исследования составила 45 (12-89) и 75 (1-116) месяцев соответственно. Совсем недавно были опубликованы данные 10-ти летних наблюдений Marburg group [8]. Ремиссия после эрадикации H.pylori была достигнута у 96 из 120 пациентов, а безрецидивная ремиссия была достигнута у 80% пациентов. Стоит также отметить, что наличие транслокации t(11;18) является важным прогностическим фактором эффективности эрадикационной терапии. Эффективность эрадикационной терапии у пациентов с выявленной транслокацией t(11;18) снижается [9], также выявление t(11;18) является отрицательным фактором прогноза при проведении химиотерапии [10].
Медиана наблюдения в этих исследования составила 45 (12-89) и 75 (1-116) месяцев соответственно. Совсем недавно были опубликованы данные 10-ти летних наблюдений Marburg group [8]. Ремиссия после эрадикации H.pylori была достигнута у 96 из 120 пациентов, а безрецидивная ремиссия была достигнута у 80% пациентов. Стоит также отметить, что наличие транслокации t(11;18) является важным прогностическим фактором эффективности эрадикационной терапии. Эффективность эрадикационной терапии у пациентов с выявленной транслокацией t(11;18) снижается [9], также выявление t(11;18) является отрицательным фактором прогноза при проведении химиотерапии [10].
Исследование роли H.pylori в патогенезе НХЛ желудка, применение эрадикационной антибактериальной терапии, открытия в области радиобиологии, изменили место дистанционной лучевой терапии в лечении НХЛ желудка. Проведение радиотерапии у пациентов с MALT лимфомой желудка I-II1 стадии в случае рецидива или прогрессирования заболевания после проведенной эрадикационной антибактериальной терапии, позволяет добиться 4-5 летней безрецидивной выживаемости у 85-100% пациентов [11]. Проведение радиотерапии также показано пациентам MALT лимфомой желудка ранней стадии, в случае, если заболевание не ассоциировано с H.pylori и проведение эрадикационной терапии не имеет смысла [12].
Проведение радиотерапии также показано пациентам MALT лимфомой желудка ранней стадии, в случае, если заболевание не ассоциировано с H.pylori и проведение эрадикационной терапии не имеет смысла [12].
Химиотерапия остается важнейшим компонентом программ лечения лимфопролиферативных заболеваний, MALT лимфома желудка не стала исключением. «Золотым стандартом» химиотерапевтиче-ского лечения уже долго время остается схема CHOP и ее модификации, которая может быть дополнена схемой CVP. В настоящее время получены результаты проспективного рандомизированного контролируемого исследования MALT лифом желудка [13], в исследовании принимал участие 241 пациент, целью исследования была оценка эффективности разных видов лечения. Использовалась одна схема химиотерапии: 3 цикла CHOP-21 + 4 цикла CVP. У всех пациентов была достигнута полная ремиссия. На отметке наблюдений 7.5 лет бессобытийная выживаемость была ниже у пациентов после лучевой терапии (52%) и хирургического лечения (52%) по сравнению с пациентами получавших химиотерапию (87%).
В то же время, продолжается исследования альтернативных схем химиотерапи, уже получены результаты проспективного исследования эффективности 2-хлордезоксиаденозина (2CdA) у пациентов с MALT лимфой желудка. [14] Применялась следующая схема: 2CdA в дозе 0.12 мг\кг, с 1 по 5 день, 4-х недельного цикла. Всего проводилось 6 циклов монохимиотерапии. В исследование было включено
26 пациентов из которых 19 пациентов с MALT лимфой желудка. У всех 19 пациентов было достигнута полная ремиссия, у 3 пациентов был выявлен рецидив через 13- 22 месяца после завершения химиотерапии, в дальнейшем ремиссия была достигнута после проведения лучевой терапии. На момент публикации результатов, период наблюдения составил 72 месяца, новых рецидивов выявлено не было [15]. Токсичность лечения была выражена слабо, в основном отмечалась гематологическая токсичность, потребовавшая уменьшения курсовой дозы у нескольких пациентов..JPG)
Схема с использованием митоксантрона, хлорамбуцила и преднизолона (МСР) показала хорошие результаты по итогам ретроспективного исследования на основании данных 19 пациентов с MALT лим-фомами различных локализаций. Среди них было 5 пациентов с MALT лимфой желудка. Полной ремиссии удалось добиться у 4 пациентов, у 1 пациента была достигнута частичная ремиссия [16]. Медиана наблюдения составила 16 месяцев, не было выявлено ни одного рецидива.
Так как клетки MALT лимфомы схожи с В-лимфоцитами, имеющими CD20 рецепторы, в схемы лечения могут включаться препараты антител к CD20 рецепторам, в частности, ритуксимаб. Было проведено ретроспективное исследование, в котором приняли участие 6 пациентов с MALT лимфомой желудка, была выявлена умеренная эффективность ритуксимаба при оценке достигнутой ремиссии (55%) [17]. Эффективность Ритуксимаба была также доказана по результатам еще одного исследования проведенного среди
27 пациентов с MALT лимфомой желудка резистентной к антибактериальной терапии, или MALT лимфо-мой желудка без признаков H. pylori [18]. Важно также отметить, что полученные данные также указывают на то, что на эффективность Ритуксимаба не влияет наличие у пациента t(11; 18)(q21; q21).
pylori [18]. Важно также отметить, что полученные данные также указывают на то, что на эффективность Ритуксимаба не влияет наличие у пациента t(11; 18)(q21; q21).
Умеренная эффективность Ритуксимаба в режиме монотерапии наводит на мысль о необходимости использования комбинированных схем лечения, таких как R-CHOP или R-CNOP. Эти схемы доказали свою высокую эффективность в качестве химиотерапии второй или третьей линии, даже у пациентов с t(11; 18)(q21; q21). По данным исследования [19] удалось добиться устойчивой полной ремиссии у всех 7 пациентов с MALT лимфомой желудка, медиана наблюдения составила 18 месяцев. В то же время, ав-
Библиографическая ссылка:
Голуб С.В., Солодкий В.А., Сотников В.М., Паньшин Г.А. Современные подходы к лечению первичных MALT-лимфом желудка // Вестник новых медицинских технологий. Электронное издание. 2015. №2. Публикация 2-6. URL: http://www.medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
2015. №2. Публикация 2-6. URL: http://www.medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
торы отмечают не очень хорошую переносимость данной схемы лечения, что не позволяет рекомендовать ее в качестве схемы химиотерапии первой линии.
Заключение. Современные подходы к лечению MALT-лимфом желудка претерпели значительные изменения за последнее десятилетия. Повсеместное использование хирургического лечения уступило место органосохраняющим методикам лечения. Достигнуты большие успехи в развитии химиотерапии, появились новые схемы, в широкую клиническую практику были внедрены препараты моноклональных антител, это позволило значительно улучшить результаты лечения. Проведение эрадикационной антибактериальной терапии в монорежиме часто позволяет добиться клинической ремиссии. Технический прогресс значительно расширил возможности радиотерапии, в первую очередь позволив добиваться подведения необходимой дозы к лечебному объему при минимальном облучении здоровых тканей, что особенно важно при облучении опухолей желудка. Не смотря на такой широкий арсенал лечебных методик, все еще не удается добиваться полной ремиссии у всех пациентов, на сегодняшний день не разработан единый алгоритм подбора оптимальной тактики лечения, в зависимости от клинической ситуации и состояния пациента. Все эти факты указывают на то, что требуется дальнейшее изучение этой непростой нозологии.
Не смотря на такой широкий арсенал лечебных методик, все еще не удается добиваться полной ремиссии у всех пациентов, на сегодняшний день не разработан единый алгоритм подбора оптимальной тактики лечения, в зависимости от клинической ситуации и состояния пациента. Все эти факты указывают на то, что требуется дальнейшее изучение этой непростой нозологии.
Литература
1. Неред С.Н., Шааенков В.А., Поддубная И.В. Хирургическое и консервативное лечение осложненных форм неходжкинских лимфом желудка // Онкология. Журнал им.П.А. Герцена. 2012. №1. C. 2832.
2. Поддубная И.В. Экстранодальные НХЛ. Клиническая гематология Под ред. М.А.Волковой. М.: Медицина, 2001. C. 336-375.
3. Aviles A., Nambo M.J., Neri N. The role of surgery in primary gastric lymphoma: results of a controlled clinical trial // Ann Surg. 2004. V. 240. P. 44-50.
2004. V. 240. P. 44-50.
4. Fischbach W., Goebeler-Kolve M.E., Dragosics B. Long term outcome of patients with gastric marginal zone B cell lymphoma of mucosa associated lymphoid tissue (MALT) following exclusive Helicobacter pylori eradication: experience from a large prospective series // Gut. 2004. V.53.P. 34-37.
5. Harris NL., Jaffe ES., Diebold Y. World Health Organization classifiacation of neoplastic diseases of the hematoetic and lymphoid tissues. Report of the Clinical Advisory Commettee Meeting – Asirlie House, Virginia, November 1997 // J. Clin. Oncol. 1999. V.17. P. 3835-3849.
6. Jager G., Neumeister P., Brezinschek R. Treatment of extranodal marginal zone B-cell lymphoma of mucosa-associated lymphoid tissue type with cladribine: a phase II study // J Clin Oncol. 2002. V. 20, №18. Р. 3872-3877.
7. Jager G., Neumeister P., Quehenberger F. Prolonged clinical remission in patients with extranodal marginal zone B-cell lymphoma of the mucosa-associated lymphoid tissue type treated with cladribine: 6 year follow-up of a phase II trial // Ann Oncol. 2006. V.17, №11. Р.1722-1723.
Jager G., Neumeister P., Quehenberger F. Prolonged clinical remission in patients with extranodal marginal zone B-cell lymphoma of the mucosa-associated lymphoid tissue type treated with cladribine: 6 year follow-up of a phase II trial // Ann Oncol. 2006. V.17, №11. Р.1722-1723.
8. Koch P., del Valle F., Berdel W.E. Primary gastrointestinal non-Hodgkin’s lymphoma: II. Combined surgical and conservative or conservative management only in localized gastric lymphoma-results of the prospective German Multicenter Study GIT NHL 01/92 // J Clin Oncol. 2001. V.19. P. 3874-3883.
9. Levy M., Copie-Bergman C., Cameiro C. Prognostic value of translocation t(11;18) in tumoral response of low-grade gastric lymphoma of mucosa-associated lymphoid tissue type to oral chemotherapy // J Clin Oncol. 2005. V. 23. P. 5061-5066.
10. Liu H., Ye H., Ruskone-Fourmestraux A. T(11;18) is a marker for all stage gastric MALT lymphomas that will not respond to H. pylori eradication // Gastroenterology. 2002. V.122. P. 1286-1294.
T(11;18) is a marker for all stage gastric MALT lymphomas that will not respond to H. pylori eradication // Gastroenterology. 2002. V.122. P. 1286-1294.
11. Martinelli G., Laszlo D., Ferreri A. Clinical activity of rituximab in gastric marginal zone non-hodgkin’s lymphoma resistant to or not eligible for anti-helicobacter pylori therapy // J Clin Oncol. 2005. V. 20, 9. Р. 1979-1983.
12. Raderer M., Jager G., Brugger S. Rituximab for treatment of advanced extranodal marginal zone B cell lymphoma of the mucosa-associated lymphoid tissue lymphoma // Oncology. 2003. V.65, №4. P.306-310.
13. Ruskoner-Fourmestraux A., Lavergne A., Aegerter P.H. Predictive factors for regression of gastric MALT lymphoma after anti- Helicobacter pylori treatment // Gut. 2001. V. 48. P.297-303.
14. Sam S.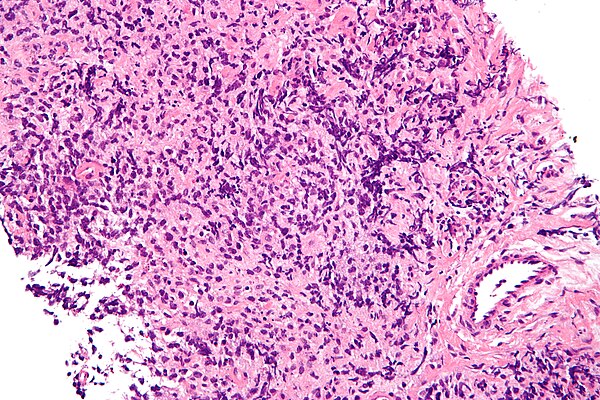 Yoon, Daniel G.Colit, Carol S. Portlock. The diminishing role of surgery in the treatment of gastric lymphoma // Ann Surg. 2004. V. 240. P. 28-37.
Yoon, Daniel G.Colit, Carol S. Portlock. The diminishing role of surgery in the treatment of gastric lymphoma // Ann Surg. 2004. V. 240. P. 28-37.
15. Vrieling C., de Jong D., Boot H. Long-term results of stomach-conserving therapy in gastric MALT lymphoma // Radiother Oncol. 2008. V. 87 P. 405-411.
16. Wohrer S., Drach J., Hejna M. Treatment of extranodal marginal zone B-cell lymphoma of mucosa-associated lymphoid tissue (MALT lymphoma) with mitoxantrone, chlorambucil and prednisone (MCP) // Ann Oncol. 2003. V.14, №12. P. 1758-1761.
Библиографическая ссылка:
Голуб С.В., Солодкий В.А., Сотников В.М., Паньшин Г.А. Современные подходы к лечению первичных MALT-лимфом желудка // Вестник новых медицинских технологий. Электронное издание. 2015. №2. Публикация 2-6. URL: http://www. medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
17. Wohrer S., Puspok Aro, Drach J. Rituximab, cyclophosphamide, doxorubicin, vincristine and prednisone (R-CHOP) for treatment of early-stage gastric diffuse large B-cell lymphoma // Ann Oncol. 2004. V.1, №15. P.1086-1090.
18. Wundisch T., Dieckhoff P., Gunther A. 10-Year follow-up of 120 patients with gastric MALT lymphoma after Helicobacter pylori eradication – histological residual disease and second cancers // J Clin Oncol. 2008. V. 34. P. 2061-2070.
19. Wundisch T., Thiede C., Morgner A. Long-term follow-up of gastric MALT lymphoma after Helicobacter pylori eradication // J Clin Oncol. 2005. V.23, №31. P.1-7.
References
1. Nered SN, Shaaenkov VA, Poddubnaya IV. Khirurgicheskoe i konservativnoe lechenie oslozhnen-nykh form nekhodzhkinskikh limfom zheludka. Onkologiya. Zhurnal im.P.A. Gertsena. 2012;1:28-32. Russian.
Nered SN, Shaaenkov VA, Poddubnaya IV. Khirurgicheskoe i konservativnoe lechenie oslozhnen-nykh form nekhodzhkinskikh limfom zheludka. Onkologiya. Zhurnal im.P.A. Gertsena. 2012;1:28-32. Russian.
2. Poddubnaya IV. Ekstranodal’nye NKhL. Klinicheskaya gematologiya Pod red. M.A.Volkovoy. Moscow: Meditsina; 2001. Russian.
3. Aviles A, Nambo MJ, Neri N. The role of surgery in primary gastric lymphoma: results of a controlled clinical trial. Ann Surg. 2004;240:44-50.
4. Fischbach W, Goebeler-Kolve ME, Dragosics B. Long term outcome of patients with gastric marginal zone B cell lymphoma of mucosa associated lymphoid tissue (MALT) following exclusive Helicobacter pylori eradication: experience from a large prospective series. Gut. 2004;53:34-7.
5. Harris NL, Jaffe ES, Diebold Y. World Health Organization classifiacation of neoplastic diseases of the hematoetic and lymphoid tissues. Report of the Clinical Advisory Commettee Meeting – Asirlie House, Virginia, November 1997. J. Clin. Oncol. 1999;17:3835-49.
Report of the Clinical Advisory Commettee Meeting – Asirlie House, Virginia, November 1997. J. Clin. Oncol. 1999;17:3835-49.
6. Jager G, Neumeister P, Brezinschek R. Treatment of extranodal marginal zone B-cell lymphoma of mucosa-associated lymphoid tissue type with cladribine: a phase II study. J Clin Oncol. 2002;20(18):3872-7.
7. Jager G, Neumeister P, Quehenberger F. Prolonged clinical remission in patients with extranodal marginal zone B-cell lymphoma of the mucosa-associated lymphoid tissue type treated with cladribine: 6 year follow-up of a phase II trial. Ann Oncol. 2006;17(11):1722-3.
8. Koch P, del Valle F, Berdel WE. Primary gastrointestinal non-Hodgkin’s lymphoma: II. Combined surgical and conservative or conservative management only in localized gastric lymphoma-results of the prospective German Multicenter Study GIT NHL 01/92. J Clin Oncol. 2001;19:3874-83.
J Clin Oncol. 2001;19:3874-83.
9. Levy M, Copie-Bergman C, Cameiro C. Prognostic value of translocation t(11; 18) in tumoral response of low-grade gastric lymphoma of mucosa-associated lymphoid tissue type to oral chemotherapy. J Clin Oncol. 2005;23:5061-6.
10. Liu H, Ye H, Ruskone-Fourmestraux A. T(11;18) is a marker for all stage gastric MALT lymphomas that will not respond to H. pylori eradication. Gastroenterology. 2002; 122:1286-94.
11. Martinelli G, Laszlo D, Ferreri A. Clinical activity of rituximab in gastric marginal zone non-hodgkin’s lymphoma resistant to or not eligible for anti-helicobacter pylori therapy. J Clin Oncol. 2005;20(9):1979-83.
12. Raderer M, Jager G, Brugger S. Rituximab for treatment of advanced extranodal marginal zone B cell lymphoma of the mucosa-associated lymphoid tissue lymphoma. Oncology. 2003;65(4):306-10.
Oncology. 2003;65(4):306-10.
13. Ruskoner-Fourmestraux A, Lavergne A, Aegerter PH. Predictive factors for regression of gastric MALT lymphoma after anti- Helicobacter pylori treatment. Gut. 2001;48:297-303.
14. Sam S. Yoon, Daniel G. Colit, Carol S. Portlock. The diminishing role of surgery in the treatment of gastric lymphoma. Ann Surg. 2004;240:28-37.
15. Vrieling C, de Jong D, Boot H. Long-term results of stomach-conserving therapy in gastric MALT lymphoma. Radiother Oncol. 2008;87:405-11.
16. Wohrer S, Drach J, Hejna M. Treatment of extranodal marginal zone B-cell lymphoma of mucosa-associated lymphoid tissue (MALT lymphoma) with mitoxantrone, chlorambucil and prednisone (MCP). nn Oncol. 2003;14(12):1758-61.
17. Wohrer S, Puspok A, Drach J. Rituximab, cyclophosphamide, doxorubicin, vincristine and prednisone (R-CHOP) for treatment of early-stage gastric diffuse large B-cell lymphoma. Ann Oncol. 2004;1(15):1086-90.
Rituximab, cyclophosphamide, doxorubicin, vincristine and prednisone (R-CHOP) for treatment of early-stage gastric diffuse large B-cell lymphoma. Ann Oncol. 2004;1(15):1086-90.
18. Wundisch T, Dieckhoff P, Gunther A. 10-Year follow-up of 120 patients with gastric MALT lymphoma after Helicobacter pylori eradication – histological residual disease and second cancers. J Clin Oncol. 2008;34:2061-70.
19. Wundisch T, Thiede C, Morgner A. Long-term follow-up of gastric MALT lymphoma after Helicobacter pylori eradication. J Clin Oncol. 2005;23(31):1-7.
Библиографическая ссылка:
Голуб С.В., Солодкий В.А., Сотников В.М., Паньшин Г.А. Современные подходы к лечению первичных MALT-лимфом желудка // Вестник новых медицинских технологий. Электронное издание. 2015. №2. Публикация 2-6. URL: http://www. medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
medtsu.tula.ru/VNMT/Bulletin/E2015-2/5130.pdf (дата обращения: 21.04.2015). DOI: 10.12737/11201
Лимфома кишечника: что нужно знать
Лимфома, наиболее распространенный тип рака крови, обычно развивается в лимфатических узлах, которые являются важной частью иммунной системы и лимфатической системы. Развитие лимфомы связано с аномальным ростом и размножением белых кровяных телец, называемых лимфоцитами. Поскольку лимфатические узлы распространены по всему телу, болезнь может появиться где угодно, но чаще всего в области шеи, подмышек и живота. Лимфома также поражает кишечник.
Лимфома кишечника встречается очень редко. Лимфомы классифицируются как лимфома Ходжкина или неходжкинская лимфома в соответствии с ее характеристиками, но кишечная лимфома обычно неходжкинская лимфома, происходящая из В- или Т-клеток. Поскольку это редкий рак, оптимального лечения не существует. Пациенты обычно лечатся стандартными методами лечения лимфомы.
Развитие лимфомы кишечника, факторы риска
Согласно исследованию «Первичная лимфома желудочно-кишечного тракта», опубликованному в 2011 году, желудочно-кишечный тракт является наиболее частым экстранодальным участком развития заболевания.Желудочно-кишечная лимфома, как правило, неходжкинская, чаще всего она возникает в желудке, тонком кишечнике и илеоцекальной области. Обычно лимфома кишечника является вторичной, что означает, что она произошла от лимфомы, возникшей где-то еще.
Диффузная В-крупноклеточная лимфома является наиболее распространенным типом лимфомы кишечника.
На развитие болезни влияют несколько факторов риска.
Мужчины более склонны к развитию, чем женщины; средний возраст постановки диагноза – 60 лет.Курение и употребление алкоголя являются факторами риска, но другие заболевания способствуют развитию лимфомы кишечника, такие как целиакия, предыдущий рак толстой кишки, болезнь Крона, семейный аденоматозный полипоз, наследственный неполипозный колоректальный рак, синдром Пейтца-Егерса, MUTYH-ассоциированный полипоз и муковисцидоз (CF). .
.
Диета с высоким содержанием клетчатки может снизить риск.
Симптомы лимфомы кишечника, диагноз
Симптомы лимфомы кишечника включают боль и спазмы в животе, необъяснимую потерю веса, нарушение всасывания принятой пищи, ректальное кровотечение и тяжелые запоры или непроходимость кишечника.Кроме того, могут наблюдаться изменения настроения, включая раздражительность, тревожность и депрессию, а также усталость и бессонницу.
Ранняя и правильная диагностика иногда затруднена, поскольку симптомы не исключают лимфому кишечника и могут быть признаками других заболеваний.
При подозрении на лимфому кишечника врач начинает диагностику, выполняя полное физическое обследование и запрашивая медицинский и семейный анамнез. Биопсия, наиболее распространенное обследование, необходимое для диагностики лимфомы, используется для анализа ткани с целью определения типа, степени и стадии заболевания.Другие обследования, которые могут потребоваться, включают лабораторные анализы, анализы крови и визуализации.
Лечение и прогноз лимфомы кишечника
Многие факторы, такие как возраст, пол, история болезни или степень и стадия заболевания, влияют на выбор лечения. CHOP (циклофосфамид, гидроксидаунорубицин, онковин, преднизон) обычно является первым выбором химиотерапии, но иногда его используют после других терапий. Биологическая терапия Ритуксимаб часто используется отдельно или в качестве дополнения к другим методам лечения.
Хирургия может быть вариантом. Наиболее частая операция – сегментарная резекция кишечника или правосторонняя гемиколэктомия. Паллиативная хирургия используется в качестве альтернативного лечения для пациентов с запущенными заболеваниями и проблемами обструкции. Лучевая терапия может быть рекомендована в качестве дополнения к химиотерапии или отдельно.
Поскольку поставить диагноз непросто и лимфома кишечника может быть агрессивной, прогноз обычно не особенно положительный.
Примечание: Lymphoma News Today – это исключительно новостной и информационный сайт об этом заболевании. Он не предоставляет медицинских консультаций, диагностики или лечения. Этот контент не предназначен для замены профессиональных медицинских рекомендаций, диагностики или лечения. Всегда обращайтесь за советом к своему врачу или другому квалифицированному поставщику медицинских услуг по любым вопросам, которые могут у вас возникнуть относительно состояния здоровья. Никогда не игнорируйте профессиональные медицинские советы и не откладывайте их поиск из-за того, что вы прочитали на этом сайте.
Он не предоставляет медицинских консультаций, диагностики или лечения. Этот контент не предназначен для замены профессиональных медицинских рекомендаций, диагностики или лечения. Всегда обращайтесь за советом к своему врачу или другому квалифицированному поставщику медицинских услуг по любым вопросам, которые могут у вас возникнуть относительно состояния здоровья. Никогда не игнорируйте профессиональные медицинские советы и не откладывайте их поиск из-за того, что вы прочитали на этом сайте.
Лимфома Действие | MALT лимфома (желудочная и не желудочная)
Что такое лимфома MALT?
Лимфома – это тип рака крови, который развивается, когда лейкоциты, называемые лимфоцитами, бесконтрольно разрастаются.Лимфоциты являются частью вашей иммунной системы. Они путешествуют по вашему телу в лимфатической системе, помогая бороться с инфекциями. Есть два типа лимфоцитов: В-лимфоциты (В-клетки) и Т-лимфоциты (Т-клетки).
Лимфомы можно разделить на лимфомы Ходжкина и неходжкинские лимфомы в зависимости от типов клеток, которые они содержат. Лимфома MALT – это медленнорастущая (низкосортная) неходжкинская лимфома, которая развивается из В-клеток. Это тип лимфомы маргинальной зоны: лимфома, которая развивается в определенной области на краю лимфоидной ткани (скопления лимфоцитов), называемой маргинальной зоной.
Лимфома MALT – это медленнорастущая (низкосортная) неходжкинская лимфома, которая развивается из В-клеток. Это тип лимфомы маргинальной зоны: лимфома, которая развивается в определенной области на краю лимфоидной ткани (скопления лимфоцитов), называемой маргинальной зоной.
Существует три типа лимфомы краевой зоны:
Лимфома MALT является наиболее распространенным типом лимфомы маргинальной зоны, но все еще встречается редко. Только около 8 из 100 человек с диагнозом неходжкинская лимфома имеют MALT лимфому.
MALT Лимфома может развиться практически в любом месте тела, но чаще всего в желудке. MALT-лимфомы обычно делятся на:
- желудочная (желудочная) лимфома MALT, составляющая около трети всех лимфом MALT
- Нежелудочная лимфома MALT, которая чаще всего поражает слюнные железы, щитовидную железу, легкие, кожу, кишечник (кишечник) или ткани вокруг глаз.
Что такое лимфоидная ткань, связанная со слизистой оболочкой?
«Слизистая оболочка» – это мягкий, влажный, защитный слой клеток, выстилающий многие части вашего тела, такие как рот, кишечник, дыхательные пути и некоторые внутренние органы. «Лимфоидная ткань» означает совокупность лимфоцитов. Лимфоидная ткань, связанная со слизистой оболочкой (MALT) – это скопление лимфоцитов в слизистой оболочке. Сюда входят миндалины в задней части горла, а также лимфоидная ткань, которая может быть разбросана по всему телу, например по кишечнику, легким, коже, щитовидной железе и слюнным (слюнным) железам.
«Лимфоидная ткань» означает совокупность лимфоцитов. Лимфоидная ткань, связанная со слизистой оболочкой (MALT) – это скопление лимфоцитов в слизистой оболочке. Сюда входят миндалины в задней части горла, а также лимфоидная ткань, которая может быть разбросана по всему телу, например по кишечнику, легким, коже, щитовидной железе и слюнным (слюнным) железам.
MALT может образовываться как часть нормальной реакции вашего организма на воспаление. Это помогает защитить вас от инфекций. Однако лимфомы MALT могут развиться, если аномальные лимфоциты собираются в этой лимфоидной ткани.
Вернуться к началу
MALT лимфома может поражать людей любого возраста, но обычно она развивается у людей в возрасте от 60 лет.
MALT лимфома чаще встречается у людей, инфицированных определенными вирусами или имеющих определенные аутоиммунные заболевания.Ученые считают, что это происходит из-за длительного воспаления, которое может вызвать образование ткани MALT.
- Желудочная лимфома MALT тесно связана с инфекцией, вызываемой бактериями, называемыми Helicobacter pylori ( H.
 pylori ). Это очень распространенная инфекция, которая может вызвать язву желудка и расстройство желудка. Обычно это не вызывает серьезных проблем. Примерно 9 из каждых 10 человек с лимфомой желудка MALT имеют инфекцию H. pylori . Однако большинство людей, у которых есть H.pylori , а не , а не , приводят к развитию лимфомы желудка MALT.
pylori ). Это очень распространенная инфекция, которая может вызвать язву желудка и расстройство желудка. Обычно это не вызывает серьезных проблем. Примерно 9 из каждых 10 человек с лимфомой желудка MALT имеют инфекцию H. pylori . Однако большинство людей, у которых есть H.pylori , а не , а не , приводят к развитию лимфомы желудка MALT. - MALT-лимфома, поражающая слезные протоки и другие ткани вокруг глаза, может быть связана с инфекцией под названием Chlamydophila psittaci , которая распространяется птицами и может вызывать инфекции легких.
- MALT-лимфома кожи может быть связана с инфекцией Borrelia burgdorferi , которая распространяется клещами и вызывает болезнь Лайма.
- MALT-лимфома, поражающая тонкий кишечник, может быть связана с инфекцией Campylobacter jejuni , частой причиной пищевого отравления.
- MALT лимфома, поражающая легкие, может быть связана с инфекцией Achromobacter xylosoxidans , которая может вызывать инфекции крови или легких, обычно у людей с пониженной иммунной системой.

- MALT лимфома, поражающая слюнные (слюнные) железы, может быть связана с аутоиммунным заболеванием, называемым синдромом Шегрена.
- MALT лимфома, поражающая щитовидную железу, может быть связана с аутоиммунным заболеванием, называемым тиреоидитом Хашимото.
- Как и другие лимфомы маргинальной зоны, MALT-лимфома также чаще встречается у людей, инфицированных вирусом гепатита C.
Однако у подавляющего большинства людей с этими инфекциями или аутоиммунными заболеваниями не , а развиваются лимфомы.
Вернуться к началу
Симптомы лимфомы MALT зависят от того, где лимфома развивается. В отличие от многих других типов лимфомы, лимфома MALT развивается вне лимфатических узлов. Обычно это не вызывает увеличения лимфатических узлов. Люди с лимфомой MALT очень редко испытывают «B-симптомы» (сочетание необъяснимой потери веса, ночной потливости или лихорадки).
Симптомы MALT-лимфомы желудка
Желудочная лимфома MALT может вообще не вызывать никаких симптомов и может быть обнаружена во время тестов на что-то еще. Однако это может вызвать такие симптомы, как:
Однако это может вызвать такие симптомы, как:
- стойкое несварение желудка (часто это единственный симптом)
- Боль в животе
- плохое самочувствие (тошнота) или тошнота (рвота)
- потеря веса.
У некоторых людей есть симптомы анемии (например, усталость или одышка), вызванные кровотечением в желудке.
Симптомы не желудочной лимфомы MALT
У большинства людей с MALT-лимфомой, развивающейся вне желудка (не-желудочный MALT), нет никаких симптомов, и лимфому обнаруживают, когда у них есть тест, чтобы исследовать что-то еще.
У некоторых людей могут быть симптомы. Это зависит от того, где развивается лимфома.
- MALT лимфома, поражающая кишечник (кишечник), может затруднить усвоение достаточного количества пищи. У вас может быть диарея, вздутие живота или боль в животе.Вы можете почувствовать сильную усталость и похудеть, даже не пытаясь этого сделать.
- MALT лимфома, поражающая слезные протоки или ткани вокруг глаза, может вызывать такие симптомы, как покраснение глаза, темно-розовые шишки внутри века или в уголках глаза, двоение в глазах, опущенное веко или выпуклый глаз.
 Симптомы обычно развиваются с одной стороны, но примерно в 1 из 10 случаев они могут поражать оба глаза.
Симптомы обычно развиваются с одной стороны, но примерно в 1 из 10 случаев они могут поражать оба глаза. - MALT лимфома, поражающая легкие, часто не вызывает никаких симптомов, но может вызвать кашель, одышку, кровохарканье или боль в груди.
- MALT лимфома, поражающая слюнные железы, может вызвать образование шишки перед ухом, во рту или челюсти.
- MALT лимфома, поражающая вашу кожу, может вызывать появление розовых, красных или пурпурных пятен или шишек на коже, чаще всего на руках, груди или спине. Они могут развиваться в одном или нескольких местах и очень медленно растут.
- MALT Лимфома, поражающая вашу щитовидную железу, может вызвать образование шишки на передней части шеи, хриплый голос, одышку или затруднение глотания.У некоторых людей могут быть симптомы недостаточной активности щитовидной железы (например, постоянное чувство усталости, чувствительность к холоду и увеличение веса).
Могут быть затронуты другие части вашего тела.
До 1 из 2 человек с лимфомой MALT имеют лимфому в нескольких частях тела. Если это так, у вас может быть целый ряд симптомов.
Вернуться к началу
Лимфома MALT обычно диагностируется путем взятия образца ткани и его изучения под микроскопом.Это включает небольшую операцию, называемую биопсией, которая обычно проводится под местной анестезией. Образец биопсии исследует опытный патологоанатом. Патологоанатом также проверяет образец на наличие определенных белков, которые обнаруживаются на поверхности клеток лимфомы. Это может помочь вашей медицинской бригаде выбрать наиболее подходящее для вас лечение.
Тип биопсии, которая вам нужна, и способ ее проведения зависят от того, где у вас развилась лимфома. Например:
- Если аномальная ткань находится в желудке или кишечнике, биопсия, вероятно, будет сделана во время теста, называемого эндоскопией.Он использует тонкую гибкую трубку с крошечной камерой на конце, чтобы заглянуть внутрь вашего тела.
 Сначала вы можете принять успокаивающее (расслабляющее) лекарство. Чтобы посмотреть на свой желудок, через рот через глотку проводят трубку в желудок (гастроскопия). Чтобы посмотреть на кишечник, трубку вводят через задний проход в кишечник (колоноскопия). Через трубку можно продеть небольшие хирургические инструменты, чтобы врач мог взять образцы биопсии. Они могут брать образцы из нескольких разных мест в желудке или кишечнике.
Сначала вы можете принять успокаивающее (расслабляющее) лекарство. Чтобы посмотреть на свой желудок, через рот через глотку проводят трубку в желудок (гастроскопия). Чтобы посмотреть на кишечник, трубку вводят через задний проход в кишечник (колоноскопия). Через трубку можно продеть небольшие хирургические инструменты, чтобы врач мог взять образцы биопсии. Они могут брать образцы из нескольких разных мест в желудке или кишечнике. - Если аномальная ткань находится в ваших легких, вам может быть назначен вид эндоскопии, называемый бронхоскопией, при которой трубка вводится через нос или рот в дыхательные пути легких.
У вас также есть другие тесты, которые помогут вашей медицинской бригаде подобрать для вас наилучшее лечение.
Скорее всего, вам нужно будет сделать дыхательный тест, чтобы проверить наличие H. pylori в желудке. Вам дали капсулу или напиток, содержащий безвредное и безвкусное химическое вещество. Если у вас H.pylori , он расщепляет химическое вещество до двуокиси углерода. Примерно через 30 минут вам нужно подуть в трубку или пакет, который проверяет уровень углекислого газа в вашем дыхании. Возможно, вам также придется предоставить образец фекалий для проверки на инфекцию H. pylori .
Примерно через 30 минут вам нужно подуть в трубку или пакет, который проверяет уровень углекислого газа в вашем дыхании. Возможно, вам также придется предоставить образец фекалий для проверки на инфекцию H. pylori .
У вас также есть анализы крови, чтобы проверить на инфекцию H. pylori , посмотреть на свое общее состояние здоровья, проверить количество клеток крови, убедиться, что ваши почки и печень работают нормально, и проверить на инфекции, такие как вирус гепатита С.
У вас есть другие тесты, чтобы выяснить, какие участки вашего тела поражены лимфомой. Это называется постановкой. Обычно это включает компьютерную томографию. Вы также можете пройти ПЭТ-сканирование, если ваш специалист считает, что это будет полезно при планировании лечения, хотя это менее распространено для лимфом маргинальной зоны, чем для других типов лимфомы. У вас может быть взят образец клеток костного мозга (биопсия костного мозга), чтобы проверить, есть ли в костном мозге клетки лимфомы, хотя при MALT-лимфомах это бывает редко. Другие промежуточные тесты зависят от того, где растет лимфома. У вас может быть:
Другие промежуточные тесты зависят от того, где растет лимфома. У вас может быть:
- УЗИ для поиска лимфомы в слюнных железах, щитовидной железе или стенке желудка или кишечника
- МРТ, если у вас лимфома вокруг глаза
- рентген грудной клетки, если у вас лимфома, поражающая легкие.
Обычно вы сдаете анализы в амбулаторных условиях. На получение всех результатов уходит несколько недель. Ожидание результатов анализов может быть тревожным временем, но для вашего врача важно собрать всю эту информацию, чтобы спланировать для вас лучшее лечение.
MALT лимфомы растут медленно, поэтому у большинства людей диагностируется ранняя (стадия 1 или 2) лимфома.
Вернуться к началу
MALT лимфома развивается медленно, и лечение обычно бывает успешным. Хотя лимфома часто рецидивирует (возвращается), ее можно лечить снова, чтобы держать ее под контролем. Большинство людей живут с этим типом лимфомы много лет. У вас могут быть периоды, когда вы чувствуете себя хорошо и не нуждаетесь в лечении, и другие периоды, когда ваши симптомы ухудшаются, и вам нужно больше лечения.
Ваш врач лучше всего сможет посоветовать вам ваше мнение с учетом ваших индивидуальных обстоятельств.
Преобразование
Иногда лимфома MALT может трансформироваться (трансформироваться) в более быстрорастущий тип лимфомы. Это происходит менее чем у 1 из каждых 10 человек с лимфомой MALT.
Если ваш врач считает, что ваша лимфома могла трансформироваться, вам может потребоваться биопсия, чтобы проверить, нет ли быстрорастущих клеток лимфомы, или сканирование ПЭТ / КТ, чтобы увидеть, какие области вашего тела поражены.Трансформированная лимфома MALT лечится так же, как и быстрорастущая (высокозлокачественная) неходжкинская лимфома, такая как диффузная большая B-клеточная лимфома (DLBCL).
Вернуться к началу
Лечение лимфомы MALT зависит от того, где находится лимфома, какие у вас симптомы и есть ли у вас инфекция, связанная с лимфомой. Основные варианты лечения:
Хирургия применяется очень редко, если лимфома поражает только одну часть вашего тела и находится в области, где ее можно безопасно удалить.
Лечение инфекций, связанных с лимфомой MALT
Первым лечением лимфомы желудка MALT обычно является лечение инфекции H. pylori . Вам могут назначить это лечение, даже если ваши тесты не выявили доказательств инфекции H. pylori , потому что ее бывает трудно обнаружить.
Лечение H. pylori обычно включает 7-дневный курс антибиотиков и кислотоснижающих препаратов. Через 6-8 недель после лечения антибиотиками вам нужно сделать анализ дыхания, чтобы проверить, исчезла ли инфекция.Если инфекция не исчезла, вам может потребоваться еще один курс антибиотиков.
Лечение H. pylori Инфекция устраняет MALT-лимфому желудка у большинства людей, но реакция на лечение может занять от 6 до 12 месяцев. Вам нужно повторить эндоскопию, чтобы проверить, подействовала ли лимфома на лечение.
Если у вас все еще осталась лимфома после лечения антибиотиками H. pylori , вам может быть назначен активный мониторинг, лучевая терапия или химио-иммунотерапия, в зависимости от того, сколько лимфомы есть и как она влияет на вас.
Если у вас не-желудочная лимфома MALT и ваш врач считает, что ваша лимфома может быть связана с инфекцией, он может предложить антибиотики в качестве первого лечения. Однако большинству людей с MALT-лимфомой не желудка требуется лучевая терапия или химио-иммунотерапия.
Активный мониторинг
Если ваша лимфома не вызывает неприятных симптомов, вам может не потребоваться немедленное лечение (кроме антибиотиков, если это связано с инфекцией). Вместо этого ваш врач может предложить внимательно наблюдать за вами, включая регулярные эндоскопии, если у вас желудочный СОЛТ, и экономить лечение до тех пор, пока оно не понадобится.Это называется активным мониторингом или «смотри и жди». Такой подход позволяет как можно дольше избежать побочных эффектов лечения. Отсрочка лечения таким образом не влияет на то, насколько хорошо оно работает, когда оно вам действительно нужно, или на то, как долго вы можете жить.
Радиотерапия
Если ваша лимфома вызывает симптомы и не связана с инфекцией, или лечение инфекции не устраняет ее, вам может быть назначена лучевая терапия. Лучевая терапия может быть очень эффективной, если лимфома поражает только несколько участков вашего тела.Однако вместо этого вам может потребоваться химио-иммунотерапия, если:
Лучевая терапия может быть очень эффективной, если лимфома поражает только несколько участков вашего тела.Однако вместо этого вам может потребоваться химио-иммунотерапия, если:
- Ваша лимфома более распространена
- ваша лимфома находится рядом с важными органами, которые могут быть повреждены радиотерапией
- Ваш врач считает, что у вас высокий риск того, что лимфома может ухудшиться или вернуться на противоположную сторону тела.
Химио-иммунотерапия
Большинство людей с лимфомой MALT, которая не связана с инфекцией или не проходит после лечения инфекции, получают терапию антителами (такими как ритуксимаб) в сочетании с химиотерапией.Иногда это называют «химио-иммунотерапией».
MALT лимфома встречается редко. Это затрудняет точное определение того, какое лечение дает лучший результат. Комбинации химио-иммунотерапевтических препаратов, которые могут быть использованы для лечения лимфомы MALT, включают:
- ритуксимаб плюс бендамустин
- ритуксимаб плюс хлорамбуцил
- Ритуксимаб плюс ЦВД (R-CVP)
- ритуксимаб плюс CHOP (R-CHOP)
- Ритуксимаб плюс флударабин (в настоящее время используется редко).

Однако ваш врач может порекомендовать другой режим (комбинацию лекарств) или спросить вас, хотите ли вы принять участие в клиническом исследовании.
Побочные эффекты лечения
Лечение по-разному влияет на людей. Каждый тип лечения или лекарства имеет свой набор возможных побочных эффектов. Ваша медицинская бригада должна предоставить вам информацию о побочных эффектах, связанных с любым лечением, которое они вам рекомендуют. Если вас беспокоят возможные побочные эффекты, запросите дополнительную информацию.Ваша медицинская бригада может посоветовать или выписать лекарства, если вы испытываете неприятные побочные эффекты во время лечения лимфомы.
Вернуться к началу
Когда вы находитесь в стадии ремиссии (отсутствие признаков лимфомы) после лечения или в течение периода активного наблюдения («смотри и жди»), вам необходимо регулярно посещать клинику для последующего наблюдения.
Ваши последующие встречи должны проверить, что:
- Вы поправляетесь после лечения
- у вас нет признаков рецидива лимфомы или ее ухудшения
- у вас не развиваются какие-либо поздние эффекты (побочные эффекты, которые развиваются через месяцы или годы после лечения).

На каждом приеме ваш врач осматривает вас и спрашивает, есть ли у вас какие-либо проблемы или симптомы. У вас могут быть анализы крови. Если у вас была лимфома желудка MALT, вам могут проходить эндоскопию каждые 3-6 месяцев в течение первых 2 лет после лечения. У вас могут быть другие тесты в зависимости от того, где у вас возникла лимфома.
Вам вряд ли удастся пройти сканирование, если у вас нет тревожных симптомов.
Вернуться к началу
MALT лимфома часто возвращается (рецидивирует) после успешного лечения, часто через несколько лет.Если лимфома MALT возвращается, она часто поражает тот же орган, что и раньше, но может вернуться в других местах. Если у вас была MALT лимфома, поражающая один глаз, слюнную железу или легкое или на одной стороне вашей щитовидной железы, она может вернуться на противоположную сторону.
Обычно вы можете пройти дополнительное лечение, чтобы дать еще один период ремиссии. Такой подход часто позволяет контролировать лимфому в течение многих лет. Лечение рецидивирующей или рефрактерной лимфомы MALT зависит от того, где находится лимфома, какое лечение вы уже прошли и как долго вы на него реагировали.
Лечение рецидивирующей или рефрактерной лимфомы MALT зависит от того, где находится лимфома, какое лечение вы уже прошли и как долго вы на него реагировали.
Если у вас MALT-лимфома желудка и инфекция H. pylori вернулась, лечение на основе антибиотиков обычно устраняет как инфекцию, так и лимфому.
Если у вас не желудочная лимфома MALT или желудочная лимфома MALT без инфекции H. pylori , вам, вероятно, потребуется другое лечение.
Несколько таргетных препаратов проходят клинические испытания. Ваш врач может спросить вас, не хотите ли вы принять участие в клиническом испытании, чтобы помочь протестировать новые методы лечения и выяснить, какое лечение лучше всего подходит для MALT-лимфомы, которая вернулась или не подействовала на предыдущее лечение (рефрактерная лимфома).
Если вы не хотите принимать участие в клиническом испытании или если для вас нет подходящего, вам, скорее всего, будет назначена лучевая терапия или ритуксимаб в сочетании с химиотерапией.
Очень редко ваша медицинская бригада может порекомендовать вам пересадку стволовых клеток с использованием ваших собственных стволовых клеток («аутологичная» трансплантация стволовых клеток). Трансплантация стволовых клеток обычно рассматривается только при лимфоме MALT, если она рецидивирует очень скоро после предыдущего лечения.Трансплантация стволовых клеток – это очень интенсивный метод лечения, и вы должны быть достаточно здоровы, чтобы получить его. Пересадка стволовых клеток позволяет получить очень высокие дозы химиотерапии. Это может дать вам больше шансов на длительную ремиссию (без признаков лимфомы), чем стандартные схемы химиотерапии.
Вернуться к началу
MALT-лимфома встречается редко, поэтому в большинство клинических испытаний также включаются люди с другими типами лимфомы низкой степени злокачественности, включая другие лимфомы маргинальной зоны.
В клинических испытаниях проходят испытания несколько целевых методов лечения лимфом маргинальной зоны, включая препараты, уже одобренные для лечения других типов лимфомы. К ним относятся:
К ним относятся:
- Ингибиторы BTK, такие как ибрутиниб, акалабрутиниб и занубрутиниб, которые блокируют сигналы, посылаемые В-клетками, чтобы помочь им выжить и делиться
- Ингибиторы PI3K, такие как иделалисиб, умбралисиб и копанлисиб, которые блокируют белок, участвующий в росте и выживании клеток лимфомы
- иммуномодуляторы, такие как леналидомид, которые изменяют работу вашей иммунной системы
- ингибиторы протеасом, такие как бортезомиб, которые нарушают баланс белков в клетках лимфомы, вмешиваясь в химические сигналы между клетками лимфомы и приводя к гибели клеток
- новых препаратов для лечения антител, таких как обинутузумаб, ублитуксимаб или варлилумаб, которые связываются с белками на поверхности клеток лимфомы, чтобы помочь вашей собственной иммунной системе разрушить их.
Некоторые из них могут быть доступны вам в ходе клинических испытаний. Если вы заинтересованы в участии в клиническом испытании, спросите своего врача, может ли оно вам подойти. Чтобы узнать больше о клинических испытаниях или найти подходящее для вас испытание, посетите Lymphoma TrialsLink.
Чтобы узнать больше о клинических испытаниях или найти подходящее для вас испытание, посетите Lymphoma TrialsLink.
Вернуться к началу
Лимфома желудочно-кишечного тракта: новая мимика
Клинические признаки по анатомическому расположению
Лимфома пищевода
Первичная лимфома пищевода встречается очень редко и составляет менее 1% всех первичных лимфом желудочно-кишечного тракта.Поражение пищевода обычно вторично по отношению к шейным или средостенным лимфатическим узлам.19 Клинически пациенты могут проявлять дисфагию, потерю веса, диспепсию или кровотечение из верхних отделов ЖКТ. Эндоскопически эти опухоли могут иметь узелковый, полиповидный, изъязвленный или стенозирующий вид. Эндоскопическое ультразвуковое исследование может использоваться для оценки глубины инвазии опухоли.20
Лимфома желудка
Желудок является наиболее часто пораженным участком желудочно-кишечного тракта среди лимфом желудочно-кишечного тракта. Лимфома MALT является наиболее распространенным подтипом, за которым следует DLBL.21 У небольшой части пациентов с инфекцией H. pylori может развиться MALT-лимфома. Бактериальная инфекция может запускать активацию Т-лимфоцитов CD4 и косвенно стимулировать В-клетки и тем самым приводить к развитию злокачественного новообразования.22 Кроме того, было отмечено, что люди с транслокацией t (11; 18) (q21; q21) по-видимому, имеют более высокую предрасположенность к развитию лимфомы MALT.23 Клинически эти пациенты могут сообщать о боли в животе, тошноте, рвоте или кровотечениях из верхних отделов ЖКТ.21 24 Эндоскопический вид лимфомы MALT варьируется от экзофитной язвенной массы до гипертрофических и увеличенных складок желудка или гиперемических изменений слизистой оболочки желудка, 24 25, как показано в случае 9.
Лимфома MALT является наиболее распространенным подтипом, за которым следует DLBL.21 У небольшой части пациентов с инфекцией H. pylori может развиться MALT-лимфома. Бактериальная инфекция может запускать активацию Т-лимфоцитов CD4 и косвенно стимулировать В-клетки и тем самым приводить к развитию злокачественного новообразования.22 Кроме того, было отмечено, что люди с транслокацией t (11; 18) (q21; q21) по-видимому, имеют более высокую предрасположенность к развитию лимфомы MALT.23 Клинически эти пациенты могут сообщать о боли в животе, тошноте, рвоте или кровотечениях из верхних отделов ЖКТ.21 24 Эндоскопический вид лимфомы MALT варьируется от экзофитной язвенной массы до гипертрофических и увеличенных складок желудка или гиперемических изменений слизистой оболочки желудка, 24 25, как показано в случае 9.
Хотя и реже, чем лимфома MALT, DLBL желудка также встречается было обнаружено, что они связаны с инфекцией H. pylori и экспрессируют CD19, CD20, CD22 и CD79. 26 27 Они могут проявляться симптомами, сходными с лимфомой MALT. Эндоскопически они часто локализуются в теле / дне желудка и могут проявляться в виде изъязвленного поражения, полиповидной массы или диффузного / очагового утолщения стенки желудка (случаи 5, 6, 8) 26
26 27 Они могут проявляться симптомами, сходными с лимфомой MALT. Эндоскопически они часто локализуются в теле / дне желудка и могут проявляться в виде изъязвленного поражения, полиповидной массы или диффузного / очагового утолщения стенки желудка (случаи 5, 6, 8) 26
Кишечная лимфома
Тонкая кишка и толстая кишка являются вторыми наиболее часто поражаемыми участками, причем наиболее часто поражается подвздошная кишка.Различные подтипы лимфомы, обнаруживаемые в кишечнике, включают MALT, DLBL, лимфому из мантийных клеток (MCL), фолликулярную лимфому (FL) и T-клеточную лимфому кишечника. 14-18 28 29 Пациенты могут иметь лихорадку, боль в животе, диарею, кровоизлияние и вес потеря (случаи 1, 3, 4). КТ брюшной полости может выявить утолщение стенки кишечника, непроходимость или изъязвление слизистой оболочки.14–18 28–30 Капсульная эндоскопия и колоноскопия используются для обнаружения этих опухолей, которые могут проявляться в виде изъязвленных поражений или диффузного утолщения слизистой оболочки с грубым или мелкозернистым внешним видом. 31 Последнее особенно полезно из-за предрасположенности лимфомы к дистальному отделу подвздошной кишки и подвздошной кишке. 31
31 Последнее особенно полезно из-за предрасположенности лимфомы к дистальному отделу подвздошной кишки и подвздошной кишке. 31
Лимфома желчного пузыря, желчного дерева, поджелудочной железы и печени
В то время как наше внимание было сосредоточено на лимфоме пищевода, желудка, малых кишечник и толстая кишка, мы должны отметить, что другие компоненты пищеварительной системы также могут вызывать первичные лимфомы. Первичная лимфома желчного пузыря, чаще всего лимфома MALT или DLBL, встречается очень редко и обычно проявляется болью в правом верхнем квадранте.32–35 MALT лимфомы, возникающие в желчных протоках в воротах ворот, также описаны как крайне редкие случаи B-клеточной лимфомы, фолликулярной лимфомы и лимфобластной лимфомы. Клинически холангиокарцинома, первичный склерозирующий холангит или панкреатит является первоначальным диагнозом, при котором истинная природа патологии выявляется во время операции35. 36 Первичные лимфомы поджелудочной железы составляют менее 0,5% всех злокачественных новообразований поджелудочной железы и обычно представляют собой диффузные В-клетки по морфологии и морфологии. чаще всего проявляется в виде образования в головке поджелудочной железы.37 В то время как вторичное поражение печени лимфомой является обычным явлением, первичные лимфомы печени составляют 0,016% всех случаев НХЛ. Боль в правом подреберье, лихорадка и потеря веса являются обычными симптомами, а гепатомегалия, а не желтуха, являются основными физическими признаками. Опять же доминирует морфология В-клеток.38
чаще всего проявляется в виде образования в головке поджелудочной железы.37 В то время как вторичное поражение печени лимфомой является обычным явлением, первичные лимфомы печени составляют 0,016% всех случаев НХЛ. Боль в правом подреберье, лихорадка и потеря веса являются обычными симптомами, а гепатомегалия, а не желтуха, являются основными физическими признаками. Опять же доминирует морфология В-клеток.38
Ведение
При лечении лимфом ЖКТ используются различные стратегии и методы лечения в зависимости от области поражения, гистологического типа и клинической стадии.12 39 40 Например, ранняя стадия фолликулярной лимфомы протекает вялотекущим течением и может сопровождаться клинической политикой “ смотри и жди ”. 41 Действительно, ретроспективное исследование Янга и его коллег отметило схожий общий уровень выживаемости в 7,5 лет среди тех, кто с фолликулярной лимфомой, которые подверглись выжидательной или агрессивной комбинированной терапии.42
Более 70% пациентов с ранней стадией (стадии классификации по Анн-Арбор, I – II I ) лимфомами MALT, ассоциированными с H. pylori может достичь ремиссии только с помощью трех- или четырехкратной эрадикационной терапии, 4 43 44 с локализацией опухоли, этнической принадлежностью пациента, глубиной инвазии и молекулярными особенностями, влияющими на частоту ответа.24 Лучевая терапия и химиотерапия предназначены для пациентов с запущенными опухолями и пациентов, не ответивших . Хирургическое вмешательство должно оказаться необходимым только в случаях перфорации или когда кровотечение невозможно контролировать эндоскопически.45 Что касается последующего наблюдения, рекомендуется проводить эндоскопию с тщательным осмотром и биопсией ранее пораженного участка каждые шесть месяцев в течение первых шести месяцев. месяцев, а затем ежегодно.45 Для отличных от H . pylori -ассоциированные MALT-лимфомы, в настоящее время отсутствует консенсус относительно оптимального начального терапевтического режима с использованием как лучевой терапии, так и химиотерапии.46
pylori может достичь ремиссии только с помощью трех- или четырехкратной эрадикационной терапии, 4 43 44 с локализацией опухоли, этнической принадлежностью пациента, глубиной инвазии и молекулярными особенностями, влияющими на частоту ответа.24 Лучевая терапия и химиотерапия предназначены для пациентов с запущенными опухолями и пациентов, не ответивших . Хирургическое вмешательство должно оказаться необходимым только в случаях перфорации или когда кровотечение невозможно контролировать эндоскопически.45 Что касается последующего наблюдения, рекомендуется проводить эндоскопию с тщательным осмотром и биопсией ранее пораженного участка каждые шесть месяцев в течение первых шести месяцев. месяцев, а затем ежегодно.45 Для отличных от H . pylori -ассоциированные MALT-лимфомы, в настоящее время отсутствует консенсус относительно оптимального начального терапевтического режима с использованием как лучевой терапии, так и химиотерапии.46
Для DLBL желудка и кишечника консенсус заключается в том, что химиотерапия, включающая ритуксимаб-циклофосфамид- Онковин-преднизолон должен быть стандартным режимом. 45 47–49 Здесь снова хирургическое вмешательство ограничивается лечением таких осложнений, как перфорация и кровотечение.45 В прошлом хирургическая резекция широко применялась при лечении пациентов с лимфомой желудочно-кишечного тракта50; большая точность предоперационной диагностики должна свести к минимуму необходимость хирургического вмешательства в настоящее время, даже в случаях кишечной непроходимости, как показано в нашем случае 1, когда химиотерапия вызвала полное исчезновение препятствующей опухоли.
45 47–49 Здесь снова хирургическое вмешательство ограничивается лечением таких осложнений, как перфорация и кровотечение.45 В прошлом хирургическая резекция широко применялась при лечении пациентов с лимфомой желудочно-кишечного тракта50; большая точность предоперационной диагностики должна свести к минимуму необходимость хирургического вмешательства в настоящее время, даже в случаях кишечной непроходимости, как показано в нашем случае 1, когда химиотерапия вызвала полное исчезновение препятствующей опухоли.
Прогноз для кишечных Т-клеточных лимфом в целом и для EATL типа I (т.е. связанного с глютеновой болезнью) и мономорфной эпителиотропной кишечной Т-клеточной лимфомы (ранее называвшейся EATL типа II), в частности, следующий. плохие и стратегии лечения этих и других редких форм лимфомы желудочно-кишечного тракта различаются в зависимости от проявления, местоположения, стадии и гистологического типа и могут включать химиотерапию, лучевую терапию, иммунотерапию, хирургическое вмешательство и трансплантацию аутологичных стволовых клеток. 51–53 В одном исследовании, которое включало различные периферические Т-клеточные лимфомы, частота ответа на циклофосфамид-онковин-преднизолон при среднем последующем наблюдении в течение 27 месяцев составила 62% 54. известно о перфорации кишечника. В одной серии из 1062 пациентов с гистологически подтвержденной лимфомой желудочно-кишечного тракта у 9% развилась перфорация, причем чуть более половины из них возникла после начала химиотерапии. Среднее время до перфорации после начала химиотерапии составляло 46 дней, чаще всего поражалась тонкая кишка; агрессивная гистология B-клеток была важным фактором риска.55
51–53 В одном исследовании, которое включало различные периферические Т-клеточные лимфомы, частота ответа на циклофосфамид-онковин-преднизолон при среднем последующем наблюдении в течение 27 месяцев составила 62% 54. известно о перфорации кишечника. В одной серии из 1062 пациентов с гистологически подтвержденной лимфомой желудочно-кишечного тракта у 9% развилась перфорация, причем чуть более половины из них возникла после начала химиотерапии. Среднее время до перфорации после начала химиотерапии составляло 46 дней, чаще всего поражалась тонкая кишка; агрессивная гистология B-клеток была важным фактором риска.55
За исключением описанной выше стратегии наблюдения за пациентами с H . pylori -ассоциированная Т-клеточная лимфома не существует руководств по эндоскопическому наблюдению за пациентами после успешного лечения других лимфом желудка, тонкой кишки или толстой кишки. Роль эндоскопического ультразвука в последующем наблюдении за лимфомой желудка еще не определена.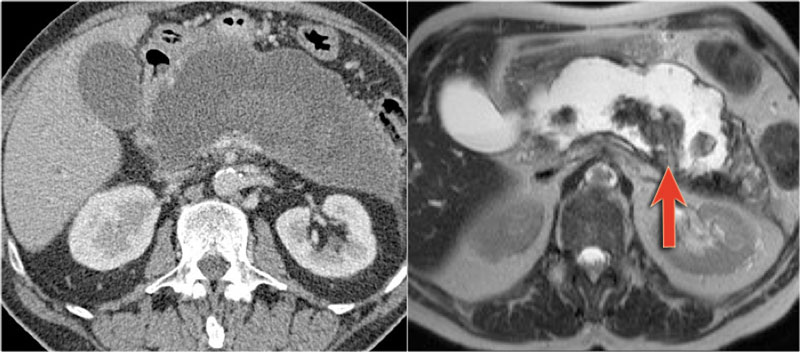 56 Также нет руководящих принципов для наблюдения за людьми из группы риска, например, с расстройствами, связанными с повышенным риском лимфомы, такими как целиакия57 или узловые лимфоидная гиперплазия.58 59
56 Также нет руководящих принципов для наблюдения за людьми из группы риска, например, с расстройствами, связанными с повышенным риском лимфомы, такими как целиакия57 или узловые лимфоидная гиперплазия.58 59
MALT Причины и методы лечения лимфомы
Лимфома – это рак лейкоцитов. Лимфома MALT – необычная форма неходжкинской лимфомы (НХЛ). MALT означает «лимфоидная ткань, связанная со слизистой оболочкой». В отличие от большинства лимфом, которые начинают расти в лимфатических узлах, этот тип лимфомы обычно возникает из ткани, которая присутствует в слизистой оболочке некоторых других органов тела.
Imtmphoto / iStock Существуют разные типы лимфоцитов, и у человека может развиться лимфома любого из этих типов.Например, есть В-лимфоциты и Т-лимфоциты, и, таким образом, есть В-клеточные лимфомы и Т-клеточные лимфомы. MALT-лимфома также известна как «экстранодальная B-клеточная лимфома маргинальной зоны», что означает, что это тип неходжкинской B-клеточной лимфомы, которая возникает не из лимфатических узлов, а из других органов.
Распространенность
MALT-лимфомы составляют лишь около 6% всех неходжкинских лимфом. Они чаще встречаются у пожилых людей, но могут встречаться и у людей в возрасте от двадцати до тридцати лет.У женщин они встречаются немного чаще, чем у мужчин.
Пораженные органы
Наиболее часто поражаемый орган при лимфоме MALT – желудок, на который приходится около половины всех случаев. Когда в желудке развивается MALT-лимфома, ее также можно назвать «желудочной MALT-лимфомой». Но другие органы также поражаются MALT лимфомой. Эта лимфома также может поражать легкие, щитовидную железу, слюнные железы и глаза.
Причины
MALT-лимфомы желудка связаны с бактериальной инфекцией.Helicobacter pylori – это тип бактерий, которые обычно поражают желудок и вызывают язвы и гастрит или раздражение и воспаление слизистой оболочки желудка. У некоторых людей эта бактерия также может вызывать лимфомы MALT. Лимфома желудка MALT не уникальна в том смысле, что другие типы лимфомы связаны с инфекциями, вызываемыми определенными бактериями, вирусами и паразитами. Это имеет смысл, когда вы думаете о лимфатической системе, в том числе о ее лимфоцитах, как о части иммунной системы, которая работает для выявления и борьбы с чужеродными организмами в нашем организме.Факторы риска лимфомы MALT также включают инфекцию Chlamydophilia psittaci и аутоиммунные заболевания.
Это имеет смысл, когда вы думаете о лимфатической системе, в том числе о ее лимфоцитах, как о части иммунной системы, которая работает для выявления и борьбы с чужеродными организмами в нашем организме.Факторы риска лимфомы MALT также включают инфекцию Chlamydophilia psittaci и аутоиммунные заболевания.
Поведение
Лимфомы MALT – это лимфомы низкой степени злокачественности. Они растут медленно и относительно долгое время остаются в пределах одного органа. Говоря о медленно растущих лимфомах, онкологи часто используют термин «вялотекущие». У большинства пациентов с MALT-лимфомой диагноз ставится раньше, чем болезнь распространилась на другие органы и лимфатические узлы.
Симптомы
Симптомы лимфомы MALT зависят от пораженного органа.Когда лимфома MALT поражает желудок, вы можете почувствовать несварение желудка или потерять вес; черный стул также возможен из-за кровотечения в желудке. Некоторые люди могут ощущать нечеткую боль в животе.
Диагностика
Чтобы диагностировать лимфому MALT, врачу необходимо взять биопсию опухоли.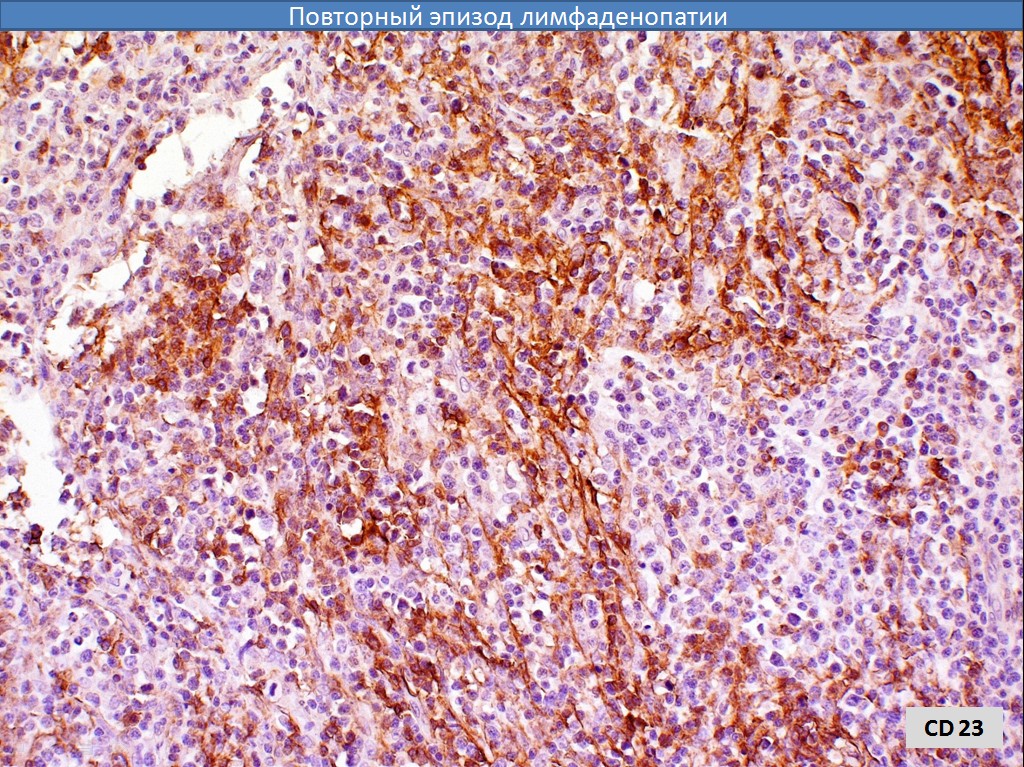 При MALT-лимфомах желудка обычно проводится эндоскопия. Врачи также проверит наличие в желудке бактерий H. pylori.Другие тесты, которые необходимо будет выполнить, включают анализы крови, сканирование брюшной полости и груди, а также анализ костного мозга.
При MALT-лимфомах желудка обычно проводится эндоскопия. Врачи также проверит наличие в желудке бактерий H. pylori.Другие тесты, которые необходимо будет выполнить, включают анализы крови, сканирование брюшной полости и груди, а также анализ костного мозга.
Стадия
Стадия лимфомы включает 3 отдельных оценки. MALT-лимфомы сначала классифицируются на разные стадии, от стадии I до стадии IV, в зависимости от того, насколько они обширны. Затем дается буква A или B в зависимости от симптомов. Также есть еще 2 буквы, E и S, в которых E означает «экстралимфатический» или вне лимфатической системы, а S означает наличие рака в селезенке.MALT-лимфомы не возникают в лимфатических узлах и обычно не распространяются на другие органы. Большинство лимфом MALT диагностируется на стадии IE, что означает, что они присутствуют только в одном органе и находятся за пределами лимфатической системы. Только около 10% лимфом MALT находятся на поздней стадии диагноза.
Процедуры
Лечение лимфомы MALT зависит от пораженного органа и стадии диагностики. У большинства пациентов местные методы лечения, такие как лучевая терапия или хирургическое вмешательство, могут быть адекватными для борьбы с заболеванием, но системная терапия, такая как химиотерапия, часто используется для лечения рака на более высоких стадиях и может использоваться для снижения риска рецидива на ранних стадиях рака.
У большинства пациентов местные методы лечения, такие как лучевая терапия или хирургическое вмешательство, могут быть адекватными для борьбы с заболеванием, но системная терапия, такая как химиотерапия, часто используется для лечения рака на более высоких стадиях и может использоваться для снижения риска рецидива на ранних стадиях рака.
Лечение MALT-лимфомы желудка заключается в искоренении инфекции, вызванной H. pylori. Одного этого достаточно для устранения рака у большого процента людей.
Слово Verywell
Использование химиотерапии при лимфомах MALT не изучалось в той же степени, что и при других лимфомах. В прошлом было принято использовать тот вид химиотерапии, который применялся при неходжкинской лимфоме низкой степени злокачественности. В случаях, когда схемы приема антибиотиков неэффективны, существует значительный консенсус в отношении того, что следует использовать химиотерапию, но меньше согласия относительно оптимальной схемы лечения.
журналов поджелудочной железы | Список проиндексированных статей
JOP – это рецензируемый журнал с открытым доступом, который дважды в месяц публикует рукописи по соответствующим темам, включая этиологию, эпидемиологию, профилактику, генетику, патофизиологию, диагностику, хирургическое и медицинское лечение заболеваний поджелудочной железы, включая рак, воспалительные заболевания, сахарный диабет, клиническую практику. панкреатология, внутренние болезни, клинические исследования, желудочно-кишечная хирургия, эндокринология, гепатология, лечение острого панкреатита, диабета, протоковой аденокарциномы поджелудочной железы и ее лечения, хронического панкреатита, нейроэндокринной опухоли, муковисцидоза и других врожденных заболеваний.
панкреатология, внутренние болезни, клинические исследования, желудочно-кишечная хирургия, эндокринология, гепатология, лечение острого панкреатита, диабета, протоковой аденокарциномы поджелудочной железы и ее лечения, хронического панкреатита, нейроэндокринной опухоли, муковисцидоза и других врожденных заболеваний.
Представленные материалы включают оригинальные исследования, тематические исследования, инновации в разработке программ, научные обзоры, теоретический дискурс и обзоры книг. Кроме того, Журнал поощряет представление ответственных предположений и комментариев. JOP. Journal of the Pancreas предоставляет актуальные обзоры и обновления, относящиеся к аномалиям поджелудочной железы и терапии, а также текущие аннотированные обзоры исследований, опубликованные в других местах, что делает журнал уникальным и ценным справочным ресурсом. Редакционная коллегия состоит из международных корифеев, которым поручено предоставлять читателям новейшую информацию, которая будет иметь большое значение для всех, кто работает в области исследований поджелудочной железы.
The JOP. Journal of Pancreas следует процессу простого слепого рецензирования для проверки качества и ценности каждой полученной рукописи. Рецензирование осуществляется под эгидой членов редакционной коллегии журнала. После первичной проверки качества каждая статья рецензируется сторонними экспертами под руководством назначенного редактора. Утверждение по крайней мере двух независимых рецензентов с последующим одобрением редактора является обязательным для принятия любой заявки.
Цитирование
Журнал индексируется: EBSCO, CNKI, ICMJE, THOMSON REUTERS ESCI (EMERGING SOURCES CITATION INDEX), COSMOS, BRITISH LIBRARY и University of Zurich – UZH
Связано с
Сеть сторонников панкреатита
Греческое общество печени, поджелудочной железы и желчевыводящих путей
Белорусский панкреатический клуб
Заявление об открытом доступе
Это журнал с открытым доступом, который позволяет бесплатно получить весь контент для отдельного пользователя или любого учреждения. Пользователям разрешается читать, скачивать, копировать, распространять, распечатывать, искать или ссылаться на полные тексты статей или использовать их для любых других законных целей без предварительного разрешения издателя или автора при условии, что автор предоставлен при необходимости кредит. Это соответствует определению открытого доступа BOAI.
Пользователям разрешается читать, скачивать, копировать, распространять, распечатывать, искать или ссылаться на полные тексты статей или использовать их для любых других законных целей без предварительного разрешения издателя или автора при условии, что автор предоставлен при необходимости кредит. Это соответствует определению открытого доступа BOAI.
Поджелудочная железа
Поджелудочная железа – это длинная плоская железа, расположенная в брюшной полости за желудком. Он производит несколько важных ферментов, которые попадают в тонкий кишечник и помогают пищеварению.Поджелудочная железа также содержит кластеры клеток, называемые островками. Клетки этих островков вырабатывают гормоны, такие как инсулин и глюкагон, которые помогают контролировать уровень глюкозы (типа сахара) в крови.
Связанные журналы поджелудочной железы
Поджелудочная железа, панкреатология, Журнал гепато-билиарно-панкреатических наук, гепатобилиарные и панкреатические заболевания International
Панкреатит
Панкреатит – это воспаление поджелудочной железы. Поджелудочная железа – это длинный ровный орган, который находится за животом в верхней части живота.Поджелудочная железа вырабатывает ферменты, которые помогают пищеварению, и гормоны, которые помогают управлять процессом обработки сахара (глюкозы) в организме. Поджелудочная железа может протекать как острый панкреатит, так и хронический панкреатит.
Поджелудочная железа – это длинный ровный орган, который находится за животом в верхней части живота.Поджелудочная железа вырабатывает ферменты, которые помогают пищеварению, и гормоны, которые помогают управлять процессом обработки сахара (глюкозы) в организме. Поджелудочная железа может протекать как острый панкреатит, так и хронический панкреатит.
Связанные журналы панкреатита
Панкреатология, Медицинский журнал Новой Англии, Журнал гепато-билиарно-панкреатических наук, Международная организация по гепатобилиарным и панкреатическим заболеваниям
Функция поджелудочной железы
Поджелудочная железа на самом деле представляет собой две железы, которые тесно перемешаны в один орган.Первый функциональный компонент – «экзокринный», а второй функциональный компонент – «эндокринный». Экзокринные »клетки, вырабатывающие ферменты, помогающие переваривать пищу, а эндокринная поджелудочная железа состоит из небольших островков клеток, называемых островками Лангерганса.
Журналы, связанные с функцией поджелудочной железы
Поджелудочная железа, заболевания поджелудочной железы и терапия, панкреатология, гепатобилиарные заболевания и заболевания поджелудочной железы International
Острый панкреатит
Острый панкреатит – это внезапное кратковременное воспаление поджелудочной железы.Другой термин, используемый для обозначения острого панкреатита, – это острый некроз поджелудочной железы. Несмотря на высокий уровень лечения, это может привести к серьезным осложнениям или даже смерти. В тяжелых случаях острый панкреатит приводит к кровотечению в железе, серьезному повреждению тканей, инфекции и образованию кисты. Он также может нанести вред другим жизненно важным органам, таким как сердце, легкие и почки. Острый панкреатит диагностируется клинически, но иногда требуется компьютерная томография, общий анализ крови, функциональные тесты почек, визуализация и т. Д.
Связанные журналы острого панкреатита
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, Американский журнал хирургии, панкреатологии, болезней органов пищеварения и печени
Хронический панкреатит
Хронический панкреатит – это необратимое воспаление поджелудочной железы, которое не заживает и не улучшается, а изменяет нормальную структуру и функции органа. Обычно это наблюдается после эпизода острого панкреатита. Еще одна серьезная причина – употребление алкоголя в больших количествах. Хронический панкреатит может проявляться как эпизоды тяжелого воспаления в поврежденной поджелудочной железе или как хроническое поражение с постоянной болью или нарушением всасывания. Диабет – частое осложнение, возникающее из-за хронического поражения поджелудочной железы, и требует лечения инсулином.
Обычно это наблюдается после эпизода острого панкреатита. Еще одна серьезная причина – употребление алкоголя в больших количествах. Хронический панкреатит может проявляться как эпизоды тяжелого воспаления в поврежденной поджелудочной железе или как хроническое поражение с постоянной болью или нарушением всасывания. Диабет – частое осложнение, возникающее из-за хронического поражения поджелудочной железы, и требует лечения инсулином.
Связанные журналы хронического панкреатита
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, Американский журнал хирургии, панкреатологии, болезней органов пищеварения и печени
Рак поджелудочной железы
Рак поджелудочной железы – злокачественное новообразование, происходящее из трансформированных клеток, возникающих в тканях, образующих поджелудочную железу.Рак поджелудочной железы (рак поджелудочной железы) в основном встречается у людей старше 60 лет. Если он диагностирован на ранней стадии, то операция по удалению рака дает шанс на излечение. В целом, чем более развит рак (чем больше он разросся и распространился), тем меньше шансов, что лечение будет излечивающим. Как экзокринные, так и эндокринные клетки поджелудочной железы могут образовывать опухоли. Но опухоли, образованные экзокринными клетками, встречаются гораздо чаще. Клетки рака поджелудочной железы не погибают программно, а продолжают расти и делиться.
В целом, чем более развит рак (чем больше он разросся и распространился), тем меньше шансов, что лечение будет излечивающим. Как экзокринные, так и эндокринные клетки поджелудочной железы могут образовывать опухоли. Но опухоли, образованные экзокринными клетками, встречаются гораздо чаще. Клетки рака поджелудочной железы не погибают программно, а продолжают расти и делиться.
Связанные журналы рака поджелудочной железы
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, Европейский журнал рака, панкреатологии, Американский журнал хирургии
Сахарный диабет
Сахарный диабет – это группа метаболических заболеваний, характеризующихся недостаточностью инсулина гормона поджелудочной железы, которая возникает в результате нарушения секреции или действия инсулина, либо того и другого. Сахарный диабет Диабет – это хроническое заболевание, а это означает, что, хотя его можно контролировать, оно длится всю жизнь.Существует три основных типа сахарного диабета: 1.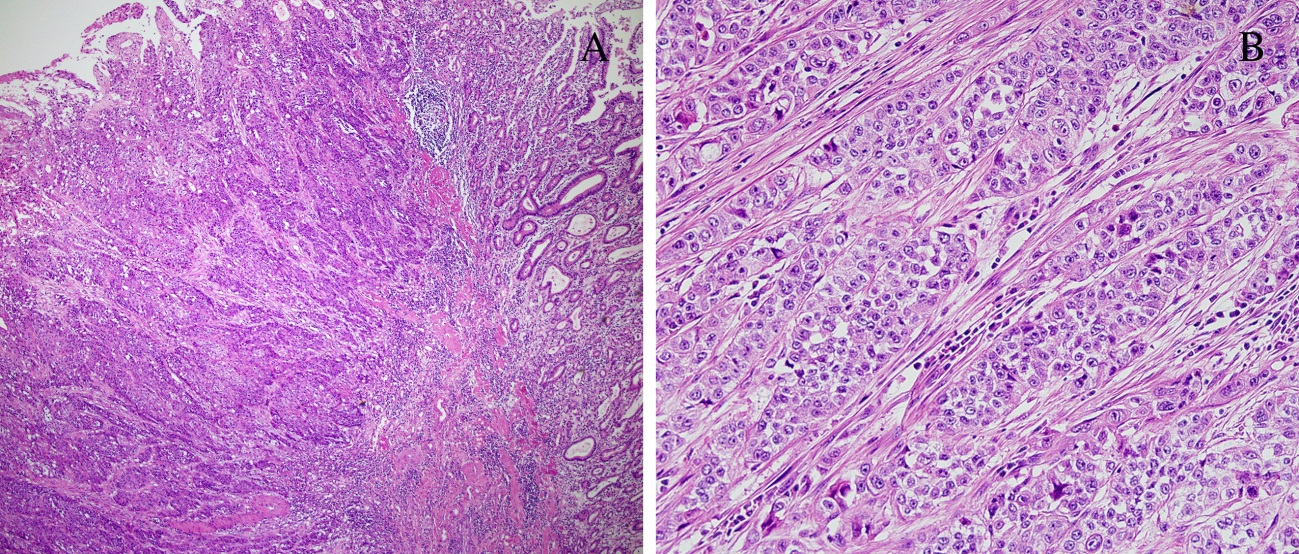 СД 1 типа; 2. Тип 2 ДМ; 3. Гестационный диабет.
СД 1 типа; 2. Тип 2 ДМ; 3. Гестационный диабет.
Связанные журналы сахарного диабета
Исследования и клиническая практика диабета, метаболизм, гастроэнтерология, панкреатология
Хирургия поджелудочной железы
Хирургия поджелудочной железы – сложная процедура и выполняется, когда это единственный вариант, который может привести к более длительному выживанию при раке поджелудочной железы и, в некоторых случаях, возможно, имеет потенциальный шанс на излечение.Применяется для лечения хронического панкреатита и других, менее распространенных доброкачественных заболеваний поджелудочной железы. Панкреатодуоденэктомия Уиппла – это операция, наиболее часто выполняемая при опухолях головки поджелудочной железы. Он включает удаление части желудка, всей двенадцатиперстной кишки, части тонкой кишки, головки поджелудочной железы, желчного протока и желчного пузыря, оставляя позади крупные кровеносные сосуды. Основная цель хирургии поджелудочной железы – снятие трудноизлечимой боли и декомпрессия соседних органов.
Связанные журналы хирургии поджелудочной железы
Гастроэнтерология, Эндоскопия желудочно-кишечного тракта, Американский журнал хирургии, Журнал детской хирургии, Панкреатология, Журнал хирургических исследований, Ланцет, Хирургия, Европейский журнал рака, болезней пищеварительной системы и печени, Европейский журнал добавок к раку, Журнал гастроинтестинальной хирургии
Аутоиммунный панкреатит
Аутоиммунный панкреатит (АИП) – это недавно обнаруженный тип хронического панкреатита, который трудно отличить от карциномы поджелудочной железы.Установлено, что аутоиммунный панкреатит (АИП) поддается лечению кортикостероидами, особенно преднизоном. В настоящее время это рассматривается как форма болезни гипер-IgG4. Существует две категории AIP: Тип 1 и Тип 2, каждая с разными клиническими профилями. Пациенты с AIP типа 1, как правило, были старше и имели высокую частоту рецидивов, но пациенты с AIP типа 2 не испытывали рецидивов и, как правило, были моложе. AIP не влияет на долгосрочную выживаемость.
AIP не влияет на долгосрочную выживаемость.
Связанный журнал аутоиммунного панкреатита
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, панкреатология, заболевания органов пищеварения и печени, клиническая гастроэнтерология и гепатология, Отчет по гастроэнтерологии, Американский журнал рентгенологии, Медицинский журнал Новой Англии
Псевдокиста поджелудочной железы
Псевдокиста поджелудочной железы – это заполненный жидкостью мешок в брюшной полости, который иногда также содержит ткани, ферменты и кровь из поджелудочной железы.Псевдокиста поджелудочной железы обычно возникает у пациентов с хроническим панкреатитом. Он также может возникать у людей с травмой поджелудочной железы или после травмы живота. Псевдокиста поджелудочной железы развивается, когда протоки поджелудочной железы повреждены воспалением, возникающим при панкреатите. В отличие от настоящих кист, псевдокиста выстлана не эпителием, а грануляционной тканью. Другие осложнения, возникающие из-за псевдокисты поджелудочной железы, включают инфекцию, кровотечение, непроходимость, разрыв, сдавление в мочевыводящей системе, желчевыводящей системе и артериовенозной системе.
Другие осложнения, возникающие из-за псевдокисты поджелудочной железы, включают инфекцию, кровотечение, непроходимость, разрыв, сдавление в мочевыводящей системе, желчевыводящей системе и артериовенозной системе.
Связанный журнал псевдокисты поджелудочной железы
Эндоскопия желудочно-кишечного тракта, Гастроэнтерология, Американский журнал хирургии, Журнал детской хирургии, панкреатология
Островковно-клеточная карцинома
Островоклеточная карцинома – это необычный рак эндокринной поджелудочной железы. На его долю приходится примерно 1,3% случаев рака поджелудочной железы. Это также известно как или несидиобластома. Опухоли островковых клеток поджелудочной железы могут быть доброкачественными и злокачественными. Островковые клетки производят множество различных гормонов; большинство опухолей выделяют только один гормон, который вызывает определенные симптомы.Существуют различные типы островковых опухолей, такие как: гастриномы (синдром Золлингера-Эллисона), глюкагономы, инсулиномы. Опухоли островковых клеток поддаются лечению даже после метастазирования. Симптомы включают потливость, головную боль, голод, беспокойство, двоение в глазах или нечеткое зрение, учащенное сердцебиение, диарею, язвы в желудке и тонкой кишке, рвоту с кровью и т. Д.
Опухоли островковых клеток поддаются лечению даже после метастазирования. Симптомы включают потливость, головную боль, голод, беспокойство, двоение в глазах или нечеткое зрение, учащенное сердцебиение, диарею, язвы в желудке и тонкой кишке, рвоту с кровью и т. Д.
Реализованные журналы островково-клеточной карциномы
Гастроэнтерология, Американский журнал хирургии, Ланцет, Патология человека, Американский журнал медицины
Трансплантация поджелудочной железы
Трансплантация поджелудочной железы – это передача здоровой поджелудочной железы от донора пациентам с диабетом.Поскольку поджелудочная железа является жизненно важным органом, родная поджелудочная железа пациента остается на месте, а пожертвованная поджелудочная железа помещается в другое место. Это делается потому, что в случае отторжения новой поджелудочной железы у пациента разовьется тяжелый диабет, и он не смог бы выжить без сохранившейся родной поджелудочной железы. Здоровая поджелудочная железа поступает от только что умершего донора или от человека с мертвым мозгом. В настоящее время трансплантация поджелудочной железы обычно проводится людям с тяжелым инсулинозависимым диабетом.
В настоящее время трансплантация поджелудочной железы обычно проводится людям с тяжелым инсулинозависимым диабетом.
Связанные журналы трансплантации поджелудочной железы
Процедуры трансплантации, гастроэнтерология, панкреатология, The Lancet, Американский журнал хирургии, Журнал хирургических исследований
Кистозный фиброз
Муковисцидоз (МВ) – это аутосомно-рецессивное генетическое заболевание, поражающее легкие, поджелудочную железу, печень и кишечник. Его основная характеристика – нарушенный транспорт хлорида и натрия через эпителий, что приводит к густым вязким секретам.Он также известен как муковисцидоз. Аномальное дыхание – самый серьезный симптом, возникающий в результате частых инфекций легких. Муковисцидоз вызывается мутацией сдвига рамки считывания в гене белка трансмембранного регулятора проводимости муковисцидоза (CFTR). Название муковисцидоз было дано из-за образования кисты в поджелудочной железе. Густая секреция слизи, возникающая из-за муковисцидоза, блокирует путь пищеварительных и эндокринных ферментов поджелудочной железы, вызывая полное повреждение поджелудочной железы.
Связанные журналы муковисцидоза
Журнал кистозного фиброза, Журнал педиатрии, гастроэнтерологии, Ланцет, Журнал детской хирургии, Журнал аллергии и клинической иммунологии, Журнал трансплантации сердца и легких, Американский журнал хирургии, респираторной медицины, Американский журнал медицины
Патофизиология
Патофизиология или физиопатология – это соединение патологии с физиологией. Патология описывает состояния во время болезненного состояния, тогда как физиология – это дисциплина, которая описывает механизмы, действующие в организме.Патология описывает ненормальное состояние, тогда как патофизиология пытается объяснить физиологические процессы, из-за которых такое состояние развивается и прогрессирует. Другими словами, патофизиология определяет функциональные изменения, связанные с заболеванием или травмой.
Связанные журналы по патофизиологии
Гастроэнтерология, панкреатология, биологическая психиатрия, журнал Американского колледжа кардиологии, патофизиология
Искусственная поджелудочная железа
Искусственная поджелудочная железа – это технология, разработанная для того, чтобы помочь людям с диабетом автоматически контролировать уровень глюкозы в крови, обеспечивая замену инсулина здоровой поджелудочной железы. Основная цель искусственной поджелудочной железы – обеспечить эффективную заместительную инсулиновую терапию, чтобы контроль уровня глюкозы в крови был нормальным и не было осложнений гипергликемии. Искусственная поджелудочная железа облегчает лечение инсулинозависимых. Эту систему носят как инсулиновую помпу и называют «искусственной поджелудочной железой», потому что она контролирует и регулирует уровень инсулина так же, как поджелудочная железа у людей без диабета.
Основная цель искусственной поджелудочной железы – обеспечить эффективную заместительную инсулиновую терапию, чтобы контроль уровня глюкозы в крови был нормальным и не было осложнений гипергликемии. Искусственная поджелудочная железа облегчает лечение инсулинозависимых. Эту систему носят как инсулиновую помпу и называют «искусственной поджелудочной железой», потому что она контролирует и регулирует уровень инсулина так же, как поджелудочная железа у людей без диабета.
Связанные журналы искусственной поджелудочной железы
Гастроэнтерология, панкреатология, Медицинский журнал Новой Англии, Американский журнал хирургии, исследований диабета и клинической практики, метаболизм
Кольцо поджелудочной железы
Кольцо поджелудочной железы – это редкое заболевание, при котором часть ткани поджелудочной железы разрастается и окружает двенадцатиперстную кишку.Эта дополнительная ткань возникает из головки поджелудочной железы. Это вызывает сужение двенадцатиперстной кишки, блокируя поступление пищи в оставшуюся часть кишечника. Частота возникновения кольцевой поджелудочной железы составляет 1 случай на 12–15 000 новорожденных. Обычно это происходит из-за аномального или внеэмбриологического развития. Однако также сообщалось о некоторых случаях заболевания у взрослых. Ранние признаки аномалии включают многоводие, низкий вес при рождении и непереносимость кормления сразу после рождения.
Частота возникновения кольцевой поджелудочной железы составляет 1 случай на 12–15 000 новорожденных. Обычно это происходит из-за аномального или внеэмбриологического развития. Однако также сообщалось о некоторых случаях заболевания у взрослых. Ранние признаки аномалии включают многоводие, низкий вес при рождении и непереносимость кормления сразу после рождения.
Связанные журналы кольцевидной железы поджелудочной железы
Журнал детской хирургии, Американский журнал хирургии, желудочно-кишечная эндоскопия, ультразвук в медицине и биологии, клиники и исследования в области гепатологии и гастроэнтерологии
Заболевания поджелудочной железы
Поджелудочная железа – это орган, который играет важную роль в пищеварении и производстве гормонов.Заболевания поджелудочной железы включают острый панкреатит, наследственный панкреатит и рак поджелудочной железы. В журнале собрана информация о заболеваниях поджелудочной железы, методах выявления, различных методах лечения и современных методах лечения заболеваний поджелудочной железы.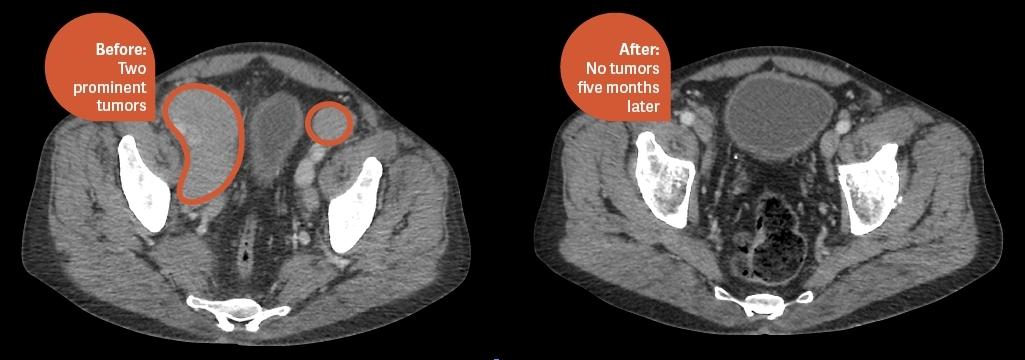
Связанные журналы заболеваний поджелудочной железы
Pancreatic Disorders & Therapy, Journal of Hepato-Bili-Pancreatic Sciences, Международный журнал гепатобилиарных и панкреатических заболеваний, Журнал гастроэнтерологии, панкреатологии и заболеваний печени
Диагностика лимфомы желудочно-кишечного тракта
«Желудочно-кишечные лимфомы – это разнообразная группа заболеваний с различной распространенностью», – говорит Лорен Б.Смит, доктор медицины, отделение патологии, Мичиганский университет, Анн-Арбор, штат Мичиган.
Примите к сведению
- Желудочно-кишечные лимфомы – это разнообразная группа заболеваний с различной распространенностью, что затрудняет диагностику.
- Симптомы первичных лимфом желудка могут имитировать другие состояния ЖКТ, а сами лимфомы желудочно-кишечного тракта могут даже имитировать друг друга.
- В этом недавнем тематическом исследовании описывается широкий спектр проявлений лимфомы желудочно-кишечного тракта, которые могут помочь практикующим врачам выбрать подходящую терапию.

Эти лимфомы составляют от 30% до 40% всех экстраузловых неходжкинских лимфом, от 10% до 15% всех неходжкинских лимфом и от 1% до 4% всех случаев рака желудочно-кишечного тракта. 1 Большинство лимфом желудочно-кишечного тракта возникают в В-клетках, наиболее типичной из которых является диффузная крупноклеточная В-клеточная лимфома (DLBCL), хотя лимфомы, происходящие из Т-клеток, также встречаются в желудочно-кишечном тракте. 2 Наиболее распространенным анатомическим участком является желудок, за ним следует тонкий и толстый кишечник (особенно подвздошная кишка), при этом лимфома пищевода встречается крайне редко. 1
Желудочно-кишечные лимфомы, особенно те, которые встречаются реже, могут быть сложными с диагностической точки зрения из-за их разнообразных клинических проявлений и гетерогенной гистопатологической и иммунофенотипической природы. 1,2
Диагностический вызов
Лимфома желудочно-кишечного тракта может клинически проявляться множеством неспецифических симптомов, от вздутия живота и диспепсии до тошноты, рвоты, диареи, боли в животе, желудочно-кишечного кровотечения, потери веса и непроходимости кишечника. 1,2 Многие атипичные реактивные и воспалительные желудочно-кишечные состояния могут имитировать или маскировать лимфомы, 2 и сами желудочно-кишечные лимфомы могут даже имитировать друг друга. 3
1,2 Многие атипичные реактивные и воспалительные желудочно-кишечные состояния могут имитировать или маскировать лимфомы, 2 и сами желудочно-кишечные лимфомы могут даже имитировать друг друга. 3
В частности, неспецифические симптомы первичных лимфом желудка при начальном проявлении могут имитировать различные клинико-патологические состояния пищеварительного тракта, включая функциональные расстройства, гастрит, заболевания поджелудочной железы и язвенную болезнь. Более чем в половине случаев физикальное обследование не дает замечательных результатов.Как следствие, точный диагноз может быть отложен, в некоторых случаях даже на несколько лет. 4
Для патологов, специализирующихся на лимфомах, и тех, кто специализируется на патологии желудочно-кишечного тракта, полезно работать вместе, чтобы отличать реактивные пролиферации от неопластических разрастаний, считает доктор Смит. «Опытные гематопатологи обычно могут различать редкие типы лимфомы с помощью комбинации иммуногистохимических исследований и иногда молекулярных исследований клональности», – добавляет она.
Точные диагностические подходы имеют важное терапевтическое значение. Во-первых, различные типы лимфом желудочно-кишечного тракта имеют агрессивное поведение, в то время как другие считаются вялотекущими, что может не требовать лечения. 2 В качестве нескольких примеров, локализованную лимфому, ассоциированную со слизистой оболочкой лимфоидной ткани (MALT), вызванную хронической инфекцией Helicobactor pylori слизистой оболочки желудка, во многих случаях можно лечить только путем искоренения основной инфекции, и фолликулярную лимфому на ранней стадии обычно может сопровождаться настороженным ожиданием. 1,2 С другой стороны, агрессивные лимфомы желудочно-кишечного тракта, такие как Т-клеточная лимфома кишечника (не указано иное), мономорфная эпителиотропная Т-клеточная лимфома кишечника (ранее Т-клеточная лимфома, ассоциированная с энтеропатией II типа) и DLBCL желудка, требуют системных химиотерапевтических вмешательств. 2,4,5 Таким образом, точность диагностики не только способствует правильному терапевтическому вмешательству, но, что не менее важно, помогает предотвратить использование чрезмерно агрессивных схем лечения. 2
2
Знания, полученные из стратегий определения стадии, также могут оптимизировать лечение. Например, чтобы четко отличить фолликулярную лимфому двенадцатиперстного типа от «классической» фолликулярной лимфомы с поражением желудочно-кишечного тракта, необходимо провести оценку стадии, такую как биопсия костного мозга и визуализирующие исследования, чтобы исключить системное заболевание и кишечное распространение забрюшинной или мезентериальной лимфомы . 2 В качестве другого примера, стадирование первичной лимфомы желудка также важно для исключения системной лимфомы с вторичным поражением желудка. 4
Корпус серии
Ануша Ширвайкар Томас, доктор медицины, отделение гастроэнтерологии, Онкологический центр Андерсона Университета Техаса, Хьюстон, Техас, и его коллеги недавно сообщили о серии случаев в British Medical Journal Open Gastroenterology , чтобы проиллюстрировать различные признаки и симптомы желудочно-кишечных лимфом и показать, как эндоскопические исследования в сочетании с биопсией и экспертной патологической оценкой могут помочь в постановке окончательного диагноза. Группа исследователей обсудила клинические и эндоскопические особенности лимфом желудка, кишечника и пищевода. 1
Группа исследователей обсудила клинические и эндоскопические особенности лимфом желудка, кишечника и пищевода. 1
Пациенты с лимфомами желудка MALT могут испытывать тошноту, рвоту, боль в животе и желудочно-кишечное кровотечение. По словам доктора Томаса и его коллег, эти лимфомы MALT эндоскопически проявляются как экзофитные изъязвленные образования, гипертрофические и разъеденные желудочные складки или гиперемированные аномалии слизистой оболочки желудка. Признаки и симптомы, связанные с DLBCL желудка, аналогичны тем, которые связаны с лимфомой MALT.Эти DLBCL обычно появляются в теле / дне желудка и эндоскопически характеризуются как полиповидная масса, изъязвление или диффузное / очаговое утолщение стенки желудка. 1
MALT, DLBCL, а также мантийно-клеточные, фолликулярные и Т-клеточные лимфомы обнаруживаются в кишечнике. Пациенты с лимфомой кишечника могут испытывать боль в животе, диарею, гематохезию, потерю веса и лихорадку.
Капсульная эндоскопия и колоноскопия показывают «изъязвленные поражения или диффузное утолщение слизистой оболочки с крупными или мелкими зернами», – сказал доктор. Томас и его коллеги написали в своем отчете. 1
Томас и его коллеги написали в своем отчете. 1
Клинические признаки и симптомы первичной лимфомы пищевода включают диспепсию, дисфагию, потерю веса и кровотечение из верхних отделов желудочно-кишечного тракта. Эти лимфомы могут проявляться эндоскопически как узловые, полиповидные, изъязвленные или стенозированные. 1
Доктор Смит и ее коллега отметили в предыдущей серии случаев лимфомы желудочно-кишечного тракта: «Диагностический подход, сочетающий ожидание общих сущностей… с поддержанием« погодного ока »для более необычных сущностей или явлений… имеет решающее значение для успешной навигации. из моря лимфоидных инфильтратов, возникающих в желудочно-кишечном тракте.” 3
Опубликовано: 13 февраля 2020 г.
Лимфома желудка – wikidoc
Главный редактор: C. Майкл Гибсон, M.S., M.D. [1]; Заместитель главного редактора: Мазия Фатима, MBBS [2]
Обзор
Первичная лимфома желудка – это рак, происходящий из лимфоцитов (разновидность лейкоцитов), образующихся в желудке.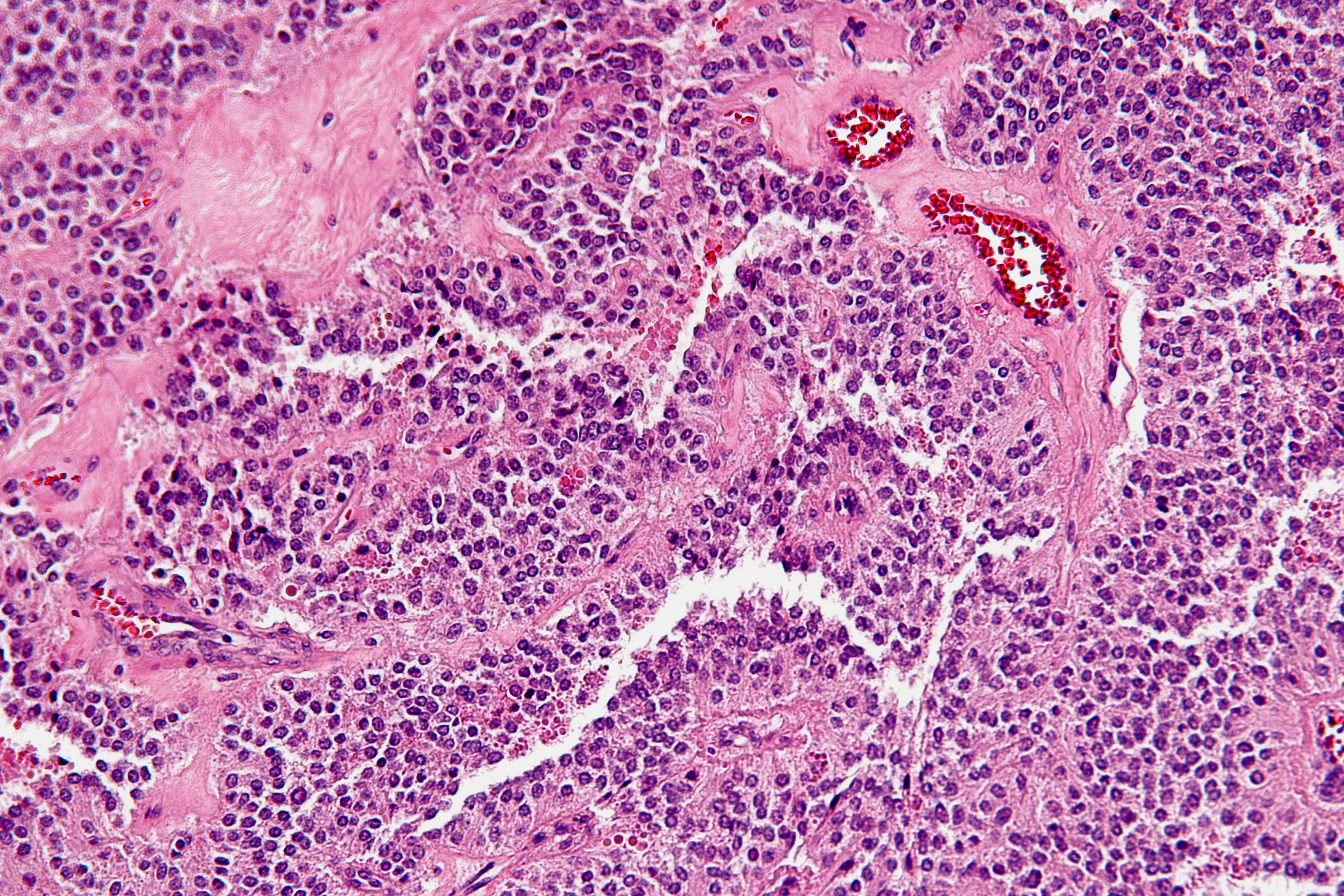 Наиболее частой причиной первичной лимфомы желудка является лимфома, связанная со слизистой оболочкой лимфоидной ткани (MALT), и диффузная крупноклеточная B-клеточная лимфома (DLBCL) желудка. Первичная лимфома желудка может быть классифицирована в соответствии с гистологией на MALT-лимфому и DLBCL. MALT-лимфому можно далее разделить на MALT-лимфому с положительной реакцией на H. pylori и MALT-лимфому с отрицательной реакцией на H. pylori. DLBCL можно разделить на 3 подгруппы, подобные В-клеткам зародышевого центра, активированные В-клетки, первичные средостенные DLBCL. Точный патогенез первичной лимфомы желудка до конца не изучен.Общие симптомы первичной лимфомы желудка включают дискомфорт в эпигастрии, анорексию, потерю веса, тошноту, связанную с рвотой или без нее, скрытое желудочно-кишечное кровотечение, преждевременное насыщение. Менее распространенные симптомы включают постоянную и ночную потливость. Пациенты с первичной лимфомой желудка обычно выглядят нормально. Жизненно важные показатели в пределах нормы, если нет осложнений.
Наиболее частой причиной первичной лимфомы желудка является лимфома, связанная со слизистой оболочкой лимфоидной ткани (MALT), и диффузная крупноклеточная B-клеточная лимфома (DLBCL) желудка. Первичная лимфома желудка может быть классифицирована в соответствии с гистологией на MALT-лимфому и DLBCL. MALT-лимфому можно далее разделить на MALT-лимфому с положительной реакцией на H. pylori и MALT-лимфому с отрицательной реакцией на H. pylori. DLBCL можно разделить на 3 подгруппы, подобные В-клеткам зародышевого центра, активированные В-клетки, первичные средостенные DLBCL. Точный патогенез первичной лимфомы желудка до конца не изучен.Общие симптомы первичной лимфомы желудка включают дискомфорт в эпигастрии, анорексию, потерю веса, тошноту, связанную с рвотой или без нее, скрытое желудочно-кишечное кровотечение, преждевременное насыщение. Менее распространенные симптомы включают постоянную и ночную потливость. Пациенты с первичной лимфомой желудка обычно выглядят нормально. Жизненно важные показатели в пределах нормы, если нет осложнений..jpg) При физикальном обследовании пациентов с первичной лимфомой желудка обычно отмечается пальпируемое образование и периферическая лимфаденопатия.Лимфому желудка следует дифференцировать от состояний с аналогичными проявлениями, таких как острый гастрит, хронический гастрит, атрофический гастрит, болезнь Крона, гастроэзофагеальная рефлюксная болезнь, язвенная болезнь желудка, гастринома и аденокарцинома желудка. Первичная лимфома желудка обычно поражает пожилых пациентов на пятом или шестом десятилетии жизни. Первичная лимфома желудка чаще встречается у мужчин, чем у женщин. Факторы риска лимфомы желудка включают Helicobacter pylori, длительную терапию иммунодепрессантами , ВИЧ-инфекцию.У большинства пациентов с первичной лимфомой желудка на 5-м десятилетии жизни появляются неспецифические симптомы. Ранние клинические признаки включают боль в эпигастрии, тошноту и рвоту. Если не лечить, у пациентов с лимфомой желудка может развиться анорексия, потеря веса и преждевременное насыщение.
При физикальном обследовании пациентов с первичной лимфомой желудка обычно отмечается пальпируемое образование и периферическая лимфаденопатия.Лимфому желудка следует дифференцировать от состояний с аналогичными проявлениями, таких как острый гастрит, хронический гастрит, атрофический гастрит, болезнь Крона, гастроэзофагеальная рефлюксная болезнь, язвенная болезнь желудка, гастринома и аденокарцинома желудка. Первичная лимфома желудка обычно поражает пожилых пациентов на пятом или шестом десятилетии жизни. Первичная лимфома желудка чаще встречается у мужчин, чем у женщин. Факторы риска лимфомы желудка включают Helicobacter pylori, длительную терапию иммунодепрессантами , ВИЧ-инфекцию.У большинства пациентов с первичной лимфомой желудка на 5-м десятилетии жизни появляются неспецифические симптомы. Ранние клинические признаки включают боль в эпигастрии, тошноту и рвоту. Если не лечить, у пациентов с лимфомой желудка может развиться анорексия, потеря веса и преждевременное насыщение. Общие осложнения лимфомы желудка включают перфорацию, кровотечение и непроходимость. Прогноз в целом хороший, и полная ремиссия может быть достигнута после 6-8 курсов химиотерапии или после операции.Эндоскопия верхних отделов желудочно-кишечного тракта с биопсией – это золотой стандарт диагностики лимфомы желудка. Лапаротомия и лапароскопия должны выполняться, когда у пациента есть такие осложнения, как перфорация или непроходимость. Эндоскопическое ультразвуковое исследование (ЭУЗИ) поможет оценить глубину инвазии лимфомы и поражение перигастральных узлов. Лимфома MALT представляет собой распространяющееся поверхностное или диффузное инфильтрирующее поражение, тогда как диффузная крупноклеточная В-клеточная лимфома имеет типичный вид массообразующего поражения при эндоскопическом ультразвуковом исследовании.Визуализирующие исследования, включая компьютерную томографию или эндоскопическое ультразвуковое исследование, полезны для определения стадии заболевания. Гематологические параметры обычно проверяются, чтобы помочь определить стадию и исключить сопутствующий лейкоз.
Общие осложнения лимфомы желудка включают перфорацию, кровотечение и непроходимость. Прогноз в целом хороший, и полная ремиссия может быть достигнута после 6-8 курсов химиотерапии или после операции.Эндоскопия верхних отделов желудочно-кишечного тракта с биопсией – это золотой стандарт диагностики лимфомы желудка. Лапаротомия и лапароскопия должны выполняться, когда у пациента есть такие осложнения, как перфорация или непроходимость. Эндоскопическое ультразвуковое исследование (ЭУЗИ) поможет оценить глубину инвазии лимфомы и поражение перигастральных узлов. Лимфома MALT представляет собой распространяющееся поверхностное или диффузное инфильтрирующее поражение, тогда как диффузная крупноклеточная В-клеточная лимфома имеет типичный вид массообразующего поражения при эндоскопическом ультразвуковом исследовании.Визуализирующие исследования, включая компьютерную томографию или эндоскопическое ультразвуковое исследование, полезны для определения стадии заболевания. Гематологические параметры обычно проверяются, чтобы помочь определить стадию и исключить сопутствующий лейкоз. Повышенный уровень ЛДГ может указывать на лимфому. Установленных мер по первичной и вторичной профилактике лимфомы желудка не существует.
Повышенный уровень ЛДГ может указывать на лимфому. Установленных мер по первичной и вторичной профилактике лимфомы желудка не существует.
Классификация
Первичная лимфома желудка может быть классифицирована в соответствии с гистологией на следующие подтипы:
- В-клеточные лимфомы бывают двух основных типов:
- MALT лимфому можно разделить на:
- DLBCL можно разделить на 3 подгруппы в зависимости от экспрессии гена:
- Зародышевый центр, подобный В-клеткам
- Активированные B-подобные
- Первичный медиастинальный DLBCL
Патофизиология
В случае DLBCL – эрадикационная терапия антибиотиками для H.pylori приводит к полной ремиссии лимфомы, подчеркивая роль H.pylori в патогенезе.
- HBV играет роль в патогенезе В-клеточной НХЛ, о чем свидетельствует повышенный риск развития НХЛ у HBsAg-положительных пациентов.
Гистопатология
Большинство лимфом желудка являются преимущественно неходжкинскими лимфомами B-клеточного происхождения. Первичная лимфома желудка может варьироваться от хорошо дифференцированных лимфом низкой степени злокачественности до лимфом высокой степени или крупноклеточной лимфомы. [5]
Первичная лимфома желудка может варьироваться от хорошо дифференцированных лимфом низкой степени злокачественности до лимфом высокой степени или крупноклеточной лимфомы. [5]
Симптомы
Общие симптомы
Общие симптомы первичной лимфомы желудка включают: [6] [7]
Менее распространенные симптомы
Менее распространенные симптомы включают:
Медицинский осмотр
Внешний вид пациента
- Пациенты с первичной лимфомой желудка обычно выглядят нормально. [7]
Знаки жизнедеятельности
Жизненно важные показатели в пределах нормы, если нет осложнения.
Осмотр брюшной полости
Дифференциальная диагностика
Лимфому желудка следует дифференцировать от состояний с аналогичными проявлениями, таких как острый гастрит, хронический гастрит, атрофический гастрит, болезнь Крона, гастроэзофагеальная рефлюксная болезнь, язвенная болезнь, гастринома и аденокарцинома желудка: [8] [9] [10] ] [11] [12] [13] [14] [15] [16]
Демография
Факторы риска
Факторы риска лимфомы желудка: [18]
Естественная история, осложнения и прогнозы
Естественная история
Осложнения
Прогноз
Диагностика
МРТ
Лимфома желудка на МРТ включает:
- Неравномерно утолщенные складки слизистой оболочки
- Нерегулярная инфильтрация подслизистой оболочки
- Кольцевидное сужение
- Экзофитный рост опухоли
- Забрюшинная лимфаденопатия.

Лечение
Профилактика
Первичная профилактика
Правильное лечение Helicobacter pylori может предотвратить лимфому MALT.
Вторичная профилактика
Нет установленных мер для вторичной профилактики лимфомы желудка.
Список литературы
- ↑ Хасселл Т., Исааксон П.Г., Крэбтри Дж. Э., Спенсер Дж. (1996). «Helicobacter pylori-специфические Т-клетки, инфильтрирующие опухоль, обеспечивают контактно-зависимую помощь для роста злокачественных В-клеток в лимфоме желудка низкой степени злокачественности из лимфоидной ткани, связанной со слизистой оболочкой». Дж. Патол . 178 (2): 122–7. DOI: 10.1002 / (SICI) 1096-9896 (199602) 178: 2 <122 :: AID-PATh586> 3.0.CO; 2-D. PMID 8683376.
- ↑ Энгельс Э.А., Чо Э.Р., Джи Ш. (2010). «Инфекция вирусом гепатита В и риск неходжкинской лимфомы в Южной Корее: когортное исследование». Ланцет Онкол . 11 (9): 827–34.
 DOI: 10.1016 / S1470-2045 (10) 70167-4. PMC 2933963. PMID 20688564.
DOI: 10.1016 / S1470-2045 (10) 70167-4. PMC 2933963. PMID 20688564. - ↑ Доусон IMP, Cornes JS, Morrison BC. Первичные злокачественные лимфоидные опухоли кишечного тракта.Br J Surg. 1961; 49: 80-89.
- ↑ Aisenberg AC. Последовательный взгляд на неходжкинскую лимфому. J Clin Oncol. 1995; 13: 2656-2675.
- ↑ 5,0 5,1 Ван Т., Гуй В, Шен Кью (2010). «Первичная неходжкинская лимфома желудочно-кишечного тракта: клинико-патологический и прогностический анализ». Med. Онкол . 27 (3): 661–6. DOI: 10.1007 / s12032-009-9265-1. PMID 19565363.
- ↑ Фримен К., Берг Дж. У., Катлер С. Дж. (1972). «Возникновение и прогноз экстранодальных лимфом». Рак . 29 (1): 252–60. PMID 5007387.
- ↑ 7.0 7.1 Koch P, del Valle F, Berdel WE, Willich NA, Reers B, Hiddemann W, Grothaus-Pinke B, Reinartz G, Brockmann J, Temmesfeld A, Schmitz R, Rübe C, Probst A , Jaenke G, Bodenstein H, Junker A, Pott C, Schultze J, Heinecke A, Parwaresch R, Tiemann M (2001).
 «Первичная неходжкинская лимфома желудочно-кишечного тракта: I. Анатомическое и гистологическое распределение, клинические особенности и данные о выживаемости 371 пациента, зарегистрированного в Немецком многоцентровом исследовании GIT NHL 01/92». J. Clin. Онкол . 19 (18): 3861–73. DOI: 10.1200 / JCO.2001.19.18.3861. PMID 11559724.
«Первичная неходжкинская лимфома желудочно-кишечного тракта: I. Анатомическое и гистологическое распределение, клинические особенности и данные о выживаемости 371 пациента, зарегистрированного в Немецком многоцентровом исследовании GIT NHL 01/92». J. Clin. Онкол . 19 (18): 3861–73. DOI: 10.1200 / JCO.2001.19.18.3861. PMID 11559724. - ↑ Сугимачи К., Инокучи К., Кувано Х., Ойва Т. (1984). «Острый гастрит классифицируется клинически в соответствии с данными серии исследований верхних отделов ЖКТ и эндоскопии». Сканд Дж Гастроэнтерол . 19 (1): 31–7. PMID 6710074.
- ↑ Сиппонен П., Маарус Х.И. (2015). «Хронический гастрит». Сканд Дж Гастроэнтерол . 50 (6): 657–67.DOI: 10.3109 / 00365521.2015.1019918. PMC 4673514. PMID 25 6.
- ↑ Sartor RB (2006). «Механизмы заболевания: патогенез болезни Крона и язвенного колита». Нат Клин Практик Гастроэнтерол Гепатол . 3 (7): 390–407.
 DOI: 10.1038 / ncpgasthep0528. PMID 16819502.
DOI: 10.1038 / ncpgasthep0528. PMID 16819502. - ↑ Сиппонен П. (1989). «Атрофический гастрит как предраковое состояние». Энн Мед . 21 (4): 287–90. PMID 2789799.
- ↑ Бадилло Р., Фрэнсис Д. (2014).«Диагностика и лечение гастроэзофагеальной рефлюксной болезни». Мир J Gastrointest Pharmacol Ther . 5 (3): 105–12. DOI: 10.4292 / wjgpt.v5.i3.105. PMC 4133436. PMID 25133039.
- ↑ Рамакришнан К., Салинас RC (2007). «Язвенная болезнь». Ам Фам Врач . 76 (7): 1005–12. PMID 17956071.
- ↑ Banasch M, Schmitz F (2007). «Диагностика и лечение гастриномы в эпоху ингибиторов протонной помпы». Wien Klin Wochenschr . 119 (19–20): 573–8. DOI: 10.1007 / s00508-007-0884-2. PMID 17985090.
- ↑ Дикен Б.Дж., Бигам Д.Л., Касс С., Макки-младший, Джой А.А., Гамильтон С.М. (2005). «Аденокарцинома желудка: обзор и рассмотрение будущих направлений».
 Энн Сург . 241 (1): 27–39. PMC 1356843. PMID 15621988.
Энн Сург . 241 (1): 27–39. PMC 1356843. PMID 15621988. - ↑ Ghimire P, Wu GY, Zhu L (2011). «Первичная лимфома желудочно-кишечного тракта». Мир Дж. Гастроэнтерол . 17 (6): 697–707. DOI: 10.3748 / wjg.v17.i6.697. PMC 3042647. PMID 213.
- ↑ Thirlby RC. Лимфома желудочно-кишечного тракта: хирургическая перспектива. Онкология (Хантингт). 1993; 7: 29-32.
- ↑ Статья NEJM
- ↑ Cogliatti SB, Schmid U, Schumacher U, Eckert F, Hansmann ML, Hedderich J, Takahashi H, Lennert K (1991). «Первичная В-клеточная лимфома желудка: клинико-патологическое исследование 145 пациентов». Гастроэнтерология . 101 (5): 1159–70.PMID 1936785.
- ↑ Мюллер А.Ф., Мэлони А., Дженкинс Д., Доулинг Ф., Смит П., Бесселл Е.М., Тогхилл П.Дж. (1995). «Первичная лимфома желудка в клинической практике 1973–1992». Кишечник . 36 (5): 679–83. PMC 1382669. PMID 7797116.

- ↑ Hauptrock B, Hess G (2008). «Ритуксимаб в лечении неходжкинской лимфомы». Биологические препараты . 2 (4): 619–33. PMC 2727901. PMID 19707443.
- ↑ Morgner A, Schmelz R, Thiede C, Stolte M, Miehlke S (2007).«Терапия лимфомы лимфоидной ткани, ассоциированной со слизистой оболочкой желудка». Мир Дж. Гастроэнтерол . 13 (26): 3554–66. PMC 4146794. PMID 17659705.
Шаблон: Гастроэнтерология.
Шаблон: Опухоли
Шаблон: WikiDoc Sources





 V. 342. P. 575–577.
V. 342. P. 575–577. , Stolte M., Fischer R. Factors influencing lymph node infiltration in primary gastric malignant lymphoma of the mucosa associated lymphoid tissue. Pathol Res Pract. 1994;190: 1077–1081.
, Stolte M., Fischer R. Factors influencing lymph node infiltration in primary gastric malignant lymphoma of the mucosa associated lymphoid tissue. Pathol Res Pract. 1994;190: 1077–1081. pylori ). Это очень распространенная инфекция, которая может вызвать язву желудка и расстройство желудка. Обычно это не вызывает серьезных проблем. Примерно 9 из каждых 10 человек с лимфомой желудка MALT имеют инфекцию H. pylori . Однако большинство людей, у которых есть H.pylori , а не , а не , приводят к развитию лимфомы желудка MALT.
pylori ). Это очень распространенная инфекция, которая может вызвать язву желудка и расстройство желудка. Обычно это не вызывает серьезных проблем. Примерно 9 из каждых 10 человек с лимфомой желудка MALT имеют инфекцию H. pylori . Однако большинство людей, у которых есть H.pylori , а не , а не , приводят к развитию лимфомы желудка MALT.
 Симптомы обычно развиваются с одной стороны, но примерно в 1 из 10 случаев они могут поражать оба глаза.
Симптомы обычно развиваются с одной стороны, но примерно в 1 из 10 случаев они могут поражать оба глаза. Сначала вы можете принять успокаивающее (расслабляющее) лекарство. Чтобы посмотреть на свой желудок, через рот через глотку проводят трубку в желудок (гастроскопия). Чтобы посмотреть на кишечник, трубку вводят через задний проход в кишечник (колоноскопия). Через трубку можно продеть небольшие хирургические инструменты, чтобы врач мог взять образцы биопсии. Они могут брать образцы из нескольких разных мест в желудке или кишечнике.
Сначала вы можете принять успокаивающее (расслабляющее) лекарство. Чтобы посмотреть на свой желудок, через рот через глотку проводят трубку в желудок (гастроскопия). Чтобы посмотреть на кишечник, трубку вводят через задний проход в кишечник (колоноскопия). Через трубку можно продеть небольшие хирургические инструменты, чтобы врач мог взять образцы биопсии. Они могут брать образцы из нескольких разных мест в желудке или кишечнике.



 DOI: 10.1016 / S1470-2045 (10) 70167-4. PMC 2933963. PMID 20688564.
DOI: 10.1016 / S1470-2045 (10) 70167-4. PMC 2933963. PMID 20688564.  «Первичная неходжкинская лимфома желудочно-кишечного тракта: I. Анатомическое и гистологическое распределение, клинические особенности и данные о выживаемости 371 пациента, зарегистрированного в Немецком многоцентровом исследовании GIT NHL 01/92». J. Clin. Онкол . 19 (18): 3861–73. DOI: 10.1200 / JCO.2001.19.18.3861. PMID 11559724.
«Первичная неходжкинская лимфома желудочно-кишечного тракта: I. Анатомическое и гистологическое распределение, клинические особенности и данные о выживаемости 371 пациента, зарегистрированного в Немецком многоцентровом исследовании GIT NHL 01/92». J. Clin. Онкол . 19 (18): 3861–73. DOI: 10.1200 / JCO.2001.19.18.3861. PMID 11559724.  DOI: 10.1038 / ncpgasthep0528. PMID 16819502.
DOI: 10.1038 / ncpgasthep0528. PMID 16819502. 